LAPORAN PRAKTIKUM
KIMIA FISIK II
“KESETIMBANGAN FASA”
TANGGAL PRAKTIKUM : 26 APRIL 2014
Disusun Oleh :
DEVI CITRA RASTUTI
1112016200056
KELOMPOK 4 :
Aini Nadhokhotani
Devita Arini Safitri
Petri Wahyu Sari
Selvia Dewi Setyani
PROGRAM STUDI PENDIDIKAN KIMIA
JURUSAN PENDIDIKAN ILMU PENGETAHUAN ALAM
FAKULTAS ILMU TARBIYAH DAN KEGURUAN
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH JAKARTA
ABSTRAK
Telah dilakukan praktikum yang bejudul kesetimbangan fasa yang memiliki tujuan agar dapat menggambarkan diagram fase system terner dan menentukan letak pleit point atau titik jalin pada diagram fasenya. Pada praktikum akan dilakukan pengukuran massa jenis pada kloroform, asam asetat glacial, dan aquades. Berdasarkan hasil pengamatan massa jenis kloroform adalah 1,44 g/ml, massa jenis asam asetat glacial 1,01 g/ml dan massa jenis akuades 0,75 g/ml. Setelah itu melakukan percobaan system tiga komponen dimana kloroform ditambahkan dengan akuades sebanyak 5 ml kemudian di titrsai dengan asam asetat glacial. Asam asetat glacial yg digunakan untuk menitrasi kloroform 3ml adalah 7,5 ml, untuk kloroform 4 ml membutuhkan 10 ml larutan asam asetat glacial, dan untuk 6 ml kloroform membutuhkan 10,1 ml larutan asam asetat glacial.
PENDAHULUAN
Untuk sistem tiga komponen, derajat kebebasan, F=3-P+2=5-P. Untuk p=1,
ada 4 derajat kebebasan. Tak mungkin menyatakan sistem seperti ini dalam bentuk
grafik yang lengkap dalam tiga dimensi, apalagi dalam dua dimensi. Oleh karena itu
biasanya sistem dinyatakan pada sugu dan tekanan yang tetap, dan derajat kebebasan
menjadi F=3-P, jadi derajat kebebasannya paling banyak adalah dua, dan dapat
dinyatakan dalam suatu bidang. Pada suhu dan tekanan tetap, variabel yang dapat
digunakan untuk menyatakan keadaan sistem tunggal yaitu Xa, Xb, dan Xc yang
dihubungkan melalui Xa+Xb+Xc=1. Komposisi salah satu komponen sudah tertentu
jika dua komponen lainnya diketahui. Sistem tiga komponen sebenarnya banyak
kemungkinannya dan yang paling umum adalah:
a. Sistem 3 komponen yang terdiri atas zar cair yang sebagian saling bercampur
b. Sistem 3 komponen yang terdiri atas dua komponen padat dan satu komponen cair
(Burhanudin, 2012, hlm 17-18).
Menurut aturan fase, derajat kebebasan diberikan oleh
F = C- P + S
= 5 – P
Dan bila tekanan tempetaur ditetapkan, persamaan di atas menjadi
Untuk satu fase kita membutuhkan dua derajat kebebasan untuk menggambarkan
system secara sempurna, dan untuk dua fase dalam kesetimbangan , satu derajat
kebebasan. Jadikita dapat menggambarkan diagram fase dalam satu bidang. Cara
terbaik untuk menggambarkan diagram fase dalam satu bidang. Cara terbaik untuk
menggambarkan system tiga komponen adalah dengan mendapatkan suatu kertas
grafik segitiga. Konsentrasi dapat dinyatakan dalam istilah % berat atau faraksi mol.
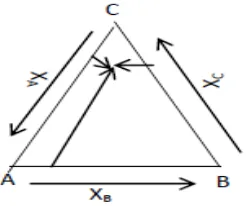
Puncak-puncak dihubungkan ke titik tengah dari sisi yang berlawanan, yaitu Aa,Bb,Cc.
Titik Nol mulai dari titik-titik a,b,c dan titik-titik A,B,C menyatakan komposisi adalah
100% atau satu. Jadi garis-garis Aa,Bb,Cc merupakan konsentrasi komponen A,B,C.
Lebih lanjut, segitiga adalah sama sisi, jumlah jarak-jarak garis tegak lurus dari
sembarang titik dalam segitiga kesisi-sisi adalah konstan dan sama dengan panjang
garis tegak lurus antar sudut dan pusat dari sisi yang berlawanan,yaitu 100% atau
satu(Dogra.2009:473).
Fraksi mol tiga komponen dari sistem terner (C = 3) sesuai dengan XA + XB +
Xc = 1.
Titik pada sisi AB : campuran biner A dan B
BC : campuran biner B dan C
AC : campuran biner A dan C
Diagram fase yang digambarkan sebagai segitiga sama sisi menjamin dipenuhinya sifat
ini secara otomatis sebab jumlah jarak ke sebuah titik didalam segitiga sama sisi yang
diukur sejajar dengan sisi-sisinya sama dengan panjang sisi segitiga itu yang dapat
Tekanan dan temperatur menentukan keadaan suatu materi kesetimbangan fasa dari
materi yang sama. Kesetimbangan fasa dari suatu sistem harus memenuhi syarat
berikut :
a. Sistem mempunyai lebih dari satu fasa meskipun materinya sama
b. Terjadi perpindahan reversibel spesi kimia dari satu fasa ke fasa lain
c. Seluruh bagian sistem mempunyai tekanan dan temperatur sama
(Endang,2008).
ALAT BAHAN DAN METODE
ALAT
1. Buret
2. Statif dan klem
3. Labu Erlenmeyer 250 ml
4. Gelas ukur 5 ml
5. Batang pengaduk
6. Neraca Ohauss
7. Piknometer
BAHAN
1. Kloroform
2. Asam asetat glacial
3. Akuades
LANGKAH KERJA
1. Membersihkan piknometer dan dikeringkan
2. Mengukur berat kosong piknometer
3. Memasukan air dalam piknometer sapai penuh dan kemudian menimbangnya
4. Mengulangi kegiatan di atas dengan mengganti air dengan kloroform dan asam
asetat glacial
Sistem tiga komponen
1. Menyiapkan alat dan bahan
2. Menyediakan labu Erlenmeyer 3 buah yang masing-masing diisi dengan 3 ml,4
ml,dan 6 ml
3. Menambahkan masing-masing 5 ml akuades,mengocok sebentar, larutan akan
membentuk dua lapisan
4. Titrasi dengan asam asetat glacial sampai kedua lapisan membentuk satu fasa
HASIL PENGAMATAN DAN PEMBAHASAN
DATA PENGAMATAN
Volume kloroform (ml)
Volume aquadest (ml) Volume asam asetat glacial (ml)
3 5 7,5
5 5 10
6 5 10,1
Massa piknometer kosong = 21,95 g
Volume piknometer = 24,674 ml
Massa piknometer + air = 40,46 g
Massa jenis air = (40,46 𝑔−21,95𝑔)/24,9 𝑚𝑙 = 0,75 g/ml Massa piknometer + kloroform = 57,8 g
Massa jenis kloroform = (57,8 𝑔−21,95𝑔)/24,674 𝑚𝑙 = 1,44 g/ml Massa piknometer + asam asetat glasial = 47,1 g
Massa jenis asam asetat glasial = (47,1 𝑔−21,95𝑔)/24,674 𝑚𝑙 = 1,01 g/ml
Massa asam asetat glacial= 1,01 x 10ml = 10,1 gram
Massa kloroform 6 ml = 1,44 x 6 ml = 8,64 gram
Massa air 5 ml = 0,75 x 5 ml = 3,75 gram
%W/W = (Berat zat terlarut/berat larutan total) x 100 %
kloroform 3 ml :
massa larutan total= (4,32+3,75+7,575)=15,645 gram
% W/W (kloroform)= 4,32/15,645 x 100% = 27,61%
% W/W (air)= 3,75/15,645 x 100% =23,96%
% W/W (asam asetat galsial )= 7,575/15,645 x 100% = 48,41 %
kloroform 5 ml:
massa larutan total : (5,76+7,2+10,1)= 23,06 gram
% W/W (kloroform)= 5,76/23.06x 100% = 24,97%
% W/W (air)= 7,2/23,06 x 100% = 31,22%
% W/W (asam asetat glasial)= 10,1/23,06 x 100% =43,79 %
kloroform 6 ml
massa larutan total : (8,64 + 3.75+10,201)= 22,591 gram
% W/W (kloroform)= 8,64/22,591 x 100% = 38,24%
% W/W (air)= 3,75/22,591 x 100% = 16,59%
% W/W (asam asetat glasial)= 10,201/22,591 x 100% = 45,15 %
%V/V= (volume zat terlarut: volume larutan total) x 100 %
kloroform 3 ml :
volume larutan total= (3+5+7,5)= 15,5 ml
% V/V (kloroform)= 3/15,5x 100% =19,35 %
% V/V (air)= 5/15,5x 100% =32,25%
% V/V (asam asetat galsial )=7,5/15,5 x 100% = 48,38%
%V/V= (volume zat terlarut: volume larutan total) x 100 % kloroform 5 ml :
volume larutan total= (5+5+10)= 20 ml
% V/V (air)= 5/20x 100% =25%
% V/V (asam asetat galsial )=10/20 x 100% = 50 %
%V/V= (volume zat terlarut:x volume larutan total) x 100 %
kloroform 6 ml :
volume larutan total= (6+5+10,1)= 21,1gram
% V/V (kloroform)= 6/21,1x 100% = 28,43%
% V/V (air)= 5/21,1x 100% =23,69%
PEMBAHASAN
Praktikum kali ini membahas tentang kesetimbangan fasa. Dengan memakai 3 jenis
larutan yang sifatnya berbeda. Diantaranya ada air yang brsifat polar,kloroform bersifat
non polar, dan asam asetat glacial yang bersifat semi polar. Ketiga zat yang berbeda sifat
ini digunakan karena ketika dicampurkan, larutan ini tidak bercampur seutuhnya,
melainkan hanya sebagian. Sebelumnya praktikan harus mengukur massa jenis dari ketiga
zat tersebut. Dengan menggunakan piknometer.
Prosedur dari praktikum ini yaitu mencampurkan klorofom dengan aquadest lalu
menitrasinya dengan asam asetat glasial. Ketika cairan kloroform dicampurkan dengan
aquades terbentuk dua fasa yang tidak saling bercampur seperti minyak dengan air. Lalu
dititrasi dengan asam asetat glasial sambil menggoyangkan labu erlenmeyer dan secara
perlahan-lahan berubah menjadi satu fasa. Tetapi jika dibiarkan terlalu lama, terbentuk lagi
menjadi dua fasa. Kesetimbangan fasa yang dimaksud adalah ketika campuran kloroform
dengan aquades sudah mencapai titik setimbang menjadi satu fasa dengan penambahan
setetes demi setetes asam asetat glasial. Volume kloroform sebanyak 3 ml mendapatkan
kesetimbangan fasa dengan titrasi asam asetat 7,5 ml. Volume kloroform sebanyak 5 ml
mendapatkan kesetimbangan fasa dengan titrasi asam asetat 10 ml. Dan volume kloroform
sebanyak 6 ml mendapatkan kesetimbangan fasa dengan titrasi asam asetat 10,1 ml. Hal
itu menunjukkan bahwa makin banyak volume asam asetat yang digunakan maka makin
banyak pula volume asam asetat glasial yang ditambahkan untuk mendapatkan
KESIMPULAN
Berdasarkan data hasil praktikum dapat disimpulkan bahwa :
Massa jenis akuades adalah 0,75 gr/ml
Massa jenis asam asetat glasial adalah 1,01 gr/ml Massa jenis kloroform adalah 1,44 gr/ml
Semakin banyak volume kloroform maka semakin banyak pula volume asam asetat
gliseral yang dibutuhkan untuk menitrasi kloroform
Asam asetat bersifat semi polar, akuades bersifat polar, dan kloroform bersifat nonpolar
DAFTAR PUSTAKA
Milama, Burhanudin. 2014. Panduan Praktikum Kimia Fisika 2. Jakarta: P-IPA FITK
UIN jkt press
S K Dogra & S Dogra. 2009. Kimia Fisik dan Soal-soal. Jakarta: Universitas Indonesia
press
Unlam,2008.
http://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=8&cad=rja&uact= 8&ved=0CGEQFjAH&url=http%3A%2F%2Falchemist08.files.wordpress.com%2F2012%2F
05%2Fpercobaan-iii-diagram-terner.doc&ei=j0VZU- XVO8iUiAfc34DYDg&usg=AFQjCNGSOhVJk5FNKwcAoXVl21_VUrtcNA&sig2=9nGkumaVy-emHVjLFjxVdA&bvm=bv.65397613,d.aGc
Widjajanti,Endang,2008.
Http://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=2&cad=rja&uact= 8&ved=0CC4QFjAB&url=http%3A%2F%2Fstaff.uny.ac.id%2Fsystem%2Ffiles%2Fpengabdi