1
PENGARUH PENAMBAHAN Al2O3 TERHADAP STRUKTUR DAN
DIELEKTRISITAS LEAD SILICATE GLASSES (GLASS FUNGSIONAL PbO-SiO2) BERBASIS PASIR BANCAR TUBAN
Desi Ayu Natalia1, Markus Diantoro1, Nandang Mufti1
1)Jurusan Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Negeri Malang
Email : natalia_desiayu@yahoo.com
ABSTRAK
Glass merupakan material amorf padat (non kristalin) yang bening dan transparan. Glass pada umumnya dibuat dari campuran 75% silika dioksida (SiO2) dan senyawa tambahan lain seperti Na2O, CaO, dll. Penambahan senyawa ini bertujuan untuk menurunkan titik leleh silika. Sintesis glass dengan variasi fungsi komposisi dan parameter lainnya juga diperlukan untuk menggali optimalisasi sifat dan struktur mikroskopis glass. Penggunaan PbO sebagai campuran glass dapat memberikan efek yang baik pada sifat optis glass. Penambahan senyawa Al2O3 pada glass sebagai doping juga dapat meningkatkan konstanta dielektrik glass. Penelitian ini menggunakan pasir Bancar Tuban sebagai sumber silika. Pasir kemudian dileaching menggunakan HCl untuk meningkatkan kemurnian silika dan dilakukan uji XRF. Pembuatan glass dilakukan dengan menggunakan metode pelelehan. Serbuk silika dicampur dengan berbagai rasio SiO2:Na2CO3:PbO:Al2O3. Selanjutnya, campuran lead silicate glasses (glass fungsional PbO-SiO2) dengan doping Al2O3 dilelehkan pada suhu 970
o
C dan diannealing pada suhu 300 oC. Kemudian dilakukan karakterisasi XRD, FTIR, SEM-EDX dan pengukuran delektrisitas menggunakan kapasitansi meter dengan variasi intensitas cahaya. Hasil XRD menunjukkan bahwa struktur glass berupa amorf. Penambahan Al2O3 tidak mengubah struktur kristal, namun mengubah struktur ikatan glass fungsional PbO-SiO2 yang ditunjukkan oleh hasil FTIR. Berdasarkan hasil FTIR terlihat adanya pergeseran nilai transmitansi glass. Morfologi dan komposisi glass ditunjukkan oleh hasil SEM-EDX. Hasil pengukuran dielektrisitas menunjukkan bahwa konstanta dielektrik glass meningkat seiring dengan penambahan Al2O3. Peningkatan intensitas menyebabkan konstanta dielektrik glass meningkat. Secara detail terlihat adanya peningkatan secara diskontinyu atau tidak linier. Kemungkinan besar terjadi kuantisasi ketika glass dikenai cahaya.
Kata Kunci : metode pelelehan, struktur, dielektrisitas, Al2O3, lead silicate glasses.
ABSTRACT
Glass is defined as amorphous solid which have characteristic of clear and transparent. Glass is generally made of a mixture of 75% silicon dioxide (SiO2) and other additional compounds such as Na2O, CaO, etc. The addition of these compounds aims to lower the melting point of silica. Synthesis glass as function of composition variation and other parameter also needed to explore the nature and structure optimization of microscopic glass The use of PbO as a mixture of glass can give a good effect on the optical properties of glass. The addition of Al2O3 compounds on glass as doping also can increase the dielectric constant glass. This study uses Bancar Tuban Sand as source of silica. The sand was leaching using Hydrochloric Acid to improve the purity of silica, and then investigated by XRF. Manufacture of glass is done by using melting method. Silica powder was mixed with various ratio of SiO2:Na2CO3:PbO:Al2O3. Subsequently, a mixture of lead silicate glasses (PbO-SiO2 functional glass) with Al2O3 doping melted at a temperature of 970 ° C and annealed at 300 oC. Glass sample was investigated by XRD, FTIR, SEM-EDX and measuring of dielectric constant use capacitance meter with variety of light intensity. Result of XRD show that structure of glass is amorphous. The addition of Al2O3 not alter the crystal structure, but changing the structure of the functional glass bonding PbO-SiO2 shown by the FTIR results. Based on the results of FTIR seen a shift in the value of transmittance glass. Morphology and composition of the glass indicated by the results of SEM-EDX. Measuring result of dielectricity show that the dielectric constant of glass increases with the addition of Al2O3. Increasing the intensity increases causing the dielectric constant glass. In detail seen an increase in discontinuous or not linear. Most likely to occur quantization when glass sample exposed to light.
2
Key word : melting method, structure, dielectricity, Al2O3, lead silicate glasses.
PENDAHULUAN
Glass merupakan material amorf padat (non kristalin) yang bening dan transparan. Perbedaan utama antara glass dan kristal yaitu
pada susunan atomnya. Glass
memiliki struktur atom yang tidak teratur (amorphous solid), sedangkan kristal memiliki struktrur atom yang teratur dan periodik. (Van Vlack, 2001:115).
Glass pada umumnya dibuat dari campuran 75% silika dioksida (SiO2) ditambah dengan Na2O, CaO dan beberapa senyawa lainnya. Penambahan ini bertujuan untuk meningkatkan sifat elektrik, optik, sifat transparansi maupun sifat terma. Sintesis dengan variasi fungsi komposisi dan parameter lainnya juga diperlukan untuk menggali optimalisasi sifat dan struktur mikroskopis glass (Gautam, 2013). Soda atau sodium karbonat, Na2CO3
biasanya ditambahkan untuk
menurunkan titik lebur sampai sekitar 1000 oC (Callister, 2010:465). Glass silika transparan memiliki banyak keuntungan seperti koefisien ekspansi termal dan konsuktivitas listrik yang rendah serta ketahanan kimia dan transparasi UV yang tinggi (Morinaga, 2002), biasanya juga efektif sebagai isolator (Callister, 2010:503).
Indonesia memiliki sumber daya alam yang sangat melimpah, termasuk silika sebagai bahan dasar pembuatan glass. Akan tetapi, faktanya bahan dasar pembuatan glass di Indonesia masih merupakan bahan impor. Semakin meningkat kebutuhan akan bahan dasar dan barang jadi dari glass membuat kecenderungan untuk impor juga
akan semakin meningkat (Lukman, 2009).
Penelitian ini menggunakan pasir Bancar Tuban sebagai sumber silika. Pantai Bancar Tuban Jawa Timur merupakan salah satu daerah yang memiliki pasir kuarsa yang sangat melimpah. Kandungan unsur silika ditemukan paling tinggi dibandingkan dengan unsur lainnya (Hadi, 2009). Penggunaan PbO
sebagai bahan campuran glass
memberikan efek yang baik pada sifat optis glass.
Al2O3 memiliki konstanta dielektrik lebih tinggi dibandingkan
dengan SiO2. Senyawa SiO2
memiliki konstanta dielektrik sebesar 3,8 sedangkan konstanta dielektrik
Al2O3 berkisar antara 9-10
(Mousumi, 2010). Penambahan
senyawa Al2O3 pada glass sebagai
doping diharapkan dapat
meningkatkan konstanta dielektrik glass. Penelitian yang dilakukan oleh
Doweidar (2001) menyatakan
bahwa penambahan Al2O3 telah meningkatkan resistivitas listrik dan energi aktivasi pada system glass Na2O-Al2O3-B2O3. Pengaruh penambahan Al2O3 pada system glass BaO-ZnO-B2O3-SiO2-Li2 O-Na2O juga telah diteliti oleh
Mousumi (2010). Konstanta
dielektrik glass BaO-ZnO-B2O3 -SiO2-Li2O-Na2O meningkat seiring peningkatan Al2O3.
Sejauh ini di Indonesia belum
ditemukan penelitian secara
komprehensif mengenai kajian
tentang sintesis glass berbasis pasir alam. Permasalahan yang paling mendasar dalam penelitian ini adalah bagaimana mensintesis silika dari bahan alam secara tepat supaya dapat digunakan sebagai bahan glass.
3
Pemilihan metode dan juga dopan yang tepat sangat penting dalam mensitesis glass. Dopan yang dipilih harus memenuhi kriteria yang cocok untuk menurunkan titik leleh dan meningkatkan sifat fisisnya. Oleh karena itu perlu dilakukan penelitian tentang Pengaruh Al2O3 Terhadap
Struktur dan Dielektrisitas Lead
Silicate Glasses (Glass Fungsional
PbO-SiO2) Berbasis Pasir Bancar
Tuban.
METODE EKSPERIMEN
Sintesis glass fungsional PbO-SiO2 dengan doping Al2O3
dilakukan dengan menggunakan
metode pelelehan (melt quench
method). Tahap pertama, pasir
Bancar dileaching menggunakan
HCl untuk meningkatkan kemurnian silika. Kandungan silika dalam pasir Bancar kemudian dikarakterisasi menggunakan XRF. Selanjutnya,
pembuatan glass fungsional
dilakukan dengan mencampur serbuk
silika dengan berbagai rasio
SiO2:Na2CO3:PbO:Al2O3. Campuran glass dilelehkan pada suhu 970 oC dengan penahanan selama 1 jam. Selanjutnya, diannealing pada suhu 300 oC dan dilakukan penahanan selama 0.5 jam. Glass didinginkan secara lambat selama 7 jam hingga mencapai suhu ruang. Hasilnya, glass terlihat transparan dan berwarna kuning.
Sampel glass kemudian
dikarakterisasi dengan menggunakan XRD untuk melihat struktur glass, FTIR untuk melihat struktur glass
berdasarkan formasi ikatan.
Morfologi dan komposisi glass dikarakterisasi menggunakan SEM-EDX. Selanjutnya, dielektrisitas glass diselidiki dengan mengukur nilai kapasitansi menggunakan kapasitansi meter. Berdasarkan nilai
kapasitansi maka dapat diketahui nilai konstanta dielektrik yang menunjukkan dielektrisitas glass.
(Persamaan 1)
Pengukuran dielektrisitas
dilakukan dengan memberikan
intensitas cahaya pada sampel untuk mengetahui respon glass terhadap intensitas. Sumber intensitas cahaya berasal dari lampu pijar 100 watt yang difokuskan menggunakan lensa cembung.
HASIL DAN PEMBAHASAN Hasil Uji XRF
Hasil uji XRF menunjukkan kandungan unsur dalam pasir Bancar sebelum dan sesudah dilakukan proses ekstraksi. Kandungan unsur silika dalam pasir sebelum ekstraksi sebesar 80.7% dan sesudah ekstraksi menjadi 86.8%.
Hasil Uji XRD
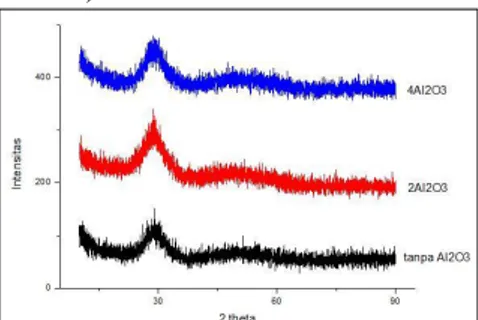
Berdasarkan hasil uji XRD, pola difraksi pada ketiga sampel glass tanpa doping Al2O3, sampel glass dengan doping Al2O3 2% mol, dan sampel glass dengan doping Al2O3 4% menunjukkan bahwa strukturnya berupa amorf (non kristalin).
Gambar 1. Struktur Glass Fungsional dengan doping 0 % mol Al2O3, 2 % mol Al2O3 dan 4 % mol Al2O3
Hasil Uji FTIR
Data hasil uji FTIR berupa grafik hubungan antara panjang gelombang dan transmitansi. Pada
4
sampel glass tanpa doping Al2O3 (Gambar 2) menunjukkan adanya ikatan Si-O-Si dengan vibrasi ikatan pada tetrahedral SiO4 pada panjang gelombang 477 cm-1. Gambar 3 merupakan hasil uji FTIR dari sampel glass dengan doping 2% mol Al2O3. Pada panjang gelombang 657 cm-1 terdapat ikatan Al-O-Al dengan vibrasi regangan asimetri pada unit
oktahedral AlO6 pada molekul
Al2O3.
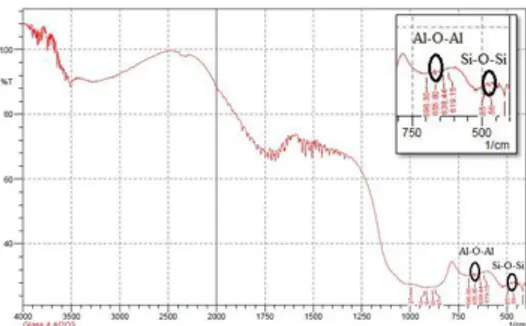
Gambar 2. FTIR sampel glass tanpa doping Al2O3
Gambar 3. FTIR sampel glass dengan doping 2% mol Al2O3
Hasil uji FTIR dari sampel glass dengan doping 4% mol Al2O3 (Gambar 3) menunjukkan adanya vibrasi ikatan Al-O-Al pada panjang gelombang 655 cm-1 dengan vibrasi
regangan asimetri pada unit
oktahedral AlO6 pada molekul
Al2O3. Selain itu juga terlihat adanya vibrasi ikatan Si-O-Si pada panjang gelombang 472 cm-1 dengan vibrasi ikatan pada tetrahedral SiO4.
Gambar 4. FTIR sampel glass dengan doping 4% mol Al2O3
Gambar 5 menunjukkan hasil uji FTIR dari sampel glass dengan doping 6% mol Al2O3. Vibrasi ikatan
Al-O-Al terjadi pada panjang
gelombang 462 cm-1 dengan vibrasi ikatan pada unit oktahedral AlO6 pada molekul Al2O3. Selain itu juga terlihat adanya vibrasi ikatan Si-O-Si pada panjang gelombang 475 cm-1
dengan vibrasi ikatan pada
tetrahedral SiO4.
Gambar 5. FTIR sampel glass dengan doping 6% mol Al2O3
Perbandingan hasil FTIR keempat sampel glass ditunjukkan oleh Gambar 6. Penambahan Al2O3
menyebabkan adanya perubahan
struktur formasi ikatan berdasarkan nilai transmitansi. Semakin tinggi
persentase mol Al2O3 yang
ditambahkan pada glass
menyebabkan terjadinya penurunan nilai transmitansi. Pada panjang gelombang diatas 1900 cm-1 terjadi penurunan nilai transmitansi seiring
dengan penambahan Al2O3,
sedangkan untuk panjang gelombang dibawah 1900 cm-1 terjadi penurunan
5
nilai transmitansi sampai pada batas optimum penambahan 4 % mol Al2O3. Penambahan 6 % mol Al2O3 menyebabkan terjadinya peningkatan kembali nilai transmitansi.
Gambar 6. Perbandingan FTIR sampel glass doping 0 % mol Al2O3, 2 % mol Al2O3 dan 4 % mol Al2O3 dan 6 % mol Al2O3
HASIL SEM-EDX
Berdasarkan hasil uji
SEM-EDX diperoleh data morfologi
sampel glass (Gambar 7). Morfologi glass dengan perbesaran 1000 kali
tidak menunjukkan adanya
perbedaan antara sampel glass tanpa Al2O3, dengan doping 2 % mol Al2O3, 4 % mol Al2O3, 6 % mol Al2O3.Namun, secara umum keempat sampel tersebut terlihat homogen.
Gambar 7. Morfologi glass (a) tanpa Al2O3 (b) 2 % mol Al2O3 (c) 4 % mol Al2O3 (d) 6 % mol Al2O3 dengan Perbesaran 1000 kali
Komposisi glass untuk
sampel dengan doping 4 % mol Al2O3 ditunjukkan pada Tabel 1. Pb memiliki komposisi paling tinggi yaitu 80,7% berat total dan berada pada kulit L. Unsur yang menempati kulit K diantaranya unsur Oksigen dengan komposisi sebesar 8,51% berat total, Na sebesar 1,12%, Al sebesar 1,55% dan Si sebesar 8,08%.
Tabel 1. Komposisi glass berdasarkan EDX
Element Tanpa Al2O3 2 % mol Al2O3 4 % mol Al2O3 6 % mol Al2O3 Wt% At% Wt% At% Wt% At% Wt% At% OK 07.64 38.14 06.80 35.07 08.51 40.44 06.73 35.09 NaK 01.78 06.20 01.26 04.52 01.12 03.71 00.64 02.31 AlK - - 01.08 03.29 01.55 04.35 01.88 05.81 SiK 08.43 23.98 08.22 24.17 08.08 21.88 07.87 23.38 PbL 82.16 31.69 82.65 32.94 80.73 29.62 82.89 33.40 Konstanta Dielektrik
Berdasarkan hasil uji
dielektrisitas menggunakan
kapasitansimeter diperoleh grafik hubungan antara intensitas dan konstanta dielektrik. Gambar 8
merupakan grafik hubungan antara intensitas dan konstanta dielektrik sampel glass PbO-SiO2 tanpa Al2O3.
Gambar 9 merupakan grafik
hubungan antara intensitas dan konstanta dielektrik sampel glass PbO-SiO2 dengan doping 2 % mol
6
Al2O3. Gambar 10 merupakan grafik hubungan antara intensitas dan konstanta dielektrik sampel glass PbO-SiO2 dengan doping 4 % mol Al2O3. Grafik hubungan antara intensitas dan konstanta dielektrik sampel glass PbO-SiO2 dengan doping 6 % mol Al2O3 disajikan pada Gambar 11.
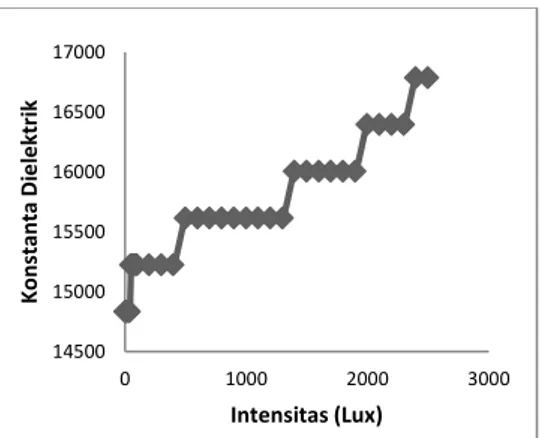
Gambar 8. Grafik Hubungan antara Intensitas dan Konstanta Dielektrik Glass PbO-SiO2 (tanpa Al2O3)
Gambar 9. Grafik Hubungan antara Intensitas dan Konstanta Dielektrik Glass PbO-SiO2 dengan 2 % mol Al2O3
Gambar 10. Grafik Hubungan antara Intensitas dan Konstanta Dielektrik Glass PbO-SiO2 dengan 4 % mol Al2O3
Gambar 11. Grafik Hubungan antara Intensitas dan Konstanta Dielektrik Glass PbO-SiO2 dengan 6 % mol Al2O3
Konstanta dielektrik glass
meningkat seiring dengan
peningkatan intensitas yang
diberikan. Hal ini menunjukkan
adanya respon glass terhadap
intensitas cahaya dimana
menunjukkan adanya sifat
optoelektrik glass. Bedasarkan grafik
terlihat adanya peningkatan
konstanta dielektrik seiring dengan
meningkatnya intensitas yang
diberikan. Secara detail terlihat
adanya diskontinyuitas yang
menyebabkan peningkatan tersebut terlihat bertingkat (step like). Hal ini disebabkan oleh adanya interaksi antara cahaya dan bahan yang berkaitan dengan absorpsi atau transmitansi. Frekuensi dari cahaya
11000 11500 12000 12500 13000 13500 14000 14500 0 1000 2000 3000 K ons tant a D ie le kt ri k Intensitas (Lux) 14000 14500 15000 15500 16000 16500 0 500 1000 1500 2000 2500 3000 K ons tant a D ie le kt ri k Intensitas (Lux) 14500 15000 15500 16000 16500 17000 0 1000 2000 3000 K ons tant a D ie le kt ri k Intensitas (Lux) 45000 46000 47000 48000 49000 50000 51000 52000 0 1000 2000 3000 K ons tant a D ie le kt ri k Intensitas (Lux)
7
yang dapat diserap oleh bahan sesuai dengan frekuensi dari vibrasi atom dalam sampel glass. Kemungkinan besar juga terjadi kuantisasi sehingga untuk menaikkan nilai konstanta dielektrik dibutuhkan rentang energi tertentu dari intensitas cahaya.
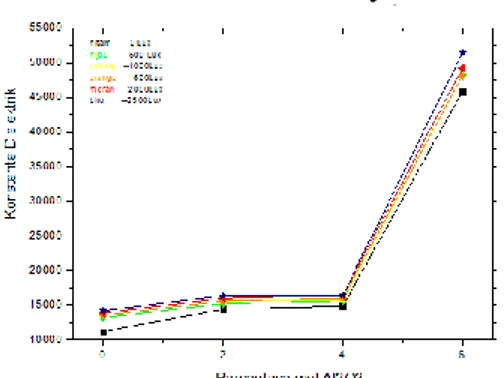
Gambar 12. Grafik Hubungan antara Presentase mol Al2O3 dan Konstanta Dielektrik Glass dengan Intensitas 0 Lux, 500 Lux, 1000 Lux, 1500 Lux, 2000 Lux dan 2500 Lux
Berdasarkan Gambar 12
teradi peningkatan konstanta
dielektrik seiring dengan
penambahan persentase Al2O3. Demikian pula dengan penambahan intesitas dari 0 Lux, 500 Lux , 1000 Lux, 1500 Lux, 2000 Lux dan 2500
Lux juga meningkatkan nilai
konstanta dielektrik glass.
KESIMPULAN
Glass PbO-SiO2 dengan
doping Al2O3 telah berhasil disintesis dengan metode pelelehan (melt
quench method) pada suhu 970 oC. Hasil glass berwarna kuning dan
tampak bening (transparan).
Penambahan Al2O3 tidak mengubah struktur kristal glass fungsional PbO-SiO2 yang ditunjukkan oleh pola difraksi XRD, namun mengubah
struktur formasi ikatan yang
ditunjukkan oleh hasil FTIR. Selain
itu, penambahan Al2O3
menyebabkan konstanta dielektrik
glass fungsional PbO-SiO2
meningkat. Glass menunjukkan
respon terhadap intensitas cahaya. Hal ini ditunjukkan dengan adanya peningkatan konstanta dielektrik glass fungsional PbO-SiO2 seiring peningkatan intensitas.
DAFTAR RUJUKAN
Ahsan, dkk. 2005. Infrared Study of the effect of P2O5 in the Structure of Lead Glasses.
Indian Journal of Pure & Applied Physics.
Callister, D. William. 2010.
Fundamental of Materials Science and engineering. The
University of Utah:
Department of Metallurgical Engineering.
Doweidar, dkk. Properties of Na2 O-Al2O3-B2O3 glasses. Material
Science and Enginering A301
(2001) 207-21.
Gautam, C. R. and A. K. Yadav. 2013. Synthesis and Optical Investigations on (Ba,Sr) TiO3 Borosilicate Glasses Doped with La2O3. Optics
and Photonic Journal.
Gautam, C. R. and A. K. Yadav. 2013. Synthesis, IR,
Crystallization and Dielectric Study of (Pb, Sr)TiO3
Borosilicate glass-ceramics.
Indian Academy of Sciences.
Gautam, C. R. and A. K. Yadav. 2010. IR Study of Pb-Sr Titanate Borosilicate Glasses.
Indian Academy of Sciences.
Gautam, C. R. and A. K. Yadav. 2012. A Review on Infrared Spectroscopy of
BorateGlasses with Effects of Different Additives.
8 International Scholarly
Research Network.
Gautam, C. R. dkk. 2011.
Crystallization Behavior and Microstructural Analysis of Lead-Rich (PbxSr1-x)TiO3 Glass Ceramics Containing 1 mole % La2O3. Hindawi
Publishing Corporation: Research Article.
Gowda, Veeranna V.C. dkk. 2013. A new approach for
understanding ion transport in glasses; example of complex alkali diborate glasses containing lead, bismuth and tellurium oxides. Indian
Academy of Sciences.
Gao, Peng dkk. 2012. Low
Temperature Sintering and Dielectric Properties of Ba0.6Sr0.4TiO3-MgO Composite Ceramics with CaO-B2O3-SiO2 glass addition. Journal of Alloys
and Compounds.
Hadiyawarman. 2008. Fabrikasi Material Nanokomposit Superkuat, Ringan dan Transparan Menggunakan Metode Simple Mixing.
Jurnal Nanosains &
Nanoteknologi, Vol. 1 No.1
Iskandar, S.M. 2010. Optical and Structural Properties of PbO-B2O3-TeO2 Glasses. Solid
State and Technology, Vol.
18. No 2 84-90. Jialin, Chen dkk. Tuning the
interfacial reaction between CaO-SrO-Al2O3-B2O3 SiO2 sealing glass-ceramic and Cr-containing interconnect:
Crystalline structure vs. glass structure. Journal of the
European Ceramic Society 34
(2014) 1989-1996.
Kalogeras, Ionnis M. dkk. 2012. The Nature of the Glassy State; Structure and Glass
Transitions. Journal of
Material Education.
Kenji Morinaga, dkk. 2002. Fabrication of transparent silica glass by powder sintering. Science and
Technology of Advenced Materials 3, 297-301.
Kittel, Charles. 2004. John Wiley &
Sons, Inc: Introduction to Solid State Physics. Berkeley:
University of California. Lukman, Mita Wulandari. 2009.
Sintesis Biomaterial
Komposit CaO-SiO2 Berbasis Material Alam (Batuan Kapur dan Pasir Kuarsa) dengan Variasi Suhu
Pemanasan dan Pengaruhnya terhadap Porositas,
Kekerasan dan
Mikrostruktur. FMIPA
Universitas Negeri Malang. Mizuno, Megumi dkk. 2005.
Leaching of Lead and Connectivity of Plumbate Networks in Lead Silicate Glass. Journal American
Ceramic Society.
Mousumi, dkk. 2010. Influence of combined Al2O3-SiO2 filler on thermal and dielectric properties of barium zinc borate glass microcomposites for barrier ribs of plasma display panels. Indian
9 Journal of Engineering &
Materials Sciences, Vol. 17
pp 199-207.
Newnham, R.E. 2005. Properties of
Material: Anisotropy, Symetri, Structure. Oxford: