BAB III
METODE PENELITIAN
3.1. Rancangan penelitian
Penelitian ini merupakan suatu penelitian observasional analitik dengan rancangan case control. Pada penelitian ini dilakukan pemeriksaan ekspresi imunohistokimia Human Epididymis Protein 4 terhadap blok paraffin jaringan kista ovarium jinak dan ovarium normal.
Dalam penelitian ini, tidak diberikan perlakuan terhadap variabel, namun hanya dilihat hasil pulasan immunohistokimia HE4. Pengukuran variabelnya hanya dilakukan satu kali dan pada satu saat.
3.2. Tempat dan waktu penelitian
`Penelitian ini dilakukan di Departemen Obstetri dan Ginekologi Fakultas Kedokteran USU, dan pemeriksaan imunohistokimia dilakukan di Laboratorium Departemen Patologi Anatomi Fakultas Kedokteran Universitas Sumatera Utara Medan. Penelitian ini dilakukan bulan Mei hingga Juni 2017.
3.3. Subjek Penelitian
Objek penelitian kelompok kasus adalah blok paraffin jaringan kista ovarium benigna yang diperoleh dari operasi ginekologi kista ovarium benigna.
karsinoma endometrium stadium dini, yang memiliki hasil histopatologi ovarium dalam batas normal.
3.4. Besar Sampel Penelitian
Besar sampel penelitian dihitung secara statistik dengan rumus87 :
dimana :
Zα = nilai baku normal dari tabel Z yang besarnya bergantung pada nilai α yang ditentukan. Nilai α=0,10 Zα= 1,64
Zβ= nilai baku normal dari tabel Z yang besarnya bergantung pada nilai β yang ditentukan. Nilai β=0,20 Zβ= 0,84
P2= Proporsi pada kista ovarium benigna = 0,2 25 Q2= 1-P2 = 0,8
P1= Proporsi pada kelompok yang nilainya merupakan ketetapan peneliti = 0,8
Q1= 1-P1 = 0,2
P1-P2= Selisih proporsi minimal yang dianggap bermakna= 0,6
P= Proporsi total = = 0,5 Q= 1-P = 0,5
Maka perhitungan besar sampel penelitian berdasarkan rumus tersebut didapatkan besar sampel minimal untuk masing-masing kelompok adalah n1= n2= 18,63 dibulatkan 19 sampel (jumlah sampel masing-masing kasus dan kontrol), sehingga total besar sampel minimal pada penelitian ini adalah 38 sampel. Namun pada penelitian ini akan dilakukan pemeriksaan imunohistokimia HE4 pada blok paraffin kista ovarium benigna sebanyak 20 sampel, dan blok paraffin jaringan ovarium normal sebanyak 20 sampel, sehingga total akan diperiksa sebanyak 40 sampel.
3.5. Kriteria Penelitian 3.5.1. Kriteria Inklusi 3.5.1.1. Kelompok Kasus
Blok parafin jaringan kista ovarium benigna yang memenuhi kriteria inklusi sebagai berikut :
1. Wanita dengan kista ovarium benigna
2. Leukosit < 11.000/mm3 , tidak dijumpai fokal infeksi 3. Tidak mempunyai riwayat tumor non ginekologis 4. Tidak mempunyai penyakit ginjal
3.5.1.2. Kelompok Kontrol
dini, yang memiliki hasil histopatologi ovarium dalam batas normal serta memenuhi kriteria inklusi sebagai berikut :
1. Wanita yang menjalani pembedahan Total Abdominal Histerektomi – Bisalfingoooforektomi dengan diagnosa non kista ovarium.
2. Tidak mempunyai penyakit ginjal.
3. Tidak mempunyai penyakit tumor non ginekologis lainnya.
3.5.2. Kriteria Eksklusi
Kriteria Eksklusi untuk kelompok kasus dan kontrol adalah :
1. Sediaan tidak dapat dianalisa oleh sebab pembuatan blok paraffin yang tidak baik atau blok paraffin telah rusak.
2. Tidak memenuhi kriteria inklusi 3.6. Etika Penelitian
Penelitian ini diajukan ke Komisi Etika Penelitian Fakultas Kedokteran Universitas Sumatera Utara untuk mendapatkan Ethical Clearence, setelah mendapatkan persetujuan dari Departemen Patologi Anatomi Fakultas Kedokteran Universitas Sumatera Utara Medan untuk pemeriksaan sampel blok paraffin di Laboratorium Patologi Anatomi Fakultas Kedokteran Universitas Sumatera Utara Medan.
3.7. Cara Kerja Penelitian
Universitas Sumatera Utara, berupa blok paraffin kista ovarium benigna dan ovarium normal.
2. Dari data histopatologi tersebut, diambil data rekam medik tentang identitas lengkap dan karakteristik pasien.
3. Dilakukan pewarnaan imunohistokimia. Prosedur imunohistokimia dilakukan di Departemen Patologi Anatomi Fakultas Kedokteran Universitas Sumatera Utara dengan melakukan pewarnaan imunohistokimia Human HE4 Antibody (R & D system). Dengan prosedur pelaksanaan sebagai berikut :
a. Deparafinisasi slide (dengan Xylol 1, Xylol 2, Xylol 3) masing-masing dikerjakan selama 5 menit
b. Kemudian dilakukan rehidrasi dengan alkohol absolute, alkohol 95%, alkohol 80%, alkohol 70%) selama 4 menit
c. Lalu dicuci dengan air mengalir selama 5 menit
d. Masukkan slide ke dalam PT Link Deko Epitope Retrieval : set up pretreat 65°C, running time 98°C selama 15 menit
e. Pap pen, segera masukkan dalam Tris Buffered Saline (TBS) pH 7,4 selama 9 menit
Tabel 3.7. Prosedur Pewarnaan
LANGKAH INSTRUKSI PENCUCIAN/
WAKTU
Pretreatment Sesuai dengan petunjuk dari data
sheet antibody primer
3x2 menit
Jaringan Primer Aplikasi reagensia dan inkubasi selama 5 menit pada suhu ruangan
3x2 menit
Parafin Blok Aplikasi reagensia dan inkubasi selama 5 menit pada suhu ruangan Antibodi Primer Sesuai dengan petunjuk dari data
sheet antibody primer
3x2 menit
PolyVue PlusTM Enhancer
Aplikasi reagensia dan inkubasi selama 10 menit pada suhu ruangan
3x2 menit
PolyVue PlusTM HRP
Aplikasi reagensia dan inkubasi selama 10 menit pada suhu ruangan
3x2 menit
DAB/ Plus Aplikasi reagensia dan inkubasi selama 5 menit pada suhu ruangan
3x2 menit
Mayer’s Hematoxylin
Aplikasi reagensia dan inkubasi selama 2 menit pada suhu ruangan lalu dicuci dengan air
3x2 menit
Dehidration/
Clearing/ Mounting
3.8. Alat, Bahan Penelitian dan Instrumen Penelitian 3.8.1. Alat-alat Penelitian
Alat-alat yang diperlukan untuk penelitian ini adalah : Mikrotom,
waterbath. Hot plate, Freezer, inkubator, staining jar, rak kaca objek, kaca objek, rak inkubasi, Pensil Diamond, Pipet Mikro, timbangan bahan kimia, kertas saring, pengukur waktu, gelas Erlenmeyer, gelas beker, tabung sentrifuge, microwave, thermolyte stirrer, kaca penutup, entelan dan mikroskop cahaya.
3.8.2. Bahan Penelitian
o Blok paraffin yang telah didiagnosa dengan pulasan Hematoksilin Eosin
sebagai jaringan kista ovarium.
o Pulasan immunohistokimia menggunakan metode The EnVision + Dual Link System kit, teknik pulasan IHK 2 langkah. Antibodi primer yang digunakan adalah Mouse monoclonal Hu-antibody HE4 dengan pengenceran 1 : 20.
The Envision + Dual Link System kit terdiri dari :
o 1 Botol Dual endogenous enzyme block ( 15 ml) o 1 Botol Labelled polymer –HRP ( 15 ml) o 1 Botol DAB + Substrat Buffer ( 18 ml) o 1 Botol DAB + Chromogen ( 1 ml) o Larutan PBS :
o NaCl 87,5 gr + KH2PO4 1,92 gr dalam aquadest 800 ml
o Bilas akan digunakan, harus diencerkan 10x. o Larutan Buffer Sitrat :
o Citric acid 2,1 gr dilarutkan dalam 1 liter aquadest. o Ditetesi dengan NaOH 2M sampai tercapai pH 6.
o Larutan DAB + Substrat-kromogen (1 ml larutan cukup untuk 10 jaringan)
:
o Langkah 1 : Masukkan ke aliquot 1 ml Substrat Buffer secukupnya ke
dalam kontainer ( tergantung dari jumlah spesimen yang akan dikerjakan)
o Langkah 2 : Untuk setiap 1 mL buffer, tambahkan setetes (20 μL) cairan
DAB + Kromogen, campurkan segera.
o Larutan DAB + Substrat kromogen ini hanya stabil dalam ± 5 hari bila
disimpan dalam suhu 2-8⁰C
3.8.3. Instrumen Penelitian
Instrumen penelitian yang akan digunakan adalah hasil pulasan immunohistokimia HE4 terhadap sampel sediaan jaringan kista ovarium benigna. Untuk penelitian terhadap pulasan immunohistokimia HE4 adalah sebagai berikut:
o Kontrol Positif: Jaringan yang telah diketahui positif terhadap HE4
pada penelitian terdahulu (dalam hal ini jaringan fibro adenoma mammae)
o Kontrol negatif : Kista Ovarium dengan antibodi primer
o Positif : Warna coklat yang tampil pada sitoplasma sel epitel maupun
o Dilakukan interpretasi sediaan tersebut oleh dua orang ahli Patologi
Anatomi. Pemeriksaan Histopatologi dilakukan dengan menggunakan mikroskop cahaya 400x
o Kemudian dilakukan analisis data ekspresi imunohistokimia HE4
masing-masing kelompok penelitian.
o Penilaian imunohistokimia untuk ekspresi HE4 menggunakan skor
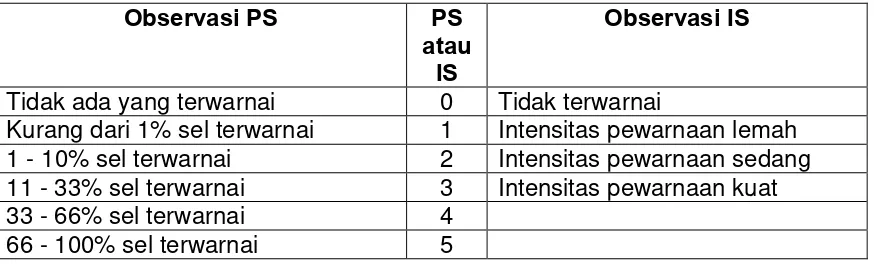
Allred karena sistem ini mempunyai sensitifitas dan spesifisitas lebih baik dibandingkan dengan penilaian secara konvensional. Skor ini adalah hasil penjumlahan skor persentase dari sel yang terwarnai atau Proportion Score (PS) dan skor intensitas pewarnaannya atau
Intensity Score (IS).
Tabel 3.8.3.1. Penilaian Proportion Score (PS) dan Intensity Score (IS).88
Observasi PS PS
atau IS
Observasi IS
Tidak ada yang terwarnai 0 Tidak terwarnai
Kurang dari 1% sel terwarnai 1 Intensitas pewarnaan lemah 1 - 10% sel terwarnai 2 Intensitas pewarnaan sedang 11 - 33% sel terwarnai 3 Intensitas pewarnaan kuat 33 - 66% sel terwarnai 4
Tabel 3.8.3.2. Interpretasi Score Allred88
Score total Interpretasi
0 – 2 Negatif
≥ 3 Positif
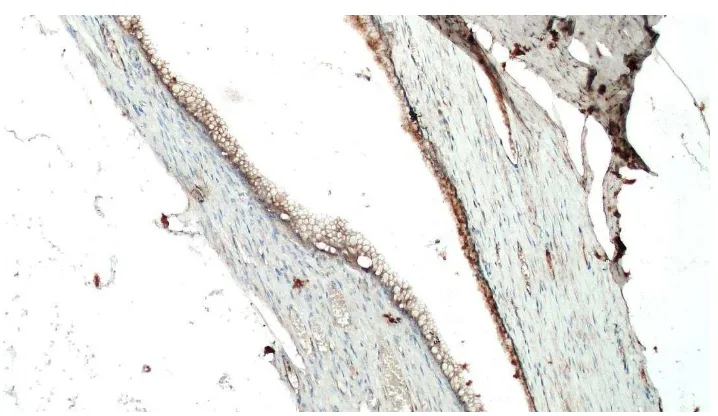
IHK HE 4, 40x (+ atau ++) No. slide: O/3926/16
IHK HE 4, 100x (+++) No. slide: O/4374/16
3.9. Analisis Data
Analisa data dan uji statistik dilakukan secara terkomputerisasi. Hasil penelitian akan disajikan ke dalam tabel distribusi frekuensi. Untuk menganalisa perbedaan akurasi dua observer akan dihitung nilai kappa, dimana jika validitas >75% maka tidak ditemukan perbedaan bermakna antara kedua pengamatan observer. Hubungan antar variabel dilakukan uji statistik Chi square dengan derajat kepercayaan 95% dan p<0,05 dianggap bermakna.
3.10. Definisi Operasional
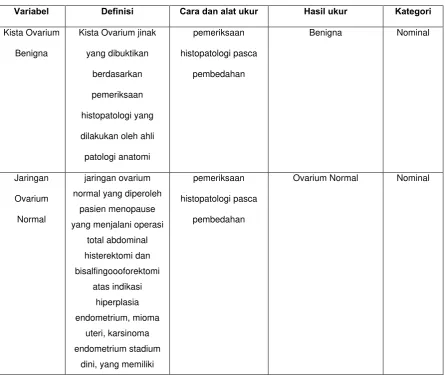
Tabel 3.10. Definisi Operasional
Variabel Definisi Cara dan alat ukur Hasil ukur Kategori
Kista Ovarium
Benigna
Kista Ovarium jinak
yang dibuktikan
hasil histopatologi
Bila terlihat tampilan
pulasan warna coklat
pada sitoplasma sel
epitel ataupun stroma
dengan menggunakan
mikroskop cahaya
pembesaran 400x pada
5 lokasi lapangan
pandang dan pada saat
yang sama kontrol (+)
juga menampilkan
warna yang sama.
Skor intensitas warna
Usia masa hidup pasien
Paritas jumlah kelahiran yang
pernah dialami
≤12 tahun >12 tahun. Nominal
3.11. Alur Penelitian
3.
Data Laporan Rekam Medik Diagnosa dan Data Umum
Pasien
Kriteria Inklusi dan Eksklusi
Sampel Blok Parafin Jaringan Ovarium
Jaringan Kista Ovarium Benigna
Jaringan Ovarium Normal
Pewarnaan Imunohistokimia Human Epididymis Protein 4
Analisa Data
BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
4.1. Hasil Penelitian
Penelitian ini menggunakan subjek penelitian kelompok kasus sebanyak 20 blok paraffin jaringan kista ovarium benigna yang diperoleh dari tindakan operasi ginekologi kasus kista ovarium jinak. Sedangkan subjek penelitian kelompok kontrol sebanyak 20 blok paraffin jaringan ovarium normal yang diperoleh dari tindakan operasi ginekologi kasus non kista ovarium benigna.
Pengamatan hasil pulasan immunohistokimia HE4 dilakukan oleh dua orang observer. Untuk menganalisa perbedaan akurasi dua observer digunakan nilai kappa, dimana didapatkan nilai uji Kappa sebesar 85,5%. Karena tidak ada perbedaan antara kedua observer, maka pada penelitian ini digunakan hasil pemeriksaan dari observer 1.
4.1.1. Karakteristik Subjek Penelitian
Tabel 4.1.1. Karakteristik Subjek Penelitian Berdasarkan Usia, Usia Menarche, Paritas, dan Indeks Massa Tubuh.
Karakteristik
Kista Ovarium Jinak Ovarium normal
(n%) (n%) orang (60%) dan lainnya dengan usia 20-50 tahun sebanyak 8 orang (40%).
Dari usia menarche baik kelompok kista ovarium jinak dan ovarium normal, terbanyak dijumpai usia menarche ≤12 tahun masing-masing 17 orang (85%) dan 15 orang (75%).
Dari indeks massa tubuh baik kelompok kista ovarium jinak dan ovarium normal, terbanyak dengan indeks massa tubuh normoweight masing-masing 14 orang (70%) dan 15 orang (75%).
4.1.2. Distribusi Histopatologi Kista Ovarium Benigna
Gambaran subjek penelitian berdasarkan klasifikasi kista ovarium benigna dapat dilihat pada tabel di bawah ini :
Tabel 4.1.2. Distribusi Histopatologi Kista Ovarium Benigna
Histopatologi Kista Ovarium Benigna Jumlah
N (%)
Epitel
Cystadenoma musinosum 8 40
Cystadenoma serosum 7 35
Kista Endometriosis 2 10
Non Epitel
Kista Dermoid 3 15
Tabel di atas menunjukkan distribusi histopatologi kista ovarium jinak, dimana terbanyak jenis epitel (85%) yaitu Cystadenoma musinosum (40%),
4.1.3. Ekspresi Immunohistokimia HE4 Pada Jaringan Kista Ovarium Benigna dan Ovarium Normal.
Hasil pengamatan terhadap ekspresi imunohistokimia HE4 pada jaringan kista ovarium benigna dan ovarium normal tampak pada tabel dibawah ini. 4.1.3. Ekspresi Immunohistokimia HE4 Pada Jaringan Kista Ovarium
Jinak dan Ovarium Normal.
Hasil pengamatan terhadap ekspresi imunohistokimia HE4 pada jaringan kista ovarium jinak dan ovarium normal tampak pada tabel dibawah ini.
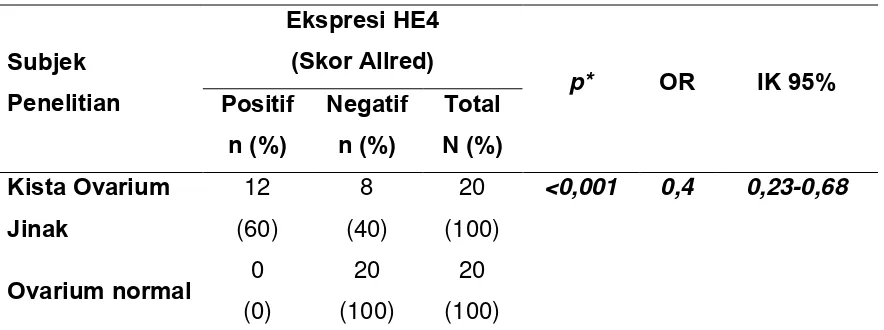
Tabel 4.1.3. Ekspresi Immunohistokimia HE4 Pada Jaringan Kista Ovarium Jinak dan Ovarium Normal.
Subjek
0,4 (IK 95% 0,23-0,68) yang berarti bahwa kista ovarium jinak memiliki kemungkinan ekspresi HE4 negatif hanya sekitar 0,4 kali lipat.
4.1.4. Ekspresi Immunohistokimia HE4 Pada Jaringan Kista Ovarium Benigna Berdasarkan Histopatologi.
Hasil pengamatan terhadap ekspresi imunohistokimia HE4 pada jaringan kista ovarium benigna berdasarkan histopatologi tampak pada tabel dibawah ini.
Tabel 4.1.4 Ekspresi imunohistokimia HE4 pada jaringan kista ovarium benigna berdasarkan subtipe histopatologi
Ekspresi HE4
p-value* Positif Negatif
n % N %
Cystadenoma musinosum 2 66,7 1 33,3 0,98
Cystadenoma serosum 5 62,5 3 37,5 0,77
Kista endometriosis 4 57,1 3 42,9 0,89
Kista dermoid 1 50,0 1 50,0 0,71
*Uji Regresi Logistik
4.2. Pembahasan
Penelitian dilakukan terhadap kelompok kasus 20 blok paraffin jaringan kista ovarium benigna yang diperoleh dari tindakan operasi ginekologi kasus kista ovarium jinak. Sedangkan subjek penelitian kelompok kontrol sebanyak 20 blok paraffin jaringan ovarium normal yang diperoleh dari tindakan operasi ginekologi kasus non kista ovarium benigna.
Hasil yang diperoleh bahwa pada kelompok kista ovarium jinak lebih banyak dengan usia 20-50 tahun sebanyak 14 orang (70%) kemudian dengan usia <20 tahun dan >50 tahun masing-masing 3 orang (15%). Pada kelompok ovarium normal lebih banyak dengan usia >50 tahun sebanyak 12 orang (60%) dan lainnya dengan usia 20-50 tahun sebanyak 8 orang (40%). (tabel 4.1.1)
Dari usia menarche baik kelompok kista ovarium jinak dan ovarium normal, terbanyak dijumpai usia menarche ≤12 tahun masing-masing 17 orang (85%) dan 15 orang (75%). (Tabel 4.1.1). Hal ini sejalan dengan teori incessant ovulation yang menunjukkan bahwa pada pasien dengan menarche yang dini terjadi peningkatan risiko kista ovarium.43,44
Dari jumlah paritas, pada kelompok kista ovarium jinak terbanyak dengan paritas ≥1 sebanyak 14 orang (70%) sedangkan kelompok ovarium normal seluruhnya dengan paritas ≥1 (100%). (Tabel 4.1.1). Suatu penelitian mendapatkan bahwa wanita nullipara akan memiliki dua kali risiko yang lebih tinggi terkena kista ovarium, tetapi alasan pastinya belum sepenuhnya jelas. Risiko ini akan menurun dengan riwayat melahirkan dan stabil pada wanita yang melahirkan sebanyak enam kali. Risiko akan menurun pada wanita yang melahirkan yang memberikan ASI dimana hal ini mungkin memiliki efek perlindungan dengan memperpanjang periode amenore.31,41,42
Dari indeks massa tubuh baik kelompok kista ovarium jinak dan ovarium normal, terbanyak dengan indeks massa tubuh normoweight masing-masing 14 orang (70%) dan 15 orang (75%). (Tabel 4.1.1). Meningkatnya distribusi lemak tubuh bagian atas, juga merupakan faktor risiko terjadinya kista ovarium. Diduga stimulasi dari estrogen ekstraovarian khususnya dari jaringan adiposa berperan dalam perkembangan kista ovarium.35
Distribusi histopatologi kista ovarium benigna, dimana terbanyak jenis epitel (85%) yaitu cystadenoma musinosum (40%), Cystadenoma serosum (35%),
kistadenoma ovarii musinosum, kistadenoma ovarii serosum, kista endometrioid, kista dermoid.22,25
Kelompok kista ovarium jinak memiliki ekspresi HE4 sebagian besar positif yaitu 12 orang (60%) dan negatif sebanyak 8 orang (40%). Sedangkan kelompok ovarium normal seluruhnya memiliki ekspresi HE4 negatif (100%). Secara statistik dijumpai adanya hubungan yang bermakna antara kelompok subjek penelitian dengan ekspresi HE4 dengan nilai p < 0,05, dengan odds ratio untuk kemungkinan ekspresi HE4 negatif sebesar 0,4 (IK 95% 0,23-0,68) yang berarti bahwa kista ovarium jinak memiliki kemungkinan ekspresi HE4 negatif hanya sekitar 0,4 kali lipat. (Tabel 4.1.3)
Ekspresi dari protein HE4 seperti pada penanda ovarium lainnya dapat diidentifikasi dengan analisa ekspresi gen dan dijumpai pada proses terkait pembentukan kista inklusi kortikal dan metaplasia Mullerian.18
Hasil penelitian ini tampaknya dapat dijawab oleh model dua pathway
dikembangkan oleh Shih dan Kurman (2004) dalam usaha untuk menggabungkan temuan klinis, histopatologis dan genetik molekuler pada kanker ovarium. Mereka juga menemukan perbedaan pada TP53 dan mutasi KRAS yang dijumpai antara tumor serosa borderline (SBT) dan karsinoma serosa. SBT menunjukkan subset tumor ovarium serosa yang non invasif, tampaknya berkembang dari kistadenoma serosa benigna, dan berkembang sangat perlahan menjadi karsinoma serosa derajat rendah. SBT tidak memiliki mutasi TP53 yang merupakan karakteristik karsinoma serosa derajat tinggi. Pengamatan ini menunjukkan formulasi yang mengklasifikasikan seluruh tumor ovarium sebagai tipe I dan tipe II. Tumor tipe I termasuk seluruh histotipe utama (serosa, endometrioid, musinosum, sel jernih, dan transisional), menunjukkan gambaran arsitektural dan inti sel derajat rendah, pertumbuhan yang lambat, dan dapat dihubungkan dengan lesi prekursor ovarium jinak. Alterasi genetik utama diantara tumor tipe I adalah mutasi KRAS dan BRAF, dimana keduanya mengaktivasi jalur sinyal MAPK onkogenik.44
BAB V
SIMPULAN DAN SARAN
5.1. Simpulan
1. Subjek penelitian kelompok kista ovarium jinak terbanyak dengan usia 20-50 tahun, usia menarche ≤12 tahun, paritas ≥1, IMT normal sedangkan kelompok ovarium normal terbanyak dengan usia >50 tahun, usia menarche ≤12 tahun, paritas ≥1, IMT normal.
2. Distribusi histopatologi kista ovarium benigna terbanyak dengan jenis epitel.
3. Ada hubungan yang bermakna antara kista ovarium benigna dengan ekspresi HE4 dengan OR sebesar 0,4.
4. Tidak ada hubungan yang bermakna antara jenis histopatologi kista ovarium benigna dengan ekspresi HE4.
5.2. Saran