BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan 2.1.1 Sistematika tumbuhan
Di dalam dunia tumbuhan, tanaman bawang merah diklasifikasikan sebagai
berikut :
Kerajaan : Plantae
Divisi : Spermatophyta
Kelas : Monocotyledoneae
Bangsa : Liliales
Suku : Liliaceae
Marga : Allium
Jenis : Allium cepa L. (Rahayu dan Berlian,1999).
2.1.2 Nama daerah
Nama daerah dari tumbuhan bawang merah : Bawang merah (Aceh dan
Palembang); pia (Batak); bawang sirah atau dasun merah (Minangkabau), barambang
sirah atau dasun merah (Minangkabau); bawang suluh (Lampung); bawang beureum
(Sunda); brambang atau brambang abang (Jawa Tengah dan Jawa Timur); bhabang
mera (Madura); jasum bang atau jasum merah (BaIi); bawangi (gorontalo); lasuna eja
(Makassar), lasuna cela (Bugis); laisuna mpilas (Roti); kalpeo miha (Timor); bawa
(Halmahera); bawa rohika (Ternate); bawa kahori (Tidore) (Rukmana, 1994).
2.1.3 Sejarah, habitat dan penyebaran
Tanaman bawang merah diduga berasal dari Asia. Sebagian literatur
menyebutkan bahwa tanaman ini dari Asia tengah (Palestina dan India), sebagian juga
menyebutkan bawang merah berasal dari Asia Barat yang berkembang ke Mesir dan
Turki. Bangsa Mesir mengenal bawang merah sejak 3200-3700 SM. Di Yunani dan
Israel, bawang merah dibudidayakan sejak 1500 SM. Eropa Barat, Timur dan Spanyol
mengenal bawang merah sejak abad kedelapan, lalu menyebar ke Amerika.
Penyebaran bawang merah telah meluas hampir ke setiap negara. Eropa Barat, Eropa
Timur, Spanyol, Amerika Serikat, Mesir dan Turki merupakan negara penghasil
bawang mereah terpenting di dunia. Di Indonesia, sentra budidaya bawang merah
diusahakan di hampir seluruh provinsi di Indonesia kecuali Riau, DKI Jakarta,
Kalimntan Barat dan Kalimantan Tengah (Rukmana, 1994). Daerah Samosir menjadi
sentra budidaya bawang merah di Sumatera Utara, (Rahayu dan Berlian,1999).
.Bawang merah termasuk tumbuhan semusim yang tumbuh dengan baik di
daerah beriklim kering yang cerah dengan udara panas, namun harus disertai
pengairan yang baik dengan ketinggian tanah 0-800 m di atas permukaan laut dan
suhu antara 25-32 0C. Tanah yang gembur dan subur serta banyak mengandung
humus sangat baik dengan pH antara 6,0-6,8 (sedikit agak asam-normal) cocok untuk
pertumbuhan bawang merah, sedangkan di tanah yang becek menyebabkan
pertumbuhan bawang merah menjadi kerdil dan umbinya mudah busuk. Pada pH
kurang dari 5,5 tanaman akan keracunan alumunium sehingga tanaman menjadi
kerdil, sebaliknya pada pH di atas 6,5 Mangan tidak dapat diserap akibatnya umbinya
menjadi kecil-kecil (Rukmana, 1994; Wibowo, 2008).
2.1.4 Morfologi tumbuhan
Bawang merah (Allium cepa L.) merupakan terna (tanaman yang berbatang
lunak karena tidak membentuk kayu) rendah yang tumbuh tegak dengan tinggi
mencapai 15-50 cm, berakar serabut dengan sistem perakaran dangkal dan tidak
Di bagian atas discus terbentuk batang semu yang tersusun dari pelepah-pelepah
daun. Batang semu yang berada dalam tanah akan berubah bentuk dan fungsinya
menjadi umbi lapis (bulbus). Beberapa helai kelopak daun terluar (2-3 helai) tipis dan
mengering tetapi cukup liat, membungkus lapisan-lapisan kelopak daun di dalamnya
sehingga membentuk umbi yang kemudian berisi cadangan makanan bagi tunas yang
akan menjdi tanaman baru. Pada pangkal umbi tumbuh akar-akar serabut. Di bagian
atas umbi terdapat mata tunas yang disebut tunas lateral dan dapat tumbuh menjadi
tanaman baru. Daun berbentuk pipa, yakni bulat kecil memanjang antara 50-70 cm,
berlubang, bagian ujungnya meruncing, berwarna hijau muda sampai hijau tua dan
letak daun melekat pada tangkai yang ukurannya relatif pendek. Bunga akan muncul
dari tunas utama (tunas apikal) di bagian tengah umbi, dengan panjang 30-90 cm dan
terdapat 50-200 kuntum yang tersusun melingkar seperti payung. Biji mempunyai
bentuk agak pipih,sewaktu masih muda berwarna bening atau putih, tetapi setelah tua
menjadi hitam. Umbi lapis bawang merah sangat bervariasi, bentuknya ada yang
bulat, bundar sampai pipi, sedangkan ukuran umbi meliputi besar, sedang, dan kecil.
Warna kulit umbi merah muda sampai merah tua (Rukmana, 1994; Rahayu dan
Berlian,1999; Wibowo, 2008).
2.1.5 Khasiat
Secara tradisional bawang merah dapat bermanfaat untuk pengobatan beberapa
penyakit, seperti disentri, jantung koroner, influenza, tekanan darah tinggi, sembelit,
luka, bisul pada kulit, jamur pada vagina (trichomoniasis), demam, masuk angin,
impotensi dan cacar air. Selain itu bawang merah dapat berkhasiat menurunkan lemak
darah, tekanan darah, mencegah pembekuan darah, menyembuhkan asma, melawan
2.2 Parasetamol
2.2.1 Uraian Kimia
Parasetamol mempunyai nama IUPAC 4’-hidroksiasetanilida dengan rumus
struktur C8H9NO2. Pemeriannya berupa serbuk hablur, putih tidak berbau, dan
memiliki rasa sedikit pahit, larut dalam air mendidih dan dalam natrium
hidroksida 1N, serta mudah larut dalam etanol (Depkes, RI., 2014). Parasetamol
merupakan metabolit aktif fenasetin yang memiliki efek antipiretik yang
ditemukan di Jerman dan telah lama digunakan sejak tahun 1893 (Wilmana, 2013;
Katzung, 2012). Efek antipiretik ditimbulkan oleh gugus aminobenzen Obat ini
merupakan inhibitor COX-1 dan COX-2 di jaringan perifer dengan efek
antiinflamasi yang tidak signifikan. Nyeri akut dan demam efektif terobati dengan
dosis 325-500 mg empat kali sehari (Wilmana, 2013).
2.2.2 Farmakokinetik
Absorpsi parasetamol bergantung pada kecepatan pengosongan lambung,
namun umumnya diabsorpsi cepat dan sempurna. Obat ini tersebar ke seluruh
cairan tubuh dan sekitar 25% dari yang diabsorpsi terikat dengan protein plasma.
(Wilmana dan Gan, 2013). Konsentrasi puncak diperoleh 30-60 menit setelah
pemberian. Sejumlah parasetamol dimetabolisme oleh enzim hati untuk diubah
menjadi parasetamol sulfat dan glukoronida yang secara farmakologi inaktif,
kurang dari 5% dieksresikan dalam bentuk tidak berubah. Metabolit yang sedikit
namun reaktif (NAPQI) bersifat penting sebab merupakan toksik terhadap hati
dan ginjal. Waktu paruh parasetamol adalah 2-3 jam dan tidak dipengaruhi fungsi
ginjal. Dosis toksik dan gangguan hati dapat memperpanjang waktu paruh (Furst,
2.2.3 Farmakodinamik
Efek analgesik parasetamol yaitu menghilangkan atau mengurangi nyeri
ringan sampai sedang seperti sakit kepala, myalgia, nyeri setelah melahirkan di
mana pemberian aspirin tidak ditoleransi pasien dengan riwayat alergi, tukak
lambung, hemophilia dan bronkospasma dan juga diberikan kepada pasien
(Wilmana dan Gan, 2013; Furst, et al., 2012). Di Indonesia, penggunaan
parasetamol sebagai analgesik dan antipiretik berkembang luas. Nyeri akut dan
demam dapt diobati dengan dosis pemberian 325-500 mg empat kali sehari
(direkomendasikan tidak melebihi 4 g) atau dosisnya diturunkan jika pemberian
untuk anak-anak (Furst, et al., 2012). Jika dosis terapi tidak memberi manfaat,
biasanya dosis lebih besar tidak menolong. Penggunaannya sebagai antiinflamasi,
misalnya untuk mengobati arthritis rheumatoid bersifat inadekuat karena
merupakan penghambat biosisntesis prostaglandin yang lemah. Karena hampir
tidak mengiritasi lambung, parasetamol sering dikombinasi dengan AINS untuk
efek analgesik (Wilmana dan Gan, 2013).
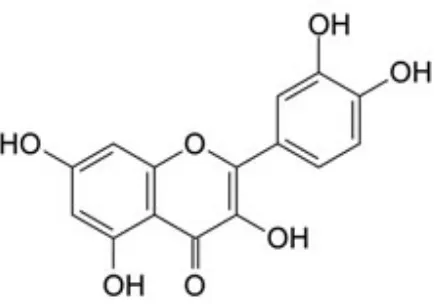
2.3 Kuersetin
Kuersetin merupakan flavonol yang tedapat dalam buah dan sayur yang
memberikan efek bermanfaat bagi tubuh, dengan efek antioksidannya yang paling
potensial di antara berbagai senyawa polifenol. Kuersetin terbukti memiliki efek
antiinflamasi, antivirus, antibakteri dan antikarsinogenik. Dalam makanan,
kuersetin lebih banyak berada dalam bentuk terikat dengan gula, asam fenolat,
untuk selanjutnya diabsorbsi dan dimetabolisme sebagai aglikon (Materska,
2008).
Gambar 2.1 Struktur Kuersetin (Domitrović, et al., 2012)
Kuersetin aglikon memiliki struktur lipofilik, namun demikian turunan
kuersetin dapat bersifat lipofilik maupun hidrofilik tergantung pada subtituen
yang terikat. Pada umumnya, turunan flavonoid dengan O-metil, C-metil dan
turunan prenil bersifat lipofilik. Glikosilasi paling tidak di satu gugus hidroksil
akan meningkatkan sifat hidrofiliknya (Materska, 2008).
Aktivitas antioksidan senyawa fenol salah satunya kuersetin dihubungkan
dengan kemampuan mentransfer satu atom H atau sebuah elektron, sama halnya
dengan pembentukan kompleks (chelation) dengan ion logam dan penghambatan
aktivitas enzim oksidase. Selain itu, aktivitas antioksidan juga disertai aktivitas
antivirus dan antibakteri. Aktivitas antioksidan ditandai dengan adanya gugus
hidroksil bebas dan posisinya yang menguntungkan. Reaksi kuersetin dengan
radikal bebas DPPH menunjukkan aktivitas antiradikalnya yang tinggi disebabkan
adanya gugus 1,2-dihidroksibenzena (katekol) di cincin B. Apabila bereaksi
dengan DPPH, kuersetin mendonorkan 2 atom H dan berubah menjadi intermediet
3-OH dan 5-OH di cincin A meningkatkan potensi antiksidan. Turunan kuersetin
memberikan efek farmakologi yang lebih rendah dibandingkan dengan bentuk
aglikonnya. Beberapa turunan kuersetin yang mengalami glikosilasi di C4’-OH
dapat menurunkan kemampuan mendonorkan H+ sehingga sifat antioksidannya
berkurang. Uji aktivitas antoksidan aglikon flavonoid, termasuk fisetin,
kaempferol, morin, mirisetin dan kuersetin menyimpulkan kemampuan potensi
penurunan radikal bebas ditunjukkan oleh gugus 4’-OH di cincin B (Brunetti, et
al., 2013).
Kuersetin dan turunannya secara umum mengalami konversi metabolik dan
berada dalam jaringan tubuh dengan mengalami glukuronasi, sulfasi dan metilasi.
Mekanisme pertama, ketiganya merupakan substrat potensial untuk enzim laktose
phlorizin hydrolaze (LPH) di brush border membran usus halus. Mekanisme
kedua memampukan absorpsi glikosida kuersetin melalui interaksi dengan
sodium-dependent glucose transporter 1 (SGLT1). Setelah diabsorpsi, glikosida
kemudian dihidrolisis oleh β-glikosidase di sitosol sebagian kecil sel mukosa
usus halus (Materska, 2008).
Kuersetin menempati jumlah terbanyak dari total flavonoid dalam bawang
merah, yakni 80% dalam bentuk kuersetin monoglukosida dan kuersetin
diglukosida (Lanzotti, 2006). Terdapat perbedaan dalam absorpsi kuersetin, 52%
diabsorpsi dalam bentuk terikat dengan glikosida, 24% diabsorpsi sebagai
aglikon, dan 17% sisanya diabsorpsi sebagai quersetin-3-rutinosida. Studi oleh
Wiczwoski, et al., menunjukkan 53,2 % kuersetin yang terdapat di kulit terluar
umbinya dalam bentuk kuersetin-4'-glukosida, kuersetin-3-glukosida, dan
kuersetin-3,4'-glukosida (Wiczwoski, et al., 2003).
Studi oleh Po’voa et al menyimpulkan bahwa kandungan flavonol terutama
kuersetin menurun dari lapisan terluar sampai ke dalam dan dari ujung atas
sampai pangkal bawah. Meningkatnya kusersetin seiring dangan bertambahnya
usia sel-sel yang menyusun lapisan umbinya, sehingga sel-sel di lapisan luar tentu
umurnya lebih tua dibandingkan di lapisan yang lebih dalam. Lapisan luar dan
bagian atas umbi paling banyak mengandung kuersetin, berkaitan dengan
fungsinya sebagai proteksi terhadap paparan sinar UV B (Gregorio et al., 2010).
2.4 Rutin
Rutin (kuersetin 3-O-rutinosida) merupakan flavonol yang terdiri dari
kuersetin aglikon dan rutinosida di atom C nomor 3 di cincin C. Rutin umumnya
terkandung di berbagai macam makanan, dan menunjukkan sejumlah aktivitas
biokimia dan farmakologi, seperti antioksidan, antiinflamasi dan antitumor. Uji
aktivitas heptoprotektor secara preventif oleh Domtrovic, dkk., menunjukkan
pemberian rutin dosis 50 dan 150 mg/kg secara peritoneal dapat
menurunkan peningkatan NO yang diinduksi CCl4. Peningkatan NO akan
memicu pembentukan nitrotirosin dan menyebabkan nekrosis (Dumitrovic, dkk.,
2.5 Hati
2.5.1 Anatomi hati
Hati merupakan organ padat terbesar dalam tubuh manusia dengan massa
mencapai 1,6 kg pada pria dan 1,4 kg pada wanita, dan menyumbang 2% massa
tubuh orang dewasa. Secara anatomi hati terletak di bawah diafragma, di kuadran
atas kanan abdomen, dengan posisi anterior dan posteriornya terlindungi oleh
tulang rusuk. Hati memiliki dua lobus dan lobus kanan enam kali lebih besar dari
lobus kiri. Hati menerima kurang lebih 1,3 liter darah per menit: 75 % berasal dari
vena (vena porta) dan sisanya dari arteri hepatik (Holt, 2008). Vena porta
membawa darah dari usus dan limpa, dan arteri membawa darah yang berasal dari
aorta, darah dari kedua pembuluh tersebut akhirnya bercampur di sinusoid
sebelum meninggalkan hati dalam vena hepatik (Murli, 2013).
Hepatosit berbentuk poligonal dengan sitoplasma yang eosinofilik dan
nukleus berbentuk oval atau bulat. Sel ini memiliki tiga permukaan, satu
menghadap sinusoid dan rongga Disse (basolateral), satu menghadap kanalikulus
(kanalikular) dan satu menghadap hepatosit yang berdekatan (lateral). Hepatosit
tersusun dalam barisan sel-sel yang berbentuk seperti jeruji di roda, dengan vena
sentral sebagai pusatnya. Tiap barisan dipisahkan oleh kapiler yang dialiri darah
yang dinamakan sinusoid, sehingga tampak seperti kanal. Kemampuan adapatasi
sinusoid sangat tinggi dan mampu memfasilitasi pertukaran molekul-molekul dari
lumen sinusoid ke hepatosit, begitu juga sebaliknya (Holt, 2008). Di sinusoid
dapat dijumpai sel endotel dan sel Kupffer. Sel endotel tersusun menyerupai
lapisan/jalur yang memudahkan pertukaran zat antara darah dengan hepatosit
stelat (sel Ito) yang perannya penting terhadap aliran darah sinusoid, fibrogenesis
dan penyimpanan vitamin A. Sel Kupffer bentuknya tidak teratur, cenderung
gepeng dan merupakan makrofag yang berperan dalam fagositosis. Terdapat juga
sel pit (sel limfosit hati) di sinusoid dan rongga Disse, sel ini mempunyai limfosit
T atau fenotip sel NK (natural killer) (Murli, 2013).
Secara mikroskopik, stuktur jaringan dijelaskan dengan konsep acinus
(modern) dan lobul (konvensional). Hepatosit dalam acinus dapat dibagi menjadi
tiga zona berdasarkan jarak sel dari traktus porta. Traktus porta terdiri atas duktus
biliaris, arteri hepatik, vena porta, pembuluh limfatik, saraf dan sel-sel inflamasi.
Mulai dari traktus porta, darah dari arteri dan vena mengalir melalui sinusoid
hingga mencapai vena sentral (Murli, 2013). Hepatosit yang berada dekat traktus
porta lebih dulu menerima nutrisi dan oksigen dari darah karenanya paling
resisten terhadap gangguan iskemik, daerah ini dinamakan zona 1 (periportal).
Hepatosit yang berada lebih jauh dari traktus porta akan menerima darah dengan
konsentrasi nutrisinya yang lebih rendah, dinamakan zona 3
(perisentral/sentrilobular), mengelilingi vena sentral dan beresiko besar
mengalami cedera hipoksia. Zona 2 (midzonal) berada di antara zona 1 dan zona
3. Pembagian fungsi metabolik berdasarkan letak zonanya dalam acinus. Zona 1
utamanya bertanggung jawab terhadap perubahan dalam darah porta, seperti kadar
glukosa dan insulin sehingga berperan dalam glikolisis dan glukoneogenesis.
Sintesis protein, β-oksidasi asam lemak, sintesis kolesterol dan sekeresi asam
empedu juga terjadi di zona 1. Hepatosit di zona 3 merupakan tempat utama
NADPH dan NADH reduktase, sehingga lebih beresiko mengalami kerusakan
yang diinduksi obat (Holt dan Smith, 2008).
Apabila dilihat dengan bantuan mikroskop elektronik, hepatosit memiliki
ciri yang menjadi karakter sel yang terlibat dalam berbagai fungsi metabolik,
yakni sejumlah mitokondria, lisosom, peroksisom, retikulum endoplasmik kasar
dan halus dan glikogen yang tersimpan di sitoplasma. Hepatosit memiliki banyak
mitokondria dan mengisi 20% dari volume keseluruhan sitoplasma. Hal ini
berkaitan dengan tingginya kebutuhan jaringan akan energi yang dipenuhi oleh
ATP yang diproduksi lewat jalur Krebs. Jumlah mitokondria di daerah
sentrilobular lebih sedikit dibanding periportal, namun ukurannya lebih besar.
Mitokondria juga terlibat dalam berbagai jalur metabolisme lain, termasuk
oksidasi asam lemak, metabolisme steroid, sintesis asam nukleat, pengaturan
kadar kalsium intrasel dan biosintesis haem. Protein yang membran mitokondria
mempunyai peran utama untuk mengatur dan mengeksekusi kematian sel
terprogram atau apoptosis. Penambahan umur akan mengurangi jumlah
mitokondria meski bentuk dan volumenya tetap. Retikulum endoplasma (RE)
kasar umumnya berada di tepi sinusoid, berkumpul di sekitar nukleus dan
mitokondria dan menjadi tempat utama sintesis berbagai protein, seperti albumin,
protein hormon dan growth factor, serta fibrionogen dan prototrombin.
Sebaliknya RE halus menyebar di seluruh hepatosit sebagai kumpulan vesikel
yang dekat dengan agregat glikogen. Fungsi RE halus adalah sintesis lipid,
akumulasi glikogen dan metabolisme obat dan steroid. Untuk melakukan semua
fungsinya membran RE halus mengandung enzim yang sangat penting yaitu
biotransformasi obat dan steroid endogen lewat sistem mono-oksigenase
mikrosom. Badan Golgi terlibat dalam sekresi empedu, pembentukan glikoprotein
dan lipoprotein serta distribusinya ke komponen intraselular, juga sintesis dan
perbaikan membran sel. Lisosom bertugas mendegradasi berbagai substrat.
Peroksisom berperan dalam oksidasi dan peroksidasi melalui pembentukan
hidrogen peroksida, juga degradasi asam lemak rantai panjang (Holt, 2008).
2.5.2 Fungsi hati
Hati mempunyai fungsi yang cukup banyak berkaitan dengan perannya
sebagai kelenjar eksokrin dan endokrin. Hati mensekresi asam empedu yang
berperan dalam emulsifikasi lemak di usus halus. Protein yang disintesis di hati
berfungsi sebagai enzim, hormon maupun protein plasma. Beberapa enzim yang
disintesis di hati juga berguna dalam proses detoksifikasi zat-zat berbahaya. Hati
ikut menjaga keseimbangan kadar glukosa dalam darah lewat proses
glikogenolisis dan glukoneogenesis. Hati melangsungkan metabolisme lemak
menjadi asam lemak, kolesterol dan lipoprotein. Hati merupakan tempat
penyimpanan vitamin terutama yang larut dalam lemak. Hati juga berperan besar
dalam detoksifikasi racun dan obat, serta memiliki sistem pertahanan tubuh
melalui sel Kupffer (Barret, et al., 2010; McKuskey, 2012).
2.5.3 Hepatotoksisitas
Hepatotoksisitas adalah cedera pada hati yang dihubungkan dengan fungsi
hati yang terganggu karena paparan obat atau agen non-infeksi. Molekul inorganik
yang dapat menyebabkan hepatotoksis contohnya arsen, fosfor, tembaga dan besi.
Senyawa organik yang berasal dari tumbuhan juga bersifat toksik, contohnya
termasuk obat-obatan juga merupakan hepatotoksin. Obat yang merusak hati akan
berdampak pada kadar enzim hati yang abnormal. Cedera hati akibat obat-obatan
atau Drug Induced Liver Injury (DILI) bertanggung jawab terhadap 5 %
pengobatan di rumah sakit dan 50% gangguan hati akut (Kumar, et al., 2014).
Banyak obat yang dapat menyebabkan toksisitas dengan gambaran biokimia,
klinis, histologi dan kronologi atau kombinasi semuanya yang khas. Beberapa
pola hepatotoksitas diketahui berdasarkan mekanisme cedera yang berbeda-beda.
Cedera hepatoseluler atau sitolitik melibatkan peningkatan kadar serum
transaminase, biasanya didahului diawali peningkatan total bilirubin dan sedikit
peningkatan ALP, contohnya isoniazid dan troglitazone. Cedera kolestatik
ditandai dengan peningkatan ALP yang cenderung lebih menonjol dibandingkan
ALT atau AST, contohnya asam klavulanat atau klorpromazin. Reaksi imun atau
hipersentivitas sering tertunda atau terjadi setelah paparan yang berulang, ditandai
demam, ruam dan eosinofilia. Fenitoin, nitrofurantoin atau halotan dapat
meningkatkan onset reaksi dan keparahan setelah pemberian berulang dalam
interval tertentu. Cedera mitokondria melibatkan steatosis mikrovesikular,
asidosis laktat dan peningkatan ringan serum aminotranferase, contohnya asam
valproat dan tetrasiklin parenteral dosis tinggi (Navarro dan Senior, 2006).
2.5.4 Mekanisme hepatotoksisitas yang diinduksi parasetamol
Setelah pemberian dosis terapi, sekitar 50-70% dosis parasetamol akan
terikat dengan glukuronida, 25-35% terikat dengan sulfat dan 5-15% sisanya
diekskresi di urin dalam bentuk konjugat asam merkapturat dan sistein. Ini
disebabkan konversi parasetamol ke bentuk reaktifnya yang bisa berikatan dengan
Hepatotoksisitas oleh parasetamol bukan sekedar kerusakan yang bersifat
tunggal namun merupakan hasil kontribusi dan integrasi berbagi
mekanisme.NAPQI terbentuk dari oksidasi langsung 2 elektron oleh sitokrom P450
(James, et al., 2003). Ketika pemberian parasetamol mencapai dosis toksik, jalur
glukoronidasi dan sulfasi mejadi jenuh. Metabolisme parasetamol dengan dosis toksik
menurunkan kadar GSH dalam hati hingga lebih dari 90%. Keadaan ini memicu
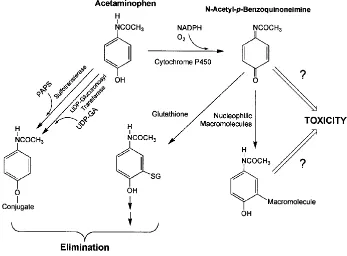
NAPQI berikatan
Gambar 2.2 Skema jalur metabolisme parasetamol (James, et al., 2003)
secara kovalen dengan gugus sulfhidril di protein sistein hepatosit membentuk
3-(cystein-S-yl)-acetaminophen (APAP-Cys) (Agarwal, et al., 2011; James, et al.,
2003). Hanya hepatosit yang mengandung ikatan parasetamol-protein dapat
mengalami nekrosis dan toksisitas berfokus pada area sentrilobular. Uji
menggunakan HPLC oleh Muddrew, et al., membuktikan jumlah ikatan
pada orang dewasa pada kasus gagal hati akut akibat parasetamol (Hinson, et al.,
2009).
Ion superoksida (O2-) dilepaskan sitokrom P450 2E1 yang juga membentuk
hidrogen peroksida (H2O2) lewat reaksi Fenton. Deplesi GSH yang seharusnya
menjadi kofaktor dalam detoksifikasi O2- meningkatkan kadar superoksida intrasel
dan stres oksidatif. Kadar nitrit oksida (NO) meningkat selama tokisisitas
parasetamol. O2- bereaksi cepat dengan NO membentuk peroksinitrit (ONOO-),
yang sangat penting dalam toksisitas, dengan konstanta laju reaksi 7 x 109 M-1 s-1
(James, et al., 2003). Peroksinitrit adalah agen penitrasi dan pengoksidasi yang
didetosifikasi oleh GSH yang berkurang akibat tokisitas parasetamol. (Agarwal, et
al., 2011). Peroksinitrit tidak hanya menyebabkan nitrasi protein tetapi juga dapat
menyerang target biologis secara luas. Nitrotirosin terbentuk di zona 3 atau
sentrilobular hati. Posisi NO menjadi cukup kritis, jika NO muncul akan bereaksi
dengan O2- membentuk peroksinitrit dan jika tidak, O2- akan menyebabkan
peroksidasi lipid (James, et al., 2003). Peroksidasi lipid merupakan oksidasi
sistematik asam lemak tidak jenuh, yang dalam hal ini menyusun membran sel,
menyebabkan fluiditas membran menurun sehingga nutrisi tidak bisa keluar
masuk sel. Diduga MPT terjadi bersamaan pembentukan RNS (Agarwal, et al.,
2011).
Oksidan stres akan mengaktifkan beberapa kinase, salah satunya adalah
C-Jun N-terminal kinase (JNK) yang kemudian bertranslokasi ke mitokondria. Ca2+
yang berakumulasi menginduksi terbentuknya pori transisi pemeabilitas membran
(MPT) yang melumpuhkan membran sel, pembengkakan matriks mitiokondria
endonuklease G and Apoptosis-inducing Factor (AIF). Hanya endonuklease G dan
AIF yang bertranslokasi ke nukleus dan memicu fragmentasi DNA (McGill, 2013).
Mitokondria kekurangan ATP sehingga tidak mampu melakukan apoptosis, suatu
program kematian sel yang membutuhkan banyak energi. Diperparah dengan
degradasi DNA, sel kemudian mengalami nekrosis.
2.5.5 Mekanisme hepatotoksisitas yang diinduksi karbon tetraklorida
Mekanisme kerusakan hati yang diinduksi parasetamol mirip dengan
kerusakan hati yang diinduksi karbon tetraklorida, yakni disebabkan radikal bebas
hasil metabolisme oleh enzim sitokrom P450. Karbon tetraklorida bersifat toksik
terhadap hati, ginjal, dan jantung sekaligus (Sulistia, 1995). Dampak racun karbon
tetraklorida (CCl4) tidak oleh molekul CCl4 tetapi oleh bentuk konversinya, yaitu
radikal bebas karbon triklorida (CCl3˙) (Robbins dan Kumar, 1995). Proses
konversi CCl4 menjadi CCl3˙ dapat digambarkan sebagai berikut:
CCl4 + e → CCl3 + Cl
-(Kumar, dkk., 2005).
Setelah masuk ke dalam hati CCl4 diaktivasi oleh enzim sitokrom P450,
(enzim fase I metabolisme xenobiotik hati) menjadi radikal karbon triklorida
(CCl3˙) dan selanjutnya CCl3˙ yang terbentuk dapat bereaksi dengan oksigen
membentuk karbon trikloro dioksida (CCl302˙) yang merupakan pencetus utama
peroksidasi lemak (Murray, dkk., 2003; Hodgson dan Levi, 2000).
Radikal bebas yang dihasilkan akan menyebabkan autooksidasi asam
lemak polifenolik yang terdapat dalam fosfolemak selaput (Robbins dan Kumar,
1995; Murray, 2000). Kemudian terjadi dekomposisi oksidatif lemak, dan
(Robbins dan Kumar, 1995). Peroksidasi lemak ini akan memicu terjadinya
peroksidasi lemak lebih lanjut (Murray, 2000).
Peroksidasi lemak menyebabkan kerusakan membran plasma yang dapat
mengakibatkan influks masif ion kalsium. Peningkatan ion kalsium merupakan
salah satu efek sitotoksik karbon tetraklorida yang akan mengaktifkan sejumlah
enzim seperti ATPase (mengurangi ATP), phospholipase (merusak membran),
protease (merusak membran dan protein sitoskleton), dan endonuclease
(memfragmentasi DNA dan kromatin). Selain itu, peningkatan ion kalsium
intraseluler juga menyebabkan peningkatan permeabilitas mitokondria dan
menginduksi terjadinya apoptosis dan kematian sel (Klaasen, dkk., 2003; Kumar,
dkk., 2005).
2.5.6 Biomarker hepatotoksisitas
Terdapat sejumlah biomarker untuk menilai hepatotoksisitas yang diukur
melalui serangkaian tes fungsi hati. Tes ini cenderung lebih menggambarkan
adanya kerusakan hati atau juga obstruksi saluran empedu dibandingkan menilai
fungsi hati, kecuali untuk estimasi protein serum (albumin dan protrombin).
Walaupun merupakan petunjuk yang lemah mengenai kapasitas hati untuk
memetabolisme obat, tes ini sangat bermanfaat pada pemantauan arah
perkembangan penyakit hati (setelah diagnose ditetapkan) dan respons psien
terhadap pengobatan (Kenward dan Tan, 2003).
a. Aspartat transminase dan Alanin transminase
Aspartat transminase (AST) dan Alanin transminase (ALT) mengkatalisis
reaksi reduksi gugus amino dari alanin atau aspartat ke α-ketoglutarat dan
terdapat di hati, otak, otot rangka dan jantung. ALT lebih banyak dijumpai di hati
dan sedikit di otot rangka dan jantung. Peningkatan ALT dan AST juga bisa
berasal dari luar hati, contohnya dari otot rangka. Hepatosit yang rusak
mengeluarkan komponen dari dalam sel termasuk ALT dan AST ke luar sel.
Enzim yang dilepaskan akhirnya masuk ke sirkulasi dan meningkatkan kadar AST
dan ALT. 80% aktivitas AST di hati manusia berasal dari isoenzim di
mitokondria, sedangkan sirkulasi AST pada manusia normal berasal dari isoenzim
di sitoplasma. Peningkatan AST yang tinggi terjadi ketika nekrosis di jaringan hati
sudah meluas, sehingga lebih dikaitkan dengan infark miokardAST terdapat di
mitokondria dan sitoplasma sel, sedangkan ALT hanya terdapat di sitoplasma .
Tingkat kenaikan AST dan ALT dikelompokkan menjadi tinggi, sedang dan
ringan. Peningkatan yang tinggi (>20 kali lipat hingga mencapai >1000 IU/L)
menandakan hepatitis virus berat, nekrosis yang diinduksi obat dan toksin lain
serta syok sirkular. Peningkatan sedang (3-20 kali lipat) biasanya terjadi pada
hepatitis akut, hepatitis neonatus, hepatitis kronik, hepatitis autoimun, hepatitis
yang diinduksi obat dan gangguan saluran empedu akut. Peningkatan ALT lebih
besar dibandingkan AST kecuali pada hepatitis kronik, bahkan AST bisa
mencapai nilai normal pada 75% penderita hepatitis akut dalam waktu 8 minggu
sejak timbulnya penyakit. Peningkatan ringan (1-3 kali lipat) biasanya dijumpai
pada hepatitis neonatus yg disebabkan sepsis, perlemakan hati, sirosis, hepatitis
steatotik non alkohol, toksisitas obat, olahraga berlebihan dan beberapa gangguan
hati lain, terkadang penigkatan ALT juga dijumpai pada orang normal (Thapa dan
Walia, 2007).
Total bilirubin adalah gabungan bilirubin yang terkonjugasi (langsung) dan
tidak terkonjugasi (tidak langsung). Hasil dari degradasi hemoglobin ini
merupakan marker dari cedera hepatobilier, termasuk kolestasis dan efek bilier.
Bilirubin dapat meningkat tanpa gangguan hati, misalnya karena hemolisis. Hasil
analisis bilirubin tidak langsung terhadap bilirubin tidak langsung tidak terlalu
dibutuhkan dibandingkan menilai jumlah keseluruhan (Thapa dan Walia, 2007).
c. ALP
ALP (alkalin fosfatase) berada di membran sel, terutama heptosit. ALP
berfungsi menghidrolisis monofosfatase pada pH basa. Beberapa isoenzim ALP
yang berasal dari hati, tulang, usus halus, ginjal dan plasenta telah diidentifikasi di
manusia dan hewan pra klinik. ALP merupakan marker utama gangguan
hepatobilier dan kolestasis, dengan peningkatan sedang sampai tinggi. Pada
sirosis bilier, ALP akan meningkat hingga 20 kali lipat dibarengi peningkatan
GGT, dengan atau tanpa peningkatan ALT (Thapa dan Walia, 2007).
d. aktivitas GGT
Aktivitas GGT (gamma glutamil transferase) berada di hati, ginjal dan
pankreas tetapi jumlahnya di hati lebih sedikit dibandingkan di ginjal. GGT
memiliki banyak fungsi seperti mengkatalisis transfer gugus glutamil ke asam
amino dan peptide rantai pendek. GGT merupakan marker penting untuk
gangguan hepatobilier khususnya kolestasis dan sensitivitasnya sangat tinggi
dengan tingkat koreksi yang rendah pada manusia. Peningkatan GGT dan ALP
membantu membedakan gangguan hati dengan tulang yang tidak disertai
peningkatan GGT (Thapa dan Walia, 2007).
Albumin disintesis di hati dan perubahan konsetrasi serunya merupakan
petunjuk yang berguna terhadap fungsi sintesis hati maupu tingkat penyakit hati
kronis. Konsentrasi albumin plasma menurun pada penyakit hati kronis tetapi
cenderung normal (Kenward dan Tan, 2003).
f. Prothrombin time (PT)
Protrombin adalah faktor pembekuan darah yang disintesis di hati dan
mempunyai waktu paruh dua sampai tiga hari. Prothrombin time merupakan
waktu yang diperlukan untuk menghasilkan clot dalam kondisi standar.
Prothrombin time biasanya diukur sebagai INR (Internasional Normalised Ratio)
atau rasio antara PT pasien dengan PT kontrol normal. INR diperpanjang oleh
adanya kegagalan sel hati (berkaitan dengan sintesis oleh sel hati) dan kolestasi
(berkaitan dengan penurunan absorpsi vitamin K). PT sangat bermanfaat untuk
memperkirakan tingkat keparahan penyakit baik yang akut maupun yang kronis