REVIEW ARTIKEL
DISLIPIDEMIA : PANDUAN TERAPI UNTUK PENYAKIT KRONIS
LUH PUTU FEBRYANA LARASANTY 198402222008012008
JURUSAN FARMASI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS UDAYANA
ABSTRAK
Dislipidemia merupakan salah satu penyakit kronis yang menjadi faktor resiko untuk penyakit kardiovaskular seperti penyakit jantung koroner dan stroke iskemik. Manisfestasi penyakit dislipidemia yang kadang tidak menunjukkan gejala yang spesifik kadang kala membuat penanganan penyakit ini menjadi terlambat dan terdiagnosa apabila telah muncul penyakit komplikasi. Sebagai seorang Apoteker, pemberian pelayanan kefarmasian untuk penyakit dislipidemia dapat menjadi salah satu upaya dalam mencegah perkembangan penyakit ini. Pemberian terapi farmakologi pada penyakit dislipidemia meliputi proses etiologi dari penyakit itu sendiri yaitu dari sumber ekstrinsik dan proses intrinsik. Golongan obat yang sampai saat ini digunakan untuk menangani penyakit dislipdemia meliputi niasin, bile acid-binding resin,
Hydroxymethylglutaryl-Coenzyme A (HMG-CoA) Reductase Inhibitors (Statin), fibrat,
ezetimibe dan minyak ikan.
PENDAHULUAN A. Lipid
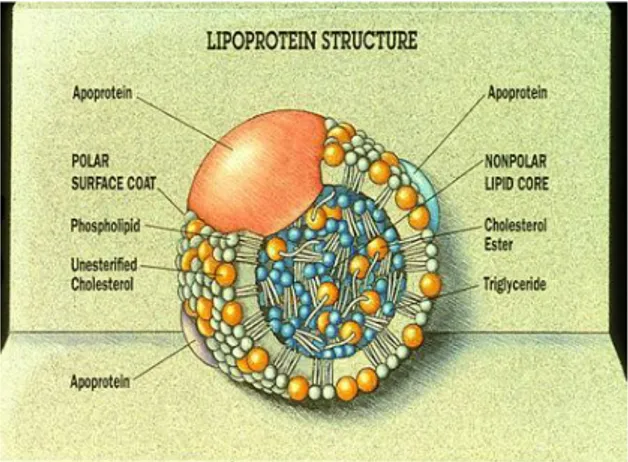
Lipid plasma yaitu kolesterol, trigliserida, fosfolipid dan asam lemak bebas, berasal dari eksogen (diet) dan dari sintesis endogen. Kolesterol dan trigliserida adalah dua jenis lipid yang relatif mempunyai makna klinis yang penting sehubungan dengan proses aterogenesis. Karena lipid tidak larut dalam plasma, lipid akan terikat pada protein sebagai mekanisme transpor dalam serum. Asam lemak bebas ditransport dalam bentuk berikatan dengan albumin. Trigliserida, kolesterol dan fosfolipid berikatan dengan protein, dimana ikatan ini akan menghasilkan empat kelas utama lipoprotein, yaitu :
1. Kilomikron
2. Lipoprotein densitas sangat rendah / very low density
lipoprotein (VLDL)
3. Lipoprotein densitas rendah /
low density lipoprotein (LDL)
4. Lipoprotein densitas tinggi /
high density lipoprotein (HDL)
Dari keempat kelas lipoprotein yang ada, LDL memiliki kadar kolesterol yang paling tinggi, kilomikron dan VLDL kaya akan trigliserida. Kadar protein tertinggi terdapat pada HDL (Carleton & Boldt, 1995).
B. Proses Metabolisme dan Transport Lipoprotein
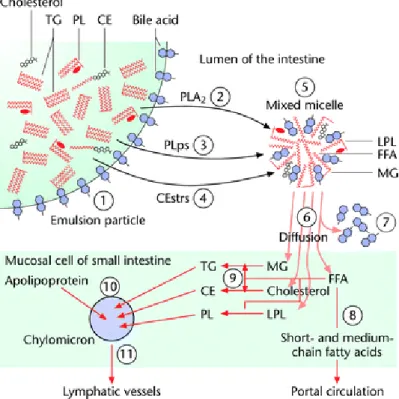
Kolesterol dari makanan dan empedu masuk ke lumen usus dan
teremulsifikasikan oleh asam empedu menjadi micelles. Micelles akan terikat pada enterosit intestinal, kemudian kolesterol dan sterol lainnya akan berpindah dari micelles menuju enterosit melalui sterol transporter. Trigliserida yang disintesis dari asam lemak yang diserap bersama dengan kolesterol dan apolipoprotein B-48
tergabung menjadi kilomikron.
Kilomikron kemudian akan dilepaskan ke sirkulasi limfatik dan akan dikonversi menjadi kilomikron remnant (melalui hilangnya trigliserida), dan kemudian akan di ambil oleh reseptor LDL hepatik-terkait protein / hepatic LDL
receptor-related protein (LRP). Partikel remnat ini akan mensuplai kebutuhan
kolesterol hepatik yang bersumber dari diet. Fungsi lain dari kilomikron adalah juga sebagai penghantar trigliserida dari diet menuju otot skelet dan jaringan adipose (Talbert, 2008).
Gambar 1. Struktur lipoprotein (http://www.medscape.org/viewarticle/550620_2)
Gambar 2. Absorpsi kolesterol intestinal dan transport (http://www.els.net/WileyCDA/ElsArticle/refId-a0000720.html)
Hati memenuhi kebutuhan
kolesterolnya sebagian besar (60%) melalui sintesis de novo dari Asetilkoenzim A. Kecepatan sintesis ditentukan pada langkah awal yaitu
sintesis asam mevalonic dari
hidroksimetilglutaril CoA (HMG CoA) dengan HMG CoA reduktase sebagai
rate-limiting enzyme (gambar 3).
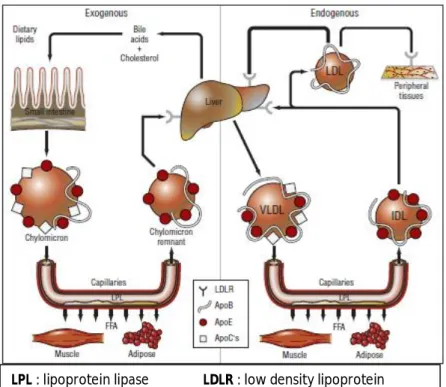
Pada sistem endogen, VLDL yang kaya akan trigliserida disekresi oleh hati dan dikonversi menjadi IDL dan kemudian menjadi LDL yang kaya akan ester kolesterol. Sejumlah LDL akan masuk ke ruang subendothelial arteri akan teroksidasi dan kemudian akan dimakan oleh makrofag, yang akan menjadi sel gabus (foam cells). Kilomikron, kilomikron remnant, VLDL, IDL dan LDL dapat diidentifikasi melalui apoprotein primer (ApoB, ApoC, ApoE)
yang ditemukan pada mereka (Talbert, 2008).
Gambar 3. Biosintesis kolesterol (http://adc.bmj.com/content/78/2/185.full)
Gambar 4. Skema sederhana sistem lipoprotein dalam transpor lipid pada manusia (Talbert, 2008)
PENGENALAN PENYAKIT A. Definisi Dislipidemia
Hasil penelitian menunjukan bahwa resiko munculnya penyakit kardiovaskular berhubungan dengan meningkatnya kadar kolesterol total dan LDL, dimana resiko penyakit kardiovaskular akan meningkat seiring dengan meningkatnya kadar kolesterol total dan LDL. Nilai LDL dapat menjadi salah satu prediktor morbiditas dan mortalitas untuk beberapa penyakit kardiovaskular. Peningkatan kadar kolesterol total, LDL-C atau kadar trigliserida, penurunan konsentrasi HDL-C, atau beberapa kombinasi dari abnormalitas tersebut didefinisikan
sebagai dislipidemia.
Hiperlipoproteinemia merupakan suatu kelainan metabolik yang ditandai
dengan peningkatan konsentrasi
abnormal dari partikel lipoprotein spesifik pada plasma, sedangkan
hiperlipidemia sendiri didefinisikan sebagai peningkatan kadar plasma kolesterol atau trigliserida atau keduanya (Roy, 2011; Talbert, 2008). Sehingga jika ingin membahas penyakit
yang berhubungan dengan
abnormalitas lipid, lebih tepat jika menggunakan istilah dislipidemia.
B. Etiologi dan Patofisiologi
Faktor resiko terjadinya
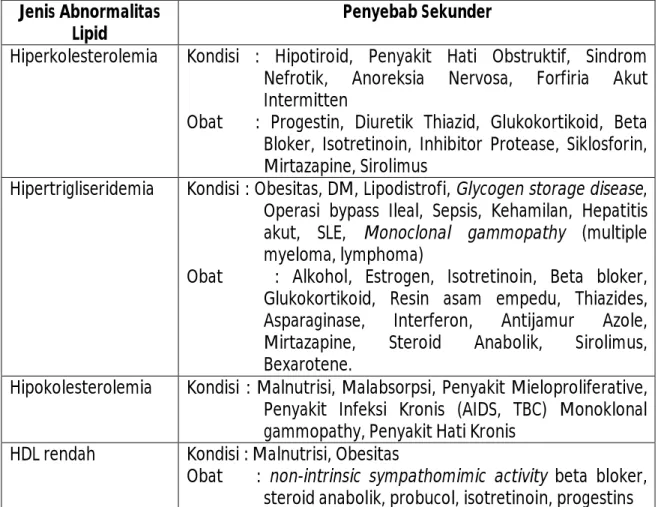
dislipidemia termasuk diantaranya adalah diet, stress, tidak aktif secara fisik dan merokok. Dislipidemia dapat bersifat primer atau genetik dan bersifat sekunder yang merupakan pengaruh dari suatu kondisi tertentu atau pengaruh dari penggunaan suatu obat yang dapat meningkatkan kadar lipid plasma (tabel 1) (Talbert, 2008).
Gangguan abnormalitas lipid apabila tidak terkontrol dapat menyebabkan mortalitas pada pasien, dimana mortalitas tertinggi muncul dari
LPL : lipoprotein lipase LDLR : low density lipoprotein
penyakit kardiovaskular dan serebrovaskular (Roy, 2011). Hipotesis
“response-to-injury” menyatakan
bahwa faktor resiko seperti LDL teroksidasi, cedera mekanik pada endotelium, homosistein yang berlebih, serangan imunologik dan induksi infeksi
dapat menyebabkan perubahan
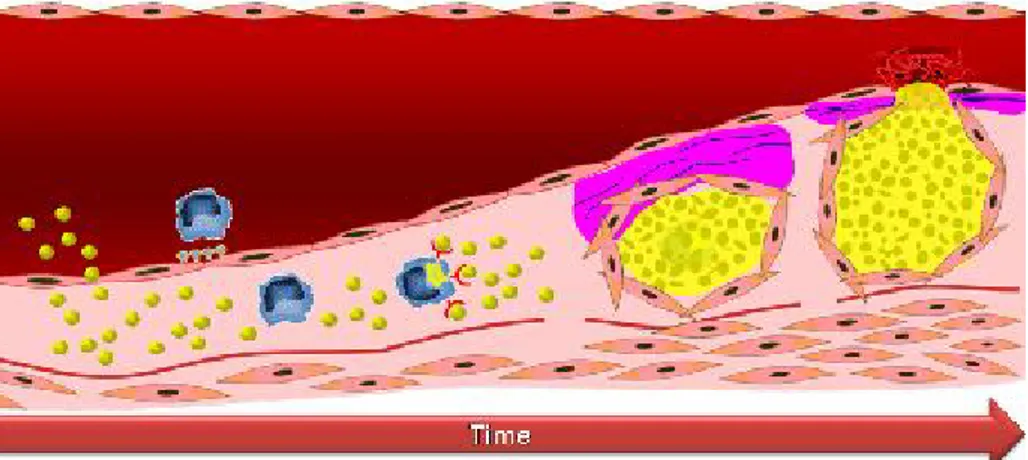
endotelial dan fungsi intimal, menyebabkan disfungsi endotelial dan serangkaian interaksi seluler yang berujung pada atherosklerosis (Talbert, 2008).
Tabel 1. Penyebab sekunder dari abnormalitas lipoprotein
Jenis Abnormalitas Lipid
Penyebab Sekunder
Hiperkolesterolemia Kondisi : Hipotiroid, Penyakit Hati Obstruktif, Sindrom Nefrotik, Anoreksia Nervosa, Forfiria Akut Intermitten
Obat : Progestin, Diuretik Thiazid, Glukokortikoid, Beta Bloker, Isotretinoin, Inhibitor Protease, Siklosforin, Mirtazapine, Sirolimus
Hipertrigliseridemia Kondisi : Obesitas, DM, Lipodistrofi, Glycogen storage disease, Operasi bypass Ileal, Sepsis, Kehamilan, Hepatitis akut, SLE, Monoclonal gammopathy (multiple myeloma, lymphoma)
Obat : Alkohol, Estrogen, Isotretinoin, Beta bloker, Glukokortikoid, Resin asam empedu, Thiazides, Asparaginase, Interferon, Antijamur Azole, Mirtazapine, Steroid Anabolik, Sirolimus, Bexarotene.
Hipokolesterolemia Kondisi : Malnutrisi, Malabsorpsi, Penyakit Mieloproliferative, Penyakit Infeksi Kronis (AIDS, TBC) Monoklonal gammopathy, Penyakit Hati Kronis
HDL rendah Kondisi : Malnutrisi, Obesitas
Obat : non-intrinsic sympathomimic activity beta bloker, steroid anabolik, probucol, isotretinoin, progestins Lesi atherosklerosis diperkirakan
muncul dari transport dan retensi dari LDL-C plasma melalui lapisan sel endotelial menuju matriks ekstraselular pada ruang subendothelial. Sekali berada pada dinding arteri, LDL akan termodifikasi secara kimia melalui oksidasi dan glikasi nonenzimatik. LDL
teroksidasi akan menyebabkan
penarikan monosit ke dinding arteri, dimana monosit akan berubah menjadi makrofag. Makrofag memiliki potensi untuk mempercepat oksidasi LDL dan
akumulasi ApoB dan merubah uptake LDL yang dimediasi reseptor pada dinding arteri dari yang mula-mula reseptor LDL biasa menjadi “reseptor scavenger” yang tidak bergantung pada kadar kolesterol dalam sel. LDL teroksidasi akan meningkatkan level
inhibitor plasminogen (promosi
koagulasi), menginduksi ekspresi endotelin (substansi vasokontriksi), menghambat ekspresi nitrit okside (vasodilator dan inhibitor platelet) dan bersifat toksik bagi makrofag bila
sangat teroksidasi. LDL teroksidasi akan memprovokasi respon inflamasi yang dimediasi oleh berbagai kemoatraktan dan sitokin, yang mana kemudian dapat menyebabkan akumulasi masif dari kolesterol. Sel yang sarat kolesterol disebut sel busa (foam cells) yang
merupakan komponen yang
menyebabkan endapan lemak pada dinding arteri (Talbert, 2008). Abnormalitas yang muncul pada sistem vaskular akibat adanya atherosklerosis antara lain adalah penyakit jantung iskemik.
Gambar 5. Proses atherosklerosis (http://users-phys.au.dk/jvn/Research-CABRA.htm)
C. Manifestasi Klinik dan Klasifikasi 1. Manifestasi klinik
Manifestasi klinik dari
hiperlipoproteinemia muncul karena adanya endapan lipid pada sistem vaskular dan mata. Secara umum
kebanyakan pasien tidak akan
menunjukan gejala tertentu untuk jangka waktu yang panjang sebelum muncul bukti klinis. Pasien dengan sindrom metabolik dapat memiliki tiga atau lebih presentasi klinik berikut : obesitas abdominal, dislipidemia aterogenik, peningkatan tekanan darah, resistensi insulin dengan atau tanpa intoleransi glukosa, keadaan
protrombotik, atau keadaan
proinflamatori.
a. Gejala : tanpa sampai dengan nyeri dada yang parah, palpitasi, berkeringat, anxietas, nafas pendek, kehilangan kesadaran atau kesulitan dalam berbicara atau
bergerak, nyeri abdomen,
kematian yang tiba-tiba.
b. Tanda : tanpa sampai dengan nyeri abdomen yang parah, pankreatitis, xanthomas eruptif, polineuropati perifer, tekanan darah tinggi, indeks massa tubuh > 30 kg/m2 atau ukuran pinggang > 40 inci (101,6 cm) pada pria atau 35 inci (88,9 cm) pada wanita.
c. Tes laboratorium : Peningkatan kolesterol total, LDL, trigliserida, apolipoprotein B, C-reactive protein serta penurunan level HDL. Klasifikasi kadar lipid dan kolesterol dapat dilihat pada tabel 2 dan tabel 3.
d. Tes diagnostik lainnya :
Lipoprotein(a), homosistein, serum amiloid A, small dense LDL (pola B), subklasifikasi HDL, isoform apolipoprotein E, apolipoprotein A-1, fibrinogen, folate, titer
Chlamydia pneumoniae,
lipoprotein terkait fosfolipase A2, omega-3 indeks. Tes diagnostik lain termasuk tes skrining manifestasi
penyakit vaskular (ankle-brachial
index, exercise testing, magnetic resonance imaging) dan diabetes
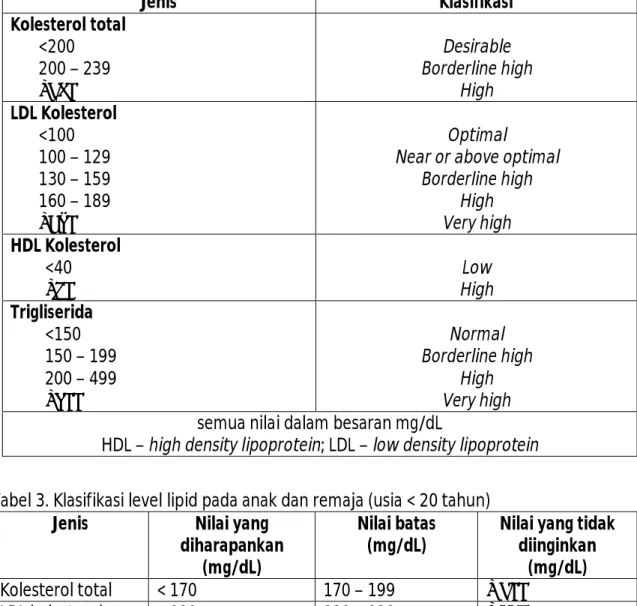
(glukosa puasa, tes toleransi glukosa oral) (Talbert, 2008). Tabel 2. Klasifikasi total kolesterol, LDL, HDL kolesterol dan trigliserida
Jenis Klasifikasi Kolesterol total <200 200 – 239 ≥240 Desirable Borderline high High LDL Kolesterol <100 100 – 129 130 – 159 160 – 189 ≥190 Optimal
Near or above optimal Borderline high High Very high HDL Kolesterol <40 ≥60 Low High Trigliserida <150 150 – 199 200 – 499 ≥500 Normal Borderline high High Very high
semua nilai dalam besaran mg/dL
HDL – high density lipoprotein; LDL – low density lipoprotein Tabel 3. Klasifikasi level lipid pada anak dan remaja (usia < 20 tahun)
Jenis Nilai yang
diharapankan (mg/dL)
Nilai batas (mg/dL)
Nilai yang tidak diinginkan
(mg/dL)
Kolesterol total < 170 170 – 199 ≥ 200
LDL kolesterol < 110 110 – 129 ≥ 130
HDL kolesterol > 45 25 – 45 < 35
Trigliserida < 125 not appicable ≥ 125
2. Klasifikasi
Hiperlipidemia dapat
diklasifikasikan menjadi hiperlipidemia primer (familial) yang disebabkan abnormalitas genetik spesifik dan hiperlipidemia sekunder (dapatan) yang disebabkan oleh kondisi lain yang dapat menyebabkan perubahan lipid plasma dan metabolisme protein (Tabel 1).
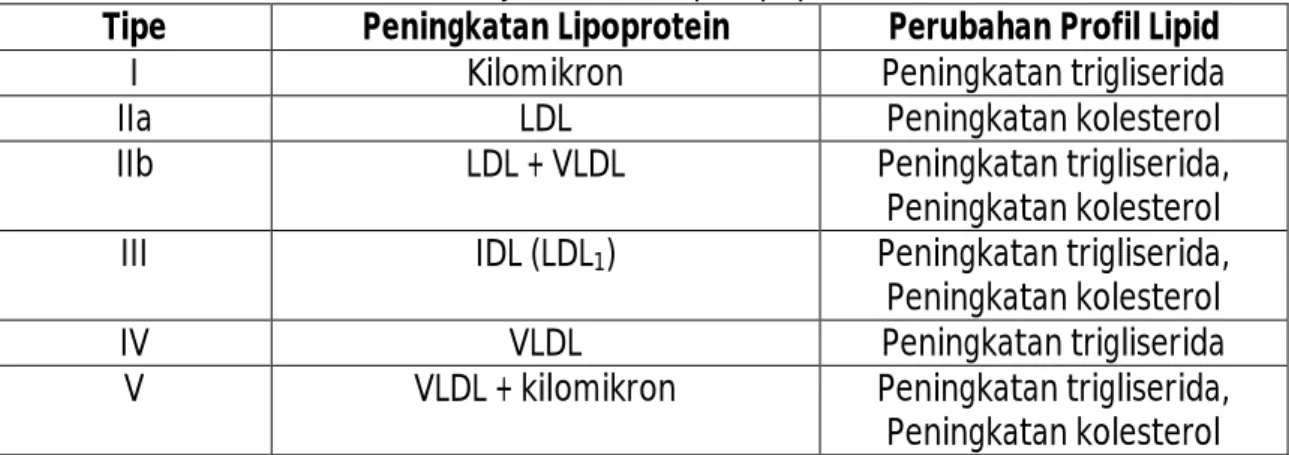
Hiperlipidemia juga dapat bersifat idiopatik, dimana penyebabkan tidak diketahui secara pasti. Klasifikasi hiperlipoproteinemia berdasarkan klasifikasi dari Fredrickson-Levy-Lees dapat dilihat pada tabel 4. Klasifikasi ini didasarkan pada deskripsi fenotipe dari dislipidemia (Fredrickson & Lees, 1965; Talbert, 2008).
Tabel 4. Klasifikasi Fredrickson-Levy-Lees dari hiperlipoproteinemia
Tipe Peningkatan Lipoprotein Perubahan Profil Lipid
I Kilomikron Peningkatan trigliserida
IIa LDL Peningkatan kolesterol
IIb LDL + VLDL Peningkatan trigliserida,
Peningkatan kolesterol
III IDL (LDL1) Peningkatan trigliserida,
Peningkatan kolesterol
IV VLDL Peningkatan trigliserida
V VLDL + kilomikron Peningkatan trigliserida,
Peningkatan kolesterol
TATALAKSANA TERAPI HIPERLIPIDEMIA
Tatalaksana terapi pada pasien hiperlipidemia harus disesuaikan dengan kondisi spesifik pasien. Faktor resiko tertentu (tabel 5 dan tabel 6) pada pasien akan mempengaruhi terapi dan target terapi pada pasien tersebut. Penurunan LDL merupakan target
dalam terapi pasien hiperlipidemia,
namun tujuan utama melakukan
perubahan gaya hidup terapetik dan terapi obat adalah untuk menurunkan resiko terjadinya atau serangan ulang dari infark miokard. Angina, gagal jantung, stroke iskemik,dan bentuk lain dari penyakit arteri perifer, misalnya stenosis karotid dan aneurisma aortik abdominal (Talbert, 2008).
Tabel 5. Faktor resiko utama (khusus LDL kolesterol) yang mempengaruhi target LDLa Usia
Pria ≥ 45 tahun
Wanita ≥ 55 tahun atau menopause prematur tanpa terapi penggantian estrogen Riwayat keluarga penyakit jantung koroner prematur (didefinisikan sebagai infark
miokard atau kematian tiba-tiba sebelum umur 55 tahun pada ayah atau hubungan kekeluargaan pria pada tingkat pertama, atau sebelum usia 65 tahun pada ibu atau hubungan kekeluargaan wanita pada tingkat pertama)
Riwayat merokok
Hipertensi (≥140/90 mmHg atau sedang menkonsumsi obat antihipertensi) HDL kolesterol rendah (<40 mg/dL)b
a. Diabetes dianggap memiliki resiko yang setara dengan penyakit jantung koroner b. HDL kolesterol ≥60 mg/dL dihitung sebagai faktor resiko “negatif”; munculnya
faktor resiko ini akan menghilangkan satu faktor resiko dari total hitungan.
A. Tatalaksana Terapi Non Farmakologi
Tatalaksana terapi non
farmakologi pada pasien hiperlipidemia perubahan gaya hidup terapetik. Perubahan gaya hidup harus dilakukan oleh seluruh pasien prior to considering
drug therapy. Komponen perubahan gaya hidup termasuk di dalamnya adalah :
1. Penurunan intake lemak jenuh dan kolesterol
2. Pilihan diet untuk menurunkan LDL, misalnya peningkatan
konsumsi stanol / sterol tumbuhan dan asupan serat 3. Penurunan berat badan
4. Meningkatkan aktivitas fisik : secara umum, aktivitas fisik
intensitas sedang selama 30 menit perhari setiap hari dalam seminggu harus digiatkan
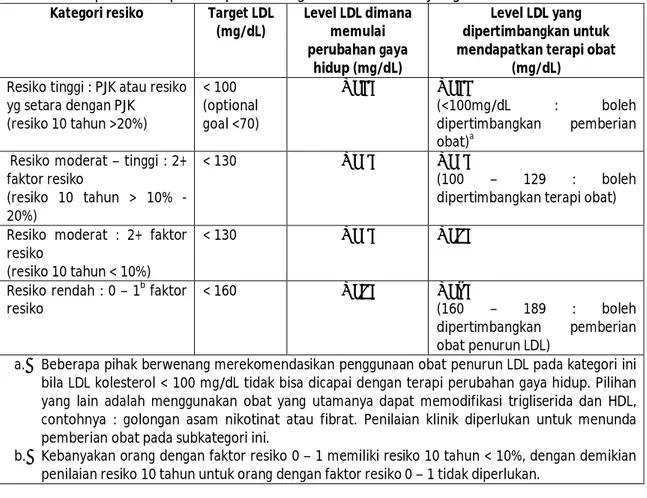
Tabel 6. Target LDL kolesterol dan titik potong untuk terapi dengan perubahan gaya hidup dan terapi obat pada kategori faktor resiko yang berbeda
Kategori resiko Target LDL (mg/dL) Level LDL dimana memulai perubahan gaya hidup (mg/dL) Level LDL yang dipertimbangkan untuk mendapatkan terapi obat
(mg/dL)
Resiko tinggi : PJK atau resiko yg setara dengan PJK (resiko 10 tahun >20%) < 100 (optional goal <70) ≥ 100 ≥ 100 (<100mg/dL : boleh dipertimbangkan pemberian obat)a
Resiko moderat – tinggi : 2+ faktor resiko
(resiko 10 tahun > 10% - 20%)
< 130 ≥ 130 ≥ 130
(100 – 129 : boleh dipertimbangkan terapi obat) Resiko moderat : 2+ faktor
resiko
(resiko 10 tahun < 10%)
< 130 ≥ 130 ≥ 160
Resiko rendah : 0 – 1b faktor resiko
< 160 ≥ 160 ≥ 190
(160 – 189 : boleh dipertimbangkan pemberian obat penurun LDL)
a. Beberapa pihak berwenang merekomendasikan penggunaan obat penurun LDL pada kategori ini bila LDL kolesterol < 100 mg/dL tidak bisa dicapai dengan terapi perubahan gaya hidup. Pilihan yang lain adalah menggunakan obat yang utamanya dapat memodifikasi trigliserida dan HDL, contohnya : golongan asam nikotinat atau fibrat. Penilaian klinik diperlukan untuk menunda pemberian obat pada subkategori ini.
b. Kebanyakan orang dengan faktor resiko 0 – 1 memiliki resiko 10 tahun < 10%, dengan demikian penilaian resiko 10 tahun untuk orang dengan faktor resiko 0 – 1 tidak diperlukan.
Pasien dengan penyakit jantung koroner atau mereka yang memiliki resiko tinggi harus dievaluasi sebelum melakukan latihan yang berat. Berat badan dan indeks massa tubuh harus diukur pada tiap pertemuan dengan dokter, dan pola gaya hidup untuk menginduksi penurunan berat badan sebesar 10% harus didiskusikan dengan pasien obesitas. Seluruh pasien harus dikonseling untuk berhenti merokok dan untuk pasien yang mengalami
hipertensi harus diterapi sesuai dengan panduan dari Joint National Committee
VII. Banyak pasien harus diberikan
percobaan selama 3 bulan (2 kali pertemuan dengan jarak tiap 6 bulan) untuk terapi diet dan perubahan gaya
hidup terapetik sebelum mulai
mendapatkan terapi obat kecuali pasien termasuk pasien dengan resiko sangat tinggi (hiperkolesterolemia berat, penyakit jantung koroner yang diketahui, resiko yang ekuivalen
dengan penyakit jantung koroner, faktor resiko ganda, sejarah keluarga
yang kuat) (Talbert, 2008).
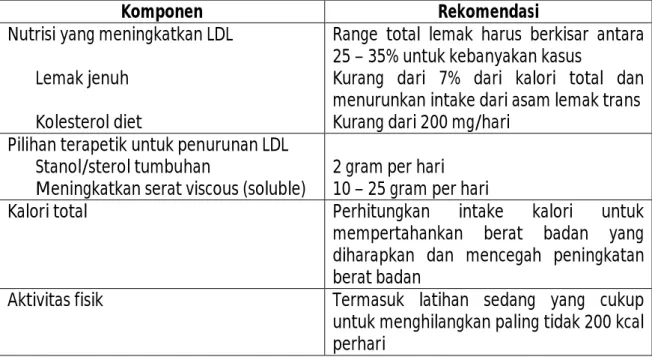
Tabel 7. Komponen esensial dari perubahan gaya hidup terapetik (Therapeutic Lifestyle
Changes / TLC)
Komponen Rekomendasi
Nutrisi yang meningkatkan LDL Lemak jenuh
Kolesterol diet
Range total lemak harus berkisar antara 25 – 35% untuk kebanyakan kasus
Kurang dari 7% dari kalori total dan menurunkan intake dari asam lemak trans Kurang dari 200 mg/hari
Pilihan terapetik untuk penurunan LDL Stanol/sterol tumbuhan
Meningkatkan serat viscous (soluble)
2 gram per hari 10 – 25 gram per hari
Kalori total Perhitungkan intake kalori untuk
mempertahankan berat badan yang diharapkan dan mencegah peningkatan berat badan
Aktivitas fisik Termasuk latihan sedang yang cukup
untuk menghilangkan paling tidak 200 kcal perhari
B. Tatalaksana Terapi Farmakologi
Terapi obat diindikasikan setelah dilakukan perubahan gaya
hidup terapetik yang adekuat.
Walaupun telah banyak obat penurun lipid yang efikasius, tidak satupun yang yang efektif untuk semua gangguan lipoprotein dan setiap obat memiliki efek samping. Berdasarkan mekanisme kerjanya, obat penurun lipid secara umum dapat dibedakan menjadi obat yang dapat menurunkan sintesis VLDL
dan LDL, obat yang dapat
meningkatkan klirens VLDL, obat yang meningkatkan katabolisme LDL, obat yang dapat menurunkan absorpsi
kolesterol, obat yang dapat
meningkatkan HDL dan kombinasinya (Talbert, 2008).
1. Niacin (Nicotinic acid)
Niacin merupakan obat
penurun lipid pertama yang dihubungkan dengan penurunan
mortalitas total. Niacin
menurunkan produksi partikel VLDL, menurunkan level LDL dan meningkatkan level HDL kolesterol. Efek rata – rata dari dosis penuh 3 – 4,5 g/hari terapi niasin adalah penurunan LDL kolesterol sebesar 15 – 25% dan peningkatan HDL kolesterol sebesar 25 – 35%. Dosis
penuh dibutuhkan untuk
mendapatkan efek LDL, namun efek HDL telah ditunjukan pada dosis yang lebih rendah yaitu pada dosis 1g/hari. Niacin juga dapat menurunkan trigliserida dan
lipoprotein A dan akan
meningkatkan level homosistein. Intoleransi terhadap niacin sering terjadi, hanya sekitar 50 – 60% pasien yang dapat menerima dosis penuh. Niacin dapat menyebabkan
flushing yang dimediasi prostaglandin yang dideskripsikan pasien sebagai ”hot flashes” atau pruritus dan dapat diturunkan
dengan pemberian pretreatment dengan aspirin (81 – 325 mg/hari) atau obat NSAID lainnya. Flushing juga dapat diturunkan dengan memulai terapi niacin dengan dosis yang sangat kecil misalnya 100 mg pada waktu makan malam. Dosis kemudian dapat digandakan setiap minggunya sampai dosis 1,5 g/hari ditoleransi. Setelah cek ulang lipid darah, dosis kemudian dapat dibagi dan ditingkatkan sampai target 3 – 4,5 g/hari tercapai. Niacin extended
release juga tersedia dan lebih
ditoleransi dengan baik pada kebanyakan pasien. Niacin juga dapat menyebabkan eksaserbasi gout dan penyakit peptik ulcer. Walaupun niacin mungkin dapat meningkatkan gula darah pada beberapa pasien, percobaan klinik menunjukan bahwa niacin aman digunakan pada pasien diabetik (Baron , 2006).
2. Bile acid-binding resin
Golongan resin pengikat
asam empedu termasuk di
dalamnya adalah kolestiramin, kolesevelam dan kolestipol. Terapi dengan obat ini dapat menurunkan insidensi dari kejadian koroner pada pria usia pertengahan sebanyak 20%, tanpa perbedaan signifikan pada efek mortalitas total. Resin bekerja dengan cara mengikat asam empedu pada
intestin. Mekanisme yang
bersamaan adalah penurunan
sirkulasi enterohepatik yang
kemudian menyebabkan hati
meningkatkan produksi asam
empedunya, menggunakan
kolesterol hepatik. Aktivitas
reseptor hepatik LDL akan
meningkat, menyebabkan
terjadinya penurunan level LDL plasma. Level trigliserida dapat meningkat sedikit pada beberapa pasien yang diterapi dengan resin pengikat asam empedu, sehingga penggunaan obat ini harus dengan peringatan pada pasien yang mengalami peningkatan trigliserida dan tidak diberikan pada semua pasien dengan kadar trigliserida diatas 500 mg/dL. Klinisi dapat
mengharapkan penurunan
sebanyak 15-25% pada level LDL kolesterol, dengan efek yang signifikan pada level HDL.
Dosis lazim dari
kolestiramin adalah 12 – 36 g resin per hari dalam dosis terbagi dengan makanan, dicampur dalam air atau dalam jus. Dosis kolestipol 20% lebih tinggi (tiap bungkus mengandung 5 g resin). Dosis dari kolesevelam adalah 625 mg per tablet, 6 – 7 tablet per hari. Obat –
obat golongan ini dapat
menyebabkan gejala
gastrointestinal, misalnya
konstipasi dan gas. Dapat
mengganggu absorpsi vitamin larut
lemak (sehingga sangat
complicating pada managemen
pasien yang mendapatkan
warfarin) dan dapat juga berikatan dengan obat lain pada saluran cerna (Baron, 2006).
3. Hydroxymethylglutaryl-Coenzyme
A (HMG-CoA) Reductase Inhibitors
(Statin)
HMG-CoA reductase
inhibitors termasuk di dalamnya
adalah atorvastatin, fluvastatin, lovstatin, pravastatin, rosuvastatin dan simvastatin. Mekanisme obat golongan ini adalah dengan menghambat rate limiting enzyme
pada pembentukan kolesterol.
Obat golongan ini dapat
menurunkan infark mikard dan mortalitas total pada pencegahan sekunder, sama halnya pada pencegahan untuk pasien pria usia pertengahan yang bebas penyakit jantung koroner. Penelitian meta
analisis menunjukan bahwa
penggunaan obat ini dapat
menurunkan resiko terjadinya stroke. Sintesis kolesterol dapat diturunkan, dengan kompensasi berupa peningkatan aktivitas reseptor LDL hepatik (dengan asumsi bahwa kemudian hati dapat lebih mengambil kolesterol yang dibutuhkan dari darah) dan terjadi penurunan level LDL kolesterol dalam sirkulasi sampai dengan 35%. Juga terjadi peningkatan sedang level HDL dan penurunan level trigliserida.
Dosis lazim atorvastatin, 10–80 mg/hari; fluvastatin, 20–40 mg/hari; lovastatin, 10–80 mg/hari; pravastatin, 10–40 mg/hari; rosuvastatin, 5–40 mg/hari; dan simvastatin, 5–40 mg/hari. Obat – obat golongan ini biasanya diberikan satu kali sehari pada saat malam hari (dimana sebagian besar sintesis kolesterol terjadi pada malam hari). Pada rentang dosis akhir yang tinggi, dosis bagi dua kali sehari dapat digunakan. Efek sampingnya antara lain miositis, yang kejadiannya dapat lebih tinggi
pada pasien yang juga
mendapatkan fibrat atau niasin
bersamaan dengan statin.
Produsen merekomendasikan
untuk melakukan monitoring enzim hati dan otot. Beberapa obat (eritromisin, siklosporin dan
antijamur azole) menurunkan metabolisme obat ini (Baron, 2006).
4. Fibric acid derivatives
Derivat asam fibrat
termasuk gemfibrozil, fenofibrat dan klofibrat. Fibrat dapat
menurunkan sintesis dan
meningkatkan pemecahan partikel VLDL, dengan efek sekunder pada level LDL dan HDL. Obat golongan ini menurunkan level LDL sampai dengan 10 – 15% dan level trigliserida sampai dengan 40% dan meningkatkan level HDL sampai 15 – 20%. Dosis lazim gemfibrozil adalah 600 mg satu atau dua kali sehari. Efek sampingnya termasuk kholelithiasis, hepatitis dan miositis. Insidensi hepatitis dan miositis dapat meningkat pada pasien yang juga mendapatkan obat penurun lipid lainnya. Hasil penelitian klinik yang besar menunjukan bahwa penggunaan klofibrat menunjukan kematian yang lebih tinggi secara signifikan, terutama karena kanker, pada kelompok perlakukan, sehingga sebaiknya tidak digunakan (Baron, 2006).
5. Ezetimibe
Ezetimibe merupakan obat
penurun lipid baru yang
mekanisme kerjanya dengan
menghambat absorpsi kolesterol dari diet dan bilier dengan memblok penyebrangan (passage) melewati dinding saluran cerna. Ezetimibe dapat menurunkan LDL kolesterol antara 15 – 20% saat digunakan sebagai monoterapi dan dapat membantu menurunkan level LDL pada pasien yang mendapatkan statin yang belum
mencapai target terapetik. Efek dari ezetimide pada penyakit jantung koroner dan keamanan jangka panjangnya belum diketahui secara pasti. Dosis lazim ezetimide adalah 10 mg/hari (Baron, 2006).
6. Suplemen minyak ikan (N-3
Polyunsaturated Fatty Acids atau N-3 PUFA atau Omega-3 Fatty Acids)
Penggunaan suplementasi minyak ikan (ikan, minyak ikan, atau minyak asam linolenik tinggi) pada dosis rendah (1 – 2 g/hari) disebutkan untuk pencegahan
penyakit jantung koroner.
Berdasarkan bukti klinis,
penggunaan suplemen minyak ikan pada dosis 3 – 4 gram perhari adalah aman dan effikasius dalam menurunkan trigliserida dan merupakan alternatif terhadap fibrat atau asam nikotinat dalam
terapi hipertrigliseridemia
(Blackmore, dkk, 2004)
Tabel 8 menunjukan rangkuman efek terapi obat penurun lipid dan lipoprotein, sedangkan pada tabel 9 dapat dilihat pilihan obat yang direkomendasikan dalam penanganan berbagai tipe hiperlipidemia.
C. Pilihan Terapi Farmakologi pada Berbagai Kondisi
Obat penurun lipid, seperti yang dijelaskan sebelumnya, tidak efektif
untuk menangani semua tipe
abnormalitas lipid, sehingga dalam pemilihannya perlu memperhatikan
abnormalitas lipid yang terjadi pada pasien, faktor resiko, penyakit penyerta dan kondisi klinis pasien.
1. Hiperkolesterolemia primer
(hiperkolesterolemia familial, hiperlipidemia familial kombinasi, hiperlipoproteinemia tipe IIa), dapat diterapi dengan resin asam
empedu, HMG-CoA reduktase
inhibitor, niacin atau ezetimibe.
Mempertimbangkan kepatuhan,
adverse effect, dan efektifitas
untuk pasien dengan
hiperkolesterolemia, statin
merupakan obat pilihan karena merupakan obat penurun LDL yang paling poten sebagai monoterapi dan cost effective pada pasien dengan penyakit arteri koroner atau faktor resiko ganda dan pada pasien pencegahan primer resiko tinggi. Pada pasien yang tidak respon dengan monoterapi statin, dapat diterapi dengan terapi
kombinasi namun perlu
pemantauan yang ketat karena dapat meningkatkan resiko efek samping dan interaksi obat. Contoh kombinasi terapi yang rasional salah satunya adalah resin pengikat asam empedu dan lovastatin, dimana terjadi peningkatan jumlah
reseptor LDL menyebabkan
degradasi LDL-C yang lebih besar; sintesis intraselular kolesterol dihambat; dan siklus enterohepatik dari asam empedu diinterupsi.
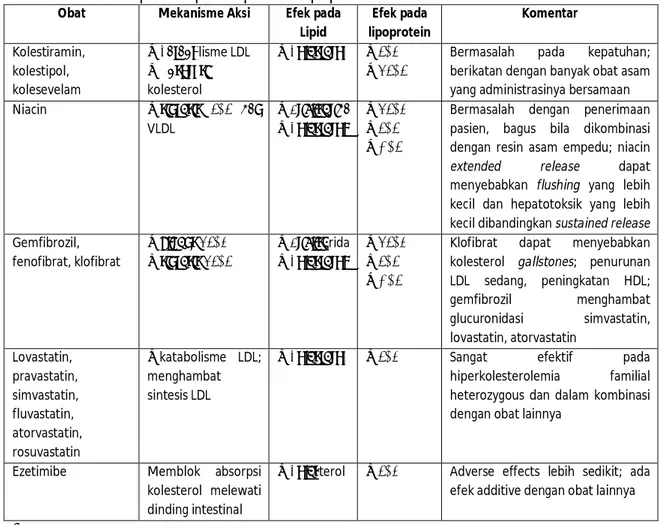
Tabel 8. Efek terapi obat pada lipid dan lipoprotein
Obat Mekanisme Aksi Efek pada
Lipid Efek pada lipoprotein Komentar Kolestiramin, kolestipol, kolesevelam ↑Katabolisme LDL ↓Absorpsi kolesterol ↓Kolesterol ↓LDL ↑VLDL
Bermasalah pada kepatuhan; berikatan dengan banyak obat asam yang administrasinya bersamaan
Niacin ↓sintesis LDL dan
VLDL ↓Trigliserida ↓Kolesterol ↓VLDL ↓LDL ↑HDL
Bermasalah dengan penerimaan pasien, bagus bila dikombinasi dengan resin asam empedu; niacin
extended release dapat
menyebabkan flushing yang lebih kecil dan hepatotoksik yang lebih kecil dibandingkan sustained release Gemfibrozil, fenofibrat, klofibrat ↑klirens VLDL ↓sintesis VLDL ↓Trigliserida ↓Kolesterol ↓VLDL ↓LDL ↑HDL
Klofibrat dapat menyebabkan kolesterol gallstones; penurunan LDL sedang, peningkatan HDL; gemfibrozil menghambat glucuronidasi simvastatin, lovastatin, atorvastatin Lovastatin, pravastatin, simvastatin, fluvastatin, atorvastatin, rosuvastatin ↑katabolisme LDL; menghambat sintesis LDL
↓Kolesterol ↓LDL Sangat efektif pada
hiperkolesterolemia familial heterozygous dan dalam kombinasi dengan obat lainnya
Ezetimibe Memblok absorpsi kolesterol melewati dinding intestinal
↓Kolesterol ↓LDL Adverse effects lebih sedikit; ada efek additive dengan obat lainnya
2. Hiperlipoproteinemia kombinasi (tipe IIb) dapat diterapi dengan statin, niacin atau gemfibrozil untuk menurunkan LDL-C tanpa
meningkatkan VLDL dan
trigliserida. Niacin merupakan obat yang paling efektif dan dapat dikombinasikan dengan resin
pengikat asam empedu.
Penggunaan resin pengikat asam empedu sebagai monoterapi untuk gangguan ini dapat meningkatkan VLDL dan trigliserida sehingga
penggunaanya sebagai obat
tunggal harus dihindari.
3. Hiperlipoproteinemia tipe III dapat diterapi dengan asam fibrat dan niacin. Walaupun asam fibrat telah dianjurkan sebagai obat pilihan untuk tipe ini, namun kurangnya data utama mengenai effikasinya dalam mempengaruhi mortalitas kardiovaskular dan sejumlah efek
samping serius yang telah
terdokumentasi dalam
pemakaiannya, membuat
penggunaan niacin juga dapat dipertimbangkan.
Tabel 9. Fenotip lipoprotein dan terapi obat yang direkomendasikan
Tipe lipoprotein Obat pilihan Terapi kombinasi
I Tidak diindikasikan -
IIa Statins
Kolestiramin atau
kolestipol Niacin
Niacin atau BAR Statin atau niacin Statin atau BAR Ezetimibe
IIb Statin
Fibrat Niacin
BAR, fibratesb, atau niacin Statin, niacin, BARa
Statin atau fibrates Ezetimibe
III Fibrat
Niacin
Statin atau niacin Statin atau fibrat Ezetimibe IV Fibrat Niacin Niacin Fibrat V Fibrat Niacin Niacin Fish oils
a. Bile acid resins (BARs) tidak digunakan sebagai terapi lini pertama apabila terjadi peningkatan trigliserida melewati baseline karena hipertrigliseridemia dapat menjadi lebih buruk pada penggunaan BAR sebagai monoterapi
b. Fibrat termasuk gemfibrosil atau fenofibrat 4. Hipertrigliseridemia, penting untuk
diingat bahwa pola gangguan lipoprotein tipe I, III, IV dan V
diasosiasikan dengan
hipertrigliseridemia. Trigliserida serum yang tinggi harus diterapi dengan mencapai berat badan yang diharapkan, konsumsi diet rendah lemak jenuh dan kolesterol, latihan fisik yang reguler, berhenti merokok dan retriksi alkohol. Obat
yang berguna untuk terapi
hiperkolesterolemia termasuk di dalamnya adalah gemfibrozil, niacin dan statin potensi tinggi (atorvastatin, rosuvastatin, dan
simvastatin). Gemfibrozil
merupakan obat pilihan pada pasien diabetes karena efek niacin terhadap kontrol glikemik kecuali
bentuk sediaan baru extended
release digunakan. Fenofibrat dapat dipilih dalam kombinasi dengan statin karena tidak mengganggu glukuronidasi dan meminimalkan interaksi obat potensial. Terapi yang sukses didefinisikan apabila terjadi penurunan trigliserida < 500 mg/dL.
5. HDL-C rendah merupakan resiko
prediktor bebas yang kuat
terhadap penyakit jantung
koroner. Managemen yang dapat dilakukan antaranya adalah reduksi
berat badan, meningkatkan
aktivitas fisik, berhenti merokok dan apabila dibutuhkan terapi obat, dapat digunakan fibrat dan niacin. Niacin merupakan obat
yang potensial untuk peningkatan yang paling besar dari HDL, efeknya lebih tampak pada bentuk sediaan reguler atau immediate release dibandingkan bentuk sediaan
sustained release.
6. Diabetik dislipidemia
dikarakterisasi dengan
hipertrigliseridemia, HDL rendah dan LDL meningkat sedikit. Diabetes memiliki resiko yang setara dengan penyakit jantung koroner. Target utama pada diabetik dislipidemia adalah menurunkan LDL-C < 100 mg/dL. Bilamana LDL > 130 mg/dL,
sebagian besar pasien
membutuhkan perubahan gaya hidup terapetik dan terapi obat. Apabila LDL-C berkisar antara 100 – 129 mg/dL, intensifkan kontrol glikemik, pilihannya termasuk
menambahkan obat untuk
dislipidemia atherogenik (fibrat, niacin) dan mengintensifkan terapi penurun LDL-C. Karena target utama pada pasien diabetik dislipidemia adalah LDL-C, terapi statin dipertimbangkan sebagai obat pilihan pertama.
7. Pasien usia lanjut,
hiperkolesterolemia merupakan faktor resiko independen terhadap terjadinya penyakit jantung koroner pada pasien usia lanjut (> 65 tahun) sama halnya dengan pasien yang lebih muda. Terapi obat pada pasien usia lanjut prinsipnya hanya berbeda sedikit dengan pasien yang lebih muda. Pasien lansia memberikan respon sebaik pasien yang lebih muda terhadap obat penurun lipid. Karena ada perubahan dalam komposisi tubuh, fungsi renal, dan
perubuhan fisiologik lainnya karena usia menyebabkan pasien usia lanjut lebih sensitif terhadap terjadinya efek samping obat penurun lipid. Pasien usia lanjut lebih sering mengalami konstipasi (resin pengikat asam empedu), gangguan kulit dan mata (niacin), gout (niacin), gallstones (fibrat), dan gangguan tulang/sendi (fibrat, statin). Untuk meminimalkan resiko efek samping, terapi harus dimulai dengan dosis rendah dan peningkatan dosis dititrasi secara perlahan. Karena kebanyakan wanita dengan penyakit jantung koroner adalah usia lanjut dan memiliki resiko osteoporosis, mereka merupakan kandidat untuk terapi diet dengan pertimbangan intake kalsium yang konsisten dengan pencegahan osteoporosis, latihan, dan kemungkinan terapi penggantian estrogen. Bukti menunjukan bahwa penggunaan obat penurun lipid statin dapat menurunkan resiko osteoporosis,
namun data dari berbagai
penelitian masih bertentangan. 8. Wanita hamil, kolesterol dan
trigliserida dapat meningkat pada masa kehamilan, dengan rata – rata peningkatan kolesterol 30 – 40 mg/dL yang muncul pada minggu 36 sampai dengan 39. Trigliserida dapat meningkat sampai dengan 150 mg/dL. Terapi obat tidak dianjurkan, ataupun dilanjutkan selama kehamilan. Bilamana pasien memiliki resiko yang sangat tinggi, resin pengikat asam empedu dapat dipertimbangkan karena tidak
munculnya eksposure obat
sistemik. Terapi diet merupakan terapi utama.
9. Anak – anak, terapi obat pada anak – anak tidak dianjurkan sampai mereka berusia 10 tahun dan lebih dewasa. Statin menunjukan tingkat keamanan dan keefektifan pada anak dan memberikan penurunan lipid yang lebih baik dibandingkan obat penurun lipid sebelumnya yang direkomendasikan (resin pengikat asam empedu).
10. Penyakit seperti sindrom nefrotik, gagal ginjal tahap akhir dan hipertensi merupakan salah satu resiko terjadinya dislipidemia dan dapat menimbulkan kesulitan untuk menterapi abnormalitas
lipid. Statin menunjukan
keefektifan dalam menurunkan kolesterol total dan LDL-C pada
pasien sindrom nefrotik, walaupun tidak bisa mengembalikannya ke level normal. Statin muncul sebagai obat yang aman dan efektif pada insufisiensi renal. Koreksi
abnormalitas lipid dapat
memperbaiki hemodinamik renal, dimana pravastatin dan fluvastatin dapat lebih aman dari statin yang lainnya, namun harus divalidasi dengan penelitian yang lebih besar. Rekomendasi untuk pasien dengan hipertensi dan hiperkolesterolemia
termasuk didalamnya adalah
menghindari penggunaan obat
yang dapat meningkatkan
kolesterol seperti diuretik dan beta bloker (Baron, 2006; Talbert, 2008).
PENUTUP
Penyakit dislipidemia
merupakan faktor resiko terhadap terjadinya penyakit kardiovaskular lainnya yang mana apabila tidak
diterapi dengan baik akan
meningkatkan morbiditas dan
mortalitas kardiovaskular. Tatalaksana terapi pada penyakit dislipidemia harus didasarkan atas etiologi dan faktor resiko yang mendasarinya. Perubahan gaya hidup terapetik merupakan suatu langkah awal yang harus dilakukan pada semua pasien hiperlipidemia baik mereka yang merupakan kandidat
untuk mendapatkan terapi obat
maupun yang bukan kandidat untuk mendapatkan terapi obat.
Terdapat 6 kelompok terapi farmakologi yang dapat digunakan untuk menterapi pasien hiperlipidemia. Namun tidak ada 1 obatpun yang efektif untuk menterapi semua jenis abnormalitas. Tatalaksana terapi obat
pada pasien dislipidemia haruslah melihat klasifikasi gangguan yang terjadi pada pasien dengan demikian pemilihan obat dapat dilakukan secara optimal. Penyesuaian dosis dan monitoring diperlukan pada pasien untuk mencapai target terapi dan meminimalkan resiko terjadinya reaksi obat yang tidak dikehendaki.
DAFTAR PUSTAKA
Baron, R.B., 2006, Lipid Abnormalities in Tierney,L.M., McPhee,S.J., Papadakis, M.A. (eds), Current
Medical Diagnosis and Treatment, 45 Edition,
McGraw-Hill, New York.
Blackmore,J.R., Bretzke, D.R., Downs, J.R., Fishman, R., Wendy, B., Fonseca, V.P., et all., 2006,
VA/DoD Clinical Practice Guideline for the Management of Dyslipidemia, Department of Veterans Affairs – Department of Defense, USA.
Carleton, P.F., Boldt, M.A., 1995, Penyakit Aterosklerotik Koroner, dalam Price,S.A., Wilson,L.M. (eds) Patofisiologi : Konsep Klinis
Proses – Proses Penyakit, Penerbit
Buku Kedokteran EGC, Jakarta. Fredrickson,D.S., Lees,R.S., 1965,
Editorial : A System for Phenotyping
Hyperlipoproteinemia, Circulation
: Journal of American Heart Association 1965, 31:321-327. Roy, H., 2011, Hyperlipoproteinemia, [Online] Sumber: http://emedicine.medscape.com/ article/1214018-overview (09 Agustus 2011). Talbert, R.L., 2008, Dyslipidemia in Dipiro, J.T., Talbert,R.L., Yee,G.C., Matzke,
G.R.,Wells,B.G.,Posey,L.M. (eds),
Pharmacotherapy : a Pathophysiologic Approach,