TUGAS KHUSUS
Evaluasi Efisiensi Energi CO
2Kompresor pada Pabrik Urea
dengan mempertimbangkan sifat Gas Non-ideal pada Tekanan
Tinggi
VI.1.1 Latar Belakang
Kompresor ini merupakan salah satu alat yang ada dalam proses pembuatan urea di pabrik urea pusri-II Pupuk Sriwidjaja Palembang. Di sini akan dievaluasi sebuah kompresor dengan tag number GB 151-J. Dalam hal ini Kompresor adalah kompresor sentrifugal dengan penggerak turbin uap yang berfungsi sebagai mengkompresi/menaikkan tekanan CO2 menuju tekanan operasi reaktor sekitar 185 kg/cm2
sehingga konversi gas CO2 (pembentukan urea) bisa optimal.
Kompresor gas CO2 GB 151-J merupakan salah satu langkah
pertama dalam memproduksikan urea dan merupakan bagian daripada sistem. Kompresor ini terdiri dari 4 stage dengan sistem intercooler antara cases.
Mengingat pentingnya fungsi kompresor 151-J, perlu dilakukan analisa dan monitoring yang terus menerus terhadap unjuk kerja kompresor tersebut. Untuk mengevaluasi unjuk kerja kompresor, perlu diketahui data spesifikasi yang menunjukan karakteristik kompresor dimaksud serta data kondisi operasi yang menunjukan kemampuan kerja kompresor secara nyata.
Kompresor CO2 GB 151
Kompresor ini terdiri dari 4 bagian dan antara tiap cases dilengkapi dengan pendingin, sebagai penggerak adalah steam turbine. Kompresor GB 151 beroperasi dengan kecepatan normal design 20100 rpm equivalent dengan kecepatan minimum 7440 rpm dan kecepatan maksimum 12260 rpm. Gas masuk kompresor pada tekanan 0.6 kg/cm2 (8.53 Psia).
Gas masuk ke stage 1 kompresor pada suhu 42.10°C. Gas yang keluar dari stage 1 pada suhu 215.86 °C didinginkan di 111-R sampai 42°C. Gas yang keluar ke stage 2 masuk pada tekanan 7 kg/cm2 (99.56 psia) kemudian keluar dari stage 2 didinginkan di 112-R sampai 41°C. Gas kemudian masuk ke stage 3 dan keluar dengan tekanan 84.53 kg/cm2 dan suhu 146.71 °C lalu didinginkan di 113-R hingga suhu 52.95
°C. Setelah itu gas masuk ke stage 4. Gas keluar dari stage 4 dengan tekanan 165 kg/cm2 dan suhu 121.08°C.
Kompresor dilengkapi dengan lube oil/seal oil console termasuk juga pompa-pompa lube oil dan seal oil yang digerakkan oleh turbin, pompa-pompa lube oil dan seal oil pelengkap (auxiliary) yang digerakkan dengan motor, tangki overhead seal oil, penyaring dan pendingin minyak, tangki pemisah gas sebelum minyak kembali ke tangki reservoir penampung minyak, alarm untuk tekanan minyak rendah start-up pompa auxiliary, alarm permukaan seal oil, dan alarm
(pemanasan). VI.1.2 Tujuan
1. Mengetahui prinsip kerja kompresor CO2 di pabrik urea dengan
meninjau segi kuantitatfinya.
2. Mengevalusi nilai efisiensi kompresor CO2 di pabrik urea pusri II.
VI.1.3 Metodologi
1. Mempelajari prinsip kerja kompresor CO2 di Pabrik Urea.
2. Observasi lapangan, dilakukan di PT. Pupuk Sriwidjaja Palembang pada Pabrik Urea Pusri II.
3. Pengambilan data design dan aktual di lapangan.
4. Penyelesaian perhitungan efisiensi dari kompresor CO2 di Pabrik
Urea pusri II. VI.1.4 Tinjauan Pustaka
Fungsi dari sebuah kompresor adalah untuk menaikkan tekanan suatu gas. Tekanan gas dapat ditingkatkan dengan memaksakan pengurangan volumenya. Ketika volumenya dikurangi, tekanannya meningkat. Sebuah kompresor “positive displacement”, memperlakukan gas dengan cara tersebut. Tetapi, sebuah kompresor sentrifugal mencapai peningkatan tekanan dengan dua tahap. Kompresor tersebut menambah energi pada gas dalam bentuk kecepatan (energi kinetik) dan kemudian merubah bentuk energi tersebut menjadi energi tekanan.
Sebuah kompresor sentrifugal menggunakan konsep kecepatan-tekanan untuk meningkatkan kecepatan-tekanan gas. Gas masuk ke sebuah impeler yang berputar melalui “mata” (eye). Vanes (daun impeler) mendorong gas ke sisi luar, melemparkan gas melalui jalur tertentu pada kecepatan tinggi. Gasnya dilemparkan ke jalur “diffuser” dan “volute” yang berada di sekitar impeler, yang relatif memiliki volume besar,
menjadi energi tekanan, sehingga tekanannya meningkat.
Karakteristik kompresor sentrifugal secara umum sebagai berikut : - Aliran discharge uniform.
- Kapasitas tersedia dari kecil sampai besar.
- Tekanan discharge dipengaruhi oleh density gas/udara.
- Mampu memberikan unjuk kerja pada efisiensi yang tinggi dengan beroperasi pada range tekanan dan kapasitas yang besar. Kompresor terdiri dari beberapa bagian yang fungsinya satu dengan yang lain saling berhubungan, diantaranya adalah :
• Bagian Statis 1. Casing
Casing merupakan bagian paling luar kompresor yang berfungsi : - Sebagai pelindung terhadap pengaruh mekanik dari luar.
- Sebagai pelindung dan penumpu/pendukung dari bagian-bagian yang bergerak.
- Sebagai tempat kedudukan nozel suction dan discharge serta bagian diam lainnya.
2. Inlet Wall
Inlet wall adalah diafram (dinding penyekat) yang dipasang pada sisi suction sebagai inlet channel dan berhubungan dengan inlet nozle. Karena berfungsi sebagai saluran gas masuk pada stage pertama, maka meterialnya harus tahan terhadap abrasive dan erosi.
3. Guide Vane
Guide vane di tempatkan pada bagian depan eye impeller pertama pada bagian suction (inlet channel). Fungsi utama guide vane adalah
yang merata.
Konstruksi vane ada yang fixed dan ada yang dapat di atur (movable) posisi sudutnya dengan tujuan agar operasi kompresor dapat bervariasi dan dicapai effisiensi dan stabilitas yang tinggi.
4. Eye Seal
Eye seal ditempatkan di sekeliling bagian luar eye impeller dan di tumpu oleh inlet wall. Eye seal selalu berbentuk satu set ring logam yang mengelilingi wearing ring impeller. Berfungsi untuk mencegah aliran balik dari gas yang keluar dari discharge impeller (tekanan tinggi) kembali masuk ke sisi suction (tekanan rendah).
5. Diffuser
Diffuser berfungsi untuk merubah energi kecepatan yang keluar dari discharge impeller menjadi energi potensial (dinamis).
Untuk multi stage dipasang diantara inter stage impeller. 6. Labirinth Seal
Labirinth seal digunakan untuk menyekat pada daerah : - Shaft dan diafragma sebagai shaft seal.
- Casing dan shaft sebagai casing seal. 7. Return Bend
Return bend sering juga disebut crossover yang berfungsi membelokan arah aliran gas dari diffuser ke return channel untuk masuk pada stage/impeller berikutnya. Return bend di bentuk oleh susunan diafragma yang dipasang dalam casing.
gas dari return bend masuk ke dalam impeller berikutnya. Return channel ada yang dilengkapi dengan fixed vane dengan tujuan memperkecil swirl (olakan aliran gas) pada saat masuk stage berikutnya sehingga dapat memperkecil vibrasi.
9. Diafragma
Diafram adalah komponen bagian dalam kompresor yang berfungsi sebagai penyekat antar stage dan tempat kedudukan eye seal maupun inter stage seal.
Dengan pemasangan diafragma secara seri, akan terbentuk tiga bagian penting, yaitu diffuser, return bend, dan return channel. Diafragma ditempatkan didalam casing dengan hubungan tongue-groove sehingga mudah dibongkar pasang.
• Bagian Dinamis 1. Shaft and Shaft Sleeve
Shaft atau poros transmisi digunakan untuk mendukung impeller dan meneruskan daya dari pengerak ke impeller. Untuk penempatan impeller pada shaft di gunakan pasak (key) dan pada multi stage, posisi pasak di buat selang-seling agar seimbang.
Sedangkan jarak antar stage dari impeller di gunakan shaft sleeve, yang berfungsi sebagai pelindung shaft terhadap pengaruh korosi, erosi dan abrasi dari aliran dan sifat gas dan untuk penempatan shaft seal diantara stage impeller.
2. Impeller
Impeller berfungsi untuk menaikan kecepatan gas dengan cara berputar, sehingga menimbulkan gaya. Hal ini menyebabkan gas
adanya perubahan jari-jari dari sumbu putar antara tip sudu masuk dengan tip sudu keluar maka terjadi kenaikan energi kecepatan.
3. Bantalan (Bearing)
Bearing adalah bagian internal kompresor yang berfungsi untuk mendukung beban radial dan aksial yang berputar dengan tujuan memperkecil gesekan dan mencegah kerusakan pada komponen lainnya. Pada kompresor sentrifugal terdapat dua jenis bearing, yaitu :
- Journal bearing
Digunakan untuk mendukung beban dengan arah radial (tegak lurus poros).
- Thrust bearing
Digunakan untuk mendukung beban ke arah aksial (sejajar poros).
4. Oil Film Seal
Oil film seal merupakan salah satu jenis seal yang digunakan dalam kompresor. Oil film seal terdiri dari satu atau dua seal ring. Pada seal jenis ini diinjeksikan minyak (oil) sebagai penyekat/perapat (seal oil) antara kedua seal ring yang memiliki clearence sangat kecil terhadap shaft. Tekanan masuk seal oil dikontrol secara proporsional berdasarkan perbedaan tekanan sekitar 5 psi diatas tekanan internal gas dan perbedaan tekanan oil-gas selalu dipertahankan.
Sehubungan dengan kondisi operasi yang tidak selalu konstan, maka untuk mempertahankan perbedaan tekanan antar seal oil dan gas dapat sesuai dengan kondisi operasi, digunakan overhead tank.
Sistem overhead tank adalah memasang tanki penampung seal oil dengan ketinggian tertentu diatas kompresor dan level seal oil dalam tanki dikontrol melalui level control operated valve, kemudian tekanan
memberikan tekanan pada permukaan seal oil.
Dengan sistem overhead tank, maka head static seal oil secara otomatis dapat menyesuaikan dengan kondisi operasi kompresor, sehingga perbedaan tekanan oil-gas proses dapat dipertahankan konstan.
Dalam perhitungan, digunakan asumsi isentropik dimana proses kompresi ideal dengan entalpi tetap (dQ=0), atau adiabatis. Effisiensi politropik, biasa disebut effisiensi tingkat kecil, yang sering digunakan karena effisiensi untuk kompresor secara keseluruhan sama dengan effisiensi untuk setiap tingkat yang digunakan. Effisiensi politropik yaitu effisiensi isentropik dari sebuah tingkat kompresor atau turbin yang dibuat konstan untuk setiap tingkat berikutnya dalam keseluruhan proses. Efisiensi isentropik setiap tingkat dapat dibuat sama dengan merancang sudu yang serupa.
VI.1.5 Landasan Teori
Dalam menghitung efisiensi kinerja kompresor digunakan asumsi politropik, tahap – tahap yang dapat dilakukan antara lain :
1. Penentuan komposisi gas masuk 2. Mencari data properties gas masuk 3. Perhitungan gas properties campuran
4. Mencari panas jenis spesifik dan specific gravity
a. Panas jenis spesifik (specifik heat ratio) dapat dicari dengan menggunakan persamaan :
dimana :
campuran.
b. Specific gravity dapat dicari dengan dua persamaan :
5. Mencari fakor kompressibilitas (Z) design dan aktual
Sehingga didapat hubungan Tr1 dan Pr1 untuk diplot kedalam grafik (compressibility chart) Z1
Tr2 dan Pr2 diplot kedalam grafik (compressibility chart) Z2
6. Menghitung besaran eksponen politropik (n) design dan aktual
7. Menghitung head politropik design dan aktual
8. Menghitung efisiensi politropik design dan aktual Efisiensi politropik dapat diketahui dengan persamaan :
Hubungan antara harga head dan efisiensi politropik menunjukan head aktual politropik, hal ini dapat dilihat dari persamaan berikut :
9. Menghitung daya kompresor design dan aktual a. daya gas (aerodynamic)
b. daya kompresor 10. Menghitung efisiensi η= VI.1.6 Perhitungan 1) Data Desain Kapasitas : 117374 Nm3/hr
Kompresor yang di evaluasi merupakan kompresor sentrifugal 4 stage dengan masing-masing stage memiliki sistem intercooler
dianggap seri menjadi 4 kompresor.
Kompresor 1
Kondisi masuk Suction LP :
Tekanan (P1) : 1.46 kg/cm2 = 20.7 Psia
Temperatur (T1) : 420C = 567.27 R
Kondisi keluar ke intercooler 2 :
Tekanan (P1*) : 7.88 kg/cm2= 112.08 Psia
Temperatur (T1*) : 210.2 0C = 870 R
Kompresor 2
Kondisi masuk dari intercooler 2:
Tekanan (P2) : 7.38 kg/cm2= 104.96 Psia
Temperatur (T2) : 42 0C = 567.27 R
Kondisi keluar ke intercooler 3 :
Tekanan (P2*) : 27.87 kg/cm2 = 396.4 Psia
Temperatur (T2*) : 187.40C = 829 R
Kompresor 3
Kondisi masuk dari intercooler 3 :
Tekanan (P3) : 27.21 kg/cm2 = 387.01 Psia
Temperatur (T3) : 420C = 567.27 R
Kondisi keluar ke intercooler 4 :
Tekanan (P3*) : 84.53 kg/cm2= 1202.3Psia
Temperatur (T3*) : 155.8 0C = 772.1 R
Kompresor 4
Kondisi masuk dari intercooler 4 :
Tekanan (P4) : 83.66 kg/cm2 = 1190 Psia
Temperatur (T4) : 550C = 590.67 R
2) Data Kondisi Operasi
Kapasitas : 94919.78 Nm3/hr
Kompresor 1
Kondisi masuk Suction LP :
Tekanan (P1) : 0.6 kg/cm2 = 8.53 Psia Temperatur (T1) : 42°C = 567.27 R Kondisi keluar ke intercooler 2 :
Tekanan (P1*) : 7.7 kg/cm2= 109.5 Psia Temperatur (T1*) : 215.86 °C = 880.2 R Kompresor 2
Kondisi masuk dari intercooler 2:
Tekanan (P2) : 7 kg/cm2= 99.56 Psia Temperatur (T2) : 42 °C = 565.47 R Kondisi keluar ke intercooler 3 :
Tekanan (P2*) : 29 kg/cm2 = 412.5Psia Temperatur (T2*) : 197.34°C = 846.8 R Kompresor 3
Kondisi masuk dari intercooler 3 :
Tekanan (P3) : 28 kg/cm2 = 398.25 Psia Temperatur (T3) : 42°C = 565.47 R
Kondisi keluar ke intercooler 4 :
Tekanan (P3*) : 85 kg/cm2= 1209 Psia Temperatur (T3*) : 146.71 °C = 755.7 R Kompresor 4
Kondisi masuk dari intercooler 4 :
Tekanan (P4) : 84 kg/cm2 = 1194.76 Psia Temperatur (T4) : 52.95°C = 587 R
Kondisi keluar Discharge HP :
Tekanan (P4*) : 165 kg/cm2= 2346.85 Psia Temperatur (T4*) : 121.08 °C = 709.6 R 3) Perhitungan Kompresor
1. Komposisi Gas
Tabel 6.1. Data Komposisi Gas Masuk Kompresor GB 151-J Suction LP
KOMPOSISI SIMBOL Data Komposisi Nitrogen N2 0 Hidrogen H2 1.6 Oxygen O2 0.4 Carbon dioxyde CO2 98
Water Vapor H2O SAT
Jumlah 100
Tabel 6.2. Data Komposisi Gas Masuk Kompresor GB 151-J intercooler
KOMPOSISI SIMBOL Data Komposisi Nitrogen N2 0.5 Hidrogen H2 1.56 Oxygen O2 2.26 Carbon dioxyde CO2 95.68
Water Vapor H2O SAT
Jumlah 100
2. Perhitungan Gas Propertis Campuran a. Kondisi 1
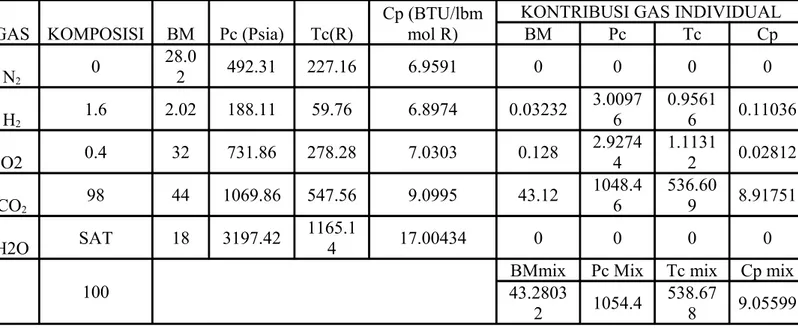
Hasil perhitungan gas propertis campuran dapat dilihat dalam tabel 3. Dimana dari perhitungan tersebut didapat harga gas propertis campuran sebagai berikut :
BM mix = 43.2803 Pc mix = 1054.4 Psia Tc mix = 538.678 oR
Cp mix = 9.05599 BTU/lbm.mol. oR
GAS KOMPOSISI BM Pc (Psia) Tc(R) mol R) BM Pc Tc Cp N2 0 28.0 2 492.31 227.16 6.9591 0 0 0 0 H2 1.6 2.02 188.11 59.76 6.8974 0.03232 3.0097 6 0.9561 6 0.11036 O2 0.4 32 731.86 278.28 7.0303 0.128 2.9274 4 1.1131 2 0.02812 CO2 98 44 1069.86 547.56 9.0995 43.12 1048.4 6 536.60 9 8.91751 H2O SAT 18 3197.42 1165.1 4 17.00434 0 0 0 0 100
BMmix Pc Mix Tc mix Cp mix 43.2803
2 1054.4
538.67
8 9.05599
b. Kondisi 2
Hasil perhitungan gas propertis campuran dapat dilihat dalam tabel 4. Dimana dari perhitungan tersebut didapat harga gas propertis campuran sebagai berikut :
BM mix = 42.4652 Pc mix = 1043.12 Psia Tc mix = 531.127 oR
Cp mix = 9.09343 BTU/lbm.mol. oR
3. Panas Jenis Spesifik dan Spesifik Gravity
a). Panas jenis spesifik
Panas jenis spesifik (specifik heat ratio) dapat dicari dengan menggunakan persamaan
dimana :
K : Panas jenis spesifik
Cp mix: Panas spesifik pada tekanan konstan, kondisi campuran.
b). Spesifik gravity
Sedangkan spesifik gravity dapat dicari dengan dua persamaan :
GAS KOMPOSISI BM (Psia)Pc Tc(R) Cp (BTU/lbm mol R) KONTRIBUSI GAS INDIVIDUAL
BM Pc Tc Cp N2 0.5 28.02 492.31 227.16 6.9611 0 0 0 0 H2 1.56 2.02 188.11 59.76 6.9115 0.031512 2.93452 0.93226 0.10782 O2 2.26 14.8 731.86 278.28 7.0456 0.33448 16.54 6.28913 0.15923 CO2 95.68 44 1069.86 547.56 9.2249 42.0992 1023.64 523.905 8.82638 H2O SAT 18 3197.42 1165.1 4 17.3772 0 0 0 0 100
BM Mix Pc Mix Tc Mix Cp Mix 42.46519
2 1043.12
531.12
4. Mencari Faktor Kompresibilitas (Z) Aktual a). Kompresor 1
- Kondisi masuk
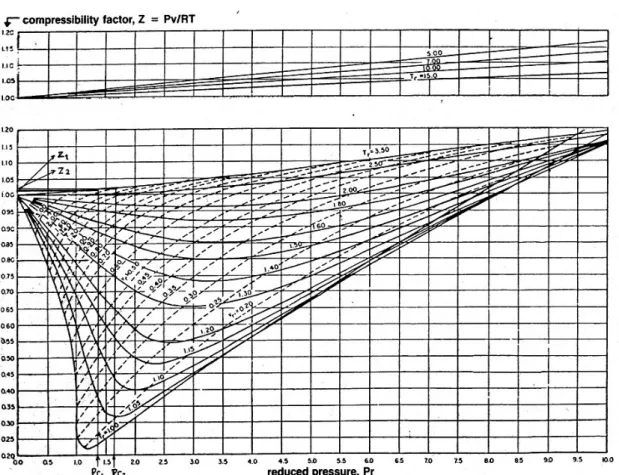
Dari hubungan Pr1 dan Tr1 pada gambar 1 didapat harga Z1 = 0.99 - Kondisi keluar
Dari hubungan Pr1* dan Tr1* pada gambar 1 didapat harga Z1* = 0.98 - Kondisi rata-rata.
b). Kompresor 2 - Kondisi masuk
Dari hubungan Pr2 dan Tr2 pada gambar 1 didapat harga Z2 = 0.98 - Kondisi keluar
Dari hubungan Pr2* dan Tr2* pada gambar 1 didapat harga Z2* = 0.97 - Kondisi rata-rata.
c). Kompresor 3 - Kondisi masuk
Dari hubungan Pr3 dan Tr3 pada gambar 1 didapat harga Z3 = 0.87 - Kondisi keluar
Dari hubungan Pr3* dan Tr3* pada gambar 1 didapat harga Z3* = 0.86 - Kondisi rata-rata.
d). Kompresor 4 - Kondisi masuk
Dari hubungan Pr4 dan Tr4 pada gambar 1 didapat harga Z4 = 0.68 - Kondisi keluar
Dari hubungan Pr4* dan Tr4* pada gambar 1 didapat harga Z4* = 0.73 - Kondisi rata-rata.
5. Mencari Faktor Kompresibilitas (Z) Desain a). Kompresor 1
- Kondisi masuk
Dari hubungan Pr1 dan Tr1 pada gambar 1 didapat harga Z1 = 0.98 - Kondisi keluar
Dari hubungan Pr1* dan Tr1* pada gambar 1 didapat harga Z1* = 1 - Kondisi rata-rata.
b). Kompresor 2 - Kondisi masuk
Dari hubungan Pr2 dan Tr2 pada gambar 1 didapat harga Z2 = 0.97 - Kondisi keluar
Dari hubungan Pr2 dan Tr2* pada gambar 1 didapat harga Z2* = 0.98 - Kondisi rata-rata.
c). Kompresor 3 - Kondisi masuk
Dari hubungan Pr3 dan Tr3 pada gambar 1 didapat harga Z3 = 0.94 - Kondisi keluar
Dari hubungan Pr3* dan Tr3* pada gambar 1 didapat harga Z3* = 0.85 - Kondisi rata-rata.
d). Kompresor 4 - Kondisi masuk
Dari hubungan Pr4 dan Tr4 pada gambar 1 didapat harga Z4 = 0.6 - Kondisi keluar
Dari hubungan Pr4* dan Tr4* pada gambar 1 didapat harga Z4* = 0. 74 - Kondisi rata-rata.
Gambar 6.2. Faktor Kompresibilitas Chart
d). Mencari harga Cp aktual - Kompresor 1
Dapat digunakan persamaan :
- Kompresor 2
Dapat digunakan persamaan :
- Kompresor 3
- Kompresor 4
Dapat digunakan persamaan :
6. Eksponen Politropik Aktual
Besarnya eksponen politropik (n) Aktual dapat dihitung dengan persamaan : - Kompresor 1 - Kompresor 2 .4 - Kompresor 3 n - Kompresor 4
7. Eksponen Politropik Desain
Besarnya eksponen politropik (n) Desain dapat dihitung dengan persamaan : - Kompresor 1
- Kompresor 2
- Kompresor 3
- Kompresor 4
8. Menghitung Head Aktual
Karena head yang dihitung adalah head dalam kondisi aktual, maka
persamaan yang digunakan menggunakan asumsi politropik, dengan rumus : - Kompresor 1 ] ;ft ] - Kompresor 2 ] ;ft ]
- Kompresor 3 ] ;ft ] - Kompresor 4 ] ;ft ] 9. Menghitung Head Desain
Karena head yang dihitung adalah head dalam kondisi desain, maka persamaan yang digunakan menggunakan asumsi politropik, dengan rumus: - Kompresor 1 ] ;ft ] - Kompresor 2 ] ;ft ] - Kompresor 3 ] ;ft ] - Kompresor 4 ] ;ft ] 10. Efisiensi Aktual
Efisiensi adalah perbandingan antara kerja sesungguhnya dengan kerja desain (teoritis). Efisiensi politropik dapat diketahui dengan persamaan : - Kompresor 1
- Kompresor 2
- Kompresor 3
- Kompresor 4
Hubungan antara harga head dan efisiensi politropik menunjukan head aktual politropik, hal ini dapat dilihat dari persamaan berikut :
11. Efisiensi Desain
Efisiensi adalah perbandingan antara kerja sesungguhnya dengan kerja desain (teoritis). Efisiensi politropik dapat diketahui dengan persamaan : - Kompresor 1
- Kompresor 2
- Kompresor 4
Hubungan antara harga head dan efisiensi politropik menunjukan head aktual politropik, hal ini dapat dilihat dari persamaan berikut :
12. Kapasitas Kompresor
b). Kapasitas operasi :
c). Dalam weight flow :
13. Daya Kompresor Aktual
b).Daya Kompresor
Daya kompresor merupakan perbandingan antara daya gas dengan
efisiensi mekanis. Di mana untuk kompresor sentrifugal kehilangan daya karena mekanis sekitar 3 %. Sehingga, daya kompresor menjadi :
14. Daya kompresor Desain
b).Daya Kompresor
Daya kompresor merupakan perbandingan antara daya gas dengan
efisiensi mekanis. Di mana untuk kompresor sentrifugal kehilangan daya karena mekanis sekitar 3 %. Sehingga, daya kompresor menjadi :
15. Efisiensi Overall Compressor 151-J η=
VI.1.7 Kesimpulan
Kompresor berfungsi untuk menaikkan tekanan fluida yang pada kasus ini fluida yang digunakan adalah gas carbon dioxyde CO2. Kompresor GB 151
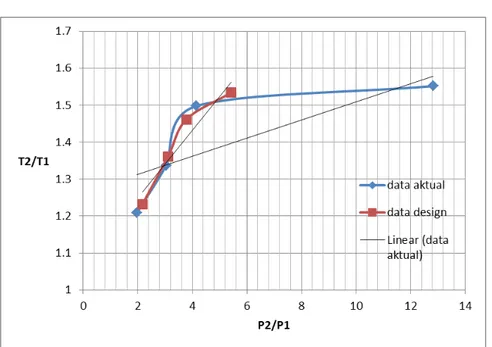
Gambar 6.3. Hubungan Antar Kompresi Politropik dan Suhu Alasan penggunaan sistem intercooler ini adalah karena selama proses kompresi berlangsung, temperatur meningkat. Peristiwa ini dikenal dengan kompresi politropik. Grafik 6.3. menunjukkan bahwa besarnya daya kompresi juga menigkat bila temperatur meningkat. Kompresor dibuat bertingkat dengan demikian mengurangi kenaikan temperatur dan meningkatkan efisiensi kompresi. Temperatur gas yang meninggalkan setiap stage didinginkan sebelum memasuki stage berikutnya.
Dari segi sistem intercooler, bisa disimpulkan pendingin antara yang sempurna dicapai bila temperatur gas meninggalkan pendingin antara adalah identik dengan temperatur gas memasuki kompresor. Konsumsi daya kompresor minimum dapat dicapai dengan pendinginan antara yang sempurna dan rasio tekanan pada semua tingkat adalah sama. Namun pendinginan antara yang sempurna sukar untuk dicapai di dalam praktek real-nya karena biaya penukar kalor air pendingin yang menjadi penghalang. Sedangkan untuk jumlah tingkat kompresor yang paling efisien adalah ditentukan oleh tekanan operasi aktual dan efisiensi kompresor yang diinginkan.
Berdasarkan hasil perhitungan (data rekapitulasi) dan kondisi mekanik terhadap evaluasi unjuk kerja kompresor sentrifugal GB 151 dapat
rendah dari desain sehingga kapasitas operasi lebih kecil dari desain, menyebabkan efisiensi secara keseluruhan di HP Case Compressor ini sebesar 80.85 %. Efisiensi yang masih dapat dikatakan tergolong baik karena dilakukan Turn Around pada tahun 2011, pada saat itulah biasanya dilakukan pengukuran-pengukuran clearance, penggantian suku cadang maupun rekondisi aparat sehingga mempengaruhi kinerja dari kompresor dari kinerja semula. Kondisi kompresor secara mekanik dalam kondisi baik dan tidak mengalami gangguan yang berarti. Pelaksanaan pemeliharaan selama ini tidak terjadi penyimpangan dari schedule yang ditetapkan.
VI.1.8 Saran
Operasi kompresor secara efisien masih memerlukan hal-hal yang penting dan harus dijaga, misalnya kandungan pengotor seperti padatan-padatan yang terkandung dalam gas dijaga seminimal mungkin sehingga kualitas dari kemurnian CO2 dalam arus masuk tetap terjaga. Selain itu perlu
adanya pengecekan pada pipa – pipa yang korosi karena dapat menyebabkan Ferro terbawa aliran. Adanya pengotor dapat mengganggu operasi compressor menjadi tidak balance dan akan menaikkan getaran (Vibration) terhadap kompresor.
Untuk menjaga unjuk kerja kompresor dapat dipertahankan sehingga target operasi terpenuhi, disarankan :
1. Parameter yang berpengaruh terhadap unjuk kerja dikembalikan sesuai kondisi desain sehingga kompresor bekerja pada efisiensi terbaik.
2. Meningkatkan preventive maintenance yang lebih baik dan terintegrasi serta penyediaan suku cadang pada bagian-bagian kompresor yang kritis.
seperti pressure gauge, temperatur gauge, flow indicator, dan yang lainnya agar parameter-parameter yang ditunjukan oleh indikator tersebut benar-benar mempresentasikan kondisi kompresor yang sebenarnya, sehingga dapat menghindari kekeliruan dalam setiap tindakan operasi yang dilakukan.
4. Pemeriksaan berkala (over haul) yang telah dilakukan hingga saat ini agar tetap dilaksanakan secara konsisten pada masa-masa yang akan dating. Karena hasil pemeriksaan berkala yang telah dilakukan terbukti dapat mencegah kerusakan besar yang mungkin akan terjadi.
Untuk mencegah gangguan operasi terhadap kompresor hal-hal sebagai berikut harus mendapatkan perhatian khusus :
1. Usahakan aliran kick back 0 agar kinerja kompresor tetap stabil.
2. Kualitas CO2 masuk kompresor diperhatikan secara teratur,
dengan melihat analyzer secara kontinyu.
3. Usahakan suhu CO2 masuk kompresor tidak terlalu jauh
dari suhu masuk design, karena dapat memperberat kerja dari sistem intercooler dan memperpendek umur alat serta efisiensi kompresor tetap terjaga.
4. Perlu dilakukan control jumlah feed CO2 yang masuk agar
tidak melebihi kapasitas kompresor yang dapat memperpendek umur kompresor.
5. Design temperatur dari gas yang keluar selalu dijaga
6. Alat pengukur vibrasi harus sering sering dicek untuk menentukan level atau tingkatan getaran dari kompresor dan hasil pengamatan harus dicatat di log sheet.
Neraca Massa dan Neraca Panas Pabrik Urea &
Identifikasi Alat Boros Energi
VI.2.1 Latar Belakang
Urea adalah suatu senyawa organik yang terdiri dari unsur karbon, hidrogen, oksigen dan nitrogen dengan rumus CON2H4 atau (NH2)2CO. Urea
juga dikenal dengan nama carbamide yang terutama digunakan di kawasan Eropa. Nama lain yang juga sering dipakai adalah carbamide resin, isourea, carbonyl diamide dan carbonyldiamine. Senyawa ini adalah senyawa organik sintesis pertama yang berhasil dibuat dari senyawa anorganik. (wikipedia, 2007).
Urea merupakan pupuk nitrogen yang paling mudah dipakai. Zat ini mengandung nitrogen paling tinggi (46%) di antara semua pupuk padat. Urea mudah dibuat menjadi pelet atau granul (butiran) dan mudah diangkut dalam bentuk curah maupun dalam kantong dan tidak mengandung bahaya ledakan. Zat ini mudah larut di dalam air dan tidak mempunyai residu garam sesudah dipakai untuk tanaman. Kadang-kadang zat ini juga digunakan untuk pemberian makanan daun. Disamping penggunaannya sebagai pupuk, urea juga digunakan sebagai tambahan makanan protein untuk hewan pemamah biak, juga dalam produksi melamin, dalam pembuatan resin, plastik, adhesif, bahan pelapis, bahan anti ciut, tekstil, dan resin perpindahan ion. Bahan ini merupakan bahan antara dalam pembuatan ammonium sulfat, asam sulfanat, dan ftalosianina (Austin, 1997).
Pabrik Urea Pusri II merupakan pabrik tertua di Pupuk Sriwidjaja Palembang. Pabrik ini dibangun pada tahun 1972 dengan kapasitas produksi 380.000 ton urea/tahun.. Saat ini pabrik urea pusri II hanya mampu memproduksi urea sebesar 1540.3 ton/hari. Hal tersebut terjadi karena umur dari alat-alat di pabrik urea pusri II yang sudah tua sehingga kinerjanya tidak dapat lagi maksimal. Selain karena umur alat yang sudah tua, banyaknya pipa-pipa steam yang bocor menjadi penyebab banyaknya energi yang hilang sehingga
merupakan pabrik yang mengonsumsi energi yang besar sekali. Energi dalam berbagai macam bentuknya digunakan untuk berbagai keperluan mulai dari proses produksi, perkantoran hingga untuk keperluan perumahan. Dengan demikian, maka pada pabrik urea pusri II akan dikaji mengenai identifikasi alat-alat boros energi di pabrik pupuk urea pusri II.
Penyusunan neraca massa dan neraca panas tentunya akan membantu dalam identifikasi alat boros energi. Selain itu, dengan adanya perhitungan neraca massa dan neraca panas tentunya dapat dihitung efisiensi beberapa alat di pabrik urea pusri II.
VI.2.2 Tujuan
Tujuan penulisan tugas khusus ini adalah sebagai berikut :
1. Mengetahui prinsip pembuatan urea dengan meninjau segi kuantitatfinya dengan neraca massa.
2. Mengidentifikasi alat boros energi secara kuantitatif dengan neraca panas.
3. Mengevalusi nilai efisiensi masing-masing unit di pabrik urea pusri II.
VI.2.3 Metodologi
Metodologi yang digunakan dalam tugas khusus ini adalah : 1. Mempelajari prinsip-prinsip pembuatan urea.
2. Observasi lapangan, dilakukan di PT. Pupuk Sriwidjaja Palembang pada pabrik urea pusri II.
VI.2.4 Tinjauan Pustaka
• Sifat Fisik Urea
Urea mempunyai rumus senyawa NH2CONH2. Kegunaan utama dari urea
adalah sebagai pupuk. Kegunaan yang lainnya adalah sebagai resin, lem, dan pelarut. Dari rumus senyawa tersebut, maka urea dapat dikategorikan sebagai amida dari asam karbamat (NH2COOH), atau diamida dari asam karbonat
(CO(OH)2). Pada temperatur ruang, urea tidak berwarna, tidak berbau, dan tidak
berasa. Di dalam air, urea akan terhidrolisa menjadi ammonium karbamat NH2COONH4, yang selanjutnya akan terdekomposisi menjadi amonia dan CO2.
Sintesis urea pertama kali dilakukan dengan cara mereaksikan amonia dan asam sianat (Woehler, 1828). Sintesis urea ini adalah pertama kali suatu senyawa organik dibentuk dengan reaksi yang melibatkan senyawa anorganik. Pada saat ini, produksi urea komersial dilakukan dengan cara mereaksikan amonia dan karbondioksida pada tekanan dan temperatur tinggi untuk membentuk amonium karbamat. Reaksi ini juga diikuti oleh reaksi dehidrasi amonium karbamat menjadi urea. Kedua reaksi ini terjadi secara seri, dan dapat dituliskan dengan persamaan reaksi berikut :
CO2 + 2NH3 NH2COONH4 ; ∆H190°C=-155kJ/mol
(karbamat)
Reaksi antara amonia dan karbondioksida merupakan reaksi yang bersifat eksotermis, sedangkan reaksi dehidrasi karbamat merupakan reaksi yang bersifat endotermis. Secara keseluruhan kedua reaksi tersebut di atas bersifat eksotermis, yang berarti dibutuhkan suplai energi panas demi berlangsungnya reaksi.
Sifat-sifat fisik dari urea dapat dilihat pada tabel 6.5., 6.6., 6.7., dan 6.8.
Tabel 6.5. Sifat fisik dan kimia urea secara umum
Titik leleh (oC) 132.7
Specific gravity pada 20oC 1.335
Bentuk kristal tetragonal
Energi pembentukan pada 25oC (cal/g.mol) -47.12
Panas pelarutan dalam air (cal/g) 58
Bulk density (g/cm3) 0.74
Panas pengkristalan (kJ/kg) 196.648
Tabel 6.6. Panas spesifik urea
Temperatur (oC) Panas spesifik (cal/g.oC)
0 0.344
50 0.397
100 0.451
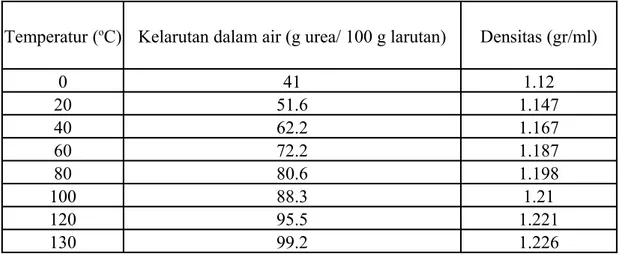
Tabel 6.7. Sifat fisik larutan urea jenuh pada setiap temperatur
Temperatur (oC) Kelarutan dalam air (g urea/ 100 g larutan) Densitas (gr/ml)
0 41 1.12 20 51.6 1.147 40 62.2 1.167 60 72.2 1.187 80 80.6 1.198 100 88.3 1.21 120 95.5 1.221 130 99.2 1.226
Tabel 6.8. Sifat fisik larutan urea jenuh pada amonia
Temperatur (oC)
Komposisi urea dalam larutan (% - w)
Tekanan uap larutan (atm) 0 36 5 20 49 7 40 68 9.4 60 79 10.8 80 84 13.3 100 90 12.5 120 96 5
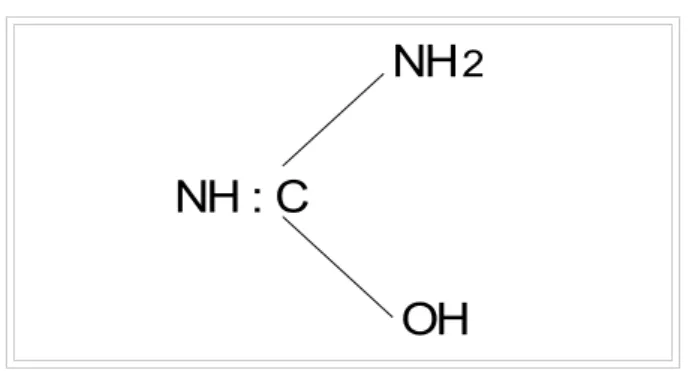
ditunjukkan pada struktur senyawa urea yang mengandung gugus -OH seperti dapat dilihat pada gambar di bawah ini :
NH : C
NH
2OH
Gambar 6.4. Struktur senyawa urea
Pada tekanan atmosferik, urea akan terdekomposisi menjadi amonia, karbondioksida, dan biuret, HN(CONH2). Senyawa biuret merupakan senyawa
yang paling tidak dikehendaki terdapat dalam campuran produk. Kandungan senyawa biuret melebihi 2 % berat akan membawa dampak negatif bagi pertumbuhan tanaman.
Urea dapat bereaksi dengan asam nitrat memebentuk urea nitrat, CO(NH2)2.HNO3, yang memiliki sifat mudah meledak bila dipanaskan. Urea padat
akan stabil pada temperatur dan tekanan ruang. Larutan urea akan terhidrolisis menjadi karbamat pada temperatur ruang. Urea juga akan mengalami dekomposisi menjadi biuret dan amonia bila mengalami pemanasan yang terlalu lama. Reaksi pembentukan biuret dapat ditulis dengan persamaan berikut ini :
2NH2CONH2 NH2CONHCONH2 + NH3
waktu pemanasan yang lama. Pada tekanan 100 – 200 atm, biuret akan bereaksi balik menjadi urea dengan kehadiran amonia.
Urea pertama akan bereaksi dengan perak nitrat (AgNO3), dan akan
membentuk senyawa turunan perak dengan rumus molekul CON2H2Ag, yang
berwarna kuning pucat. Dengan kehadiran natrium bromida (NaBr) dan natrium hidroksida, urea akan bereaksi menghasilkan nitrogen dan karbondioksida. Reaksi yang berlangsung dapat dituliskan dengan persamaan :
NH2CONH2 + 3 NaBr + 2NaOH N2 + 3NaBr + Na2CO3 + 3H2O
Reaksi antara urea dan alkohol akan menghasilkan ester dari asam karbamat, yang biasa dikenal dengan sebutan urethan. Reaksi yang berlangsung dapat dituliskan dengan persamaan :
NH2CONH2 + ROH NH2COOR + NH3
Urea akan bereaksi dengan formaldehid dan akan membentuk senyawa monometilurea, NH2CONHCH2OH, dimetilurea, atau senyawa lainnya tergantung
dari rasio molar formaldehid terhadap urea dan kondisi PH dari larutan. Urea juga akan bereaksi dengan hidrogen peroksida membentuk senyawa CO(NH2)2H2O2,
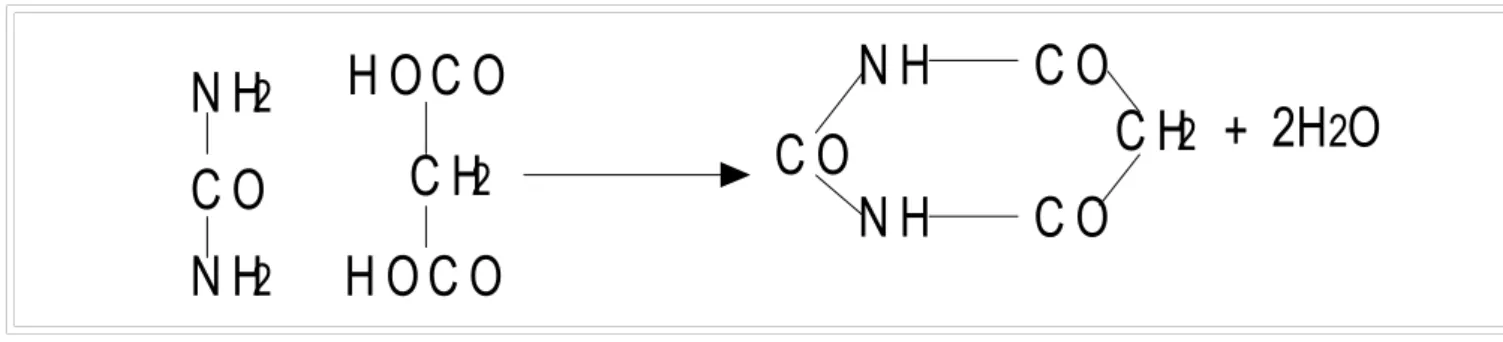
obatan merupakan senyawa yang disintesis dari urea dan asam malonat, menghasilkkan asam barbiturat. Reaksi dari pembentukan asam barbiturat tersebut dapat dituliskan dengan persamaan di bawah ini :
N H
2
C O
N H
2
H O C O
C H
2
H O C O
C O
N H
C O
N H
C O
C H
2
+ 2H
2
O
Gambar 6.5. Reaksi Pembentukan Senyawa Asam barbiturate
• Reaksi Sintesis Urea
Sintesis urea pertama kali dilakukan dengan cara mereaksikan amonia dan asam sianat (Woehler, 1828). Sintesis urea ini adalah pertama kali suatu senyawa organik dibentuk dengan reaksi yang melibatkan senyawa anorganik. Pada saat ini, produksi urea komersial dilakukan dengan cara mereaksikan amonia dan karbondioksida pada tekanan dan temperatur tinggi untuk membentuk amonium karbamat. Reaksi ini juga diikuti oleh reaksi dehidrasi amonium karbamat menjadi urea. Kedua reaksi ini terjadi secara seri, dan dapat dituliskan dengan persamaan reaksi berikut :
NH2COONH4 NH2CONH2 + H2O; ∆H180°C = 42kJ/mol
(urea)
Reaksi antara amonia dan karbondioksida merupakan reaksi yang bersifat eksotermis, sedangkan reaksi dehidrasi karbamat merupakan reaksi yang bersifat endotermis. Secara keseluruhan kedua reaksi tersebut di atas bersifat eksotermis, yang berarti dibutuhkan suplai energi panas demi berlangsungnya reaksi. Reaksi pembentukan urea juga merupakan reaksi kesetimbangan. Nilai konstanta kesetimbangan (K) pada berbagai temperatur dapat dilihat pada tabel 6.9.
Tabel 6.9. Konstanta kesetimbangan reaksi sintesis urea pada berbagai temperatur
T (oC) K
100 2.32
150 2.08
200 1.86
250 1.721
Reaksi sintesis urea merupakan reaksi yang berorde satu. Dengan demikian maka persamaan kinetik dari reaksi sintesis urea dapat dinyatakan dengan persamaan : m n CCO CNH k dt dCurea ) 2 ( ) ( 3 =
C urea = konsentrasi urea yang terbentuk K = konstanta kinetika reaksi
CCO2 = konsentrasi karbondioksida
n, m = orde reaksi dimana n + m =1
Sedangkan konstanta kinetika reaksi pada berbagai temperatur dapat dilihat pada tabel 6.10.
Tabel 6.10. Konstanta kinetika reaksi pembentukan urea pada berbagai temperatur T (oC) kx105 (s-1) 100 2.93 150 1.98 200 0.89 250 0.62
(Sumber : Wahlco Brocure, 1983)
Reaksi sintesis urea merupakan reaksi non-katalitik. Untuk melaksanakan reakasi ini diperlukan tekanan dan temperatur yang tinggi. Temperatur tinggi disini berfungsi untuk mempercepat laju reaksi, sedangkan tekanan yang tinggi dibutuhkan untuk menggeser konversi kesetimbangan ke arah produk, karena reaksi ini melibatkan peningkatan jumlah mol.
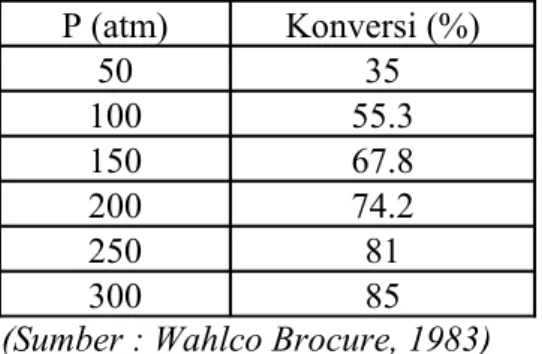
Konversi urea pada berbagai temperatur dapat dilihat pada tabel 6.11. Sedangkan konversi urea pada berbagai tekanan dapat dilihat pada tabel 6.12.. Tabel 6.11. Konversi urea pada berbagai temperatur
T (oC) Konversi (%)
150 82
200 66. 5
450 43
500 38
(Sumber : Wahlco Brocure, 1983)
Tabel 6.12. Konversi urea pada berbagai tekanan P (atm) Konversi (%) 50 35 100 55.3 150 67.8 200 74.2 250 81 300 85
(Sumber : Wahlco Brocure, 1983)
Karena reaksi sintesis urea merupakan reaksi yang bersifat eksotermik, maka diperlukan temperatur serendah mungkin untuk mencapai konversi reaksi yang tinggi. Akan tetapi bila reaksi dilaksanakan pada temperatur rendah, hal ini akan mengakibatkan laju reaksi yang rendah. Untuk mengatasi hal ini, maka diperlukan optimasi temperatur agar laju reaksi dapat berlangsung cepat dengan tingkat konversi yang tinggi. Selain itu tekanan tinggi juga diperlukan untuk mencapai tingkat konversi yang tinggi. Tekanan operasi yang dipilih hendaknya juga harus memperhatikan aspek keselamatan di pabrik. Temperatur operasi reaktor sintesis urea di PT Pupuk Sriwidjaja Palembang adalah sebesar 190-200°C, sedangakan tekanan operasi reaktor adalah sebesar 250 kg/cm2 –g ( 217,
88 atm-g).
VI.2.5 Landasan Teori 1) Neraca Massa
Karena tidak ada akumulasi atau diasumsikan steady state sehingga terbentuk persamaan neraca massa sebagai berikut :
[massa masuk]=[massa keluar]
Asumsi-asumsi yang digunakan dalam perhitungan neraca massa adalah :
a. Kondisi steady state (akumulasi = 0).
b. Tidak ada pengotor seperti padatan-padatan yang terikut di dalam sistem.
c. Massa yang keluar dari unit sintesa = Massa masuk unit purifikasi d. Tidak ada perubahan massa di fluidizing dryer pada unit finishing
karena perubahan massa dianggap sangat kecil sehingga dapat diabaikan.
e. Perhitungan dibatasi hanya sampai unit finishing karena setelah unit finishing dianggap hanya terdapat proses packaging dan perubahan massa tidak terlalu signifikan sehingga dapat diabaikan. Untuk perhitungan konversi (X) di reaktor urea secara empiris, dapat dituliskan sebagai berikut :
X = { 0,2616 (a) + 0,01945 (a)2 + 0,0382 (a) (b) – 0,1160 (b) – 0,02732 (a)
(t/100) – 0,1030 (b) (t/100) + 1,640 (t/100) – 0,1394 (t/100)3 – 1,869}.
100%
Dimana : a = Mol ratio NH3/CO2 total (a) b = Mol ratio H2O/CO2 total (b) t = Temperatur operasi (190°C-200°C) 2) Neraca Panas
[Energi masuk] – [energi keluar] + [energi yang terbangkitkan sistem] – [energi yang terkonsumsi sistem] = [energi terakumulasi dalam sistem] 1. Reaksi kimia yang bersifat eksotermis ( menghasilkan panas),
maka energi yang dihasilkan disebut sebagai energi yang terbangkitkan sistem.
2. Reaksi kimia yang bersifat endotermis (membutuhkan panas), maka energi yang dihasilkan disebut sebagai energi yang terkonsumsi oleh sistem.
3. Untuk sistem dengan proses steady state, maka energi yang terakumulasi = 0
Neraca panas / energi / tenaga :
a. NP total pada sistem alir ( flow sistem) pada keadaan steady state
Input= output
Persamaan di atas sering dipakai untuk kasus transportasi fluida, yaitu persamaan Bernoulli.
b. Neraca Energi untuk proses kimia ( non flow sistem ). Sistem non alir dianggap terjadi di dalam alat-alat proses, misal alat penukar panas (HE=heat exchanger), reaktor, dan alat-alat transfer massa lainnya.
Pada sistem ini, biasanya EP dan EK <<< Q dan W, sehingga EP dan EK dapat diabaikan dan
∆U + ∆PV = Q − W
∆H = ∆U + ∆PV = Q − W ∆H = Q − W
H2 – H1 = Q – W
Untuk beberapa proses, biasanya nilai W sangat kecil. Sehingga :
H2 – H1 = Q = ∆H
Dengan, H1 = entalpi arus masuk (titik satu), H2 = entalpi arus keluar (titik dua).
Macam-macam perubahan entalpi (panas):
1. Panas sensible (panas yang bisa dirasakan perubahan suhunya).
Kapasitas panas (cp ) = banyaknya panas yang dibutuhkan untuk menaikkan suhu setiap satuan massa setiap satuan suhu.
Untuk padatan dan gas, Cp merupakan fungsi suhu. Beberapa sumber data-data Cp :
a. Cp = f (T) ; appendix D, Coulson and Richardson, “ Chemical Engineering”. Table E.1. Himmelblau. b. Cp dalam bentuk grafik; Geankoplis; Perry.
c. Cp untuk foods and biological material; appendix A.4, Geankoplis,”Transport Processes and Unit Operation”.
2. Panas laten ( panas perubahan fase dengan suhu tetap). a. Panas peleburan (dari fase padat menjadi cair). b. Panas sublimasi (dari fase padat menjadi gas ). c. Panas kondensasi (dari fase gas menjadi cair). d.. Panas kristalisasi (dari fase cair menjadi padat). e. Panas penguapan (dari fase cair menjadi gas).
pada proses yang melibatkan reaksi kimia)
ΔHr bernilai positif menunjukkan reaksi membutuhkan panas
ΔHr bernilai negatif menunjukkan reaksi menghasilkan panas
Jika reaksi tidak dijalankan pada kondisi standar, maka dapat dilakukan :
a) Suhu umpan dibayangkan diturunkan atau dinaikkan sampai suhu standar, kemudian
b) Direaksikan pada kondisi standar
c) Suhu produk dinaikkan sampai suhu keluar d) Selanjutnya panas reaksi dihitung
VI.2.6 Perhitungan
Pra rancangan pabrik pembuatan Pupuk Urea Pusri II dari Gas Sintesis dilaksanakan untuk kapasitas produksi sebesar 1540.3 ton/hari, dengan ketentuan sebagai berikut:
1 hari kerja = 24 jam
Basis = 1 jam operasi
Maka kapasitas produksi Pupuk Urea tiap jam adalah: =
Bahan Baku dan Berat Molekul Bahan Baku yang digunakan (Wikipedia, 2007; Perry, 1999) :
− Nitrogen (N2) = 28 g/mol
− Hidrogen (H2) = 2 g/mol
− Ammonia (NH3) = 17 g/mol
Berat Molekul Urea = 60 kg/kmol
Kemurnian Urea yang dihasilkan = 99 % x 64183 kg/jam = 63541 kg/jam 1) Neraca Massa A. Unit Sintesa a. Reaktor Urea CO2 Feed Unit Sintesa NH3 Feed Out to purifikasi Recycle
Dengan Rate CO2 65.68% :
Data yang diperoleh dari lapangan pada tanggal 1 Februari 2012 - 29 Februari 2012 adalah sebagai berikut :
Aliran 1: CO2 = 11833.8 Kg/Jam (100%wt)
Aliran 2: NH3 = 24602 Kg/Jam (100%wt)
Aliran 3: UREA = 11892.837 Kg/Jam (18,11%wt) NH3 = 19044.3 Kg/Jam (29,0%wt)
CO2 = 17711.199 Kg/Jam (26,97%wt)
H2O = 16732.716 Kg/Jam (25,48%wt)
BIURET = 288.948 Kg/Jam (0,44%wt) Basis : 1 Jam Operasi
Komposisi Inlet Reaktor:
UREA = 11892.837 Kg = 198.21 Kmol NH3 Total = 24602 + 19044.3 = 42543.7 Kg = 2567.43 Kmol CO2 Total = 11833.8 + 17711.199 = 29544.99 Kg
H2O = 16732.716 Kg = 929.6 Kmol Biuret = 288.948 Kg = 2.8 Kmol *Mole Ratio : = 1.38 *Konversi CO2 menjadi Urea
X = {(0,2616 . 3.82)–(0,01945 .(3.82)2)+(0,0382 .(3.82).(1.38))-(0,1160 .
1.38))-(0,02732. (3.82).(190/100))-(0,1030.1.38)(190/100))+(1,640. (190/100))-(0,1394(190/100)3)- 1,869)} x 100%
= 55.8876 %
Untuk urea yang terbentuk karena reaksi dengan asumsi semua CO2 bereaksi
dengan NH3 membentuk karbamat dan karbamat terhitung dalam bentuk NH3 dan
CO2 maka :
Urea hasil reaksi = X . CO2 masuk reaktor
= 0,558876 . 671.477 = 375.27 Kmol/Jam CO2 yang bereaksi = 375.27 Kmol/Jam
NH3 yang bereaksi = 2 x 375.27
= 750.54 Kmol/Jam H2O hasil reaksi = 375.27 Kmol/Jam
*Menghitung aliran keluar dari reaktor :
CO2 keluar reaktor = CO2 masuk – CO2 bereaksi
= 671.477 – 375.27 = 296.2 Kmol/Jam H2O keluar reaktor = 375.27 + 929.6
Konversi biuret menjadi urea pada data design
= x 100 %
= 35,052% / jam x 1 jam/60 menit = 0,584% / menit
Biuret yang menjadi urea = 0,584% / menit x 25 menit (waktu tinggal) x 2.8 = 0,408
Urea yang terbentuk dari biuret = 2 x 0,408 = 0.8176
Total urea yang keluar reaktor = 375.27 + 198.21 + 0.8176 = 574.3 Kmol/Jam
Biuret yang keluar reaktor = biuret masuk – biuret yang menjadi urea = 2.8 – 0.8176
= 1.9824 Kmol/Jam
NH3 keluar reaktor = NH3 masuk + NH3 bereaksi dengan CO2 - NH3 bereaksi
dengan biuret
= 2567.43 – 750.54 – 0,408 = 1816.482 Kmol/Jam Tabel 6.13. Komposisi umpan masuk reaktor
Komponen Kg/Jam BM Kmol/Jam
CO2 11833.8 44 268.95
NH3 24602 17 1415.411
Tabel 6.14. Komposisi umpan masuk reaktor dari recycle
Komponen Kg/Jam BM Kmol/Jam
Urea 11892.837 60 198.21
H2O 16732.716 18 929.60
Biuret 288.948 103 2.81
Tabel 6.15. komposisi aliran keluar dari reaktor (DC-151)
Komponen BM Kmol/jam Kg/jam
Urea 60 574.3 34458 NH3 17 1816.482 30880.194 CO2 44 296.2 13032.8 H2O 18 1304.87 23487.66 Biuret 103 1.9824 204.1872 Total - 3993.8344 102,063
Tabel 6.16. Material Balance Reaktor Urea
KOMPOSISI (%)
INLET REAKTOR OUTLET REAKTOR
DC 151 DC 151 S-104 S-104 Kg/H % Kg/H % UREA 11892.837 11.77 34458 33.76 NH3 42543.7 42.12 30880.194 30.26 CO2 29544.99 29.25 13032.8 12.77 H2O 16732.716 16.57 23487.66 23.01 BIURET 288.948 0.29 204.1872 0.20 TOTAL 101003.19 1.00 102062.84 100
Dengan Rate CO2 100% : Komposisi Inlet Reaktor:
UREA = 5916 Kg
= 98.60 Kmol NH3 Total = 142996 Kg
CO2 Total = 88776 Kg = 2017.64 Kmol H2O = 27063 Kg = 1503.50 Kmol Biuret = 206 Kg = 2 Kmol *Mole Ratio : = 0.52 *Konversi CO2 menjadi Urea
X = {(0,2616 . )–(0,01945 .( )2)+(0,0382 .( ).( 0.52))-(0,1160 .
0.52))-(0,02732. ( ).(190/100))-(0,1030.0.52)(190/100))+(1,640. (190/100))-(0,1394(190/100)3)-1,869)} x 100%
= 73.48 %
Untuk urea yang terbentuk karena reaksi dengan asumsi semua CO2 bereaksi
dengan NH3 membentuk karbamat dan karbamat terhitung dalam bentuk NH3 dan
CO2 maka :
Urea hasil reaksi = X . CO2 masuk reaktor
= 0.7348 . 2017.64 = 1482.5 Kmol/Jam CO2 yang bereaksi = 1482.5 Kmol/Jam
NH3 yang bereaksi = 2 x 1482.5
= 2965 Kmol/Jam H2O hasil reaksi = 1482.5 Kmol/Jam
*Menghitung aliran keluar dari reaktor :
CO2 keluar reaktor = CO2 masuk – CO2 bereaksi
H2O keluar reaktor = 1482.5 + 1503.50
= 2986 Kmol/Jam
Konversi biuret menjadi urea pada data design = x 100 %
= 35,052% / jam x 1 jam/60 menit
= 0,584% / menit Biuret yang menjadi urea = 0,584% / menit x 25 menit (waktu tinggal) x 2
= 0,292
Urea yang terbentuk dari biuret = 2 x 0,292 = 0.584
Total urea yang keluar reaktor = 1482.5 + 98.60 + 0.584 = 1581.684 Kmol/Jam
Biuret yang keluar reaktor = biuret masuk – biuret yang menjadi urea = 2 – 0.584
= 1.416 Kmol/Jam
NH3 keluar reaktor = NH3 masuk + NH3 bereaksi dengan CO2 - NH3 bereaksi
dengan biuret
= 8411.53 – 2965 – 0,292 = 5446.238 Kmol/Jam
Tabel 6.17. Komposisi umpan masuk total reaktor (DC 151)
Komponen BM Kmol/jam Kg/jam
Urea 60 98.6 5916 NH3 17 8411.53 142996 CO2 44 2017.64 88776 H2O 18 1503.5 27063 Biuret 103 2.00 206 Total - 12033.26384 264,957
Tabel 6.18. Menghitung komposisi aliran keluar dari reaktor (DC-151)
CO2 44 535.14 23546.16
H2O 18 2751.72 49530.96
Biuret 103 1.416 145.85
Total - 10316.198 260,710
Tabel 6.19. Material Balance Reaktor Urea :
KOMPOSISI (%)
INLET REAKTOR OUTLET REAKTOR
DC 151 DC 151 S-104 S-104 Kg/H % Kg/H % UREA 5916 2.23 94901.04 36.40 NH3 142996 53.97 92586.046 35.51 CO2 88776 33.51 23546.16 9.03 H2O 27063 10.21 49530.96 19.00 BIURET 206 0.08 145.848 0.06 TOTAL 264957 100.00 260710.05 100.00 Efisiensi reaktor = = = 76 %
Dari perhitungan efisiensi reaktor didapatkan efisiensi sebesar 76%, hal ini disebakan karena rate CO2 aktual dan design cukup berbeda. Dalam kondisi actual
dan pembutiran karena umur alat yang sudah tua dan kinerjanya sudah jauh menurun dari semula sehingga perlu dilakukan penyesuaian, salah satunya adalah dengan pengurangan rate CO2 masuk.
Aliran keluar reaktor kemudian dialirkan melewati stripping dan carbamate condenser. Dari hasil pengambilan data lapangan, komposisi aliran keluar dari unit sintesis menuju unit purifikasi adalah sebagai berikut :
Tabel 6.20. Aliran Masuk Unit Purifikasi
Komponen BM Kmol/jam Kg/jam
Urea 60 1389 83358 NH3 17 5458 92780 CO2 44 666 29299 H2O 18 2752 49531 Biuret 103 2 180 Total - 10266 255148
Jumlah Urea dari reaktor menuju unit purifikasi berkurang dari 94901.04 kg/jam menjadi 83358 kg/jam, hal ini terjadi karena ada sebagian urea yang dikembalikan ke reaktor setelah melewati carbamate condenser dengan tujuan agar diperoleh konversi yang lebih tinggi.
a. High Pressure Decomposer (HPD)
HPD berfungsi untuk menguraikan sebanyak mungkin ammonium karbamat menjadi gas NH3 dan CO2 dan melepaskan kelebihan
NH3 dengan cara penurunan tekanan melalui pemanasan
menggunakan steam condensate. Hal yang harus diperhatikan adalah pembentukan biuret dan hydolisa urea pada temperatur tinggi dengan cara mengatur waktu tinggal sependek mungkin.
Tabel 6.21. Material Balance HPD KOMPOSISI
(%)
INLET HPD OUTLET HPD (TO
LPD) OUTLET HPD (TO HPA) HPD Inlet from Reaktor Out to HPA Out to LPA
Kg/H % Kg/H % Kg/H % UREA 83358 32.67 78428 64.31 0 0 NH3 92780 36.37 6945 5.69 21190 41.19 CO2 29299 11.48 4980 1.62 23225 45.14 H2O 49531 19.41 34252 28.08 7034 13.67 BIURET 180 0.07 370 0.3 0 0 TOTAL 255148 100 124975 100 51449 100
b. Low Pressure Decomposer (LPD)
LPD berfungsi untuk menguapkan ekses (kelebihan) NH3 dan menguraikan ammonium karbamat menjadi gas NH3 dan CO2 dengan cara penurunan tekanan dan pemanasan Falling Film Heater dan gas dari proses Condensate Stripper.
Tabel 6.22. Material Balance LPD
KOMPOSISI INLET LPD OUTLET LPD (TO OUTLET LPD (TO
LPD Inlet from bottom HPD Out to LPA Out to GS
(%) DA 202 DA 202 DA 202 Kg/H % Kg/H % Kg/H % UREA 78428 64.31 77707 68.36 77707 68.36 NH3 6945 5.69 1037 0.91 1037 0.91 CO2 4980 1.62 688 0.61 688 0.61 H2O 34252 28.08 33810 29.74 33810 29.74 BIURET 370 0.3 431 0.38 431 0.38 TOTAL 124975 100 113673 100 113673 100 c. Gas separator (GS)
Tabel 6.23. Material Balance GS KOMPOSISI
(%)
INLET GS OUTLET GS (TO
CONCENTRATOR) OUTLET GS (TO OGA) Gas Separator Inlet from botto m LPD Out to OGA Out to Crystallizer
Kg/H % Kg/H % Kg/H % UREA 77707 68.36 53482 71.34 0 0 NH3 1037 0.91 359 0.48 561 14.19 CO2 688 0.61 238 0.32 359 9.08 H2O 33810 29.74 20552 27.41 3033 76.73 BIURET 431 0.38 339 0.45 0 0 TOTAL 113673 100 74970 100 3953 100
C. Unit kristalisasi dan pembutiran
Urea dari Urea Solution Tank yang sudah bebas kandungan karbamat dikristalkan pada kondisi vacuum oleh Crystalizer. Kristal urea yang terjadi dipisahkan dari larutan induk (mother liquor) di Centrifuge. Kemudian kristal urea dikeringkan dan dihembuskan oleh udara panas ke Melter (dibuat lelehan) yang selanjutnya di prill-kan di Prilling Tower sambil didinginkan dengan udara kering.
a. Crystallizer
Merupakan tempat mengkristalkan larutan urea dengan cara divacuumkan, sehingga uap airnya menguap dan dikirim ke PCT. Larutan urea selanjutnya membentuk kristal dan turun ke bawah.
1. Vacuum Concentrator
Merupakan tempat menguapkan air dari larutan urea. 2. Crystallizer
Merupakan tempat mengkristalkan larutan urea yang turun dari vacuum concentrator, dimana kristal akan tumbuh menjadi besar karena adanya kontak dengan larutan urea yang supersaturated, sampai kandungan kristal ureanya 30-35% berat.
Asumsi massa masuk crystallizer = massa keluar crystallizer Tabel 6.24. Material Balance Crystallizer
KOMPOSISI (%)
INLET CRYSTALLIZER OUTLET CRYSTALLIZER
A B C D Kg/H % Kg/H % Kg/H % Kg/H % UREA 53482 71.34 957864 85.30 132670 84.43 878463 84.43 NH3 359 0.48 2392 0.21 358 0.23 2393 0.23 CO2 238 0.32 2168 0.19 326 0.2 2081 0.20 H2O 20552 27.41 137200 12.22 20719 13.17 137029 13.17 CRYSTALLIZER Inlet from bottom GS
Out to Centrifuge
Inlet from bottom Centrifuge
TOTAL 74970 100 1122886 100 157178 100 1040462 100
Dimana, A = Aliran masuk dari gas separator B = Aliran masuk dari dasar concentrator C = Keluar ke centrifuge
D = Keluar ke concentrator b. Centrifuge
Berfungsi memisahkan kristal urea dari larutan induk dengan bantuan prethickener FD-202. Lima unit prethickener dan centrifuge ini disiapkan untuk mendapatkan produk 100% dengan kadar air sekitar 1,9%. Larutan induk yang dipisahkan oleh prethickener dan centrifuge mengalir ke bawah dan ditampung di Mother Liquor Tank FA-203, dipanasi dengan steam melalui tube untuk menghindari kristalisasi.
Tabel 6.25. Material Balance Centrifuge
KOMPOSISI (%)
INLET CENTRIFUGE CENTRIFUGE (TO OUTLET FLUIDIZING DRYER)
OUTLET CENTRIFUGE (TO MOTHER LIQUOR
TANK)
GF 201 GF 201 GF 201
Kg/H % Kg/H % Kg/H %
UREA 132670 84.43 47927 97.78 84943 78.39
CENTRIFUGE Inlet from Crystallizer
Out to Fluidizing Dryer
CO2 326 0.2 0 0 326 0.3
H2O 20719 13.17 958 1.95 19761 18.24
BIURET 3105 1.97 133 0.27 2972 2.74
TOTAL 157178 100 49018 100 108360 100
c. Fluidizing Dryer
Berfungsi sebagai tempat mengeringkan kristal urea dengan bantuan udara panas sampai kandungan air < 0,2% dan mengalirkan kristal urea tersebut menuju cyclone. Udara panas dijaga pada temperatur 120°C dan tidak boleh melebihi 130°C (titik leleh urea dalah 132,7°C).
Asumsi yang digunakan adalah
Massa masuk Fluidizing Dryer = Massa keluar Fluidizing Dryer d. Screw Conveyor
Massa masuk Screw Conveyor = Massa keluar Fluidizing Dryer Tabel 6.26. Material Balance Screw Conveyor
KOMPOSISI (%)
INLET SCREW OUTLET SCREW
JD 301A/B JD 301A/B
Kg/H % Kg/H %
UREA 47927 97.78 47832 99.43
NH3 0 0 0 0
BIURET 133 0.27 132 0.27
TOTAL 49018 100 48107 100
e. Melter
Massa Masuk Melter = Massa keluar Screw Conveyor
Q steam Q condensat
Tabel 6.27. Material Balance Melter
KOMPOSISI (%)
INLET MELTER OUTLET MELTER
EA 301 EA 301 Kg/H % Kg/H % UREA 47832 99.43 63194 99.1 NH3 0 0 0 0 CO2 0 0 0 0 H2O 143 0.3 190 0.3 BIURET 132 0.27 382 0.6 TOTAL 48107 100 63766 100 MELTER Inlet from Scew Conveyor
Berfungsi sebagai tempat membutirkan urea dari melter dengan bantuan Distributor FJ-301 dan udara panas sebagai pendingin butiran urea. Urea prill dikumpulkan di Fluidizing Cooler FD-302 dan overflow ke Trommel FD-303. Produk urea dikirim ke Bulk Storage dengan Belt Conveyor.
Tabel 6.28. Material Balance Prilling Tower
KOMPOSISI (%)
INLET PRILLING OUTLET PRILLING
Kg/H % Kg/H % UREA 47382 99.43 62969 99.1 NH3 0 0 0 0.0 CO2 0 0 0 0.0 H2O 143 0.3 191 0.3 BIURET 132 0.27 381 0.6 TOTAL 47657 100 63541 100.0
Data yang diperoleh dari lapangan pada tanggal 1 Februari – 29 Februari 2012 adalah sebagai berikut :
Tabel 6.29. Data Suhu Masuk dan Suhu Keluar Alat di Pabrik Urea
ALAT DATA SUHU (°C)
Suhu Masuk Suhu Keluar Reaktor 176 (Recycle) 190 156 (CO2) 73 (NH3) Stripper 178 192 CC1 190 177 CC2 187 177 HPD 156 155 (To HPAC) 165 (to LPD) LPD 149 120 (to LPA) 122 (to GS) GS 117 117 (to OGA) 92 (to crystallizer)
HPAC 149 (gas in) 109 (gas out)
35 (cw in) 94 (cw out) Crystallizer 70 68 Centrifuge 68 68 Fluidizing Dryer 68 100 Melter 100 138 Prilling tower 138 43 1. Unit Sintesis a. Reaktor Kondisi umpan masuk
Temperatur : NH3 = 73 oC
CO2 = 156 oC
Tekanan pada reaktor = 165 Kg/cm2
Reaksi :
2 NH3 + CO2 NH4CO2NH2 ∆H1 = +36 Kkal/mol
NH2CO2NH4 NH2CONH2 + H2O ∆H2 = 7,7 Kkal/mol
NH2CONH2 NH2CONHCONH2 + NH3 ∆H3=+4,28 Kkal/mol
Qmasuk = Q CO2 + Q NH3 + Q recycle Q CO2 = m
∫
cp dT = 268.95 jam kmol . 1000 kmol gmol 1∫
123 25 (10,34 + 0,00274 T - 1955002 T ) dT = 268950 jam gmol∫
156 25 (10,34 T + 2 00274 , 0 T2 + T 195500 ) dT T CO2 = 156 oC T NH3 = 73 oC T Recycle = 173 oC Q 1 25 oC 25 oC Q2 190 oCjam 2 ) 25 156 ( 195500 − ] = 268950 jam gmol x (2879.4) cal /gmol = 774412070.2 cal / jam = 774412 kcal / jam = 3242308.1616 kJ / jam Q NH3 = m
∫
cp dT = 1415.411 jam kmol . 1000 kmol gmol 1∫
73 25 (6,70 + 0,00630 T) dT = 1415411 jam gmol∫
73 25 (6,70 T + 2 00630 , 0 T2) dT = 1415411 jam gmol x [6,70 (73 - 25) + 2 00630 , 0 (732 - 252)]cal/gmol = 1415411 jam gmol x (336.4176) cal / gmol = 476169171.6 cal / jam = 476169.1716 kcal / jam = 1993625.0876 kJ / jam∫
= 9820.5 jam kmol . 1000 kmol gmol 1∫
173 25 (7,563 + 3,4225.10-3T + 2,5728.10-7 - 2 65688 T ) dT = 9820500 jam gmol∫
173 25 (7,563 T + 2 10 . 4225 , 3 −3 T2 + 3 10 . 5728 . 2 −7 T3 + T 65688 ) dT = 9820500 jam gmol x [7,563(173 -25) + 2 10 . 4225 , 3 −3 (1732 - 252) + 3 10 . 5728 . 2 −7 (1733 - 253) + ) 25 173 ( 65688 − ] = 9820500 jam gmol x [1613.75] cal / gmol = 15847831880 cal /jam = 15847831.88 kcal / jam = 66351702.51 kJ / jam Qmasuk = Q CO2 + Q NH3 + Q recycle = 3242308.1616 + 1993625.0876 + 66351702.51 = 71587635.76 kJ / jam= Q urea + Q NH3 + Q CO2 + Q H2O + Q biuret Q urea = m
∫
cp dT = 1581.684 jam kmol . 1000 kmol gmol 1∫
190 25 (0,3437 + 0,001073 T) dT = 1581684 jam gmol∫
190 25 (0,3437 T + 2 001073 , 0 T2) dT = 1581684 jam gmol x [0,3437 (190 -25) + 2 001073 , 0 (1902-252)]cal/gmol = 1581684 jam gmol x (75.74) cal / gmol = 119796746.2 cal / jam = 119796.7462 kcal / jam = 501229.58 kJ / jam Q NH3 = m∫
cp dT = 5446.238 jam kmol . 1000 kmol gmol 1∫
190 25 (6,7 + 0,00630 T) dT = 5446238 jam gmol∫
190 25 (6,70 T + 2 00630 , 0 T2) dT = 5446238 jam gmol x [6,70 (190 – 25) + 2 00630 , 0 (1902 – 252)]cal / gmol= 5446238
jam x [1217.24] cal / gmol
= 6629378743 cal / jam = 6629378.743 kcal / jam = 27737320.66 kJ / jam Q CO2 = m
∫
cp dT = 535.14 jam kmol x 1000 kmol gmol 1∫
190 25 (10,34 + 0,00274 T - 1955002 T ) dT = 535140 jam gmol∫
190 25 (10,34 T + 2 00274 , 0 T2 + T 195500 ) dT = 535140 jam gmol x [10,34 (190 - 25) + 2 00274 , 0 (1902 - 252) + ) 25 190 ( 195500 − ] cal / gmol = 535140 jam gmol x [2939.55] cal / gmol = 1573070787 cal / jam = 1573070.787 kcal / jam = 6581728.17 kJ / jam Q H2O = m∫
cp dT = 2751.72 jam kmol x 1000 kmol gmol 1∫
190 25 (8,22 + 0,00015T + 0,00000134T2)dTjam 25
∫
2 3 = 2751720 jam gmol x [8,22 (190 – 25) + 2 00015 , 0 (1902 - 252) + 3 00000134 , 0 (1903 - 253 )] cal / gmol = 2751720 jam gmol x [1362.01] cal / gmol = 3747890334 cal / jam = 3747890.334 kcal / jam = 15691667.25 kJ / jam Qbiuret = m∫
cp dT = 1.416 jam kmol x 1000 kmol gmol 1∫
190 25 (0,3437 + 0,001037 T) dT = 1416 jam gmol∫
190 25 (0,3437 T + 2 001073 , 0 T2) dT = 1416 jam gmol x [0,3437 (190 - 25) + 2 001073 , 0 (1902 - 252)] cal /gmol = 1416 jam gmol x [75.74] cal /gmol = 107247.84 cal / jam = 107.24784 kcal / jam = 448.72 kJ / jamQkeluar = Qurea + QNH3 + QCO2 + QH2O + Qbiuret = (501229.58 + 27737320.66 + 6581728.17 + 15691667.25 + 448.72) kJ / jam = 50512394.38 kJ / jam Reaksi : 2 NH3 + CO2 NH4CO2NH2 (-∆H1) =-36 kcal/mol NH2CO2NH4 NH2CONH2 + H2O (-∆H2)=+7,7 kcal/mol
2 NH2CONH2 NH2CONHCONH2 + NH3 (-∆H3) = +4,28 kcal/mol
NH3 + CO2 + NH2CONH2 NH2CONHCONH2 + NH3 + H2O
Qreaksi = Ft ΔHr ; Ft = mol total bereaksi
Qreaksi= 7761.95 kmol/jam x (- 100500 kJ/kmol)
= - 780075975 kJ/jam
Qin + Qdihasilkan sistem = Q out + Q reaksi
71587635.76 + Qdihasilkan sistem = 52142293.5 - 780075975 Qdihasilkan sistem = -799521317.3 kJ/jam
Reaksi overall pembentukan urea merupakan reaksi eksothermis, sehingga reaksi menghasilkan panas, kemudian sebagian kecil panas tersebut digunakan untuk proses hidrasi karbamat menjadi urea. Dari seksi sintesa banyak sekali panas yang dapat dimanfaatkan, dapat terlihat banyaknya teknologi – teknologi baru dalam
(-ΔHr) = - 24.02 kcal/mol = -100.5 kJ/mol = -100500 kJ/kmol
efisiensi unit sintesa dan konsep hemat energi.
2. Unit Purifikasi/Dekomposisi a. HPD (High Pressure Decomposer)
1. Aliran panas yang masuk HPD
T = 156 °C Tref = 25 °C P = 17.5 kg/cm2
Tabel 6.30. Aliran Panas Masuk HPD
Komponen F (kmol/jam) Cp (kJ/kmol K) ΔT (K) Q1 (kJ/jam)
Urea 1389.30 138.60 131.00 25224964.38 NH3 5457.65 39.83 131.00 28476528.79 CO2 665.89 42.65 131.00 3720407.00 H2O 2751.72 78.06 131.00 28138726.20 Biuret 1.75 149.63 131.00 34221.88 Total 10266.30 85594848.24
2. Aliran panas keluar HPD to LPD
T = 165 °C Tref = 25 °C P = 17.5 kg/cm2
Tabel 6.31. Aliran Panas Keluar HPD to LPD
Komponen F (kmol/jam) Cp (kJ/kmol K) ΔT (K) Q2 (kJ/jam)
Urea 1307.13 138.79 140.00 25398384.95 NH3 408.53 40.1 140.00 2293484.12 CO2 113.18 42.91 140.00 679928.45 H2O 1902.89 78.52 140.00 20918076.98 Biuret 3.59 151.24 140.00 75986.73 Total 3735.32 49365861.23
3. Aliran panas keluar HPD to HPA
T = 155 °C Tref = 25 °C P = 17.5 kg/cm2 Tabel 6.32. Aliran Panas keluar HPD to HPA
Komponen F (kmol/jam) Cp (kJ/kmol K) ΔT (K) Q3 (kJ/jam)
Urea 0.00 138.60 130.00 0.00
H2O 390.78 35.68 130.00 1812583.64
Biuret 0.00 149.63 130.00 0.00
Total 2165.09 11193297.62
4. Panas Laten to HPA
Tabel 6.33. Panas Laten di HPD
Komponen F (kg/jam) λ (kJ/kg) Q4 (kJ/jam)
NH3 21190.00 1369 29009110 CO2 23225.00 574 13331150 H2O 7034.00 2257 15875738 Total 51449.00 58215998 Qin = 85594848.24 kJ / jam Qout = 118775156.85 kJ / jam
Panas yang dibebankan pada reboiler HPD = Qout – Qin
= 118775156.85-85594848.24
= 33180308.61 kJ / jam
Mencari massa steam yang dibutuhkan Tsin = 200 °C = 473 K
Tsout = 183 °C = 456 K
T ref = 25 °C = 298 K �ref = 2565. 78 kJ/kmol
Cpudara = 29.98 kJ/kmol.K
Asumsi yang digunakan adalah :
• panas yang disupply steam = panas yang dibebankan pada reboiler
• Cp udara dianggap tidak tergantung suhu
Q steam masuk – Q steam keluar = Q fluida keluar –Q fluida masuk Qsin = (0,7 ms. [Cpsteam.(Tsin-Tref)+�ref])+0,3 ms.Cpair (Tsin-Tref)
= 7697 ms
Qsout = ms. Cpair (Tsout-Tref)
= ms. 29.98 (456-298)
= 4736.84 ms
(7697 ms + 4736.84 ms) kJ/kmol= 33180308.61 kJ/jam
ms = 2668.548 kmol/jam
b. LPD (Low Pressure Decomposer) 1. Aliran panas yang masuk LPD
T = 149 °C Tref = 25 °C P = 2.3 kg/cm2
Tabel 6.34. Aliran Panas Masuk LPD
Komponen F (kmol/jam) Cp (kJ/kmol K) ΔT (K) Q1 (kJ/jam)
Urea 1307.13 138.42 124.00 22435741.10 NH3 408.53 39.56 124.00 2004016.52 CO2 113.18 42.40 124.00 595064.73 H2O 1902.89 77.65 124.00 18322155.96 Biuret 3.59 148.00 124.00 65860.72 Total 3735.32 43422839.02
2. Aliran panas keluar LPD to GS
T = 122 °C Tref = 25 °C P = 2.3kg/cm2
Tabel 6.35 Aliran Panas Keluar LPD to GS
Komponen F (kmol/jam) Cp (kJ/kmol K) ΔT (K) Q2 (kJ/jam)
Urea 1295.12 138.82 97.00 17439445.28 NH3 61.00 40.15 97.00 237567.55 CO2 15.64 42.95 97.00 65143.44 H2O 1878.33 76.50 97.00 13938172.50 Biuret 4.18 151.50 97.00 61433.18 Total 3254.27 31741761.94