NUWAIIR
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
2
KAJIAN IMPEDANSI DAN KAPASITANSI LISTRIK
PADA MEMBRAN TELUR AYAM RAS
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
NUWAIIR
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
oleh Jajang Juansah, M.Si dan Dr. Kiagus Dahlan
Membran didefinisikan sebagai suatu lapisan yang memisahkan dua fasa dan mengatur
perpindahan massa dari kedua fasa yang dipisahkan. Karakteristik membran mencakup; sifat
listrik, mekanik, termal dan sebagainya. Sifat listrik suatu bahan dapat dilihat dengan melakukan
pengukuran impedansi, kapasitansi dan loss coefficien Metode yang digunakan adalah mengukur
impedansi, kapasitansi dan dielektrik dengan LCR meter yang dirangkaikan dengan plat kapasitor
yang didalamnya terdapat membran. Perendaman dan tanpa perendaman dalam larutan CaCl
2,
MgCl
2, KCl dengan variasi konsentrasi serta aquades dari membran telur ayam ras untuk
mengukur sifat listrik yang meliputi kapasitansi (Cs), impedansi (Z), dan loss coefficient (D).
Perlakuan perebusan mengakibatkan nilai kapasitansi lebih kecil dari yang tidak direbus dan nilai
impedansi menjadi lebih besar dibanding tanpa perebusan. Hasil SEM membran telur ayam petelur
yang direbus tetapi tidak mengalami proses perendaman warna permukaan membrannya lebih
hitam dari yang tidak di rebus. Ukuran pori membran telur hasil perebusan lebih besar dari
membran yang tidak direbus.
Judul
: Kajian Impedansi dan Kapasitansi Listrik Pada Membran Telur Ayam
Ras
Nama
: Nuwaiir
NRP :
G74104032
Menyetujui :
Pembimbing I
Pembimbing II
Jajang Juansah, M. Si
Dr.
Kiagus
Dahlan
NIP. 132 311 933
NIP. 131 663 021
Mengetahui :
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. drh. Hasim, DEA.
NIP. 131 578 806
Puji dan syukur penulis panjatkan terhadap Allah SWT yang telah memberikan rahmat dan
karunia-Nya sehingga begitu banyak nikmat yang tak terhingga jumlahnya. Hanya dengan izin dan
kemudahan yang diberikan-Nya, penulis dapat menyelesaikan Skripsi dengan judul “”.
Penulis mengucapkan terima kasih kepada Bapak Jajang Juansah, M. Si dan Bapak Dr.
Kiagus Dahlan sebagai dosen pembimbing, Ayah, Umi, Kakak, Ka Arif, Adik dan keluarga besar
penulis atas dukungan materil dan sprituil, Devi, Dila, Eli, Inna, Fie, Ulil, Nunung, Asfini, Riski
dan teman-teman Fisika angkatan 41, teman-teman Raihana, teman-teman wisma rosa serta
seluruh pihak yang telah membantu penulis dalam menyelesaikan skripsi ini.
Pengembangan membran sintetik untuk aplikasi filtrasi dan teknologi lainnya sudah mulai
dikembangkan. Berbagai penelitian telah dilakukan dalam penerapan teknologi membran. Salah
satunya adalah karakterisasi sifat listrik membran. Oleh kerana itu penulis tertarik melakukan
penelitian membran alami untuk mengkaji kesesuaiannya dalam aplikasi teknologi.
Penulis menyadari dalam tulisan ini masih terdapat kekurangan, oleh karena itu penulis
mengharapkan saran dan kritik yang membangun untuk hasil yang lebih baik. Semoga skripsi ini
dapat memberikan sumbangan yang Allah berikan manfaatnya kepada semuanya.
Bogor, Mei 2009
Penulis
Riwayat Hidup
Penulis dilahirkan di Tangerang pada 8 Februari 1986 dari Bapak Rifai
dan ibu Halimah Hanum. Penulis merupakan putri kedua dari tiga bersaudara.
Penulis mengikuti pendidikan Dasar di SDN Binong II Tangerang dan
lulus pada tahun 1998. Pendidikan Lanjutan Tingkat Pertama dapat
diselesaikan penulis pada tahun 2001 di SLTPN 9 Tangerang. Pendidikan Menengah Atas dapat
diselesaikan penulis pada tahun 2004 di SMUN 6 Tangerang dan pada tahun yang sama penulis
diterima di Institut Pertanian Bogor, Program Studi Fisika, Fakultas Matematika dan Ilmu
Pengetahuan Alam melalui jalur USMI.
Halaman
DAFTAR GAMBAR ...i
DAFTAR LAMPIRAN ...ii
PENDAHULUAN ...1
Latar Belakang ...1
Tujuan Penelitian ...1
Hipotesis ...1
TINJAUAN PUSTAK A ... 1
Membran ...1
Membran Telur ...2
Larutan Elektrolit ...3
Kapasitor ...3
Kapasitansi ...4
Impedansi ...4
Dielektrik ...5
Loss Coefficient ...6
SEM ...6
BAHAN DAN METODE ...7
Tempat dan waktu Penelitian ...7
Alat dan Bahan ...7
Metode Penelitian ...7
Pelaksanaan Penelitian ...7
Persiapan Penelitian ...7
Persiapan Eksperimen ...7
Pengamatan ...7
Analiasis Data ...7
HASIL DAN PEMBAHASAN ...8
Kapasitansi Membran dari Ayam Petelur Tanpa Perebusan ...8
Kapasitansi Membran dari Ayam Petelur dengan Perebusan ...9
Impedansi Membran dari Ayam Petelur Tanpa Perebusan ...10
Impedansi Membran Ayam dari Petelur dengan Perebusan ...11
Loss Coefficient Membran dari Ayam Petelur Tanpa Perebusan ...12
Loss Coefficient Membran dari Ayam Petelur dengan Perebusan ...13
Impedansi Imajiner Membran dari Ayam Petelur Tanpa Perebusan ...14
Impedansi Real Membran dari Ayam Petelur Tanpa Perebusan ...15
Impedansi Real Membran dari Ayam Petelur dengan Perebusan ...16
Analisis SEM ...17
KESIMPULAN DAN SARAN ...17
Kesimpulan ...17
Saran ...18
DAFTAR PUSTAKA ...18
DAFTAR GAMBAR
Halaman
1 Skema plat kapasitor ... 4
2 Model rangkaian membran ... 5
3 Pandangan molekuler mengenai dielektrik ... 5
4 . Ilustrasi sudut pada penentuan loss coefficient I dan I
C ...6
5 Skema rangkaian sistem pengukuran impedansi, kapasitansi dan loss coefficient... 7
6 Grafik frekuensi vs kapasitansi pada berbagai konsentrasi perendaman..
(a) KCl (b) MgCl
2, (c) CaCl
2, dan (d) aquades dan tanpa... 8
7 Grafik frekuensi vs kapasitansi pada berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d) aquades, dan (e) tanpa perendaman ... 9
8 Grafik frekuensi vs impedansi pada berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d) aquades dan tanpa perendaman... 10
9 Grafik frekuensi vs impedansi pada berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d) aquades dan (e) tanpa perendaman ... 11
10 Grafik frekuensi vs impedansi pada berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d) aquades dan tanpa perendaman... 11
11 Grafik frekuensi vs loss coefficient pada berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d) aquades dan (e) tanpa perendaman ... 12
12 Grafik frekuensi vs Z*Sin θ pada berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d) aquades dan tanpa perendaman... 13
13 Grafik frekuensi vs Z*Cos θ pada berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d) aquades dan tanpa perendaman... 14
14 Grafik frekuensi vs Z*Sin θ pada berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d) aquades dan (e) tanpa perendaman ... 15
15 Grafik frekuensi vs Z*Sinθ pada berbagai konsentrasi perendaman
a) KCl, (b) MgCl
2, (c) CaCl
2, (d) aquades dan tanpa perendaman... 16
16 SEM membran dari ayam petelur yang direbus ... 17
ii
DAFTAR LAMPIRAN
Halaman
1 Diagrram Alir penelitian ... 21
2 Alat-alat Penelitian... 22
3 Data membran telur tanpa direbus dan tanpa direndam ... 23
4. Data membran telur tanpa direbus direndam aquades... 24
5 Data membran telur tanpa direbus dan direndam KCl 0,2 mM... 25
6 Data membran telur tanpa direbus dan direndam KCl 1 mM... 26
7 Data membran telur tanpa direbus dan direndam KCl 10 mM... 27
8 Data membran telur tanpa direbus dan direndam MgCl
20,2 mM... 28
9 Data membran telur tanpa direbus dan direndam MgCl
21 mM... 29
10 Data membran telur tanpa direbus dan direndam MgCl
210 mM... 30
11 Data membran telur tanpa direbus dan direndam CaCl
20,2 mM... 31
12 Data membran telur tanpa direbus dan direndam CaCl
21 mM... 32
13 Data membran telur tanpa direbus dan direndam CaCl
210 mM... 33
14. Data membran telur direbus dan tanpa direndam... 34
15 Data membran telur direbus direndam aquades ... 35
16 Data membran telur direbus dan direndam KCl 0,2 mM ... 36
17 Data membran telur direbus dan direndam KCl 1 mM ... 37
18 Data membran telur direbus dan direndam KCl 10 mM ... 38
19 Data membran telur direbus dan direndam MgCl
20,2 mM ... 39
20 Data membran telur direbus dan direndam MgCl
21 mM ... 40
21 Data membran telur direbus dan direndam MgCl
210 mM ... 41
22 Data membran telur direbus dan direndam CaCl
20,2 mM ... 42
1
PENDAHULUAN
Latar Belakang
Membran adalah fasa (padat atau cair)
yang berfungsi sebagai penghalang aliran ion
atau molekul yang berada dalam larutan, yang
merupakan penghubung dua daerah yang
memiliki karakter yang berbeda. Karakter
tersebut diantaranya: perbedaan konsentrasi,
suhu, tekanan, viskositas dan komposisi
larutan. Jenis, sifat dan ukuran pori
mempengaruhi kinerja membran. Lingkungan
juga berpengaruh pada sistem kerja membran
(Rakhmanudin, 2005).
Teknologi membran telah banyak
diaplikasikan dalam berbagai bidang, seperti
pada teknologi industri, biologi, kimia, fisika
dan kesehatan. Jika dilihat dari segi energi,
teknologi membran tergolong teknologi yang
hemat dan bersih karena saat
mengoperasikannya tidak diperlukan energi
yang besar. Selain itu juga tidak diperlukan
zat-zat kimia pendukung yang menimbulkan
masalah baru sehubungan dengan limbah
(Huriawati, 2006).
Membran terbagi atas dua jenis yaitu
membran alami dan sintetik. Membran telur
merupakan merupakan salah satu dari
membran alami. Karakteristik membran ini
meliputi sifat listrik, termal, mekanik dan
sebagainya. Sifat kelistrikan dapat dilihat
dengan melakukan pengukuran konduktansi,
kapasitansi, impedansi dan loss coefficient.
Sedangkan mekanik dengan melakukan uji
tarik, uji tekan, uji getar dan uji geser.
Telur memiliki suplai protein dengan
asam amino yang hampir sempurna untuk
memenuhi kebutuhan tubuh, begitu pula
kandungan mineral dan vitaminnya. Telur juga
mengandung asam amino esensial (asam
amino yang tidak dapat diproduksi tubuh
sehingga harus dipasok dari makanan yang
lengkap).
Secara fisik, telur terdiri dari empat bagian
yaitu cangkang atau kulit luar (shell), lapisan
selaput (membrane shell), putih telur (egg
white), dan kuning telur (yolk).
Pada proses makhluk hidupnya membran
telur berfungsi sebagai pelindung embrio atau
pelindung putih telur dan kuning telur agar
tidak keluar dan terkontaminasi oleh zat yang
tigak diinginkan. Membran telur memiliki
pori-pori yang berfungsi sebagai media lalu
lintas gas oksigen (O
2) dan karbondioksida
(CO
2). Dalam prosesnya membran telur
dikategorikan sebagai media yang penting.
Proses perebusan dan perendaman membran
telur memberikan pengaruh pada sifat-sifat
membran telur tersebut (Mahrani, 2008).
Tujuan Penelitian
Penelitian ini bertujuan untuk mengukur
sifat listrik yang meliputi kapasitansi (Cs),
impedansi (Z), dan loss coefficient (D) dari
membran telur ayam ras berdasarkan tanpa
perebusan dan dengan perebusan serta
perendamam pada larutan garam dengan
variasi konsentrasi, perendaman dalam
aquades dan tanpa perendaman.
Hipotesis
Kondisi membran telur yang direbus
mengakibatkan nilai kapasitansi yang lebih
kecil dari telur yang tidak direbus.
TINJAUAN PUSTAKA
Membran
Membran dapat didefinisikan sebagai
lapisan tipis semipermiabel di antara dua fasa.
Fasa pertama adalah feed atau larutan
pengumpan yaitu komponen atau partikel yang
akan dipisahkan. Fasa yang kedua adalah
permeate yaitu hasil pemisahan. Kemampuan
pemisahan yang dimiliki oleh membran untuk
melewatkan suatu senyawa kimia atau molekul
diakibatkan oleh adanya perbedaan sifat fisika
atau kimia antara membran dengan senyawa
kimia (Syam, 2006).
Berdasarkan eksitensinya
membran terdiri dari membran alami dan
membran sintetik. Membran alami adalah
membran pada sistem dan proses kehidupan
makhluk hidup. Komponen utama membran
alami adalah lipid dan protein, sedangkan
membran sintetik adalah membran buatan
yang dapat terbuat dari bahan alami atau bahan
non alami (Huriawati, 2006).
Berdasarkan kelistrikannya membran
terdiri atas membran bermuatan tetap dan
membran bermuatan netral. Membran
bermuatan tetap dapat dilalui oleh ion-ion
tertentu. Membran bermuatan tetap yang hanya
dapat dilalui oleh kation saja disebut Kation
Exchange Membrane (KEM), sedangkan jika
anion saja disebut Anion Exchange Membrane
(AEM). Selain kedua membran tersebut ada
juga membran yang merupakan gabungan
keduanya yang disebut Double Fixed Charge
Membrane (DFCM). KEM dan AEM memiliki
karakter berbeda dan pada aplikasinya dapat
digunakan bersamaan. Membran bermuatan
tetap dapat digunakan dalam proses industri,
seperti proses elektrodialisis, fuel cell dan
berbagai proses filtrasi. Membran bermuatan
netral banyak digunakan dalam aplikasi
bidang-bidang sains dan teknologi. Membran
netral terdiri dari polimer yang tidak mengikat
ion-ion tetap. Membran netral juga dapat
bersifat selektif terhadap larutan-larutan
kimiawi. Selektivitas membran ditentukan oleh
unsur-unsur penyusun (monomer), ukuran
kimia, ukuran pori, daya tahan terhadap
tekanan dan suhu, resistivitas dan konduktansi
serta kelistrikan lainnya (Rakhmanudin, 2005).
Jika dilihat dari bentuknya membran
terdiri dari membran simetri dan asimetri.
Membran simetri memiliki struktur pori yang
homogen dan relatif sama, ketebalannya antara
10-200 µm. Sedangkan membran asimetrik
memiliki ukuran dan kerapatan yang tidak
sama. Membran jenis ini memiliki dua lapisan,
yaitu lapisan kulit yang tipis dan rapat (skin
layer) dengan ketebalan < 0,5 µm serta lapisan
pendukung yang berpori dengan ketebalan
50-200µm (Maryati, 2003).
Dalam operasi membran dikenal dua jenis
aliran umpan, yaitu aliran cross-flow dan
aliran dead-end. Pada sistem cross flow, arah
aliran umpan parallel atau sejajar pada
permukaan membran. Aliran parallel tersebut
akan menghasilkan gaya geser (shear forces)
atau turbulensi didekat permukaan membran
sehingga pembentukan filter cake (deposisi
partikel yang menumpuk pada permukaan
membran) relatif kecil. Pada aliran dead end,
keseluruhan dari fluida melewati membran
(sebagai media filter) dan partikel tertahan
pada membran, dengan demikian fluida umpan
mengalir melalui tahanan membran dan
tahanan penumpukan partikel pada permukaan
membran (Suprihanto et al. 2004).
Berdasarkan gradient tekanan sebagai
gaya dorongnya dan permeabilitasnya,
membran dapat dibedakan menjadi beberapa
jenis yaitu (Mulder,1996):
a. Mikrofiltrasi (MF), Membran jenis ini
beroperasi pada tekanan berkisar 0,1-2 Bar
dan batasan permeabilitasnya > 50 L/m
2.
jam bar.
b. Ultrafiltrasi (UF), membran jenis ini
beroperasi pada tekanan antara 1-5 Bar
dan batasan permeabilitasnya adalah
10-50 L/m
2jam bar
c. Nanofiltrasi, membran ini beroperasi pada
tekanan antara 5-20 Bar dan batasan
permeabilitasnya mencapai 1,4-12 L/m
2jam bar.
d. Reverse Osmosis (RO), membran ini
beroperasi pada tekanan antara 10-100 bar
dan batasan permeabilitasnya mencapai
0,05-1,4 L/m
2jam bar.
Berdasarkan jenis pemisahan dan
strukturnya,
membran dapat dibagi menjadi 3
kategori
:
a. Porous membrane. Pemisahan
berdasarkan atas ukuran partikel dari
zat-zat yang akan dipisahkan. Hanya partikel
dengan ukuran tertentu yang dapat
melewati membran sedangkan sisanya
akan tertahan. Berdasarkan klasifikasi dari
IUPAC, pori dapat dikelompokkan
menjadi macropores (>50nm), mesopores
(2-50nm), dan micropores (<2nm).
Porous membrane digunakan pada
microfiltration dan ultrafiltration.
b. Non-porous membrane. Dapat digunakan
untuk memisahkan molekul dengan
ukuran yang sama, baik gas maupun
cairan.
Pada non-porous membrane, tidak
terdapat pori seperti halnya porous
membrane. Perpindahan molekul terjadi
melalui mekanisme difusi
.
Jadi, molekul
terlarut di dalam membran, baru kemudian
berdifusi melewati membran tersebut.
c. Carrier membrane. Pada carriers
membrane, perpindahan terjadi dengan
bantuan
carrier molecule yang
mentransportasikan komponen yang
diinginkan untuk melewati membran.
Carrier molecule memiliki afinitas yang
spesifik terhadap salah satu komponen
sehingga pemisahan dengan selektifitas
yang tinggi dapat dicapai.
Membran Telur
Sebagai bahan pangan, telur merupakan
gudang semua zat gizi yang dibutuhkan tubuh
kecuali vitamin C dan K. Vitamin yang
terpenting pada telur adalah vitamin B12 yang
dapat memperbaiki fungsi saraf. Tidak hanya
itu, telur juga mengandung lesithin (emulsifier
alami) yang kaya akan cholin. Cholin terlibat
dalam pemindahan kolesterol melalui
peredaran darah dan mambantu metabolisme
lemak. Cholin juga merupakan komponen
penting dari membran sel dan jaringan saraf.
Telur tersusun dari kuning telur (yolk),
putih telur (albumen), kerabang tipis, kerabang
telur, dan beberapa bagian lain yang cukup
kompleks. Kerabang telur terdiri atas dua
bagian, yaitu kerabang tipis (membran) baik
luar dan dalam yang dihasilkan oleh istmus
dan kerabang telur keras. Tebal kerabang telur
300 mm. Kerabang telur terdiri atas bahan
kering 98,4% dan air 1,6%. Bahan kering
terdiri dari protein 3,3%dan mineral 95,1%.
Mineral yang paling banyak terdapat pada
kerabang telur adalah CaCO
3(98,43%),
3
Lapisan kerabang telur terdiri dari kutikula,
membran palisadik, membrane cone, membran
mamiler, dan membran kerabang dalam
(Yuwanta, 2004).
Cangkang telur merupakan bagian telur
paling luar, berlapis keras setebal 0,2-0,4 mm
dan mengandung kalsium karbonat yang
berfungsi melindungi bagian dalam telur. Pada
kulit telur terdapat pori-pori yang dapat dilalui
udara. Warnanya bervariasi mulai dari putih
sampai kecokelatan tergantung pada jenis
unggasnya. Namun perbedaan warna sama
sekali tidak mempengaruhi kualitas telur.
Lapisan tipis yang terletak antara kulit luar dan
isi telur (putih dan kuning telur) disebut
memban shell atau selaput lapisan yang terdiri
dari lapisan membran dalam dan membran
luar, keduanya mirip dinding yang
menghalangi bakteri (Wirakusumah).
Membran telur adalah membran alami
yaitu membran dalam proses makhluk hidup.
Membran telur dalam proses makhluk
hidupnya dikategorikan sebagai alat filtrasi
pencegah masuknya zat yang tidak diinginkan.
Membran telur merupakan membran yang
bermuatan netral. Sesuai dengan fungsi aslinya
membran telur diusahakan pengembangannya
sebagai alat filtrasi dalam aplikasi teknologi.
Efektivitas kerja membran sangat dipengaruhi
kualitas telur. Apabila telur yang digunakan
berkualitas buruk maka akan diperoleh hasil
yang tidak sesuai dengan yang diharapkan
karena membran tipisnya juga berkualitas
buruk (Mahrani, 2008).
Larutan Elektrolit
Larutan adalah campuran homogen dalam
molekul, atom atau ion dari dua zat atau lebih.
Suatu larutan disebut campuran karena
susunannya dapat berubah-ubah. Sifat larutan
terdiri atas homogen dan heterogen. Larutan
homogen merupakan larutan yang susunannya
seragam sehingga tidak dapat diamati adanya
bagian-bagian yang berlainan. Sedangkan
dalam campuran heterogen,
permukaan-permukaan tertentu dapat dideteksi antara
fase-fase yang terpisah. Komponen yang paling
banyak dalam larutan disebut pelarut (solvent)
dan komponen yang kuantitasnya lebih kecil
disebbut zat terlarut (solute) (Charlas et all.
1984).
Kelarutan ditentukan oleh konsentrasi zat
terlarut dalam larutan jenuhnya. Konsentrasi
merupakan banyaknya zat terlarut dalam
pelarut ataupun larutan. Konsentrasi dapat
dinyatakan dalam persen, molar, molal, persen
mol, fraksi mol dan ppm. Larutan jenuh adalah
larutan yang mengandung zat terlarut dalam
jumlah yang diperlukan untuk adanya
kesetimbangan antara zat terlarut yang larut
dan yang tidak larut. Larutan jenuh tidak dapat
menampung zat terlarut lebih banyak., tetapi
larutan ini belum tentu suatu larutan pekat.
Konsentrasi molar (M) adalah banyaknya
partikel zat terlarut dalam larutan yaitu
konsentrasi molar. Secara matematis dapat
dinyakan dengan:
Banyaknya mol zat terlarut
M =
Banyaknya liter larutan (1)
Berdasarkan daya hantar listriknya,
larutan dapat dibagi menjadi larutan elektrolit
dan non elektrolit. Sedangkan elektrolit dapat
dikelompokkan menjadi larutan elektrolit kuat
dan elektrolit lemah.
Elektrolit merupakan zat yang jika
dilarutkan ke dalam air akan terurai menjadi
ion-ion (terionisasi), sehingga dapat
menghantarkan listrik. Zat yang dalam air akan
terurai seluruhnya menjadi ion-ion (terionisasi
sempurna) disebut elektrolit kuat. Zat yang
tergolong elektrolit kuat seperti: KCl, MgCl
2,
CaCl
2,NaCl dan lain-lain. Zat yang hanya
sebagian kecil molekulnya larut bereaksi
dengan air untuk membentuk ion (terionisasi
sebagian) disebut elektrolit lemah. Zat yang
tergolong elektrolit lemah seperti: NH
3,
H
2SO
3, CH
3COOH, dan lain-lain.
Larutan non elektrolit adalah larutan yang
tidak dapat menghantarkan arus listrik, karena
zat terlarutnya dalam pelarut tidak dapat
menghasilkan ion-ion. Larutan urea, sukrosa,
glukosa, alkohol, dan lain-lain merupakan
larutan jenis ini.
Kapasitor
Kapasitor adalah dua buah penghantar
sebarang yang terisolasi, mengangkut
muatan-muatan yang sama besarnya dan berlawanan
tanda sebesar +q dan -q (Halliday dan Resnick,
1996).
Salah satu struktur sebuah kapasitor
adalah duah plat penghantar yang ditempatkan
berdekatan tetapi tidak bersentuhan. Jika kedua
tegangan diberi tegangan listrik, maka muatan
positif akan terkumpul pada salah satu
penghantar dan muatan negatif pada
penghantar lainnya. Muatan positif tidak dapat
mengalir menuju plat bermuatan negatif
sebaliknya karena terpisah oleh bahan
dielektrik yang non konduktif. Muatan ini
tersimpan selama tidak ada konduksi pada
ujung-ujung kakinya (Sulastri ,2006).
Kapasitansi
Kapasitansi adalah besaran yang
menyatakan kemampuan dari suatu kapasitor
untuk dapat menampung muatan listrik (Tipler,
1996). Kapasitansi bergantung pada ukuran
dan bentuk konduktor dan akan bertambah bila
ada sebuah material pengisolasi atau dielektrik
(Young dan Freedman, 2003). Untuk tinjauan
kapasitor keping sejajar, faktor geometri yang
menentukan adalah luas penampang keping
sejajar dan jarak antara kepingnya, sedangkan
sifat bahan dielektriknya ditentukan oleh nilai
konstanta dielektrik bahannya (Sulastri, 2006).
Kapasitansi diukur berdasarkan besar
muatan yang dapat disimpan pada suatu
kenaikan tegangan (Woollard, 1988). Dapat
dituliskan:
C = nilai kapasitansi dalam F (farad)
Q = muatan elektron dalam C (coulomb)
V = besar tegangan dalam V (volt)
Gambar 2. Model rangkaian membran
(Benavente, 2000)
Permukaan kapasitor yang berhubungan
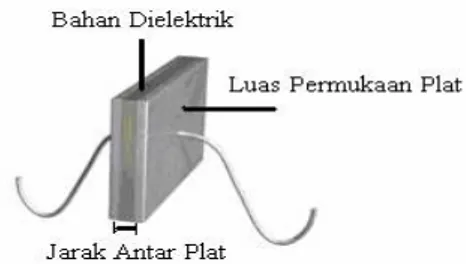
biasanya berbentuk plat rata. Kapasitansi dari
suatu kapsitor dipengaruhi oleh tiga faktor
yaitu pada luas plat, jarak antar plat dan
medium penyekat atau bahan dielektris. Untuk
kapasitor plat sejajar yang masing-masing
memiliki luas A dan dipisahkan oleh jarak d
yang berisi udara, kapasitansi dinyatakan
dengan:
A = luas area plat (m
2)
d = jarak antar plat (m)
ε
0= permitivitas ruang hampa
= 8,85×10
-12F/m
Gambar 1. Skema kapasitor plat sejajar
Ketika luas area plat meningkat, maka
kapasitansi akan meningkat. Ketika jarak antar
plat besar, maka nilai kapasitansi berkurang.
Ketika bahan dielektrik besar, maka
kapasitansi akan meningkat. Dengan
mempertimbangkan tiga faktor tersebut, maka
kapasitansi kapasitor antar dua plat sejajar
dapat dihitung
menggunakan
rumusan
:
K = tetapan dielektrik
Sel membran dapat dimodelkan dengan
rangkaian listrik yang terdiri dari gabungan
kapasitor dan resistor (Coster).
Gabungan seri antara Z
1dan Z
2serta
melihat perumusan Zm maka akan
menghasilkan nilai kapasitansi membran.
dimana
ω
=
2
π
f
merupakan frekuensi sudut
sehingga kapasitansi bergantung pada
frekuensi.
R
CR
R
C
C
1 ~ 1 1 ~1
C
I
G
Z
ω
+
=
2 ~ 2 2 ~1
C
I
G
Z
ω
+
=
m m mC
I
G
Z
ω
~ ~1
+
=
2 2 2 2 2 2)
2
1
(
)
2
1
(
)
2
1
(
2
1
2
1
1
2
C
C
G
G
C
C
C
C
C
G
C
G
Cm
+
+
+
+
+
+
=
ω
ω
5
Grafik frekuensi dengan kapasitansi
Impedansi
Jika kapasitor dirangkaikan dengan
resistor dan induktor pada rangkaian arus
bolak-balik (AC), maka hambatan total
rangkaian itu dikenal dengan impedansi.
Secara pendekatan, suatu hambatan (R)
diambil untuk menghadirkan komponen
dissipative (menghilangkan) respon dielektrik,
sedangkan suatu kapasitansi (C)
menggambarkan komponen penyimpan
dielektrik bahan. Jika suatu sirkuit paralel R–C
yang ditunjukkan pada gambar 2
dipertimbangkan, maka hal tersebut
menciptakan suatu model yang cukup dari
polarisasi dielektrik pada cakupan frekuensi
yang didominasi oleh perpindahan muatan
bebas. Keseluruhan impedansi dari sirkuit
diberikan oleh penjumlahan kontribusi
hambatan dan kapasitansi (Azizah, 2008).
Resistansi dari kapasitansi C adalah
R=1/(jωC), dimana j merupakan satuan
imajiner. Pada rangkaian (R
P) dan kapasitansi
(reaktansi 1/(ωC
P) yang terangkai paralel dapat
dperoleh dari Hukum Kirchoff,
Dari persamaan (5) diperoleh:
Jika ditambahkan R
ssecara seri pada elemen
RC maka diperoleh:
dimana ω digantikan dengan 2πf. Real (Z
re)
dan bagian imajiner (Z
im) dari impedansi
kompleks Z adalah:
dan
(Gitter, 2007)
Impedansi bergantung pada frekuensi. Jika
frekuensi itu bertambah, X
Lbertambah dan X
Cberkurang; maka selalu ada satu fre pada
saat X
Ldan X
Csama dan X
L–X
Cadalah nol.
Pada frekuensi ini impedansi Z adalah:
atau
Z = impedansi (Ω)
R = hambatan (Ω)
X
L= reaktansi induktif (Ω)
X
C= reaktansi kapasitif (Ω)
f = frekuensi (Hz)
L = induktansi (H)
C = kapasitas kapasitor (F)
(Giancoli, 2001)
Dielektrik dan Loss Coefficient
Ruang antara konduktor pada suatu
kapasitor biasanya diisi dengan bahan isolator
yang dinamakan dielektrik, misalnya kaca,
kertas, mika, dan lain-lain.
Eksperimen yang dilakukan Faraday
menunjukkan bahwa
adanya dielektrik
menyebabkan
kapasitansi bertambah.
Penambahan kapasitansi ini
disebabkan
karena adanya
dielektrik mengakibatkan
medan listrik
di antara kapasitor
berkurang.
Sifat dielektrik adalah sifat yang dapat
menggambarkan kemampuan bahan untuk
menyimpan energi dalam bahan dan
menghamburkan energi dalam bentuk panas,
ketika bahan tersebut diekspos pada medan
arus listrik. Sifat ini dihasilkan dari arus
pengisian dan arus hilang yang berhubungan
dengan kapasitansi listrik dan tahanan material
(Silalahi, 2003).
Bahan dielektrik suatu kapasitor berfungsi
untuk menghambat aliran arus antar plat.
Bahan dielektrik dinilai berdasarkan
kemampuan bahan untuk mempengaruhi gaya
elektrostatik pada suhu tertentu yang disebut
konstanta dielektrik. Kemampuan dari bahan
dielektrik untuk mendukun gaya elektrostatik
berbanding lurus dengan konstanta dielektrik
(Putri, 2007).
Karakteristik yang dimiliki oleh semua
bahan dielektrik, baik yang berupa cairan,
padatan atau gas, berbentuk kristal atau bukan,
Cm
ialah kemampuan untuk menyimpan energi
listrik. Penyimpanan ini terjadi dengan
pergeseran relatif kedudukan muatan positif
internal dan muatan negatif internal terhadap
gaya atomik dan molekular yang normal
(Hayt, 1986).
(a)
(b)
(c)
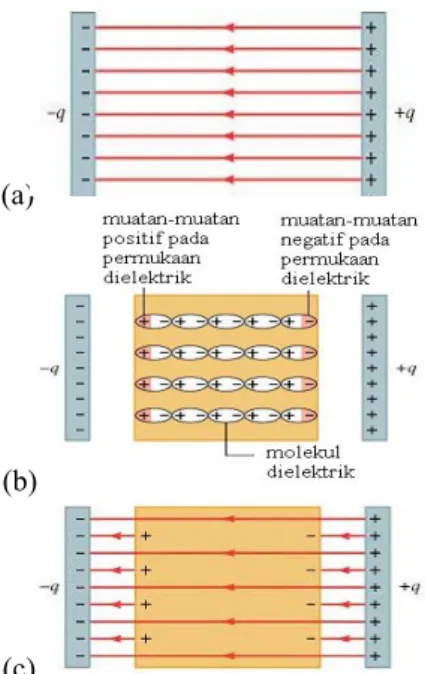
Gambar 3. Pandangan molekuler mengenai
efek dielektrik
Kapasitor mempunyai muatan +q pada
satu pelat dan –q di pelat yang lain (Gambar
3a). Kapasitor diisolasi sehingga muatan tidak
bisa mengalir ke pelat atau dari
pelat-pelat tersebut. Dielektrik di sisipkan di antara
kedua pelat (Gambar 3b). Molekul-molekul
dielektrik mungkin merupakan polar.
Maksudnya, walaupun molekul-molekul
tersebut netral, elektron-elektronnya mungkin
tidak terdistribusi merata, sehingga satu bagian
dari molekul akan positif dan bagian lainnya
negatif. Karena adanya medan listrik di antara
pelat-pelat tersebut, molekul-molekul akan
cenderung menjadi terorientasi sebagaimana
digambarkan. Bahkan jika molekul-molekul
itu bukan polar, medan listrik di antara pelat
akan menginduksi beberapa pemisahan muatan
pada molekul. Beberapa garis medan listrik
sebenarnya tidak menembus dielektrik, tetapi
berakhir (dan mulai kembali) pada
muatan-muatan yang diinduksi pada permukaan
dielektrik (Giancoli, 2001).
Permitivitas atau sifat dielektrik
digambarkan sebagai suatu permitivitas relatif
komplek yang merupakan nilai pembagi antara
permitivitas absolut dengan permitivitas ruang
hampa (Nyfors dan Vainikainen, 1989 dalam
Rynnanen, 1995):
0
εε
ε
abs=
dimana ε
abs= permitivitas absolut bahan
ε
o= permitivitas ruang hampa
(8,85×10
-12F/m)
ε = permitivitas relatif bahan
Karena permitivitas merupakan suatu
bilangan kompleks maka dapat dinyatakan
dalam dua bagian yang terdiri dari komponen
nyata dan khayal (Risman, 1991 dan
Rynnanen,1995) yaitu:
δε
ε
ε
ε
je
j
′′
=
−−
′
=
dimana ε = permitivitas relatif kompleks
ε
'= tetapan dielektrik
ε
"= faktor kehilangan dielektrik
j = unit imajiner (√-1)
δ = sudut kehilangan dielektrik
Bagian nyata permitivitas diketahui
sebagai tetapan dielektrik ε
'yang menunjukkan
kemampuan bahan untuk menyimpan energi
listrik, sedangkan komponen khayal
merupakan faktor dielektrik ε
"menyatakan
kemampuan bahan untuk menghamburkan atau
melepaskan energi dan mengkonversinya
menjadi panas yang nilainya selalu positif dsan
biasanya lebih kecil dari ε
'.
Menurut Mohsenin (1984), tetapan
dielektrik didefinisikan sebagai perbandingan
antara kapasitas bahan, C dengan kapasitansi
runang hampa, C
0 0C
C
=
ε
0ε
ε
ε
′
=
dimana ε
omenunjukkan ruang hampa dan ε
merupakan permitivitas relatif kompleks.
Tetapan dielektrik ε
'menunjukkan
kemampuan bahan untuk menyimpan energi
dalam bentuk medan listrik yang berfungsi
sebagai kondensor sehingga dapat dinyatakan
dalam persamaan (2), dimana C merupakan
kapasitas bahan, Q menunjukkan muatan
dalam bahan dan V adalah beda potensial.
Loss Coefficient merupakan faktor
hamburan energi pada bahan (Harmen, 2001).
Sudu Loss Coefficient D merupakan sudut
yang dibentuk antara arus total (I)arus bolak
balik (ac) dan arus pengisian I
Cpada kapasitor
7
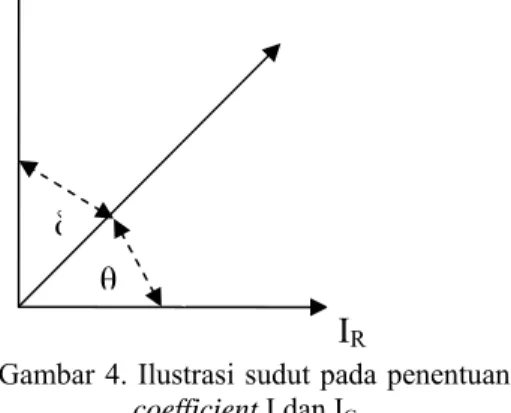
Gambar 4. Ilustrasi sudut pada penentuan loss
coefficient I dan I
CPada medium yang ideal, didalam
dielektrik kapasitor tidak ada energi hilang
yang terjadi dan arus akan membentuk sudut
90
0terhadap voltase. Jika terjadi kehilangan
energi, maka sudut fase akan berkurang, dan
loss coefficient akan bertambah berdasarkan
hubungan sebagai berikut:
Loss coefficient D = 90
0– sudut fase (12)
Pada frekunsi yang diberikan, dielektrik
dapat diperlihatkan sebagai sirkuit paralelyang
terdiri dari kapasitansi dan tahanan yang ideal.
Apabila tegangan sinusoidal diberikan
pada dielektrik ini maka akan menghasilkan
arus pengisian, dimana arah arus sudut adalah
90
0terhadap tegangan. Pada waktu yang sama
terjadi kehilangan arus IR dalam fase yang
sama dengan V yang diberikan. Sudut θ yang
memisahkan antara arus total I dengan
tegangan disebut sudut fase. Cos θ merupakan
faktor tenaga (PF). Pada kasus kehilangan
energi dielektrik rendah (low loss dielectric),
apabila δ kecil, maka cos θ bisa menggantikan
tan δ. Untuk dielektrik dengan kehilangan
cukup besar, hibungan berikut dapat digunakan
menghitung loss coefficient:
Loss coefficient dapat dinyatakan dengan
persamaaan berikut:
dimana ω adalah frekuensi angular dan C
adalah kapasitansi (Harmen, 2001).
Atom dan molekul merupakan unsur
bermuatan yang terdiri dari partikel bermuatan
negatif (elektron) yang mengelilingi partikel
bermuatan positif (proton) dan neutron sebagai
pusatnya. Ketika bahan sebagai dielektrik
diberikan suatu medan listrik yang tetap,
muatan-muatan listrik dalam dielektrik
tersebut cenderung berpisah atau terpolarisasi,
muatan negatif mengarah ke elektroda positif
dan muatan positif mengarah ke elektroda
negatif. Berbeda dengan konduktor apabila
diberikan suatu medan listrik akan terjadi
aliran arus, dimana muatan-muatan negatif
dalam bahan tersebut bergerak.
SEM
SEM merupakan alat untuk melihat benda
yang sangat kecil dalam bentuk stereo dengan
skala pembesaran tinggi. Alat tersebut
menggunakan sinar elektron berenergi tinggi
untuk melihat objeknya yang sangat kecil.
Prinsip kerja SEM adalah mendeteksi elektron
yang dipancarkan oleh suatu sampel padatan
ketika ditembakkan oleh berkas elektron
berenergi tinggi secara kontinu yang
dipercepat di dalam electromagnetic coil yang
dihubungkan dengan tabung sinar katode
sehingga dihasilkan suatu informasi mengenai
keadaan permukaan suatu sampel senyawa
(Steven, 2003).
Sebelum dianalisis dengan SEM, sampel
harus dipreparasi terlebih dahulu. Hal-hal yang
harus dipenuhi untuk menyiapkan sampel,
yaitu menghilangkan seluruh pelarut, air, atau
bahan lain yang dapat menguap ketika di
dalam vakum dan menipiskan sampel yang
akan dianalisis. Jika spesimen merupakan
isolator, seperti tanaman, kuku jari, dan
keramik, maka perlu dilapisi dengan bahan
konduktor. Bahan konduktor yang biasa
digunakan adalah emas, perak, dan aliansi
emas dan paladium. Pelapisan dilakukan dalam
ruang penguapan vakum (Sutiani, 1997).
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penilitian dilaksanakan di Loboratorium
Biofisika Departemen Fisika Fakultas
Matematika dan Ilmu Pengetahuan Alam,
Institut Pertanian Bogor mulai bulan Juli 2008
sampai Oktober 2008.
Alat dan Bahan
Bahan-bahan yang digunakan dalam
penelitian ini adalah membran Telur, serbuk
KCl, MgCl
2, CaCl
2, PCB, kabel, FeCl
3dan
Aquades.
Alat yang dipergunakan adalah nampan
plastik, pemotong PCB, gunting, neraca
analitik, gelas ukur, pengaduk kaca, spatula,
cawan petri dan LCR meter.
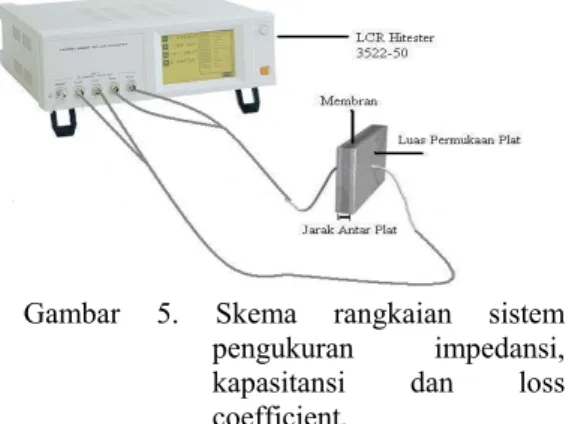
Metode Penelitian
Metode yang digunakan adalah mengukur
impedansi, kapasitansi dan dielektrik dengan
LCR meter yang dirangkaikan dengan plat
kapasitor yang didalamnya terdapat membran.
I
Cδ
θ
Pelaksanaan Penelitian
Pelaksanaan penelitian meliputi persiapan
penelitian, persiapan eksperimen, eksperimen,
analisa data dan dilanjutkan dengan
pembahasan hasil dalam bentuk skripsi.
Persiapan penelitian
Persiapan penelitian yang dilakukan
meliputi studi literatur yang dibutuhkan dalam
penelitian baik berupa pengumpulan
sumber-sumber acuan berupa buku, jurnal, skripsi,
referensi dan sebagainya. Selain itu
dipersiapkan dasar-dasar teori serta perumusan
fisika dan matematika yang diperlukan dalam
penelitian.
Persiapan Eksperimen
Persiapan eksperimen yang dilakukan
antara lain adalah persiapan alat, persiapan
bahan dan perancangan sistem.
1. Persiapan Peralatan
Plat kapasitor yang digunakan dalam
penelitian ini terbuat dari PCB berukuran
luar (2 x 1.5)cm dan bagian tengah
berukuran (1.5 x 1.5) cm.
2. Persiapan Bahan
a. Telur direbus dan tidak direbus,
selaput putih telur (membran) dilepas
dari cangkang. Membran dipotong
dengan ukuran (1,5×1,5)cm
2.
b. Membuat larutan KCl, MgCl
2dan
CaCl
2masing-masing dengan
konsentrasi 0,2mM, 1mM dan 10mM.
3. Perancangan Sistem
Pengukuran Impedansi, Kapasitansi dan
Loss Coefficient menggunakan LCR
meter Hi Tester Hioki 3522-50 dan plat
kapasitor.
Eksperimen
Pengesetan alat eksperimen sedemikian
rupa. Penempatan membran berada dalam plat
kapasitor.
Gambar 5. Skema rangkaian sistem
pengukuran impedansi,
kapasitansi dan loss
coefficient.
Membran yang diamati adalah membran
yang tanpa direbus dan membran yang direbus.
Membran yang tanpa direbus dan direbus
diamati lagi yaitu dengan direndam aquades,
larutan KCl, MgCl
2, dan CaCl
2dengan
masing-masing konsentrasi 0,2mM; 1mM dan
10mM. Frekuensi yang digunakan dalam
pengukuran bervariasi dari 10kHz sampai 100
kHz dengan interval 5 kHz. Perendaman
dilakukan selama 10 menit.
Pengambilan data
Pengambilan data di ambil dengan tiga
kali pengulangan dari membran yang tanpa
direbus dan tanpa direndam, membran tanpa
direbus dan direndam aquades, membran tanpa
direbus dan direndam larutan KCl, MgCl
2dan
CaCl
2dengan masing-masing konsentrasi 0,2
mM; 1mM dan 10mM, kemudian membran
yang direbus dan tanpa direndam, membran
yang direbus dan direndam aquades serta
membran yang direbus dan direndam laritan
KCl, MgCl
2, dan CaCl
2dengan masing-masing
konsentrasi 0,2 mM;1mM dan 10 mM.
Analisa Data
Analisa data yang dilakukan adalah
menggambarkan hubungan tanpa perendaman,
larutan aquades, konsentrasi larutan KCl,
MgCl
2, CaCl
2,terhadap frekuensi, impedansi,
kapasitansi, dan konstanta dielektrik membran.
HASIL DAN PEMBAHASAN
Kapasitansi Membran Telur dari Ayam
Petelur Tanpa Perebusan
Dari data eksperimen didapatkan grafik
seperti yang terlihat pada gambar 6.
Dari grafik terlihat nilai kapasitansi yang
bervariasi terhadap frekuensi mengalami
penurunan dengan bertambahnya frekuensi
yang diberikan, baik pada frekuensi rendah
maupun frekuensi tinggi.
Frekuensi berpengaruh terhadap bahan
dielektrik itu sendiri, yaitu dengan naiknya
frekuensi maka semakin banyak gelombang
yang ditransmisikan tiap detiknya, sebelum
kapasitor terisi penuh arah arus listrik sudah
berbalik sehingga terjadi pengosongan muatan
dalam kapsitor dengan cepat, yang
mengakibatkan muatan dalam kapasitor
semakin berkurang dan kemampuan kapasitor
untuk menyimpan muatan semakin kecil
(Sutrisno, 1984). Dengan adanya bahan
dielektrik di antara plat kapasitor akan
memunculkan muatan-muatan permukaan
9
yang cenderung memperlemah medan listrik
semula dalam dielektrik. Pelemahan medan
listrik ini menyebabkan pengurangan beda
potensial antara plat-plat kapasitor yang berisi
bahan dielektrik (Tippler, 1996).
0 500 1000 1500 2000 2500 3000 3500 4000 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) K a pa s ita n s i (nF) KCl 0,2 mM KCl 1 mM KCl 10 mM
(a)
0 1000 2000 3000 4000 5000 6000 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) K a pa s it a ns i ( n F ) MgCl2 0,2 mM MgCl2 1 mM MgCl2 10 mM(b)
0 500 1000 1500 2000 2500 3000 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) K a pa s ita ns i ( n F) CaCl2 0,2 mM CaCl2 1 mM CaCl2 10 mM(c)
0 10 20 30 40 50 60 70 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) K a pa s it a ns i ( n F) tanpa direndam direndam aquadest(d)
Gambar
6.
Grafik frekuensi vs kapasitansi
pada berbagai konsentrasi
perendaman (a) KCl (b) MgCl
2, (c)
CaCl
2, dan (d) aquades dan tanpa
perendaman
Gambar 6 menunjukkan kurva hubungan
frekuensi dengan kapasitansi membran ayam
petelur tanpa perebusan terhadap konsentrasi
larutan KCl, MgCl
2, CaCl
2dan direndam
aquades serta tanpa direndam. Nilai
kapasitansi untuk semua perlakuan mengami
penurunan.
Pada larutan KCl dan CaCl
2dengan
konsentrasi 10 mM nilai kapasitansinya
mendekati sama tingginya yaitu sekitar
2750nF dan 3500nF sedangkan larutan MgCl
2dengan konsentrasi yang sama yaitu 10 mM,
nilai kapasitansinya rendah dibandingkan
dengan konsentrasi yang lainnya.. Nilai
kapasitansi larutan KCl dan CaCl
2dengan
konsentrasi 10 mM lebih tinggi dibandingkan
dengan konsentrasi 0,2 mM dan 1 mM tetapi
pada konsentrasi 0,2 mM larutan KCl, nilai
kapasitansi lebih tinggi dari 0,2 mM larutan
CaCl
2. penurunan kapasitansi yang signifikan
terjadi saat direndam aquades yaitu dari
kisaran nilai 62nF ke 16nF hingga 0,5nF.
Pada konsentrasi 0,2mM – 10mM
impedansi meningkat. Kenaikan impedansi
yang signifikan terjadi pada konsentrasi
0,2mM sedangkan peningkatan impedansi
pada konsentrasi 1mM dan 10mM tidak
signifikan.
Nilai kapasitansi sebuah kapasitor keping
sejajar dipengaruhi oleh luas penampang
keping, jarak antar kepeing dan sifat bahan
dielektrik. Nilai kapasitansi akan sebanding
dengan besarnya konstanta dielektrik bahan.
Keberadaan bahan dielektrik yaitu
membran telur (selaput tipis berwarna putih
yang berada dalam cangkang telur) diantara
kepng sejajar dapat menyebabkan lemahnya
medan listrik diantara keping kapasitor
sehingga kapasitansinya turun.
Bahan dielektrik merupakan suatu bahan
non konduktor yang tidak mempunyai elektron
bebas, apabila diberikan suatu medan listrik
bermuatan positif dan negatif maka akan
bergerak ke arah elektroda negatif dan positif,
keadaan seperti ini disebut polarisasi (Harmen,
2001). Medan listrik diantara keping kapasitor
menjadi lemah diakibatkan oleh pengaruh
polarisasi. Frekuensi mengalami kenaikan,
maka total polarisasi berkurang dan
mengakibatkan konstanta dielektrik berkurang.
Kapasitansi Membran Telur dari Ayam
Petelur dengan Perebusan
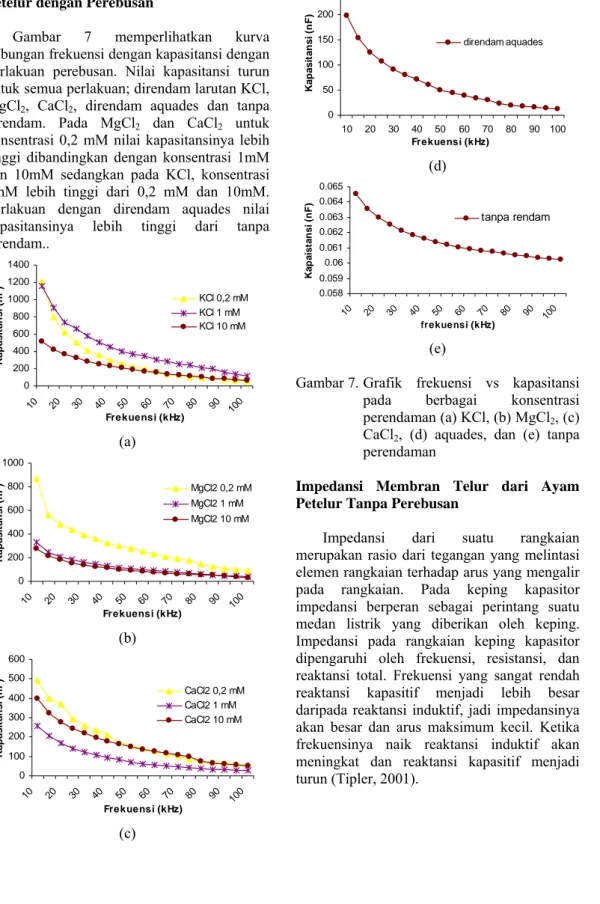
Gambar 7 memperlihatkan kurva
hubungan frekuensi dengan kapasitansi dengan
perlakuan perebusan. Nilai kapasitansi turun
untuk semua perlakuan; direndam larutan KCl,
MgCl
2, CaCl
2, direndam aquades dan tanpa
direndam. Pada MgCl
2dan CaCl
2untuk
konsentrasi 0,2 mM nilai kapasitansinya lebih
tinggi dibandingkan dengan konsentrasi 1mM
dan 10mM sedangkan pada KCl, konsentrasi
1mM lebih tinggi dari 0,2 mM dan 10mM.
Perlakuan dengan direndam aquades nilai
kapasitansinya lebih tinggi dari tanpa
direndam..
0 200 400 600 800 1000 1200 1400 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) K a p a s it a ns i (nF) KCl 0,2 mM KCl 1 mM KCl 10 mM(a)
0 200 400 600 800 1000 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) K a p a s it a ns i (nF) MgCl2 0,2 mM MgCl2 1 mM MgCl2 10 mM(b)
0 100 200 300 400 500 600 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) K ap asit an si ( n F ) CaCl2 0,2 mM CaCl2 1 mM CaCl2 10 mM(c)
0 50 100 150 200 250 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) K a p a s ita n s i (nF ) direndam aquades(d)
0.058 0.059 0.06 0.061 0.062 0.063 0.064 0.065 10 20 30 40 50 60 70 80 90 100 frekuensi (kHz) K a p a ist a n s i ( n F ) tanpa rendam(e)
Gambar
7.
Grafik frekuensi vs kapasitansi
pada berbagai konsentrasi
perendaman (a) KCl, (b) MgCl
2, (c)
CaCl
2, (d) aquades, dan (e) tanpa
perendaman
Impedansi Membran Telur dari Ayam
Petelur Tanpa Perebusan
Impedansi dari suatu rangkaian
merupakan rasio dari tegangan yang melintasi
elemen rangkaian terhadap arus yang mengalir
pada rangkaian. Pada keping kapasitor
impedansi berperan sebagai perintang suatu
medan listrik yang diberikan oleh keping.
Impedansi pada rangkaian keping kapasitor
dipengaruhi oleh frekuensi, resistansi, dan
reaktansi total. Frekuensi yang sangat rendah
reaktansi kapasitif menjadi lebih besar
daripada reaktansi induktif, jadi impedansinya
akan besar dan arus maksimum kecil. Ketika
frekuensinya naik reaktansi induktif akan
meningkat dan reaktansi kapasitif menjadi
turun (Tipler, 2001).
11
0 0.005 0.01 0.015 0.02 0.025 0.03 0.035 0.04 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Im pe da ns i (k O h m)) KCl 0,2 mM KCl 1 mM KCl 10 mM(a)
0 0.005 0.01 0.015 0.02 0.025 0.03 0.035 0.04 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Im p e da ns i (k O hm) MgCl2 0,2 mM MgCl2 1 mM MgCl 10 mM(b)
0 0.005 0.01 0.015 0.02 0.025 0.03 0.035 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Im pe da n s i ( k O h m) CaCl2 0,2 mM CaCl2 1 mM CaCl2 10 mM(c)
0 2 4 6 8 10 12 14 16 18 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Im pe da n s i (k H z ) tanpa direndam direndam aquades(d)
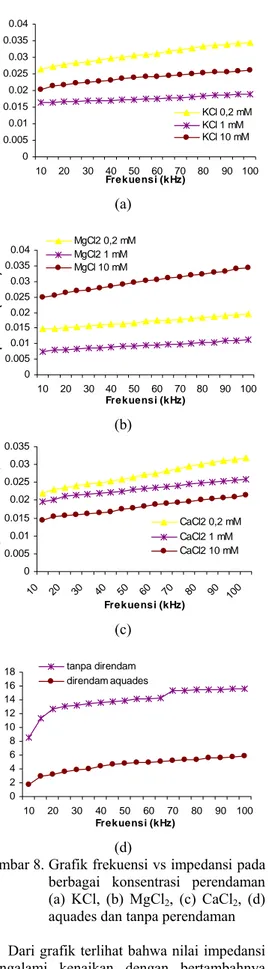
Gambar 8. Grafik frekuensi vs impedansi pada
berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d)
aquades dan tanpa perendaman
Dari grafik terlihat bahwa nilai impedansi
mengalami kenaikan dengan bertambahnya
frekuensi yang diberikan.
Pada larutan KCl dan CaCl
2dengan
konsentrasi 0,2 mM nilai kapasitansinya lebih
tinggi dari konsentrasi 1mM dan 10 mM,
sedangkan untuk larutan MgCl
2konsentrasi
yang lebih tinggi berada pada 10 mM.
Nilai impedansi tertinggi ketika tidak
diberikan perlakuan yaitu tanpa direndam
dengan aquades maupun larutan garam adalah
dari 8 kHz sampai sekitar 15,8 kHz.
Konsentrasi ion menentukan jumlah
banyaknya ion yang ada pada larutan. Pada
perebusan dan tanpa perebusan konsentrasi
tidak berhubungan dengan suatu kelinearan
pada grafik tetapi konsentrasi mempengaruhi
nilai impedansi.
Impedansi Membran Telur dari Ayam
Petelur dengan Perebusan
Dari grafik di atas kita dapat melihat
bahwa nilai impedansi naik kecuali yang tanpa
direndam yaitu nilai impedansinya menurun.
Pada KCl 0,2 mM nilainya menyimpang
dari yang lainnya yaitu ketika frenkuensinya
mencapai kira-kira 25 kHz sampai 100kHz
kenaikan impedansi signifikan dari 0,4 kOhm
sampai sekitar 2,3 kOhm.
0 0.5 1 1.5 2 2.5 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Im pe da n s i (k O h m ) KCl 0,2 mM KCl 1 mM KCl 10 mM
(a)
0 0.05 0.1 0.15 0.2 0.25 0.3 0.35 0.4 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Im p e da ns i (k O h m ) MgCl2 0,2 mM MgCl2 1 mM MgCl2 10 mM(b)
0 0.1 0.2 0.3 0.4 0.5 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Im pe da ns i (k O h m) CaCl2 0,2 mM CaCl2 1 mM CaCl2 10 mM
(c)
0 0.2 0.4 0.6 0.8 1 1.2 1.4 1.6 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Im p e da ns i ( k O h m) direndam aquades(d)
0 50 100 150 200 250 300 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Im pe da ns i ( k O hm ) tanpa rendam(e)
Gambar 9. Grafik frekuensi vs impedansi pada
berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d)
aquades dan (e) tanpa perendaman
Nilai impedansi menurun mulai dari
frekuensi 10 kHz sampai 100 kHz dengan 247
kOhm sampai sekitar 26 kOhm.
Secara umum untuk membran tanpa
perebusan dan membran dengan perebusan
menunjukkan nilai impedansi yang cenderung
naik walaupun pada sebagian perlakuan terjadi
penyimpangan. Penyimpangan-penyimpangan
tersebut disebabkan oleh keterbatasan sistem
kerja yang dilakukan selain dari pengaruh
konsentrasi dan perebusan dan tanpa
perebusan . Sistem kerja ini mempunyai
pengaruh yang cukup siknifikan apabila kerja
yang dilakukan tidak dengan hati-hati.
Loss Coefficient Membran Telur dari Ayam
Petelur Tanpa Perebusan
Persamaan (14) menerangkan bagaimana
hubungan frekuensi dan kapasitansi terhadap
loss coefficient. Frekuensi dan kapasitansi
yang besar membuat nilai loss coefficient
menjadi kecil. Bertambahnya frekuensi maka
semakn banyak energi yang ditransmisikan
dan dikonversi menjadi panas. Selain itu
berdampak pada menurunnya kemampuan
kapasitor dalam menyimpan muatan, hal ini
membuat makin banyak energi yang
dihamburkan dan dikonversi menjadi energi
lain.
0 2 4 6 8 10 12 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) L o s s C o e ff ici en t KCl 0,2 mM KCl 1 mM KCl 10 mM(a)
0 2 4 6 8 10 12 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) L o ss C o e ff ic ien t MgCl2 0,2 mM MgCl2 1 mM MgCl2 10 mM(b)
0 2 4 6 8 10 12 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) L o ss C o e ff icien t CaCl2 0,2 mM CaCl2 1 mM CaCl2 10 mM(c)
13
0 0.5 1 1.5 2 2.5 3 3.5 4 4.5 5 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) L o s s C o ef fi cien t tanpa rendam direndam aquades(d)
Gambar 10. Grafik frekuensi vs impedansi
pada berbagai konsentrasi
perendaman (a) KCl, (b) MgCl
2,
(c) CaCl
2, (d) aquades dan tanpa
perendaman
Nilai loss coefficient yang terlihat pada
gambar 10a, 10b dan 10c mengalami kenaikan
terhadap frekuensi. Semakin besar frekuensi
maka nilai loss coefficient semakin besar. Pada
perlakuan yang diberikan larutan KCl dan
MgCl
2dengan konsentrasi 10mM, loss
coffisient tertinggi yaitu mulai dari 3,4 sampai
kira-kira 9.
Untuk perlakuan yang direndam aquades
dan tanpa direndam nilai loss coeffisient
sebaliknya yaitu menurun. Ketika frekuensi
10kHz loss coffisient yang tanpa direndam
sebesar 4,3, kemudian frekuensi 20kHz loss
coeffisient menjadi 2,7 hingga frekuensi
100kHz menjadi 0,3. Rentang nilai dari
frekuensi 10kHz ke 20 kHz sebesar 1,57
sedangkan rentang nilai dari frekuensi 20kHz
ke 30 kHz sampai 100 kHz sekitar 0,03 sampai
0,59. Nilai loss coeffisient yang direndam
aquades mulai dari 4,7 sampai 0,97 dengan
frekuensi 10kHz hingga 100kHz.
Loss Coefficient Membran Telur dari Ayam
Petelur dengan Perebusan
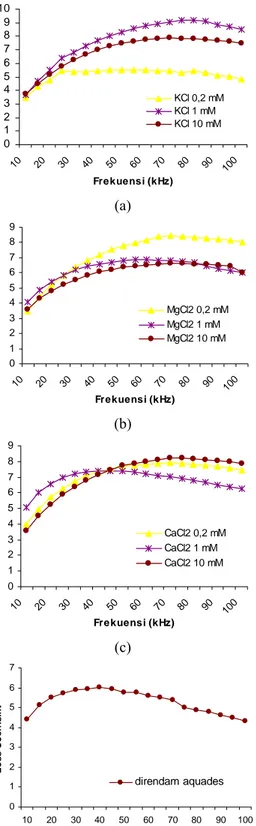
Gambar 11 memperlihatkan kurva
hubungan frekuensi dengan loss coeffisient.
Untuk membran yang direndam larutan KCl,
MgCl
2dan CaCl
2serta direndam dengan
aquades nilai coeffisient naik-turun. Contoh,
pada KCl 0,2mM nilai loss coeffisient dari
frekuensi 10 kHz – 25 kHz mengalami
kenaikan yaitu 3,4 – 5,4. Ketika frekuensi
mencapai 30 kHz nilai loss coeffisient turun
menjadi 5,38 kemudian naik lagi pada
frekuensi 35 kHz – 45 kHz sebesar 5,39 –
5,51. Pada frekuensi 55 kHz loss coeffisient
turun lagi mencapai 5,47 kemudian naik lagi
ketika frekuensi 60 kHz menjadi 5,50 kHz
selanjutnya turun lagi pada frekuensi 65 kHz
menjadi 5,428. Nilai loss coeffisient naik lagi
ketika frekuensi mencapai 70 kHz yaitu
sebesar 5,429 kemudian turun lagi pada
frekuensi 75 kHz menjadi 5,3 selanjutnya naik
lagi pada frekuensi 80 kHz menjadi 5,4 dan
turun lagi ketika frekuensi mencapai 85 kHz –
100 kHz menjadi 5,29 – 4,8.
0 1 2 3 4 5 6 7 8 9 10 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Los s C oe fi c ie nt KCl 0,2 mM KCl 1 mM KCl 10 mM(a)
0 1 2 3 4 5 6 7 8 9 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) L o ss C o e ff isi en t MgCl2 0,2 mM MgCl2 1 mM MgCl2 10 mM(b)
0 1 2 3 4 5 6 7 8 9 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) L o ss C o ef fi ci en t CaCl2 0,2 mM CaCl2 1 mM CaCl2 10 mM(c)
0 1 2 3 4 5 6 7 10 20 30 40 50 60 70 80 90 100 Frekueansi (kHz) L o ss C o ef fi si n t direndam aquades(d)
0 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) L o ss C o e ff ic ien t tanpa rendam(e)
Gamba 11. Grafik frekuensi vs loss coefficient
pada berbagai konsentrasi
perendaman (a) KCl, (b) MgCl
2, (c)
CaCl
2, (d) aquades dan (e) tanpa
perendaman
Nilai loss coeffisient untuk perlakuan
tanpa direndam menurun. Dapat dilihat dari
grafik di atas ketika frekuensi 10 kHz ke 20
kHz hingga 100 kHz. Nilai loss coeffisient
turun dari 0,069 menjadi 0,061 hingga 0,042.
Impedansi Imajiner Membran Telur dari
Ayam Petelur Tanpa Perebusan
Dari grafik dapat dilihat bahwa bentuk
grafiknya terbalik, ini menunjukkan bagian
imajiner dari impedansi. Untuk membran
yalng direndam dalam larutan garam, nilai
impedansi naik sedangkan yang direndam
aquades dan tanpa direndam nilai impedansi
menurun.
-0.012 -0.01 -0.008 -0.006 -0.004 -0.002 0 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* s in θ KCl 0,2 mM KCl 1 mM KCl 10 mM(a)
-0.008 -0.007 -0.006 -0.005 -0.004 -0.003 -0.002 -0.001 0 10 20 30 40 50 60 70 80 90 100 Frek ue ns i (kHz) Z* s in θ MgCl2 0,2 mM MgCl2 1 mM MgCl2 10 mM(b)
-0.009 -0.008 -0.007 -0.006 -0.005 -0.004 -0.003 -0.002 -0.001 0 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* s in θ CaCl2 0,2 mM CaCl2 1 mM CaCl2 10 mM(c)
-16 -14 -12 -10 -8 -6 -4 -2 0 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* s in θ tanpa direndam direndam aquades(d)
Gambar 12. Grafik frekuensi vs Z imajiner
pada berbagai konsentrasi
perendaman (a) KCl, (b) MgCl
2,
(c) CaCl
2, (d) aquades dan tanpa
perendaman
Nilai impedansi yang direndam dengan
KCl, MgCl
2, CaCl
2dan aquades lebih kecil
dari yang tanpa direndam. Ini menunjukkan
pengaruh ion-ion dari larutan garam tersebut
dan molekul air pada aquades mempengaruhi
impedansi sehingga nilainya menjadi kecil.
Impedansi Real Membran Telur dari Ayam
Petelur Tanpa Perebusan
Berdasarkan gambar 13 menunjukkan
grafiknya sama dengan impedansi yang tanpa
direbus tetapi nilai impedansinya berbeda
15
sedikit. Untuk membran yang tanpa direndam
grafiknya berbeda dengan impedansi yang
tanpa perebusan tanpa cos θ. Pada frekuensi 10
kHz – 30 kHz nilai Zcosθ naik, ketika
mencapai frekuensi 35 kHz – 100 kHz
nilainya turun sedangkan nilai impedansi yang
tanpa direbus tanpa cos θ dari frekuensi 10
kHz – 100 kHz semuanya naik, tidak
mengalami penurunan.
0 0.005 0.01 0.015 0.02 0.025 0.03 0.035 0.04 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* C os θ KCl 0,2 mM KCl 1 mM KCl 10 mM(a)
0 0.005 0.01 0.015 0.02 0.025 0.03 0.035 0.04 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* C o s θ MgCl2 0,2 mM MgCl2 1 mM MgCl2 10 mM(b)
0 0.005 0.01 0.015 0.02 0.025 0.03 0.035 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* C os Th e ta CaCl2 0,2 mM CaCl2 1 mM CaCl2 10 mM(c)
0 2 4 6 8 10 12 14 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* C os θ tanpa direndam direndam aquades(d)
Gambar 13. Grafik frekuensi vs Z real pada
berbagai konsentrasi perendaman
(a) KCl, (b) MgCl
2, (c) CaCl
2, (d)
aquades dan tanpa perendaman
Grafik diatas menunjukkan bagian real
dari impedansi. Untuk perlakuan tanpa
perebusan nilai impedansi lebih kecil
dibanding perebusan.
Impedansi Imajiner Membran Telur dari
Ayam Petelur dengan Perebusan
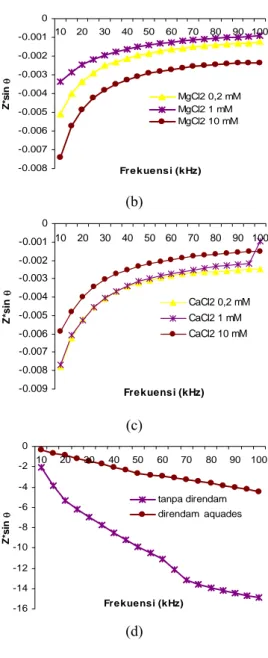
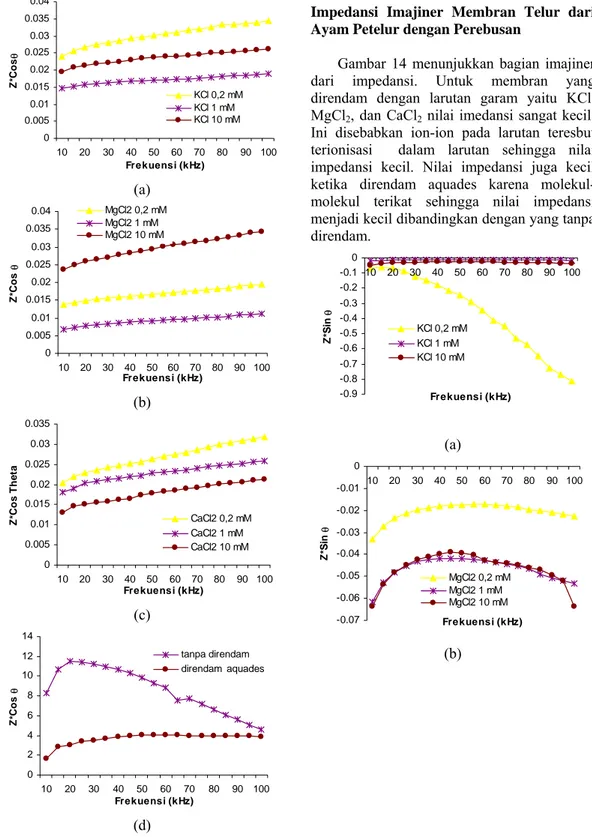
Gambar 14 menunjukkan bagian imajiner
dari impedansi. Untuk membran yang
direndam dengan larutan garam yaitu KCl,
MgCl
2, dan CaCl
2nilai imedansi sangat kecil.
Ini disebabkan ion-ion pada larutan teresbut
terionisasi dalam larutan sehingga nilai
impedansi kecil. Nilai impedansi juga kecil
ketika direndam aquades karena
molekul-molekul terikat sehingga nilai impedansi
menjadi kecil dibandingkan dengan yang tanpa
direndam.
-0.9 -0.8 -0.7 -0.6 -0.5 -0.4 -0.3 -0.2 -0.1 0 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* S in θ KCl 0,2 mM KCl 1 mM KCl 10 mM(a)
-0.07 -0.06 -0.05 -0.04 -0.03 -0.02 -0.01 0 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* S in θ MgCl2 0,2 mM MgCl2 1 mM MgCl2 10 mM(b)
-0.08 -0.07 -0.06 -0.05 -0.04 -0.03 -0.02 -0.01 0 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* S in θ CaCl2 0,2 mM CaCl2 1 mM CaCl2 10 mM
(c)
-0.4 -0.35 -0.3 -0.25 -0.2 -0.15 -0.1 -0.05 0 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* S in θ direndam aquades(d)
-300 -250 -200 -150 -100 -50 0 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* S in θ tanpa direndam(e)
Gambar 14. Grafik frekuensi vs Z imajiner
pada berbagai konsentrasi
perendaman (a) KCl, (b) MgCl
2,
(c) CaCl
2, (d) aquades dan (e)
tanpa perendaman
Membran dengan perlakuan tanpa
direndam nilai impedansi naik dari frekuensi
10 kHz – 100 kHz tidak mengalami
penurunan, berbeda dengan yang diberi
perlakuan dengan direndam larutan garam dan
aquades. Membran yang direndam larutan
garam dan aquades nilai impedansinya
naik-turun.
Impedansi Real Membran Telur dari Ayam
Petelur dengan Perebusan
Berdasarkan gambar 15 menunjukkan
grafiknya sama dengan impedansi yang
direbus tetapi nilai impedansinya berbeda
sedikit. Untuk membran yang tanpa direndam
nilai impedansi Zcos θ berbeda jauh dengan
nilai impedansi membran yang direbus tanpa
cos θ. Nilai Zcos θ lebih kecil dari impedansi
yang tanpa cos θ.
0 0.5 1 1.5 2 2.5 10 20 30 40 50 60 70 80 90 100 Frekuensi (kHz) Z* C os θ KCl 0,2 mM KCl 1 mM KCl 10 mM