PEMISAHAN PUFA YANG DIHASILKAN DARI BEBERAPA
MINYAK NABATI SECARA FRAKSINASI KOMPLEKSASI
UREA
T E S I S
Oleh
MAYURID
077006025/KM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
MEDAN
2009
SE K O L A H P A SCA S AR JANAPEMISAHAN PUFA YANG DIHASILKAN DARI BEBERAPA
MINYAK NABATI SECARA FRAKSINASI KOMPLEKSASI
UREA
T E S I S
Diajukan Sebagai Salah Satu Syarat untuk Memperoleh Gelar Magister Sains dalam Program Studi Ilmu Kimia pada Sekolah Pascasarjana Universitas Sumatera Utara
Oleh
MAYURID
077006025/KM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
MEDAN
2009
Judul Tesis : PEMISAHAN PUFA YANG DIHASILKAN DARI BEBERAPA MINYAK NABATI SECARA
FRAKSINASI KOMPLEKSASI UREA
Nama Mahasiswa : Mayurid
Nomor Pokok : 077006025
Program Studi : Kimia
Menyetujui Komisi Pembimbing
(Prof. Dr.Tonel Barus) (
Ketua
Drs. Mimpin Ginting, MS)
Anggota
Ketua Program Studi, Direktur,
(Prof. Basuki Wirjosentono, MS, Ph.D) (Prof. Dr. Ir. T. Chairun Nisa. B, MSc
Tanggal lulus : 22 Juni 2009
Telah diuji pada Tanggal 22 Juni 2009
PANITIA PENGUJI TESIS
Ketua : Prof. Basuki Wirjosentono, M.S, Ph.D
Anggota : 1. Prof.Dr. Tonel Barus
2. Drs Mimpin Ginting, M.S 3. Prof. Dr. Jamaran Kaban, M.Sc 4. Dr. Lamek Marpaung, M.Sc
PERNYATAAN
PEMISAHAN PUFA YANG DIHASILKAN DARI BEBERAPA
MINYAK NABATI SECARA FRAKSINASI KOMPLEKSASI
UREA
TESIS
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan sepanjang pengetahuan juga tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Medan, 22 Juni 2009 Penulis,
ABSTRAK
Pemanfaatan minyak baik sebagai edible oil maupun sebagai bahan oleokimia sangat tergantung kepada jenis asam lemak yang terikat pada gliserida tersebut. Minyak dengan kandungan asam lemak tidak jenuh seperti linoleat, linolenat dan oleat memiliki kegunaan tersendiri dimana dalam edible oil linolenat bermanfaat dalam kesehatan sedangkan linoleat dan oleat meningkatkan cita rasa pada makanan, demikian juga halnya pemanfaatan ketiga jenis asam lemak tersebut dalam oleokimia memiliki kegunaan yang berbeda.
Dalam penelitian ini dilakukan peningkatan konsentrat PUFA yakni linoleat dan linolenat dari asam lemak lainnya terhadap asam lemak yang terdapat pada minyak kemiri, kedelai dan minyak jarak pagar yang dilakukan melalui tahapan saponifikasi, netralisasi dilanjutkan fraksinasi kompleksasi urea.
Hasil penelitian ini berdasarkan analisis kromatografi gas terhadap metil ester asam lemak menunjukkan bahwa setelah fraksinasi kompleksasi urea terjadi adanya kenaikan PUFA ( C18:2 dan C18:3 ) pada minyak kemiri sebesar 60,04 %, minyak kedelai sebesar 52,89 % dan minyak jarak pagar sebesar 73,40 %.
Kata Kunci : PUFA, minyak kemiri, minyak kedelai, minyak jarak pagar, kompleksai urea
ABSTRACT
The use of oil as edible oil or as material for oleochemistry is defended to the kind of fat orchid that closed to the gliserida. Oil with containing fat orchid is not stagnant like linoleic, linolenic and oleic have the use it self where in edible oil linoleic is advantage in health while linoleic and oleic is used for the nice of food, And also with advantages of the three kind of the fat orchid but oleochemistry has the difference uses .
In this this research we developed thes uses of concentrate of PUFA like linoleic and linolenic from other fat orchid to the fat orchid that there is in cadle nuts oil, soya bean oil and castor oil which are done through some. Steps safonification, netralisation that is going on to fracsination urea complecity.
The result of this research is based on cromatografi gas to metal ester, orchid fat shows that after fracsination complexcity urea is happened in the developing of PUFA ( C18 : 2 and C18 : 3 ) to the caddle nuts about 60,04 %, soyabean oil is about 52,89 % and castor oil is about 73,40 %.
Key Word : PUFA, cadle nuts oil, soyabean oil , castor oil, urea complekxation
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah memberikan rahmad dan karuniannya, sehingga penulis dapat menyelesaikan tesis yang berjudul : Pemisahan
PUFA yang dihasilkan dari beberapa minyak nabati secara fraksinasi
kompleksasi urea.
Tesis ini disusun sebagai syarat untuk memperoleh gelar Magister Sain pada sekolah pasca sarjana Universitas Sumatera Utara. Penulis menyadari bahwa tesis ini masih jauh dari kesempurnaan.Pada kesempatan ini penulis dengan kerendahan hati sangat mengharapkan kritik dan saran.
Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada BAPEDDA Sumatera Utara yang telah memberikan beasiswa kepada penulis untuk dapat menempuh strata pendidikan S 2 ini. Terima kasih keada Rektor Sumatera Utara Bapak Prof..Chairuddin P.Lubis, DTM & H,Sp.A(K) atas kesempatan dan fasilitas yang telah diberikan kepada penulis untuk mengikuti pendidikan.Terima kasih kepada Direktur Sekolah Pascasarjana ibu Prof.Dr.Ir.Chairun Nisa B, M.Sc. Terima kasih kepada ketua program studi kimia Bapak Prof.Basuki Wirjosentono, M.S, Ph.D.
Terima kasih yang sebesar-besarnya dan penghargaan yang setinggi-tingginya kepada :
1. Prof .Dr. Tonel Barus selaku dosen pembimbing utama dan Drs Mimpin Ginting M.S selaku anggota komisi pembimbing yang setiap saat dengan penuh perhatian memberikan bimbingan dan saran sehingga tesis ini dapat diselesaikan.
2. Kepada kepala laboratorium kimia organik dan kimia bahan bahan alam FMIPA USU Medan beserta staf dan asisten atas fasilitas dan sarana yang diberikan
3. Kepala laboratorium RISPA Medan atas bantuannya dalam menganalisis sampel.
4. Ketua yayasan Hajjah Rachmah Nasution H. Abdul Manan Muis yang telah memberikan izin kepada penulis untuk pendidikan dalam program studi kimia pada pasca sarjana Universitas Sumatera Utara. 5. Rekan-rekan program studi kimia pada sekolah pasca sarjana
Universitas Sumatera Utara dan rekan-rekan seprofesi al Azhar Medan yang namanya tidak mungkin disebutkan satu per satu, atas segala bentuk bantuan yang penulis terima selama mengikuti pendidikan. Akhirnya saya mengucapkan terima kasih yang setinggi-tingginya kepada ayahanda Usman Amin ( Alm ) dan ibunda tercinta Aisyah Yusuf B.A ( Almh ), Istri tercinta Rosmayanna siregar S.Pd, ananda M.Ali Azzahri dan Azimah Azzahra dan seluruh keluarga yang dengan penuh kasih sayang memberikan dorongan dan doa sehingga penulis dapat menyelesaikan pendidikan.
Akhir kata penulis harapkan semoga tulisan ini bermanfaat bagi perkembangan ilmu kimia. Semoga Allah SWT meridhoi kita .Amin.
Medan, 22 Juni 2009 Penulis
RIWAYAT HIDUP
Penulis dilahirkan di Sigli pada tanggal 27 April 1972 dan anak kedua dari tiga bersaudara dari pasangan Usman Amin ( Alm ) dan Aisyah Yusuf B.A ( Almh ). Penulis menamatkan pendidikan dasar di Madrasah Ibtidaiyah Negeri Medan ( MIN Medan ) dari tahun 1979 sampai tahun 1985, Sekolah Menengah Negeri ( SMP N ) 6 medan dari tahun 1985 samapi tahun 1988, Sekolah Menengah Atas Negeri (SMAN ) 1 Sigli dari tahun 1988 sampai tahun 1991.
Penulis melanjutkan pendidikan sarjana di IKIP Negeri Medan dari tahun 1992 sampai tahun 1998.pada tahun 2007 penulis mendapatkan kesempatan untuk melanjutkan studi melalui beasiswa pemerintah Sumatera Utara di USU Medan dengan program studi pasca sarjana kimia dan menamatkan pendidikan tersebut pada bulan Juni 2009 di Medan.
DAFTAR ISI
Halaman
ABSTRAK... i
ABSTRACT... ii
KATA PENGANTAR... iii
RIWAYAT HIDUP... vi
DAFTAR ISI... vii
DAFTAR TABEL... x
DAFTAR GAMBAR... xi
DAFTAR LAMPIRAN ... xii
BAB I PENDAHULUAN... 1 1.1. Latar Belakang... 1 1.2. Permasalahan... 3 1.3. Tujuan Penelitian... 3 1.4. Manfaat Penelitian... 3 1.5. Metode Penelitian... 4
BAB II TINJAUAN PUSTAKA... 5
2.1. Kemiri ( Aleurites moluccana) ... 5
2.1.1.Komposisi Minyak Kemiri... 5
2.2.1.Komposisi Minyak Jarak pagar... 6
2.3. Kedelai ( Glycine max L )... 7
2.3.1.Komposisi Minyak Kedelai... 8
2.4. Asam Lemak... 9
2.5. Beberapa Asam Lemak Penyusun Gliserida... 10
2.6.Klasifikasi Asam Lemak... 12
2.6.1 Kegunaan asam lemak tak jenuh... 16
2.6.2. Pemisahan Asam Lemak Dalam Industri... 16
2.7. Kompleksasi Urea... 23
2.8. Kromatografi Gas Cair... 25
BAB III METODELOGI PENELITIAN... 35
3.1. Lokasi Penelitian... 35
3.2. Bahan dan Alat... 35
3.3. Prosedur Penelitian... 36
3.3.1.Isolasi Minyak Kemiri dari Inti Biji Kemiri... 36
3.3.2.Isolasi Minyak Jarak dari Inti Biji Jarak... 36
3.3.3.Isolasi Minyak Kedelai dari Inti Biji Kedelai... 37
3.4. Pemisahan PUFA dari masing-masing minyak Nabati... 37
3.4.1.Minyak Kemiri... 37
3.4.2.Minyak Jarak... 38
3.5. Bagan Penelitian... 40
3.5.1 Isolasi Minyak dari Inti Biji Kemiri, Kedelai dan Jarak Pagar ... 40
3.5.2. Pemisahan PUFA dari masing-masing minyak Nabati... 41
BAB IV HASIL DAN PEMBAHASAN... 43
4.1 Hasil Penelitian ... 43
4.1.1.Isolasi Minyak Kemiri, Kedelai dan Jarak Pagar... 43
4.1.2.Hasil Analisis Kromatografi Gas Cair ( KGC ) Sebelum Kompleksasi Urea... 43
4.1.3.Hasil Analisis Kromatografi Gas Cair ( KGC ) setelah kompleksasi urea... ... 46
4.2. Pembahasan ... 49
4.2.1. Isolasi Minyak Kemiri, Kedelai dan Jarak Pagar... 49
4.2.2. Isolasi PUFA dari asam lemak lainnya... 52
4.2.3.Hasil Analisis Kromatografi Gas Cair ( KGC ) ... 55
BAB V KESIMPULAN DAN SARAN... 58
5.1. Kesimpulan... 58
5.2. Saran ... 58
DAFTAR TABEL
Nomor Judul Halaman
1. Komposisi Asam Lemak ( % ) Minyak Kemiri... 6
2. Komposisi Asam Lemak ( % ) Minyak Jarak... 6
3. Komposisi Asam Lemak ( % ) Minyak Kedelai... 8
4. Jenis-jenis Asam Lemak... 11
5. Titik Beku Beberapa Asam Lemak ... 12
6. Hasil Perolehan Minyak Kemiri, Kedelai dan Jarak Pagar... 43
7. Hasil analisis KGC dari Komposisi Asam Lemak minyak Kemiri... 44
8. Hasil analisis KGC dari Komposisi Asam Lemak minyak kedelai... 45
9. Hasil analisis KGC dari Komposisi Asam Lemak minyak Jarak Pagar... 46
10. Hasil analisis KGC dari Komposisi Asam Lemak minyak Kemiri setelah Kompleksasi urea... 47
11. Hasil analisis KGC dari Komposisi Asam Lemak minyak Kedelai setelah Kompleksasi urea... 48
12. Hasil analisis KGC dari Komposisi Asam Lemak minyak Jarak Pagar setelah Kompleksasi urea... 49
DAFTAR GAMBAR
Nomor Judul Halaman
1. Struktur Kimia Asam Laurat... 13
2. Struktur Kimia Asam Oleat... 14
3. Struktur Kimia Asam Linolenat... 14
4. Reaksi antara asam lemak dengan NaOH... 17
5. Reaksi Penyabunan Mono dan Digliserida dalam Minyak... 19
6. Skema alat penyuling asam lemak bebas... 20
7. Reaksi re-esterifikasi dengan mono dan digliserida... 22
8. Kompleks Inklusi Urea... 24
9. Diagram alir Kromatografi gas cair... 26
10. Output dari kolom... 31
11. Area Puncak... 33
12. Reaksi Penyabunan Terhadap Trigliserida... 50
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Kromatogram dari Komposisi Asam Lemak Minyak
KemiriSebelumKompleksasi Urea... ... 61 2. Kromatogram dari Komposisi Asam
LemakMinyakKedelaiSebelumKompleksasi Urea... 62 3 Kromatogram dari Komposisi Asam Lemak Minyak Jarak Pagar
Sebelum Kompleksasi Urea... ... 63 4 Kromatogram dari Komposisi Asam Lemak Minyak Kemiri
Setelah Kompleksasi Urea... 64 5. Kromatogram dari Komposisi Asam Lemak Minyak Kedelai
SetelahKompleksasi Urea... 65 6. Kromatogram dari Komposisi Asam Lemak Minyak Jarak Pagar
BAB I
PENDAHULUAN
1.1. Latar Belakang
Pemanfaatan lemak/minyak baik sebagai edible oil maupun sebagai bahan oleokimia sangat tergantung kepada jenis asam lemak yang terdapat pada gliserida tersebut. Minyak yang kaya akan kandungan asam lemak jenuh menengah seperti minyak kelapa maupun minyak inti sawit banyak digunakan sebagai edible oil sedangkan lemak dengan kandungan asam lemak jenuh rantai panjang yang tinggi banyak digunakan sebagai bahan oleokimia ( Richter dan Knaut,1984 ).
Minyak dengan kandungan asam lemak tidak jenuh tinggi ( PUFA) seperti asam lemak oleat, linolenat dan omega 3 memiliki kegunaan tersendiri seperti asam lemak linolenat sangat bermanfaat dalam kesehatan dan asam linoleat meningkatkan rasa yang enak bagi konsumen ( Knight,1976 ).
Penggunaan dari asam lemak tak jenuh (PUFA) dalam industri kosmetika maupun industri lainnya memiliki kegunaan tersendiri seperti : pembuatan senyawa poliol, bahan cat, pernis, sabun, obat-obatan dan sebagai bahan baku senyawa polimer yakni poliuretan, polietilen, polipropilen, poliisoprena dan lain-lain ( Ketaren.S, 2005).
Asam lemak tak jenuh termasuk asam lemak esensial, artinya asam lemak yang tidak dapat disintesis dalam tubuh manusia, tetapi harus didatangkan dari luar tubuh. Asam lemak tak jenuh yang mengandung satu ikatan rangkap disebut asam lemak tidak jenuh mono ( Mono Unsaturated Fatty Acid, MUFA ) sedangkan yang
mengandung dua atau lebih ikatan rangkap disebut asam lemak tidak jenuh poli ( Poli
Unsaturated Fatty Acid, PUFA ).
Pemisahan asam lemak jenuh seperti laurat, palmitat dan stearat dalam industri oleokimia dapat dilakukan ke dalam bentuk tunggal melalui destilasi fraksinasi terhadap campuran asam lemak ataupun dalam bentuk metil ester asam lemak campuran. Peningkatan Poly Unsaturated Fatty Acid (PUFA) melalui cara destilasi fraksinasi ini sukar dilakukan disebabkan masing-masing asam lemak tak jenuh disamping membentuk campuran yang azetrop juga dapat mengalami perubahan komposisi. Usaha pemisahan PUFA telah dilakukan melalui fraksinasi menggunakan pelarut dan juga destilasi menggunakan destilasi molekuler, disamping adanya yang terdegradasi ternyata pemisahan PUFA tidak dapat dilakukan dengan sempurna. Pemisahan PUFA melalui fraksinasi kompleksasi urea, diharapkan kandungan asam lemak tak jenuh majemuknya dapat ditingkatkan tanpa mengalami degradasi seperti yang dilakukan terhadap pemisahan PUFA dari minyak ikan antara asam lemak tersebut dapat dipisahkan antara asam lemak lainnya.
Asam lemak dari minyak nabati yang kaya akan oleat, linoleat dan linolenat diharapkan melalui kompleksasi urea secara fraksinasi dapat dipisahkan atau ditingkatkan konsentrasinya dari asam lemak campuran lainnya.
Beberapa minyak nabati diantaranya minyak kemiri, minyak jarak dan minyak kedelai yang mudah diperoleh memiliki kandungan asam lemak tidak jenuh yang besar dan berbeda satu sama lain komposisinya.
Berdasarkan hal tersebut di atas peneliti tertarik untuk memisahkan asam lemak tak jenuh majemuk (PUFA) dari asam lemak lainnya yang ada dalam minyak kemiri, minyak jarak dan minyak kedelai dengan cara fraksinasi kompleksasi urea
1.2. Permasalahan
Apakah asam lemak tak jenuh majemuk (PUFA) yang diperoleh dari minyak kemiri, minyak jarak pagar dan minyak kedelai dapat ditingkatkan konsentrasinya melalui fraksinasi kristalisasi secara kompleksasi urea
1.3 Tujuan Penelitian
Penelitian ini bertujuan untuk meningkatkan jumlah asam lemak tak jenuh majemuk (PUFA) terhadap asam lemak lainnya yang diperoleh dari minyak kemiri,minyak jarak pagar dan minyak kedelai.
1.4 Manfaat Penelitian
Metode kompleksasi urea yang digunakan untuk memisahkan atau meningkatkan jumlah asam lemak tak jenuh majemuk (PUFA) dari minyak kemiri, minyak jarak pagar dan minyak kedelai memberikan konstribusi besar untuk pemanfaatan berbagai asam lemak untuk meningkatkan nilai ekonomis dari suatu minyak tertentu .
Juga dapat memberikan informasi terhadap industri oleokimia bahwa melalui metode kompleksasi urea secara fraksinasi dapat ditingkatkan konsentrat asam lemak tak jenuh yang terdapat pada minyak nabati seperti minyak kemiri, minyak kedelai dan minyak jarak pagar.
1.5.Metode Penelitian
Penelitian ini adalah eksperimen laboratorium. Biji kemiri, biji jarak pagar dan biji kedelai yang digunakan diambil diperoleh dari pasar lokal yang ada di kota Medan. Biji kemiri, biji jarak pagar dan biji kedelai yang kering dan halus ( Milt ) dimaserasi dengan pelarut n-heksana untuk mendapatkan minyak. Selanjutnya masing-masing minyak yang diperoleh ditentukan komposisi asam lemaknya dalam bentuk metil ester asam lemak ( MEAL ) melalui analisis KGC.
Minyak kemiri, minyak kedelai dan minyak jarak pagar yang diperoleh dari maserasi setelah disaponifikasi dilanjutkan hidrolisis selanjutnya dilakukan pemisahan jenis asam lemak tak jenuh majemuknya ( PUFA) dari asam lemak lainnya melalui fraksinasi dengan kompleksasi urea. Selanjutnya asam lemak dari minyak kemiri, minyak kedelai dan minyak jarak pagar yang telah difraksinasi dengan kompleksasi urea dilakukan analisis KGC kembali untuk dibandingkan dengan hasil analisis KGC dari minyak kemiri, minyak kedelai dan minyak jarak pagar sebelum dilakukan fraksinasi kompleksasi urea.
BAB II
TINJAUAN PUSTAKA
2.1. Kemiri ( Aleurites moluccana )
Tanaman kemiri ( aleurites moluccana ) berpohon besar dengan tinggi 25-40 meter, beranting banyak, mempunyai tunas muda yang tertutup rapat oleh bulu yang berwarna putih keabu-abuan atau cokelat. Daun muda berlekuk tiga atau lima, sedang daun tua berbentuk bulat dengan ujung meruncing. Daun tersebut mempunyai kelenjar berwarna hijau kekuningan.bunga kemiri merupakan bunga majemuk yang berumah satu, berwarna putih dan bertangkai pendek. Buah kemiri berkulit keras berdiameter 5 cm didalamnya terdapat satu atau dua biji yang diselubungi kulit biji yang keras dengan permukaan kasar dan beralur. Tanaman kemiri baik tumbuh dipegunungan pada ketinggian 1200 meter dari permukaan laut ( Sunanto H, 1994 ).
2.1.1. Komposisi Minyak Kemiri
Setiap 100 g daging biji kemiri mengandung 636 kalori, 19 g protein, 63 g lemak, 8 g karbohidrat, 80 mg kalsium, 200 mg fosfor, 2 mg besi, 0,06 mg vitamin B dan 7 g air. Bagian biji mengandung minyak sebesar 55-56 % dan kadar minyak dalam daging buah sebesar 60 %. Asam lemak minyak ditunjukkan tabel di bawah ini.
Tabel 1. Komposisi asam lemak ( % ) minyak kemiri
Asam Lemak Jumlah ( % )
Asam linolenat 28,5
Asam oleat 10,5
Asam linoleat 48,5
Asam palmitat 55
Asam stearat 6,7
Sumber : Bailey, A.E (1950 )
2.2. Jarak Pagar (Jatropa curcas linn)
Biji jarak pagar (Jatropa curcas linn) merupakan sumber minyak nabati. Biji jarak diperoleh dari pohon jarak yang menghasilkan biji. Biji jarak pagar terdiri dari 60 % berat kernel (daging biji) dan 40 % berat kulit. Inti biji jarak pagar mengandung sekitar 50 % minyak sehingga dapat diekstrak menjadi minyak jarak pagar dengan cara mekanis ataupun ekstraksi dengan pelarut organik seperti heksana (Hambali, dkk., 2006).
2.2.1.Komposisi Minyak Jarak pagar
Biji jarak terdiri dari 75 persen kernel (daging biji) dan 25 persen kulit dengan komposisi sebagai berikut :
Tabel 2. Komposisi asam lemak ( % ) minyak jarak
Asam Lemak Jumlah ( % )
Asam linolenat 2 – 4 Asam oleat 35 – 64 Asam linoleat 19 – 42 Asam palmitat 2 – 17 Asam stearat 5 – 10 Sumber : Sudrajat.R (2006)
Minyak jarak pagar mempunyai keunikan tersendiri karena komponen penyusun utamanya adalah 77,3 % asam lemak tak jenuh yaitu oleat (C18 :1) , linoleat (C18:2) dan linolenat ( C18:3 ).
Minyak jarak pagar dan turunannya digunakan dalam industri cat, varnish, pelumas, tinta cetak, linoleum, oil cloth dan sebagai bahan baku dalam industri-industri plastik dan nilon. Dalam jumlah kecil minyak jarak digunakan dalam pembuatan kosmetik, semir dan lilin.
2.3. Kedelai ( Glycine max L )
Kedelai adalah tanaman semusim yang biasa diusahakan pada musim kemarau,karena tidak memerlukan air dalam jumlah besar. Umumnya kedelai tumbuh didaerah ketinggian 0 sampai 500 m dari permukaan laut. Berdasarkan klasifikasi botani,kedelai termasuk famili Leguminosae. Tanaman kedelai tumbuh tegak sedangkan kedelai liar tumbuh menjalar. Kedelai termasuk tanaman berbiji ganda, berakar tunggang. Pada akhir tumbuh bintil-bintil akar yang berisi Rizobium japanicum yang dapat mengikat nitrogen dari udara. Rizobium japanicum hidup bersimbiose dengan kedelai dan membantu sintesa protein kedelai.Bunga kedelai disebut bunga kupu-kupu yang biasa bergerombol dibawah ketiak daun dengan jumlah bunga 13-15 buah, tetapi 75 persen dari bunga ini sering gugur (Atjung,1990).
2.3.1. Komposisi Minyak Kedelai
Kadar minyak kedelai relatif lebih rendah dibandingkan dengan jenis kacang-kacangan lainnya, tetapi lebih tinggi daripada kadar minyak serealia. Kadar protein kedelai yang tinggi menyebabkan kedelai lebih banyak digunakan sebagai sumber potein daripada sebagai sumber minyak. Asam lemak minyak kedelai sebagian besar terdiri dari asam lemak esensial yang sangat dibutuhkan oleh tubuh. Adapun komposisi minyak kedelai sebagai berikut.
Tabel 3. Komposisi asam lemak ( % )minyak kedelai
Asam Lemak Jumlah ( % )
Asam lemak tidak jenuh (85 %)
-asam linoleat 15 – 64
-asam oleat 11 – 60
-asam linolenat 1 – 12
-asam arachidonat 1,5
Asam lemak jenuh (15 %)
- asam palmitat 7 – 10
- asam stearat 2 – 5
- asam arschidat 0,2 – 1
- asam laurat 0 – 0,1
Sumber : Bailey A.E (1950)
Minyak kedelai banyak digunakan untuk pembuatan minyak salat, minyak goreng, serta untuk segala keperluan pangan.Lebih dari 50 % produk pangan dibuat dari minyak kedelai, terutama margarin dan shortening. Hampir 90 % dari produksi minyak kedelai digunakan dibidang pangan. Minyak kedelai juga digunakan pada pabrik lilin, sabun, varnish, cat, semir, insektisida dan desinfektan.
2.4 Asam Lemak
Asam lemak bersama-sama dengan gliserol sebagai gliserida merupakan
penyusun utama minyak nabati atau lemak dan merupakan bahan baku untuk semua lipida pada makhluk hidup. Asam ini mudah dijumpai dalam minyak makan (goreng), margarin, atau lemak hewan dan menentukan nilai gizinya. Secara alami, asam lemak bisa berbentuk bebas ( karena lemak yang terhidrolisis ) maupun terikat sebagai
gliserida.
Asam lemak tidak lain adalah asam alkanoat atau asam karboksilat berderajat
tinggi ( rantai C lebih dari 6 ). Karena berguna dalam mengenal ciri-cirinya, asam lemak dibedakan menjadi asam lemak jenuh dan asam lemak tak jenuh. Asam lemak
jenuh hanya memiliki ikatan tunggal di antara atom-atom karbon penyusunnya, sementara asam lemak tak jenuh memiliki paling sedikit satu ikatan ganda di antara atom-atom karbon penyusunnya.
Asam lemak merupakan asam lemah dan dalam air terdisosiasi sebagian. Umumnya berfase cair atau padat pada suhu ruang (27° C ). Semakin panjang rantai C penyusunnya, semakin mudah membeku dan juga semakin sukar larut dalam pelarut polar.
Asam lemak jenuh bersifat lebih stabil (tidak mudah bereaksi) daripada asam lemak tak jenuh. Ikatan ganda pada asam lemak tak jenuh mudah bereaksi dengan oksigen ( mudah teroksidasi ). Karena itu, dikenal istilah bilangan oksidasi bagi asam lemak.
Keberadaan ikatan ganda pada asam lemak tak jenuh menjadikannya memiliki dua bentuk: cis dan trans. Semua asam lemak nabati alami hanya memiliki bentuk
cis. Asam lemak bentuk trans ( trans fatty acid, dilambangkan dengan "E", hanya
diproduksi oleh sisa metabolisme hewan atau dibuat secara sintetis. Akibat polarisasi atom H, asam lemak cis memiliki rantai yang melengkung. Asam lemak trans karena atom H-nya berseberangan tidak mengalami efek polarisasi yang kuat dan rantainya tetap relatif lurus.
Ketengikan (Ingg. rancidity) terjadi karena asam lemak pada suhu ruang dirombak akibat hidrolisis atau oksidasi menjadi hidrokarbon, alkanal, atau keton,
serta sedikit epoksi dan alkohol (alkanol). Bau yang kurang sedap muncul akibat campuran dari berbagai produk ini ( Ketaren S, 2005 ).
2.5. Beberapa asam lemak Penyusun Gliserida
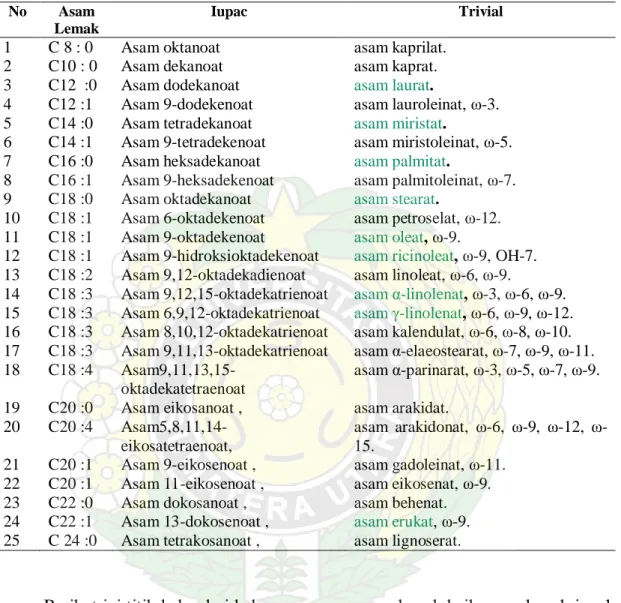
Berdasarkan panjang rantai atom karbon (C), berikut sejumlah asam lemak alami (bukan sintetis) yang dikenal. Nama yang disebut lebih dahulu adalah nama sistematik dari IUPAC dan diikuti dengan nama trivialnya.
Tabel 4. Jenis-jenis asam lemak
No Asam
Lemak
Iupac Trivial
1 C 8 : 0 Asam oktanoat asam kaprilat. 2 C10 : 0 Asam dekanoat asam kaprat. 3 C12 :0 Asam dodekanoat asam laurat.
4 C12 :1 Asam 9-dodekenoat asam lauroleinat, ω-3. 5 C14 :0 Asam tetradekanoat asam miristat.
6 C14 :1 Asam 9-tetradekenoat asam miristoleinat, ω-5. 7 C16 :0 Asam heksadekanoat asam palmitat.
8 C16 :1 Asam 9-heksadekenoat asam palmitoleinat, ω-7. 9 C18 :0 Asam oktadekanoat asam stearat.
10 C18 :1 Asam 6-oktadekenoat asam petroselat, ω-12. 11 C18 :1 Asam 9-oktadekenoat asam oleat, ω-9.
12 C18 :1 Asam 9-hidroksioktadekenoat asam ricinoleat, ω-9, OH-7. 13 C18 :2 Asam 9,12-oktadekadienoat asam linoleat, ω-6, ω-9.
14 C18 :3 Asam 9,12,15-oktadekatrienoat asam α-linolenat, ω-3, ω-6, ω-9. 15 C18 :3 Asam 6,9,12-oktadekatrienoat asam γ-linolenat, ω-6, ω-9, ω-12. 16 C18 :3 Asam 8,10,12-oktadekatrienoat asam kalendulat, ω-6, ω-8, ω-10. 17 C18 :3 Asam 9,11,13-oktadekatrienoat asam α-elaeostearat, ω-7, ω-9, ω-11. 18 C18 :4
Asam9,11,13,15-oktadekatetraenoat
asam α-parinarat, ω-3, ω-5, ω-7, ω-9. 19 C20 :0 Asam eikosanoat , asam arakidat.
20 C20 :4 Asam5,8,11,14-eikosatetraenoat,
asam arakidonat, 6, 9, 12, ω-15.
21 C20 :1 Asam 9-eikosenoat , asam gadoleinat, ω-11. 22 C20 :1 Asam 11-eikosenoat , asam eikosenat, ω-9. 23 C22 :0 Asam dokosanoat , asam behenat. 24 C22 :1 Asam 13-dokosenoat , asam erukat, ω-9.
25 C 24 :0 Asam tetrakosanoat , asam lignoserat.
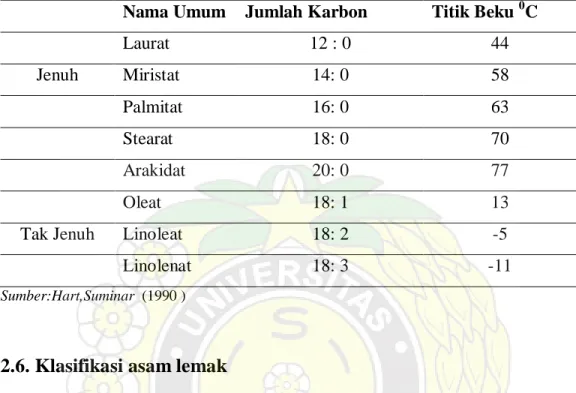
Berikut ini titik beku dari beberapa asam –asam lemak baik asam lemak jenuh maupun asam lemak tak jenuh. dapat dilihat dari tabel 5
Tabel 5. Ttitik beku beberapa asam lemak
Nama Umum Jumlah Karbon Titik Beku 0C
Laurat 12 : 0 44 Jenuh Miristat 14: 0 58 Palmitat 16: 0 63 Stearat 18: 0 70 Arakidat 20: 0 77 Oleat 18: 1 13
Tak Jenuh Linoleat 18: 2 -5
Linolenat 18: 3 -11
Sumber:Hart,Suminar (1990 )
2.6. Klasifikasi asam lemak
Agar supaya para pembaca menjadi lebih mudah mengerti soal minyak, maka perlu untuk mengetahui beberapa istilah perminyakan yang akan dipakai untuk menjelaskan uraian dibawah ini. Apakah bedanya antara lemak dan minyak? Istilah lemak dan minyak sering kali dipakai secara serabutan. Secara harafiah perbedaan yang sebenarnya adalah, lemak akan tetap berbentuk padat (solid) pada suhu kamar; contoh, Lemak hewani, “lard” (gajih), sedangkan minyak akan tetap berbentuk cair (liquid); contoh, minyak sayur, seperti asal jagung, kedele, biji bunga matahari, biji kapok, canola dll). Padahal keduanya adalah termasuk golongan lemak dan dalam istilah ilmu kimia disebut fats (gajih) atau fatty acids (asam lemak). Lemak jenuh (gajih) adalah trigleserida (triglyceride), demikian pula lemak tak jenuh (minyak
sayur) adalah trigleserida juga.Setiap molekul trigleserida mengandung 3 Molekul asam lemak.
Berdasarkan ada atau tidaknya ikatan ganda (double bonds) dalam struktur kimiawinya, molekul asam-asam lemak yang terkandung dalam trigleserida, asal lemak atau minyak dapat dibagi menjadi 3 kelompok; yakni (1) Golongan minyak dengan asam lemak jenuh (saturated fatty acids), (2) Golongan minyak dengan asam lemak tak Jenuh tunggal (mono-unsaturated fatty acids, MUFA ) dan (3) Golongan minyak dengan asam lemak tak jenuh majemuk ( Poly - unsaturated fatty acids, PUFA ).
ContohJenis-jenisAsamLemak
Saturated Fatty Acid (SFA = Asam Lemak Jenuh)
O
HO
lauric acid
Gambar 1.Struktur kimia asam laurat
Asam lemak jenuh, asam laurat (lauric acid) terdiri dari 12 atom karbon, yang diikat jenuh oleh atom hidrogen dan tidak ada ikatan ganda. Asam lemak ini tergolong asam lemak rantai sedang (medium, MCFA) dan banyak ditemukan dalam air susu ibu dan minyak kelapa.
O
OH
oleic acid
Gambar 2.Struktur kimia asam oleat
Asam lemak tak jenuh tunggal, asam oleat (oleic acid) terdiri dari 18 atom karbon di mana 1 pasang karbon atom diganti oleh satu ikatan ganda dan asam lemak ini tergolong dalam asam lemak rantai panjang (LCFA) serta kebanyakan ditemukan dalam minyak sayur seperti kedele dan canola.
Poly-Unsaturated Fatty Acid (PUFA = Asam lemak tak Jenuh majemuk)
O
OH
linoleic acid
Asam lemak tak jenuh ganda, asam lenoleat (linoleic acid) terdiri dari 18 atom karbon dengan 2 ikatan ganda (majemuk) dan tergolong dalam asam lemak rantai panjang (LCFA) serta banyak ditemukan pada minyak sayur seperti kedele, jagung dan canola.
Perlu diketahui pula, bahwa asam lemak juga bisa dibedakan berdasarkan panjang rantai atom karbon, dengan demikian bisa dibagi lagi menjadi 3 kelompok : 1. Golongan minyak dengan asam lemak rantai karbon pendek (Short Chain Fatty Acids=SCFA), terdiri dari 2-6 atom karbon saja, seperti asam cuka dan asam mentega.
2. Golongan minyak dengan asam lemak rantai karbon sedang (medium) (Medium Chain Fatty Acids=MCFA), terdiri dari 8-16 atom karbon, seperti minyak kelapa, minyak sawit dan minyak palm
3. Golongan minyak dengan asam lemak rantai karbon panjang (Long Chain Fatty Acids = LCFA), yang terdiri dari 18 atau lebih atom karbon. Semua jenis minyak sayur yang sekarang dijual di pasaran adalah tergolong dalam LCFA.
Perbedaan dalam ketiga jenis golongan asam lemak berantai karbon ini mempunyai proses pencernaan dan metabolisme didalam tubuh yang berbeda dan menghasilkan produk2 komponen zat bioaktif yang sangat berbeda pula. Maka setiap jenis golongan asam lemak mempunyai dampak fisiologis dan biologis yang sangat berbeda pula terhadap kesehatan kita ( Wibraham.dkk, 2005 ).
2.6.1 Kegunaan Asam Lemak Tak Jenuh
PUFA dilihat dari edible oil sangat bermanfaat buat kesehatan terhadap tubuh diantaranya akan membantu proses tumbuh-kembang otak (kecerdasan), serta perkembangan indera penglihatan dan sistem kekebalan tubuh bayi dan balita.PUFA juga dapat mencegah terjadinya peningkatan klosterol dan serangan jantung koroner. Dalam industri oleokimia PUFA banyak digunakan sebagai bahan obat-obatan terutama untuk pengobatan hyperlipidemia. PUFA juga digunakan sebagai bahan pengemulsi mempunyai peranan yang sangat penting baik dalam industri pengolahan pangan maupun industri non pangan. Di dalam industri pangan, bahan pengemulsi digunakan untuk berbagai tujuan, seperti meningkatkan kestabilan dan kesamaan mutu produk-produk emulsi. Selain itu juga minyak dan lemak digunakan sebagai penambah cita rasa pada makanan. Produk-produk yang menggunakan bahan pengemulsi yang dapat kita jumpai sehari-hari adalah es krim, mentega, margarin, keju, krem, sosis, saladresing dan mayonaise. ( Ki-Teak, et.al , 1990 ).
2.6.2. Pemisahan Asam Lemak Dalam Industri
Proses pemisahan asam lemak dalam industri terutama industri oleokimia dapat dilakukan dalam beberapa cara seperti cara netralisasi, penyulingan, dan dengan cara penggunaan pelarut organik
Cara Netralisasi
Netralisasi ialah suatu proses untuk memisahkan asam lemak dari minyak atau lemak dengan cara mereaksikan asam lemak dengan basa atau pereaksi lainnya sehingga membentu sabun.
Netralisasi dengan kautik soda banyak dilakukan dalam skala industri, karena lebih efisien dan lebih murah dibandingkan dengan cara netralisasi lainnya.Selaian itu penggunaan kaustik soda, membantu mengurangi zat warna dan kotoran yang berupa getah dan lendir dalam minyak
O O
R – C + Na+ -OH katalis R – C + H2O
- O – H+ O – Na Air
Asam lemak Sabun
Gambar 4. Reaksi antara asam lemak dengan NaOH
Sabun yang terbentuk dapat membantu pemisahan zat warna dan kotoran seperti fosfatida dan protein dengan cara membentuk emulsi. Sabun atau emulsi yang terbentuk dapat dipisahkan dari minyak dengan cara sentrifusi.
Dengan cara hidrasi dan dibantu dengan proses pemisahan sabun secara mekanis, makanetralisasi dengan menggunakan kaustik soda dapat menghilangkan fosfatida, protein, resin dan suspensi dalam minyak yang tidak dapat dihilangkan dengan proses pemisahan gum. Komponen minor dalam minyak berupa sterol, klorofil, vitamin E dan karotenoid hanya sebagian kecil dapat dikurangi dengan cara netralisasi.
Netralisasi menggunakan kaustik soda akan menyabunkan sejumlah kecil trigliserida.Molekul mono dan digliserida lebih mudah bereaksi dengan persenyawaan alkali.Reaksi penyabunan mono dan digliserida dalam minyak terjadi sebagai berikut:
O CH2 – O – C – R 1
CH2 – OH O
CH2 – (O H) + NaOH katalis CH (OH) + R1 – C
CH2 OH O – Na
CH2OH
O CH2 – O – C – R 1
O CH2 – OH O
CH2 – O – C – R 2 + 2 NaOH katalis CH (OH) + R1 – C
CH2 OH O – Na CH2OH O R2 – C O – Na
Gambar 5. Reaksi Penyabunan Mono dan Digliserida dalam Minyak
Cara Penyulingan
Proses pemisahan asam lemak dengan cara penyulingan adalah proses penguapan asam lemak bebas, langsung dari minyak tanpa mereaksikannya dengan larutan basa, sehingga asam lemak yang terpisah tetap utuh.Minyak kasar yang akan disuling terlebih dahulu dipanaskan dalam alat penukar kalor. Selanjutnya minyak tersebut dialirkan secara kontinu ke dalam alat penyuling dengan letak horizontal sebagaimana ditunjukkan dalam gambar berikut
Keterangan gambar
1.Tangki tempat minyak kasar 7. Pendingin 2. Pipa untuk mengalirkan minyak kasar 8.Gas pemanas
3.Heat exchanger 9.10.Pipa untuk mengalirkan gas 4.Treatment vessel 11.Petak tempat minyak
5. Pipa pengatur pemasukan 12.Pipa yang dihubungkan dengan dan kondensor 6.Pipa pengeluaran minyak
Gambar 6. Skema alat penyuling asam lemak bebas
Disepanjang dasar ketel terdapat pipa-pipa berlubang tempat menginjeksikan uap air ke dalam minyak yang sudah dipanaskan pada suhu kurang lebih 240 0C.
Kadang-kadang ke dalam ketel disemprotkan superheated steam bersama air, yang akan berubah menjadi uap air panas pada tekanan rendah ( kurang lebih 25 mm Hg ), sehingga asam lemak bebas menguap bersama-sama dengan uap air panas
3 12 6 9 5 11 10 8 4 1
tersebut.Hasil sulingan berupa campuran uap air dan asam lemak bebas akan mengembun dalam kondensor pada suhu 70-80 0C.
Untuk menghindari kerusakan minyak selama proses penyulingan karena suhu yang terlalu tinggi maka asam lemak bebas yang tertinggal dalam minyak dengan kadar lebih rendah dari 1 persen harus dinetralkan dengan menggunakan persenyawaan basa.Minyak kasar dengan kadar asam lemak bebas yang tinggi umumnya mengandung fraksi mono dan digliserida yang terbentuk dari hasil hidrolisa sebagian molekul trigliserida.
Selama proses penyulingan, asam lemak akan mengadakan reaksi re-esterifikasi dengan mono dan digliserida sehingga membentuk trigliserida, dengan reaksi sebagai berikut: O CH2 – O – C – R1 O CH2 – O – C – R 1 O CH – OH + 2 R2COOH CH – O – C – R 2 + H2O O CH2 – OH2 CH2 – O –C – R 3 Monogliserida Trigliserida
O CH2 – O – C – R1 O CH2 – O – C – R 1 O CH – O – C – R + 1 R2COOH CH – O – C – R + H2O O CH2 – OH CH2 – O –C – R 2
Gambar 7. Reaksi re-esterifikasi dengan mono dan digliserida
Pemisahan asam lemak bebas dengan cara penyulingan digunakan untuk menetralkan minyak kasar yang mengandung kadar asam lemak bebas lebih kecil dari 8 persen lebih baik dinetralkan dengan menggunakan persenyawaan basa.
Cara Penggunaan Pelarut Organik
Perbedaan kelarutan antara asam lemak bebas dan trigliserida dalam pelarut organik digunakan sebagai dasar pemisahan asam lemak bebas dari minyak.Pelarut yang paling baik digunakan untuk memisahkan asam lemak bebas adalah propana dan piridina.
Piridina merupakan pelarut minyak dan jika ditambahkan air dalam jumlah kecil, maka trigliserida akan terpisah.Trigliserida tidak larut dalam piridina, sedangkan asam lemak bebas tetap larut sempurna .Minyak dapat dipisahkan dengan
pelarut dengan cara dekantasi, sedangkan pelarut dipisahkan dari asam lemak bebas dengan cara penyulingan.Dengan menggunakan alkohol sebagai pelarut, maka kelarutan trigliserida dalam alkohol akan bertambah besar dengan bertambahnya kadar asam lemak bebas, sehingga pemisahan antara asam lemak bebas dari trigliserida lebih sukar dilakukan.( Ketaren.S, 2005 )
2.7. Kompleksasi Urea
Kompleksasi urea telah digunakan secara luas untuk mengkonsentratkan asam lemak jenuh dari berbagai sumber termasuk dari minyak hewani dan minyak
nabati.Ratnayake et.al memperlihatkan skala rintisan 20 g urea untuk konsentrat asam lemak.Dibandingkan dengan metode lain untuk menghasilkan konsentrat asam lemak tak jenuh, fraksinasi urea memungkinkan penanganan sejumlah besar bahan dalam peralatan sederhana karena proses hanya membutuhkan pemakaian yang terbatas dari pelarut organik yang kurang bersifat toksik seperti etanol, maka ini akan lebih ramah terhadap lingkungan dan juga lebih efektif dari segi biaya karena urea itu relatif lebih murah.
Seperti halnya inovasi teknik-teknik penting lainnya, komplek inklusi urea ditemukan secara tidak sengaja oleh MF Bengen dari jerman pada tahun 1940. Bengen ketika itu sedang meneliti pengaruh urea terhadap protein dalam susu pasteurisasi, ternyata urea tersebut membentuk struktur kristal dengan 1-oktanol. Penelitiannya lebih jauh menunjukkan bahwa urea membentuk struktur klatrat
(clathrate) atau kristal dengan senyawa-senyawa hidrokarbon berantai lurus yang termasuk ke dalam golongan n-alkana,n-alkanol, dan asam lemak bebas, tetapi tidak mampu membentuk komplek dengan molekul yang bercabang atau berbentuk siklik. Pada awal tahun 1950, struktur kristal urea berhasil difoto oleh AE.Smith dan menunjukkan bahwa kristal berbentuk heksagonal. Penerapan teknik kristalisasi urea ini pada awalnya banyak digunakan oleh industri minyak untuk memisahkan hidrokarbon berantai lurus dan bercabang.Perkembangan selanjutnya menunjukkan bahwa pembentukan komplek urea ini dapat digunakan untuk memisahkan asam lemak dan turunan alkil, meliputi ester malam ( wax ), lemak alkohol, aldehida,keton, peroksida, dan klorida.Perkembangan terakhir menunjukkan bahwa beberapa senyawa lain dapat membentuk komplek dengan urea, yaitu polimer linear seperi poli 9 etilen glikol ), dan poli ( L asam laktat ), dan cabang dari polimer yang berantai lurus.
Urea membentuk senyawa dengan molekul yang mengandung cincin alkil linier yang bekerja sebagai tempat dengan molekul urea yang komplek dalam struktur berbentuk spiral sebagai hasil pendinginan.Pemisahan senyawa urea dari fraksi senyawa bukan urea secara efektif memindahkan asam lemak yang jenuh dan asam lemak tidak jenuh dalam cincin panjang dan memperkaya ekstrak cairan pada asam lemak yang tidak jenuh ( Ratnayake, et.al, 1988 )
2.8.Kromatografi Gas Cair
Kromatografi gas-cair atau lebih umum disebut kromatografi gas merupakan analisis yang sangat bermanfaat. Seluruh bentuk kromatografi terdiri dari fase diam dan fase gerak. Dalam kromatografi gas-cair, fase gerak adalah gas seperti helium dan fase diam adalah cairan yang mempunyai titik didih yang tinggi diserap pada padatan.
Bagaimana kecepatan suatu senyawa tertentu bergerak melalui mesin, akan tergantung pada seberapa lama waktu yang dihabiskan untuk bergerak dengan gas dan sebaliknya melekat pada cairan dengan jalan yang sama. Secara umum gambaran kromatografi gas seperti pada gambar 4 berikut.
Gambar 9. Diagram alir kromatografi gas-cair
Injeksi sampel
Sejumlah kecil sampel yang akan dianalisis diinjeksikan pada mesin menggunakan semprit kecil. Jarum semprit menembus lempengan karet tebal (Lempengan karet ini disebut septum) yang mana akan mengubah bentuknya kembali secara otomatis ketika semprit ditarik keluar dari lempengan karet tersebut. Injektor berada dalam oven yang mana temperaturnya dapat dikontrol. Oven tersebut cukup panas sehingga sampel dapat mendidih dan diangkut ke kolom oleh gas pembawa misalnya helium atau gas lainnya.
Cara kerja kolom
Material padatan
Ada dua tipe utama kolom dalam kromatografi gas-cair. Tipe pertama, tube panjang dan tipis berisi material padatan; Tipe kedua, lebih tipis dan memiliki fase diam yang berikatan dengan pada bagian terdalam permukaannya.
Untuk menyederhanakan, kita akan melihat pada kolom terpadatkan. Kolom biasanya dibuat dari baja tak berkarat dengan panjang antara 1 sampai 4 meter, dengan diameter internal sampai 4 mm. Kolom digulung sehingga dapat disesuakan dengan oven yang terkontrol secara termostatis. Kolom dipadatkan dengan tanah diatomae, yang merupakan batu yang sangat berpori. Tanah ini dilapisis dengan cairan bertitik didih tinggi, biasanya polimer lilin.
Temperatur kolom
Temperatur kolom dapat bervariasi antara 50 oC sampai 250 oC. Temperatur kolom lebih rendah daripada gerbang injeksi pada oven, sehingga beberapa komponen campuran dapat berkondensasi pada awal kolom. Dalam beberapa kasus, seperti yang anda akan lihat pada bagian bawah, kolom memulai pada temperatur rendah dan kemudian terus menerus menjadi lebih panas dibawah pengawasan komputer saat analisis berlangsung.
Pemisahan berlangsung pada kolom
Ada tiga hal yang dapat berlangsung pada molekul tertentu dalam campuran yang diinjeksikan pada kolom:
1. Molekul dapat berkondensasi pada fase diam.
2. Molekul dapat larut dalam cairan pada permukaan fase diam
Dari ketiga kemungkinan itu, tak satupun yang bersifat permanen. Senyawa yang mempunyai titik didih yang lebih tinggi dari temperatur kolom secara jelas cenderung akan berkondensasi pada bagian awal kolom. Namun, beberapa bagian dari senyawa tersebut akan menguap kembali dengan dengan jalan yang sama seperti air yang menguap saat udara panas, meskipun temperatur dibawah 100 oC. Peluangnya akan berkondensasi lebih sedikit selama berada didalam kolom.
Sama halnya untuk beberapa molekul dapat larut dalam fase diam cair. Beberapa senyawa akan lebih mudah larut dalam cairan dibanding yang lainnya. Senyawa yang lebih mudah larut akan menghabiskan waktunya untuk diserap pada fase diam: sedangkan senyawa yang suka larut akan menghabiskan waktunya lebih banyak dalam fase gas.
Proses dimana zat membagi dirinya menjadi dua pelarut yang tidak bercampurkan karena perbedaan kelarutan, dimana kelarutan dalam satu pelarut satu lebih mudah dibanding dengan pelarut lainnya disebut sebagai partisi. Sekarang, anda bisa beralasan untuk memperdebatkan bahwa gas seperti helium tidak dapat dijelaskan sebagai pelarut Tetapi, istilah partisi masih dapat digunakan dalam kromatografi gas-cair.
Anda dapat mengatakan bahwa substansi antara fase diam cair dan gas. Beberapa molekul dalam substansi menghabiskan waktu untuk larut dalam cairan dan beberapa lainnya menghabiskan waktu untuk bergerak bersama-sama dengan gas.
Waktu.Retensi
Waktu yang digunakan oleh senyawa tertentu untuk bergerak melalui kolom menuju ke detektor disebut sebagi waktu retensi. Waktu ini diukur berdasarkan waktu dari saat sampel diinjeksikan pada titik dimana tampilan menunujukkan tinggi puncak maksimum untuk senyawa itu.
Setiap senyawa memiliki waktu retensi yang berbeda. Untuk senyawa tertentu, waktu retensi sangat bervariasi dan bergantung pada:
1. Titik didih senyawa. Senyawa yang mendidih pada temperatur yang lebih tinggi daripada temperatur kolom, akan menghabiskan hampir seluruh waktunya untuk berkondensasi sebagai cairan pada awal kolom. Dengan demikian, titik didih yang tinggi akan memiliki waktu retensi yang lama.
2. Kelarutan dalam fase cair. Senyawa yang lebih mudah larut dalam fase cair, akan mempunyai waktu lebih singkat untuk dibawa oleh gas pembawa.. Kelarutan yang tinggi dalam fase cair berarti memiiki waktu retensi yang lama.
3. Temperatur kolom. Temperatur tinggi menyebakan pergerakan molekul-molekul dalam fase gas; baik karena molekul-molekul-molekul-molekul lebih mudah menguap, atau karena energi atraksi yang tinggi cairan dan oleh karena itu tidak lama tertambatkan. Temperatur kolom yang tinggi mempersingkat waktu retensi untuk segala sesuatunya di dalam kolom.
Untuk memberikan sampel dan kolom, tidak ada banyak yang bisa dikerjakan menggunakan titik didih senyawa atau kelarutannya dalam fase cair,tetapi anda dapat mempunyai Pengatur temperatur.Semakin rendah temperatur kolom semakin baik pemisahan yang akan anda dapatkan, tetapi akan memakan waktu yang lama untuk mendapatkan senyawa karena kondensasi yang lama pada bagian awal kolom. Dengan kata lain, menggunakan temperatur tinggi, segala sesuatunya akan melalui kolom lebih cepat, tetapi pemisihannya kurang baik. Jika segala sesuatunya melalui kolom dalam waktu yang sangat singkat, tidak akan terdapat jarak antara puncak-puncak dalam kromatogram. Jawabannya dimulai dengan kolom dengan suhu yang rendah kemudian perlahan-lahan secara teratur temperaturnya dinaikkan.Pada awalnya, senyawa yang menghabiskan lebih banyak waktunya dalam fase gas akan melalui kolom secara cepat dan dapat dideteksi. Dengan adanya sedikit pertambahan temperatur akan memperjelas senyawa. Peningkatan temperatur masih dapat lebih `melekatan` molekul-molekul fase diam melalui kolom.
Detektor
Ada beberapa tipe detektor yang biasa digunakan. Detektor ionisasi nyala
dijelaskan pada bagian bawah penjelasan ini, merupakan detektor yang umum dan lebih mudah untuk dijelaskan daripada detektor alternatif lainnya. Detektor Ionisasi Nyala
Dalam mekanisme reaksi, pembakaran senyawa organik merupakan hal yang sangat kompleks. Selama proses, sejumlah ion-ion dan elektron-elektron dihasilkan dalam nyala. Kehadiran ion dan elektron dapat dideteksi.
Seluruh detektor ditutup dalam oven yang lebih panas dibanding dengan temperatur kolom. Hal itu menghentikan kondensasi dalam detektor.
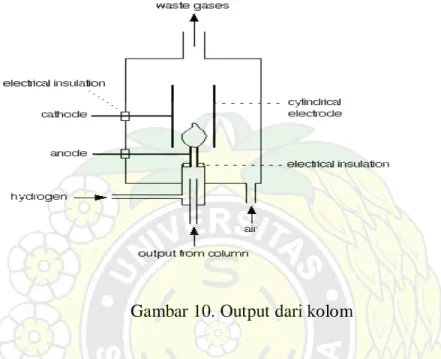
Gambar 10. Output dari kolom
Jika tidak terdapat senyawa organik datang dari kolom, anda hanya memiliki nyala hidrogen yang terbakar dalam air. Sekarang, anggaplah bahwa satu senyawa dalam campuran anda analisa mulai masuk ke dalam detektor. Ketika dibakar, itu akan menghasilkan sejumlah ion-ion dan elektron-elektron dalam nyala. Ion positif akan beratraksi pada katoda silinder. Ion-ion negatif dan elektron-elektron akan beratraksi pancarannya masing-masing yang mana merupakan anoda.
Hal ini serupa dengan apa yang terjadi selama elektrolisis normal. Pada katoda, ion positif akan mendatangi elektron-elektron dari katoda dan menjadi netral. Pada anoda, beberapa elektron dalam nyala akan dipindahkan pada elektroda
positif; ion-ion negatif akan memberikan elektron-elektronnya pada elektroda dan menjadi.netral.
Kehilangam elektron-elektron dari satu elektroda dan perolehan dari elektroda lain, akan menghasilkan aliran elektron-elektron dalam sirkuit eksternal dari anoda ke katoda. Dengan kata lain, anda akan memperoleh arus listrik. Arus yang diperoleh tidak besar, tetapi dapat diperkuat. Jika senyawa-senyawa organik lebih banyak dalam nyala, maka akan banyak juga dihasilkan ion-ion, dan dengan demikian akan terjadi arus listrik yang lebih kuat. Ini adalah pendekatan yang beralasan, khususnya jka anda berbicara tentang senyawa-senyawa yang serupa, arus yang anda ukur sebanding dengan jumlah senyawa dalam nyala.
Kekurangan detektorionisasi nyala
Kekurangan utama dari detektor ini adalah pengrusakan setiap hasil yang keluar dari kolom sebagaimana yang terdeteksi. Jika anda akan mengrimkan hasil ke spektrometer massa, misalnya untuk analisa lanjut, anda tidak dapat menggunakan detektor.tipe.ini.
Penerjemahan.hasil dari detektor
Hasil akan direkam sebagai urutan puncak-puncak; setiap puncak mewakili satu senyawa dalam campuran yang melalui detektor. Sepanjang anda mengontrol secara hati-hati kondisi dalam kolom, anda dapat menggunakan waktu retensi untuk membantu mengidentifikasi senyawa yang tampak-tentu saja anda atau seseorang lain telah menganalisa senyawa murni dari berbagai senyawa pada kondisi yang sama.
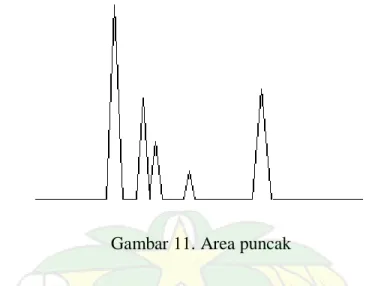
Gambar 11. Area puncak
Area dibawah puncak sebanding dengan jumlah setiap senyawa yang telah melewati detektor, dan area ini dapat dihitung secara otomatis melalui komputer yang dihubungkan dengan monitor. Area yang akan diukur tampak sebagai bagian yang berwarna hijau dalam gambar yang disederhanakan. Perlu dicatat bahwa tinggi puncak tidak merupakan masalah, tetapi total area dibawah puncak. Dalam beberapa contoh tertentu, bagian kiri gambar adalah puncak tertinggi dan memiliki area yang paling luas. Hal ini tidak selalu merupakan hal seharusnya. Mungkin saja sejumlah besar satu senyawa dapat tampak, tetapi dapat terbukti dari kolom dalam jumlah relatif sedikit melalui jumlah yang lama. Pengukuran area selain tinggi puncak dapat dipergunakan dalam hal ini.
Perangkaian kromatogram gas pada spektrometer massa
Hal ini tidak dapat dillakukan menggunakan detektor ionisasi nyala, karena detektor dapat merusak senyawa yang melaluinya. Anggaplah anda menggunakan detektor yang tidak merusak senyawa. Ketika detektor menunjukkan puncak, beberapa diantaranya melalui detektor dan pada waktu itu dapat dibelokkan pada spektrometer massa. Hal ini akan memberikan pola fragmentasi yang dapat dibandingkan dengan data dasar senyawa yang telah diketahui sebelumnya pada komputer. Itu berarti bahwa identitas senyawa-senyawa dalam jumlah besar dapat dihasilkan tanpa harus mengetahui waktu retensinya ( Gliter ,1991 ).
BAB III
METODELOGI PENELITIAN
3.1. Lokasi Penelitian
Lokasi penelitian ini dilakukan di laboratorium kimia organik FMIPA USU Medan dan untuk analisis kromatografi gas cair ( KGC ) dilakukan di Riset dan Penelitian Kelapa Sawit (RPKS ) Medan.
3.2. Bahan dan Alat
Bahan –bahan yang digunakan dalam penelitian ini adalah : inti biji kemiri yang diperoleh dari pasar lokal (yang biasa dikonsumsi oleh masyarakat), sedangkan bahan-bahan kimia yang digunakan terdiri dari n-heksana,natrium sulfat anhidrus, akuades, metanol/kloroform, kalium hidroksida, etanol, asam klorida, urea berderajat p.a buatan E.Merk sedangkan gas nitrogen diperoleh dari produksi industri gas yang ada di kota Medan.
Alat-alat yang digunakan dalam penelitian ini terdiri dari alat-alat gelas yang umum digunakan dalam laboratorium, blender, seperangkat alat pengaduk mekanik, neraca analitik, seperangkat alat rotari evaporator, kertas saring dan analisis kromatografi gas cair ( KGC ) .
3.3. Prosedur Penelitian
3.3.1. Isolasi Minyak Kemiri Dari Inti Biji Kemiri
Inti biji kemiri yang diperoleh dari pasar lokal dikeringkan dalam lemari pengering selama 48 jam dengan suhu 40 0C. Biji yang telah kering kemudian di blender sampai halus dan milt yang terbentuk dimaserasi dengan perendaman menggunakan pelarut n-heksana selama 48 jam dan selanjutnya disaring dengan menggunakan kertas saring. Filtrat yang diperoleh dipisahkan dari padatan dan dikeringkan dengan Na2SO4 anhidrus kemudian disaring. Filtrat dari hasil sampel
dirotarievaporator sehingga diperoleh minyak kemiri yang kering dan telah bebas dari pelarut. Selanjutnya dianalisis komposisi asam lemaknya dengan kromatografi gas cair ( KGC ) dalam bentuk metil ester asam lemak.
3.3.2. Isolasi Minyak Jarak Dari Inti Biji Jarak
Inti biji jarak yang diperoleh dari pasar lokal dikeringkan dalam lemari pengering selama 48 jam dengan suhu 40 0C. Biji yang telah kering kemudian di blender sampai halus dan milt yang terbentuk dimaserasi dengan perendaman menggunakan pelarut n-heksana selama 48 jam dan selanjutnya disaring dengan menggunakan kertas saring. Filtrat yang diperoleh dipisahkan dari padatan dan dikeringkan dengan Na2SO4 anhidrus kemudian disaring.Filtrat dari hasil sampel
dirotarievaporator sehingga diperoleh minyak jarak yang kering dan telah bebas dari pelarut. Selanjutnya dianalisis komposisi asam lemaknya dengan kromatografi gas cair ( KGC ) dalam bentuk metil ester asam lemak.
3.3.3. Isolasi Minyak Kedelai Dari Inti Biji Kedelai
Inti biji kedelai yang diperoleh dari pasar lokal dikeringkan dalam lemari pengering selama 48 jam dengan suhu 40 0C. Biji yang telah kering kemudian di blender sampai halus dan milt yang terbentuk dimaserasi dengan perendaman menggunakan pelarut n-heksana selama 48 jam dan selanjutnya disaring dengan menggunakan kertas saring .Filtrat yang diperoleh dipisahkan dari padatan dan dikeringkan dengan Na2SO4 anhidrus kemudian disaring. Filtrat dari hasil sampel
dirotarievaporator sehingga diperoleh minyak kedelai yang kering dan telah bebas dari pelarut. Selanjutnya dianalisis komposisi asam lemaknya dengan kromatografi gas cair ( KGC ) dalam bentuk senyawa metil ester
3.4. Pemisahan PUFA dari masing-masing minyak Nabati
3.4.1.Minyak kemiri
Minyak kemiri sebanyak 50 g dimasukkan dalam labu dan ditambahkan 11,3 g KOH, 40 ml etanol 95 % dan 12,5 ml akuades selama 1 jam di bawah aliran Nitrogen. setelah dibiarkan pada suhu kamar kemudian asam lemak diekstrak dengan n-heksana dilanjutkan dengan penambahan 60 ml akuades dan diasamkan hingga pH 1 dengan menggunakan HCl 6 N. Lapisan hexana ini dipisahkan dan diuapkan dengan menggunakan rotari evaporator. selanjutnya sebanyak 10 gr asam lemak ditambahkan pada urea dengan perbandingan 1 : 3,5 (w/w) dan etanol ditambahkan juga pada rasio 1 : 3,7 (w/v) berdasarkan atas berat urea. Campuran ini dipanaskan pada suhu 70 0C dengan pengadukan untuk melarutkan semua urea sampai
menghasilkan larutan homogen. Bahan ini disimpan selama 6 jam pada suhu kamar dan diteruskan dengan penyimpanan dalam lemari kulkas selama 24 jam untuk membentuk kristalisasi. Kristal urea ini dipisahkan dengan filtrasi dan fraksi non urea yang komplek diencerkan dengan 100 ml akuades dan diasamkan dengan HCl 6 N hingga pH 4,5 selanjutnya diekstrak dua kali dengan 50 ml hexana. Ekstrak hexana ini diuapkan melalui rotari evaporator. Konsentrat PUFA dicuci dengan Nitrogen dan disimpan dalam kulkas selanjutnya dilakukan analisis kromatografi gas cair ( KGC) dalam bentuk senyawa metil ester.
3.4.2.Minyak Jarak
Minyak jarak sebanyak 50 g dimasukkan dalam labu dan ditambahkan 11,3 g KOH, 40 ml etanol 95 % dan 12,5 ml akuades selama 1 jam di bawah aliran Nitrogen. Setelah dibiarkan pada suhu kamar asam lemak diekstrak dengan n-heksana dilanjutkan dengan penambahan 60 ml akuades dan diasamkan hingga pH 1 dengan menggunakan HCl 6 N. Lapisan hexana ini dipisahkan dan diuapkan dengan menggunakan rotari evaporator.selanjutnya sebanyak 10 g asam lemak ditambahkan pada urea dengan perbandingan 1 : 3,5 (w/w) dan etanol ditambahkan juga pada rasio 1 : 3,7 (w/v) berdasarkan atas berat urea.Campuran ini dipanaskan pada suhu 70 0C dengan pengadukan untuk melarutkan semua urea sampai menghasilkan larutan homogen. Bahan ini disimpan selama 6 jam pada suhu kamar dan diteruskan dengan penyimpanan dalam lemari kulkas selama 24 jam untuk membentuk kristalisasi. Kristal urea ini dipisahkan dengan filtrasi dan fraksi non urea yang komplek diencerkan dengan 100 ml aquades dan diasamkan dengan HCl 6 N hingga pH 4,5
selanjutnya diekstrak dua kali dengan 50 ml hexana. Ekstrak hexana ini diuapkan melalui rotari evaporator. Konsentrat PUFA dicuci dengan Nitrogen dan disimpan dalam kulkas selanjutnya dilakukan analisis kromatografi gas cair ( KGC) dalam bentuk senyawa metil ester.
3.4.3.Minyak Kedelai
Minyak kedelai sebanyak 50 g dimasukkan dalam labu dan ditambahkan 11,3 g KOH, 40 ml etanol 95 % dan 12,5 ml akuades selama 1 jam di bawah aliran Nitrogen. setelah dibiarkan pada suhu kamar asam lemak kemudian diekstrak dengan n-heksana dilanjutkan dengan penambahan 60 ml aquades dan diasamkan hingga pH 1 dengan menggunakan HCl 6 N. Lapisan hexana ini dipisahkan dan diuapkan dengan menggunakan rotari evaporator. Selanjutnya sebanyak 10 g asam lemak ditambahkan pada urea dengan perbandingan 1 : 3,5 (w/w) dan etanol ditambahkan juga pada rasio 1 : 3,7(w/v) berdasarkan atas berat urea. Campuran ini dipanaskan pada suhu 70 0C dengan pengadukan untuk melarutkan semua urea sampai menghasilkan larutan homogen. Bahan ini disimpan selama 6 jam pada suhu kamar dan diteruskan dengan penyimpanan dalam lemari kulkas selama 24 jam untuk membentuk kristalisasi. Kristal urea ini dipisahkan dengan filtrasi dan fraksi non urea yang komplek diencerkan dengan 100 ml akuades dan diasamkan dengan HCl 6 N hingga pH 4,5 selanjutnya diekstrak dua kali dengan 50 ml hexana.Ekstrak hexana ini diuapkan melalui rotari evaporator.Konsentrat PUFA dicuci dengan Nitrogen dan disimpan dalam kulkas selanjutnya dilakukan analisis kromatografi gas cair ( KGC) dalam bentuk senyawa metil ester.
3.5 Bagan Penelitian
3.5.1. Isolasi Minyak Dari Inti Biji Kemiri, Kedelai dan Jarak Pagar
DAFTAR PUS
Dikeringkan dalam lemari pengering 60 0C
Diblender sampai halus
Dimaserasi dengan pelarut n-Heksana
disaring + Na2SO4 anhidros disaring dirotarievaporasi
Inti Biji Kemiri
Inti Biji Kemiri Kering
Filtrat Padatan (ampas minyak Residu Filtrat Minyak Kemiri (Residu) n-heksana (Destilat) KGC
3.5.2. Pemisahan PUFA dari masing-masing minyak Nabati
+ KOH, etanol dan akuades direfluk selama 1 jam di bawah aliran gas N2
Didinginkan
Akuades,HCl 6 N sampai pH 1
Diekstrak dengan n heksana
Dirotari evaporasi
+ urea dengan perbandingan 1 : 3,5 (w/w)
+ etanol dengan rasio 1 :3,7
panaskan pada suhu 70 0C diaduk GaramAsam lemak gliserol Minyak kemiri Asam lemak n-heksana Destilat Asam lemak campuran Campuran homogen
Dibiarkan pada suhu kamar selama 6 jam Dan disimpan dalam kulkas selama 24 jam
difiltrasi
Diencerkan dengan akuades
Diasamkan dengan HCl pH = 4,5 Diekstrak 2 kali dengan heksana Dirotari epavorasi
Kristal urea Larutan non urea
konsentrat
BAB IV
HASIL DAN PEMBAHASAN
4.1.Hasil Penelitian
4.1.1.Isolasi Minyak Kemiri,Kedelai dan Jarak Pagar
Dari hasil penentuan secara kuantitatif minyak kemiri, minyak kedelai dan
minyak jarak pagar diperoleh hasil seperti pada tabel 6.
Tabel 6. Hasil Perolehan Minyak Kemiri, Kedelai dan Jarak Pagar
No Minyak Berat Basah
( gr ) Berat Kering ( gr ) Berat Minyak ( gr ) Persen % 1 Kemiri 4000 3200 1845 57,65 2 Kedelai 4000 3600 600 16,66 3 Jarak Pagar 4000 2800 1427 51,00
4.1.2.Hasil Analisis Kromatografi Gas Cair ( KGC ) sebelum Kompleksasi Urea
Minyak kemiri yang merupakan suatu trigliserida dari asam-asam lemak jenuh
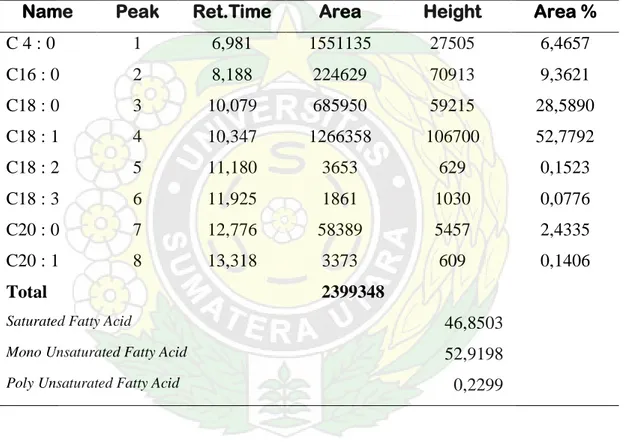
maupun asam-asam lemak tak jenuh ( PUFA), Dari hasil pemeriksaan analisis KGC terhadap metil ester asam lemak yang dikandungnya memberikan kromatogram sebanyak 8 puncak ( lampiran 1 ).
Dari hasil analisis asam lemak dengan menggunakan KGC maka diperoleh komposisi asam-asam lemak yang terdapat pada minyak kemiri seperti tercantum pada tabel 7.
Tabel 7. Hasil analisis KGC dari komposisi asam lemak minyak kemiri
Name Peak Ret.Time Area Height Area %
C 4 : 0 1 6,981 1551135 27505 6,4657 C16 : 0 2 8,188 224629 70913 9,3621 C18 : 0 3 10,079 685950 59215 28,5890 C18 : 1 4 10,347 1266358 106700 52,7792 C18 : 2 5 11,180 3653 629 0,1523 C18 : 3 6 11,925 1861 1030 0,0776 C20 : 0 7 12,776 58389 5457 2,4335 C20 : 1 8 13,318 3373 609 0,1406 Total 2399348
Saturated Fatty Acid 46,8503
Mono Unsaturated Fatty Acid 52,9198 Poly Unsaturated Fatty Acid 0,2299
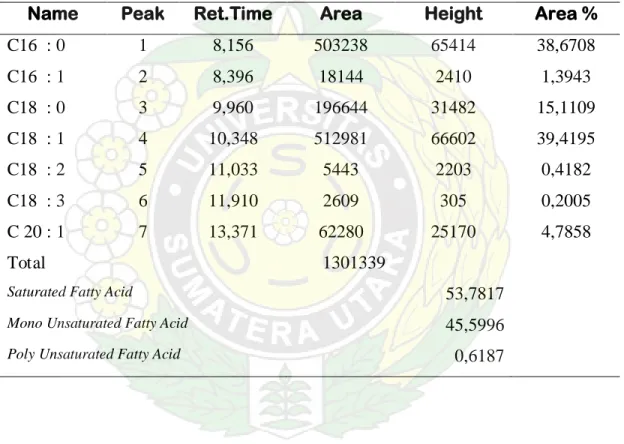
Minyak kedelai yang merupakan suatu trigliserida dari asam-asam lemak
jenuh maupun asam-asam lemak tak jenuh ( PUFA), Dari hasil pemeriksaan analisis KGC terhadap metil ester asam lemak yang dikandungnya memberikan kromatogram sebanyak 7 puncak ( lampiran 2 ).
Dari hasil analisis asam lemak dengan menggunakan KGC terhadap metil ester asam lemak yang dikandungnya maka diperoleh komposisi asam-asam lemak yang terdapat pada minyak kedelai seperti tercantum pada tabel 8.
Tabel 8. Hasil analisis KGC dari komposisi asam lemak minyak kedelai
Name Peak Ret.Time Area Height Area %
C16 : 0 1 8,156 503238 65414 38,6708 C16 : 1 2 8,396 18144 2410 1,3943 C18 : 0 3 9,960 196644 31482 15,1109 C18 : 1 4 10,348 512981 66602 39,4195 C18 : 2 5 11,033 5443 2203 0,4182 C18 : 3 6 11,910 2609 305 0,2005 C 20 : 1 7 13,371 62280 25170 4,7858 Total 1301339
Saturated Fatty Acid 53,7817
Mono Unsaturated Fatty Acid 45,5996 Poly Unsaturated Fatty Acid 0,6187
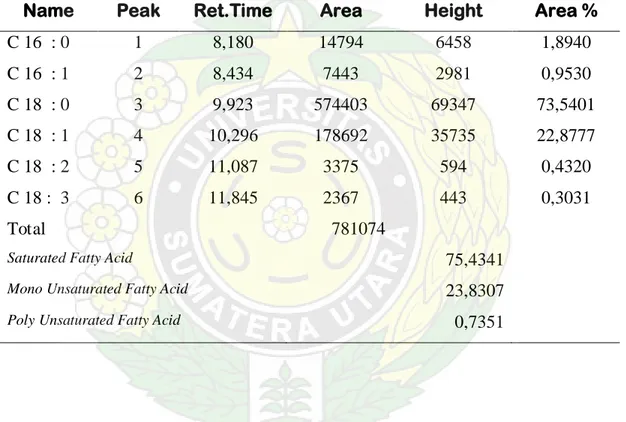
Minyak Jarak Pagar yang merupakan suatu trigeliserida dari asam-asam lemak
jenuh maupun asam-asam lemak tak jenuh ( PUFA), dari hasil pemeriksaan analisis KGC terhadap metil ester asam lemak yang dikandungnya memberikan kromatogram ada sebanyak 6 puncak ( lampiran 3).
Dari hasil analisis asam lemak dengan menggunakan KGC terhadap metil ester asam lemak yang dikandungnya maka diperoleh komposisi asam-asam lemak yang terdapat pada minyak jarak pagar seperti tercantum pada tabel 9.
Tabel 9. Hasil analisis KGC dari komposisi asam lemak minyak jarak pagar
Name Peak Ret.Time Area Height Area %
C 16 : 0 1 8,180 14794 6458 1,8940 C 16 : 1 2 8,434 7443 2981 0,9530 C 18 : 0 3 9,923 574403 69347 73,5401 C 18 : 1 4 10,296 178692 35735 22,8777 C 18 : 2 5 11,087 3375 594 0,4320 C 18 : 3 6 11,845 2367 443 0,3031 Total 781074
Saturated Fatty Acid 75,4341
Mono Unsaturated Fatty Acid 23,8307 Poly Unsaturated Fatty Acid 0,7351
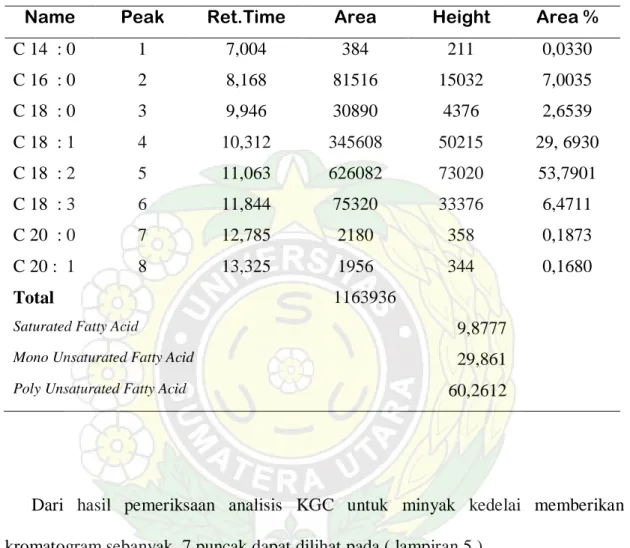
4.1.3. Hasil Analisis Kromatografi Gas Cair ( KGC ) Setelah Kompleksasi Urea
Dari hasil pemeriksaan analisis KGC untuk minyak kemiri memberikan kromatogram ada sebanyak 8 puncak dapat dilihat pada ( lampiran 4 ).
Dari hasil KGC minyak kemiri setelah kompeksasi urea maka diperoleh asam-asam lemak yang dapat dilihat pada tabel 10.
Tabel 10. Hasil analisis KGC dari komposisi asam lemak minyak kemiri setelah kompleksasi urea
Name Peak Ret.Time Area Height Area %
C 14 : 0 1 7,004 384 211 0,0330 C 16 : 0 2 8,168 81516 15032 7,0035 C 18 : 0 3 9,946 30890 4376 2,6539 C 18 : 1 4 10,312 345608 50215 29, 6930 C 18 : 2 5 11,063 626082 73020 53,7901 C 18 : 3 6 11,844 75320 33376 6,4711 C 20 : 0 7 12,785 2180 358 0,1873 C 20 : 1 8 13,325 1956 344 0,1680 Total 1163936
Saturated Fatty Acid 9,8777
Mono Unsaturated Fatty Acid 29,861 Poly Unsaturated Fatty Acid 60,2612
Dari hasil pemeriksaan analisis KGC untuk minyak kedelai memberikan kromatogram sebanyak 7 puncak dapat dilihat pada ( lampiran 5 ).
Dari hasil analisis asam lemak dengan menggunakan KGC minyak kedelai setelah kompeksasi urea maka diperoleh asam-asam lemak yang dapat dilihat pada tabel 11.
Tabel 11. Hasil analisis KGC dari komposisi asam lemak minyak kedelai setelah kompleksasi urea
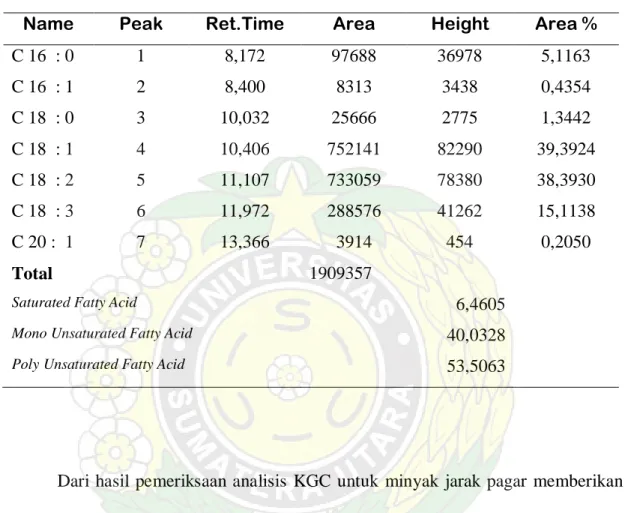
Name Peak Ret.Time Area Height Area %
C 16 : 0 1 8,172 97688 36978 5,1163 C 16 : 1 2 8,400 8313 3438 0,4354 C 18 : 0 3 10,032 25666 2775 1,3442 C 18 : 1 4 10,406 752141 82290 39,3924 C 18 : 2 5 11,107 733059 78380 38,3930 C 18 : 3 6 11,972 288576 41262 15,1138 C 20 : 1 7 13,366 3914 454 0,2050 Total 1909357
Saturated Fatty Acid 6,4605
Mono Unsaturated Fatty Acid 40,0328 Poly Unsaturated Fatty Acid 53,5063
Dari hasil pemeriksaan analisis KGC untuk minyak jarak pagar memberikan kromatogram sebanyak 8 puncak dapat dilihat pada ( lampiran 6 ).
Dari hasil analisis asasm lemak dengan menggunakan KGC minyakjarak pagar setelah kompeksasi urea maka diperoleh asam-asam lemak yang dapat dilihat pada tabel 12.
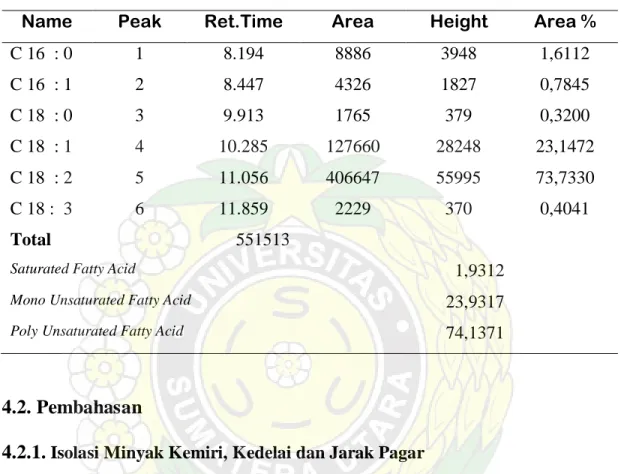
Tabel 12. Hasil analisis KGC dari komposisi asam lemak minyak jarak pagar setelah kompleksasi urea
Name Peak Ret.Time Area Height Area %
C 16 : 0 1 8.194 8886 3948 1,6112 C 16 : 1 2 8.447 4326 1827 0,7845 C 18 : 0 3 9.913 1765 379 0,3200 C 18 : 1 4 10.285 127660 28248 23,1472 C 18 : 2 5 11.056 406647 55995 73,7330 C 18 : 3 6 11.859 2229 370 0,4041 Total 551513
Saturated Fatty Acid 1,9312
Mono Unsaturated Fatty Acid 23,9317 Poly Unsaturated Fatty Acid 74,1371
4.2. Pembahasan
4.2.1. Isolasi Minyak Kemiri, Kedelai dan Jarak Pagar
Pemilihan ekstraksi pelarut secara maserasi untuk isolasi minyak kemiri,minyak
kedelai dan minyak jarak pagar dikarenakan ketiga jenis minyak ini mengandung asam lemak tidak jenuh seperti linoleat dan linolenat yang sangat rentan akan pemutusan ikatan rangkap pada suhu yang ekstrim.Dengan maserasi ekstraksi minyak dapat dilakukan pada suhu kamar sehingga pemutusan ikatan rangkap asam lemak penyusun minyak dapat dihindari.Pelarut yang digunakan dalam maserasi yang dilakukan menggunakan n-heksana karena n- heksana adalah pelarut non polar yang umum digunakan untuk ekstraksi dalam skala laboratorium maupun industri