Nisbah Bobot Zeolit dan Arang Sekam Padi Sebagai Adsorben dalam Pengolahan Limbah Cair Laboratorium Kimia
Weight Ratio Of Zeolite and Rice Husk Charcoal As Adsorbant in the Chemical Laboratory’s Wastewater Treatment
Oleh : Olvi Lakahina
652012017
TUGAS AKHIR
Diajukan kepada Program Studi Kimia, Fakultas Sains dan Matematika guna memenuhi sebagian dari persyaratan untuk mencapai gelar Sarjana Sains
Program Studi Kimia Fakultas Sains dan Matematika Universitas Kristen Satya Wacana
Salatiga 2016
v DAFTAR ISI
Lembar Pengesahan...ii
Pernyataan Keaslian Karya Tulis Tugas Akhir...iii
Pernyataan Persetujuan Publikasi...iv
DAFTAR ISI...v
DAFTAR TABEL...vi
Abstract...1
1. PENDAHULUAN...2
2. METODE PENELITIAN...3
2.1. Waktu dan Tempat Penelitian...3
2.2. Bahan dan Piranti...3
2.3. Metode...3
2.3.1. Karakterisasi Limbah Cair Laboratorium Kimia...3
2.3.2. Preparasi Zeolit Teraktivasi...3
2.3.3. Preparasi Arang Sekam Padi...3
2.3.4. Pemberian Perlakuan...4
2.3.5. Pengukuran Parameter Fisiko – Kimiawi...4
2.4. Isoterm Adsorpsi...4
2.5. Analisis Data...5
3. HASIL DAN PEMBAHASAN...6
3.1. Karakterisasi Awal Parameter Fisiko Kimiawi Limbah Cair Laboratorium Kimia...6
3.2. Efektivitas Pengolahan Limbah Cair Laboratorium Kimia dengan Berbagai Penambahan Bobot Zeolit (g) dalam Waktu Kontak 240 Menit...8
3.3. Rataan Kandungan Parameter Fisko-Kimiawi Limbah Cair Laboratorium Kimia Antar Penambahan Berbagai Bobot Arang Sekam Padi dalam Waktu Kontak 180 menit berikutnya...9
3.4. Efektivitas Pengolahan Limbah Cair Laboratorium Kimia Antar Penambahan Berbagai Bobot Arang Sekam Padi (g) dalam Waktu Kontak 180 menit berikutnya...11
3.5. Isoterm Adsorpsi Parameter Fisiko-Kimiawi Limbah Cair Laboratorium Kimia dengan Menggunakan Zeolit dan Arang Sekam Padi dalam Waktu Kontak 480 menit...12
4. KESIMPULAN...17
5. SARAN...17
DAFTAR PUSTAKA...18 Halaman
vi
DAFTAR TABEL
1. Parameter – Parameter Limbah Cair Laboratorium denganMetode/Piranti Penelitian...4 2. Karakteristik Awal Parameter Fisiko-Kimiawi Limbah Cair Laboratorium Kimia...6 3. Rataan Kandungan Parameter Fisiko-Kimiawi (𝑋± SE) Limbah Cair Laboratorium Kimia
Berbagai Penambahan...7 4. Efektivitas (%) Berbagai Bobot Zeolit Dalam Pengelohan Limbah Cair Laboratorium
Kimia dalam Waktu Kontak 240 menit...8 5. Rataan Kandungan Parameter Fisiko-Kimiawi (𝑋 ± SE) Limbah Cair Laboratorium Kimia
Antar Penambahan Berbagai Bobot Arang Sekam Padi dalam Waktu Kontak 180 menit berikutnya...10 6. Efektivitas (%) Berbagai Bobot Arang Sekam Padi (ASP) dalam Pengelohan Limbah Cair Laboratorium Kimia dalam Waktu Kontak 180 menit berikutnya...11 7. Isoterm Adsorpsi Langmuir dan Freundlich Parameter Fisiko – Kimiawi Limbah Cair
Laboratorium Kimia Menggunakan Zeolit dan Arang Sekam Padi...13 8. Penentuan Standar Deviasi pada Persamaan Isoterm Adsorpsi Limbah Cair Laboratorium
Kimia Menggunakan Zeolit dalam Waktu Kontak 240 Menit...15 9. Penentuan Standar Deviasi pada Persamaan Isoterm Adsorpsi Limbah Cair Laboratorium
Kimia Menggunakan Arang Sekam Padi dalam Waktu Kontak 180 Menit
berikutnya...16 Halaman Tabel
1
Nisbah Bobot Zeolit dan Arang Sekam Padi Sebagai Adsorben dalam Pengolahan Limbah Cair Laboratorium Kimia
Weight Ratio Of Zeolite and Rice Husk Charcoal As Adsorbant in the Chemical Laboratory’s Wastewater Treatment
Olvi Lakahina*, Sri Hartini**, dan A. Ign. Kristijanto** *Mahasiswa Program Studi Kimia Fakultas Sains dan Matematika
**Dosen Program Studi Kimia Fakultas Sains dan Matematika Universitas Kristen Satya Wacana, Salatiga
Jln. Diponegoro no 52-60 Salatiga50711 Jawa Tengah – Indonesia olvilakahina02@gmail.com
Abstract
The purpose of this study is to determine the effectiveness of weight ratio of zeolite and rice husk charcoal in lowering the physico-chemical parameters of liquid waste chemical laboratory and determine the adsorption isotherm models weight ratio of zeolite and rice husk charcoal. Data were analyzed using Randomized Completely Block Design (RCBD), 5 treatments and 5 replications. As a block is the time analysis. As the treatment is different variations of the weight ratio of zeolite and rice husk (grams/gram), namely (5:5); (6:4); (7:3); (8 2) and (9:1). The treatment of its adsorbent were given separately and both of it is treated with stirring. To test the difference between treatment means, the Honestly Significant Differences (HSD) were used with 5% level of significance.
The results showed that the effectivenessof giving 8 grams zeolite for 240 minutes is 99.20% (COD); 68.78% (Cu) and 94.53%(Pb), respectively. While the effectiveness of giving 2 grams rice husk charcoal in the next 180 minutes are 42.34% (COD); 70.75% (Cu) dan 84.30% (Pb), respectively. The maximum adsorption capacity of giving 8 grams zeolite within 240 minutes is COD = 166.670 mg/g (followed Freundlich isotherm model); Cu = 0.327 mg/g (followed Freundlich isotherm model); Pb = 0.754 mg/g (followed Langmuir isotherm model), respectively. While the absorption capacity of giving 2 grams rice husk charcoal in the next 180 minutes are : COD = 3.490x105mg/g (followed Freundlich isotherm model); Cu = 0.084 mg/g (followed Freundlich isotherm model); Pb = 0.782 mg/g (followed Langmuir isotherm model), respectively.
2 1. PENDAHULUAN
Limbah cair laboratorium kimia merupakan salah satu faktor pencemar lingkungan yang berdampak buruk bagi makhluk hidup dan sekitarnya. Berdasarkan data yang diperoleh dari Sekretariat RAN-GRK (2012) menunjukkan bahwa limbah cair yang dihasilkan di Jawa Tengah mencapai 1.159.592.400 m3 per tahun, sehingga perlu dikelola terlebih dahulu. Hasil karakterisasi limbah cair laboratorium kimia UKSW mengandung logam berat yaitu Cu, Fe, Cr, Mn, Al, Zn, Pb, Cd, Ni, Hg, dan As. Pencemaran lingkungan akibat logam berat sudah seharusnya mendapat penanganan yang tepat. Salah satu metode penghilangan logam berat dapat dilakukan dengan adsorbsi. Adsorbsi merupakan salah satu metode yang dapat dilakukan untuk menjerap ion logam kedalam adsorben (Gatri., 2012). Beberapa bahan yang dapat digunakan sebagai adsorben adalah sekam padi, arang aktif, kulit kacang, ampas teh, kopi, kulit jeruk dan zeolit.
Zeolit adalah alumina silikat yang mempunyai struktur berpori yang didalamnya ditempati oleh molekul air dan ion-ion logam alkali seperti natrium, kalium, magnesium dan kalsium sehingga zeolit dapat berpotensi sebagai adsorben (Azamia., 2012). Dalam Margaretadkk.(2013) menyatakan bahwa zeolit mampu menyerap ion logam berat dengan urutan Pb2+>Cd2+>Cu2+>Co2+> Cr2+>Zn2+>Mn2+>Hg2+.
Menurut Ismail dan Waliuddin (1996 dalam Bakri, 2008) sekam padi mengandung 50 % selulosa, 25 – 30 % lignin, 15 – 20 % silika dan memiliki struktur berporiyang dapat berpotensi sebagai adsorben. Hasil penelitian Nhapi dkk. (2011) menunjukkan bahwa 2 g/L arang sekam padi mampu menurunkan kandungan logam berat dalam air limbah industri tekstil dengan mengikuti urutan Zn>Pb>Cu>Cd. Berdasarkan latar belakang diatas maka tujuan dari penelitian ini adalah :
1. Menentukan efektivitas nisbah bobot zeolit dan arang sekam padi dalam menurunkan parameter fisiko-kimiawi limbah cair laboratorium kimia.
2. Menentukan kapasitas adsorpsi dan model isoterm nisbah bobot zeolit dan arang sekam padi.
3 2. METODE PENELITIAN
2.1. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan di Laboratorium Kimia Lingkungan, Progdi Kimia, Fakultas Sains dan Matematika, Universitas Kristen Satya Wacana dari bulan Oktober 2015-April 2016.
2.2. Bahan dan Piranti
Zeolit diperoleh dari toko bahan kimia dan sekam padi diperoleh dari pabrik penyelepan padi di Salatiga. Limbah cair diperoleh dari Laboratorium Kimia Fakultas Sains dan Matematika UKSW. Bahan kimiawi yang digunakan antara lain akuades, HCl, K2Cr2O7, Ag2SO4, H2SO4 , HgSO4, FAS (Ferrous Amonium Sulfat), indikator Ferroin dan NaOH.
Piranti yang digunakan antara lain refluks, Spektrofotometer HACH DR/EL 2000, pH meter HANNA Instrument 9812, Neraca Analitis (Mettler H80), Atomic Absorption Spectroscopy (AAS) Perkin Elmer 3110.
2.3. Metode
2.3.1. Karakterisasi Limbah Cair Laboratorium Kimia
Limbah cair Laboratorium Kimia yang belum diolah dikarakterisasi terlebih dahulu untuk mengetahui paramter fisiko-kimiawi termasuk kandungan logam berat sebelum dilakukan perlakuan dengan adsorben.
2.3.2. Preparasi Zeolit Teraktivasi (Subariyaha dkk., 2013)
Zeolit dicuci dengan akuades berulang-ulang, kemudian dikeringkan dalam oven pada suhu 110°C selama 24 jam dan didesikator. Zeolit sebanyak 100 g direndam dalam 2000 mL HCl 1 M. Campuran diaduk dengan pengaduk magnet selama 3 jam, kemudian dibilas dengan akuades sampai pH netral dan dikeringkan dalam oven suhu 110°C sampai kering.
2.3.3. Preparasi Arang Sekam Padi (Nurhasni dkk., 2014)
Arang sekam padi dicuci dengan akuades berulang-ulang sampai bersih kemudian diaktivasi dengan NaOH 0,5M selama 3 jam kemudian disaring dan dicuci sampai bersih hingga pH netral kemudian dikeringkan dalam oven 110°C sampai kering.
4
2.3.4. Pemberian Perlakuan
Lima (5) beaker glass ukuran 1 L masing-masing diisi dengan air limbah sebanyak 1 L. Selanjutnya diberi nisbah bobot adsorben zeolit sebanyak 5, 6, 7, 8 dan 9 g selama 240 menit kemudian dilanjutkan dengan penambahan arang sekam padi dengan bobot 5, 4, 3, 2 dan 1 g dan diaduk dengan menggunakan magnetik stirer hingga 480 menit.
2.3.5. Pengukuran Parameter Fisiko – Kimiawi
Perubahan-perubahan yang terjadi selama perlakuan dapat diketahui dengan melakukan beberapa analisa terhadap parameter fisika dan kimia (Tabel 1).
Tabel 1. Parameter – Parameter Limbah Cair Laboratorium dengan Metode/Piranti Penelitian
Parameter Piranti
Fisikawi
TDS (Total Dissolved Solids) (ppm) TDS meter (HANNA Instrument 9812) TSS (Total Suspended Solid) (mg/l) Spektrofotometer HACH DR/EL 2000 Kimiawi
pH pH meter (HANNA Instrument 9812)
COD (Chemical Oxygen Demand) (mg/L) Titrimetrik (Alaerts dan Santika, 1987)
Pb (mg/L) Perkin Elmer AAS 3110
Cu (mg/L) HACH DR/EL 2000-Spektrofotometer
2.4. Isoterm Adsorpsi
Untuk menjelaskan isoterm adsorpsi, digunakan 2 isoterm yaitu Langmuir dan Freundlich. Langmuir mendefinisikan bahwa kapasitas adsorpsi maksimum terjadi membentuk lapisan tunggal (monolayer). Persamaan isoterm adsorpsi Langmuir dapat ditulis sebagai berikut (Suseno., 2012) :
𝐶𝑒𝑞 𝑞𝑒𝑞 = 1 𝑄𝑏+ 𝐶𝑒𝑞 𝑄 Keterangan :
Ceq (mg/L) :Konsentrasi akhir parameter fisiko-kimiawi saat kesetimbangan qeq (mg/g) :Massa parameter yang diserap gram adsorben
Q :Massa parameter pada saat 1 gram adsorben yang dapatmenjerap secara sempurna
5
Nilai b dan Q diperoleh dengan membuat grafik hubungan antara Ceq/qeq versus Ceq.
Dari persamaan Langmuir berdasarkan nilai faktor pemisahan (RL) dapat
diindikasikan tipe dari isoterm Langmuir, yaitu : (RL = 0) menunjukkan bahwa irreversible, (0< RL< 1) menunjukkan bahwa favourable, (RL = 1) menunjukkan
bahwa linier dan (RL> 1) menunjukkan bahwa unfavourable. Nilai dari RL dapat
dihitung dengan persamaan (Senthilkumar 2011 dalam Putra., 2014) :
𝑹𝑳 = 𝟏
𝟏 + 𝑲𝑳𝑪𝒐 Keterangan :
RL : Nilai Faktor Pemisahan
KL : Konstanta Langmuir
Co : Konsentrasi Awal Logam
Freundlich mengasumsikan bahwa terdapat lebih dari satu lapisan permukaan (multilayer) dan persamaan isoterm adsorpsi Freundlich adalah sebagai berikut (Suseno., 2012):
log 𝑞𝑒𝑞 = log 𝐾𝑓+
1
𝑛log 𝐶𝑒𝑞 Keterangan :
qeq :Jumlah adsorbat terjerap per satuan bobot adsorben
Ceq (mg/L) :Konsentrasi akhir parameter fisiko-kimiawi saat kesetimbangan
n :Konstanta empiris Freundlich
Kf : Kapasitas adsorpsi (mg/g)
Nilai Kf dan n diperoleh dengan membuat grafik hubungan antara log qeq versus log Ceq.
2.5. Analisis Data
Data hasil penelitian dianalisis dengan Rancangan Acak Kelompok dengan 5 perlakuan dan 5 kali ulangan. Sebagai perlakuan adalah variasi nisbah bobot zeolit dan arang sekam padi (g/g) yaitu 5:5 ; 6:4 ; 7:3 ; 8:2 dan 9:1, sedangkan sebagai kelompok adalah waktu analisis. Pengujian purata antar
6
perlakuan digunakan uji Beda Nyata Jujur (BNJ) dengan tingkat kebermaknaan 5% (Steel dan Torie, 1989).
3. HASIL DAN PEMBAHASAN
3.1. Karakterisasi Awal Parameter Fisiko Kimiawi Limbah Cair Laboratorium Kimia
Hasil karakterisasi awal air limbah laboratorium kimia sebelum diberi perlakuan disajikan pada Tabel 2.
Tabel 2. Karakteristik Awal Parameter Fisiko-Kimiawi Limbah Cair Laboratorium Kimia
Parameter Awal *Baku Mutu Keterangan
FISIKAWI TDS (ppm) 1.210 2.000 M TSS (mg/L) 8,6 100 M KIMIAWI pH 2,3 6 - 9 TM COD (mg/L) 11.184 100 TM Cu (mg/L) 3,35 2 TM Pb (mg/L) 7,145 0,1 TM Keterangan :
M = Memenuhi ; TM = Tidak Memenuhi
*Baku Mutu sesuai Peraturan Daerah Provinsi Jawa Tengah No. 5 Tahun 2012 tentang Baku Mutu Limbah Cair yang belum ditentukan Baku Mutunya. Keteragan ini juga berlaku untuk Tabel 3 sampai 6
Dari Tabel 2 terlihat bahwa TDS dan TSS telah memenuhi baku mutu sebelum diberi perlakuan, sedangkan parameter kimia pH, COD, Cu dan Pb belum memenuhi standar baku mutu yang ditetapkan. Agar limbah memenuhi baku mutu maka perlu diolah terlebih dahulu dan dalam penelitian ini digunakan campuran berbagai nisbah adsorben zeolit dan arang sekam padi yaitu : 5:5 ; 6:4 ; 7:3 ; 8:2 dan 9:1 (g/g). Perlakuan diberikan secara terpisah yaitu zeolit diberikan terlebih dahulu sesuai bobotnya selama 240 menit selanjutnya setelah 240 menit diberikan arang sekam padi sesuai nisbahnya. Kandungan parameter fisiko-kimiawi yaitu TDS, TSS, pH, COD, Cu dan Pb dalam waktu 240 menit disajikan dalam Tabel 3 (dan Lampiran 1).
7
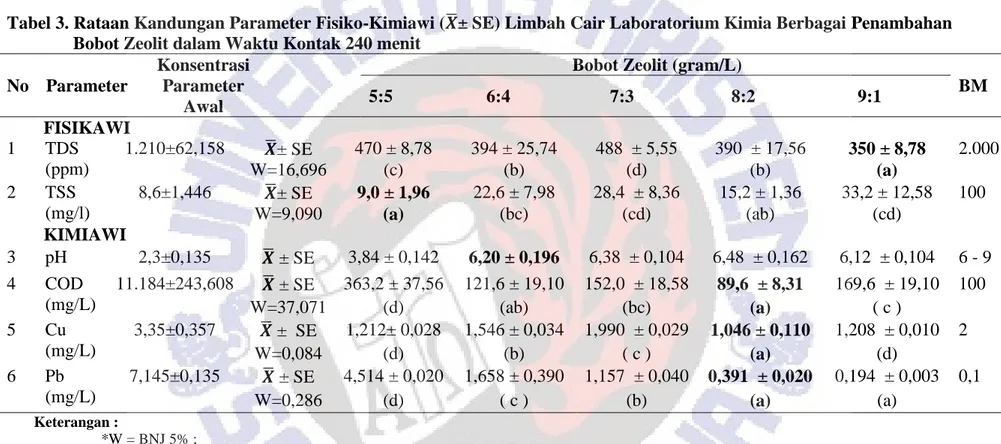
Tabel 3. Rataan Kandungan Parameter Fisiko-Kimiawi (𝑿̅± SE) Limbah Cair Laboratorium Kimia Berbagai Penambahan Bobot Zeolit dalam Waktu Kontak 240 menit
No Parameter
Konsentrasi Parameter
Awal
Bobot Zeolit (gram/L)
BM 5:5 6:4 7:3 8:2 9:1 FISIKAWI 1 TDS (ppm) 1.210±62,158 𝑿̅± SE 470 ± 8,78 394 ± 25,74 488 ± 5,55 390 ± 17,56 350 ± 8,78 2.000 W=16,696 (c) (b) (d) (b) (a) 2 TSS (mg/l) 8,6±1,446 𝑿̅± SE 9,0 ± 1,96 22,6 ± 7,98 28,4 ± 8,36 15,2 ± 1,36 33,2 ± 12,58 100 W=9,090 (a) (bc) (cd) (ab) (cd) KIMIAWI 3 pH 2,3±0,135 𝑿̅ ± SE 3,84 ± 0,142 6,20 ± 0,196 6,38 ± 0,104 6,48 ± 0,162 6,12 ± 0,104 6 - 9 4 COD (mg/L) 11.184±243,608 𝑿̅ ± SE 363,2 ± 37,56 121,6 ± 19,10 152,0 ± 18,58 89,6 ± 8,31 169,6 ± 19,10 100 W=37,071 (d) (ab) (bc) (a) ( c ) 5 Cu (mg/L) 3,35±0,357 𝑿̅ ± SE 1,212± 0,028 1,546 ± 0,034 1,990 ± 0,029 1,046 ± 0,110 1,208 ± 0,010 2 W=0,084 (d) (b) ( c ) (a) (d) 6 Pb (mg/L) 7,145±0,135 𝑿̅ ± SE 4,514 ± 0,020 1,658 ± 0,390 1,157 ± 0,040 0,391 ± 0,020 0,194 ± 0,003 0,1 W=0,286 (d) ( c ) (b) (a) (a) Keterangan : *W = BNJ 5% ;
*Angka-angka yang diikuti dengan huruf yang sama menunjukkan antar perlakuan tidak ada berbeda bermakna, sebaliknya angka-angka yang diikuti huruf yang berbeda menunjukkan adanya beda nyata. Keterangan ini juga berlaku untuk Tabel 5.
8
Dari Tabel 3 tampak bahwa berbagai variasi pemberian zeolit selama 240 menit mampu menurunkan rataan TDS berkisar antara 350 ± 8,78 ppm sampai 488 ± 5,55 ppm. Sebaliknya TSS mengalami kenaikan dengan rataan berkisar antara 9,0 ± 1,96mg/L sampai 33,2 ± 12,58 mg/L. Untuk pH terjadi kenaikan dengan rentang rataan berkisar antara 3,84 ± 0,142 sampai 6,48 ± 0,162. Pemberian 8 g zeolit mampu menurunkan COD dengan rataan 89,6± 8,31 mg/L dan hasil penelitian ini sejalan dengan hasil penelitian Azamia (2012) yang menunjukkan bahwa 25 g zeolit/100 ml air limbah laboratorium kimia selama 1 jam mampu menurunkan COD dari 2.470,75 mg/L menjadi 1.121,4 mg/L. Untuk ion logam Cu dan Pb terjadi penurunan pada pemberian 8 g zeolit dengan rataan berturut-turut 1,046 ± 0,110 mg/L dan 0,391 ± 0,020 mg/L. Hasil penelitian ini sejalan dengan penelitian Solikah & Utami (2014) yang menunjukkan bahwa zeolit 0,015 g dalam 10 ml larutan Cu2+1,3566 ppm selama 75 menit mampu menurunkan logam Cu2+ 68,6348% dan pada Dursun & Pala (2007) menunjukkan bahwa 2 g zeolit dalam 100 ml larutan Pb2+ 1,6 ppm selama 1 jam mampu menurunkan Pb2+ 67%.
3.2. Efektivitas Pengolahan Limbah Cair Laboratorium Kimia dengan Berbagai Penambahan Bobot Zeolit (g) dalam Waktu Kontak 240 menit
Berikut akan disajikan efektivitas pengolahan limbah cair laboratorium kimia dengan berbagai bobot zeolit (g) dalam waktu kontak 240 menit berkisar antara 68,78% - 99,20% (Tabel 4).
Tabel 4. Efektivitas (%) Berbagai Bobot Zeolit Dalam Pengelohan Limbah Cair Laboratorium Kimia dalam Waktu Kontak 240 menit Parameter Bobot Zeolit Konsentrasi
awal Konsentrasi Akhir Efektivitas (%) BM Fisikawi TDS (ppm) 9 1.210 350 71,07 2.000 TSS (mg/l) 5 8,6 9 - 100 Kimiawi pH 6 2,3 6,20 - 6 - 9 COD (mg/l) 8 11184 89,6 99,20 100 Cu (mg/l) 8 3,35 1,046 68,78 2 Pb (mg/l) 8 7,145 0,391 94,53 0,1
9
Dari Tabel 4 terlihat bahwa pemberian 9 gzeolit efektif menurunkan TDS dengan efektivitas 71,07%, sedangkan pemberian 6 gzeolit efektif menaikkan pH dari 2,3 menjadi 6,20. Hasil penelitian ini sejalan dengan penelitian Holub dkk. (2013) yang menunjukkan bahwa 1 g zeolit dalam 100 ml larutan logam Pb2+ 10 ppm mampu menaikkan pH dari 5 menjadi 7,1 dengan efektifitas 29,58%. Pada pemberian 8 g zeolit efektif menurunkan COD 99,20% dan sejalan dengan penelitian Azamia (2012) yang menunjukkan bahwa 25 g zeolit dalam 100 ml air limbah laboratorium kimia selama 1 jam mampu menurunkan COD 54,61%. Pemberian 8 g zeolit efektif menurunkan ion logam Cu dan Pb dengan efektivitas berturut-turut 68,78% dan 94,53%. Hasil penelitian ini sejalan dengan penelitian Salam dkk. (2011) yang menunjukkan bahwa 5 g zeolit dalam 1 L larutan Cu2+ 10 ppm selama 3 jam mampu menurunkan Cu2+ 91-97,5% dan Anggara dkk. (2013) menunjukkan bahwa zeolit 25 g/100 ml larutan Pb2+ 75 ppm mampu menurunkan ion Pb2+ sebesar 96,7%.
3.3. Rataan Kandungan Parameter Fisko-Kimiawi Limbah Cair
Laboratorium Kimia Antar Penambahan Berbagai Bobot Arang Sekam Padi dalam Waktu Kontak 180 menit berikutnya
Pada pemberian zeolit selama 240 menit menunjukkan bahwa ion logam Pb belum memenuhi baku mutu maka perlu dioptimalkan dengan penambahan arang sekam padi sesuai dengan nisbah bobotnya dengan waktu kontak 180 menit. Kandungan parameter fisiko-kimiawi yaitu TDS, TSS, pH, COD, Cu dan Pb dalam waktu kontak dalam waktu kontak 180 menit berikutnya disajikan pada Tabel 5 (dan Lampiran 2).
10
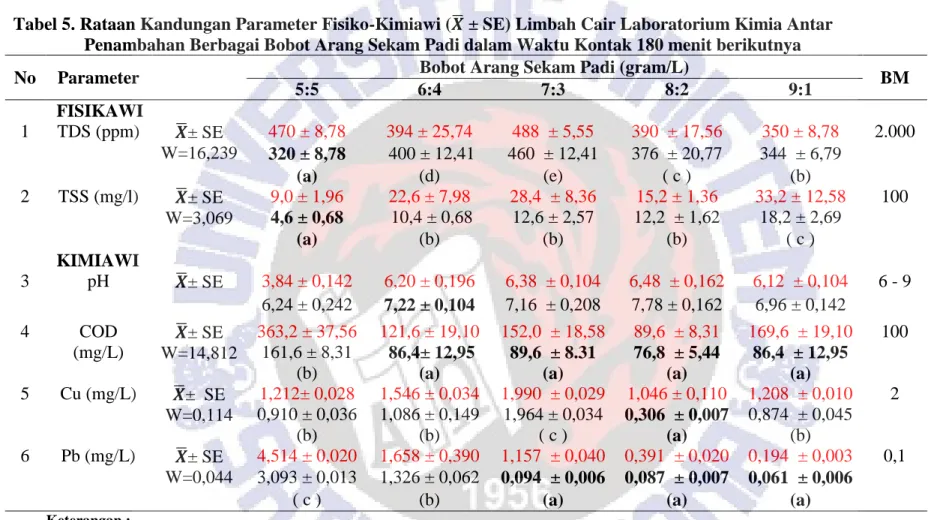
Tabel 5. Rataan Kandungan Parameter Fisiko-Kimiawi (𝑿̅ ± SE) Limbah Cair Laboratorium Kimia Antar Penambahan Berbagai Bobot Arang Sekam Padi dalam Waktu Kontak 180 menit berikutnya
No Parameter Bobot Arang Sekam Padi (gram/L) BM
5:5 6:4 7:3 8:2 9:1 FISIKAWI 1 TDS (ppm) 𝑿̅± SE W=16,239 470 ± 8,78 394 ± 25,74 488 ± 5,55 390 ± 17,56 350 ± 8,78 2.000 320 ± 8,78 400 ± 12,41 460 ± 12,41 376 ± 20,77 344 ± 6,79 (a) (d) (e) ( c ) (b) 2 TSS (mg/l) 𝑿̅± SE W=3,069 9,0 ± 1,96 22,6 ± 7,98 28,4 ± 8,36 15,2 ± 1,36 33,2 ± 12,58 100 4,6 ± 0,68 10,4 ± 0,68 12,6 ± 2,57 12,2 ± 1,62 18,2 ± 2,69 (a) (b) (b) (b) ( c ) KIMIAWI 3 pH 𝑿̅± SE 3,84 ± 0,142 6,20 ± 0,196 6,38 ± 0,104 6,48 ± 0,162 6,12 ± 0,104 6 - 9 6,24 ± 0,242 7,22 ± 0,104 7,16 ± 0,208 7,78 ± 0,162 6,96 ± 0,142 4 COD (mg/L) 𝑿̅± SE W=14,812 363,2 ± 37,56 121,6 ± 19,10 152,0 ± 18,58 89,6 ± 8,31 169,6 ± 19,10 100 161,6 ± 8,31 86,4± 12,95 89,6 ± 8.31 76,8 ± 5,44 86,4 ± 12,95
(b) (a) (a) (a) (a)
5 Cu (mg/L) 𝑿̅± SE W=0,114 1,212± 0,028 1,546 ± 0,034 1,990 ± 0,029 1,046 ± 0,110 1,208 ± 0,010 2 0,910 ± 0,036 1,086 ± 0,149 1,964 ± 0,034 0,306 ± 0,007 0,874 ± 0,045 (b) (b) ( c ) (a) (b) 6 Pb (mg/L) 𝑿̅± SE W=0,044 4,514 ± 0,020 1,658 ± 0,390 1,157 ± 0,040 0,391 ± 0,020 0,194 ± 0,003 0,1 3,093 ± 0,013 1,326 ± 0,062 0,094 ± 0,006 0,087 ± 0,007 0,061 ± 0,006
( c ) (b) (a) (a) (a)
Keterangan :
Angka-angka yang dicetak warna merah merupakan kondisi awal limbah untuk tiap parameter fisiko-kimiawi limbah cair Laboratorium Kimia
11
Dari Tabel 5 tampak bahwa variasi penambahan arang sekam padi mampu menurunkan TDS dengan rataan berkisar antara 320 ± 8,78 ppm sampai460 ± 12,41 ppm dan TSS juga mengalami penurunan dengan rataan berkisar antara 4,6 ± 0,68 mg/L sampai 18,2 ± 2,69 mg/L. Untuk pH terjadi kenaikan pada penambahan variasi arang sekam padi dengan rentang rataan 6,24 ± 0,242 sampai 7,78 ± 0,162. Pemberian 2 g arang sekam padi mampu menurunkan COD dengan rataan 76,8± 5,44 mg/L. Hasil penelitian ini sejalan dengan penenlitian Swathi dkk. (2014) yang menunjukkan bahwa pemberian arang sekam padi 2 mg dalam 250 ml air limbah penyamakan kulit mampu menurunkan kandungan COD dari 1.400 mg/L menjadi 506,6 mg/L. Pemberian 2 g arang sekam padi mampu menurunkan ion logam Cu dan Pb dengan rataan berturut-turut 0,306 ± 0,007 mg/L dan 0,087 ± 0,007mg/L. Hasil penelitian ini sejalan dengan penelitian Nurhasni dkk. (2014) yang menunjukkan bahwa 0,5 g arang sekam padi dalam 10 ml air limbah laboratorium kimia mampu menurunkan ion logam Cu 78,57% selama 2,5 jam dan mampu menurunkan Pb 99,38% dalam air limbah multikomponen selama 3 jam.
3.4. Efektivitas Pengolahan Limbah Cair Laboratorium Kimia Antar Penambahan Berbagai Bobot Arang Sekam Padi (g) dalam Waktu Kontak 180 menit berikutnya.
Berikut akan disajikan efektivitas pengolahan limbah cair laboratorium kimia antar penambahan berbagai bobot arang sekam padi (g) dalam waktu kontak 180 menit berikutnya berkisar antara 31,91% -84,30% (Tabel 6).
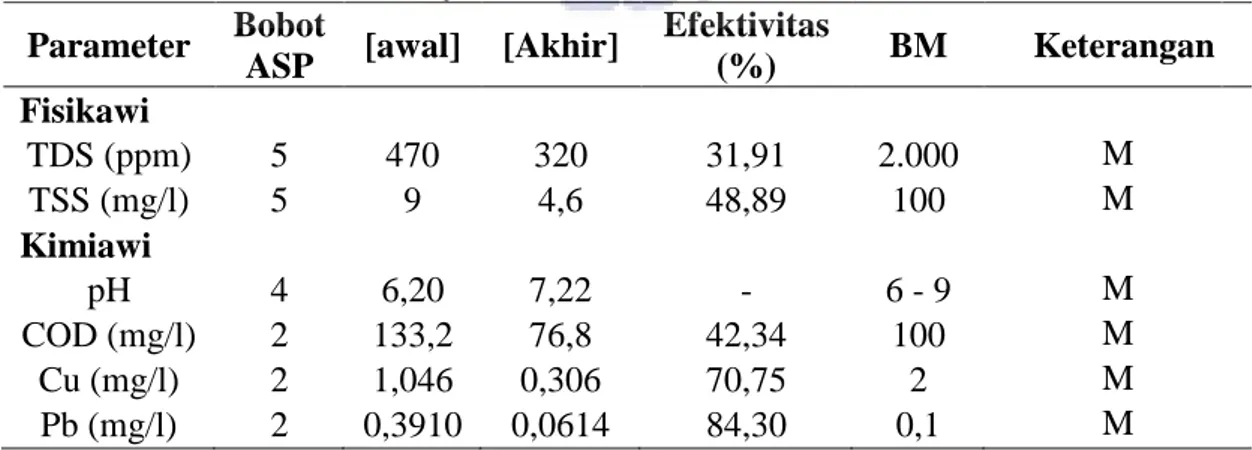
Tabel 6. Efektivitas (%) Berbagai Bobot Arang Sekam Padi (ASP) dalam Pengelohan Limbah Cair Laboratorium Kimia dalam Waktu Kontak 180 menit berikutnya
Parameter Bobot
ASP [awal] [Akhir]
Efektivitas (%) BM Keterangan Fisikawi TDS (ppm) 5 470 320 31,91 2.000 M TSS (mg/l) 5 9 4,6 48,89 100 M Kimiawi pH 4 6,20 7,22 - 6 - 9 M COD (mg/l) 2 133,2 76,8 42,34 100 M Cu (mg/l) 2 1,046 0,306 70,75 2 M Pb (mg/l) 2 0,3910 0,0614 84,30 0,1 M
12
Dari Tabel 6 terlihat bahwa penambahan 5 g arang sekam padi efektif menurunkan TDS dan TSS dengan efektivitas berkisar antara 31,91% sampai 48,89%. Sedangkan penambahan 4 g arang sekam padi efektif menaikkan pH dari 6,20 menjadi 7,22. Pada penambahan 2 g arang sekam padi efektif menurunkan COD 42,34%. Hasil penelitian ini sejalan dengan penelitian Munneer dkk. (2010) yang menunjukkan bahwa 10 g sekam padi efektif menurunkan COD pada air limbah tekstil dengan efektivitas 59%. Pada penambahan 2 g arang sekam padi juga mampu menurunkan ion logam Cu dan Pb dengan efektivitas berturut-turut 70,75% dan 84,30%. Hasil penelitian ini sejalan dengan penelitian Sethi (2014) yang menunjukkan bahwa 1 g arang sekam padi dalam 100 ml larutan campuran logam berat Cu, Pb dan Zn dengan konsetrasi 1-20 ppm mampu menurunkan kandungan logam dengan urutan Zn>Pb>Cu dan efektivitas berturut-turut 96,64%, 96,45% dan 96,31%.
3.5. Isoterm Adsorpsi Parameter Fisiko-Kimiawi Limbah Cair
Laboratorium Kimia dengan Menggunakan Zeolit dan Arang Sekam Padi dalam Waktu Kontak 480 menit.
Hasil perhitungan Isoterm adsorpsi Langmuir dan Freundlich parameter fisiko-kimiawi limbah cair Laboratorium Kimia di sajikan dalam Tabel 7 (dan Lampiran 3).
13
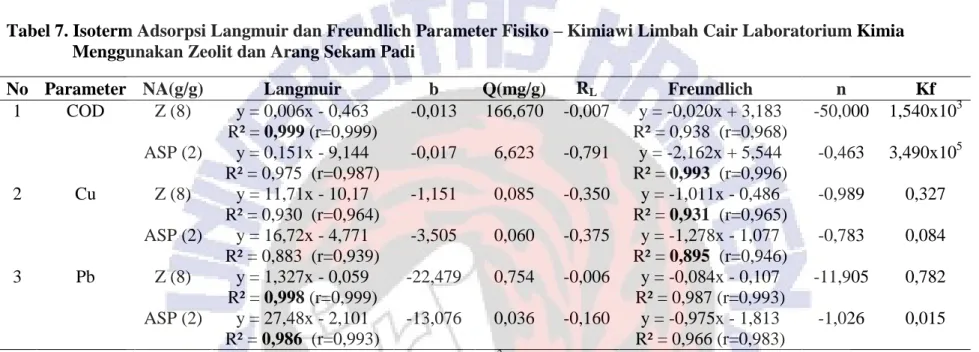
Tabel 7. Isoterm Adsorpsi Langmuir dan Freundlich Parameter Fisiko – Kimiawi Limbah Cair Laboratorium Kimia Menggunakan Zeolit dan Arang Sekam Padi
No Parameter NA(g/g) Langmuir b Q(mg/g) RL Freundlich n Kf
1 COD Z (8) y = 0,006x - 0,463 R² = 0,999 (r=0,999) -0,013 166,670 -0,007 y = -0,020x + 3,183 R² = 0,938 (r=0,968) -50,000 1,540x103 ASP (2) y = 0,151x - 9,144 R² = 0,975 (r=0,987) -0,017 6,623 -0,791 y = -2,162x + 5,544 R² = 0,993 (r=0,996) -0,463 3,490x105 2 Cu Z (8) y = 11,71x - 10,17 R² = 0,930 (r=0,964) -1,151 0,085 -0,350 y = -1,011x - 0,486 R² = 0,931 (r=0,965) -0,989 0,327 ASP (2) y = 16,72x - 4,771 R² = 0,883 (r=0,939) -3,505 0,060 -0,375 y = -1,278x - 1,077 R² = 0,895 (r=0,946) -0,783 0,084 3 Pb Z (8) y = 1,327x - 0,059 R² = 0,998 (r=0,999) -22,479 0,754 -0,006 y = -0,084x - 0,107 R² = 0,987 (r=0,993) -11,905 0,782 ASP (2) y = 27,48x - 2,101 R² = 0,986 (r=0,993) -13,076 0,036 -0,160 y = -0,975x - 1,813 R² = 0,966 (r=0,983) -1,026 0,015 Keterangan : NA = Nisbah Adsorben ; Z = Zeolit ; ASP = Arang Sekam Padi ; R2 = Koefisien Determinasi ; r = Koefisien Korelasi ; b = Konstanta Langmuir ;
14
Dari Tabel 7 terlihat bahwa model isoterm adsorpsi COD mengikuti model Langmuir pada pemberian 8 g zeolit dengan nilai R2 0,999 dan kapasitas adsorpsi 166,670 mg/g. Sedangkan pada pemberian arang sekam padi mengikuti model Freundlich dengan nilai R2 0,996 dan kapasitas adsorpsi 3,490x105 mg/g. Hasil penelitian ini sejalan dengan penelitian Abuzar dkk. (2014) yang menunjukkan bahwa model isoterm adsorpsi COD menggunakan serbuk kulit jagung mengikuti model Langmuir dengan nilai R2 0,987 dan kapasitas adsorpsi 27,75 mg/g. Dilanjutkan oleh Sholeh dkk. (2012) menunjukkan bahwa model isoterm COD menggunakan abu terbang bagas mengikuti model Freundlich dengan nilai R2 0,93 dan kapasitas adsorpsi 0,4360.
Model isoterm adsorpsi ion logam Cu mengikuti model Freundlich pada pemberian 8 g zeolit dengan nilai R2 0,964 dan kapasitas adsorpsi 0,327 mg/g. Demikian juga pada penambahan 2 g arang sekam padi mengikuti model Freundlich dengan nilai R2 0,946 dan kapasitas adsorpsi 0,084mg/g. Hasil penelitian ini sejalan dengan Estiaty (2012) yang menunjukkan bahwa model isoterm ion logam Cu menggunakan zeolit mengikuti model Freundlich dengan nilai R2 0,996.
Model isoterm adsorpsi ion logam Pb mengikuti model isoterm Langmuir pada pemberian 8 g zeolit dengan nilai R2 0,999 dan kapasitas adsorpsi 0,754 mg/g. Demikian juga pada pemberian 2 g arang sekam padi mengikuti model isoterm Langmuir dengan nilai R2 0,993 dan kapasitas adsorpsi 0,782 mg/g. Hasil penelitian ini sejalan dengan penelitian Hanjanattri dkk. (2014) yang menunjukkan bahwa model isoterm adsorpsi zeolit pada logam Pb mengikuti model Langmuir dengan kapasitas adsorpsi 5,057 mg/g. Dilanjutkan oleh Asrari dkk. (2010) yang menunjukkan bahwa model isoterm logam Pb2+ arang sekam padi mengikuti model Langmuir dengan kapasitas adsorpsi 0,62 mg/g.
Tipe isoterm Langmuir berdasarkan nilai faktor pemisahan (RL) pada parameter
COD, Cu dan Pb (Tabel 7) tidak dapat diindikasikan karena niali RL bernilai negatif.
Untuk menguatkan hasil pada Tabel 7, dicari standar deviasi yang terkecil untuk menentukan persamaan isoterm mana yang lebih sesuai (Mulyatna dkk., 2003). Penentuan standar deviasi disajikan dalam Tabel 8 dan Tabel 9 (Lampiran 4 dan 5).
15
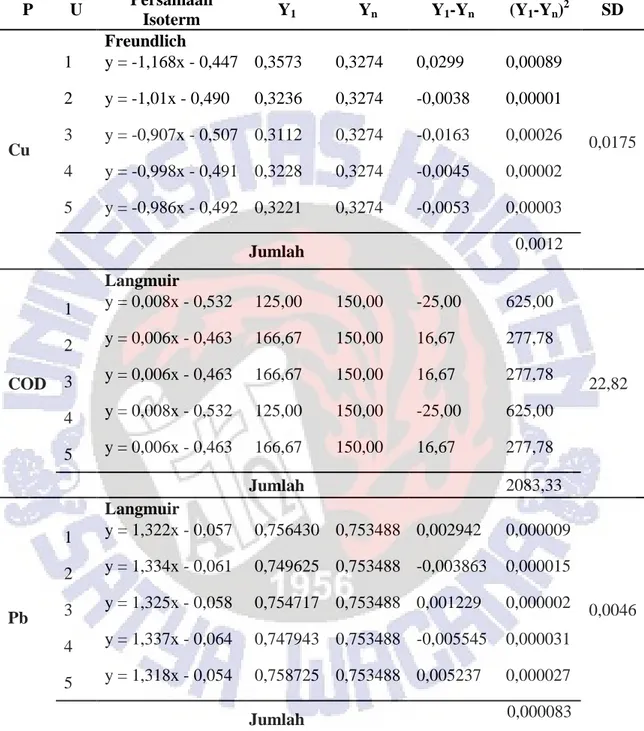
Tabel 8. Penentuan Standar Deviasi pada Persamaan Isoterm Adsorpsi Limbah Cair Laboratorium Kimia Menggunakan Zeolit dalam Waktu Kontak 240 Menit
P U Persamaan Isoterm Y1 Yn Y1-Yn (Y1-Yn) 2 SD Cu Freundlich 0,0175 1 y = -1,168x - 0,447 0,3573 0,3274 0,0299 0,00089 2 y = -1,01x - 0,490 0,3236 0,3274 -0,0038 0,00001 3 y = -0,907x - 0,507 0,3112 0,3274 -0,0163 0,00026 4 y = -0,998x - 0,491 0,3228 0,3274 -0,0045 0,00002 5 y = -0,986x - 0,492 0,3221 0,3274 -0,0053 0,00003 Jumlah 0,0012 COD Langmuir 22,82 1 y = 0,008x - 0,532 125,00 150,00 -25,00 625,00 2 y = 0,006x - 0,463 166,67 150,00 16,67 277,78 3 y = 0,006x - 0,463 166,67 150,00 16,67 277,78 4 y = 0,008x - 0,532 125,00 150,00 -25,00 625,00 5 y = 0,006x - 0,463 166,67 150,00 16,67 277,78 Jumlah 2083,33 Pb Langmuir 0,0046 1 y = 1,322x - 0,057 0,756430 0,753488 0,002942 0,000009 2 y = 1,334x - 0,061 0,749625 0,753488 -0,003863 0,000015 3 y = 1,325x - 0,058 0,754717 0,753488 0,001229 0,000002 4 y = 1,337x - 0,064 0,747943 0,753488 -0,005545 0,000031 5 y = 1,318x - 0,054 0,758725 0,753488 0,005237 0,000027 Jumlah 0,000083
Keterangan : P = Parameter ; U = Ulangan ; Y1 = Nilai kapasitas adsorpsi ; Yn = Rata-rata setiap ulangan
; SD = Standar deviasi ; Keterangan ini juga berlaku untuk Tabel 9
Dari Tabel 8 terlihat bahwa pada pemberian zeolit untuk parameter Cu mengikuti model isoterm adsorpsi Freundlich dengan SD = 0,0175; COD mengikuti model isoterm adsorpsi Langmuir dengan SD = 22,82; dan Pb mengikuti model isoterm adsorpsi Langmuir dengan SD = 0,0046.
16
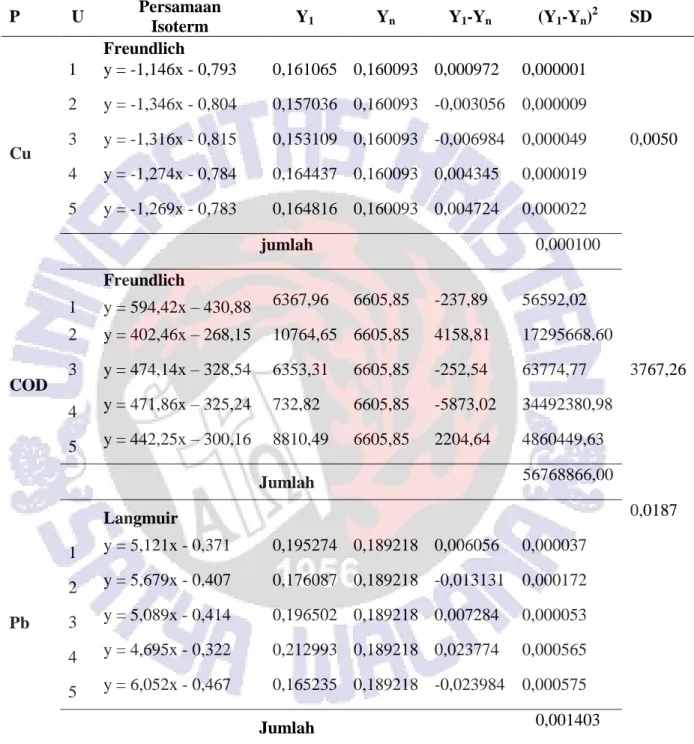
Tabel 9. Penentuan Standar Deviasi pada Persamaan Isoterm Adsorpsi Limbah Cair Laboratorium Kimia Menggunakan Arang Sekam Padi dalam Waktu Kontak 180 Menit berikutnya P U Persamaan Isoterm Y1 Yn Y1-Yn (Y1-Yn) 2 SD Cu Freundlich 1 y = -1,146x - 0,793 0,161065 0,160093 0,000972 0,000001 0,0050 2 y = -1,346x - 0,804 0,157036 0,160093 -0,003056 0,000009 3 y = -1,316x - 0,815 0,153109 0,160093 -0,006984 0,000049 4 y = -1,274x - 0,784 0,164437 0,160093 0,004345 0,000019 5 y = -1,269x - 0,783 0,164816 0,160093 0,004724 0,000022 jumlah 0,000100 COD Freundlich 1 y = 594,42x – 430,88 6367,96 6605,85 -237,89 56592,02 3767,26 2 y = 402,46x – 268,15 10764,65 6605,85 4158,81 17295668,60 3 y = 474,14x – 328,54 6353,31 6605,85 -252,54 63774,77 4 y = 471,86x – 325,24 732,82 6605,85 -5873,02 34492380,98 5 y = 442,25x – 300,16 8810,49 6605,85 2204,64 4860449,63 Jumlah 56768866,00 Pb Langmuir 0,0187 1 y = 5,121x - 0,371 0,195274 0,189218 0,006056 0,000037 2 y = 5,679x - 0,407 0,176087 0,189218 -0,013131 0,000172 3 y = 5,089x - 0,414 0,196502 0,189218 0,007284 0,000053 4 y = 4,695x - 0,322 0,212993 0,189218 0,023774 0,000565 5 y = 6,052x - 0,467 0,165235 0,189218 -0,023984 0,000575 Jumlah 0,001403
Dari Tabel 9 terlihat bahwa pada pemberian arang sekam padi untuk parameter Cu mengikuti model isoterm adsorpsi Freundlich dengan SD = 0,0050 ; COD mengikuti model isoterm adsorpsi Freundlich dengan SD = 3767,26 ; dan Pb mengikuti model isoterm adsorpsi Langmuir dengan SD = 0,0187.
17 4. KESIMPULAN
Berdasarkan hasil penelitian dapat ditarik kesimpulan sebagai berikut :
1. Efektivitas pemberian 8 g zeolit selama 240 menit adalah 99,20% (COD); 68,78% (Cu) dan 94,53% (Pb). Sedangkan efektivitas pemberian 2 g arang sekam padi selama 180 menit berikiutnya adalah 42,34% (COD); 70,75% (Cu) dan 84,30% (Pb).
2. Kapasitas adsorpsi maksimum pada pemberian zeolit 8 g dalam waktu 240 menit adalah : COD = 166,670 mg/g (mengikuti model isoterm Langmuir); Cu = 0,327 mg/g (mengikuti model isoterm Freundlich) dan Pb = 0,754 mg/g (mengikuti model isoterm Langmuir). Sedangkan kapasitas adsorpsi pemberian arang sekam padi 2 g dalam waktu 180 menit berikutnya adalah : COD = 3,490x105 mg/g (mengikuti model isoterm Freundlich) ; Cu = 0,084 mg/g (mengikuti model isoterm Freundlich) dan Pb = 0,782 mg/g (mengikuti model isoterm Langmuir).
5. SARAN
Untuk penelitian selanjutnya sebaiknya digunakan zeolit yang diaktivasi dengan penambahan basa dan arang sekam padi yang diaktivasi dengan asam.
18
DAFTAR PUSTAKA
Abuzar, S.S., Dewilda, Y. & Stefani, W., 2014. Analisis Penyisihan Chemical Oxygen Demand (COD) Limbah Cair Hotel Menggunakan Serbuk Kulit Jagung. Jurnal
Teknik Lingkungan UNAND, 11(1), pp.18-27.
Alaerts, G. & Santika, S.S., 1987. Metode Penelitian Air. Usaha Nasional. Surabaya. Anggara, P.A., Wahyuni, S. & Prasetya, A.T., 2013. Optimalisasi Zeolit Alam
Wonosari dengan Proses Aktivasi Secara Fisis dan Kimia. Indonesian Journal of
Chemical Science, 2(1), pp.72-77.
Asrari, E., Tavallali, H. & Hagshenas, M., 2010. Removal of Zn(II) and Pb (II) ions Using Rice Husk in Food Industrial Wastewater. J. Appl. Sci. Environ. Manage, 4(14), pp.159-62.
Azamia, M., 2012. Pengolahan Limbah Cair Laboratorium Kimia Dalam Penurunan Kadar Organik Serta Logam Berat Fe, Mn, Cr dengan Metode Koagulasi dan Adsorbsi. Skripsi. Depok: Program Studi Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Indonesia.
Bakri, 2008. Komponen Kimia dan Fisik Abu Sekam Padi sebagai SCM untuk Pembuatan Komposit Semen. Jurnal Perennial, 5(1), pp.9-14.
Dursun, S. & Pala, A., 2007. Lead pollution removal from water using a natural zeolite.
J. Int. Environmental Application & Science, 2(1&2), pp.11-19.
Estiaty, L.M., 2012. Kesetimbangan dan Kinetika AdsorpsiI Ion Cu2+ Pada Zeolit-H.
Riset Geologi dan Pertambangan, 2(2), pp.127-41.
Gatri, D., 2012. Modifikasi Zeolit Alam dengan Polianilin (PANI) Sebagai Adsorben Logam Berat. Skripsi. Depok: Universitas Indonesia.
Hanjanattri, S., Krisdiyanto, D., Khamidinal & Sedyadi, E., 2014. Adsorpsi Ion Logam Pb2+ Pada Limbah Accu Zuur PT Muhtomas Menggunakan Zeolit Alam Teraktivasi Asam Sulfat. Seminar Nasional Kimia Dan Pendidikan Kimia VI. Hendrawan, A., 2010. Adsorbsi Unsur Pengotor Larutan Natrium Silikat Menggunakan
Zeolit Alam Karengunggal. Skripsi. Jakarta: Universitas Islam Negeri Syarif Hidayatullah.
Holub, M., Balintova, M., Pavlikova, P. & Palascakova, L., 2013. Study of Sorption Properties of Zeolite in Acidic Conditions in Dependence on Particle Size.
Chemical Engineering Transactions, 32, pp.559-64.
Irmanto, S., 2009. Penurunan TSS, BOD dan COD Limbah Cair Industri Tahu di Desa Cilongok Kabupaten Banyumas Menggunakan Sistem Zeolit Teraktivasi dan Terimpregnasi TiO2. Molekul, 4(2), pp.83-93.
Majeed, M.R., Muhammed, A.S. & Rasheed, K.A., 2014. The Removal of Zinc, Chromium and Nickel from Industrial Waste Water using Rice Husk. Iraqi
19
Margeta, K., Logar, N.Z., Šiljeg, M. & Farkaš, A., 2013. Natural Zeolites in Water
Treatment – How Effective is Their Use. [Online] INTECH Available at:
http://creativecommons.org/licenses/by/3.0 [Accessed 20 Mei 2016].
Mulytna, L., Pradiko, H. & Nasution, U.K., 2003. Pemilihan Persamaan Adsorpsi Isoterm Pada Penentuan Kapasitas Adsorpsi Kulit Kacang Tanah Terhadap Zat Warna Remazol Golden Yellow 6. INFOMATEK, 5(3), pp.131-40.
Munandar, A., Krisdiyanto, D., Khamidinal & Artsanti, P., 2014. Adsorpsi Logam Pb dan Fe dengan Zeolit Alam Teraktivasi Asam Sulfat. In Seminar Nasional Kimia
dan Pendidikan Kimia VI. Surakarta, 2014. ISBN 979363174-0.
Munneer, M., Bhatti, I.A. & Adeel, S., 2010. Removal of Zn, Pb and Cr in Textile WastewaterUsing Rice Husk as a Biosorbent. Asian Journal of Chemistry, 22(10), pp.7453-59.
Nhapi, I; Banadda, N; Murenzi, R; Sekomo, C B; Wali, U G., 2011. Removal of Heavy Metals from Industrial Wastewater Using Rice Husks. The Open Environmental
Engineering Journal, 4, pp.170-80.
Nurhasni, Hendrawati & Saniyyah, N., 2014. Sekam Padi untuk Menyerap Ion Logam Tembaga dan Timbal dalam Air Limbah. IV(1), pp.36-44.
Putra, ADK 2014, 'Nisbah Bobot Campuran Kulit Jeruk dan Arang Tongkol Jagung Sebagai Adsorben Dalam Pengolahan Air Limbah Tekstil', Skripsi, Universitas Kristen Satya Wacana, Salatiga.
Salam, O.E.A., Reiad, N.A. & ElShafei, M.M., 2011. A study of the removal characteristics of heavy metals from wastewater by low-cost adsorbents. Journal
of Advanced Research, 2, pp.297–303.
Sekretariat RAN-GRK, 2012. Sekretariat RAN-GRK. [Online] Available at: Hyperlink
"ranradgrk.bappenas.go.id/rangrk/english/c0mponent/content/article/102-bahasa/status-provinsi/115-jateng"
ranradgrk.bappenas.go.id/rangrk/english/c0mponent/content/article/102-bahasa/status-provinsi/115-jateng [Diunduh 16 Juni 2015].
Sethi, T., 2014. Characterization and Application of Rice Husk for Removal of Heavy Metals from Laboratory Prepared Waste Water. Thesis. Odisha, India: Department of Civil Engineering National Institute of Technology Rourkela. Sholeh, M., Prasetya, A. & Sarto, 26-34. Pengolahan Air Limbah Industri Penyamakan
Kulit Menggunakan Abu Terbang Bagas Secara Batch. Majalah Kulit, Karet dan
Plastik, 28(1), p.2012.
Solikah, S. & Utami, B., 2014. Perbedaan Penggunaan Adsorben dari Zeolit Alam Teraktivasi dan Zeolit Alam Terimmobilisasi Dithizon Untuk Penyerapan Ion Logam Tembaga (Cu2+). Makalah Seminar Nasional Kimia dan Pendidikan Kimia. Surakarta: UNS.
20
Steel, R.G.D. and J. H. Torie, 1981. Principle and Procedures of Statistic A Biometrical Approach, 2nd ed. Mc Graw-Hill International. Book Co, Kuga Kusha, Japan. Subariyaha, I., Zakariab, A. & Purwamargapratala, Y., 2013. Karakterisasi Zeolit Alam
Lampung Teraktivasi Asam Kloridadan Termodifikasi Asam Fosfat. Jurnal
Teknologi Pengelolaan Limbah (Journal of Waste Management Technology) ISSN 1410-9565, 16, pp.17-24.
Suseno, H.P., 2012. Pengurangan Chemical Oxygen Demand (COD) dan Krom Dalam Air Limbah Industri Penyamakan Kulit Menggunakan Abu Terbang Bagas. In
Prosiding Seminar Nasional Aplikasi Sains & Teknologi (SNAST) Periode III.
Yogyakarta, 2012. ISSN: 1979-911X.
Swathi, M; Singh, A Sathya; Aravind, S; Sudhakar, P K Ashi; Gobinath, R; devi, D Saranya., 2014. Adsorption studies on tannery wastewater using rice husk.
Scholars Journal of Engineering and Technology (SJET), 2(2B), pp.253-57.
Syauqiah, I., Amalia, M. & Kartini, H.A., 2011. Analisis Variasi Waktudan Kecepatan Pengadukpada Proses Adsorpsi Limbah Logam Beratdengan Arang Aktif. Info
Teknik, 12(1), pp.11-20.
Wahistina, R., Ellyke & Pujiati, R.S., 2013. Analisis Perbedaan Penurunan Kadar BOD Dan COD pada Limbah Cair Industri Tahu Menggunakan Zeolit (Studi di Pabrik Tahu di Desa Kraton Kecamatan Kencong Kabupaten Jember). Artikel Ilmiah. Jember: Bagian Kesehatan Lingkungan dan Kesehatan dan Keselamatan Kerja, Fakultas Kesehatan Masyarakat Universitas Jember.