PENYERAPAN $TRONSIUM DENGAN SORBEN ANORGANIK
(Oksida Logam dan Zeolit)
Thamzil Las, Husen Zamroni
Pusat Pengembangan Pengelolaan Limbah Radioaktif-BATAN, Serpong
ABSTRAK
PENYERAPAN STRONSIUM DENGAN SORBEN ANORGANIK. Memisahkan zat radioaktif (Sr-90) yang terdapat dalam limbah dapat dilakukan dengan cara pengen'dapan atau dengan cara pertukaran ion anorganik antara lain zeotit lampung (ZL), zeolit Bayah (ZB), oksida logam (Ti02, dan Mn02). Limbah radioaktif cair mengandung Sr-90 dengan aktivitas awat 2,7,1O'2/!Cilmt digunakan sebagai umpan. Kemampuan penyerapan yang diperoleh pada kondisi optimum untuk ZL yaitu pad a pH 4 (Kd=6971,9 mllg), ZB pad a pH 6 (Kd= 7159,7 ml/g), Ti02 pada pH 7 (Kd=8164,4
mVg), Mn02 pad a pH 10 (Kd=55943,5 mllg), Mn02-B pada pH 12 (Kd =9035,1 mllg), Kapasitas tukar kation pad a pH
optimum ZB adalah 1,92 meq/g, ZL adalah 1,93 meq/g, Ti02 adalah 1,94 meq/g, Mn02 adalah 1,98 meq/g dan MnOz adalah 1,95 meq/g.
ABSTRACT
SEPARATION OF STRONTIUM BY INORGANIC SORBEN. The separation of Sr-90 in liquid radioactive wastes was conducted by metal oxides, i.e., Ti02 Mn02 and natural zeolites from Lampung and Bayah. Radioactive wastes containing 2,7 10-2 uCilml was used as feed solution to obtain the separation efficiency and distribution coefficient. The distribution coefficient of Sr was obtained to be 6971,9 mill on ZL (pH 4), 7159,7 mllg on ZB (pH 6), and 8164.4 ml/g on Mn02 (pH 7). The CEC value was obtained to be 1,92 meq/g on ZB, 1,93 meq/g on ZL, 1,94 meq/g on Ti02, and 1,95 meq/g on Mn02.
PENDAHULUAN
Meningkatnya
kegiatan
industri
permintaan energi mendorong manusia untuk
mencari sumber energi baru disamping
sumber energi yang sudah ada. Sumber
energi baru sebagai energi altematif yang
berkembang dengan pesat sampai saat ini
adalah sumber energi yang berasal dari
pembelahan inti-inti atom bahan fisi dan
energi
yang
dihasilkan dikenal
sebagai
energi nuklir. Penerapan teknologi nuklir
untuk
menghasilkan
energi
dapat
berkembang dengan pesat karena telah
terbukti bahwa dengan teknologi nuklir dapat
menghasilkan energi dengan biaya yang
relatif lebih murah daripada energi yang
berasal dari pembangkit listrik yang lain.
Oi samping dapat diterapkan dalam
bidang energi, teknologi nuklir dapat juga
diterapkan
dalam
bidang
kedokteran,
pertanian,
riset,
hidrologi,
industri
dan
sebagainya.
Hal
yang harus
diperhatikan dalam
pemanfaatan
teknologi
nuklir
biasanya
disertai dengan timbulnya limbah radioaktif
hal
ini
memerlukan
penanganan yang
seksama.
Limbah
radioaktif
dapat
menimbulkan bahaya pada manusia dan
lingkungan. Jadi disamping mendatangkan
manfaat yang sangat besar, teknologi nuklir
dapat juga menimbulkan limbah yang harus
dikelola dengan baik.
Pengoperasian reaktor
daya
(PLTN)
dapat
menimbulkan
unsur-unsur
yang
bersifat radioaktif akibat proses tisi maupun
aktivasi. Limbah radioaktif merupakan bahan
yang sudah tidak terpakai lagi, limbah
tersebut tidak dapat didispersikan fangsung
ke lingkungan melainkan setelah diencerkan,
atau disimpan pada tempat
dan waktu
tertentu. Penempatan limbah radioaktif ke
lingkungan dapat mendatangkan berbagai
macam akibat negatif pada manusia apabila
cara
penyimpanannya
dilakukan
tanpa
mempelajari
terlebih
dahulu
kondisi
lingkungan yang memenuhi syarat untuk
dipakai sebagai lokasi penyimpanan limbah
radioaktif maupun tidak memperhitungkan
aktivitas
limbah
radioaktif
yang
akan
disimpan.
Jalan
yang
sering
ditempuh
untuk
menekan serendah mungkin aktivitas limbah
radioaktif yang didispersikan ialah dengan
mengolah limbah terlebih dahulu sebeJum
didispersikan ke lingkungan. Jenis limbah
yang
bervariasi
menyebabkan
sistim
pengolah limbah yang bermacam-macam.
Masing-masing sistim hanya efektif jika
dipakai untuk mengolah limbah jenis yang
tertentu saja. Agar pelaksanaan pengolahan
limbah radioaktif dapat memberikan hasil
yang memuaskan, maka harus dilakukan
pemilihan proses dengan seksama sehingga
proses itu sesuai dengan jenis limbah yang
akan
diolah.
Keberhasilan
pelaksanaan
pengolahan
limbah
radioaktif
sangat
dipengaruhi
oleh
keberhasilan
dalam
melakukan pemilihan proses yang cocok
untuk mengolah limbah tersebut, sedang pemilihan proses yang cocok dapat dilakukan apabila jenis maupun aktivitas radionuklida yang terkandung dalam limbah itu diketahui.
Dalam penelitian ini dilakukan percobaan penyerapan Sr-90 dalam simulasi limbah radioaktif cair aktivitas rendah dengan menggunakan sorben Ti02, Mn02 dan Zeolit lampung (Zl) dan Zeolit B,ayah (ZB). Limbah simulasi yang dibuat sesuai dengan limbah radioaktif yang ditimbulkan oleh pengoperasian instalasi nuklir.
TAT A KERJA
setelah itu memipet 20 ml larutan limbah ini ke dalam botol yang telah terisi masing-masing adsorbent. Kemudian larutan ini dirolling dengan menggunakan Shacker-mineralogical roller selama 7 hari. Setelah disentrifuge, kemudian disentrifuge selama 10 menit dan dibiarkan selama 5 menit pula, setelah itu memipet larutan terse but masing-masing 20 ml ke dalam botol yang kosong. . Kemudian larutan ini dihitung (dicacah) dengan alat LSA untuk mengetahui kemampuan penyerapan adsorbent terhadap limbah tersebut.
Efisiensi pemisahan (Ef) dihitung dengan menggunakan rumus di bawah ini :
Sedangkan Kapasitas Tukar Kation (KTK) dan Koefisien Distribusi (Kd) dihitung dengan menggunakan rumus :
Peralatan
Beberapa peralatan yang digunakan dalam penelitian ini adalah Shacker-mineralogical roller (Karlkob) untuk pengaduk (rolling) adsorben dan cairan limbah, lSA (Liquid Scintillation Analityc) untuk pencacahan aktivitas Sr-90, Alat Centrifuge Fisher Scientific (Marathon 21K) untuk pemisahan endapan dengan filtrat cairan limbah, Timbangan digital Mettler 4E 200 untuk menentukan berat sampel, Oven pengering sam pel (WTB Binder), pH meter Coming 220 untuk pengukuran pH larutan. Bahan-bahan
Bahan-bahan kimia yang yang digunakan berkualitas PA diantaranya Ti02 99%, Mn02 90%. ZB ukuran 20-40 mesh, Zl ukuran -50+100 mesh dan Stronsiumm-90 dari Amersham dibuat sebagai limbah simulasi. Menimbang SrC12.6H20 sebanyak 5 gram kemudian ditambahkan limbah simulasi Sr-90 sampai volumenya mencapai 1000 ml ke dalam labu ukur.
Ef= Co-Ci X100% Co
dimana :
Ef =Efisiensi pemisahan Co =Aktivitas limbah awal
Cj =Aktivitas beningan
KTK =Co-Ct V
C
o
x- xN
W
KTK = Kapasitas Tukar Kation Co =Aktivitas limbah awal Ct =Aktivitas beningan V =Volume (ml) W = Berat (g) N
=
Normalitas Kd= Co - Ct V Ct Xw (1) (2) (3)Sorben yang digunakan
Zeolit mumi lampung dan Bayah dipersiapkan sesuai dengan prosedur (Thamzil dkk)menggunakan metoda sedimentasi dalam cairan metil iodida (CH31). Zeolit dan sorben lain dikeringkan pada suhu 1100C dalam oven selama 3 jam dan disimpan pada desikator yang mengandung NaCI jenuh.
Menentukan Ef, KTK dan Kd
Menimbang masing-masing adsorbent (Zl, ZB, Ti02 dan Mn02) sebanyak 0,1 gram ke dalam botol polyetylen. Menyiapkan limbah simulasi Sr-90 sebanyak 1000 ml dan menentukan pH optimum untuk masing-masing adsorbent (lL, lB, Ti02, dan Mn02)
dimana :
Kd = Koefisien distribusi W = Serat (gram) V = Volume (ml)
Co =Aktivitas limbah awal Ct =Aktivitas beningan
HASll DAN DISKUSI Pengaruh waktu kontak
Setelah di rolling beberapa waktu diperoleh waktu kontak penyerapan Sr-90 dengan adsorbent ZL dan lB memerlukan waktu 8 jam untuk mencapai kondisi optimum, sedangkan untuk Ti02 dan Mn02 masing-masing memerlukan waktu penyerapan 5 jam dan 6jam.
100 90 80 ,.... 70 ~ 60" .~'I} 50 ::!i 40 w 30 20 10 o o 4 8 12 16 20 24 Waktu (jam) 8000 r-·---·--'" 7000 • ~ :::: 6000 ~ 5000 .; 4000 .", .~ 3000 ~o 2000 ~ 1000 a o 1 2 3 4 5 6 7 8 9 10 11 pll
Gambar 1. Pengaruh waktu kontak terhadap efisiensl penyerapan
Pengaruh pH terhadap kemampuan penyerapan
Cairan limbah mengandung Sr-90 sebanyak 20 0'11 dikontakkan dengan
penukar ion anorganik, dirolling dengan kecepatan 200 rpm selama 7 hari. Kemudian dipipet 10 0'11 dan disentrifuge selama 10
menit dengan kecepatan konstan 900 rpm.
,.... 8000 -.---.., ~ 7000 -.~ 6000 '5 5000 .i!2.., 4000 ~ 3000 ;§ 2000 ~ 1000 :..: a+~--T---T---r ...·--T---·"I- ..-+1----'---'--'-,+ ---'-'---1 o 1 2 3 4 5 6 7 8 9 1011 pll
Gambar 2. Pengaruh pH pada Kd dari ZL
Halit perhltungan Kd pads borbogal pH antara 2 - 12 dapat dilihat pada Gambar 2 untuk ZL. Nilai Kd cenderung meningkat pad a pH 3-5 (6158-6456 ml/gr), dengan pH 4 mencapai Kd yang tertinggi mencapai 6972 mllg. Pada pH 6-7 cenderung rendah begitu pula nilai Kd rendah pada suasana basa.
Gambar 3 memperlihatkan hubungan ZB dengan nilai Kd cenderung r'neningkat pada pH antara 5-7. Pada pH 6 nilai Kd mencapai harga tertinggi yaitu 7160 ml/gr. Pada pH 8-11 nilai Kd cenderung sedang sekitar 3000 mllg. Pada ZB harga Kd dan 11 mulai naik
pada pH 2 - 6.
Gambar 3. Pengaruh pH pada Kd dari ZB
Hal ini dikarenakan penambahan HN03 pekat (ion HJ, sehingga harga Kd dan 11 semakin
baik, berarti pertukaran ion terjadi dengan baik, kemudian dari pH 7 - 11 terjadi penurunan.
Adsorbent ZL, harga Kd mulai mengalami kenaikan dari pH 2 sampai pH 7, hal ini dipengaruhi oleh penambahan HN03 pekat, sehingga pemisahan semakin baik. Pada pH 8 mengaJami penurunan harga Kd dan 11, kemudian pada pH 12 mencapai
optimum.
Harga KTK dari ZL oada pH optimum (pH 12) diperoleh 1,79 berarti Sr-90 yang terse rap sebanyak 1,79 meq setiap gram zeolit, sedangkan KTK dari ZB diperoleh 1,88 pada pH optimum (pH 6), Hal ini berarti kemampuan penyerapan dari ZB lebih besar dari ZL. 9000
r---l
'" 8000 • ~ 7000 -~ 6000 ..c .!= 5000 >8 4000 c: .:!:! 3000 ~ 2000 ~ 1000 a o 1 2 3 4 5 6 7 8 9 10 11 piI
Gambar 4. Pengaruh pH pada Kd dari Oksida TiOz
Gambar 4 memperlihatkan nilai Kd TiOz yang cenderung meningkat pad a pH antara 6-7 dengan nilai Kd tertinggi pada pH 7 (8184
pembentukan Ti02 sebagai penukar ion semakin baik dengan reaksi pertukaran ssebagai berikut :
4Ti02 + 2H20 2H2 Ti20S + S~+ 2H+
Tabel1 Nilai Kd dan KT
Sam pel EffisiensiKd KTK(%j 1 1805,0 82,31,6 2 3786,0 95,71,9 3 3786,0 95,81,9 Tabel 2 Nilai Kd d o o 1 2 3 4 5 6 7 8 9 1011 pH
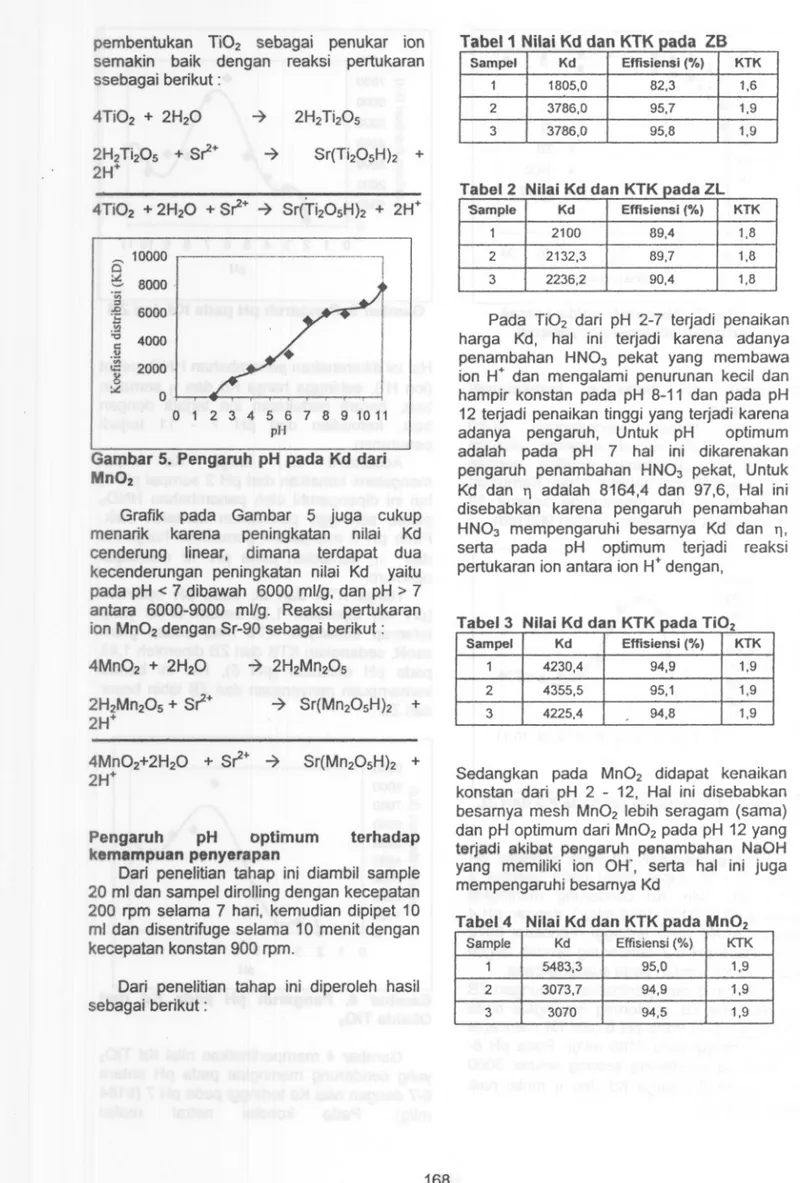
Gambar 5. Pengaruh pH pada Kd dari
MnOz
Grafik pada Gambar 5 juga cukup menarik karena peningkatan nilai Kd cenderung linear, dimana terdapat dua kecenderungan peningkatan nilai Kd yaitu pada pH < 7 dibawah 6000 mllg, dan pH > 7 antara 6000-9000 ml/g. Reaksi pertukaran ion Mn02 dengan Sr-90 sebagai berikut:
2000 'Sample EffisiensiKdKTK(%j 1 21001,889,4 2 2132,3 89,71,8 3 2236,2 90,41,8
.
Sam pel Kd EffisiensiKTK(%j 1 4230,41,994,9 2 4355,51,995,1 3 4225,41,994,8Pada Ti02 dari pH 2-7 terjadi penaikan harga Kd, hal ini terjadi karena adanya penambahan HN03 pekat yang membawa ion H+ dan mengalami penurunan kecil dan hampir konstan pada pH 8-11 dan pada pH 12 terjadi penaikan tinggi yang terjadi karena adanya pengaruh, Untuk pH optimum adalah pada pH 7 hal ini dikarenakan pengaruh penambahan HN03 pekat, Untuk Kd dan '1 adalah 8164,4 dan 97,6, Hal ini disebabkan karena pengaruh penambahan HN03 mempengaruhi besarnya Kd dan '1,
serta pada pH optimum terjadi reaksi pertukaran ion antara ion H+ dengan,
Tabel 3 Nilai Kd dan KTK Dada TiO
l
4000 100006
~ 8000 '""
:el:
6000.~
"'" c:"
.;;; 0;:8
:..:Tabel 4 Nilai Kd dan KTK Dad Pengaruh pH optimum terhadap
kemampuan penyerapan
Darl penelitian tahap in; diambil sample 20 ml dan sampel dirolling dengan kecepatan 200 rpm selama 7 hari, kemudian dipipet 10 ml dan disentrifuge selama 10 men it dengan kecepatan konstan 900 rpm.
Dari penelitian tahap ini diperoleh hasil sebagai berikut :
Sedangkan pada Mn02 didapat kenaikan konstan dari pH 2 - 12, Hal ini disebabkan besarnya mesh Mn02 lebih seragam (sama) dan pH optimum dari Mn02 pada pH 12 yang terjadi akibat pengaruh penambahan NaOH yang memiliki ion OH', serta hal ini juga mempengaruhi besarnya Kd - ---a, Sample Kd EffisiensiKTK(%j 1 5483,3 95,01,9 2 3073,7 94,91,9 3 3070 94,51,9
Tabcl 5.
Kd
&Efisiensi pemisahan pada
H
and Clay Molecular London, JJ Adsorbent PH Kd (ml/g) KTK ZL 4 6971,9 1,8 Z,B 6 7159,7 1,9 Ti02 7 8164,4 1,9 Mn02 12 9035,1 1,9 KESIMPULANBerdasarkan dari hasil-hasil yang diperoleh dari penelitian ini, dapat ditarik beberapa kesimpulan sebagai berikut : 1. Oari pengaruh waktu kontak, diperoleh
bahwa penyerapan zeolit Lampung lebih baik daripada Zeolit Bayah, penyerapan Mn02 Pabrik lebih baik dari Mn02 Buatan, dan penyerapan Mn02 Pabrik lebih baik dari Ti02, serta penyerapan Ti02 lebih baik dari Zeolit, Penyerapan Mn02 Pabrik terhadap Sr-90 lebih baik dibandingkan ke empat adsorbent diatas, 2. Kondisi optimum yang diperoleh berdasarkan percobaan yang dilakukan adalah pada pH 12 untuk Zeolit Lampung, Ti02, Mn02 Pabrik, sedangkan untuk Zeolit Bayah dan Mn02 Buatan adafah pada pH 6,
3. Pada kondisi optimum ini diperoleh efisiensi pemisahan radionuklida Sr~90 adalah :
• Untuk Zeolit Bayah sebesar 95,26% • Untuk Zeolit Lampung sebesar
98,44%
• Untuk Ti02 sebesar 88,49%
• Untuk Mn02 Pabrik sebesar 73,62%
SARAN
Dalam pengolahan limbah radioaktif cair dengan aktivitas rendah penggunaan adsobent dari alam (Zeolit) penyerapannya terhadap limbah cukup tlnggl eflslenslnya selain itu mudah didapat dan harganya lebih murah dari adsorbent sintetis.
Zeolit mempunyai tingkat pemakaian yang lebih panjang karena bentuk kristalnya lebih stabil sehingga tidak mudah hancur oleh pelapukan.
DAFTAR PUSTAKA
1. MUMPTON. FA and SAND. L.B. "Natural Zeolite, Occurrence, Properties and Uses", Pergamon Press, Oxford, (1978).
2. GASARACI, M. CECILLE. L, " New Separation Chemistry Technique for Radioactive waste and Other Specific Applications", London, Elsevier Applied Science, (1991).
3. LAWRENCE, K WANG. "Handbook of Industrial Waste Treatment", New York, Marcel Dekker, (1992)
4. EILBECK, W.J. MATTOCK. G, "Chemical Processes in Waste Water Treatment", London, Ellis Horwood, (1987).
5. LAS, THAMZIL, "Use of Natural Zeolite for Nuclear Waste Treatmen" Departement of Chemistry and applied Chemistry, Univesity of Salford, The United Kingdom (1989).
6. FLANGEN, E.M., KHATAMI, H., SZIMANSKI, H.A., Intrared Structure Studies of Zeolit Framework, Molecular Sieve Zeolit I, American Society Advances in Chemistry Series no. 101, Washington D.C., (1991)
7. BARRER, R.M., "Zeolites Minerals as Sorbents and Sieves", academic Press, (1978).
8. HAMDAN, H., "Introduction to Zeolites" : Synthesis, Characterization and Modification, University Teknologi Malaysia, Malaysia, (1992).
9. LAS, T., et al., '~ Pemanfaatan Mineral Zeolit Untuk Pengolahan Limbah", Laporan Akhir Riset Unggulan Terpadu, RISTEK / DRN, Batan, (1997).