AKSONA
Vol. 1 No. 3 September – Desember 2016Pemanfaatan Kadar Granulosit Sebagai Prediktor Risiko Infeksi
dan Keluaran Fungsional pada Penderita Stroke Akut
Fadil*, Wardah Rahmatul Islamiyah**
* Peserta PPDS Departemen Neurologi FK Universitas Airlangga - RSUD Dr. Soetomo Surabaya **Staf pengajar Departemen Neurologi FK Universitas Airlangga/RSUD Dr. Soetomo Surabaya
ABSTRAK
Latar belakang: Pada penderita stroke akut, granulosit berperan dalam proses terjadinya Stroke associated infection (SAI). Kejadian SAI akan menyebabkan buruknya keluaran klinis fungsional penderita stroke. Tujuan: Mengetahui peran jumlah granulosit pada stroke akut dalam memperkirakan risiko SAI dan keluaran klinis fungsional penderita stroke akut. Metode: jenis penelitian ini adalah observasional analitik dengan rancangan penelitian cross sectional study. Metode pengambilan sampel dengan cara consecutive sampling pada pasien stroke akut yang memenuhi kriteria inklusi dan eksklusi. Subyek penelitian yang datang ke IRD RSUD dr. Soetomo Surabaya akan diambil darahnya untuk dilakukan pemeriksaan jumlah granulosit. Kemudian subyek dinilai ada tidaknya tanda dan gejala SAI serta dinilai keluaran klinis fungsional penderita dan pada hari ke 3 dan ke 7 perawatan di ruangan saraf dengan menggunakan sistem skoring Glasgow outcome scale (GOS). Hasil: Didapatkan angka kejadian SAI pada penelitian ini sebesar 15.4%, dimana tidak didapatkan perbedaan signifikan kadar granulosit antara kelompok SAI dan tidak (p=0.938) serta tidak ada korelasi antara kadar granulosit dengan SAI (p = 0.102). Terdapat korelasi negatif kuat antara kadar granulosit saat MRS dengan keluaran fungsional stroke (GOS) pada hari ke-7 (r = -0.629, p = 0.01). Kesimpulan: Tidak ada korelasi antara kadar granulosit dengan SAI, namun terdapat korelasi negatif kuat antara kadar granulosit saat MRS dengan keluaran fungsional stroke (GOS). Pada penelitian ditemukan beberapa prediktor keluaran fungsional stroke yaitu kadar granulosit saat MRS dan skor NIHSS saat MRS.
PENDAHULUAN
Angka kejadian stroke-associated infection (SAI) adalah 21–65%. Angka ini tetap tinggi meskipun telah dilakukan berbagai upaya pencegahan seperti mengurangi tindakan invasif ataupun penggunaan antibiotika profilaksis. Hal ini terjadi karena SAI lebih dikarenakan adanya kondisi
imunodepresi paska stroke (Chammoro et al,2006).
Perkembangan ilmu pengetahuan menunjukkan bahwa sistem saraf pusat dan sistem imun merupakan dua supersistem penting yang memiliki hubungan sangat erat. Interaksi fungsional ini dapat dilihat dari terjadinya berbagai macam manifestasi imunologis paska cedera sistem saraf pusat, begitu pula sebaliknya. Benang merah yang mampu menghubungkan kedua supersistem ini adalah aksis hipotalamus-pituitari-adrenal (HPA). Kondisi ini juga dapat ditemui pada kasus stroke akut (Chammoro et al, 2007). Serangkaian otopsi pada penderita stroke yang mengalami kematian dalam minggu pertama menunjukkan bahwa
penyebab kematian tertinggi adalah kerusakan otak berupa edema serebri yang disertai herniasi transtentorial. Sedangkan penyebab kematian kedua adalah komplikasi paska stroke
akut seperti infeksi (Chammoro et al,2007). Pada berbagai
tipe stroke, 16–61% penderita akan mengalami peningkatan suhu tubuh, 21–65% di antaranya didiagnosa mengalami infeksi, dan 10–22% penderita mengalami pneumonia. Risiko tertinggi terjadinya infeksi terutama pada dua hari pertama paska serangan stroke (Meisel et al,2004).
SAI akan meningkatkan mortalitas dan memperburuk keluaran klinis penderita stroke. Prognosis stroke tergantung pada insidens komplikasi yang terjadi selama perjalanan penyakit. Pneumonia bakterial merupakan komplikasi tersering pada penderita stroke. Stroke ringan tanpa gejala sekalipun bisa menyebabkan komplikasi pneumoni ini. Penurunan refleks bulbar, penurunan kesadaran, posisi tirah baring dan aspirasi merupakan beberapa faktor yang berperan terhadap kejadian aspirasi pneumoni. Akan tetapi aspirasi saja masih belum dapat menerangkan tingginya insiden
56 Jurnal Aksona, Vol. 1. No. 3 September–Desember 2016: 55-60
pneumoni bakterial pada fase aku–t stroke. Hal terpenting yang dapat menjelaskan kejadian ini adalah peran stroke akut terhadap supresi sistem imun, yang akan menyebabkan infeksi bakterial spontan (Prass et al,2006).
Seperti telah diketahui bersama, respons aksis HPA pada kondisi stroke akut adalah peningkatan sekresi kortisol. Peningkatan komponen ini merupakan petanda adanya respons inflamasi akut dalam tubuh. Ketika terjadi stroke, mekanisme inflamasi yang terjadi memicu datangnya leukosit ke tempat inflamasi, sehingga terjadilah leukositosis. Kuantitas leukositosis yang terjadi sama dengan respons pada sistem imun (Girod dan Brotman, 2004), yaitu menyebabkan peningkatan jumlah neutrofil dan penurunan jumlah limfosit dan monosit (Coller,2005). Granulosit merupakan subtipe leukosit yang paling awal mengalami peningkatan ekspresi gen ketika terjadi stroke akut (Bhatti dan Shaikh, 2007; Buck,2008). Stress akan meningkatkan apoptosis sel limfosit
T dan Th, tetapi tidak mempengaruhi sel limfosit B (Urra et
al,2008). Beberapa proses imun tersebut yang menyebabkan
seorang penderita stroke akut mengalami penurunan sistem imun dan rentan mengalami infeksi spontan. Hal ini tentu saja akan memperburuk keluaran klinis fungsional dan meningkatkan risiko kematian penderita stroke pada fase akut. Adanya metode untuk deteksi dini risiko infeksi pada fase akut stroke, tentu saja akan sangat bermanfaat dan memberikan kontribusi penting dalam memprediksi keluaran fungsional klinis penderita dan menjadi dasar berbagai upaya pencegahan infeksi paska stroke akut. Metode ini diharapkan merupakan suatu metode yang mudah dan murah untuk dikerjakan, namun memiliki efektivitas yang tinggi dalam mendeteksi kemungkinan risiko infeksi pada penderita stroke akut. Hingga saat ini belum diketahui peran jumlah granulosit dalam memprediksi risiko SAI dan keluaran fungsional stroke akut. Oleh karena itu, peneliti mencoba membuktikan peran granulositosis dalam mendeteksi kemungkinan terjadinya risiko infeksi pada penderita stroke akut, sehingga dapat memperkirakan keluaran klinis fungsional penderita stroke pada minggu pertama.
TUJUAN
Mengetahui peran kadar granulosit pada stroke akut dalam memperkirakan risiko SAI dan keluaran klinis fungsional penderita stroke akut.
METODE PENELITIAN Jenis / rancangan penelitian
Jenis penelitian yang dilakukan bersifat observasional analitik . Subyek penelitian adalah semua pasien stroke akut yang berkunjung di IRD dan dirawat di ruang saraf RSUD Dr. Soetomo Surabaya, serta memenuhi kriteria inklusi dan eksklusi. Penelitian ini dimaksudkan untuk mencari hubungan antara jumlah granulosit dengan risiko SAI dan keluaran fungsional pasien stroke akut.
Rancangan yang dipakai adalah cross sectional study.
Rancangan ini dipilih karena dianggap sesuai dengan masalah yang diteliti serta tujuan yang hendak dicapai.
Populasi, besar sampel, teknik pengambilan sampel
• Populasi Target
Populasi dalam penelitian ini adalah semua orang penderita stroke akut
• Populasi Terjangkau
Penderita stroke akut yang berkunjung ke IRD dan dirawat di ruang saraf RSUD Dr. Soetomo pada periode Desember 2010–Agustus 2011.
• Sampel Penelitian
Penderita stroke akut yang berkunjung ke IRD dan dirawat di ruang saraf RSUD Dr. Soetomo dan memenuhi kriteria inklusi–eksklusi selama periode Desember 2010–Agustus 2011.
• Kriteria inklusi dan eksklusi
Kriteria Inklusi
1. Penderita stroke akut
2. NIHSS saat masuk rumah sakit 0–15 3. Onset kurang dari 24 jam
4. GCS lebih dari 11
5. Hasil CT scan menunjukkan lesi vaskuler berupa trombotik atau perdarahan
6. Usia antara 30–65 tahun. 7. Jenis kelamin pria
8. Tidak mengalami infeksi sebelum serangan (luka,panas)
9. Tidak mengalami penyakit jantung iskemik akut
10. Tidak terdapat gangguan metabolik (elektrolit, fungsi liver, fungsi ginjal, dan asam basa) 11. Tidak ada riwayat menggunakan antibiotika
dalam kurun waktu maksimal 3 minggu sebelum serangan stroke
Kriteria Eksklusi
1. Tidak bersedia ikut dalam penelitian 2. Mengundurkan diri
3. Meninggal selama periode penelitian • Teknik pengambilan sampel
Metode pengambilan sampel penelitian dilakukan
menurut kasus yang datang berturut – turut (sampling
from consecutive admission) sampai tercapai jumlah sampel yang telah ditetapkan.
Lokasi penelitian
Pengambilan sampel penelitian dilakukan di IRD dan ruang saraf RSUD Dr. Soetomo, Surabaya.
Rancangan analisis data
• Data yang diperoleh dari lembar pengumpulan data kemudian diperiksa
• Perbedaan kadar granulosit antara kelompok SAI dan tidak dianalisis dengan t-test.
57 Fadil dan Wardah Rahmatul Islamiyah: Pemanfaatan Kadar Granulosit
dengan analisis pearson. Kemudian dilakukan analisis
multivariate untuk beberapa faktor yang diduga berperan sebagai prediktor GOS dengan menggunakan regresi linear ANOVA
• Untuk korelasi gula darah dan NIHSS saat MRS dengan
GOS dianalisis dengan spearman
HASIL
Penelitian dilakukan selama ± 10 bulan dan diperoleh besar sampel penelitian 26 sampel
Karakteristik Subyek Penelitian
Pada penelitian ini dilakukan uji normalitas sebaran data dasar dengan menggunakan uji Shapiro-Wilk, ditemukan data dengan distribusi yang normal pada variabel usia, tekanan darah sistolik, tekanan darah diastolik, leukosit saat MRS, granulosit saat MRS(p >0.05) tampak pada tabel 1. Dari 26
subyek penelitian, ditemukan 4 orang (15.4%) mengalami
SAI selama perawatan tujuh hari di ruangan rawat inap Dep/ SMF Neurologi RSUD dr. Soetomo.
Karakteristik Subyek yang Mengalami SAI dan Tidak Mengalami SAI
Untuk mengetahui karakteristik subyek yang mengalami SAI dan tidak, maka dilakukan perbandingan beberapa karakteristik, dengan hasil yang tampak pada tabel 2. Dari tabel 2 tampak bahwa tidak ada perbedaan yang signifikan pada beberapa variabel dasar. Karena memang pada penelitian ini diupayakan semua subyek dalam kondisi yang hampir sama, dengan harapan memperkecil pengaruh faktor lain yang akan mempengaruhi memburuknya outcome dan kejadian SAI.
Pada studi ini memang tidak dijumpai perbedaan signifikan rerata jumlah granulosit antara kelompok SAI dan tidak (p = 0.938), akan tetapi bila diamati, tampak bahwa dari 4 subyek yang mengalami SAI, memiliki rerata
jumlah granulosit saat MRS 75.175 ± 11.793 gr%. Angka
ini menunjukkan angka di atas normal, mengingat jumlah granulosit normal adalah 65–75 gr%. Sedangkan rerata jumlah granulosit saat MRS pada kelompok yang tidak
Skema alur penelitian
4 10.Tidak terdapat gangguan metabolik (elektrolit, fungsi liver, fungsi ginjal,
dan asam basa)
11.Tidak ada riwayat menggunakan antibiotika dalam kurun waktu maksimal 3 minggu sebelum serangan stroke
Kriteria Eksklusi
1. Tidak bersedia ikut dalam penelitian 2. Mengundurkan diri
3. Meninggal selama periode penelitian
Teknik pengambilan sampel
Metode pengambilan sampel penelitian dilakukan menurut kasus yang datang berturut – turut (sampling from consecutive admission) sampai tercapai jumlah sampel yang telah ditetapkan.
Lokasi penelitian
Pengambilan sampel penelitian dilakukan di IRD dan ruang saraf RSUD Dr. Soetomo, Surabaya.
Rancangan analisis data
Data yang diperoleh dari lembar pengumpulan data kemudian diperiksa Perbedaan kadar granulosit antara kelompok SAI dan tidak dianalisis dengan t-test. Korelasi antara kadar granulosit dan GOS dinilai dengan analisis pearson. Kemudian dilakukan analisis multivariate untuk beberapa faktor yang diduga berperan sebagai prediktor GOS dengan menggunakan regresi linear ANOVA Untuk korelasi gula darah dan NIHSS saat MRS dengan GOS dianalisis dengan spearman
Skema alur penelitian
Penderita stroke akut yang datang ke IRD RSUD Dr. Soetomo Surabaya
Sampel penelitian
Pemeriksaan granulosit
Analisa statistik
Inklusi Eksklusi
Pemeriksaan GOS pada hari ke 7 perawatan Pemeriksaan adanya tanda
dan gejala SAI pada hari ke 3 dan 7 perawatan
mengalami SAI selama masa perawatan masih dalam batas normal. Sehingga tetap perlu diwaspadai risiko SAI pada pasien yang memiliki jumlah granulosit saat MRS lebih dari 75 gr%.
Untuk mengetahui risiko kejadian SAI terkait kadar granulosit, maka dilakukan pengelompokan kadar granulosit menjadi kelompok normal (<75 gr%) dan kelompok kadar granulosit tinggi (>75 gr%) (lihat tabel 9.3). Kemudian dilakukan analisis regesi logistik dengan hasil tidak didapatkan korelasi yang bermakna antara kadar granulosit
dengan SAI (p = 0.102) tampak pada tabel 3.
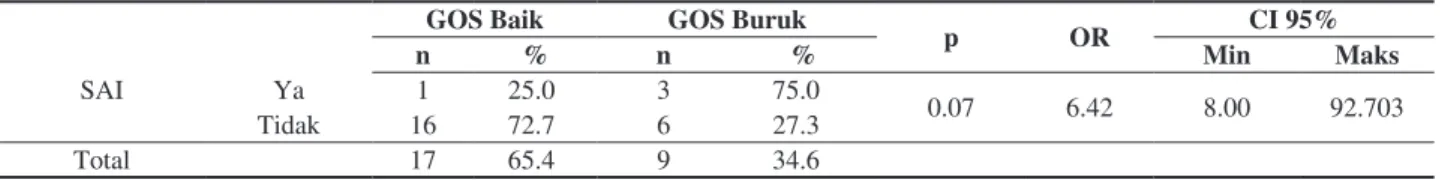
Untuk mengetahui peran SAI terhadap GOS, maka dilakukan pengelompokan GOS. Untuk nilai GOS ≤ 3 dimasukkan dalam kelompok buruk, nilai GOS ≥ 4 baik. Kemudian dilakukan analisis korelasi kelompok SAI dengan
GOS (tabel 4). Dari pemeriksaan crosstab tidak didapatkan
korelasi antara SAI dengan GOS (p = 0.07). Hal ini sesuai
dengan hasil tabel 3 yang menunjukkan tidak ada perbedaan signifikan GOS hari ke-7 antara kelompok SAI dan tidak (p = 0.082).
Selanjutnya dilakukan analisis multivariate untuk mengetahui kekuatan prediktor dari granulosit terhadap GOS dengan mengikutsertakan faktor – faktor karakteristik subyek penelitian lainnya dengan menggunakan analisis regresi linier (tabel 5). Pada penelitian ini ditemukan ada tiga variabel yang memiliki nilai korelasi yang signifikan yaitu kadar leukosit saat MRS, granulosit saat MRS dan NIHSS saat MRS (p < 0.05).
PEMBAHASAN
Pada penelitian ini didapatkan angka kejadian infeksi paska stroke adalah 15,4%. angka ini hampir sama dengan beberapa studi lain yang menyebutkan angka kejadian infeksi paska stroke dini adalah 16% (Hamidon, 2003). Ionita dkk menyebutkan prevalensi SAI adalah 11.2–22% (Ionita, 2011). Sedangkan studi lain menyebutkan sekitar 26% penderita stroke akut akan mengalami SAI dalam tujuh hari pertama onset stroke (Vargas et al,2006). Studi lain yang lebih spesifik menyebutkan bahwa angka kejadian infeksi saluran nafas paska stroke adalah 1 – 33% sedangkan angka kejadian infeksi saluran kemih 2 – 27% Variasi rentang angka kejadian ini disebabkan oleh perbedaan seting studi. Kejadian SAI akan lebih sering dijumpai pada pasien yang menjalani perawatan di ruang perawatan intensif. (Emsley, 2008).
Faktor risiko terjadinya SAI adalah sebagai berikut : kondisi pasien yang buruk saat masuk rumah sakit, infark sirkulasi anterior total, Barthel Index kurang dari 5, Glasgow Coma Scale kurang dari 9, infark di teritori arteri cerebri media, usia tua, atrial fibrilasi, jenis kelamin
wanita, penggunaan NGT, riwayat congestive heart failure,
penggunaan ventilator, infark ganglia basalis non lakunar, disfagia, NIHSS lebih dari 10, abnormalitas foto thoraks saat masuk rumah sakit dan riwayat DM (Emsley 2008). Beberapa faktor risiko tersebut sudah dicoba untuk dikontrol oleh peneliti melalui beberapa komponen kriteria inklusi
58 Jurnal Aksona, Vol. 1. No. 3 September–Desember 2016: 55-60
dan menggunakan seting rawat inap biasa (bukan perawatan intensif). Setelah dilakukan analisis multivariate diketahui bahwa kadar granulosit dan skor NIHSS saat masuk rumah sakit memiliki peran besar sebagai beberapa prediktor penting bagi keluaran fungsional stroke (GOS).
Banyak komponen darah pada pemeriksaan darah sederhana yang dapat digunakan sebagai prediktor SAI. Seperti halnya monosit. Monosit adalah mayor sel dari imunitas innate yang juga berperan pada imunitas adaptif. Monosit dapat mencapai susunan saraf pusat dalam 4 jam onset stroke dan mengalami infiltrasi maksimal hingga 7 hari paska stroke. Akan tetapi komponen ini tidak kami pilih karena pada suatu studi eksperimental diketahui bahwa monosit selain dapat memicu proses inflamasi paska stroke juga berperan dalam proses resoluasi inflamasi, sehingga monosit bisa berperan ganda sebagai proinflamasi maupun antiinflamasi, tergantung diferensiasi dan mekanisme yang diaktivasi. Diferensiasinya tidak dapat diprediksi rentang waktunya (Urra et al, 2009).
Bila dilihat dari hasil penelitian ini, ternyata tidak ada korelasi antara kadar granulosit dengan SAI. Akan tetapi didapatkan korelasi negatif kuat (r = -0.629) antara granulosit dengan GOS. Hal ini menunjukkan bahwa ternyata peran granulosit terhadap lebih utama melalui mekanisme kerusakan sawar darah otak dan bukan melalui mekanisme SAI. Pemilihan granulosit disebabkan oleh karena adanya komponen dalam granul sitoplasma granulosit berupa matriks metaloproteinase (MMP-9) yang akan merusak kolagen pembuluh darah dan sawar darah otak, yang berakibat edema serebri. Terjadinya edema serebri akan memperburuk keluaran klinis fungsional penderita stroke akut (Nakagawa et al,1998).
Granulosit mengandung sejumlah enzim proteolitik yang tersimpan dalam granul intrasel, di antaranya adalah serine protease, cathepsin G, elastase, gelatinase dan matrix metalloproteinase-9 (MMP-9). MMP 9 merupakan mediator patologis kuat pada saat fase akut stroke. Enzim ini akan menyebabkan proteolisis bahan neurovaskular seperti protein tight juction yang penting bagi integritas sawar darah otak dan merupakan komponen matrik ekstraseluler yang berhubungan dengan viabilitas pembuluh darah dan sel neuronal serebral. Protein spesifik sawar darad otak yang diserang oleh MMP-9 neutrofil adalah claudin-5. Peningkatan neutrofil pada fase akut stroke tentu saja akan menyebabkan gangguan permeabilitas sawar darah otak. Gangguan ini bersifat irreversibel (Horstmann,2003; McColl et al,2008; Rosenberg,2009).
Akumulasi peningkatan granulosit ini akan bertahan dalam jumlah yang tinggi selama 6–24 jam paska onset dan selanjutnya akan mengalami penurunan tapi masih dapat diukur hingga 5 minggu. perifer (Audebert et al,2004). Hal inilah yang menjadi dasar pemilihan subyek penelitian dengan onset kurang dari 24 jam, untuk mendapatkan akumulasi granulosit dalam darah.
Penelitian ini juga membuktikan dugaan adanya peran granulosit sebagai salah satu prediktor untuk keluaran fungsional stroke akut pada hari ke-7, didapatkan korelasi
negatif kuat antara kadar granulosit saat masuk rumah sakit dengan keluaran fungsional stroke (GOS) pada hari ke-7 yaitu r = -0.629 (p = 0.01).
Temuan ini diharapkan bisa dijadikan dasar dalam menentukan strategi terapi untuk mendapatkan keluaran fungsional yang baik, melalui temuan adanya granulositosis pada saat awal masuk rumah sakit (kurang dari 24 jam onset). Pemeriksaan granulosit merupakan pemeriksaan sederhana, murah, termasuk dalam pemeriksaan darah lengkap rutin pada semua penderita stroke akut. Sehingga diharapkan dengan pemanfaatan komponen sederhana ini dapat dilakukan strategi penatalaksanaan yang tepat untuk mencegah outcome yang buruk. Strategi yang diberikan bisa dengan pemberian obat yang menekan inflamasi maupun terapi untuk menghambat peran MMP-9 yang mempengaruhi keluaran fungsional. Peran granulosit terhadap MMP-9 yang menyebabkan proteolisis bahan neurovaskular seperti protein tight juction yang penting bagi integritas sawar darah otak dan merupakan komponen matrik ekstraseluler yang berhubungan dengan viabilitas pembuluh darah dan sel neuronal serebral. Protein spesifik sawar darad otak yang diserang oleh MMP-9 neutrofil adalah claudin-5. Peningkatan neutrofil pada fase akut stroke tentu saja akan menyebabkan gangguan permeabilitas sawar darah otak. Gangguan ini bersifat irreversibel. Adanya MMP-9 merupakan prognostik buruk pada stroke (Horstmann, 2003). MMP-9 dapat diinhibisi oleh enzim tissue inhibitors of metalloproteinase (TIMP)-1 (Rosenber, 2009). Oleh karena itu dicoba dikembangkan berbagai obat untuk mengaktifkan TIMP-1, di antaranya adalah penggunaan simvastatin yang dapat meningkatkan rasio MMP-9/TIMP serum pada pasien stroke iskemik akut (Kurzepa, 2006).
KESIMPULAN
• Angka kejadian SAI pada penelitian ini 15.4%. • Tidak didapatkan perbedaan signifikan kadar granulosit
antara kelompok SAI dan tidak (p=0.938) dan tidak
ada korelasi antara kadar granulosit dengan SAI (p =
0.102).
• Terdapat korelasi negatif kuat antara kadar granulosit saat MRS dengan keluaran fungsional stroke (GOS)
pada hari ke-7 (r = -0.629, p = 0.01)
• Pada penelitian ditemukan beberapa prediktor keluaran fungsional stroke yaitu kadar granulosit saat MRS dan skor NIHSS saat MRS.
SARAN
• Perlu dilakukan penelitian dengan seting perawatan intensif, karena pada kelompok tersebut lebih memiliki risiko tinggi untuk mengalami SAI.
• Perlu dilakukan penelitian lanjutan untuk mencari prediktor outcome stroke selain kadar granulosit saat MRS dan skor NIHSS saat MRS.
• Perlu dilakukan penelitian lanjutan mengenai peran beberapa strategi terapi untuk menekan fungsi granulosit, sebagai upaya mencegah keluaran fungsional stroke yang buruk.
DAFTAR PUSTAKA
Aminoff MJ, Greenberg DA, Simon RP, 2005. Clinical Neurology 6thed.
New York: Lange Medical Books/McGraw-Hill, pp. 285–319 Audebert HJ et al, 2004. Systemic inflammatory respons depends on
initial stroke severity but is attenuated by succesfull thrombolysis. Stroke 25: 2128–2133.
Bhatti R, Shaikh D M, 2007. The Effect of Exercise on Blood Parameters. Pak J Physiol 3(2): 1–3
Boehr M, Frotscher M, 2005. Hypothalamus in Duus’s Topical Diagnosis in neurology. 4th completely revised edition : Thieme Stuttgart,pp 284–288
Buck B H et al, 2008. Early Neutrophilia Is Associated With Volume of Ischemic Tissue in Acute Stroke. Stroke 39: 355–360
Chamorro A et al, 2006. Interleukin 10, monocytes and increased risk of early infection in ischaemic stroke. J Neurol Neurosurg Psychiatry 77:1279–1281
Chamorro A, Urra X, Planas AM, 2007. Infection after Acute Ischemic Stroke A Manifestation of Brain-Induced Immunodepression, Stroke 38:1097–1103
Chrousos GP,1995.The hyphothalamic-pituitary-adrenal axis and immune-mediated inflammation. The New England Journal of Medicine 332(20):1352–1362
Coller B S, 2005. Leukocytosis and Ischemic Vascular Disease Morbidity and Mortality : Is It Time to Intervene ? Arterioscler Thromb Vasc Biol 25: 658–670
Dimopoulou I et al, 2005. Endocrine Alteration in Critically Ill Patients with Stroke During the Early Recovery Period. Neurocritical Care 03: 224–229
Dirnagl U et al, 2007. Stroke-induced immunodepression : Experimental evidence and clinical relevance. Stroke 38:770–773
Emsley HCA, Hopkins SJ, 2008. Acute Ischaemic Stroke and Infection : recent and emerging concepts. Lancet (7):341–353
Girod J P, Brotman D J, 2004. Does altered glucocorticoid homeostasis increase cardiovascular risk ? Cardiovascular Research 64: 217– 226
Hamidon EE et al, 2003. The Predictors of Early Infection After An Acute Ischemic Stroke. Singapore Med J 44(7): 344–346
Hilker R et al,2003. Nosocomial pneumonia after acute stroke implication for neurological intensive care medicine. Stroke 34:975–981 Horstmann S et al, 2003. Profiles of Matrix Metalloproteinases, Their
Inhibitors, and Laminin in Stroke Patients Influences of Different Therapies. Stroke 34:2165–2172
Ionita CC et al, 2011. Acute Ischemic Stroke and Infections, Journal of Stroke and Cerebrovascular Disease 20(1):1–9
Jennett B, 2005. Development of Glasgow coma and outcome scales. Nepal Journal of Neuroscience 2: 24–28
Kurzepa J et al, 2006. Simvastatin could prevent increase of the serum MMP 9/TIMP ratio in acute ischemic stroke. Folia Biologica (Praha) 52:181–183
Li F, Omae T, Fisher M, 1999. Spontaneous Hyperthermia and its Mechanism in the Intraluminal Suture Middle Cerebral Artery Occlusion Model of Rats. Stroke 30: 2464–2471
Licinio J, Frost P, 2000. The neuroimmune-endocrine axis: pathophysiological implication for the central nervous system cytokines and hypothalamus-pituitary-adrenal hormone dynamics. Brazilian Journal of Medical and Biological Research 33: 1141– 1148
McColl BW, Rothwell NJ, Allan SM, 2008. Systemic inflammation alters the kinetics of cerebrovascular tight junction disruption after experimental stroke in mice. The Journal of Neuroscience 28(38):9451–9462
Meisel C et al, 2004. Preventive antibacterial treatment improves the general medical and neurological outcome in a mouse model of stroke. Stroke 35:2–6
Nakagawa M et al, 1998. Glucocorticoid-induced granulocytosis : Contribution of marrow release and demargination of intravascular granulocytes. Circulation 98:2307–2313
Nakagawa T et al, 1997. High incidence of pneumonia in elderly patients with basal ganglia infarction. Arch Intern Med 157:321–324 Offner H et al,2006. Splenic atrophy in experimental stroke is accompanied
by increased regulatory T cells and circulating macrophages. J Immunol 176:6523–6531
Olsson T et al, 1992. Abnormalitas at Different Levels of the Hypothalamic-Pituitary-Adrenocortical Axis Early After Stroke. Stroke 23: 1573–1576
Prass K et al,2006. Stroke propagates bacterial aspiration to pneumonia in a model of cerebral ischemia. Stroke 37:2607–2612
Rosenberg, 2009. Matrix Metalloproteinases and their multiple roles in neurodegenartive disease. Lancet 8:205–217
Turnbull A V, Rivier C L, 1999. Regulation of the Hypothalamic-Pituitary-Adrenal Axis by Cytokines: Actions and Mechanisms of Action. Physiological Reviews 79(1):1–71
Urra X et al, 2008. Harms and Benefits of Lymphocyte Subpopulations in Patients with Acute Stroke. Neuroscience xx(xxx): 1–10
Urra X et al,2009. Monocytes are major players in the prognosis and risk of infection after acute stroke. Stroke 40:1262–1268
Vargas M et al, 2006. Clinical consequences of infection in patients with acute stroke : Is it prime time for further antibiotic trial? Stroke 37:461–465
Whyte D G, Johnson A K, 2007. Lesions of the anteroventral third ventricle region exaggerate neuroendocrine and thermogenic but not behavioral responses to a novel environment. Am J Physiol Regul Integr Comp Physiol 292: R137–R142
LAMPIRAN
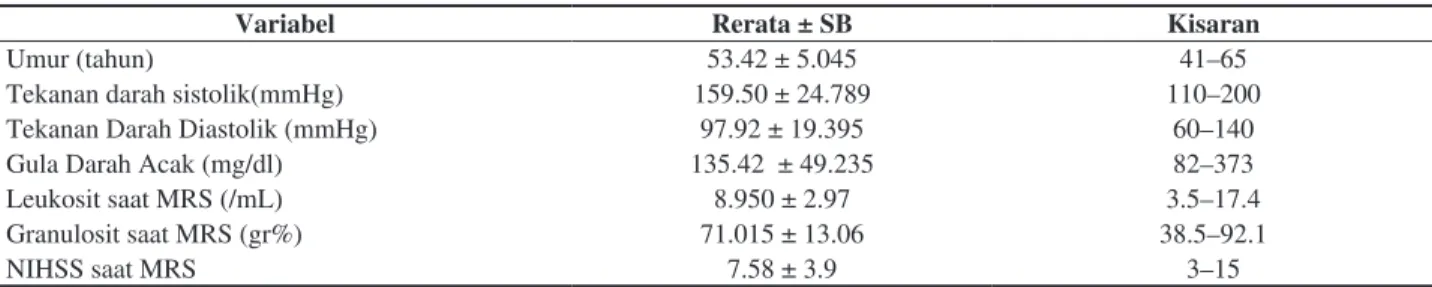
Tabel 1. Karakteristik Subyek Penelitian.
Variabel Rerata ± SB Kisaran
Umur (tahun) 53.42 ± 5.045 41–65
Tekanan darah sistolik(mmHg) 159.50 ± 24.789 110–200
Tekanan Darah Diastolik (mmHg) 97.92 ± 19.395 60–140
Gula Darah Acak (mg/dl) 135.42 ± 49.235 82–373
Leukosit saat MRS (/mL) 8.950 ± 2.97 3.5–17.4
Granulosit saat MRS (gr%) 71.015 ± 13.06 38.5–92.1
60 Jurnal Aksona, Vol. 1. No. 3 September–Desember 2016: 55-60
Tabel 2. Perbandingan karakteristik subyek penelitian SAI dan tidak.
Variabel SAI (+) SAI (-) p
Umur (tahun) 55 ± 3.162 53.03 ± 6.344 0.172 TD sistolik (mmHg) 167.50 ±22.174 158.57 ± 24.640 0.748 TD diastolik (mmHg) 102.50 ± 28.723 97.20 ± 16.380 0.289 GDA (mg/dL) 116.50 ± 18.664 145.27 ± 73.385 0.235 Leukosit saat MRS (/mL) 10.900 ± 3.486 9.060 ± 3.0705 0.962 Granulosit saat MRS (gr%) 75.175 ± 11.793 70.259 ± 13.395 0.938 NIHSS saat MRS 9.25 ± 3.862 7.27 ± 3.918 0.414
GOS hari ke-7 2.75 ± 2 4,05 ± 1 0.082
Hasil CT scan 2 pasien ICH 1 pasien iskemik1 pasien normal
Tabel 3. Hasil analisis bivariate kadar granulosit dengan risiko SAI.
SAI Tidak SAI
p OR CI 95%
n % n % Min Maks
Kelompok
granulosit TinggiN 13 30.06.2 157 93.870.0 0.102 6.42 0.563 73.351
Total 4 15.4 22 84.6%
Tabel 4. Hasil analisis bivariate SAI dengan GOS.
GOS Baik GOS Buruk
p OR CI 95%
n % n % Min Maks
SAI Ya 1 25.0 3 75.0 0.07 6.42 8.00 92.703
Tidak 16 72.7 6 27.3
Total 17 65.4 9 34.6
Tabel 5. Rekapan tabulasi silang korelasi karakteristik subyek penelitian dengan GOS.
No Variabel r P value Simpulan
1 2 3 4 5 6 7 Umur
Tekanan darah sistolik Tekanan darah diastolik Kadar leukosit saat MRS Kadar granulosit saat MRS Gula darah acak
NIHSS saat MRS -0.045 0.096 -0.007 -0.513 -0.629 0.769 -0.573 0.825 0.640 0.971 0.07 0.01 0.769 0.02 Tidak signifikan Tidak signifikan Tidak signifikan signifikan Signifikan Tidak signifikan Signifikan Jumlah 26 100.00