BAB II
DASAR TEORI
Pembelajaran tentang proses pengolahan besi merupakan hal yang penting untuk dipelajari, mengingat logam tersebut digunakan pada berbagai macam aplikasi. Teknik yang paling umum digunakan secara komersial yaitu dengan menggunakan blast furnace dan juga converter. Pada blast furnace reaksi yang terjadi yaitu sebagai berikut [8] :
• 3Fe2O3+CO Î 2 Fe3O4+CO2
3Fe2O3+C Î 2 Fe3O4+CO
• Fe3O4+CO Î 3FeO+CO2
Fe3O4+ C Î 3FeO+CO
• FeO+CO Î Fe+CO2
FeO+C Î Fe+CO
Meskipun dapat terlihat bahwa bijih besi dapat direduksi secara langsung dengan menggunakan karbon padat, namun reduksi dengan menggunakan gas CO mengindikasikan reaksi utama yang terjadi pada beberapa percobaan reduksi bijih besi yang telah dilakukan [9-13].
Pemrosesan reduksi bijih besi dengan menggunakan blast furnace memiliki kelemahan utama, yaitu karena temperatur proses yang terlalu tinggi maka logam lain ( Si, Mn, dll.) akan banyak yang ikut melebur bersama dengan Fe sehingga akan sulit untuk dipisahkan. Oleh karena itu dikembangkan suatu metode baru untuk mengatasi hal tersebut dengan menggunakan proses reduksi langsung.
Proses reduksi langsung adalah proses pengurangan oksigen dari besi oksida dimana besi oksida tersebut tidak mengalami perubahan fasa, yaitu fasa padat. Proses reduksi langsung menggunakan zat pereduksi yang afinitas terhadap
oksigen lebih besar daripada besi oksida. Proses ini dilakukan dengan menggunakan temperatur tinggi, namun lebih rendah dari temperatur yang digunakan pada pemrosesan dengan menggunakan blast furnace.
Banyak studi yang dilakukan untuk mempelajari proses reduksi langsung, Usui et al. mempelajari tentang proses prereduksi pada besi oksida dengan menggunakan batu bara dan juga gas dengan reaksi utama yang terjadi antara besi oksida dan hydrogen [14]. Ishikawa et al. secara sukses mempelajari tentang reduksi pada wustit (Fe1)xO dengan menggunakan karbon padat [15] .
Untuk lebih memahami proses reduksi langsung, dipaparkan pada dasar teori dibahan ini :
2.1 PRINSIP DASAR PROSES REDUKSI BESI OKSIDA
Proses reduksi langsung merupakan reduksi bijih besi dengan menghindari fasa cair. Proses ini dilakukan dengan menggunakan pereduktor seperti karbon (coal), minyak bumi dan juga gas metana (CH4). Prinsip dasar proses ini adalah
mengurangi kadar oksigen dengan menggunakan unsur yang afinitas terhadap O (oksigen) lebih besar daripada Fe (besi). Proses ini dilakukan tanpa mengubah fasa, yaitu fasa padat. Hasil akhir proses ini menghasilkan bijih besi yang didalamnya masih terdapat oksida. Proses reduksi langsung digunakan dengan beberapa alasan sebagai berikut :
a. Menggunakan batu bara/ gas bumi sebagai pengganti kokas b. Produk berkualitas tinggi
c. Kapasitas produksi bisa rendah, sesuai dengan permintaan pasar d. Emisi CO2 rendah sehingga lebih ramah terhadap lingkungan
2.1.1 Termokimia
Reaksi kimia selalu melibatkan pelepasan maupun penyerapan energi. Hal tersebut menunjukkan bahwa setiap material memiliki energi. Energi dilepaskan apabila dalam suatu reaksi produk memiliki energi yang lebih rendah daripada pereaktan, sedangkan suatu reaksi dikatakan menyerap energi apabila produk memiliki energi yang lebih tinggi daripada pereaktan [16].
Panas merupakan bentuk energi yang umum pada suatu reaksi. Derajat panas juga dapat diukur dengan suhu. Panas yang dimiliki oleh suatu material merupakan entalpi dari material tersebut yang diberi lambang H.
Ketika suatu unsur bereaksi dengan unsur lain membentuk suatu senyawa, energi panas yang digunakan pada reaksi tersebut disebut sebagai energi panas pembentukan (entalpi pembentukan) yang diberi lambang ∆Hf. Contoh entalpi
pembentukan adalah sebagai berikut :
C + ½O2 Î CO ∆Hf = - 26.416 cal/mol
C + O2 Î CO2 ∆Hf = - 94.052 cal/mol
Ketika suatu senyawa bereaksi dengan senyawa lain membentuk suatu senyawa baru maka ∆Hf berubah menjadi ∆Hpenguraian, oleh karena itu besar
∆Hf harus dibalik. Contohnya sebagai berikut :
Apabila ∆H reaksi bernilai positif maka reaksi merupakan reaksi endotermik (menyerap panas). Apabila ∆H bernilai negatif maka reaksi merupakan reaksi eksotermik ( melepaskan panas).
2.1.2 Energi Bebas
Energi bebas merupakan selisih antara total energi pada sistem dengan energi ikatan, TS. Energi bebas reaksi kimia pada temperatur konstan dirumuskan sebagai berikut [16]:
∆ ∆ ∆ ………..(2.1)
Keterangan :
∆F = Energi bebas cal/mol ∆H = Entalpi cal/mol
T = Temperatur K
∆S = Perubahan entropi
Fe3O4 + CO Î 3FeO + CO2 ∆H = + 30664
Apabila ∆F bernilai negatif maka reaksi tersebut dapat berjalan secara spontan, namun apabila suatu reaksi ∆F bernilai positif maka reaksi tersebut tidak dapat berjalan secara spontan. Contoh energi bebas beberapa reaksi sebagai berikut [16] :
2Fe + O2Æ 2FeO ∆FTo = -124.100 + 29.90T cal/molO2 (298 – 1642oK)
6FeO + O2Æ2Fe3O4 ∆FTo = -149.240 + 59.80T cal/molO2 (298 – 1642oK)
4Fe3O4 + O2Æ6Fe2O3 ∆FTo = -119.240 + 67.24T cal/molO2 (298 – 1460oK)
2C + O2Æ 2CO ∆FTo = -53.400 - 42.0 T cal/molO2 (298 – 2500oK)
C + O2Æ CO2 ∆FTo = -94.200 - 0.2 T cal/molO2 (298 – 2000oK)
2CO + O2Æ 2 CO2 ∆FTo = -135.000 + 41.6 T cal/molO2(298 – 2000oK)
C + CO2 Æ2CO ∆FTo = +40.800 + 41.8 T cal/molO2 (298 – 2000oK)
2H2 + O2Æ2H2O ∆FTo = -117.800 + 26.2 T cal/molO2(298 – 2500oK)
Energi bebas suatu reaksi juga dapat ditentukan dengan menggunakan prinsip kesetimbangan kimia. Pada reaksi kimia :
A + B Î C + D
Kecepatan reaksi pereaktan sama dengan kecepatan pereaksi produk (Vpereaktan = Vproduk). Energi bebas dapat ditentukan dengan Persamaan 2.2.
∆ ° RTlnK RTln CA DB………..……….(2.2)
Keterangan :
∆Fo = Energi bebas cal/mol R = konstanta gas
T = Temperatur K
a = aktivitas
Aktivitas pada gas sama dengan tekanan parsial yang dimiliki oleh gas tersebut. Untuk material padat dan cair, sama dengan konsentrasi yang dimiliki.
Energi bebas yang dimiliki oleh suatu reaksi dapat diplot kedalam suatu grafik bersama dengan temperatur. Grafik yang memuat energi bebas versus temperatur disebut sebagai Diagram Ellingham seperti ditunjukkan pada Gambar 2.1. Pada diagram Ellingham, logam yang aktif secara kimia memiliki energi bebas yang paling tinggi (negatif) dalam membentuk oksida terletak pada diagram dibagian paling bawah. Sedangkan untuk logam yang memiliki energi bebas terkecil (positif) dalam membentuk oksida terletak pada diagram dibagian paling atas. Nilai dari ∆Fo untuk reaksi oksidasi merupakan ukuran afinitas kimia suatu logam terhadap oksigen. Semakin negatif nilai ∆Fo suatu logam menunjukkan logam tersebut semakin stabil dalam bentuk oksida.
Dari diagram Ellingham pada Gambar 2.1, kita dapat mengetahui temperatur minimal yang dibutuhkan agar reaksi tersebut dapat terjadi. Hal tersebut dapat ditunjukkan oleh perpotongan antara kurva oksidasi dan reduksi.
Termodinamika hanya dapat digunakan untuk menentukan apakah suatu reaksi dapat berjalan spontan ataukah tidak pada temperatur tertentu berdasarkan energi bebas yang dimiliki. Namun tidak dapat digunakan untuk menentukan laju reaksi. Perpotongan antara garis reaksi oksidasi dan reduksi secara termodinamika menunjukkan bahwa reaksi tersebut dapat berjalan pada temperatur tertentu.
Selain menggunakan diagram Ellingham, kita juga dapat menentukan termodinamika suatu reaksi melalui perhitungan energi bebas ∆F dari reaksi tersebut dengan menggunakan ∆Fo referensi seperti yang telah tercantum diatas.
2 t ( ( ( 2.1.3 Term Reak tahap antara (I) 3 Fe2 (II) Fe3O (III) FeO+ G modinamika ksi reduksi d a lain [16] : Fe2O3 2O3 +CO Î O4+CO Î +CO Î Gambar 2.1 D a Reaksi Re dengan meng I Î Fe3 Î 2 Fe3O Î 3FeO+ Î Fe+CO Diagram Elli eduksi Besi ggunaan karb II O4 Î F O4+CO2 +CO2 O2 ingham [16] Oksida bon monoks III FeO Î ∆H = -∆H = ∆H = -ida (CO) me Fe 12636 cal 8664 cal 4136 cal emiliki tiga
Secara termodinamika energi bebas dari ketiga reaksi tersebut dapat ditentukan sebagai berikut :
Persamaan (I)
6Fe2O3 Æ 4Fe3O4 + O2 ∆FTo = +119.240 - 67.24T cal/molO2
2CO + O2Æ 2 CO2 ∆FTo = -135.000 + 41.6 T cal/molO2
6Fe2O3 + 2CO Î 4Fe3O4+ 2CO2 ∆FTo = -15.760 - 25.64 T cal/molO2
Atau
3Fe2O3 + CO Î 2Fe3O4+ CO2 ∆FTo = -7.880 - 12.82 T cal/molO2
Persamaan (II)
2Fe3O4Æ6FeO + O2 ∆FTo = +149.240 - 59.80T cal/molO2
2CO + O2Æ 2 CO2 ∆FTo = -135.000 + 41.6 T cal/molO2
2Fe3O4+2CO Î 6FeO+2CO2 ∆FTo = + 14.240 - 18.2 T cal/molO2
Atau
Fe3O4+CO Î 3FeO+CO2 ∆FTo = + 7120 - 9.1 T cal/molO2
Persamaan (III)
2FeO Æ2Fe + O2 ∆FTo = +124.100 - 29.90T cal/molO2
2CO + O2Æ 2 CO2 ∆FTo = -135.000 + 41.6 T cal/molO2
2FeO + 2CO Î 2Fe + 2CO2 ∆FTo = -10.900 + 11.7 T cal/molO2
FeO + CO Î Fe + CO2 ∆FTo = -5.450 + 5.85 T cal/molO2
Hasil perhitungan energi bebas diatas menunjukkan bahwa ketiga reaksi tersebut dapat berjalan spontan. Secara termodinamika menunjukkan ketiga reaksi tersebut feasible untuk dilakukan.
2.1.4 Reaksi Boudouard
Proses reduksi langsung menggunakan kesetimbangan antara besi, hematite, magnetit, wustit, karbonmonoksida, karbondioksida, serta karbon padat pada tekanan 1 atm seperti ditunjukkan dalam diagram Bauer Glassner dan Boudouard pada Gambar 2.2. Kesetimbangan tersebut merupakan dasar dilakukannya proses reduksi langsung dengan menggunakan karbon padat.
Gambar 2.2. Diagram Bauer Glassner dan Boudouard [16]
Dalam diagram tersebut terdapat kesetimbangan besi oksida dengan campuran gas CO/ CO2, antara lain :
• Garis kesetimbangan Boudouard : CO2 + C = 2CO
• Garis kesetimbangan : 3Fe2O3 + CO = 2Fe3O4+ CO2
• Garis kesetimbangan : Fe3O4 + CO = 3FeO + CO2
• Garis kesetimbangan : FeO + CO = Fe + CO2
Dari garis kesetimbangan Boudouard, pada temperatur 1000 0C terdapat
100 % gas CO. Apabila temperatur diturunkan maka kesetimbangan tersebut tidak tercapai sehingga terjadi penguraian dari gas CO menjadi CO2 dan C. Sehingga
jumlah gas CO (pereduktor) akan berkurang.
Pada daerah disebelah kiri garis kesetimbangan boudouard maka gas CO2
akan lebih stabil sehingga gas CO yang ada akan terurai menjadi CO2. Pada
daerah disebelah kanan garis kesetimbangan boudouard gas CO lebih stabil sehingga gas CO2 akan mengalami reaksi boudouard membentuk gas CO.Hal
tersebut merupakan contoh dari prinsip Le Chatelier, reaksi boudouard merupakan reaksi yang endotermik sehingga membutuhkan temperatur tinggi untuk dapat berjalan.
Dari Diagram Bauer Glassner dan Boudouard pada Gambar 2.2 , senyawa yang terbentuk sangat dipengaruhi oleh perbandingan antara CO/CO2 dan juga
temperatur operasi. Misal pada temperatur 7000C dengan perbandingan CO/CO2
adalah 60:40, maka senyawa yang paling stabil adalah wustit. Magnetit akan tereduksi menjadi wustit, sedangkan Fe akan mengalami oksidasi menjadi wustit.
Hal penting yang dapat disimpulkan dari kesetimbangan Boudouard antara garis kesetimbangan wustit/Fe dan garis kesetimbangan boudouard berpotongan pada temperatur 7000C. Hal tersebut menunjukkan bahwa temperatur minimum yang dibutuhkan untuk mereduksi wustit menjadi Fe adalah 7000C. Antara garis
kesetimbangan Magnetit/wustit dan garis kesetimbangan boudouard berpotongan pada temperatur 6500C. Hal tersebut menunjukkan bahwa temperatur minimum yang dibutuhkan untuk mereduksi magnetit menjadi wustit adalah 6500C. Temperatur minimum diatas pada tekanam 1 atm. Sangat tidak mungkin reaksi dapat berjalan dibawah temperatur minimum karena karbonmonoksida terurai menjadi karbondioksida.
2.2 MEKANISME REDUKSI LANGSUNG
Mekanisme reduksi langsung besi oksida dengan karbon padat terdiri dari : 1. Pembentukan gas reduktor
2. Adsorbsi gas pada besi oksida 3. Proses difusi dalam besi oksida
2.2.1 Pembentukan Gas Reduktor
Bila karbon dengan adanya oksigen pada temperatur tertinggi akan terbentuk gas CO menurut reaksi :
C + O2 Î CO2
CO2 + C Î 2CO
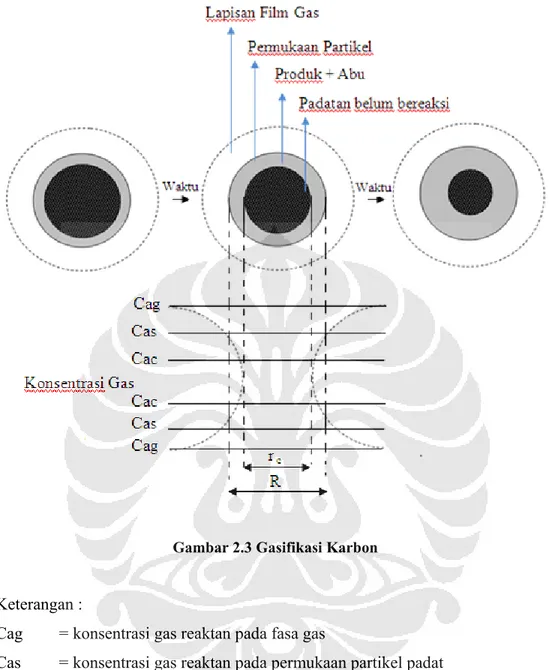
Karbondioksida yang dibentuk dapat bereaksi kembali dengan karbon sehingga terbentuk karbonmonoksida sesuai dengan reaksi boudouard. Karbon tersebut berasal dari karbon dan gas CO yang merupakan gas reduktor yang akan mereduksi besi oksida. Pada proses pembakaran karbon terjadi pembentukan lapisan film. Gas CO yang terbentuk konsentrasinya lebih rendah bila dibandingkan dengan konsentrasi gas CO pada fraksi padat. Selain gas CO sebagai reduktor yang terbentuk dari pembakaran tadi, dihasilkan juga abu yang mempengaruhi jumlah molekul gas reduktor tiap satuan volume. Gas-gas yang terjadi dipengaruhi oleh kecepatan molar transformasi karbon padat tiap satuan waktu dan satuan volume.
Proses pembentukan gas CO berjalan dengan seiring waktu, seperti ditunjukkan pada Gambar 2.3 . Semakin lama waktu reaksi maka semakin banyak karbon yang bereaksi dengan karbondioksida membentuk karbonmonoksida yang digunakan sebagai pereduktor.
Gambar 2.3 Gasifikasi Karbon
Keterangan :
Cag = konsentrasi gas reaktan pada fasa gas
Cas = konsentrasi gas reaktan pada permukaan partikel padat
Cac = konsentrasi gas reaktan pada permukaan padatan yang belum tereaksi Crc = konsentrasi gas produk pada permukaan padatan yang belum tereaksi Crs = konsentrasi gas produk pada permukaan partikel padat
Crg = konsentrasi gas produk pada fasa gas R = jari-jari partikel padat
Secara empiris ditulis
...(2.3) Keterangan :
Vc = Kecepatan molar transformasi karbon ( mol C/ cm3. det) kc = konstanta gasifikasi karbon (det-1)
n0CO2 = konsentrasi gas CO2 dalam fasa gas (mol/cm3)
n’CO2 = konsentrasi gas CO2 pada kesetimbangan permukaan reaksi karbon
padat (mol/cm3)
Sedangkan
. . ...(2.4)
. exp RT ...(2.5)
Keterangan :
kr = konstantan reaktifitas (cm3/g. det) Mc = jumlah karbon( g/ cm3)
n = faktor Thiele’s untuk pori-pori Hc = reaktifitas batu bara
Pada temperatur diatas 9000C, n = 1 Sehingga diperoleh :
. Mc. exp RT ...(2.6) Dari Persamaan 2.3 dan 2.6 didapatkan :
. Mc. exp RT n0CO2 n’CO2 ...(2.7)
Dari Persamaan – Persamaan diatas maka dapat disimpulkan bahwa gasifikasi karbon yang menghasilkan gas reduktor merupakan molar transformasi karbon didalam karbon yang tergantung pada reaktifitas karbon dan jumlah karbon.
Reaksi gasifikasi karbon dengan CO2 merupakan reaksi endotermik, oleh
karena itu reaksi ini terjadi pada temperatur tinggi. Pada temperatur 10000C akan dihasilkan 100% CO pada tekanan 1 atm. Laju reaksi secara keseluruhan dikendalikan oleh laju gasifikasi karbon [16]. Laju gasifikasi karbon ditentukan oleh beberapa faktor yaitu reaktivitas karbon, temperatur dan juga ketersediaan panas yang digunakan untuk mempertahankan reaksi hingga mencapai temperatur operasi [16].
Reaktivitas yang dimiliki oleh material yang mengandung karbon (carbonaceous material) sangat bervariasi. Luas permukaan karbon yang memungkinkan terjadinya reaksi antara karbon dengan CO2 merupakan hal yang
penting, yang ditentukan oleh ukuran partikel material dan juga porositas yang dimiliki oleh material. Charcoal, arang dan juga kokas memiliki porositas dan reaktivitas yang lebih tinggi daripada material karbon alami seperti kayu, karbon, dan grafit. Charcoal lebih reaktif daripada kokas pada temperatur rendah.Kokas yang dibuat dengan tipe karbon yang berbeda-beda(lignit, bituminous, anthracite) juga akan memberikan reaktivitas yang berbeda-beda.
Pada banyak kasus, laju reaksi serta produktivitas dari proses reduksi langsung ditentukan oleh beberapa faktor yang saling terhubung yaitu :
Transfer panas (heat transfer)
Reaktivitas karbon (carbon reactivity)
Reducibility besi oksida (iron oxide reducibility)
Ukuran partikel karbon, jumlah karbon yang tersedia, serta tipe karbon yang digunakan sangat berpengaruh terhadap laju gasifikasi. Ukuran partikel yang kecil dan ketersediaan dalam jumlah banyak akan meningkatkan luas permukaan yang mungkin untuk terjadi reaksi gasifikasi karbon sehingga dapat meningkatkan laju reaksi[16].
2.3.2 Adsorbsi Gas Pada Besi Oksida
Adsorbsi adalah proses terikatnya gas reduktor pada permukaan besi oksida yang disebabkan oleh energi secara fisika dan kimia. Fisika adsorbsi merupakan daya yang terjadi oleh bergeraknya masing-masing molekul gas, yang dibatasi oleh jumlah molekul gas yang menumbuk luas permukaan besi oksida dalam satuan waktu. Kimia adsorbsi adalah daya kimia antara gas dengan padatan (besi oksida), dimana gas melingkupi dan berinteraksi dengan permukaan besi oksida. Kimia adsorbsi sangat bergantung pada kemampuan dan kecenderungan antar gas dan besi oksida dalam bertukar ion elektron atau memberi dari orbitnya.
Dalam wustit ( Fe1-yO), dimana y merupakan tempat kosong ion besi
terhadap kisi-kisi besi atau mol fraksi dari tempat kosong ion besi. Dengan adanya gas CO maka akan menyebabkan pengurangan oksigen dan bersamaan dengan proses tersebut terjadi pembentukan ion bervalensi 2 dalam posisi kisi normal menurut reaksi [8] :
keterangan :
= tempat ion kosong dalam wustit
= cacat elektron
Fe2+ Fe2+ = divalen ion besi pada wustit dalam kondisi kisi normal
Pada permukaan besi oksida akan terbentuk ikatan baru sebagai produk yaitu akan terbentuk Fe metalik dengan ikatan logam, dilain pihak akan terbentuk gas CO2
sebagai hasil dari reaksi adsorbsi oksigen.
Pengurangan oksigen dapat ditunjukkan dengan adanya perbedaan konsentrasi gas CO2 antara fasa gas dengan fasa kesetimbangan pada permukaan
besi oksida. Dengan demikian oksigen yang hilang tiap satuan waktu dan satuan volume secara empiris dapat ditulis sebagai berikut :
...(2.8) Sedangkan :
...(2.9)
Dimana :
Vo = jumlah oksigen yang dihilangkan ( mol O/ cm3. det)
Vc = kecepatan molar transformasi karbon ( mol C/ cm3. det) kFe = konstanta kecepatan reduksi (det-1)
n”CO2 = konsentrasi gas CO2 pada permukaan reaksi besi oksida (mol/ cm3)
n’CO2 = konsentrasi gas CO2 pada kesetimbangan reaksi permukaan karbon
padat (mol/ cm3)
noCO2 = konsentrasi gas CO2 dalam fasa gas (mol/ cm3)
kC = konstanta gasifikasi karbon (det-1)
HFe = karakterisasi besi oksida
R = derajat reduksi = jumlah oksigen yang hilang jumlah oksigen mula-mula T = temperatur pengukuran proses (K)
Pada keadaan setimbang maka kecepatan molar transformasi gasifikasi karbon sama dengan molar transformasi oksigen yang hilang (Vc=Vo). Oleh karena itu diperoleh konsentrasi CO2 pada fasa gas sebagai fungsi dari konstanta
Persamaan 2 .8.
...(2.10)
sehingga kecepatan reduksi menjadi :
...(2.11) Vo = kFe (n”CO2 - noCO2)
Vo maks. = kFe (n”CO2 – n’CO2)
Dari Persamaan 2.11 dapat terlihat bahwa kecepatan reaksi reduksi tergantung dari konstanta gasifikasi karbon dan konstanta reduksi besi oksida. Apabila,
• Reaktifitas karbon lebih kecil dibandingkan dengan kemampuan reduksi besi oksida : kc < kFe maka terjadi Vo ~ 0
• Reaktifitas karbon lebih besar dibandingkan dengan kemampuan reduksi besi oksida : kc > kFe maka terjadi Vo = Vo maks.
...(2.12) Vo maks. merupakan kecepatan maksimum reduksi pada permukaan besi oksida pada temperatur reduksi. Untuk temperatur diatas 9000C, didapatkan n’CO2 <<
n”CO2 , maka didapatkan Persamaan kecepatan :
...(2.13) Dari Persamaan 2.12 didapatkan kecepatan molar oksigen yang hilang pada temperatur diatas 9000C adalah :
...(2.14) Dengan demikian tampak bahwa pengurangan oksigen tiap satuan waktu dan volume merupakan fungsi dari karakteristik besi oksida, reaktifitas karbon, jumlah karbon dan temperatur.
2.3.3 Proses Difusi Dalam Besi Oksida 2.2.3.1 Dasar Difusi
Difusi didefinisikan sebagai pergerakan atom didalam suatu material dengan fasa padat, cair ataupun gas. Fokus pada pembahasan disini adalah pada material denga fasa padat, yaitu besi oksida pada temperatur tinggi.
Vo maks. = kFe (n”CO2 )
Pada temperatur tinggi tempat atom kosong akan bergerak semakin cepat dengan meningkatnya temperatur. Diperlukan energi untuk menggerakkan sebuah tempat atom kosong dari suatu keadaan setimbang ke keadaan setimbang yang lain, sebesar ∆ Hm. Selain itu juga diperlukan juga energi untuk membentuk tempat atom kosong sebesar ∆ Hv. Sehingga difusi tidak hanya tergantung pada pergerakan tempat kosong termasuk pada pergerakan atom tetapi juga pada fraksi kedudukan tempat yang atomnya kosong. Konsekuensi dengan bertambahnya tempat atom kosong yaitu meningkatkan kecepatan difusi atau meningkatnya difusifitas dengan meningkatnya temperatur.
. ∆ ∆ / ...(2.15)
∆ ∆ ...(2.16)
Sehingga diperoleh
. / ...(2.17)
Dimana :
D = Difusifitas (koefisien difusi) (cm2. det-1) Do = Koefisien difusi standard (cm2. det-1)
Q = energi aktivasi ( kal.mol-1) R = konstanta gas (1.987 kcal/mol) T = Temperatur (K)
2.2.3.2 Mekanisme Reaksi
Reduciability dari besi oksida sangat dipengaruhi oleh porositas yang dimiliki oleh besi oksida tersebut. Semakin tinggi porositas maka akan mempermudah difusi gas pereduktor CO pada besi oksida sehingga akan meningkatkan laju reduksi. Pellet hasil aglomerisasi memiliki porositas yang jauh lebih tinggi daripada pellet yang disinter, sehingga reduciability pellet hasil aglomerisasi jauh lebih tinggi daripada pellet hasil sinter.
Ukuran partikel pereaksi seperti karbon juga sangat berpengaruh. Semakin kecil partikel karbon maka semakin luas permukaan yang memungkinkan terjadi reaksi, sehingga laju pembentukan CO semakin tinggi.
Mekanisme reaksi reduksi langsung pada pellet berpori sangat tergantung dari difusi CO untuk menyentuh permukaan besi oksida dan bereaksi. Semakin banyak pori-pori, semakin mudah CO berdifusi kedalam pellet sehingga laju reaksi reduksi akan berjalan semakin cepat. Semakin sedikit pori-pori, semakin sulit CO untuk bereduksi sehingga laju reaksi reduksi akan berjalan semakin lambat. Mekanisme reduksi langsung seperti ditunjukkan pada Gambar 2.4 .
Gambar 2.4 Mekanisme reduksi langsung pada pellet berporos [16]
Pada material yang bebas poros maka reaksi reduksi menggunakan mekanisme solid state difffusion of ferrous ion.
waktu waktu Gas CO2 Gas CO Fe2O3 Fe3O4 FeO FeO
2.4 METODE KARAKTERISASI PRODUK
Metode karakterisasi yang digunakan untuk mengidentifikasi pereaksi serta produk akhir dapat dilakukan dengan metode XRD maupun XRF.
2.3.3 X-Ray Fluorecence (XRF)
Ketika x-ray primer tereksitasi dari x-ray tube atau radiaoaktif menabrak sampel, x-ray dapat diserap oleh atom atau disebarkan pada seluruh permukaan material. Proses dimana x-ray diserap oleh atom dengan mentransfer seluruh energinya ke elektron yang paling dalam dinamakan protoelectric effect. Prinsip kerja XRF dapat dijelaskan sebagai berikut :
• Selama proses jika x-ray mempunyai energi yang cukup maka elektron akan terlempar dari kulitnya yang lebih dalam (tereksitasi), menciptakan vacancy pada kulitnya , ditunjukkan pada Gambar 2.5.
Gambar 2.5 Elektron tereksitasi keluar [17]
• Vacancy itu mengakibatkan kondisi yang tidak stabil pada atom. Untuk menstabilkan kondisi maka elektron dari luar ditransfer untuk menutupi vacancy tersebut, seperti ditunjukkan pada Gambar 2.6. Misalnya elektron dari kulit L dan M mengisi kekosongan yang ada. Pada proses perpindahan tersebut energy dibebaskan karena adanya perpindahan dari kulit yang memiliki energy lebih tinggi (L/M) kedalam kulit yang memiliki energy paling rendah (K). Emisi yang dikeluarkan oleh setiap material memiliki karakter khusus.
Gambar 2.6 Pengisian kekosongan elektron [17]
• Proses tersebut memberikan karakteristik dari x-ray, yang energinya berasal dari perbedaan energi ikatan antar kulit yang berhubungan. X-ray yang dihasilkan dari proses ini disebut “X-Ray Flourecence” atau XRF (Gambar 2.7).
Gambar 2.7 Pelepasan energi [17]
• Proses untuk mendeteksi dan menganalisa X-Ray yang dihasilkan disebut “X-ray Flourecence analysis.
• Karena spektrum X-ray maka pada saat penyinaran suatu material akan didapatkan multiple peak pada intensitas yang berbeda, seperti ditunjukkan pada gambar Gambar 2.8.
Contoh :
Gambar 2.8 Contoh hasil XRF
• Karakterisasi x-ray yang ditandai oleh K,L,M, atau N untuk menunjukkan kulit asalnya. Model yang lain yaitu alfa, beta, atau gamma dibuat untuk menandai x-ray yang berasal dari elektron transisi dari kulit yang lebih tinggi. • Kα dihasilkan dari transisi elektron dari kulit L ke K dan x-ray Kβ dihasilkan
dari transisi elektron dari M menuju kulit K, dll.
Metoda x-ray banyak digunakan untuk menentukan komposisi elemen dari material. Karena metode ini cepat dan tidak merusak sampel metoda ini dipilih unutk penggunaan pada aplikasi lapangan dan proses produksi pada industri untuk mengontrol material. Berdasarkan penggunaanya, x-ray dapat dihasilkan tidak hanya dari x-ray primer tapi juga sumber eksitasi primer yang lain seperti partikel α, proton, atau eletron energi tinggi.
2.3.4 X-ray diffraction (XRD)
XRD dilakukan dengan menembakkan sinar X-Ray pada material kemudian pantulannya akan ditangkap oleh detektor, ditunjukkan pada Gambar 2.9. Prinsip dari XRD dimana elektron yang berada pada bidang elektromagnetik akan bertolak dengan frekuensi yang sama, ditunjukkan pada Gambar 2.10. Ketika berkas x-ray menumbuk atom, elektron disekitar atom akan mulai
Iceland Basalt Fluorescence Spectrum
Cou nts
terpantul kesegala arah dengan frekuensi yang sama sebagai berkas sinar datang, seperti ditunjukkan pada Gambar 2.11. Hampir di semua arah mempunyai interferensi yang saling melemahkan, yaitu gelombang gabungan keluar dari fasa dan tidak ada resultan energi meninggalkan sampel padat. Walau bagaimanapun atom pada kristal tergabung pada pola umum dan pada beberapa arah akan menghasilkan inteferensi yang saling menguatkan. Oleh sebab itu berkas sinar diffraksi akan digambarkan sebagai berkas sinar dari sejumlah sinar tersebar yang saling menguatkan satu sama lain.
Gambar 2.9 Mekanisme X-Ray Diffraction [18]
Gambar 2.10 Geometri pemantulan X-Ray [18]
Gambar 2.11 Interaksi antara photon dengan atom [18]
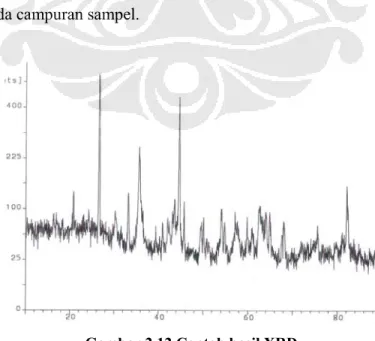
Pada Gambar 2.12 dapat terlihat contoh hasil XRD. Hasil dari XRD dapat digunakan untuk mendeteksi secara kualitatif senyawa yang terkandung dalam suatu material. Setiap senyawa pasti memiliki posisi 2θ yang berbeda.
XRD juga dapat digunakan untuk menganalisa secara kuantitatif, berdasarkan pernyataan dari B.D.Culity dalam buku Element of X-Ray Diffraction menyatakan bahwa analisa kuantitafif dengan XRD dapat dilakukan dengan memanfaatkan intensitas hasil pengukuran. Faktanya intensitas tergantung dari konsentrasi pada campuran sampel.
Hubungan antara intensitas dengan konsentrasi tidak selalu linear, karena intensitas difraksi tergantung dari koefisien absorbsi pada setiap campuran yang bervariasi berdasarkan konsentrasi.
Aplikasi XRD biasanya digunakan adalah untuk analisa kimia, meliputi identifikasi fasa, investivigasi fasa temperatur tinggi ataupun rendah, solid solution dan menentukan parameter sel dari material baru.
![Gambar 2.4 Mekanisme reduksi langsung pada pellet berporos [16]](https://thumb-ap.123doks.com/thumbv2/123dok/4082547.3043417/18.918.197.775.382.739/gambar-mekanisme-reduksi-langsung-pada-pellet-berporos.webp)
![Gambar 2.9 Mekanisme X-Ray Diffraction [18]](https://thumb-ap.123doks.com/thumbv2/123dok/4082547.3043417/22.918.247.764.350.1000/gambar-mekanisme-x-ray-diffraction.webp)