PERFORMA ANALITIK ELKTRODE ENZIM GLUKOSA DEHIDROGENASE
FLAVIN ADENIN DINUKLEOTIDA TERIMOBILISASI ZEOLIT TIPE A UNTUK
DETEKSI GLUKOSA
1)
Raudhatul Fadhilah
,
2)Latifah Kosim Darusman
,
3)Dyah Iswantini
1)
Program Studi Pendidikan Kimia Universitas Muhammadiyah Pontianak, Pontianak (email: raudhatul_fadhilah@yahoo.com)
2)
Departemen Kimia Institut Pertanian Bogor, Bogor 3)
Pusat Studi Biofarmaka, Bogor
ABSTRACT
A glucose sensor was developed to measure glucose levels, both of blood glucose and
glucose in the foods and beverages. The analytical performance of these new glucose
sensors was continuously improved, producing better linearity and sensitivity. The technique
selection and immobilization matrix are key factors for sensor development, so that the
prospecting of materials that can be used as a matrix for supporting enzyme, continue to be
explore. The purpose of this study was to determine the linearity and sensitivity of the
enzyme glucose dehydrogenase (GDH) that were immobilized on zeolite type A. The
resulting enzyme electrode with zeolite type A showed linearity were 0.06 mM-10.00 mM.
Linear range that result is quite narrow when compared with the normal range of blood
glucose concentration in humans is from 4 to 6 mM, so that GDH-FAD enzyme electrode
with zeolite type A is more suitable to use in the determination of glucose concentration in
the foods and beverages. A GDH-FAD enzyme electrode showed a high sensitivity were
2.41 µA mM
-1. High sensitivity was achieved by combining two immobilization techniques,
physical adsorption on zeolite and entrapment on carbon paste, so that electron transfer
becomes faster and efficient.
Keywords: enzyme electrode, linearity, sensitivity, zeolite type A
ABSTRAK
Sensor glukosa telah dikembangkan secara luas untuk mengukur kadar glukosa, baik
glukosa darah maupun glukosa dalam makanan dan minuman. Performa analitik sensor
glukosa terus ditingkatkan untuk menghasilkan sensor dengan rentang kerja dan sensitivitas
yang semakin baik. Faktor kunci keberhasilan dalam pengembangan sensor glukosa
berbasis enzim adalah ketepatan penggunaan teknik dan matriks imobilisasi sehingga
eksplorasi material yang dapat digunakan sebagai matriks pengimobilisasi terus dilakukan.
Tujuan dari penelitian ini adalah menentukan linearitas dan sensitivitas elektrode enzim
glukosa dehidrogenase flavin adenin dinukleotida (GDH-FAD) yang diimobilisasi pada zeolit
tipe A. Hasil penelitian menunjukkan bahwa elektrode enzim GDH-FAD yang diimobilisasi
dengan zeolit tipe A menghasilkan linearitas 0.06 mM-10.00 mM. Daerah linear yang
dihasilkan cukup sempit jika dibandingkan dengan rentang konsentrasi glukosa darah
normal pada manusia yaitu dari 4 sampai 6 mM, sehingga elektrode enzim GDH-FAD
dengan zeolit tipe A lebih cocok diaplikasikan dalam makanan dan minuman. Elektrode
enzim GDH-FAD menunjukkan sensitivitas yang tinggi yaitu 2,41 µA mM
-1, hal ini
disebabkan oleh penggunaan dua teknik imobilisasi, yaitu adsorpsi fisik antara enzim
dengan zeolit dan penjebakan enzim dalam pasta karbon sehingga transfer elektron menjadi
lebih cepat dan efisien.
1. PENDAHULUAN
Pembangunan kesehatan Indonesia diarahkan guna meningkatkan kesadaran,
kemauan dan kemampuan hidup sehat bagi setiap penduduk agar terwujud derajat
kesehatan yang optimal. Perubahan gaya hidup terutama di kota-kota besar, menyebabkan
meningkatnya prevalensi penyakit degeneratif, seperti penyakit jantung koroner, hipertensi,
hiperlipidemia, diabetes mellitus dan lain-lain
[1]. Kemajuan dan inovasi ilmu pengetahuan
dan teknologi di bidang kesehatan, memungkinkan dilakukannya upaya pengendalian
berupa kegiatan promosi dan pencegahan serta penanggulangan penyakit termasuk
penyakit tidak menular
[2]. Penyakit tidak menular (PTM) bukan saja masalah di negara
industri, tetapi juga merupakan masalah di negara berkembang
[3]. Berdasarkan estimasi
terkini dari WHO, penyakit tidak menular menyebabkan sekitar 52% kematian dan 38%
beban penyakit di SEAR (South East Asia Region), yaitu Bangladesh, Butan, India,
Indonesia, Korea Utara, Maldives, Myanmar, Nepal, Sri Lanka, dan Thailand. Penyakit tidak
menular seperti kanker, gangguan respirasi, kardiovaskular dan diabetes mellitus dapat
menimbulkan kerugian sosial ekonomi, khususnya masyarakat yang sedang berkembang
termasuk negara maju
[3].
Diabetes mellitus (DM) adalah penyakit kronis yang ditandai dengan kadar glukosa
darah yang tinggi akibat pankreas tidak memproduksi insulin yang cukup atau ketika tubuh
tidak dapat secara efektif menggunakan insulin yang dihasilkan. Berdasarkan data Badan
Kesehatan Dunia (WHO) pada tahun 2011, 346 juta orang di seluruh dunia mengidap
diabetes. Untuk Indonesia, WHO memprediksi kenaikan jumlah penderita DM dari 8,4 juta
pada tahun 2000 menjadi sekitar 21,3 juta pada tahun 2030. Tingginya angka tersebut
menjadikan Indonesia peringkat keempat jumlah penderita DM terbanyak di dunia setelah
Amerika Serikat, India, dan Cina
[4]. Pendekatan baru untuk mendiagnosis, mengobati,
mengenali lebih awal dan pencegahan penyakit tersebut diperlukan untuk menghadapi
tantangan ini. Bagi penderita DM, menjaga glukosa darah mendekati normal dapat
mengurangi resiko komplikasi lanjutan. Untuk menjaga tingkat glukosa darah pada daerah
aman, diperlukan alat untuk memantau glukosa darah. Saat ini, sensor untuk keperluan
tersebut masih diimpor dari negara lain dengan harga yang relatif mahal. Oleh karena itu,
dibutuhkan penelitian yang intensif untuk mengembangkan pemenuhan biosensor yang
murah, akurat dan mudah penggunaanya.
Biosensor di dunia pertama kali dikembangkan oleh Leland Clark tahun 1956. Clark
menggunakan enzim glukosa oksidase (GOD) sebagai komponen pengenal analit yang
bereaksi spesifik dengan glukosa dan secara alamiah dihasilkan dari jamur Aspergillus
niger. Mekanisme kerja enzim ini sangat bergantung pada keberadaan oksigen. Akibatnya,
sama. Hal tersebut, mendorong penggantian enzim GOD dengan enzim glukosa
dehidrogenase (GDH). Enzim GDH spesifik terhadap substrat glukosa dan aktivitasnya tidak
dipengaruhi oleh kadar oksigen
[5]. Koenzim yang cocok untuk membuat biosensor yang
tidak memerlukan O
2sebagai akseptor elektron atau nikotin adenin dinukleotida (NAD)
sebagai koenzim, salah satunya adalah flavin adenin dinukleotida (FAD)
[6].
Perkembangan biosensor glukosa sampai saat ini di antaranya adalah elektrode enzim
GOD dengan film nanokomposit kitosan/grafena/nanopartikel emas yang dibuat oleh Shan
et al. (2010)
[7]menunjukkan bahwa sensitivitas sensor glukosa sebesar 0.55 µA mM
-1dengan daerah linear antara 2 sampai 10 mM (R = 0.999). Biosensor glukosa amperometri
memanfaatkan GDH-FAD yang diimobilisasi pada nanokomposit elektrode menghasilkan
sensitivitas 2.20 µA mM
-1dengan menghasilkan 2 daerah linear, yaitu antara 50 sampai 960
µM dan dari 70 sampai 620 µM
[5].
Faktor kunci keberhasilan Monosik et al. (2012)
[5]menghasilkan sensitivitas sensor
yang tinggi dikarenakan penggunaan kitosan sebagai matriks pengimobilisasi enzim. Enzim
diadsorpsi pada kitosan model sandwich sehingga menyediakan lingkungan yang hidrofilik
yang cocok dengan enzim. Oleh karena itu pencarian material lain sebagai matriks
pengimobilisasi enzim perlu dieksplorasi. Salah satu kandidat material yang paling
menjanjikan sebagai matriks pendukung adsorpsi enzim GDH adalah zeolit. Hal ini
disebabkan oleh sifat zeolit yang memiliki karakteristik struktur yang unik dan tahan
terhadap biodegradasi serta permukaan dapat dimodifikasi dan mudah disiapkan dengan
rongga mulai dari mikro pori (< 20 Å)
[8]. Oleh karena itu, penelitian ini bertujuan menentukan
linearitas dan sensitivitas elektrode enzim glukosa dehidrogenase flavin adenin dinukleotida
(GDH-FAD) yang diimobilisasi pada zeolit tipe A.
2. METODE PENELITIAN
Penelitian ini terdiri atas 4 tahap. Tahap pertama yaitu pembuatan dan karakterisasi
elektrode pasta karbon. Tahap kedua, yaitu imobilisasi enzim GDH pada matriks zeolit tipe
A dan permukaan elektrode pasta karbon. Tahap ketiga, yaitu penentuan performa analitik
meliputi: sensitivitas dan linearitas pengukuran dengan metode elektrokimia.
2.1 Pembuatan dan karakterisasi elektrode pasta karbon
[9]Elektrode pasta karbon dibuat dari campuran grafit dan parafin cair 2:1. Grafit dicampur
dengan parafin cair hingga membentuk pasta. Kemudian pasta karbon dimasukkan ke
dalam badan elektrode hingga memadat sampai ke permukaan kaca. Permukaan kaca
elektrode dihaluskan dan dibersihkan dengan ampelas dan kertas minyak. Elektrode ini
selanjutnya dikarakterisasi dengan elektrolit pendukung KCl 0.10 M menggunakan teknik
voltametri siklik. Pengukuran ini menggunakan elektrode pembanding Ag/AgCl dan
elektrode bantu kawat platina.
2.2 Imobilisasi enzim GDH pada zeolit tipe A
Enzim GDH diimobilisasi dengan metode adsorpsi menggunakan nanopartikel zeolit
dengan memodifikasi penelitian Salih (2012)
[10]. Modifikasi yang dilakukan yaitu
penggantian enzim urease dengan enzim GDH. Imobilisasi enzim GDH dilakukan dengan
menyiapkan 8.0 U/mL enzim GDH, gliserol (10%). Setelah itu, zeolit tipe A dengan
komposisi tertentu dicampurkan dengan gliserol (10%) dan 1 mL larutan enzim GDH
kemudian diaduk hingga homogen. Campuran selanjunya dishaker selama 24 jam.
Kemudian larutan diteteskan pada permukaan elektrode pasta karbon dan didiamkan hingga
pelarutnya menguap/mengering. Selanjutnya permukaan elektrode dilapisi dengan membran
dialisis, ditutup dengan jaring nilon, dan diikat dengan parafilm. Elektrode kemudian
direndam dalam bufer fosfat pada suhu 5 ºC ketika tidak digunakan, untuk memberikan
keadaan yang sama dengan lingkungan sebenarnya. Elektrode dapat langsung digunakan
untuk pengukuran aktivitas GDH secara elektrokimia.
2.3 Penentuan parameter analitik
Sensitivitas metode analisis adalah perbandingan perubahan respon instrumental
terhadap perubahan konsentrasi analit. Sensitivitas diperoleh dari nilai kemiringan kurva.
Penentuan konsentrasi linear ditetapkan melalui pengukuran larutan standar D-glukosa
pada kondisi optimum elektrode dan parameter instrumen pada berbagai rentang
konsentrasi. Arus puncak yang terbaca dialurkan terhadap konsentrasi larutan standar untuk
memperoleh kurva kalibrasi. Linearitas dan daerah kerja diperoleh dari interpretasi kurva
kalibrasi. Konsentrasi yang memberikan hubungan linear adalah rentang konsentrasi kerja
elektrode. Hubungan yang linear dinyatakan dengan koefisien korelasi (r) yang mengikuti
Persamaan 1.
- =
∑ 0123 342̅617347 8 690:∑ 123 342̅6;<:∑ 173 347=6;<9>/;
(1)
Dengan x
iadalah konsentrasi larutan D-glukosa ke-i, @̅ adalah konsentrasi rata-rata larutan
D-glukosa, y
iadalah arus puncak yang terukur pada konsentrasi larutan D-glukosa ke-i dan
3. BAHAN DAN ALAT
Bahan-bahan yang digunakan dalam penelitian ini adalah enzim GDH berasal dari
Aspergillus sp. dengan aktivitas 1050 U/mg dibeli dari Sekisui Inggris, FADNa
2.×H
2O dibeli
dari Sigma, aquabides, air bebas ion, NaCl, KCl, gliserol, grafit, parafin cair, D-glukosa,
kalium ferisianida, larutan bufer fosfat, membran dialisis, NaOH, gas N
2, amonium serium
sulfat, etanol, metanol, zeolit tipe A.
Alat atau instrumen yang digunakan dalam penelitian antara lain eDAQ
Potensiostat-Galvanostat (Ecorder 410) yang dilengkapi dengan perangkat lunak Echem v2.1.0 dengan
sistem 3 elektrode (elektrode Ag/AgCl sebagai elektrode pembanding, elektrode pasta
karbon sebagai elektrode kerja, elektrode platina sebagai elektrode bantu), sel elektrokimia,
scanning electron microscopy (SEM), pipet mikro serta alat-alat gelas yang lazim digunakan
di laboratorium.
4. HASIL DAN PEMBAHASAN
4.1 Imobilisasi enzim GDH pada zeolit tipe A
Imobilisasi enzim bertujuan meningkatkan sensitivitas enzim. Imobilisasi yang dilakukan
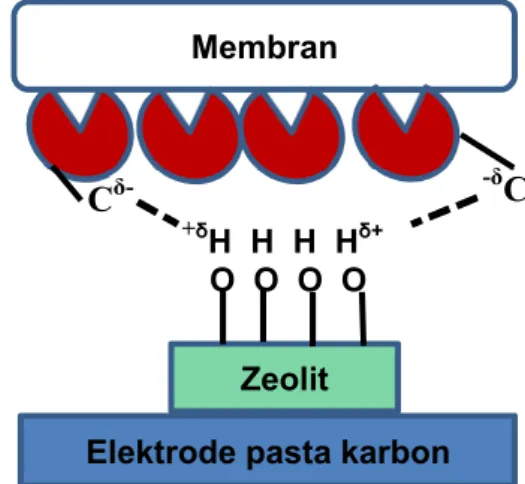
melalui model dengan ilustrasi seperti pada Gambar 1 berikut.
Gambar 1. Imobilisasi enzim pada zeolit tipe A
Gambar 1 memperlihatkan bahwa enzim diimobilisasi pada zeolit tipe A dan elektrode
pasta karbon. Pada model ini menggabungkan dua teknik imobilisasi (adsorpsi fisik dan
penjebakan), yaitu enzim diimobilisasi terlebih dahulu pada nanopartikel zeolit kemudian
diteteskan pada elektrode pasta karbon dan ditutup dengan membran dialisis. Untuk
mengetahui enzim telah terimobilisasi pada zeolit tipe A, dilakukan pencirian dengan
menggunakan SEM (Gambar 2).
+δ
H H H H
δ+O O O O
Elektrode pasta karbon
Membran
Zeolit
C
δ--δ