PENGENDAPAN KROMIUM HEKSAVALEN DENGAN
SERBUK BESI
ANDRE BRAMANDITA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2009
ABSTRAK
ANDRE BRAMANDITA. Pengendapan Kromium Heksavalen dengan Serbuk
Besi. Dibimbing oleh ETI ROHAETI dan ZULHAN ARIF.
Kromium adalah unsur golongan transisi dan banyak dijumpai di alam
dalam bentuk trivalen dan heksavalen. Kromium heksavalen memiliki sifat yang
lebih toksik dibandingkan dengan bentuk trivalennya. Keberadaan kromium
heksavalen pada limbah cair industri tekstil memerlukan pengolahan agar tidak
mencemari lingkungan. Untuk itu diperlukan suatu metode yang murah dan
efektif dalam mengendapkan kromium heksavalen pada limbah tekstil. Penelitian
ini meliputi: penentuan pengaruh pH, penentuan pengaruh kecepatan pengocokan,
penentuan pengaruh waktu pengocokan, dan penentuan pengaruh jumlah serbuk
besi; serta penerapannya pada limbah tekstil. Metode yang digunakan dalam
penerapan pada limbah tekstil meliputi: penentuan konsentrasi kromium
heksavalen larutan limbah tekstil, penentuan konsentrasi kromium heksavalen
larutan limbah tekstil dengan metode penambahan standar, dan pengendapan
kromium heksavalen larutan limbah tekstil dengan serbuk besi. Pengukuran
konsentrasi kromium heksavalen dilakukan dengan metode spektrofotometri sinar
tampak. Kondisi optimum pH, kecepatan pengocokan, jumlah serbuk besi, dan
waktu pengocokan berturut-turut adalah pH 3, 450 rpm, 5 gram, dan 10 menit
yang memberikan nilai konsentrasi kromium heksavalen tersisa berturut-turut
sebesar 16.98 ppm, 15.96 ppm, 0.24 ppm, dan 0.14 ppm. Serbuk besi sangat baik
digunakan untuk mengendapkan kromiumium heksavalen dari larutan limbah
tekstil karena mampu mengendapkan kromiumium heksavalen dalam jumlah yang
banyak dalam waktu yang relatif singkat. Nilai serapan kromium heksavalen
larutan limbah tekstil setelah direaksikan dengan serbuk besi pada kondisi
optimum adalah sebesar 0.002 untuk larutan limbah proses pewarnaan tekstil, dan
sebesar 0.000 untuk larutan limbah akhir tekstil.
ABSTRACT
ANDRE BRAMANDITA. Removal of Hexavalent Chromium with Scrap Iron
Filling. Supervised by ETI ROHAETI dan ZULHAN ARIF
Chromium is a transition element commonly found in the environment as
trivalent and hexavalent forms. Apparently, the hexavalent form is much more
toxic than the trivalent form. Textile wastewater treatment is required in order to
prevent hexavalent chromium to contaminate the environment. The methods of
this research consisted of effect of pH determination, effect of agitating rate
determination, effect of agitating time determination, and effect of iron level
determination; and its application in textile wastewater sample. The methods used
in textile wastewater application are: determination of textile wastewater
hexavalent chromium concentration, determination of textile wastewater
hexavalent chromium concentration with standard addition method, and removal
of hexavalent chromium in textile wastewater with scrap iron filling.
Concentration of hexavalent chromium was determined using visible light
spectrophotometry method. Optimum conditions of pH, agitating rate, iron
amount, and agitating time obtained were pH 3, 450 rpm, 5 grams, and 10 minutes
giving concentrations of hexavalent chromium 16.98 ppm, 15.96 ppm, 0.24 ppm,
and 0.14 ppm, respectively. Iron filling could effectively remove hexavalent
chromium ions from textile wastewater in a relatively short time. Absorbance of
hexavalent chromium in textile coloring process wastewater after the addition of
iron filling was 0.002, whereas in textile final wastewater was 0.000.
PENGENDAPAN KROMIUM HEKSAVALEN DENGAN
SERBUK BESI
ANDRE BRAMANDITA
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2009
Judul
: Pengendapan Kromium Heksavalen dengan Serbuk Besi
Nama
: Andre Bramandita
NIM
: G44202042
Disetujui
Pembimbing I
Pembimbing II
Dr. Eti Rohaeti, MS Zulhan Arif S.Si
NIP 196008071987032001
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. drh. Hasim, DEA
NIP 196103281986011002
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala
berkat dan karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah
dengan judul Pengendapan Kromium Heksavalen dengan Serbuk Besi. Karya
ilmiah ini merupakan hasil penelitian yang dilakukan oleh penulis dari bulan
Maret sampai Desember 2008 di Laboratorium Kimia Analitik, Departemen
Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian
Bogor.
Penulis mengucapkan terima kasih kepada Ibu Dr. Eti Rohaeti, MS, Bapak
Zulhan Arif, S.Si dan Bapak Prof. Dr. Ir. M. Sri Saeni, MS (alm) selaku
pembimbing yang telah memberikan bimbingan dan pengarahan kepada penulis
dalam menyelesaikan karya ilmiah ini.
Ungkapan terima kasih juga penulis sampaikan kepada kedua orang tua dan
keluarga yang telah memberikan dukungan moral dan materi. Penulis juga
berterima kasih kepada teman-teman kimia IPB (Steve, Budi Asti, Budi Putra,
Yuyun, Henny, Sari, Cumi dkk, Away dkk, Tesar dkk), teman-teman asrama C2
(Ichsan, Sigit, Fajar, Faisal, Fadli, Fahmi), teman-teman cba8 (Angga, Noni,
Penny, Ria, Iqbal, Bian, Aris) atas persahabatan yang telah dijalani selama penulis
berkuliah di IPB. Selain itu juga penulis berterima kasih kepada Mas Heri, Mas
Eko, seluruh dosen dan staf pengajar di lingkungan IPB, serta para staf dan
laboran di laboratorium kimia analitik (Pak Eman, Pak Ridwan, Pak Kosasih, Pak
Dede, Bu Nunung) yang telah banyak memberikan nasihat dan arahan kepada
penulis dalam menjalankan kuliah dan penelitian.
Semoga karya ilmiah ini bermanfaat.
Bogor, April 2009
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 5 Februari 1985 sebagai anak
pertama dari dua bersaudara, anak dari pasangan Martin Luther Linting dan Yulin
Linting.
Tahun 2002 penulis lulus dari SMUN 1 Depok dan pada tahun yang sama
lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB (USMI) pada
Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis pernah menjadi asisten praktikum mata
kuliah Spektrofotometri pada tahun ajaran 2005-2006. Pada tahun 2005 penulis
melaksanakan praktik lapangan di PT Indomilk, Jakarta.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... vi
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Kromium... 1
Kromium Heksavalen ... 2
Limbah Industri Tekstil ... 2
Pengendapan Kromium Heksavalen dengan Serbuk Besi ... 3
Pengukuran Kromium ... 3
Metode Penambahan Standar ... 4
BAHAN DAN METODE
Alat dan Bahan... 4
Lingkup Penelitian ... 4
HASIL DAN PEMBAHASAN
Panjang Gelombang Maksimum... 6
Pengaruh pH ... 7
Pengaruh Kecepatan Pengocokan ... 7
Pengaruh Jumlah Serbuk Besi ... 8
Pengaruh Waktu Pengocokan ... 8
Konsentrasi Kromium Heksavalen Larutan Limbah
Tekstil... 9
Konsentrasi Kromium Heksavalen Larutan Limbah
Tekstil dengan Metode Penambahan Standar... 9
Pengendapan Kromium Heksavalen Larutan Limbah Tekstil dengan
Serbuk Besi ... 10
SIMPULAN DAN SARAN ... 10
DAFTAR PUSTAKA ... 11
DAFTAR GAMBAR
Halaman
1 Larutan dan peralatan metode penambahan standar ... 4
2 Hubungan panjang gelombang dengan serapan larutan kompleks
DPC-Cr(VI) ... 6
3 Hubungan panjang gelombang dengan serapan larutan kompleks
DPC-Cr(VI) dengan penambahan Ce(IV)... 6
4 Hubungan panjang gelombang dengan serapan larutan Ce(IV)... 7
5 Hubungan pH larutan dengan konsentrasi kromium heksavalen ... 7
6 Hubungan konsentrasi kromium heksavalen dengan kecepatan
pengocokan... 8
7 Hubungan konsentrasi kromium heksavalen dengan jumlah
serbuk besi ... 8
8 Hubungan konsentrasi kromium heksavalen dengan waktu
pengocokan ... 9
9 Hubungan konsentrasi dengan serapan larutan standar dan
larutan limbah proses pewarnaan tekstil dengan penambahan standar..
9
10 Hubungan konsentrasi dengan serapan larutan standar dan larutan
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian……… 14
2 Serapan larutan Cr(VI) pada panjang gelombang 400-635 nm………... 15
3 Serapan larutan kompleks DPC-Cr(VI) dengan penambahan
Ce(IV) pada panjang gelombang 410-630 nm………….………... 15
4 Serapan larutan Ce(IV) pada panjang gelombang 345-530 nm ... 16
5 Kurva standar penentuan pengaruh pH , jumlah serbuk besi,
kecepatan pengocokan dan waktu pengocokan ... 16
6 Pengukuran serapan larutan hasil penentuan pengaruh pH….……... 16
7 Pengukuran serapan larutan hasil penentuan kecepatan pengocokan…... 17
8 Pengukuran serapan larutan hasil penentuan pengaruh jumlah
serbuk besi……….……... 17
9 Pengukuran serapan larutan hasil penentuan pengaruh waktu
Pengocokan……….. 18
10 Plot Penyebaran Tiga Dimensi ……….. 19
11 Pengukuran serapan larutan limbah tekstil... 22
12 Kurva standar pengukuran konsentrasi krom heksavalen larutan
limbah tekstil dengan metode penambahan standar……….. 22
13 Pengukuran serapan larutan limbah tekstil dengan penambahan standar 23
14 Contoh perhitungan konsentrasi krom heksavalen larutan
limbah proses pewarnaan tekstil dengan metode penambahan standar.. 23
15 Hasil pengukuran konsentrasi krom heksavalen dan krom total
dengan metode AAS………... 23
16 Perhitungan kemiringan kurva standar dan kurva penambahan
PENDAHULUAN
Kromium merupakan logam transisi golongan VI B yang dapat memiliki tingkat valensi yang bervariasi antara -2 dan +6. Pada kadar yang rendah, kromium tergolong logam esensial bagi manusia yang berguna terutama dalam metabolisme karbohidrat karena bersama-sama dengan insulin menjaga kadar gula darah. Kekurangan kromium dapat mengganggu metabolisme karbohdrat, lemak, dan protein serta mengganggu pertumbuhan (Kusnoputranto 1996). Namun, kromium pada jumlah yang tinggi dapat menyebabkan reaksi alergi, peradangan, keracunan, kerusakan organ tubuh, penyakit kanker, bahkan kematian (King 1994).
Kromium banyak digunakan oleh berbagai macam industri, salah satunya adalah industri tekstil. Industri tekstil merupakan industri yang mengolah serat menjadi bahan pakaian dengan kromium sebagai zat pengoksidasi pada proses penyempurnaan tekstil. Karena itu pula limbah cair dari industri tekstil mengandung kromium dengan konsentrasi tinggi. Limbah tersebut dapat membahayakan lingkungan karena kromium, terutama kromium heksavalen, merupakan jenis bahan berbahaya dan beracun (B3) (Wahyuadi 2004).
Keberadaan kromium pada limbah cair industri tekstil memerlukan pengolahan agar tidak mencemari lingkungan. Sejumlah metode telah digunakan untuk mengolah limbah cair yang mengandung kromium trivalen, dengan penekanan pada penyingkiran dan daur ulang. Metode-metode tersebut di antaranya adalah pengendapan, pertukaran ion, ekstraksi pelarut, penjerapan, dan teknik osmosis balik. Metode pengendapan merupakan metode yang paling banyak digunakan karena mempunyai beberapa kelebihan, di antaranya adalah biaya yang rendah dan proses yang sederhana.
Sebagian besar metode pengendapan kromium yang murah dan efektif adalah metode pengendapan kromium trivalen. Metode-metode tersebut hanya mengendapkan kromium trivalen saja, sedangkan di dalam limbah tekstil, selain terdapat kromium trivalen, juga terdapat kromium heksavalen yang jauh lebih toksik, mutagenik dan karsinogenik dibandingkan dengan kromium trivalen.
Beberapa metode telah ditemukan untuk menyingkirkan kromium heksavalen dari suatu larutan, salah satunya adalah dengan metode adsorpsi fisiko kimia (Hideaki et al 2002; Bowman 2003). Namun metode tersebut membutuhkan biaya yang cukup
tinggi. Metode lainnya adalah dengan menggunakan kultur bakteri (Chen dan Hao 1998) yang tidak membutuhkan biaya tinggi. Namun zat-zat beracun pada lokasi pembuangan limbah dapat mengurangi pertumbuhan dan efektivitas bakteri tersebut. Untuk itu diperlukan suatu metode yang murah dan efektif dalam mengendapkan kromium heksavalen pada limbah tekstil.
Junyapoon dan Weerapong (2006) telah mengendapkan kromium heksavalen pada limbah kromium sintetis menggunakan serbuk besi. Serbuk besi dipilih karena besi sebagai Fe(0) merupakan reduktor yang sangat kuat. Selain itu serbuk besi juga mudah didapatkan. Metode yang digunakan pun berbiaya rendah. Penelitian ini bertujuan mengkaji ulang metode pengendapan kromium heksavalen dengan serbuk besi (Junyapoon dan Weerapong 2006), yang meliputi: penentuan pengaruh pH, penentuan pengaruh kecepatan pengocokan, penentuan pengaruh waktu pengocokan, dan penentuan pengaruh jumlah serbuk besi; serta penerapannya pada limbah tekstil.
TINJAUAN PUSTAKA
Kromium
Dalam lingkungan hidup, kromium ditemukan dalam bentuk kromium logam, bivalen, trivalen, dan heksavalen. kromium logam memilki massa jenis (20oC) sebesar 7,19 g/cm3, titik leleh sebesar 1875oC, titik didih sebesar 2658oC, dan tergolong logam yang mengkilap, keras serta tahan karat sehingga sering digunakan sebagai pelindung logam lain.
Logam kromium larut dalam asam klorida encer atau pekat. Jika tidak terkena udara, akan terbentuk ion-ion kromium(II) atau kromium bivalen . Kromium bivalen termasuk senyawa pereduksi kuat. Dengan adanya oksigen dari atmosfer, kromium sebagian atau seluruhnya menjadi teroksidasi ke dalam trivalen. Dalam bentuk heksavalen, kromium terdapat sebagai CrO42- dan Cr2O72-,
sedangkan bentuk trivalen terdapat sebagai Cr3+, [Cr(OH)]2+, [Cr(OH)2]+, dan [Cr(OH)4]-
(Clesceri et al. 1998). Kedua bentuk kromium tersebut mempunyai karakteristik kimiawi yang sangat berbeda. kromium heksavalen hampir semuanya berbentuk senyawaan anionik, sangat larut dalam perairan dan relatif stabil meskipun senyawaan ini merupakan agen pengoksidasi yang kuat di dalam larutan asam. kromium trivalen stabil, dan berasal dari dikromium trioksida atau kromium
trioksida, Cr2O3. Di alam, baik kromium
trivalen maupun heksavalen bergabung dengan unsur-unsur lain membentuk senyawa-senyawa yang stabil, misalnya kromium trivalen ditemukan dalam bentuk senyawa kromium oksida dan kromium sulfat, sedangkan kromium heksavalen dalam bentuk senyawaan dikromiumat dan kromiumat (Kusnoputranto 1996; Manahan 2003).
Kromium dapat membentuk senyawa-senyawa dengan berbagai macam warna yang mempunyai kegunaan dalam industri. Timbal kromiumat (PbCrO4), juga dikenal dengan
kromium kuning, telah digunakan sebagai pigmen kuning dalam cat. Kromium trioksida (Cr2O3), juga dikenal dengan kromium hijau,
adalah senyawa terbanyak ke-9 yang ada di kulit bumi dan biasa digunakan sebagai pigmen hijau. Senyawa kromium juga biasa digunakan untuk melapisi alumunium agar terlindungi dari karat (Jefferson Lab 2006).
Dalam sistem biologis, kromium trivalen termasuk logam esensial bagi manusia (Massaro 1997, Manahan 2003). Dalam dosis 20-50 µg per 100 g bobot badan, kromium memiliki fungsi yang baik dalam metabolisme karbohidrat, metabolisme lipid, sintesis protein, dan metabolisme asam nukleat (Mertz 1987). Dalam metabolisme karbohidrat, kromium memiliki fungsi mempengaruhi kemampuan reseptor insulin dalam berinteraksi dengan insulin sehingga insulin dapat aktif bekerja mengatur kadar gula darah. Insulin yang aktif akan meningkatkan pengambilan glukosa yang kemudian mungkin terolah menjadi lemak.
Dalam sintesis protein, keberadaan kromium mempengaruhi pembentukan asam amino glisin, serin dan metionin, sedangkan dalam metabolisme asam nukleat, kromium yang mampu berikatan dengan asam nukleat dapat melindungi RNA dari denaturasi oleh panas dan menjaga struktur tersier asam nukleat. Kekurangan kromium trivalen dalam tubuh menyebabkan penurunan kerja hormon insulin yang kemudian dapat menimbulkan penyakit diabetes melitus, hiperglisemia, dan glukosuria, menyebabkan penurunan bobot badan, kadar asam lemak tinggi, gangguan proses pernafasan, dan kelainan dalam metabolisme nitrogen (King 1994).
Selain digolongkan sebagai logam esensial, kromium juga digolongkan dalam kelompok logam berat dengat sifat sangat beracun dan dalam kelompok senyawa yang karsinogen terhadap manusia. Keracunan oleh kromium menyebabkan gangguan kesehatan yang tidak pulih dalam waktu singkat (Sutamihardja 2002).
Kromium Heksavalen
Kromium heksavalen memiliki sifat yang lebih toksik dibandingkan dengan bentuk trivalennya. kromium heksavalen dapat menyebabkan kerusakan hati, ginjal, pendarahan di dalam tubuh, dermatitis, kerusakan saluran pernafasan dan kanker paru-paru, walaupun kasus keracunan kromium relatif sudah jarang karena peningkatan keselamatan di daerah industri. Bahaya jangka panjang terhadap saluran pernapasan dan kulit dapat menyebabkan perforasi (pelubangan) dan ulkus septumnasi, peradangan rongga hidung, perdarahan hidung yang sering, dan ulkus jaringan kulit. Respon yang lebih umum terjadi adalah reaksi alergi kulit terhadap kromium yang berasal dari berbagai produk seperti kulit samak kromium, semen, ragi bir, pengawet kayu, cat, lem, dan pewarna kayu. (Kusnoputranto 1996).
Kromium Heksavalen digolongkan sebagai karsinogenik terhadap manusia. Oleh United States Enviromental Protection Agency (USEPA). Percobaan laboratorium membuktikan bahwa senyawa-senyawa kromium heksavalen atau hasil-hasil reaksi antaranya di dalam sel dapat menyebabkan kerusakan pada materi genetik. Studi lain pada binatang percobaan menunjukkan bahwa bentuk kromium tersebut dapat menyebabkan masalah reproduksi. Efek yang sangat berbahaya dari kromium heksavalen menyebabkan pemerintah memasukkan kromium heksavalen dalam kriteria nilai baku mutu air. Menurut Peraturan Pemerintah Republik Indonesia nomor 82 tahun 2001, air golongan A, B, dan C hanya boleh mengandung kromium heksavalen maksimum 0.05 ppm. Sedangkan air golongan D hanya boleh mengandung maksimum 0.1 ppm.
Limbah Industri Tekstil
Industri tekstil adalah industri yang menghasilkan pakaian dan bahan pakaian dari bahan baku serat. Secara umum, pembuatan tekstil pada industri meliputi 3 tahap, yaitu pembuatan benang, pembuatan kain, dan proses penyempurnaan.
Proses penyempurnaan tekstil adalah suatu pengolahan tekstil yang untuk meningkatkan mutu bahan tekstil tersebut. Penyempurnaan bahan tekstil dapat dilakukan pada bentuk serat, benang, maupun kain.
Proses penyempurnaan tekstil melibatkan pemakaian senyawa kromium dalam jumlah besar. Senyawa kromium tersebut adalah kalium dikromat (K2Cr2O7) yang digunakan
untuk mengoksidasi zat warna belerang (Sugiharto 1987).
Dengan asam sulfat, kalium dikromat dapat melepaskan oksigen dengan reaksi: K2Cr2O7 + 4H2SO4 → K2SO4 + Cr2(SO4)3 +
4H2O + 3On
Dengan asam klorida tidak mengeluarkan oksigen, tetapi gas klor karena asam klorida mudah dioksidasi menjadi gas klor
K2Cr2O7 + 14HCl → 2KCl + 2CrCl3 + 7H2O
+ 3Cl2 (Sugiharto 1987).
Karena adanya pemakaian kromium di dalam industri tekstil, maka Sugiharto (1987) menyarankan parameter-parameter yang perlu diperhatikan dalam pemeriksaan air limbah industri tekstil adalah BOD, COD, pH, padatan tersuspensi, padatan terlarut total, minyak dan lemak, warna, suhu, kandungan fenol, sulfida, dan kromium. Berdasarkan Keputusan Menteri Negara Lingkungan Hidup (Kep 51/MENLH/10/1995) tentang baku mutu limbah cair bagi kegiatan industri, ambang batas kromium total dalam limbah cair industri tekstil adalah sebanyak 1 mg/L.
Pengendapan Kromium Heksavalen dengan Serbuk Besi
Besi adalah logam transisi golongan VIII B bernomor atom 28 dengan simbol Fe. Besi memiliki massa atom sebesar 55,845 g/mol, memiliki tingkat valensi bervariasi, yaitu +2, +3, +4, dan +6, . Besi memiliki massa jenis sebesar 7.86 g/cm3, titik leleh sebesar 1538 oC dan titik didih sebesar 2861oC. Besi merupakan unsur logam yang sangat melimpah di alam. Besi diyakini sebagai unsur yang paling melimpah ke-6 di alam semesta dan unsur paling melimpah ke-4 di bumi. Di bumi bagian dalam, konsentrasi besi lebih besar dari 80%. Berat besi secara keseluruhan di bumi menyumbang hampir 35% massa bumi.
Di alam, besi terdapat sebagai biji besi (Fe2O3) dan hampir tidak pernah ditemukan
sebagai unsur bebas. Untuk mendapatkan besi murni dari bijih besi, maka perlu dilakukan reduksi kimia untuk menyingkirkan senyawa-senyawa pengotor. Besi merupakan bahan dasar pembuatan baja. Selain itu, besi juga digunakan sebagai campuran logam (King 1994).
Logam besi valensi nol merupakan reaktan yang sangat menjanjikan karena harganya murah, mudah didapatkan, serta efektif dalam menghilangkan kontaminan. Sebagai pereduksi yang kuat, besi sering dipakai dalam reaksi dehalogenasi, mengurangi senyawa nitro aromatik, menghilangkan larutan pewarna, dan
menyingkirkan logam-logam berat (Junyapoon & Weerapong 2006).
Menurut Junyapoon & Weerapong (2006), pengendapan kromium heksavalen (Cr (VI)) dengan serbuk besi (besi bervalensi nol/Fe (0)) berdasar pada perubahan kromium dari bentuk toksik ke bentuk kurang toksik. Kromium heksavalen, yang merupakan oksidator kuat, diubah menjadi kromium trivalen yang kurang berbahaya dan kelarutannya dalam air lebih rendah sehingga mudah untuk diendapkan. Reduksi Cr(VI) oleh Fe(0) menghasilkan ion ferrat (Fe(III)) dan ion-ion kromium trivalen (Persamaan 1 atau 2). Kromium trivalen dapat dihilangkan dengan cara presipitasi atau ko-presipitasi sebagai campuran Fe(III) dan Cr(III) hidroksida seperti yang tertera pada persamaan 3 atau persamaan 4.
Cr6+ + Fe0 Cr3+ + Fe3+ (1) CrO42- + Fe0 + 8 H+ Cr3+ + Fe3+ + 4 H2O (2) (1-x)Fe3+ + (x)Cr3+ + 3 H2O (CrxFe(1-x)(OH)3(s) + 3 H+ (3) (1-x)Fe3+ + (x)Cr3+ + 2 H2O Fe(1-x)CrxOOH(s) + 3 H+ (4) Pengukuran Kromium
Beberapa metode telah digunakan untuk pengukuran kromium total dan kromium heksavalen pada berbagai material. Salah satunya adalah spektrofotometri sinar tampak. Kromium heksavalen bila ditambah 1,5-difenilkarbazida (DPC) dalam larutan asam membentuk kompleks berwarna merah violet yang intensitasnya sebanding dengan banyaknya kromium heksavalen dalam contoh. Pewarnaan dengan DPC cukup sensitif dengan nilai absorptivitas molar kira-kira 40.000 Lmol-1 cm-1 pada 540 nm (Clesceri 1989). Untuk mendapatkan kromium heksavalen dari sampel limbah tekstil, terlebih dahulu sampel dioksidasi dengan oksidator kuat yang akan mengoksidasi kromium trivalen menjadi kromium heksavalen. Menurut Noroozifar (2003), serium sangat efektif untuk mengoksidasi kromium trivalen menjadi kromium heksavalen. Kemampuan serium (Ce(IV)) dalam mengkonversi kromium trivalen menjadi kromium heksavalen sebesar 100 % (Wijayanti 2005). Nilai ini lebih baik bila dibandingkan dengan KMnO4 yang mampu mengkonversi 91%
Metode Penambahan Standar
Menurut Zellmer (1998), metode penambahan standar perlu dilakukan apabila matriks dari suatu sampel dapat mempengaruhi sensitivitas pengukuran sampel tersebut. Dengan kata lain, kemiringan dari kurva standar yang berpelarut air destilasi berbeda dengan kemiringan kurva yang berpelarut air rawa (atau matriks apapun yang kebetulan dipakai).
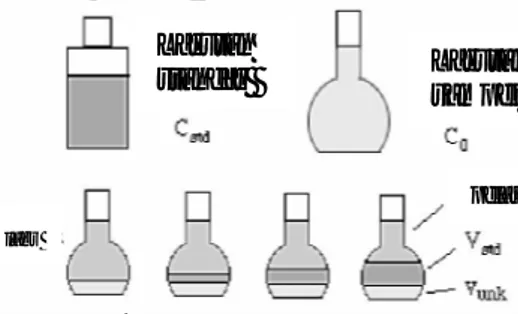
Untuk melakukan penambahan standar, kita perlu menyiapkan larutan dan peralatan sebagai berikut.
Gambar 1 Larutan dan peralatan metode penambahan standar
Volume yang konstan (Vunk) dari larutan
yang tidak dketahui ditambahkan ke dalam masing-masing labu ukur dengan volume Vflask. Kemudian ditambahkan larutan stok
dengan variasi volume yang semakin meningkat (Vstd). Terakhir, semua labu ukur
ditera dan dikocok. Konsentrasi dan volume larutan stok yang ditambahkan sebaiknya sedemikian rupa sehingga konsentrasi larutan yang tidak diketahui tersebut bertambah sebesar 30% pada masing-masing labu ukur.
Konsentrasi krom heksavalen pada setiap labu ukur (Cunk) dapat diketahui dengan
persamaan:
Karena nilai R=(K) x (konsentrasi), maka:
Jika Csa = CstdVstd/ , maka:
y = b + mx
Setelah mengukur nilai dari seperangkat larutan penambahan standar tersebut, hasilnya diplot, lalu diteruskan ke y=0 untuk mendapatkan nilai Csa. Nilai negatifnya dapat
digunakan untuk mendapatkan konsentrasi kromium heksavalen sampel limbah (Co).
BAHAN DAN METODE
Alat dan Bahan
Alat-alat yang digunakan adalah pengocok Heidolph Titramax 101 dan spektrofotometer UV-VIS Spectronic 20 D+. Bahan-bahan yang digunakan adalah Ce(NH4)2(SO4)3, 1,5-difenilkarbazida (DPC),
larutan Cr(VI) 30 ppm, serbuk besi, limbah proses pewarnaan tekstil dan limbah akhir teksil yang diambil dari pabrik tekstil PT Unitex.
Lingkup Penelitian
Penelitian ini meliputi beberapa tahap, yaitu preparasi serbuk besi, preparasi larutan bahan (larutan Cr(VI) 30 ppm, larutan DPC 0.25%, dan larutan Ce(IV) 0.4%), penentuan konsentrasi kromium total dan kromium heksavalen larutan sintetik, penentuan pengaruh pH, pengaruh kecepatan pengocok, pengaruh waktu pengocokan, pengaruh jumlah serbuk besi, penentuan konsentrasi kromium heksavalen larutan limbah tekstil, penentuan konsentrasi kromium heksavalen larutan limbah tekstil dengan metode penambahan standar, dan pengendapan kromium heksavalen larutan limbah tekstil dengan serbuk besi.
Preparasi Serbuk Besi
Serbuk besi direndam dalam HCl 3% dan dikocok dengan pengocok pada kecepatan 150 rpm selama 30 menit. HCl dibuang, kemudian serbuk besi dicuci dengan akuades lalu dibilas dengan aseton. Setelah itu, serbuk besi dikeringkan di dalam oven dengan suhu 105-110oC sampai bobotnya konstan.
Larutan standar Larutan sampel Vlabu pelarut Vlabu Vlabu Vlabu Vlabu Vlabu Vlabu Vlabu Vlabu Vlabu Vlabu
Preparasi Larutan Bahan
Larutan Cr(VI) 30 ppm dibuat dengan cara melarutkan 0.0848 g K2Cr2O7 ke dalam
akuades sehingga diperoleh satu liter larutan. Larutan DPC 0.25% dibuat dengan cara melarutkan 0.25 g DPC ke dalam aseton PA sehingga diperoleh 100 ml larutan.
Larutan Ce(IV) 0.4% dibuat dengan cara melarutkan 0,1207 g Ce(NH4)2(SO4)3 dalam
HNO3 0,5 M sehinga diperoleh 100 ml
larutan.
Pembuatan Kurva Standar
Pembuatan kurva standar menggunakan larutan standar Cr6+ dengan konsentrasi Cr6+ 0, 0.1, 0.2, 0.3, 0.4, 0.5, dan 0.75 ppm. Sebanyak 1 ml larutan kromium pada berbagai konsentrasi tersebut masing-masing dimasukkan ke dalam labu ukur 25 ml, kemudian ditambah 7 tetes H2SO4 18 N dan 1
ml DPC. Labu ditera, lalu dikocok dan dibiarkan 10 menit sebelum diukur serapannya pada panjang gelombang 540 nm. Pengukuran juga dilakukan pada larutan blanko. Kemudian dibuat kurva hubungan antara konsentrasi dan serapan.
Penentuan Konsentrasi Kromium
Heksavalen dan kromium Total Larutan kromium
Sebanyak 1 ml larutan kromium dimasukkan ke dalam labu ukur 25 ml, kemudian ditambah 7 tetes H2SO4 18 N dan 1
ml DPC. Labu ditera, lalu dikocok dan dibiarkan 10 menit sebelum diukur serapannya pada panjang gelombang 540 nm. Konsentrasi Cr6+ ditentukan dengan kurva standar.
Agar konsentrasi kromium total dapat dianalisis dengan spektrofotometer, maka Cr3+ perlu dioksidasi menjadi Cr6+. Oksidator yang digunakan adalah larutan Ce(IV) 0,4 %. Penentuan konsentrasi kromium heksavalen menggunakan kurva standar. Sebanyak 1 ml larutan kromium dimasukkan ke dalam labu ukur 25 ml, kemudian ditambahkan 1 ml larutan Ce(IV), 7 tetes H2SO4 18 N dan 1 ml
DPC. Labu ditera, lalu dikocok dan dibiarkan 10 menit sebelum diukur serapannya pada panjang gelombang 540 nm.
Penentuan Pengaruh pH
Larutan kromium sebanyak 50 ml dimasukkan ke dalam erlenmeyer 200 ml kemudian ditambahkan serbuk besi sebanyak 1 g. Setelah itu disesuaikan pH-nya dengan variasi 2, 3, 4, 5, 6 dengan cara menambahkan 0,5 M HNO3 atau 0,5 M NaOH. Campuran
lalu dikocok dengan pengocok pada kecepatan 150 rpm selama 30 menit. Setelah itu larutan
disaring menggunakan saringan vakum untuk menghilangkan serbuk besinya. Sebanyak 1 ml filtrat dimasukkan ke dalam labu ukur 25 ml kemudian ditambahkan 7 tetes H2SO4 18
N, dan 1 ml DPC, lalu ditambahkan akuades hingga tanda batas. Larutan dikocok dan didiamkan selama 5-10 menit sebelum diukur dengan spektrofotometer.
Penentuan Pengaruh Kecepatan
Pengocokan
Larutan kromium sebanyak 50 ml dimasukkan ke dalam erlenmeyer 200 ml kemudian ditambahkan serbuk besi sebanyak 1 g. Setelah itu diatur pH-nya menjadi 3 dengan cara menambahkan 0,5 M HNO3 atau
0,5 M NaOH. Campuran lalu dikocok dengan variasi kecepatan 150, 300, 450, 600 rpm selama 30 menit. Prosedur selanjutnya sama dengan prosedur penentuan pengaruh pH.
Penentuan Pengaruh Jumlah Serbuk Besi
Larutan kromium sebanyak 50 ml dimasukkan ke dalam erlenmeyer 200 ml kemudian ditambahkan serbuk besi yang telah dicuci dengan variasi 0.1, 0.5, 1, 1.5, 2, 2.5, 3, 4, 5, dan 6 gram. Setelah itu diatur pH-nya menjadi 3 dengan cara menambahkan 0,5 M HNO3 atau 0,5 M NaOH. Campuran lalu
dikocok dengan kecepatan 150 rpm selama 30 menit. Prosedur selanjutnya sama dengan prosedur penentuan pengaruh pH.
Penentuan Pengaruh Waktu Pengocokan
Larutan kromium sebanyak 50 ml dimasukkan ke dalam erlenmeyer 200 ml kemudian ditambahkan serbuk besi yang telah dicuci sebanyak 5 g. Setelah itu diatur pH-nya menjadi 3 dengan cara menambahkan 0,5 M HNO3 atau 0,5 M NaOH. Campuran lalu
dikocok dengan kecepatan 150 rpm selama waktu yang bervariasi (2, 4, 6, 8, dan 10 menit). Prosedur selanjutnya sama dengan prosedur penentuan pengaruh pH.
Penentuan Konsentrasi Kromium
Heksavalen Larutan Limbah Tekstil
Sebanyak 1 ml larutan limbah proses pewarnaan tekstil dimasukkan ke dalam labu ukur 25 ml. Prosedur selanjutnya sama dengan prosedur penentuan konsentrasi kromium heksavalen dan kromium total larutan sintetik.
Sebanyak 1 ml larutan limbah akhir tekstil dimasukkan ke dalam labu ukur 25 ml. Prosedur selanjutnya sama dengan prosedur penentuan konsentrasi kromium heksavalen dan kromium total larutan sintetik.
Penentuan Konsentrasi Kromium Heksavalen Larutan Limbah Tekstil Dengan Metode Penambahan Standar
Larutan standar Cr6+ sebanyak 12,5 ml dengan variasi konsentrasi Cr6+ 0, 0.1, 0.2, 0.3, 0.4, 0.5, dan 0.75 ppm masing-masing dimasukkan ke dalam labu ukur. Ke dalam setiap labu ukur ditambahkan limbah proses pewarnaan tekstil sebanyak 12,5 ml. Prosedur selanjutnya sama dengan prosedur penentuan konsentrasi kromium heksavalen. Pengukuran juga dilakukan pada larutan blanko. Kemudian dibuat kurva hubungan antara konsentrasi dan serapan.
Larutan standar Cr6+ sebanyak 12,5 ml dengan variasi konsentrasi Cr6+ 0, 0.1, 0.2, 0.3, 0.4, 0.5, dan 0.75 ppm masing-masing dimasukkan ke dalam labu ukur. Ke dalam setiap labu ukur ditambahkan limbah akhir tekstil sebanyak 12,5 ml. Prosedur selanjutnya sama dengan prosedur penentuan konsentrasi kromium heksavalen . Pengukuran juga dilakukan pada larutan blanko. Kemudian dibuat kurva hubungan antara konsentrasi dan serapan.
Pengendapan Kromium Heksavalen
Larutan Limbah Tekstil Dengan Serbuk Besi
Larutan limbah proses pewarnaan tekstil sebanyak 50 ml dimasukkan ke dalam erlenmeyer 200 ml kemudian ditambahkan serbuk besi sebanyak 5 g. Setelah itu disesuaikan pH-nya menjadi 3 dengan cara menambahkan 0,5 M HNO3 atau 0,5 M
NaOH. Campuran lalu dikocok dengan pengocok pada kecepatan 450 rpm selama 10 menit. Prosedur selanjutnya sama dengan prosedur penentuan pengaruh pH.
Larutan limbah akhir tekstil sebanyak 50 ml dimasukkan ke dalam erlenmeyer 200 ml kemudian ditambahkan serbuk besi sebanyak 5 g. Setelah itu disesuaikan pH-nya menjadi 3 dengan cara menambahkan 0,5 M HNO3 atau
0,5 M NaOH. Campuran lalu dikocok dengan pengocok pada kecepatan 450 rpm selama 10 menit. Prosedur selanjutnya sama dengan prosedur penentuan pengaruh pH.
HASIL DAN PEMBAHASAN
Panjang Gelombang Maksimum
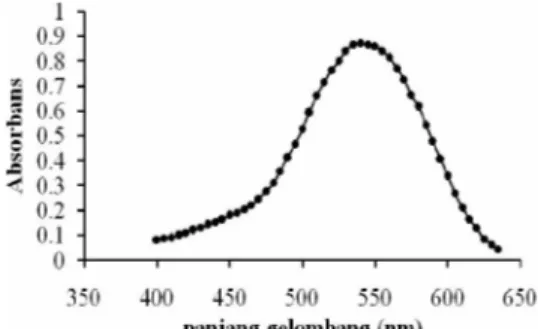
Pengukuran serapan larutan kompleks DPC-kromium heksavalen 1.2 ppm pada berbagai panjang gelombang memberikan hasil serapan maksimum (λ maks) pada 540 nm. Serapan pada 540 nm untuk larutan kompleks DPC-kromium heksavalen 1.2 ppm adalah sebesar 0.873 (Lampiran 2). Kurva
hubungan serapan pada berbagai panjang gelombang tertera pada Gambar 2.
Gambar 2 Hubungan panjang gelombang dengan serapan larutan kompleks DPC-Cr(VI).
Pengukuran serapan larutan kompleks DPC-kromium heksavalen 1.2 ppm dengan penambahan larutan Ce(IV) pada berbagai panjang gelombang memberikan hasil λ maks sebesar 540 nm. Serapan pada 540 nm untuk larutan kompleks DPC-kromium heksavalen 1.2 ppm dengan penambahan larutan Ce(IV) adalah sebesar 0.555 (Lampiran 3). Kurva hubungan serapan pada berbagai panjang gelombang tertera pada Gambar 3.
Gambar 3 Hubungan panjang gelombang dengan serapan larutan kompleks DPC-Cr(VI) dengan penambahan Ce(IV)
Pengukuran larutan kromium heksavalen selanjutnya hanya dilakukan pada panjang gelombang 540 nm. Pengukuran serapan larutan pada panjang gelombang maksimum memiliki ketelitian yang tinggi dan dapat mengurangi kesalahan pengukuran dalam menentukan konsentrasi suatu senyawa secara spektrofotometri karena pengukuran pada panjang gelombang maksimum akan meningkatkan kepekaan analisis.
Penambahan Ce(IV) menyebabkan terjadinya perbedaan nilai serapan antara larutan kompleks DPC-kromium tanpa penambahan larutan Ce(IV) dan larutan kompleks DPC-kromium dengan penambahan larutan Ce(IV) . Hal ini terjadi karena larutan Ce(IV) mempunyai warna kuning yang menyerap sinar pada wilayah panjang gelombang 400-480 nm (Gambar 4), sehingga
menganggu pengukuran serapan larutan kompleks DPC-kromium heksavalen yang berwarna ungu dan penyerapan warnanya berada pada wilayah panjang gelombang 500-560 nm (Day & Underwood 2002). Namun penambahan Ce(IV) tidak menggeser panjang gelombang serapan maksimum karena warna larutan tetap menjadi ungu sehingga panjang gelombang 540 nm juga dipakai untuk penentuan konsentrasi kromium heksavalen total.
Gambar 4 Hubungan panjang gelombang dengan serapan larutan Ce (IV)
Pengaruh pH
Kondisi keasaman memiliki pengaruh yang cukup besar terhadap reaksi reduksi Cr(VI) oleh Fe(0). Menurut persamaan (2), reduksi Cr(VI) dapat terjadi pada suasana asam, yaitu pada pH rendah. Bertambahnya jumlah H+ akan menggeser kesetimbangan reaksi reduksi Cr (VI) ke arah kanan sehingga jumlah Cr(VI) yang tereduksi bertambah banyak (Junyapoon & Weerapong 2006).
Nilai serapan pada larutan kromium heksavalen yang telah direaksikan dengan sebuk besi menunjukkan jumlah kromium heksavalen yang tersisa pada larutan. Semakin kecil nilai serapan, maka konsentrasi kromium heksavalen yang tersisa semakin kecil. Nilai pH optimum adalah nilai pH yang menunjukkan konsentrasi terkecil.
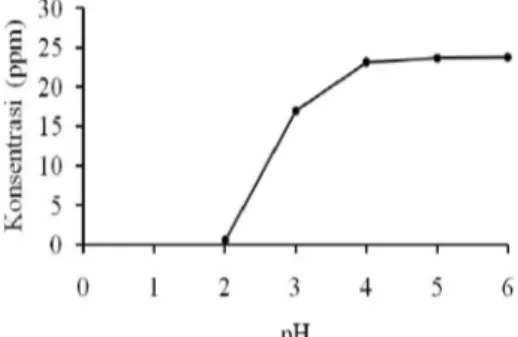
Hasil penelitian menunjukkan bahwa nilai konsentrasi terkecil diberikan oleh larutan yang memiliki pH 2, yaitu sebesar 0.483 ppm (Gambar 5 dan Lampiran 6). Namun hal tersebut tidak menunjukkan bahwa pH 2 adalah pH yang optimum karena secara fisik dapat terlihat bahwa pada pH 2 larutan menjadi keruh setelah direaksikan dengan serbuk besi, sedangkan warna larutan kromium heksavalen pada pH yang lainnya adalah jingga. Seiring dengan kenaikan pH, warna jingga larutan semakin pudar. Pada pH 3, warna jingga larutan menjadi sangat pudar
dan terlihat lebih bening dibandingkan pada pH lainnya. Ini menunjukkan bahwa pada pH 3, konsentrasi kromium heksavalen yang tersisa paling kecil. Hal ini sesuai dengan hasil yang diperoleh Junyapoon & Weerapong (2006) yaitu nilai pH optimum pengendapan kromium heksavalen dengan serbuk besi adalah pada pH 3.
Gambar 5 Hubungan pH larutan dengan konsentrasi kromium heksavalen
Nilai konsentrasi yang kecil pada pH 2 disebabkan oleh kekeruhan larutan. Kekeruhan tersebut mengganggu pembentukan warna ungu kompleks DPC-kromium heksavalen. Kekeruhan tersebut disebabkan oleh pH larutan yang terlalu rendah yang berakibat pada proses pengkaratan besi yang meningkat dengan sangat cepat (Junyapoon & Weerapong 2006). Tidak terbentuknya warna jingga pada pH 2 dapat disebabkan oleh karena tidak adanya kesetimbangan ion kromiumat-dikromiumat sehingga yang ada pada larutan tersebut hanyalah ion-ion kromiumat (HCrO4-) yang
tidak menghasilkan warna jingga (Cotton & Wilkinson 1989).
Pengaruh Kecepatan Pengocokan
Produk reaksi akan terbentuk jika: molekul-molekul reaktan saling bertumbukan, tumbukan tersebut memiliki cukup energi, dan molekul-molekul tersebut bertumbukan pada orientasi yang tepat (Kotz et al. 2006). Salah satu cara agar molekul-molekul reaktan dapat bertumbukan adalah dengan melakukan pengocokan.
Variasi pengocokan pada larutan kromium heksavalen yang telah ditambahkan dengan besi menunjukkan nilai serapan yang berbeda. Pada pengocokan dengan kecepatan 150 rpm, nilai konsentrasi kromium heksavalen yang tersisa adalah sebesar 21.63 ppm. Nilai konsentrasi kromium heksavalen menurun menjadi 20.52 ppm pada kecepatan
pengocokan 300 rpm. Nilai konsentrasi kromium heksavalen kembali meningkat pada kecepatan 450 rpm, yaitu sebesar 24.97 ppm. Nilai tersebut menurun pada kecepatan 600 rpm, yaitu sebesar 15.96 ppm (Gambar 6 dan Lampiran 7).
Gambar 6 Hubungan konsentrasi kromium heksavalen dengan kecepatan pengocokan
Ketidakteraturan perubahan nilai konsentrasi kromium heksavalen pada variasi-variasi kecepatan pengocokan berkaitan dengan kesetimbangan reaksi. Nilai konsentrasi kromium heksavalen pada kecepatan pengocokan 450 rpm menunjukkan nilai yang tinggi. Hal ini karena pada kecepatan tersebut, reaksi pengendapan berada pada keadaan setimbangnya. Nilai konsentrasi kromium heksavalen pada kecepatan pengocokan 600 rpm menunjukkan nilai yang paling rendah. . Hal ini terjadi karena pada kecepatan tersebut reaksi dapat lebih cepat mencapai tahap kesetimbangannya, sehingga pada saat pengocokan telah selesai, reaksi telah melewati tahap kesetimbangannya. Ketika reaksi telah melewati tahap kesetimbangan, reaksi akan cenderung berbalik arah (Hargis 1998). Hal ini menyebabkan reaksi menjadi berbalik arah menuju pembentukan Cr(VI).
Hasil penelitian menunjukkan bahwa kecepatan pengocokan optimum pengendapan kromium heksavalen dengan serbuk besi adalah pada kecepatan 450 rpm. Hasil ini tidak sesuai dengan penelitian Junyapoon & Weerapong (2006) yang tidak dapat menemukan kondisi optimum kecepatan pengocokan karena peralatan pengocok yang digunakan pada penelitian Junyapoon & Weerapong (2006) memiliki kecepatan pengocokan maksimum pada 250 rpm.
Pengaruh Jumlah Serbuk Besi
Jumlah serbuk besi akan mempengaruhi konsentrasi kromium heksavalen yang mengendap, menurut persamaan (1) atau (2)
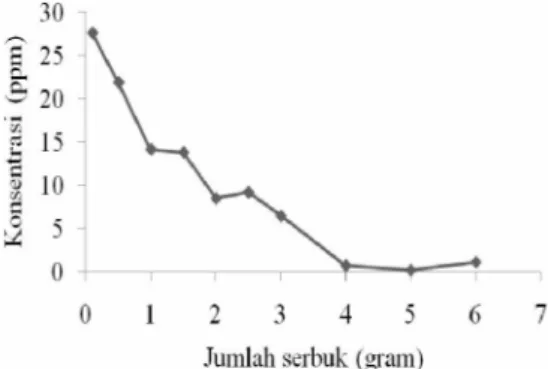
dan (3) atau (4). Hasil penelitian menunjukkan adanya penurunan konsentrasi kromium heksavalen seiring dengan bertambahnya jumlah serbuk besi sampai dengan 5 gram. Pada jumlah serbuk besi lebih dari 5 gram, terjadi kenaikan kembali konsentrasi kromium heksavalen (Gambar 7 dan Lampiran 8). Ini menunjukkan bahwa jumlah optimum serbuk besi pada pengendapan kromium heksavalen dengan serbuk besi adalah sebesar 5 gram.
Gambar 7 Hubungan konsentrasi kromium heksavalen dengan jumlah serbuk besi
Penurunan konsentrasi kromium heksavalen seiring dengan bertambahnya jumlah serbuk besi sesuai dengan penelitian Junyapoon & Weerapong (2006). Dengan bertambahnya jumlah serbuk besi, maka jumlah sisi aktif reaksi dari serbuk besi akan meningkat sehingga jumlah kromium heksavalen yang bereaksi pun akan meningkat. Namun kenaikan kembali konsentrasi kom heksavalen pada jumlah serbuk besi sebanyak 6 gram tidak sesuai dengan penelitian Junyapoon & Weerapong (2006), yaitu bahwa setelah mencapai jumlah optimum, konsentrasi kromium heksavalen tidak akan meningkat. Hasil penelitian Junyapoon & Weerapong (2006) juga menunjukkan perbedaan pada jumlah optimum serbuk besi, yaitu sebesar 1 gram. Hal ini dapat disebabkan oleh perbedaan sumber dan ukuran serbuk besi, dan kondisi peralatan laboratorium yang digunakan.
Pengaruh Waktu Pengocokan
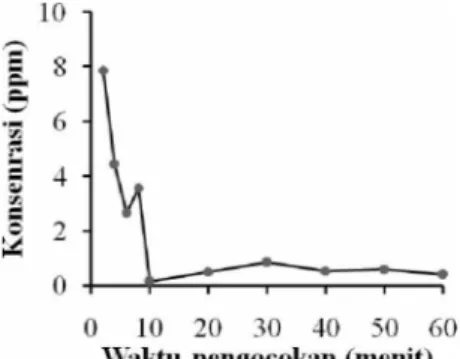
Pengocokan larutan kromium dengan serbuk besi memerlukan waktu agar kromium heksavalen dapat tereduksi oleh besi. Hasil penelitian menunjukkan kecenderungan penurunan konsentrasi kromium heksavalen seiring bertambahnya waktu pengocokan. Hal ini dapat terjadi karena bertambahnya waktu akan menjaga keberlangsungan reduksi Cr(VI) sampai titik kesetimbangannya
tercapai. Pada waktu pengocokan 10 menit, konsentrasi kromium heksavalen berada pada nilai terendahnya, yaitu 0.14 ppm. Setelah 10 menit, konsentrasi kromium heksavalen kembali meningkat (Gambar 8 dan Lampiran 9). Hal ini dapat disebabkan oleh kesetimbangan reaksi yang telah melewati titik kesetimbangannya sehingga kromium heksavalen akan kembali terbentuk. Ketika reaksi telah melewati tahap kesetimbangan, reaksi akan cenderung berbalik arah (Hargis 1998). Hasil ini tidak sesuai dengan penelitian Junyapoon & Weerapong (2006), yaitu bahwa waktu pengocokan optimum pengendapan kromium heksavalen dengan serbuk besi adalah 180 menit. Hal ini dapat disebabkan oleh perbedaan jumlah serbuk besi yang dipakai. Junyapoon & Weerapong (2006) memakai serbuk besi sebanyak 1 gram, berdasarkan pada jumlah optimum serbuk besi pada penelitian tersebut, sedangkan penelitian ini menggunakan serbuk besi sebanyak 5 gram, berdasarkan pada jumlah optimum serbuk besi pada penelitian ini.
Gambar 8 Hubungan konsentrasi kromium heksavalen dengan waktu pengocokan
Hubungan konsentrasi terhadap berbagai macam kondisi (kecepatan pengocokan, jumlah serbuk besi, pH, dan waktu pengocokan) yang digambarkan ke dalam bentuk plot penyebaran tiga dimensi dapat dilihat pada Lampiran 10.
Konsentrasi Kromium Heksavalen Larutan Limbah Tekstil
Hasil pengukuran serapan kromium heksavalen larutan limbah akhir tekstil menunjukkan nilai 0.003 (Lampiran 11). Nilai tersebut menunjukkan bahwa konsentrasi kromium heksavalen pada larutan tersebut sangat kecil. Hal ini karena proses pengolahan limbah pabrik tekstil tempat limbah ini berasal berjalan dengan baik. Namun pengukuran konsentrasi kromium heksavalen yang akurat tidak dapat dilakukan pada larutan tersebut dengan menggunakan metode
spektrofotometri karena larutan tersebut memiliki banyak matriks pengotor. Pengotor tersebut dapat mengganggu respon instrumen dalam mengukur analat, atau bahkan dapat menghasilkan respon instrumen sendiri (Harris 2003). Karena itu perlu dilakukan metode penambahan standar.
Hasil pengukuran serapan larutan limbah proses pewarnaan tekstil menunjukkan nilai 0.011 (Lampiran 11). Namun nilai tersebut tidak dapat dikatakan akurat karena larutan tersebut sudah berwarna ungu sebelum direaksikan dengan DPC. Hal ini mengganggu pengukuran karena hasil pembentukan kompleks DPC-kromium juga menghasilkan warna ungu. Karena itu perlu dilakukan metode penambahan standar.
Konsentrasi Kromium Heksavalen Larutan Limbah Tekstil Dengan Metode
Penambahan Standar
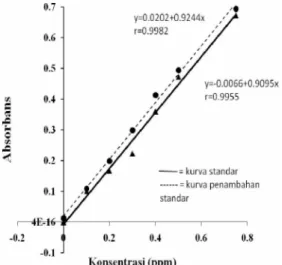
Kurva penambahan standar larutan limbah proses pewarnaan tekstil mempunyai kemiringan yang berbeda dengan kurva standar (Gambar 9). Ini menunjukkan bahwa matriks dari larutan limbah tersebut mempengaruhi pengukuran sampel.
Gambar 9 Hubungan konsentrasi kromium heksavalen dengan serapan larutan standar dan larutan limbah proses pewarnaan tekstil dengan penambahan standar
Dengan meneruskan kurva hingga menyentuh sumbu x (y=0) maka didapatkan konsentrasi kromium heksavalen larutan limbah proses pewarnaan tekstil, yaitu sebesar 0.42 ppm (Lampiran 14). Hasil ini berbeda dengan hasil pengukuran konsentrasi kromium heksavalen dengan memakai metode AAS, yaitu <0.01 ppm (Lampiran 15). Nilai konsentrasi yang kecil dari hasil metode AAS menunjukkan bahwa konsentrasi kromium heksavalen pada limbah proses pewarnaan
tekstil tersebut tidak melewati ambang batas maksimum kromium heksavalen di dalam air, yaitu sebesar 0.05 ppm (Peraturan Pemerintah Republik Indonesia nomor 82 tahun 2001). Sedangkan jika mengacu pada metode penambahan standar, konsentrasi kromium heksavalen pada limbah proses pewarnaan tekstil tersebut telah melewati ambang batas maksimum kromium heksavalen di dalam air. Hal ini disebabkan oleh perbedaan ketepatan kedua metode tersebut.
Kurva penambahan standar larutan limbah akhir tekstil mempunyai kemiringan yang sama dengan kurva standar (Gambar 10). Hal ini juga ditunjukkan oleh slope kedua kurva yang memiliki nilai yang hampir sama, yaitu 0.88 pada kurva standar dan 0.90 pada kurva penambahan standar (Lampiran 16). Ini menunjukkan bahwa matriks pada larutan limbah akhir tekstil tersebut tidak terlalu mengganggu pengukuran konsentrasi kromium heksavalen pada larutan limbah tersebut. Pengukuran konsentrasi kromium heksavalen larutan limbah akhir tekstil dapat dilakukan dengan menggunakan perbandingan kemiringan kurva (Brewer 1980).
Gambar 10 Hubungan konsentrasi kromium heksavalen dengan serapan larutan standar dan larutan limbah akhir tekstil dengan penambahan standar
Serapan yang terukur pada setiap penambahan standar merupakan jumlah dari serapan standar dan serapan sampel (Brewer 1980). Dari nilai serapan sampel larutan limbah akhir tekstil, dapat diketahui konsentrasi sampel tersebut dengan metode kemiringan kurva, yaitu sebesar 0.04 ppm (Lampiran 17). Hasil ini menunjukkan bahwa konsentrasi kromium heksavalen larutan limbah tersebut tidak melebihi ambang batas maksimum kromium heksavalen di dalam air.
Pengendapan Kromium Heksavalen Larutan Limbah Tekstil Dengan Serbuk
Besi
Kondisi yang dipakai untuk pengendapan kromium heksavalen larutan limbah tekstil dengan serbuk besi adalah kondisi optimum yang telah didapatkan melalui penentuan pengaruh pH, penentuan kecepatan pengocokan, penentuan jumlah serbuk besi, dan penentuan waktu pengocokan. Kondisi optimumnya adalah pada pH 3, kecepatan 450 rpm, jumlah besi 5 gram, dan waktu pengocokan 10 menit.
Pengukuran serapan setelah pengendapan menghasilkan nilai serapan sebesar 0.002 pada larutan limbah proses pewarnaan tekstil, dan sebesar 0.000 pada larutan limbah akhir tekstil (Lampiran 18). Hal ini menunjukkan bahwa kondisi optimum yang telah didapatkan sebelumnya dapat dipakai pada larutan limbah tekstil asli.
SIMPULAN DAN SARAN
Simpulan
Kondisi optimum pH, kecepatan pengocokan, jumlah serbuk besi, dan waktu pengocokan pengendapan kromium heksavalen dengan serbuk besi berturut-turut adalah pH 3, 450 rpm, 5 gram, dan 10 menit yang memberikan nilai konsentrasi kromium heksavalen tersisa berturut-turut sebesar 16.98 ppm, 15.96 ppm, 0.24 ppm, dan 0.14 ppm.
Serbuk besi sangat baik digunakan untuk mengendapkan kromium heksavalen dari larutan limbah tekstil karena mampu mengendapkan kromium heksavalen dalam jumlah yang banyak dalam waktu yang relatif singkat. Nilai serapan kromium heksavalen larutan limbah tekstil setelah direaksikan dengan serbuk besi pada kondisi optimum adalah sebesar 0.002 untuk larutan limbah proses pewarnaan tekstil, dan sebesar 0.000 untuk larutan limbah akhir tekstil.
Saran
Sebaiknya digunakan larutan sampel limbah yang lebih banyak mengandung kromium heksavalen daripada limbah yang digunakan pada penelitian ini sehingga efektifitas serbuk besi dalam megendapkan kromium heksavalen dapat ditelaah lebih jauh. Perlu dicari metode pengukuran konsentrasi kromium heksavalen selain metode spektrofotometri yang tidak menghasilkan warna ungu agar pengukuran tidak terganggu
oleh warna ungu larutan limbah proses pewarnaan tekstil.
DAFTAR PUSTAKA
Bowman RS. 2003. Applications of surfactant-modified zeolites to environmental remediation. Microporous and Mesoporous Materials 61:43-56.Brewer S. 1980. Solving Problems in Analytical Chemistry. New York: John Wiley and Sons.
Cotton FA, Wilkinson G. 1989. Kimia Anorganik Dasar. Sahati Suharto, penerjemah. Jakarta: UI-Press. Terjemahan dari: Basic Inorganic Chemistry.
Chen JM, Hao OJ. 1998. Microbial Chromium(VI) Reduction. Critical Rev. Environ Sci Technol 28:219-251.
Clesceri LS, Greenberg AE, Eaton AD. 1998. Standard Methods for the the Examination of Water and Wastewater. Ed ke-20. Washington DC: Apha Awwa Wes.
Day RA, Underwood AL. 2002. Analisis Kimia Kuantitatif. Sopyan I, penerjemah; Simarmata L, editor. Ed ke-6. Jakarta: Erlangga. Terjemahan dari: Quantitative Analysis.
Hargis LG. 1988. Analytical Chemistry: Principles and Techniques. New Jersey: Prentice Hall.
Harris DC. 2003. Quantitative Chemical Analysis. Ed ke-6. New York: W.H. Freeman.
Hideaki Y, Toshiiyuki Y, Takashi T. 2002. Adsorption of chromate and arsenate by amino-functionalized MCM-41 and SBA-1. Chem Mater 14:4603-4610.
Jefferson Lab. Chrome Element. http://education.jlab.org/itselemental/ ele024.html [31 Des 2006].
Junyapoon S, Weerapong S. 2006. Removal of Hexavalent Chromium from
Aqueos Solutions by Scrap Iron Filings. KMITL Sci Tech J 6:1-12. King RB. 1994. Encyclopedia of Inorganic
Chemistry. Chicester: John Willey and Sons.
Kotz JC, Treichel MP, Weaver CG. 2006. Chemistry and Chemical Reactivity. Ed ke-6. Belmont: Thomson Brooks/Cole.
Kusnoputranto H. 1996. Toksikologi Lingkungan Logam Toksik dan B3. Jakarta: UI-Press.
Manahan SE. 2003. Toxicology Chemistry and Biochemistry. Ed ke-3. New York: Lewis Publishers.
Martha F. 2004. Penetapan Limit Deteksi dan Limit Respon Linear serta Pengaruh Oksidasi terhadap Pengukuran kromium dengan Spektrofotometri Sinar Tampak [Skripsi]. Bogor: Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Massaro EJ. 1997. Handbook of Human
Toxicology. New York: CRC Press.
Mertz W. 1987. Trace Element in Human and Animal Nutrition. Ed ke-5. San Diego: Academic Press.
Noroozifar M, Khorasani-Motlagh M. 2003. Specific Extraction of Chromium as Tetrabutylammonium-Chromate and Spectrophotometric Determination by Diphenylcarbazide: Speciation of Chromium in Effluent Streams. Anal Sci 19:705-708.
Peraturan Pemerintah. 2001. PP No 82 tentang Pengolahan Kualitas Air dan Pengendalian Pencemaran Air. Sugiharto. 1987. Dasar-dasar Pengolahan Air
Limbah. Cetakan ke-1. Jakarta: UI-Press.
Sutamihardja, RTM. 2002. Toksikologi Lingkungan. Bogor: Institut Pertanian Bogor.
Wahyuadi SJ. 2004. Pengolahan dan Pemanfaatan Limbah Industri Penyamakan Kulit. http://www.KimPraswil.go.id/balitba
ng/Puskim/protek_Kim/ttg_Kim_Li mbah_kulit.html [17 Mar 2007]. Wijayanti E. 2005. Ekstraksi kromium
Heksavalen sebagai Tetrabutil Amonium-kromiumat dan Pengukuran secara Spektrofotometri Sinar Tampak [Skripsi]. Bogor: Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Zellmer DL. 1998. Standard Addition. http://zimmer.csufresno.edu/~davidz/ Chem106/StdAddn/StdAddn.html [6 Jan 2009].
14
Lampiran 1 Bagan alir penelitian
Preparasi serbuk besi Sampel Larutan Krom Penentuan kadar krom
heksavalen dan total awal
Ragam pH Ragam dosis serbuk besi
Saring
Penentuan kadar krom heksavalen dan total akhir
Filtrat Ragam kecepatan pengadukan Ragam waktu pengocokan Optimasi Penerapan kondisi optimum pada limbah tekstil
15
Lampiran 2 Serapan larutan Cr(VI) pada panjang gelombang 400-635 nm
Panjang gelombang (nm) Serapan Panjang gelombang (nm) Serapan
400 0.081 520 0.764 405 0.088 525 0.801 410 0.091 530 0.841 415 0.099 535 0.866 420 0.109 540 0.873 425 0.120 545 0.866 430 0.131 550 0.860 435 0.142 555 0.841 440 0.153 560 0.812 445 0.166 565 0.769 450 0.179 570 0.725 455 0.189 575 0.665 460 0.206 580 0.616 465 0.221 585 0.543 470 0.245 590 0.478 475 0.277 595 0.406 480 0.311 600 0.337 485 0.358 605 0.266 490 0.413 610 0.211 495 0.465 615 0.166 500 0.528 620 0.127 505 0.591 625 0.084 510 0.661 630 0.063 515 0.712 635 0.043
Lampiran 3 Serapan larutan kompleks DPC-Cr(VI) dengan penambahan Ce(IV) pada panjang gelombang 410-630 nm
Panjang gelombang (nm) Serapan Panjang gelombang (nm) Serapan
410 0.007 525 0.503 415 0.015 530 0.528 420 0.025 535 0.543 425 0.036 540 0.555 430 0.048 545 0.552 435 0.053 550 0.549 440 0.063 555 0.534 445 0.072 560 0.517 450 0.083 565 0.489 455 0.091 570 0.458 460 0.100 575 0.427 465 0.115 580 0.391 470 0.130 585 0.348 475 0.153 590 0.309 480 0.177 595 0.270 485 0.210 600 0.181 490 0.241 605 0.148 495 0.283 610 0.118 500 0.322 615 0.091 505 0.364 620 0.070 510 0.404 625 0.050 515 0.441 630 0.036 520 0.473
16
Lampiran 4 Serapan larutan Ce(IV) pada panjang gelombang 345-530 nm
Panjang gelombang (nm) Serapan Panjang gelombang (nm) Serapan
345 1.142 440 0.686 350 1.251 445 0.568 355 1.301 450 0.463 360 1.376 455 0.387 365 1.420 460 0.316 370 1.494 465 0.253 375 1.585 470 0.202 380 1.657 475 0.158 385 1.744 480 0.124 390 1.795 485 0.096 395 1.853 490 0.072 400 1.853 495 0.059 405 1.795 500 0.049 410 1.657 505 0.037 415 1.318 510 0.028 420 1.154 515 0.016 425 1.154 520 0.012 430 0.974 525 0.007 435 0.818 530 0.005
Lampiran 5 Kurva standar penentuan pengaruh pH , jumlah serbuk besi, kecepatan pengocokan dan waktu pengocokan
Konsentrasi (ppm) Serapan 0.00 0.10 0.20 0.30 0.40 0.50 0.75 0.000 0.066 0.165 0.238 0.334 0.446 0.616
Lampiran 6 Pengukuran serapan larutan hasil penentuan pengaruh pH Ulangan 1 Ulangan 2 pH Serapan 2 3 4 5 6 0.010 0.575 0.780 0.807 0.812 Ulangan 3 Rerata pH Serapan 2 3 4 5 6 0.013 0.599 0.812 0.830 0.836 pH Serapan 2 3 4 5 6 0.013 0.585 0.801 0.824 0.824 pH Serapan Konsentrasi (ppm) 2 3 4 5 6 0.012 0.586 0.798 0.820 0.824 0.48 16.98 23.06 23.70 23.81
17
Contoh perhitungan konsentrasi: Persamaan kurva standar, y = -0.0048+0.8701x 0.012 = -0.0048+0.8701x x = 0.012+0.0048 0.8701 = 0.0193
Konsentrasi = x. faktor pengenceran= 0.0193. = 0.48 ppm
Lampiran 7 Pengukuran serapan larutan hasil penentuan kecepatan pengocokan Ulangan 1 Ulangan 2 Kecepatan (rpm) Serapan 150 300 450 600 0.726 0.690 0.848 0.529 Ulangan 3 Rerata Kecepatan (rpm) Serapan 150 300 450 600 0.770 0.726 0.860 0.556 Contoh perhitungan konsentrasi: Persamaan kurva standar, y = -0.0048+0.8701x 0.748 = -0.0048+0.8701x x = 0.748+0.0048 0.8701 = 0.8652
Konsentrasi = x. faktor pengenceran= 0.8652. = 21.63 ppm
Lampiran 8 Pengukuran serapan larutan hasil penentuan pengaruh jumlah serbuk besi Ulangan 1 Ulangan 2
Jumlah serbuk (gram) Serapan 0.1 0.5 1.0 1.5 2.0 2.5 3.0 4.0 5.0 6.0 0.886 0.690 0.479 0.471 0.301 0.299 0.218 0.019 0.003 0.036 Kecepatan (rpm) Serapan 150 300 450 600 0.750 0.712 0.886 0.569
Kecepatan (rpm) Serapan Konsentrasi (ppm) 150 300 450 600 0.748 0.710 0.864 0.551 21.63 20.52 24.97 15.96
Jumlah serbuk (gram) Serapan 0.1 0.5 1.0 1.5 2.0 2.5 3.0 4.0 5.0 6.0 0.951 0.759 0.474 0.481 0.271 0.326 0.223 0.024 0.004 0.034
18
Lanjutan Lampiran 8
Ulangan 3 Rerata Jumlah serbuk (gram) Serapan
0.1 0.5 1.0 1.5 2.0 2.5 3.0 4.0 5.0 6.0 1.046 0.836 0.511 0.476 0.305 0.322 0.222 0.023 0.003 0.035 Contoh perhitungan konsentrasi: Persamaan kurva standar, y = -0.0048+0.8701x 0.956 = -0.0048+0.8701x x = 0.956+0.0048 0.8701 = 1.1042
Konsentrasi = x. faktor pengenceran= 1.1042. = 27.60 ppm
Lampiran 9 Pengukuran serapan larutan hasil penentuan pengaruh waktu pengocokan Ulangan 1 Ulangan 2 Waktu pengocokan (menit) Serapan 2 4 6 8 10 20 30 40 50 60 0.270 0.152 0.090 0.119 0.000 0.005 0.009 0.005 0.009 0.000 Rerata Waktu pengocokan (menit) Serapan Konsentrasi (ppm) 2 4 6 8 10 20 30 40 50 60 0.269 0.150 0.087 0.119 0.000 0.004 0.015 0.005 0.007 0.000 7.87 4.45 2.64 3.56 0.14 0.25 0.57 0.28 0.34 0.14
Jumlah serbuk (gram) Serapan Konsentrasi (ppm) 0.1 0.5 1.0 1.5 2.0 2.5 3.0 4.0 5.0 6.0 0.956 0.758 0.488 0.476 0.292 0.316 0.221 0.022 0.004 0.035 27.60 21.91 14.15 13.82 8.52 9.21 6.48 0.77 0.24 1.15 Waktu pengocokan (menit) Serapan 2 4 6 8 10 20 30 40 50 60 0.268 0.148 0.084 0.119 0.000 0.003 0.021 0.005 0.006 0.000
19
Lanjutan Lampiran 9
Contoh perhitungan konsentrasi: Persamaan kurva standar, y = -0.0048+0.8701x 0.269 = -0.0048+0.8701x x = 0.012+0.0048 0.8701 = 0.3147
Konsentrasi = x. faktor pengenceran= 0.3147. = 7.87 ppm
Lampiran 10 Plot Penyebaran Tiga Dimensi
Hubungan dari berbagai macam kondisi (kecepatan pengocokan, waktu,pH, dan waktu pengocokan) dapat digambarkan ke dalam bentuk plot penyebaran tiga dimensi sebagai berikut: a. Plot penyebaran tiga dimensi konsentrasi terhadap jumlah serbuk besi dan pH.
b. Plot penyebaran tiga dimensi konsentrasi terhadap kecepatan pengocokan dan waktu pengocokan
c. Plot penyebaran tiga dimensi konsentrasi terhadap jumlah serbuk besi dan kecepatan pengocokan
d. Plot penyebaran tiga dimensi konsentrasi terhadap waktu pengocokan dan pH e. Plot penyebaran tiga dimensi konsentrasi terhadap kecepatan pengocokan dan pH
f. Plot penyebaran tiga dimensi konsentrasi terhadap jumlah serbuk besi dan waktu pengocokan
(a) 6 Konse ntrasi (ppm) 0 4 10 pH 20 30 0 2 4 2 6 Ju ml ah se rbu k be si (gram)
20 Lanjutan Lampiran 10 (b) 60 40 Konsentrasi (ppm) 0 10 20 Waktu (menit) 20 200 400 0 600 Kecepatan (rpm)
Plot Penyebaran 3D Konsentrasi terhadap Kecepatan Pengocokan dan Waktu Kontak
(c) 600 Konsentrasi (ppm) 0 400 10 20 30 0 2 200 Kecepatan pengocokan (rpm) 4 6
Jumlah serbuk besi (ppm)
21 Lanjutan Lampiran 10 (d) 6 Konse ntrasi (ppm) 0 4 10 pH 20 0 20 2 40 60 Waktu (m e nit)
Plot Penyebaran 3D Konsentrasi Terhadap Waktu Kontak dan pH
(e) 6 Konse ntrasi (ppm) 0 4 10 pH 20 200 2 400 600 Ke ce patan pe n gocokan (rpm)
22 Lanjutan Lampiran 10 (f) 60 40 Konse ntrasi (ppm) 0 10 20 30
W aktu (me n it)
20 0 2 4 0 6 Ju ml ah se rbu k be si (gram)
Plot Penyebaran 3D Konsentrasi Terhadap Jumlah Serbuk Besi dan Waktu
Lampiran 11 Pengukuran serapan larutan limbah tekstil
Jenis Limbah Serapan
Ulangan 1 Ulangan 2 Rerata Limbah proses pewarnaan tekstil
Limbah akhir tekstil
0.012 0.000 0.011 0.005 0.012 0.003
Lampiran 12 Kurva standar pengukuran konsentrasi krom heksavalen larutan limbah tekstil dengan metode penambahan standar
Konsentrasi (ppm) Serapan 0.0 0.1 0.2 0.3 0.4 0.5 0.75 0.000 0.101 0.167 0.223 0.361 0.474 0.674
23
Lampiran 13 Pengukuran serapan larutan limbah tekstil dengan penambahan standar Limbah proses pewarnaan
Limbah akhir
Konsentrasi standar(ppm) Serapan 0.0 0.1 0.2 0.3 0.4 0.5 0.75 0.119 0.169 0.277 0.337 0.381 0.456 0.575
Lampiran 14 Contoh perhitungan konsentrasi krom heksavalen larutan limbah proses pewarnaan tekstil dengan metode penambahan standar
Konsentrasi larutan limbah dapat dihitung dengan persamaan:
;
C0 = konsentrasi larutan limbahCSA = nilai (x) dari persamaan kurva penambahan standar
(y = 0.1315 + 0.6197x) saat y = 0 Vflask = Volume labu ukur
Vunk = Volume sampel larutan limbah
Mencari nilai x: y = 0.1315 + 0.6197x 0 = 0.1315 + 0.6197x x = 0 – 0.1315 0.6197 = -0.212 Mencari nilai C0: C0 = - (- 0.212) x 25.00 ml 12.50 ml = 0.42 ppm
Lampiran 15 Hasil pengukuran konsentrasi krom heksavalen dan krom total dengan metode AAS Certificate No : LT-405-1055
Sample Id : Textile Wastewater
Parameter Result Unit Analysis Method Total Chromium, Cr Hexavalent Chromium, Cr6+ <0.01 <0.01 ppm ppm SMEWW 21th (2005): 3111B SMEWW 21th (2005): 3500-Cr. B Konsentrasi standar (ppm) Serapan
0.0 0.1 0.2 0.3 0.4 0.5 0.75 0.012 0.109 0.199 0.299 0.413 0.495 0.695
24
Lampiran 16 Perhitungan kemiringan kurva standar dan kurva penambahan standar limbah akhir tekstil
Kurva standar Limbah Akhir
Konsentrasi (ppm) Serapan 0.00 0.10 0.20 0.30 0.40 0.50 0.75 0.000 0.101 0.167 0.223 0.361 0.474 0.674 Slope (kemiringan kurva) = Δ Serapan Δ Konsentrasi = 0.674 – 0.101 0.75 – 0.1 = 0.88
Slope (kemiringan kurva) = Δ Serapan Δ Konsentrasi = 0.695 – 0.109 0.75 – 0.1 = 0.90
Lampiran 17 Pengukuran konsentrasi krom heksavalen limbah akhir tekstil dengan metode penambahan standar
Konsentrasi standar (ppm) Serapan Konsentrasi (ppm) 0.10 0.20 0.30 0.40 0.50 0.75 0.109 0.199 0.299 0.413 0.495 0.695 0.02 0.03 0.04 0.07 0.06 0.04 Rerata = 0.04 Contoh perhitungan: AT = Astd + Ac = Cstd Єstd + Cc Єc ; AT = Serapan total Astd = Serapan standar Ac = Serapan sampel Cstd = Konsentrasi standar Cc = Konsentrasi sampel
Єstd = Absorbtivitas molar standar (slope kurva standar)
Єc = Absorbtivitas molar sampel (slope kurva penambahan standar)
Cc = AT - Cstd Єstd Єc
= 0.109 – 0.02(0.88) 0.90 = 0.02 ppm
Lampiran 18 Pengukuran serapan larutan limbah tekstil setelah direaksikan dengan serbuk besi
Jenis Limbah Serapan
Ulangan 1 Ulangan 2 Rerata Limbah proses pewarnaan tekstil
Limbah akhir tekstil
0.000 0.000 0.004 0.000 0.002 0.000 Konsentrasi standar (ppm) Serapan
0.00 0.10 0.20 0.30 0.40 0.50 0.75 0.012 0.109 0.199 0.299 0.413 0.495 0.695