i
EFEK NEFROPROTEKTIF PEMBERIAN JANGKA PANJANG EKSTRAK METANOL-AIR BIJI Persea americana Mill. TERHADAP
KADAR KREATININ DAN GAMBARAN HISTOLOGIS GINJAL PADA TIKUS TERINDUKSI KARBON TETRAKLORIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
PRISCILLA DIANA VIVI VIONITA
108114043
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Segala Perkara dapat Kutanggung di dalam Dia yang Memberi
Kekuatan kepadaku (Filipi 4:13)
“Our greatest weakness lies in giving up. The most certain
way to succeed is always to try just one more time (Thomas
A. Edison). You are never too old to set another goal or to
dream a new dream (C. S. Lewis). Remember, that the future
belongs to those who believe of beauty their dreams (Elamor Roosvelt)”
The Show Must Go On
Kupersembahkan karya ini untuk
Tuhan Yesus Kristus dan Bunda Maria sumber kekuatanku..
Bapak, Mami, dan Mas Adip yang selalu memberiku kasih sayang,
semangat dan motivasi..
vii PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala
perlindungan dan berkat yang telah diberikan sehingga skripsi berjudul “Efek
Nefroprotektif Pemberian Jangka Panjang Ekstrak Metanol-Air Biji Persea
Americana Mill. terhadap Kadar Kreatinin dan Gambaran Histologis Ginjal pada
Tikus Terinduksi Karbon Tetraklorida” yang disusun untuk memenuhi
persyaratan memperoleh gelar Sarjana Strata Satu Program Studi Farmasi (S.
Farm.) dapat dikerjakan dengan baik dan lancar.
Penulis menyadari bahwa penulisan skripsin ini tidak terlepas dari
berbagai pihak. Kesempatan ini penulis pergunakan untuk mengungkapkan rasa
terimaksih kepada :
1. Dekan Fakultas Farmasi Universitas Sanata Dharma yang telah mengijinkan
penulis menjalankan pembelajaran selama masa studi.
2. Ibu Phebe Hendra, M. Si., Ph. D., Apt. selaku Dosen Pembimbing Skripsi yang
telah membimbing, selalu mendampingi, dan memberikan saran selama
penyusunan skripsi.
3. dr.Fenty, M.Kes., Sp.PK., selaku Dosen Penguji yang telah memberikan kritik
dan saran selama penyusunan skripsi.
4. Prof. Dr. C.J. Soegihardjo, Apt. selaku Dosen Penguji yang telah memberikan
kritik dan saran selama penyusunan skripsi.
5. Ibu Rini Dwiastuti, M.Si., Apt. selaku Kepala Penanggungjawab Laboratorium
Fakultas Farmasi yang telah memberikan ijin dalam penggunaan fasilitas
viii
6. Bapak Yohanes Dwiatmaka, M.Si. yang telah menyediakan waktu untuk
memberikan bantuan dalam determinasi tanaman Persea americana Mill.
7. Pak Kayat, Pak Heru, Pak Parjiman, Pak Wagiran, Pak Parlan, Pak Kunto, dan
Pak Bimo selaku laboran laboratorium Fakultas Farmasi yang telah membantu
penulis dalam proses pelaksanaan penelitian di laboratorium.
8. Keluargaku tercinta Mbah Tri, Mbah Sobrah, Rm. Karnan, Mbak Lina, Markus
Y.P., Mas Yocep, Mario yang selalu memberi motivasi, perhatian dan doa
demi kelancaran studi dan penyusunan naskah skripsi.
9. Teman-teman seperjuangan alpukat Angelia Rosari, Rotua Winata S., Inneke
Devi Permatasari, Komang Ayu N., Ni Luh Putu Dian P.P., Lydia Setiawan,
Gidion K. Y., Irene, Ike Kumalasari A., Yuditha A. Q., Adrienne R. A., dan
tentunya tim go go metanol (Liana R. G., Robert D. P., M. M. Sasadara V.)
atas segala kerjasama, bantuan dan semangat yang selalu bergelora dalam
penyusunan skripsi ini dari awal hingga akhir.
10. Teman, sahabat sekaligus keluargaku, Angelia Rosari, Agustinus Hendy
Larsen, Denny Krisandi, Priscilla Novelia Sari, Gabriela Indria P., Cece Fretty,
atas kebersamaan, kekeluargaan, keceriaan, suka duka, semangat dan motivasi
yang diberikan.
11. Teman-temanku Wisma Ananda, Arellia Oktaviori, Eva Christiana, Priskila
Agnes S., Heni Ariyanti (Kak Bohen), Mbak Ndit, Indah, Maria, Brigitta
Rosalia, dan Eva Ekayanti atas keceriaan, suka duka, kebersamaan,
kekeluargaan, semangat dan motivasi, serta saran yang diberikan, terutama
ix
12. Teman-teman praktikum, Adrienne R. A., Therezita S. L., Inggrid R. T.,
Angelina Pangala, Pande P. Krishna W., Tirzayana A. T., dan Catharina A. atas
bantuan, kerjasama dan motivasi yang diberikan.
13. Teman-teman FKK-A 2010 dan seluruh angkatan 2010, serta seluruh teman
baik di Fakultas Farmasi maupun teman-teman lain, terima kasih atas
kebersamaan yang kita bangun.
14. Semua pihak yang tidak dapat penulis sebutkan satu per satu sehingga penulis
dapat menyelesaikan tugas akhir ini dengan baik.
Penulis menyadari bahwa tugas akhir ini belum sempurna dan masih
banyak kekurangan sehingga penulis berharap kritik dan saran dari semua
pihak. Akhir kata, penulis berharap semoga tugas akhir ini dapat bermanfaat
bagi semua pihak terutama di bidang ilmu Farmasi.
x
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN PENULIS ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ... xviii
INTISARI ... xx
ABSTRACT ... xxi
BAB I PENGANTAR ... 1
A.Latar Belakang ... 1
1. Perumusan Masalah ... 4
2. Keaslian Penelitian ... 4
3. Manfaat Penelitian ... 5
B.Tujuan Penelitian ... 6
1. Tujuan Umum ... 6
xi
BAB II PENELAAHAN PUSTAKA ... 7
A.Ginjal ... 7
1. Anatomi Ginjal ... 7
2. Fisiologi Ginjal ... 15
B.Kerusakan ginjal ... 17
C.Kreatinin ... 19
1. Metabolisme Kreatinin ... 19
2. Metode Pemeriksaan Kreatinin ... 21
D.Nefrotoksisitas ... 21
1. Faktor Penyebab Nefrotoksisitas ... 21
2. Nefrotoksikan ... 23
E. Karbon Tetraklorida ... 23
F. Antioksidan ... 26
G.Ekstraksi ... 26
H.Persea americana Mill. ... 27
1. Taksonomi ... 27
2. Sinonim ... 28
3. Nama Lain ... 28
4. Morfologi ... 28
5. Kandungan Kimia ... 29
6. Khasiat dan Kegunaan ... 29
I. Landasan Teori ... 30
xii
BAB III METODE PENELITIAN... 32
A.Jenis dan Rancangan Penelitian ... 32
B.Variabel Penelitian dan Definisi Operasional ... 32
1. Variabel Utama ... 32
2. Variabel Pengacau ... 32
3. Definisi Operasional ... 33
C.Bahan Penelitian ... 34
1. Bahan Utama ... 34
2. Bahan Kimia ... 34
D.Alat atau Instrument Penelitian ... 35
1. Alat Ekstraksi ... 35
2. Alat Uji Nefroprotektif ... 35
E. Tata Cara Penelitian ... 36
1. Determinasi Serbuk Biji P. americana ... 36
2. Pengumpulan Bahan ... 36
3. Pembuatan Serbuk ... 36
4. Penetapan Kadar Air Serbuk Biji Persea americana Mill. ... 36
5. Pembuatan Pelarut Metanol-Air (70:30) ... 37
6. Pembuatan Ekstrak Metanol-Air Biji P. americana ... 37
7. Penetapan Konsentrasi Pekat Ekstrak ... 38
8. Penetapan Dosis Ekstrak Metanol-Air Biji P. americana ... 38
9. Pembuatan Larutan Karbon Tetraklorida ... 39
xiii
11.Uji Pendahuluan ... 39
12.Pengelompokan dan Perlakuan Hewan Uji ... 40
13.Pembuatan Serum ... 41
14.Penetapan Aktivitas Serum Kontrol Serum Kreatinin ... 41
15.Pembuatan Larutan Formalin 10% ... 42
16.Pencuplikan Organ Ginjal Tikus untuk Pengamatan Gambaran Histologis ... 42
17.Pembuatan Preparat Histologi Ginjal ... 43
F. Tata Cara Analisis Hasil ... 43
BAB IV HASIL DAN PEMBAHASAN ... 45
A.Penyiapan Bahan ... 45
1. Hasil Determinasi Serbuk Biji P. americana ... 45
2. Penetapan Kadar Air Serbuk Biji P. americana ... 46
3. Hasil Penimbangan Bobot Ekstrak Metanol-Air Biji P. americana ... 46
B.Uji Pendahuluan ... 47
1. Penentuan Dosis Nefrotoksik Karbon Tetraklorida ... 47
2. Penentuan Waktu Pencuplikan Darah ... 47
3. Penetapan Lama Pemejanan Ekstrak Metanol-Air Biji P. americana ... 50
4. Penetapan Dosis Ekstrak Metanol-Air Biji P. americana ... 50
C.Hasil Uji Efek Nefroprotektif Ekstrak Metanol-Air Biji P. americana ... 51
1. Kontrol Negatif Olive Oil 2 ml/kgBB ... 53
2. Kontrol Nefrotoksin Karbon Tetraklorida Dosis 2 ml/kgBB ... 55
xiv
4. Kelompok Perlakuan Ekstrak Metanol-Air Biji P. americana Dosis
0,35 g/kgBB, 0,7 g/kgBB, dan 1,4 g/kgBB pada Tikus Jantan Galur
Wistar Terinduksi Karbon Tetraklorida Dosis 2 ml/kgBB ... 57
5. Pemeriksaan Histologis Ginjal ... 59
a. Kontrol Nefrotoksin CCl4 2 ml/kgBB ... 60
b. Kontrol Negatif Olive Oil 2 ml/kgBB ... 61
c. Kontrol Ekstrak Metanol-Air Biji P. americana dosis 1,4 g/kgBB ... 63
d. Perlakuan Ekstrak Metanol-Air Biji P. americana dosis 0,35 dan 0,7 g/kgBB ... 65
e. Perlakuan Ekstrak Metanol-Air Biji P. americana dosis 1,4 g /kgBB ... 65
D.Rangkuman Pembahasan ... 66
BAB V KESIMPULAN DAN SARAN ... 69
A.Kesimpulan ... 69
B.Saran ... 69
DAFTAR PUSTAKA ... 70
LAMPIRAN ... 75
xv DAFTAR TABEL
Tabel I Kadar Normal Kreatinin Beberapa Jenis Hewan ... 20
Tabel II Beberapa Toksikan yang Menyebabkan Kerusakan pada Bagian-Bagian Nefron ... 23
Tabel III Rata-rata Kadar Serum Kreatinin Tikus Setelah Pemberian Karbon Tetraklorida Dosis 2 ml/kgBB pada Selang Waktu 0, 24, 48, dan 72 jam (n=5) ... 48
Tabel IV Hasil Uji Scheffe Terhadap Kadar Serum Kreatinin Tikus Setelah Pemberian Karbon Tetraklorida Dosis 2 ml/kgBB pada Selang Waktu 0, 24, 48, dan 72 jam (n=5) ... 49
Tabel V Purata ± SE Kadar Serum Kreatinin Praperlakuan Ekstrak Metanol-Air Biji P. americana Terinduksi Karbon Tetraklorida Dosis 2 ml/kgBB (n=5) ... 52
Tabel VI Hasil Uji Scheffe Kadar Serum Kreatinin Setelah Pemberian Karbon Tetraklorida Dosis 2 ml/kgBB pada Kelompok Perlakuan ... 53
Tabel VII Rata-Rata Kadar Serum Kreatinin Tikus Setelah Pemberian Olive Oil Dosis 2 ml/kgBB pada Selang Waktu 0 dan 48 ... 54
Tabel VIII Hasil Uji T-Paired Kadar Serum Kreatinin Setelah Pemberian Olive Oil Dosis 2 ml/kgBB pada Selang Waktu 0 dan 48 ... 55
Tabel IX Hasil Pemerikasaan Gambaran Histologis Ginjal Tikus ... 60
Tabel X Hasil Rendemen Ekstrak Metanol-Air Biji P. americana ... 95
xvi DAFTAR GAMBAR
Gambar 1 Struktur Ginjal ... 8
Gambar 2 Struktur Nefron ... 9
Gambar 3 Struktur Glomerulus dan Kapiler Glomerular ... 10
Gambar 4 Korpuskular Ginjal secara Mikroskopik ... 11
Gambar 5 Tubulus Kontortus Proksimal dan Tubulus Kontortus Distal secara Mikroskopik ... 13
Gambar 6 Duktus Koligens secara Mikroskopik ... 13
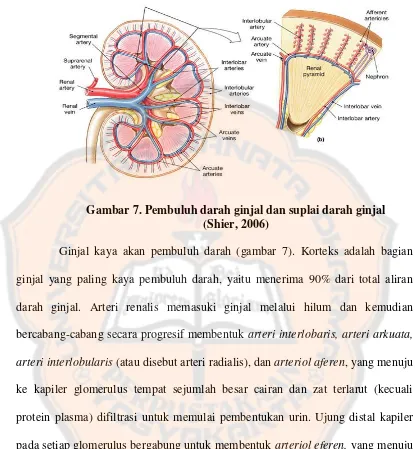
Gambar 7 Pembuluh Darah Ginjal dan Suplai Darah Ginjal ... 14
Gambar 8 Mekanisme Pembentukan Urin Melalui Proses Filtrasi, Reabsorbsi, dan Sekresi ... 16
Gambar 9 Gambaran Mikroskopik Ginjal Normal ... 18
Gambar 10 Struktur Molekul Karbon Tetraklorida ... 23
Gambar 11 Mekanisme Biotransformasi dan Oksidasi Karbon Tetraklorida ... 25
Gambar 12 Diagram Batang Rata-Rata Kadar Serum Kreatinin Tikus Setelah Pemberian Karbon Tetraklorida Dosis 2 ml/kgBB pada Selang Waktu 0, 24, 49, dan 72 jam ... 48
xvii
Gambar 14 Diagram Batang Rata-Rata Aktivitas Serum Kreatinin
Setelah Pemberian Olive Oil Dosis 2 ml/kgBB pada Selang
Waktu 0 dan 48 ... 54
Gambar 15 Fotomikroskopik Ginjal Tikus Normal ... 60
Gambar 16 Fotomikroskopik DHET Ginjal Tikus ... 61
Gambar 17 Fotomikroskopik ITC Ginjal Tikus ... 62
Gambar 18 Fotomikroskopik Nefritis Interstitialis Ginjal Tikus ... 63
Gambar 19 Fotomikroskopik Perivaskulitis Ginjal Tikus ... 64
Gambar 20 Fotomikroskopik Intratubular Hialin Cast ... 65
xviii DAFTAR LAMPIRAN
Lampiran 1 Foto Biji dan Serbuk Biji P. Americana ... 76
Lampiran 2 Foto Ekstrak Metanol-Air Kental Biji P. americana ... 76
Lampiran 3 Foto Larutan Ekstrak Metanol-Air Biji P. americana ... 76
Lampiran 4 Surat Pengesahan Determinasi Serbuk Biji P. americana ... 77
Lampiran 5 Hasil determinasi serbuk biji P. americana ... 78 Lampiran 6 Surat Pengesahan Medical and Health Research Ethics Commitee (MHREC) ... 80
Lampiran 7 Analisis Statistik Kadar Serum Kreatinin pada Uji Penentuan Waktu Pencuplikan Darah Tikus Terinduksi Karbon Tetraklorida Dosis 2 ml/kg BB ... 81
Lampiran 8 Analisis Statistik Kadar Serum Kreatinin 6 Kelompok Perlakuan Ekstrak Metanol-Air Biji P. americana setelah Terinduksi Kabon Tetraklorida 2 ml/kg BB ... 84
Lampiran 9 Analisis Statistik Kadar Kreatinin Serum pada Perlakuan Kontrol Negatif Olive Oil Dosis 2 mL/kgBB ... 89
Lampiran 10 Perhitungan Efek Nefroprotektif (%) ... 91
Lampiran 11 Perhitungan Penetapan Peringkat Dosis Ekstrak Metanol-Air Biji P.americana Kelompok Perlakuan ... 92
Lampiran 12 Perhitungan Konversi Dosis untuk Manusia ... 92
Lampiran 13 Penetapan Kadar Air Serbuk ... 93
xix
Lampiran 15 Bobot Pengeringan Ekstrak Metanol-Air Biji P.
americana ... 95
Lampiran 16 Hasil Pengukuran Validitas dan Reabilitas Serum Kontrol
Kreatinin ... 96
xx INTISARI
Penelitian ini bertujuan untuk mendapatkan informasi mengenai pengaruh nefroprotektif dan dosis efektif pemberian jangka panjang ekstrak metanol-air biji Persea americana Mill. terhadap penurunan kadar serum kreatinin dan gambaran histologis ginjal tikus terinduksi karbon tetraklorida.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Metode yang dilakukan adalah pengukuran kadar kreatinin serum pada jam ke-48 setelah pemberian karbon tetraklorida sebagai nefrotoksin. Sebanyak 30 ekor tikus jantan galur Wistar, umur 2-3 bulan, dan berat ± 150-250 gram dibagi secara acak ke dalam enam kelompok perlakuan. Kelompok I (kontrol nefrotoksin) diberi karbon tetraklorida dengan dosis 2 ml/kg BB secara i.p, kelompok II (kontrol negatif) diberi olive oil dosis 2 ml/kg BB secara i.p, kelompok III (kontrol ekstrak) diberi ekstrak metanol-air biji Persea americana Mill., kelompok IV-VI (perlakuan) masing-masing diberi ekstrak metanol-air biji Persea americana Mill. dengan tiga peringkat dosis, yaitu masing-masing 0,35; 0,7; 1,4 g/kgBB secara oral sekali sehari selama enam hari berturut-turut, kemudian pada hari ke tujuh semua perlakuan diberi karbon tetraklorida dosis 2 ml/kg BB secara i.p. Pada jam ke-48 sesudahnya, darah diambil dari sinus orbitalis mata untuk penetapan kadar serum kreatinin dan data dihitung menggunakan ANOVA.
Berdasarkan penelitian ini, ekstrak metanol-air biji Persea americana
Mill. memberikan efek nefroprotektif yang ditunjukkan dengan adanya penurunan kadar serum kreatinin pada tikus Wistar terinduksi karbon tetraklorida. Efek nefroprotektif dari ekstrak metanol-air Persea americana Mill. dosis 0,35; 0,7; and 1,4 g/kg BB berturut-turut adalah 123,81%, 104,76%, dan 80,95%. Gambaran histologis organ ginjal kelompok IV-VI menunjukkan tidak ada perubahan patologi spesifik.
xxi ABSTRACT
This present research aims to get information about nephroprotective effect of water-methanol extract Persea. americana Mill. seed for reducing creatinine serum level and kidney histology preview in rats induced by carbon tetrachloride and get an effective dose.
This research was done with direct sampling design. This experiment used Wistar male rats, at the age of 2-3 months, and weight ± 150-250 g. The rats were devided into six treatment groups. The first group (nephrotoxin control) was given carbon tetrachloride 2 ml/kgBW i.p. Then, the second group (negative control) was given olive oil 2 ml/kg BW. The third group (extract control) was given water-methanol extract of to P. americana seed at the dose of 1.4 g/kg BW. Fourth until six groups were given methanol-water extract of Persea americana
Mill. seed at the dose of 0.35; 0.7; and 1.4 g/kg BW orally once a day for six days successively and then in the seventh day all of the teatment group were given carbon tetrachloride 2 ml/kgBW by i.p. Fourty-eight hours later, blood was collected from the orbital sinus eye to be measured creatinine serum level. Then it was analyzed statistically.
Based on the result of this research, water-methanol extract P. ameriana
Mill. seed give nephroprotective effects for reducing of creatinine serum level in rats induced by carbon tetrachloride. There was a relation between dose and response which was seen from the more over the biggest dose, response of reducing of creatinine serum level was decrease. Nephroprotective effect with dose of 0,35; 0,7; and 1,4 g/kgBW successively were 123.81%, 104.76%, and 80.95%. Kidney histology preview in the grup IV-VI show there were no alterationin spesific patology. This study showed that extract water-methanol had nephroprotective effect.
1 BAB I PENGANTAR A. Latar Belakang
Ginjal merupakan organ yang bekerja untuk menyaring darah sebanyak
kurang lebih 200 liter tiap harinya dan juga membuang sisa-sisa metabolisme
serta kelebihan cairan tubuh melalui urine. Selain membuang sisa-sisa
metabolisme tubuh melalui urine, ginjal juga berfungsi dalam melakukan kontrol
terhadap sekresi hormon-hormon aldosteron dan Anti Diuretic Hormone (ADH),
mengatur metabolisme ion kalsium dan vitamin D, serta menghasilkan hormon,
antara lain eritropoetin yang berperan dalam pembentukan sel darah merah, renin
yang berperan dalam mengatur tekanan darah, kalsitriol atau vitamin D3 dan
hormon prostaglandin (Rasjidi, 2008).
Penyakit ginjal kronik (CKD) adalah masalah kesehatan yang terjadi di
seluruh dunia. Menurut laporan WHO tahun 2002 dan Global Burden Disease
(GDB), penyakit ginjal dan saluran kemih berkontribusi dalam penyakit global
dengan angka kematian 850.000 jiwa setiap tahunnya dan 15.010.167 jiwa
mengalami kecacatan (Schieppati, Giuseppe, 2005). Selain itu, di Amerika insiden
dan prevalensi penyakit ginjal mengalami peningkatan beberapa tahun terakhir.
Sekitar 20 juta penduduk Amerika dari tahun 1988 hingga 1994 atau sekitar 11%
dari penduduk mengidap penyakit ginjal kronis (fase 1-5) (Robinson, 2006).
Jumlah insidensi dan prevalensi gagal ginjal kronik terminal di Indonesia
belum diketahui secara pasti. Besarnya insidensi gagal ginjal kronik terminal di
Besarnya prevalensi gagal ginjal kronik terminal di Indonesia diperkirkan
sebesar 200 – 250 orang tiap 1 juta penduduk pertahun (Bakri, 2005). Berdasarkan
tingginya prevalensi penyakit ginjal perlu dilakukan penelitian terhadap sumber
daya hayati sebagai alternatif obat baru.
Adanya gangguan pada organ ginjal dapat menyebabkan terjadinya
penumpukan air dan toksin dalam tubuh sehingga berpengaruh pada homeostatis
tubuh (Robbin dan Cotran, 2007). Salah satu penanda adanya kerusakan ginjal
adalah tingginya kadar kreatinin. Kadar kreatinin, yaitu suatu bahan sisa
metabolisme sel otot yang beredar dalam darah. Kreatinin diekskresikan
seluruhnya dalam urin melalui filtrasi glomerulus. Ketika terjadi penurunan
kecepatan filtrasi glomerulus, kadar kreatinin akan meningkat berbanding terbalik
dengan kecepatan ekskresi (Huether, McCance, Brashers, dan Rote, 2008). Oleh
karena itu, kreatinin juga bisa digunakan untuk mengukur kemampuan fungsi
ginjal (Rasjidi, 2008).
Alpukat (Persea americana Mill.) merupakan jenis tanaman yang dikenal
berfungsi mengobati hipertensi (Anaka, Raymond, dan Stephen, 2009). Pada
penelitian Marlinda, Meiske, Audy (2012), menyebutkan bahwa kandungan
metabolit sekunder yang terdapat dalam biji Persea americana Mill. (P.
americana) meliputi alkaloid, triterpenoid, tanin, flavonoid, saponin, dan
memiliki aktivitas terhadap penghambatan radikal DPPH. Kandungan flavonoid
pada P. americana bersifat larut air dan merupakan antioksidan yang sangat kuat.
perlindungan dan anti kanker yang kuat dalam melawan tahap-tahap
karsinogenesis (Arukwe, Amadi, Duru, Agomuo, Adindu,Odika, Lele, 2012).
Karbon tetraklorida yang digunakan sebagai senyawa model dapat
menyebabkan stres oksidatif pada beberapa fungsi fisiologis hewan uji. Karbon
tetraklorida ini bersifat hepatotoksik dan nefrotoksik. Di dalam tubuh akan
dimetabolisme oleh enzim sitokrom P450 membentuk triklorometil (
•
CCl3) dantriklorometilperoksida (
•
OOCCl3) yang bersifat lebih reaktif. Radikal bebas yangdihasilkan dapat menginduksi kerusakan dan disfungsi DNA dan protein sehingga
menyebabkan peroksidase lipid pada ginjal (Makni, Chtourou, Garoui,
Boudawara, dan Fetoui (2011). Terbentuknya ikatan kovalen antara radikal bebas
dengan lemak mikrosomal dan protein membran menyebabkan kerusakan pada
tubulus proksimal ginjal dan perubahan pada beberapa granular pneumosit
(Ramarajan, Somasundaram, Subramanian, Pandian, 2012).
Penelitian ini dilakukan dengan penentuan dosis dan pemberian jangka
panjang ekstrak metanol biji P. americana. Penggunaan larutan penyari ekstrak
didasarkan pada penelitian yang dilakukan oleh Carpena, Morcuende, Andradre,
Kylli, Ertevez (2011), bahwa biji P. americana yang memiliki kandungan
antioksidan flavonoid diekstraksi menggunakan pelarut metanol. Adanya
antioksidan dari biji P. americana dapat menangkap radikal bebas dari karbon
tetraklorida sehingga mengurangi kerusakan pada tubulus proksimal ginjal.
Eksplorasi biji P. americana di Indonesia masih belum banyak dilakukan,
membuktikan efek nefroprotektif ekstrak metanol P. americana pada tikus
terinduksi karbon tetraklorida perlu dilakukan.
1. Perumusan masalah
Berdasarkan latar belakang penelitian di atas, dapat dirumuskan
permasalahan sebagai berikut:
1. Apakah pemberian jangka panjang ekstrak metanol-air biji P. americana
mempunyai pengaruh nefroprotektif terhadap kadar kreatinin dan gambaran histologis organ ginjal tikus jantan galur Wistar terinduksi karbon tetraklorida ? 2. Berapa besar dosis efektif nefroprotektif ekstrak metanol-air biji P. americana
pada tikus jantan galur Wistar terinduksi karbon tetraklorida ?
2. Keaslian penelitian
Sejauh penelusuran pustaka yang dilakukan oleh peneliti, penelitian biji buah P. americana pernah dilakukan oleh Marlinda, dkk. (2012), yang melaporkan kandungan metabolit sekunder biji P. americana meliputi alkaloid, triterpenoid, tanin, flavonoid, dan saponin. Penelitian Malangi, dkk (2012) menunjukkan
adanya kandungan tanin yang diisolasi dari ekstrak etanol P. americana memiliki
aktivitas penangkapan radikal bebas terhadap DPPH. Penelitian Anaka, dkk.
(2009) melaporkan bahwa ekstrak biji P. americana mempunyai khasiat
mengobati hipertensi pada tikus Sprague-Dawley. Pada penelitian Ramos,
Moreno, Cevallos, Navarro, Siciliano, Modragon, Ortega, 2012, menyebutkan
bahwa ekstrak biji P. americana mampu menurunkan kadar kolesterol pada model
tikus hiperkolesterolemia. Selain itu, P. americana juga mempunyai aktivitas
antimikroba (Idris, Ndukwe, Gimba, 2009). Penelitian yang dilakukan oleh
bahwa ekstrak metanol pada kulit dan biji P. americana memilki kadar fenolik
yang tinggi dan mempunyai aktivitas antioksidan. Selain itu pada ekstrak metanol,
etil asetat, dan aseton dari kulit dan biji P. americana mempunyai aktivitas
antioksidan terhadapradikal CUPRAC, DPPH, dan ABTS (Carpena, dkk., 2011).
Sepanjang penelusuran pustaka yang dilakukan oleh peneliti, penelitian
terkait dengan pengaruh nefroprotektif ekstrak metanol biji P. americana terhadap
penurunan kadar serum kreatinin pada tikus jantan galur Wistar terinduksi karbon
tetraklorida belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat teoritis
Penelitian ini diharapkan dapat memberikan sumbangan ilmu pengetahuan
mengenai pengaruh pemberian jangka panjang ekstrak metanol-air biji P.
americana terhadap parameter kadar kreatinin dan gambaran histologis
organ ginjal tikus yang terinduksi karbon tetraklorida.
b. Manfaat praktis
Penelitian ini dapat dijadikan bahan pertimbangan masyarakat untuk
menggunakan biji P. americana dengan dosis yang diperoleh dalam
B. Tujuan Penelitian 1. Tujuan umum
Penelitian ini bertujuan untuk membuktikan adanya pengaruh
nefroprotektif pemberian jangka panjang ekstrak metanol-air biji P. americana
pada tikus jantan galur Wistar terinduksi karbon tetraklorida.
2. Tujuan khusus
Penelitian ini bertujuan untuk mengetahui dosis efektif pemberian jangka
panjang ekstrak metanol-air biji P. americana sebagai nefroprotektif pada tikus
7 BAB II
PENELAAHAN PUSTAKA
A. Ginjal
Ginjal adalah sepasang organ yang terletak di area retroperitoneum
(McPhee dan Ganong, 2010). Struktur anatomi dan fisiologi ginjal adalah sebagai
berikut :
1. Anatomi ginjal
Ginjal merupakan organ berbentuk seperti kacang, yang panjangnya
sekitar 11 cm lebar 6 cm, tebal 3 cm, serta beratnya 150 gram atau seukuran
kepalan tangan. Ginjal melekat pada posisinya karena berikatan dengan suatu
massa lemak. Selubung fasia renal fibroelastik membungkus ginjal dan lemak
ginjal (Ross dan Wilson, 2011).
Setiap ginjal dilindungi dan distabilkan oleh 3 lapisan yang berupa
jaringan ikat, antara lain :
a. Kapsul fibrosa, lapisan serat kolagen yang menutupi permukaan luar dari
seluruh organ.
b. Kapsul lemak perineal, lapisan tebal dari jaringan adiposa (jaringan lemak)
yang menyelimuti kapsul fibrosa.
c. Fasia ginjal, suatu lapisan luar fibrosa yang padat yang mengikat ginjal dengan
struktur di sekitarnya. Serat kolagen mengembang keluar dari kapsul fibrosa
Secara histologis ginjal terdiri dari unsur utama yaitu glomerulus, tubulus dan
interstitium, dan pembuluh darah (Kumar, Abbas, dan Fausto, 2010).
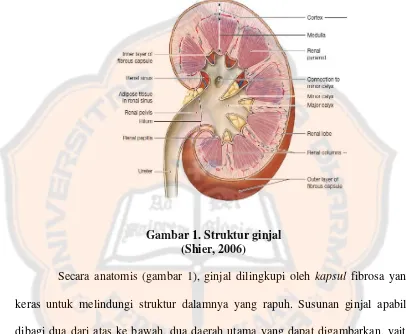
Gambar 1. Struktur ginjal (Shier, 2006)
Secara anatomis (gambar 1), ginjal dilingkupi oleh kapsul fibrosa yang
keras untuk melindungi struktur dalamnya yang rapuh. Susunan ginjal apabila
dibagi dua dari atas ke bawah, dua daerah utama yang dapat digambarkan, yaitu
korteks (bagian luar) dan medula (bagian dalam) (Guyton dan Hall, 2006).
Medula ginjal terbagi menjadi beberapa massa jaringan membentuk kerucut yang
disebut piramida ginjal. Dasar dari setiap piramida masing-masing dimulai pada
perbatasan antara korteks dan medula dan berakhir di papilla. Papilla menonjol
ke dalam ruang dari pelvis ginjal, yaitu sambungan dari ujung ureter bagian atas
yang berbentuk corong. Batas luar pelvis terbagi menjadi kantong-kantong dengan
ujung terbuka yang disebut kalises mayor, yang meluas ke bawah dan terbagi
Dinding kalises, pelvis, dan ureter terdiri dari elemen-elemen kontraktil yang
mendorong urin maju menuju kandung kemih, tempat urin disimpan sampai
dikeluarkan melalui mikturisi (Guyton dan Hall, 2006).
Setiap ginjal terdiri dari sekitar 1 juta unit fungsional mikroskopis yang
dikenal sebagai nefron, yang terikat bersama oleh jaringan ikat (Sherwood, 2009).
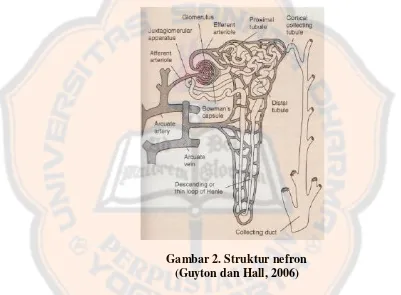
Gambar 2. Struktur nefron (Guyton dan Hall, 2006)
Setiap nefron terdiri dari tiga bagian utama, yaitu glomerulus, kapsula
bowman, dan dua buah tubulus panjang. Tubulus tersebut dibagi menjadi tubulus
kontortus proksimal, ansa henle dan tubulus kontortus distal, dan yang terakhir
adalah tubulus pengumpul (gambar 2) (Guyton dan Hall, 2006).
Bagian dari nefron akan dijelaskan masing-masing, yaitu sebagai berikut:
a.Korpuskular ginjal. Korpuskular ginjal terdiri dari seberkas kapiler yang
disebut glomerulus dan dikelilingi oleh kapsul glomerular (bowman) (gambar
terdapat di sepanjang arteriol. Glomerulus berfungsi untuk filtrasi air dan zat
terlarut dalam darah. Sedangkan kapsula bowman merupakan suatu pelebaran
nefron yang dibatasi oleh epitel yang menyelubungi glomerulus untuk
mengumpulkan zat terlarut yang difiltrasi oleh glomerulus (Sherwood, 2006).
Gambar 3. Struktur Glomerulus dan kapiler glomerular (Huether dan McCance, 2008)
Glomerulus terdiri dari jaringan anastomosis kapiler yang dibatasi oleh
endotel berpori, dan dibungkus oleh dua lapisan epitel, yang membentuk suatu
lapisan yang berhubungan dengan lapisan yang membentuk simpai Bowman
dan tubulus ginjal (Kumar, dkk., 2010; McPhee dan Ganong, 2010).
Lapisan epitel yang membungkus glomerulus yaitu epitel viseral dan
epitel parietal. Epitel viseral bergabung ke dalam dan menjadi bagian intrinsik
dinding kapiler, yang dipisahkan dari sel endotel oleh sebuah membran basal.
(urinary space), rongga tempat filtrat plasma berkumpul pertama kali (Kumar,
dkk., 2010). Lapisan parietal simpai glomerular terdiri atas selapis sel
skuamosa yang ditunjang lamina basal dan selapis tipis serat retikular di luar
(Mescher, 2011).
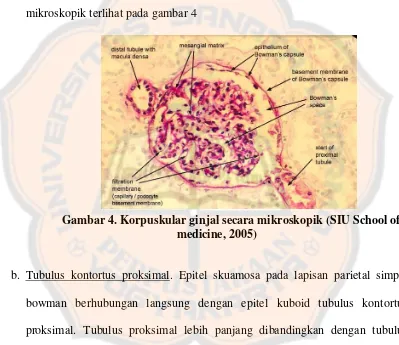
Dinding kapiler glomerulus terdiri dari struktur-struktur yang secara
mikroskopik terlihat pada gambar 4
Gambar 4. Korpuskular ginjal secara mikroskopik (SIU School of medicine, 2005)
b. Tubulus kontortus proksimal. Epitel skuamosa pada lapisan parietal simpai
bowman berhubungan langsung dengan epitel kuboid tubulus kontortus
proksimal. Tubulus proksimal lebih panjang dibandingkan dengan tubulus
distal sehingga lebih sering tampak pada potongan korteks ginjal. Sel tubulus
proksimal mereabsorbsi 60-65% air yang disaring dalam korpuskel ginjal,
beserta hampir semua nutrien, ion, vitamin, dan protein plasma kecil. Air dan
zat terlarutnya diangkut secara langsung melalui dinding tubulus dan segera
Sel-sel tubulus proksimal memiliki sitoplasma asidofilik karena adanya
mitokondria. Bagian apeks sel memiliki banyak mikrovili panjang yang
membentuk suatu brush border untuk reabsorbsi. Pada sediaan histologis,
brush border dapat tidak teratur dan lumennya tampak terisi serabut (Mescher,
2011).
Sel epitel tubulus sangat peka terhadap anoksia dan rentan terhadap
toksin. Beberapa faktor yang menyebabkan tubulus mudah mengalami
ketoksikan, yaitu termasuk permukaan luas bermuatan listrik untuk reabsorbsi
tubulus, sistem transpor aktif ion dan asam organik, dan kemampuan
melakukan pemekatan secara efektif, selain itu kadar sitokrom P450 yang
tinggi untuk mendetoksifikasi atau mengaktifkan toksikan (Robbins dan
Cotran, 2007).
c. Ansa henle. Tubulus kontortus proksimal berlanjut sebagai tubulus yang lebih
pendek dan memiliki segmen yang tipis yang membentuk lengkung tajam
berbentuk huruf U. Bagian pars desendens dari ansa henle terbentang dari
korteks ke bagian medula. Bagian pars asendens berjalan kembali dari medula
ke arah korteks ginjal. Segmen asendens dan desendens terdiri atas selapis sel
kuboid di dekat korteks (Mescher, 2011).
d. Tubulus distal. Tubulus kontortus distal lebih pendek dari tubulus proksimal.
Bagian tubulus distal ini berkelok-kelok di bagian korteks dan berakhir di
duktus koligens. Bagian awal tubulus distal yang lurus berkontak dengan kutub
vaskular di korpuskel ginjal dan membentuk apparatus juxtaglomerularis
kontortus proksimal karena lebih kecil dan tidak memiliki brush border.
(Sherwood, 2006;Mescher, 2011).
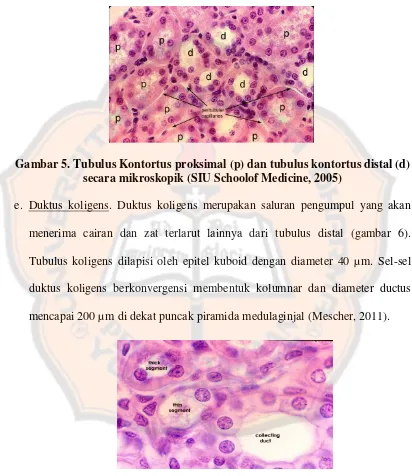
Gambar 5. Tubulus Kontortus proksimal (p) dan tubulus kontortus distal (d) secara mikroskopik (SIU Schoolof Medicine, 2005)
e. Duktus koligens. Duktus koligens merupakan saluran pengumpul yang akan
menerima cairan dan zat terlarut lainnya dari tubulus distal (gambar 6).
Tubulus koligens dilapisi oleh epitel kuboid dengan diameter 40 µm. Sel-sel
duktus koligens berkonvergensi membentuk kolumnar dan diameter ductus
mencapai 200 µm di dekat puncak piramida medulaginjal (Mescher, 2011).
Gambar 7. Pembuluh darah ginjal dan suplai darah ginjal (Shier, 2006)
Ginjal kaya akan pembuluh darah (gambar 7). Korteks adalah bagian
ginjal yang paling kaya pembuluh darah, yaitu menerima 90% dari total aliran
darah ginjal. Arteri renalis memasuki ginjal melalui hilum dan kemudian
bercabang-cabang secara progresif membentuk arteri interlobaris, arteri arkuata,
arteri interlobularis (atau disebut arteri radialis), dan arteriol aferen, yang menuju
ke kapiler glomerulus tempat sejumlah besar cairan dan zat terlarut (kecuali
protein plasma) difiltrasi untuk memulai pembentukan urin. Ujung distal kapiler
pada setiap glomerulus bergabung untuk membentuk arteriol eferen, yang menuju
jaringan kapiler kedua, yaitu kapiler peritubular, yang mengelilingi tubulus ginjal
(Guyton dan Hall, 2006).
Arteri ginjal merupakan cabang dari abdominal aorta yang masuk ke
ginjal, mentransportasi sebagian besar darah ke ginjal. Setiap ginjal memperoleh
20 - 25% dari total hasil pemompaan jantung. Secara normal, pada orang sehat,
Kapiler peritubulus mengosongkan isinya ke dalam pembuluh sistem
vena, yang berjalan secara paralel dengan pembuluh arteriol dan secara progresif
membentuk vena interlobularis, vena arkuata, vena interlobaris, dan vena
renalis, yang meninggalkan ginjal di samping arteri renalis dan ureter (Guyton
dan Hall, 2006). Vena ginjal kemudian bergabung dengan vena kava inferior yang
berada di rongga perut (Shier, 2006).
2. Fisiologi ginjal
Fungsi utama dari ginjal adalah untuk membersihkan tubuh dari
bahan-bahan sisa hasil pencernaan atau yang diproduksi oleh metabolisme, serta
mengontrol volume dan komposisi cairan tubuh. Ginjal melakukan fungsi penting
ini dengan cara menyaring plasma dan memisahkan zat dari filtrat dengan
kecepatan yang bervariasi, bergantung pada kebutuhan tubuh. Zat-zat yang tidak
diperlukan lagi dalam filtrat akan dibuang dengan cara mengekskresikannya ke
dalam urin, sedangkan zat yang dibutuhkan dikembalikan ke dalam darah
(Guyton dan Hall, 2006).
Fungsi lain dari ginjal selain untuk membuang produk buangan dari
sel-sel tubuh, mempunyai beberapa fungsi lain yang berperan dalam keseimbangan
esensial, antara lain:
a. Mengatur volume darah dan tekanan darah, yaitu dengan menyesuaikan
b. Mengatur konsentrasi plasma dari sodium, potasium, klorida, dan ion lainnya,
yaitu dengan mengatur jumlah yang diekskresikan ke urin dan mengontrol
level ion kalsium melalui sintesis kalsitriol.
c. Membantu menstabilkan pH darah, dengan mengontrol pengeluaran ion
hidrogen dan ion bikarbonat ke dalam urin.
d. Menjaga kestabilan nutrisi, dengan mencegah ekskresi berlebih pada urin
ketika mengekskresikan produk organik buangan, khususnya produk buangan
nitrogen, seperti urea dan asam urat (Martini,2009).
Gambar 8. Mekanisme pembentukan urin melalui proses filtrasi, reabsorbsi, dan sekresi
(Laboratorium AmerindBio-Clinic, 2010)
Langkah pertama dalam pembentukan urin adalah filtrasi glomerulus.
Dalam keadaan normal, 20% plasma yang masuk ke glomerulus disaring. Filtrat
yang sudah terbentuk akan dialirkan melalui tubulus, bahan-bahan yang
bermanfaat bagi tubuh dikembalikan ke plasma kapiler peritubulus. Perpindahan
ini disebut reabsorbsi tubulus. Bahan-bahan yang direabsorbsi tidak keluar dari
tubuh melalui urin tetapi dibawa oleh kapiler peritubulus ke sistem vena dan
kemudian ke jantung untuk diresirkulasi. Proses ginjal ketiga, sekresi tubulus,
merupakan pemindahan selektif bahan-bahan dari kapiler peritubulus ke dalam
lumen tubulus. Mekanisme ini untuk mengeluarkan bahan yang tidak terfiltrasi
dari kapiler peritubulus ke dalam lumen tubulus. Ekskresi urin adalah pengeluaran
bahan-bahan dari tubuh ke dalam urin. Semua konstituen plasma yang
disekresikan tetapi tidak direabsorbsi akan tetap di tubulus dan mengalir ke pelvis
ginjal untuk disekresikan sebagai urin (Sherwood, 2009). Urin yang dikeluarkan
mengandung air dengan ureum, kreatinin, fosfat dan sulfat hasil proses
katabolisme. Selain itu juga terdapat asam urat, K+, dan H+ hasil penukaran
dengan Na+ atas pengaruh aldosteron di tubulus distal. Protein dalam keadaan
normal diekskresi dalam jumlah sedikit. Glukosa yang difiltrasi akan direabsorpsi
di tubulus proksimal, tetapi dengan makin tinggi kadarnya dalam filtrat glomeruli
maka makin banyak pula glukosa yang dikeluarkan bersama urin (gambar 8)
(Laboratorium Amerind Bio-Clinic, 2010).
B. Kerusakan Ginjal
Fungsi utama ginjal adalah organ eliminasi yang penting bagi tubuh.
Beberapa obat atau zat kimia yang beredar dalam sirkulasi sistemik akan dibawa
ke ginjal. Akibatnya akan terjadi proses perubahan struktur ginjal (Manggarwati,
Berikut gambaran kondisi ginjal normal yang dilihat secara mikroskopik
(gambar 9).
Gambar 9. Gambaran mikroskopik ginjal normal (diwarnai dengan haematoxylin dan eosin). (A) Korteks ginjal, 1: renal corpuscle; 2: proximal convoluted tubules; 3:
distal convoluted tubules; 4: Bowman's capsulae space. (B) Medula ginjal, 1: thick ascending limb of the loop of Henle; 2: interstitial connective tissue (Gunin, 2000)
Penyakit ginjal sangat kompleks, untuk mempermudah memahami maka
penyakit ginjal dibagi berdasarkan empat komponen morfologi dasar, yaitu
glomerulus, tubulus, interstisium, dan pembuluh darah. Kebanyakan penyakit
pada glomerulus disebabkan oleh proses imunologik, sedangkan penyakit pada
tubulus dan interstisium sering disebabkan oleh senyawa toksik atau infeksi.
a.Penyakit glomerulus. Glomerulonefritis kronis merupakan penyebab tersering
gagal ginjal kronis. Glomerulus dapat mengalami cidera sebagai akibat dari
faktor perjalanan penyakit sistemik, misalnya lupus eritematosus, hipertensi
dan diabetes melitus. Glomerulonefritis dibagi menjadi sindrom nefrotik akut,
glomerulonefritis progresif cepat, sindrom nefrotik, gagal ginjal kronis dan
hematuria atau proteinuria asimtomatik.
b.Penyakit pada tubulus dan interstisium. Penyakit yang mengenai dua
Nekrosis Tubulus Akut (NTA) dan gagal ginjal akut serta reaksi peradangan di
tubulus dan interstisium (nefritis tubulointerstisium). NTA ditandai secara
morfologis dengan morfologis kerusakan sel epitel dan secara klinis oleh
penurunan fungsi ginjal secara akut.
c.Penyakit pembuluh darah. Adanya penyakit vaskular sistemik dapat mengenai
pembuluh ginjal. Penyakit yang menyerang bagian pembuluh darah ginjal yaitu
nefrosklerosis jinak, hipertensi maligna, dan nefrosklerosis akseleratif,
steanosis arteri renalis, mikroangiopati tromboliitik, dll (Robbin dan Cotran,
2007).
C. Kreatinin 1. Metabolisme kreatinin
Kreatin disintesis di dalam hati dari metionin, glisin, dan arginin. Dalam
otot rangka, kreatin difosforilasi membentuk fosforil kreatin, yang merupakan
simpanan tenaga penting bagi sintesis ATP. ATP yang dibentuk oleh glikolisis
dan fosforilasi oksidatif bereaksi dengan kreatin membentuk ADP dan
fosfokreatin yang mengandung ikatan fosfat energi tinggi, lebih tinggi dari ATP.
Fosfokreatin dapat saling memindahkan energi dengan ATP. Bila ATP banyak
dalam sel, sebagian besar energinya digunakan untuk mensintesis fosfokreatin,
sehingga terbentuk cadangan energi. Jika ATP mulai habis, energi dalam
fosfokreatin ditransfer kembali menjadi ATP. Jadi hubungan antara fosfokreatin
Kreatinin diekskresikan seluruhnya dalam urin melalui filtrasi
glomerulus. Kreatinin merupakan indeks laju filtrasi glomerulus yang lebih
cermat dibandingkan ureum karena kecepatan produksinya terutama pada fungsi
massa otot yang sedikit sekali mengalami perubahan. Oleh karena itu, pada
kondisi normal, kreatinin dijumpai dalam urin dengan konsentrasi sedikit.
Konsentrasi dan ekskresi total harian kreatinin tetap konstan meskipun ada
perubahan pola makanan. Kadar kreatinin dalam darah dapat digunakan untuk
mendiagnosis adanya kegagalan ginjal, yaitu dengan mengukur laju filtrasi
glomerulus (Sumarny, 2006). Pada kegagalan ginjal kronis, dengan kecepatan
filtrasi glomerulus yang menurun, kadar kreatinin plasma akan meningkat
berbanding terbalik dengan kecepatan ekskresi (Huether, McCance, Brashers, dan
Rote, 2008). Kadar kreatinin bervariasi sesuai dengan jenis hewan. Kadar normal
kreatinin pada beberapa jenis hewan adalah sebagai berikut (tabel I).
Hewan Kadar Normal (mg/dL) Kreatinin Kelinci 0,8-1,8 Marmut 0,6-2,2 Hamster 0,25-0,60
Mencit 0,31-1,0 Tikus 0,2-0,8
2. Metode pemeriksaan kreatinin
Macam pemeriksaan kreatinin darah adalah :
a. Jaffe Reaction. Dasar dari metode ini adalah kreatinin dalam suasana alkalis
dengan asam pikrat membentuk senyawa kuning jingga. Alat yang digunakan
adalah photometer.
b. Kinetik. Dasar metode ini relatif sama hanya dalam pengukuran dibutuhkan
sekali pembacaan. Alat yang digunakan adalah autoanalyzer.
c. Enzimatik. Dasar metode ini adalah dengan adanya substrat dalam sampel
bereaksi dengan enzim membentuk senyawa enzim substrat dengan
menggunakan alat photometer (Price dan Wilson, 1985).
Meskipun sejumlah kecil diekskresi, tes kliren kreatinin merupakan suatu
tes untuk memperkirakan GFR (Glomerular Filtration Rate) dalam klinik (Price
dan Wilson, 1985).
D. Nefrotoksisitas 1. Faktor penyebab nefrotoksisitas
Beberapa faktor yang berperan dalam perusakan ginjal akibat adanya
toksikan, antara lain:
a. Suplai darah ke dalam ginjal
Aliran darah yang mengandung toksikan dari hasil pemompaan jantung,
masuk ke dalam ginjal dan terdistribusi tidak merata. Darah lebih banyak
terdistribusi ke bagian korteks dibandingkan dengan medulla dan papilla. Oleh
bagian korteks dan berpotensi besar mempengaruhi kerusakan korteks
dibandingkan dengan medula dan papilla.
b. Konsentrasi toksikan dalam cairan intraluminal
Konsentrasi toksikan yang tinggi dan kelarutan toksikan yang rendah
pada saat proses reabsorpsi, menyebabkan obstruksi ginjal akut. Proses
reabsorbsi yang panjang akan meningkatkan konsentrasi toksikan dalam
intraluminal, yaitu dari 10 mM menjadi 50 mM ketika mencapai tubulus
proksimal, 66 mM ketika mencapai lengkung henle, 200 mM ketika mencapai
tubulus distal, dan konsentrasi tertinggi terjadi ketika mencapai duktus
pengumpul, yaitu 2000 mM. Adanya konsentrasi toksikan yang tinggi dalam
intraluminal dikarenakan toksikan mempunyai kelarutan yang rendah,
sehingga menyebabkan obstruksi akut ginjal.
c. Reabsorbsi dan/ atau sekresi toksikan melewati sel tubulus
Proses transpor aktif dalam tubulus proksimal dapat menyebabkan
peningkatan konsentrasi intraseluler toksikan. Selama sekresi aktif dan/ atau
reabsorbsi, substrat akan terakumulasi dalam sel tubulus proksimal dengan
konsentrasi yang tinggi dibandingkan dengan yang berada di cairan luminal
atau darah peritubular.
d. Biotransformasi protoksikan menjadi intermediet reaktif
Suatu segmen dari nefron mempunyai kapasitas metabolisme bioaktif.
Misalnya, tubulus proksimal dan distal mengandung isoenzim sitokrom P450
monooksigenase yang memediasi bioaktivasi intrarenal dari beberapa
interstisial papila yang ikut ambil bagian dalam co-oxidation dari protoksikan,
sehingga menghasilkan kerusakan selektif papila (Wallace dan Tarloff, 2010).
2. Nefrotoksikan
Beberapa senyawa memiliki aktivitas sebagai nefrotoksikan, seperti
terlihat pada tabel II.
Tabel II. Beberapa toksikan yang menyebabkan kerusakan pada bagian-bagian nefron
Glomerulus Tubulus Proksimal Tubulus Distal/ Tubulus Pengumpul
Karbon tetraklorida (gambar 10) merupakan senyawa yang berbentuk
cairan jernih, bersifat mudah menguap, tidak berwarna, dan bebau khas. Senyawa
karbon tetraklorida mempunyai BM 153,82 dan sangat sukar larut dalam air
(Direktorat Jenderal Pengawasan Obat dan Makanan, 1995). Karbon tetraklorida
merupakan molekul sederhana, yang jika diberikan kepada berbagai spesies,
menyebabkan nekrosis sentrilobuler dan perlemakan hati (Timbrell,2008).
Karbon tetraklorida merupakan senyawa model yang bersifat nefrotoksik
dan dapat menyebabkan Nekrosis Tubuler Akut (NTA). Radikal bebas yang
dihasilkan menyebabkan kerusakan pada tubulus proksimal ginjal dan perubahan
pada beberapa granular pneumosit (Ramarajan, dkk., 2012). Kerusakan yang
terjadi pada tubulus proksimal ginjal ini tidak disertai dengan kerusakan membran
basalis sehingga memungkinkan untuk terjadinya regenerasi sel epitelnya. Karena
itu, Nekrosis Tubular akut yang disebabkan karbon tetraklorida bersifat reversibel
(Underwood, 2000).
Penyebab terjadinya kerusakan jaringan oleh karbon tetraklorida
tergantung pada metabolisme aktivasi oleh sitokrom P450, terutama CYP2EI.
Enzim mikrosomal CYP2EI akan mempengaruhi aktivasi metabolit dari senyawa
yang terbentuk, yaitu dapat meningkatkan atau mengurangi sifat toksik dari
senyawa induk. Pada metabolisme kabon tetraklorida CYP2EI berfungsi sebagai
agen pereduksi dan mengkatalis adisi elektron yang mengakibatkan hilangnya
satu ion klorin sehingga terbentuk radikal bebas triklorometil (•CCl3) (gambar 11)
oksigen (O2) akan berubah menjadi radikal bebas triklorometilperoksi (•OOCCl3)
yang bersifat lebih reaktif (Gregus dan Klaaseen, 2001).
Gambar 11. Mekanisme biotransformasi dan oksidasi karbon tetraklorida (Trimbell, 2008)
Hasil lain dari reaksi ini adalah dari terbentuknya senyawa oksigen
reaktif selanjutnya mengakibatkan peroksidasi lipid (Timbrell, 2008). Phosgen
yang terbentuk dari reaksi merupakan intermediet yang bersifat sangat reaktif dan
dapat bereaksi dengan makromolekul seluler untuk menginduksi terjadinya
kerusakan sel (Hodgson, 2010).
Fungsi mitokondria ginjal juga dapat terganggu oleh karena induksi
karbon tetraklorida, termasuk menyebabkan efluks kalsium melintasi membran
mitokondria (Natarajan, Basivireddy, Ramachandran, Thomas,Ramamoorthy, dan
Pulimood, 2006). Radikal bebas yang terbentuk akan berikatan dengan golongan
sulfidril seperti glutation dan protein tiol, sehingga menyebabkan peroksidasi lipid
reaktif yang terbentuk dapat berikatan kovalen dengan dengan makromolekul
jaringan, yang menyebabkan jaringan mengalami kerusakan (Eaton, Gallogher,
Bammler, dan Kunze, 1995).
F. Antioksidan
Antioksidan dalam pengertian kimia, merupakan senyawa pemberi
elektron. Antioksidan bekerja dengan cara mendonorkan satu elektronnya kepada
senyawa yang bersifat oksidan sehingga aktivitas senyawa oksidan tersebut bisa
terhambat. Antioksidan menstabilkan radikal bebas dengan melengkapi
kekurangan elektron yang dimiliki radikal bebas dan menghambat terjadinya
reaksi berantai dari pembentukan radikal bebas (Winarsi, 2007).
G. Ekstraksi
Ekstrak adalah sediaan kering, kental atau cair yang dibuat dengan
menyari simplisia, diluar cahaya matahari langsung. Ekstrak kering harus mudah
digerus menjadi serbuk. Cairan penyari yang dapat digunakan dalam pembuatan
ekstrak yaitu air, etanol, eter, atau campuran etanol dan air (Badan Pengawasan
Obat dan Makanan RI, 2010).
Metode maserasi merupakan salah satu metode ekstraksi sederhana yang
dilakukan dengan cara merendam serbuk simplisia dalam cairan penyari selama
beberapa hari pada temperatur kamar dan terlindung dari cahaya sambil diaduk
(Badan Pengawasan Obat dan Makanan RI, 2010). Dengan metode maserasi,
larut akibat perbedaan konsentrasi antara larutan dalam sel dan di luar sel. Larutan
dengan konsentrasi tinggi akan terdesak keluar dan diganti oleh cairan penyari
dengan konsentrasi rendah (proses difusi). Peristiwa tersebut akan terjadi secara
berulang-ulang hingga terjadi keseimbangan konsentrasi antara larutan di luar sel
dan di dalam sel. Selanjutnya endapan dipisahkan dan filtrat dipekatkan
(Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1986). Pada proses akhir
ekstraksi semua atau hampir pelarut diuapkan dan serbuk yang tersisa
diperlakukan sedemikian rupa hingga memenuhi baku yang telah ditetapkan
(Badan Pengawasan Obat dan Makanan Republik Indonesia, 2005).
H. Persea americana Mill. 1. Taksonomi
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh)
Super Divisi : Spermatophyta (Menghasilkan biji)
Divisi : Magnoliophyta (Tumbuhan berbunga)
Kelas : Magnoliopsida (berkeping dua / dikotil)
Sub Kelas : Magnoliidae
Ordo : Laurales
Famili : Lauraceae
Genus : Persea
Spesies : Persea americana Mill.
2. Sinonim
Laurus persea L., Persea americana var. angustifolia Miranda, Persea
americana var. drymifolia (Schldtl &Cham) S. F. Blake, Persea americana var.
nubigena (L. O. Williams) L.E. Kopp, Persea drymifolia Schldtl. & Cham.,
Persea edulis Raf., Persea floccosa Mez, Persea gigantea L. O. Williams, Persea
gratissima C. F. Gaertn., Persea gratissima var. drimyfolia (Schldtl. & Cham.)
Mez, Persea gratissima var. macrophylla Meisn., Persea gratissima var. oblonga
Meisn., Persea gratissima var. praecox Nees, Persea gratissima var. vulgaris
Meisn., Persea pleiogyna Blake, Persea nubigena L. O. Williams, Persea
paucitriplinervia Lundell, Persea persea (L.) Cockerell, Persea streyermarkii C.
K. Allen. (Lim, 2012).
3. Nama lain
Alligator pear, avocado, avocado-per, butter fruit (Inggris), avocado
(Filipina), avocat, avocatier, zabelbok, zaboka (Prancis), alligatorbirne,
avocadobirne (Jerman), adpukat, avokad (Indonesia), apukado, avokado
(Malaysia), Aguacate, Pagua (Spanyol), awokado (Thailand) (Yasir, Das, Kharya,
2010).
4. Morfologi
Tanaman Persea americana berupa pohon yang selalu hijau, yang
tingginya mencapai 20 m. Pohon terdiri dari daun tunggal, tersusun spiral, tepi
daun rata; panjang tangkai daun 1,5-5 cm; daun berbentuk elips hingga lanset,
bulat telur hingga bulat telur sungsang, panjang daun 5-40 cm dan lebar 3-15 cm,
yang muncul di ujung cabang; bunga banci tersusun atas 3 daun mahkota,
memiliki bau harum; perhiasan bunga tersusun atas dua lingkaran; benang sari 9
di dalam 3 lingkaran; kumpulan benang sari di bagian dalam mengeluarkan 2
nektar di bagian dasarnya; putik terdiri atas satu ruang bakal buah, tangkai kepala
putik ramping dengan kepala putik tunggal (simple papillate stigma). Buah besar
berdaging dan berair (berry), berbiji tunggal, permukaan buah halus, panjang 7-20
cm. Buah besar dan bulat, dilapisi dua lapisan dan dua kotiledon besar yang
melindungi embrio kecil (Proseanet, 2012).
Pada umumnya tanaman alpukat dapat tumbuh di dataran rendah
sampai dataran tinggi, yaitu 5-1500 m dpl. Namun tanaman akan tumbuh baik
pada ketinggian 200-1000 m dpl (Kemal, 2001).
5. Kandungan kimia
Biji Persea americana Mill. memiliki kandungan metabolit yang
berbeda-beda kadarnya. Kandungan metabolit sekunder pada biji Persea
americana, meliputi alkaloid, triterpenoid, tanin, flavonoid, dan saponin
(Marlinda, dkk., 2012).
6. Khasiat dan kegunaan
Kandungan metabolit buah dan biji Persea americana Mill, dilaporkan
mempunyai khasiat yang efektif yaitu untuk melawan hepatotoksisitas, inflamasi,
kanker, dan mengobati hipertensi (Arukwe, dkk., 2012). Adanya kandungan
flavonoid dapat mencegah kerusakan oksidatif sel, mempunyai aktifitas
perlindungan dan anti kanker yang kuat melawan tahap-tahap dalam
diketahui mempunyai beberapa khasiat, yaitu sebagai astringen, anti diare, anti
bakteri dan antioksidan.
I. Landasan Teori
Ginjal merupakan organ yang bekerja untuk menyaring darah sebanyak
kurang lebih 200 liter tiap harinya dan juga membuang sisa-sisa metabolisme
serta kelebihan cairan tubuh melalui urine (Rasjidi, 2008).
Adanya gangguan pada organ ginjal dapat menyebabkan terjadinya
penumpukan bahan-bahan beracun, seperti ureum dan nitrogen. Oleh karena itu,
kadar nitogen urea (BUN/ Blood Urea Nitrogen) dapat digunakan untuk
mengukur kemampuan fungsi ginjal. Selain itu dapat juga dihitung dari kadar
kreatinin, yaitu suatu bahan sisa metabolisme sel otot yang beredar dalam darah.
Fungsi ginjal disini adalah membuang kreatinin darah ke dalam urine. Jika fungsi
ginjal menurun tentunya kadar kreatinin dalam darah akan meningkat. Oleh
karena itu, kreatinin juga bisa digunakan untuk mengukur kemampuan fungsi
ginjal (Rasjidi, 2008).
Karbon tetraklorida merupakan senyawa model yang bersifat hepatotoksik
dan nefrotoksik. Senyawa ini akan dimetabolisme oleh enzim sitokrom P450
sehingga terbentuk radikal bebas triklorometil (
•
CCl3) dan triklorometil peroksi(
•
CCl3O2) yang bersifat lebih reaktif (Makni, dkk., 2011). Radikal bebastriklorometil berikatan secara kovalen dengan lemak mikrosomal dan protein, dan
akan bereaksi secara langsung dengan membran fosfolipid dan kolesterol yang
mengaktifkan senyawa oksigen reaktif selanjutnya mengakibatkan peroksidasi
lipid (Timbrell, 2008).
Adanya antioksidan dapat melindungi jaringan dari efek radikal bebas, ROS
(reactive oxygen species), dan peroksidasi lipid dan memperlambat proses
perjalanan penyakit kronis (Makni, dkk., 2011).
Pada penelitian Carpena, dkk. (2011), kandungan flavonoid dalam biji P.
americana mempunyai aktivitas antioksidan terhadap radikal CUPRAC, DPPH,
dan ABTS, melalui ekstraksi dengan larutan penyari metanol. Penelitian ini
dilakukan untuk membuktikan kemampuan kandungan antioksidan P. americana
sebagai nefroprotektif terhadap kerusakan ginjal akibat adanya radikal bebas
yang dihasilkan oleh karbon tetraklorida.
J. Hipotesis
Pemberian ekstrak metanol-air biji P. americana jangka panjang pada tikus
terinduksi karbon tetraklorida memiliki efek nefroprotektif terhadap kadar serum
32 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni dengan
rancangan penelitian acak lengkap pola searah.
B. Variabel Penelitian dan Definisi Operasional
Variabel- variabel yang digunakan adalah sebagai berikut :
1. Variabel utama
a. Variabel bebas
Variabel bebas dalam penelitian ini adalah variasi dosis pemberian
ekstrak metanol-air biji P. americana.
b. Variabel tergantung
Variabel tergantung penelitian ini adalah penurunan kadar serum
kreatinin dan gambaran histologis ginjal akibat pemberian jangka panjang
ekstrak metanol-air biji P. americana pada tikus jantan galur Wistar terinduksi
karbon tetraklorida.
2. Variabel pengacau
a. Variabel pengacau terkendali
Variabel pengacau terkendali dalam penelitian ini adalah kondisi hewan
uji, yaitu tikus jantan galur Wistar dengan berat badan 150-250 g dan umur 2-3
bulan, frekuensi pemberian ekstrak metanol-air biji P. americana satu kali
cara pemberian senyawa pada tikus dilakukan secara per oral dan
intraperitoneal, dan bahan uji yang digunakan berupa biji P. americana yang
diperoleh dari Padang, Sumatera Barat diambil pada bulan Januari 2013.
b. Variabel pengacau tak terkendali
Variabel pengacau tak terkendali dalam penelitian ini adalah kondisi
patologis dari tikus jantan galur Wistar yang digunakan.
3. Definisi operasional
a. Ekstrak metanol-air biji P. americana. Ekstrak metanol-air biji P.
americana adalah ekstrak kental yang diperoleh dengan mengekstraksi
serbuk kering biji P. americana seberat 10,0 g yang dilarutkan dalam 100
ml pelarut metanol-air secara maserasi (perendaman) selama 5x24 jam, hasil maserasi kemudian disaring menggunakan corong Buchner, yang dilapisi
kertas saring, sehingga diperoleh filtrat. Serbuk sisa perendaman
diremaserasi kembali dengan metanol 70% selama 2x24 jam. Setelah
remaserasi, disaring dengan kertas saring, dievaporasi dengan suhu 70˚C
dan diuapkan di atas waterbath dengan suhu 80˚C, hingga diperoleh bobot
ekstrak tetap.
b. Dosis ekstrak metanol-air biji P. americana. Dosis ekstrak metanol-air biji
P. americana adalah sejumlah (gram) ekstrak metanol-air biji P. americana
tiap satuan kg berat badan dari subyek uji. Ekstrak biji P. americana dibuat
dengan mengekstraksi sejumlah (gram) serbuk biji P. americana dalam
c. Penurunan kadar serum kreatinin. Didefinisikan sebagai kemampuan
ekstrak metanol-air biji P. americana pada dosis tertentu untuk menurunkan
kadar serum kreatinin pada tikus jantan galur Wistar terinduksi karbon
tetraklorida.
d. Pemberian jangka panjang. Pemberian ekstrak metanol-air biji P. americana
satu kali selama enam hari berturut-turut.
C. Bahan Penelitian 1. Bahan utama
a. Hewan uji yang digunakan berupa tikus jantan galur Wistar dengan umur
2-3 bulan dan berat badan 150-250 g yang diperoleh dari Laboratorium Imono
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
b. Biji P. americana yang diperoleh dari Padang, Sumatera Barat yang diambil
pada bulan Januari 2013.
2. Bahan kimia
a. Bahan nefrotoksin yang digunakan adalah karbon tetraklorida yang
diperoleh dari Laboratorium Kimia Analisis Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
b. Metanol dan air suling sebagai pelarut yang digunakan untuk pembuatan
sediaan uji diperoleh dari Laboratorium Farmakologi Fitokimia Fakultas
c. Aqua bidestilata untuk blanko pengujian kreatinin, yang dipeoleh dari
laboratorium Kimia Analisis Instrumental Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
d. Kontrol serum Kreatinin Cobas® (PreciControl ClinChem Multi 2)
Roche/Hitachi analyzer
e. Olive oil Bertolli®
f. Reagen serum kreatinin
D. Alat atau Instrumen Penelitian
1. Alat ekstraksi
Seperangkat alat gelas berupa beker gelas, erlenmeyer, gelas ukur, labu
ukur, cawan porselen, corong Buchner, pipet tetes, batang pengaduk (pyrex
Iwaki Glass®). Mesin penyerbuk Retsch®, ayakan no 40 Electric Sieve Shaker
Indotest Multi Lab®, timbangan analitik Mettler Toledo®, moisture balance,
orbital shaker Optima®, rotary vacuum evaporator IKAVAC®, oven
Memmert®.
2. Alat uji nefroprotektif
Seperangkat alat gelas berupa bekker glass, gelas ukur, tabung reaksi,
labu ukur, pipet tetes, batang pengaduk (Pyrex Iwaki Glass®). Timbangan
elektrik Mettler Toledo®, sentrifuge Centurion Scientific®, vortex Genie
Wilten®, spuit per oral dan syringe 3 cc Terumo®, spuit ip. dan syringe 1 cc
E. Tata Cara Penelitian 1. Determinasi serbuk biji P. americana
Determinasi biji P. americana dilakukan dengan mencocokan ciri-ciri
makroskopis dan mikrokopis serbuk biji P. americana yang berasal dari
Padang dengan serbuk biji yang telah diketahui pasti merupakan serbuk biji P.
americana Mill berdasar ciri-ciri morfologinya.
2. Pengumpulan bahan
Bahan uji yang digunakan adalah biji P. americana yang sudah dalam
bentuk serbuk berwarna kuning kecoklatan, yang diperoleh dari wilayah
Padang, Sumatera Barat, pada bulan Januari 2013.
3. Pembuatan serbuk
Biji P. americana dicuci bersih di bawah air mengalir dan bagian kulit ari
dari biji alpukat tersebut dibuang. Setelah bersih biji dipotong kecil-kecil dan
diangin-anginkan hingga biji tidak tampak basah kemudian dilakukan
pengeringan menggunakan oven pada suhu 50 ˚C selama 24 jam. Setelah
kering biji dibuat serbuk dan diayak dengan ayakan nomor 40 supaya
kandungan fitokimia yang terkandung dalam biji P. americana lebih mudah
terekstrak karena luas permukaan serbuk yang kontak dengan pelarut semakin
besar.
4. Penetapan kadar air serbuk biji Persea americana Mill
Penetapan kadar air serbuk biji P. americana bertujuan untuk mengetahui
yaitu kurang dari 10% (Direktorat Jenderal Pengawasan Obat dan Makanan,
1995).
Penetapan kadar air serbuk biji P. americana dilakukan dengan
menggunakan alat moisture balance menggunakan metode susut bobot
pengeringan. Serbuk dipanaskan pada suhu 105 ˚C selama 15 menit.
Kemudian serbuk ditimbang ulang dan dihitung sebagai bobot sesudah
pemanasan. Selisih bobot sebelum pemanasan dan sesudah pemanasan
merupakan kadar air dari sampel yang diteliti.
5. Pembuatan pelarut metanol-air (70:30)
Larutan metanol-air (70:30) digunakan sebagai cairan penyari pada tahap
maserasi pembuatan ekstrak biji P. americana. Dasar pemilihan larutan penyari
ini berdasarkan penelitian yang dilakukan oleh Carpena, dkk. (2011), yang
menyatakan bahwa biji P. americana yang diekstraksi dengan metanol-air
(70:30) dapat menyari senyawa yang mempunyai aktivitas antioksidan yang
bersifat polar.
6. Pembuatan ekstrak metanol-air biji P. americana
Ekstraksi dilakukan dengan cara maserasi. Sebanyak 10 g serbuk biji P.
americana direndam dalam 100 mL pelarut metanol-air (70:30) pada suhu
kamar selama 5x24 jam. Tujuan dilarutkan dalam pelarut metanol agar
senyawa kimia yang terkandung dalam biji P. americana dapat larut dalam
pelarut. Setelah dilakukan perendaman, hasil maserasi kemudian disaring
menggunakan corong Buchner, yang dilapisi kertas saring, sehingga diperoleh
selama 2x24 jam. Filtrat hasil saringan dipindahkan dalam labu alas bulat
untuk dievaporasi. Tujuan proses evaporasi adalah menguapkan cairan penyari
pada proses maserasi. Prinsip alat vaccum evaporator adalah menguapkan
pelarut dengan suhu rendah dan berputar dan menggunakan tekanan tinggi
untuk membantu proses penguapan. Hasil evaporasi dituangkan dalam cawan
porselen yang telah ditimbang sebelumnya, agar mempermudah perhitungan
rendemen ekstrak yang akan diperoleh. Cawan porselen yang berisi larutan
hasil evaporasi dipanaskan di atas waterbath dengan suhu 80 ˚C untuk
mendapatkan ekstrak metanol-air biji P. americana yang kental dengan bobot
pengeringan ekstrak yang tetap. Menghitung rata-rata rendemen lima replikasi
ekstrak metanol biji Persea americana kental yang telah dibuat.
Rendemen ekstrak = berat cawan ekstrak kental – berat cawan kosong
Rata-rata rendemen = = 2,78 g
7. Penetapan konsentrasi pekat ekstrak
Konsentrasi yang dapat digunakan adalah konsentrasi pekat yang dapat
dibuat dimana pada konsentrasi tersebut ekstrak dapat dimasukkan serta
dikeluarkan dari spuit oral. Cara pembuatannya adalah dengan melarutkan
ekstrak per cawannya dengan pelarut yang sesuai, yaitu CMC Na 1%
(Kurniawati, dkk., 2011).
8. Penetapan dosis ekstrak metanol-air biji P. americana
Penetapan peringkat dosis didasarkan pada perhitungan dengan bobot