Malang, 26 Maret 2016
1217
PERBANDINGAN AKTIVITAS ANTIOKSIDAN BUAH PEPAYA (Carica papaya L.) DAN BUAH JAMBU BIJI MERAH (Psidium guajava L.)
Novi Febrianti, Mila Indra Rohmana, Irfan Yunianto, Risanti Dhaniaputri
Program Studi Pendidikan Biologi, FKIP, Universitas Ahmad Dahlan Kampus III, Jl. Prof. Dr. Soepomo, SH, Yogyakarta, 55164 Indonesia
Email : novifebrianti@pbio.uad.ac.id
Abstrak
Antioksidan adalah molekul penting yang dibutuhkan tubuh untuk menangkap radikal bebas yang dapat merusak sel-sel tubuh. Buah-buahan mengandung berbagai jenis senyawa antioksidan alami. Penelitian ini bertujuan untuk membandingkan aktivitas antioksidan dua jenis buah tropis lokal yang banyak dikonsumsi masyarakat Indonesia, yaitu buah pepaya dan buah jambu biji merah. Buah pepaya dan buah jambu biji merah diekstrak dengan metode maserasi dengan pelarut etanol 96%. Aktivitas antioksidan diukur menggunakan 3 uji, yaitu uji kandungan asam askorbat (vitamin C), uji total fenol, dan uji penangkapan radikal DPPH menggunakan spektrofotometer. Hasil penelitian menunjukkan bahwa terdapat perbedaan rata-rata kandungan asam askorbat, total fenol, dan kemampuan penangkapan radikal DPPH pada buah pepaya dan buah jambu biji merah, berturut-turut yaitu 48,4 mg/100g dan 49,86 mg/100g untuk asam askorbat, 26,564 µg/mL dan 75,700 µg/mL untuk total fenol, 594,617 mg/ml dan 559,600 mg/ml untuk penangkapan DPPH. Kata kunci : aktivitas antioksidan, buah pepaya, buah jambu biji merah, asam askorbat,
fenol, DPPH
Abstract
Antioxidant is an important molecule that is needed by the body to scavenge free radicals. Fruits contain many types of natural antioxidants. The purpose af this study is to compare the antioxidant activity of 2 types of local tropical fruit, papaya and red guava fruit, those are consumed much by Indonesian people,. Papaya and red guava fruit were extracted by maceration technique using 96% ethanol. Antioxidant activity was measured by ascorbic acid (vitamin C), phenolic total, and DPPH test using spectrophotometre. The experiment‘s result exhibited different levels of ascorbic acid, phenol, and DPPH radical svacenge in papaya and red guava fruits. Average concentration of ascorbic acid is 48,4 mg/100g and 49,86 mg/100g, total phenol is 26,564 µg/mL and 75,700 µg/mL, and DPPH radical scavenge is 594,617 mg/ml and 559,600 mg/ml respectively for papaya and red guava fruit.
Keywords: antioxidant activity, papaya fruit, red guava fruit, ascorbic acid, phenol, DPPH
Pendahuluan
Indonesia adalah negara tropis yang memiliki kekayaan sumber daya alam yang melimpah. Salah satu kekayaan sumber daya alam tersebut adalah keanekaragaman jenis buah-buahan tropis. Buah-buah tropis tersebut umumnya ditanam sendiri ataupun di perkebunan khusus. Pepaya dan jambu biji merah adalah jenis buah-buahan tropis lokal
Malang, 26 Maret 2016
1218
yang banyak dikonsumsi masyarakat dan mudah ditemukan, baik dijual di pasar ataupun ditanam sendiri oleh masyarakat.
Buah-buahan memiliki berbagai senyawa antioksidan alami yang tinggi. Antioksidan alami umumnya lebih aman untuk dikonsumsi dan dapat meningkatkan derajat kesehatan tubuh, dibandingkan dengan antioksidan sintetis. Menurut Prakash et al. (2001) senyawa antioksidan yang dihasilkan dari tumbuhan seperti vitamin C, vitamin E, karoten, golongan fenol terutama polifenol, dan flavonoid berpotensi untuk mengurangi risiko berbagai penyakit degeneratif.
Senyawa antioksidan memiliki peran yang sangat penting dalam kesehatan. Berbagai bukti ilmiah menunjukkan bahwa senyawa antioksidan mengurangi risiko terhadap penyakit kronis seperti kanker dan penyakit jantung koroner. Penelitian Febrianti dan Widayati (2014) mendapatkan bahwa pemberian jus buah pepaya pada mencit yang dipaparkan asap rokok menyebabkan struktur pulmo mencit kembali normal. Mariyanti (2013) dan Imam & Juwono (2006) mendapatkan bahwa jus tomat juga mempunyai efek positif untuk mencegah kerusakan pulmo dan meningkatkan motilitas spermatozoa mencit yang dipaparkan asap rokok karena aktivitas antioksidannya yang tinggi.
Berdasarkan data Riskesdas tahun 2013, hanya 6,5% penduduk Indonesia yang remaja dan dewasa mengkonsumsi buah dan sayur dalam jumlah yang cukup. Dari data tersebut terlihat bahwa konsumsi buah dan sayur di Indonesia masih sangat rendah. Hal ini dipengaruhi oleh pola makan masyarakat Indonesia yang kurang dalam mengkonsumsi buah. Penelitian ini bertujuan untuk membandingkan aktivitas antioksidan buah pepaya dan jambu biji merah. berdasarkan kandungan asam askorbat, total fenol, dan aktivitas penangkapan radikal DPPH Dengan penelitian ini diharapkan masyarakat Indonesia akan lebih meningkat kesadarannya untuk mengkonsumsi berbagai jenis buah tropis yang tumbuh di Indonesia.
Metode Penelitian
Identifikasi Tanaman
Identifikasi tanaman pepaya (Carica papaya L.) dan jambu biji merah (Psidium guajava
L.) dilakukan di Laboratorium Sistematik Tumbuhan Fakultas Biologi Universitas Gadjah Mada.
Pengumpulan Simplisia
Buah pepaya dan jambu diperoleh dari desa Karangpakis kecamatan Nusawungu kabupaten Cilacap pada bulan Mei 2015.
Persiapan dan Ekstraksi Buah
Persiapan dan ekstraksi buah mengacu pada metode Nurliyana (2010) dengan dimodifikasi. Buah jambu biji merah dan pepaya dicuci bersih dan kupas untuk memisahkan kulit dan daging buahnya. Untuk pepaya dikupas dan dipisahkan dengan bijinya, sedangkan untuk jambu biji merah tidak dikupas. Daging buah yang sudah bersih dipotong kecil-kecil kemudian diblender untuk mendapatkan sediaan seperti pasta selama beberapa menit. Sampel yang berupa sediaan pasta dituangkan ke dalam toples kaca dan ditambahkan ethanol 96% sebanyak 500 ml. Campuran ini diaduk hingga homogen dan disimpan selama 24 jam, setelah itu disaring menggunakan vakum yang dilapisi kertas saring. Filtrate yang didapat diuapkan menggunakan rotary evaporator selama beberapa
Malang, 26 Maret 2016
1219
jam pada suhu 70oC untuk menghilangkan pelarutnya. Setelah didapatkan ekstrak kental, kemudian dilakukan freeze dry untuk menghilangkan sisa air yang terdapat didalam ekstrak, sehingga didapatkan ekstrak kering.
Penentuan Total Asam Askorbat (TAA)
Ekstraksi Sampel dan pembuatan larutan iodium
Sebanyak ± 1.00 gram sampel bubuk dimasukkan dalam labu takar 10 ml dan ditambahkan aquades sampai tera, kemudian disaring.
Larutan iodium 0,01 N dibuat dengan cara mencampurkan 2,00 gram KI dan I2 ,
kemudian dilarutkan sampai volume 1 liter dengan aquades selama semalam untk melarutkan iod secara sempurna.
Penentuan Konsentrasi Asam Askorbat
Sebanyak 1,00 ml filtrate hasil ekstarksi diencerkan ke dalam 10,00 ml aquades dan diambil 2 ml filtrat hasil pengenceran yang dimasukkan ke dalam Erlenmeyer, lalu ditambahkan dengan 0,4 ml larutan amilum (soluble starch) 1%. Larutan kemudian dititrasi dengan 0,01 N iodium. Titik akhir titrasi ditandai denagan perubahan warna larutan menjadi semburat biru.0,01 N setara dengan 0,88 mg asam askorbat.
Konsentrasi asam askorbat dihitung dengan rumus: Asam askorbat (mg/ 100 g sampel)
Uji Kandungan Fenolik Total
Pembuatan larutan stok asam galat 100 mg/ml
Sebanyak 10,0 mg standar asam galat dilarutkan sampai homogen dengan aquades dan dimasukkan dalam labu takar 100,0 ml kemudian ditambahkan aquades sampai batas tera.
Pembuatan natrium karbonat 7,5% dan pereaksi follin ciocalteu (FC)
Menimbang 7,5 g natrium karbonat kemudian dilarutkan dengan aquades sampai homogen dan dimasukkan dalam 100 ml kemudian ditambah aquades sampai batas tera.
Mengambil 10,0 ml larutan FC standar kemudian dimasukkan dalam labu takar 100,0 ml dan ditambahkan aquades sambai batas tera.
Penentuan kurva kalibrasi
Membuat kurva kalibrasi dengan 7 titik pada variasi 20, 30, 40, 50, 60, 70, 80 µg/ml dalam labu takar 10 ml dari larutan stock. Mengambil variasi volume 2,0 ml; 3,0 ml; 4,0 ml; 5,0 ml; 6,0 ml; 7,0 ml; 8,0 ml; dari larutan induk kemudian ditambahkan aquades sampai batas labu takar 10 ml. 300 µL masing-masing larutan standar ditambahkan 1,5 NaCO3 7,5% divortek dan didiamkan selama 3 menit dan ditambahkan 1,2 ml larutan FC kemudian dilakukan pengukuran pada saat OT dan lamda maksimalnya pada alat spektrofotometer.
Pengukuran kadar fenol
50 mg sampel ekstrak dilarutkan dalam aquases kemudian disonikator selama 20 menit. Larutan ekstrak tersebut dimasukkan dalam labu takar 50,0 ml dan ditambah aquades sampai tanda batas tera. Kemudian 300 µL sampel ditambahkan 1,5 NaCO3 7,5% divortek dan didiamkan selama 3 menit dan ditambahkan 1,2 ml larutan FC
Malang, 26 Maret 2016
1220
kemudian dilakukan pengukuran pada saat OT dan lamda maksimalnya pada spektrofotometer.
Uji DPPH
Pembuatan larutan DPPH 0,15 mM
Larutan DPPH 1 mM dibuat dengan melarutkan 19,7 mg kristal DPPH dalam 50,0 ml ethanol. Larutan DPPH 0,15 mM dibuat dengan mengencerkan larutan DPPH 1 mM dengan pelarut ethanol untuk segera digunakan dan dijaga dalam temperatur rendah serta terlindung dari cahaya.
Pembuatan larutan sampel
Larutan sampel ekstrak ethanol dibuat dengan 10,0 mg sampel dalam 10,0 ml ethanol p.a. Dari larutan tersebut dibuat larutan dengan 5 konsentrasi yaitu 5,0 mg/ml; 4,0 mg/ml; 3,0 mg/ml; 2,0 mg/ml; dan 1 mg/ml untuk buah pepaya dan buah jambu biji merah. Pembuatan konsentrasi didasarkan pada hasil orientasi.
Pembuatan larutan kontrol negatif dan positif
Kontrol negatif dibuat dengan cara mencampurkan 1,0 ml ethanol dan 1,0 ml pereaksi DPPH 0,15 mM. Kontrol positif dibuat dengan cara 10,0 mg kuersetin dalam 10,0 ml ethanol p.a. Dari larutan tersebut dibuat larutan dengan 6 konsentrasi yaitu 5,0 mg/ml; 3,5 mg/ml; 2,5 mg/ml; 2,0 mg/ml; 2 mg/ml; 1,5 mg/ml; dan 1 mg/ml. Pembuatan konsentrasi didasarkan pada hasil orientasi.
Penentuan operating time (waktu operasional)
Pada penentuan operating time 1,0 ml larutan uji dikocok dengan 1,0 ml larutan DPPH 0,15 mM, kemudian diamati absorbansinya selama 90 menit pada panjang gelombang 517 nm.
Pengukuran absorbansi larutan
Pengukuran absorbansi larutan dilakukan dengan cara 1,0 ml larutan uji (sampel atau kontrol positif) dengan berbagai konsentrasi dikocok kuat dengan 1,0 ml larutan DPPH 0,15 mM. Campuran larutan tersebut disimpan ditempat gelap selama operating time. Kemudian absorbansinya diukur pada panjang gelombang serapan maksimal DPPH dengan spektrofotometer UV-Vis. Larutan blangko yang digunakan adalah ethanol yang akan dibaca absorbansinya.
Analisis data
Data yang diperoleh dianalisis distribusi dan homogenitasnya menggunakan uji distribusi normal (Kolmogorov-Smirnov), dan uji Levene. Data yang berdistribusi normal dan homogen selanjutnya diuji t-test (Independent Sample Test) untuk mengetahui perbedaan yang bermakna.
Hasil dan Pembahasan
Asam askorbat merupakan salah satu jenis antioksidan yang penting. Pada penelitian ini kadar asam askorbat diukur dengan menggunakan metode titrasi iodium. Larutan iodium digunakan sebagai titran dan pada larutan sampel yang ditambahkan amilum 1% sebagai titer. Menurut Khopkar (1990) amilum dijadikan sebagai indikator pada proses titrasi karena amilum dapat menekan iodida pada konsentrasi < 10ˉ⁵. Titrasi dihentikan
Malang, 26 Maret 2016
1221
tepat pada saat larutan berubah warna menjadi semburat biru. Semakin cepat perubahan warna terjadi menunjukkan bahwa kandungan vitamin C semakin tinggi. Pada proses titrasi dilakukan 3 kali pengulangan untuk setiap sampel buah.
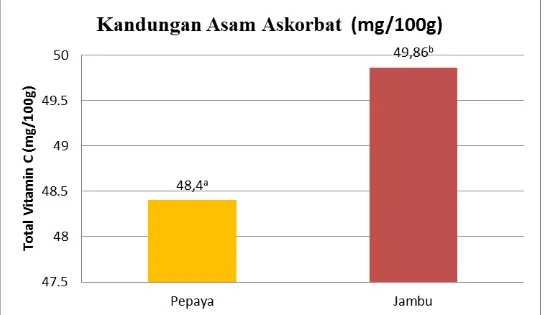
Berdasarkan data hasil titrasi dengan 3x pengulangan diketahui bahwa ekstrak etanol buah pepaya memiliki rata-rata kandungan vitamin C sebesar 48,4 mg/100,g sedangkan ekstrak etanol buah jambu biji merah sebesar 49,86 mg/100g. Berdasarkan hasil uji t diketahui bahwa rata-rata kandungan vitamin C buah pepaya dan buah jambu biji merah memiliki perbedaan yang bermakna (ditunjukkan dengan huruf superskrip yang berbeda pada Gambar 1).
Gambar 1. Diagram kandungan asam askorbat buah pepaya dan buah jambu biji merah Perbedaan kandungan asam askorbat pada buah-buahan dapat dipengaruhi oleh berbagai faktor, antara lain varietas, spesies, kultivar, dan kondisi panen. Variabel lain yang berpengaruh adalah suhu lingkungan, proses fotosintesis, kelembaban relatif, stres oksidatif, paparan matahari. Polutan juga dianggap sebagai kontributor utama yang mempengaruhi variasi kandungan asam askorbat. Tingkat kematangan buah mempengaruhi banyaknya kadar vitamin C pada buah. Semakin masak buah maka semakin tinggi kadar asam askorbatnya. Hal ini disebabkan karena selama proses pemasakan buah mengalami peningkatan kadar askorbat (Gull et. al, 2012).
Asam askorbat dikenal memiliki sifat yang mudah larut dalam air dan mudah rusak dengan pemanasan yang terlalu lama. Beberapa faktor yang mempengaruhi konsentrasi asam askorbat pada suatu bahan makanan adalah jangka waktu penyimpanan, paparan sinar matahari, dan faktor pemanasan (Sinaga, 2011). Menurut Almatsier (2004) proses pencucian dan pemasakan buah dengan pemanasan yang terlalu lama dapat menghilangkan kandungan asam askorbat.
Uji Kandungan Total Fenol
Senyawa fenol merupakan salah satu senyawa yang umum dijumpai pada tanaman. Senyawa fenol berfungsi sebagai antimutasi, antikanker, antipenuaan, dan antioksidan. Beberapa macam senyawa fenol yang mempunyai korelasi tinggi dengan aktivitas
Malang, 26 Maret 2016
1222
antioksidan yaitu asam fenol (asam galat) dan polifenol (flavonoid). Beberapa penelitian menunjukkan bahwa aktivitas antioksidan sangat berhubungan dengan kandungan senyawa fenol pada suatu bahan (Nurliyana, 2010).
Pada penentuan kadar fenolik total, larutan standar yang digunakan adalah asam galat atau asam 3,4,5-trihidroksibenzoat dengan variasi konsentrasi 20, 30, 40, 50, 60, 70, 80 µg/ml. Hasil pembacaan sampel menunjukkan bahwa ekstrak buah pepaya memiliki rata-rata kandungan fenol total sebesar 26,564 µg/mL dan jambu biji merah 75,700 µg/m. Terdapat perbedaan yang bermakna kandungan total fenol kedua jenis buah ssetelah dianalisis dengan tji t (Gambar 2).
Gambar 2. Diagram kandungan total fenol buah pepaya dan buah jambu biji merah.
Kandungan polifenol pada buah-buahan ditentukan oleh warna buah, buah-buahan yang berwarna gelap memiliki kandungan polifenol yang lebih tinggi. Buah jambu biji merah memiliki warna merah yang intensitas warnanya lebih tinggi dibanding buah pepaya yang berwarna oranye. Hal ini terbukti dalam penelitian ini, kandungan total fenol dalam buah jambu biji merah lebih besar dibandingkan buah pepaya. Tingginya total fenol pada buah jambu biji merah kemungkinan juga disebabkan karena bagian buah jambu biji merah yang dianalisis adalah kulit, daging buah, dan bijinya, sedangkan pepaya hanya daging buahnya saja yang diekstrak. Menurut Nurliya (2010) senyawa fenol lebih banyak ditemukan pada bagian tumbuhan yang tidak dapat dimakan seperti kulit, biji, daun, dan batang.
Aktivitas Penangkapan Radikal DPPH
Penangkapan radikal DPPH merupakan salah satu metode yang digunakan untuk mengetahui aktivitas antioksidan suatu bahan. Kemampuan senyawa atau bahan uji dalam menangkap radikal DPPH menunjukkan bahwa senyawa atau bahan tersebut memiliki aktivitas sebagai antioksidan. Penggunaan DPPH sebagai metode penangkapan radikal bebas karena mudah digunakan, mempunyai sensitifitas yang tinggi dan dapat menganalisis bahan dalam jumlah yang besar dalam waktu yang singkat.
Malang, 26 Maret 2016
1223
Perubahan warna DPPH dari ungu menjadi kuning setelah reduksi, dapat ditetapkan secara kuantitatif dengan penurunan absorbansi pada panjang gelombang 517 nm. Senyawa DPPH yang berwarna kuning yang stabil sedangkan flavonoid kehilangan atom H akan menjadi radikal bebas baru yang lebih stabil dan tidak reaktif karena adanya efek resonansi inti aromatik. Pada dasarnya absorbansi yang diukur adalah absorbansi larutan DPPH yang tidak bereaksi dengan senyawa antioksidan. Semakin besar konsentrasi larutan bahan uji maka absorbansi yang dihasilkan semakin kecil karena yang terukur adalah sisa DPPH yang tidak bereaksi dengan antioksidan. Semakin kecil absorbansi yang dihasilkan maka semakin besar aktivitas penangkapan radikal DPPH.
Harga ES50 berbanding terbalik dengan kemampuan senyawa untuk menangkap radikal bebas. Rendahnya nilai ES50 menunjukkan tingginya aktivitas penangkapan radikal bebas. Semakin besar harga ES50 maka aktivitas antioksidan melalui penangkapan radikal bebas semakin kecil. Pada penelitian ini diperoleh nilai rata-rata ES50 594,617 mg/ml untuk pepaya dan 559,600 mg/ml untuk jambu biji merah, dan 374,499 mg/ml untuk kuersetin yang merupakan kontrol positif (Gambar 3).
Gambar 3. Diagram aktivitas penangkapan radikal DPPH (nilai ES 50) Berdasarkan h hasil ini diketahui bahwa buah jambu biji merah mempunyai aktivitas penangkapan radikal DPPH lebih tinggi dibandingkan pepaya. Hasil ini sejalan dengan hasil uji asam askorbat dan total fenol yang mendapatkan bahwa buah jambu biji merah mempunyai kandungan kedua senyawa tersebut lebih tinggi. Hal ini membuktikan bahwa tingginya kandungan asam askorbat dan total fenol akan mengakibatkan semakin besarnya aktivitas penangkapan radikal DPPH.
Aktivitas penangkapan radikal DPPH buah pepaya dan jambu biji merah ternyata lebih rendah dibandingkan kontrol positif kuersetin. Kuersetin adalah senyawa flavonoid dari tumbuhan yang mempunyai aktivitas antioksidan karena kemampuannya menangkap radikal-radikal dan oksigen aktif. Campuran berbagai senyawa antioksidan yang terkandung dalam buah-buah yang diuji ternyata memiliki aktivitas yang lebih rendah dibanding kontrol kuersetin murni. Lebih rendahnya aktivitas penangkapan radikal DPPH ini kemungkinan juga karena terjadinya proses oksidasi pada sampel buah selama proses penelitian.
Malang, 26 Maret 2016
1224
Kesimpulan
Buah jambu biji merah memiliki aktivitas antioksidan yang lebih tinggi daripada buah pepaya, berdasarkan kandungan asam askorbat, total fenol, dan aktivitas penangkapan radikal DPPH.
Ucapan Terimakasih
Penelitian ini merupakan bagian penelitian yang dibiayai oleh Dirjen Pendidikan Tinggi Kemenristekdikti melalui hibah desentralisasi skim hibah bersaing tahun 2015. Untuk itu peneliti mengucapkan terimakasih keada Dirjen Dikti dan semua pihak yang telah membantu sehingga terlaksananya penelitian ini.
Daftar Pustaka
Almatsier, S. 2004. Prinsip Dasar Ilmu Gizi.Gramedia Pustaka Utama. Jakarta.
Febrianti, N., & Widayati, R.S. 2014, Pengaruh Jus Buah Pepaya (Carica papaya) terhadap Gambaran Histopatologik Pulmo Mencit (Mus musculus), Bioedukatika 2 (2)
Gull, Javaria . 2012.Variation in Antioxidant Attributes at Three Ripening Stages of Guava (Psidium guajava L.)Fruit from Different Geographical Regions of Pakistan.Molecules.ISSN 1420-3049.
Imam, D. & Juwono.2006. Pengaruh Pemberian Jus Buah Tomat (Lycopersicum
esculentum Mill) Terhadap Motilitas Spermatozoa MencitBalb/c Jantan yang Diberi
Paparan Asap Rokok. Karya Tulis Ilmiah. Fakultas Kedokteran Universitas Diponegoro, Semarang.
Khopkar, S.M. 1990. Konsep Dasar Kimia Analitik. Jakarta : UI Press.
Marianti, A, 2009, Aktivitas Antioksidan Jus Tomat pada Pencegahan Kerusakan Jaringan Paru-paru Mencit yang dipapar Asap Rokok, Biosaintifika, 1(1): 1-10
Nurliyana, R., Syed Zahir,I., Mustapha Suleiman, K., Aisyah, M.R. dan Kamarul Rahim, K. 2010. Antioxidant study of pulps and peels of dragon fruits: a comparative study. International Food Research Journal. 17: 367-375.
Prakash, Aruna, Fred Rigelhof, dan Eugene Miller. 2001. Antioxidant Activity Medallion Laboratories : Analithycal Progress. A publication of Medallion Labs : 1-4.