PRINSIP SINTESIS SENYAWA
ANALGETIK
Senyawa Analgetik: Asam Mefenamat, Parasetamol, dan
Asetosal.
Prinsip dasar Reaksi Sintesisnya adalah: Reaksi EAS, Reaksi
SEA (SUBTITUSI ELEKTROFILIK
AROMATIS)
Subtitusi Elektrofilik (SE) Aromatis
Subtitusi elektrofilik:
mengganti hidrogen pada cincin benzen
Mekanisme SE
Tahap 1 : Serangan E+ membentuk sigma kompleks
Tahap 2 : lepasnya proton pada sigma kompleks membentuk produk subtitusi
Membutuhkan E
+yang lebih kuat dibandingkan Br
2.
Gunakan katalis asam lewis kuat, FeBr
3.
+ FeBr3 Br Br Br Br FeBr3 + − − H CH+ Br H CH+ Br H C H + Br H
-complex with the positive charge, distributed only between
ortho- and para-positions
Br -Br
Br
Br -H+
Addition Substitution (aromaticity is restored) Proceeds through a -complex
FeBr3 Br2
Br
Klorinasi dan Iodinasi
Klorinasi serupa dengan brominasi. Katalis yang digunakan
AlCl
3.
Iodinasi membutuhkan agen pengoksidasi asam, seperti asam
nitat, yang akan mengoksidasi iodin menjadi ion I
+.
Nitrasi Benzen
Untuk membentuk elektrofil ion NO
2+digunakan
H
2SO
4dengan HNO
3.
H O N O O H O S O H O O + HSO4 _ H O N O H O + H O N O H O + H2O + N O O + Elektrofil E+Mekanisme
+
H2SO4 H CH+ O2N H CH+ O2N H C H + O2N HProceeds through a -complex HNO3 NO2+
+
H 2O HSO4-+
Nitronium-cation O2N -H+Gunakan SO
3dan asam sulfat berasap untuk menghasilkan
ion HSO
3+Mekanisme Sulfonasi
+
H2SO4 H CH+ HO3S H CH+ HO3S H C H + HO3S HProceeds through a -complex
SO3 HSO3+
+
HSO4-HO3S
Sintesis alkil benzen menggunakan alkil halida dan asam lewis, biasanya AlCl3.
Reaksi alkil halida dengan asam lewis akan menghasilkan karbokation yang berperan sebagai
elektrofil.
Sumber karbokation lain : alkena + HF atau alkohol+ BF3.
Elektrofil : Alkilasi Friedel-Crafts
CH3 CH CH3 Cl + AlCl3 CH3 C H3C H Cl AlCl3 + _ H2C CH CH3 HF H3C CH CH3 F + _ H3C CH CH3 OH BF3 H3C CH CH3 O H + BF3 H3C CH+ CH3 + HOBF3 _
C CH3 CH3 H + H H CH(CH3)2 + H H CH(CH3)2 B F F F OH CH CH3 CH3 + HF B F OH F +
-Mekanisme : Alkilasi Friedel-Crafts
Alkilasi Friedel-Crafts memiliki beberapa keterbatasan diantaranya adalah : Karbokation yang terbentuk mengalami penaatan ulang.
Produk alkil benzena lebih reakstif dibandingkan benzen sehingga dapat menyebabkan terjadinya polialkilasi.
Asil klorida digunakan untuk
menggantikan alkil klorida. R C O Cl AlCl3 R C O AlCl3 Cl + _ R C O AlCl3 Cl + _ AlCl4 + _ + R C O R C O + C O R + H C H O R + Cl AlCl3 _ C O R + HCl AlCl3
Mekanisme : Asilasi Friedel-Crafts
• Ion intermediet asilium distabilisasi oleh resonansi dan tidak mengalami penataan ulang seperti karbokation.
• Produk fenil keton bersifat kurang reaktif dibandingkan benzen, sehingga akan menghindari poliasilasi.
Asilasi Friedel-Crafts
Asilbenzen yang terbentuk dapat dikonversi menjadi alkil benzen melalui reaksi dengan HCl (aq) dan amalgam Zn.
+ CH3CH2C O Cl 1) AlCl3 2) H2O C O CH2CH3 Zn(Hg) aq. HCl CH2CH2CH3 Reduksi Clemmensen :
Formilasi Gatterman-Koch
Untuk menghasilkan benzaldehida digunakan reaksi yang lain.
Untuk menghasilkan formil klorida (merupakan senyawa yang tidak stabil) gunakan
campuran dalam tekanan tinggi dari CO, HCl, dan katalis.
CO + HCl H C O Cl AlCl3/CuCl H C O + AlCl4 _ C O H + C O H + HCl +
Subtituen Pengaktivasi
Gugus Fungsi :
Senyawa : Tidak punya PEB
Subtituen Pendeaktivasi
Subtituen Pendeaktivasi
Contoh reaksi SE pada
Benzen tersubtitusi
Nitrasi Toluena
Toluena bereaksi 25 kali lebih cepat dibanding benzen. Gugus metil berperan sebagai pengaktivasi.
Campuran produk mengandung molekul disubtitusi dengan posisi orto dan
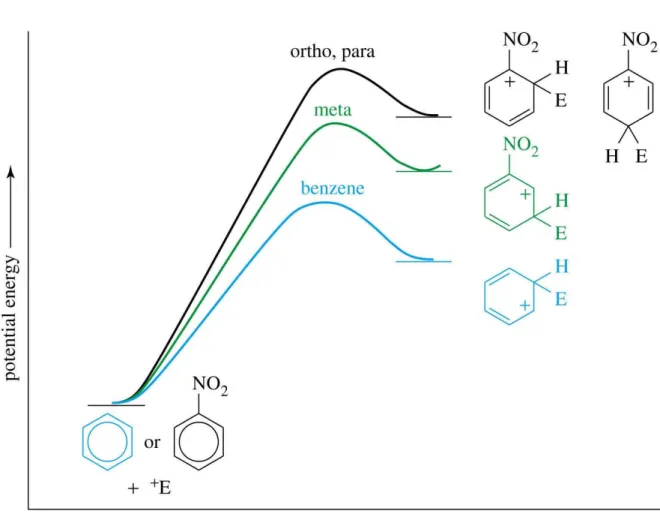
Nitrasi Toluena
Intermediat lebih stabil jika nitrasi
terjadi pada posisi orto atau para
Mekanisme dan Sigma kompleks
serangan pada posisi orto
serangan pada posisi meta serangan pada posisi para
3o lebih disukasi
Subtitusi Pada Nitrobenzen
• Nitrobenzen bereaksi 100.000 kali lebih lambat
dibanding benzen.
• Gugus metil berperan sebagai pendeaktivasi.
• Campuran produk mengandung molekul disubtitusi
dengan posisi meta lebih banyak.
• Subtituen pendeaktivasi mendeaktivasi pada semua
posisi, tetapi posisi meta kurang dideaktivasi.
Subtitusi Pada Nitrobenzen
Mekanisme dan Sigma
kompleks
serangan pada posisi orto
serangan pada posisi meta serangan pada posisi para
sangat tidak stabil
Subtitusi Pada Nitrobenzen
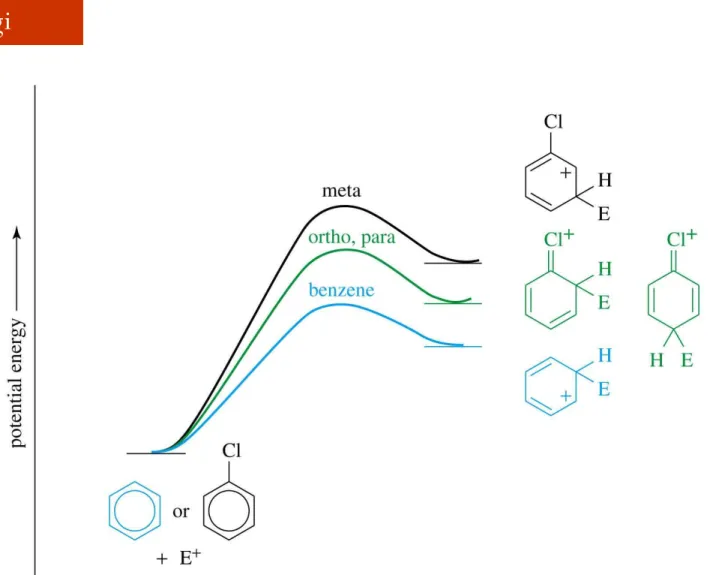
Halobenzen
Halogen mendeaktivasi pada SE tetapi akan mengarahkan subtituen pada
posisi orto, para.
Karena halogen sangat elektronegatif, mereka akan menarik kerapatan
elektron dari cincin secara induktif melalui ikatan sigma (mendeaktivasi).
Tetapi halogen memiliki PEB yang dapat menstabilkan sigma kompleks
melalui efek resonansi (mengarahkan pada orto-para).
Br E+ Br H E + (+) (+) (+) Para attack Meta attack Br E+ Br H H E + (+) (+)
Energy Diagram
Subtitusi Nukleofilik
Pada Benzen
Substitusi Nukleofilik Aromatis
Nukleofilik mengganti gugus pergi pada cincin aromatis.
Subtituen penarik elektron akan mengaktivasi cincin terhadap subtitusi
nukleofilik.
Mekanisme Subtitusi Nukleofilik
Tahap 1. Serangan Nu-(OH-) memberikan sigma yang distabilkan resonansi
Mekanisme Benzuna
Pereaksinya adalah halobenzena yang tidak memiliki gugus penarik
elektron pada cincin benzen.
Gunakan basa yang sangat kuat seperti NaNH2.
Intermediet Benzuna
CH3 H H H NH2 CH3 H H H NH2 _ or CH3 H H H NH2 CH3 H H H NH2 _ meta-toluidine para-toluidine Mekanisme reaksi :Sintesis p-nitroanilin dari
acetanilide
Prinsip
Substitusi elektrofilik pada aromatik (nitrasi) ion nitronium pada posisi para dari asetanilid.
Nitrasi dilakukan dengan menambahkan asam nitrat pekat dan asam sulfat pekat. Diteruskan dengan hidrolisis ion asetat dari gugus fungsi asetamido dengan
Tahap 1: Asetilasi Aniline
Tahap pertama kita perlu menghilangkan proteksi gugus asetil
pada Nitrogen di Anilin
Gugus asetil merupakan penarik elektron yang mengakibatkan
membuat pasangan elektron bebas pada nitrogen kurang reaktif
baik dalam reaksi oksidasi atau reaksi protonasi.
Asam nitrat yang digunakan dalam langkah nitrasi adalah agen
pengoksidasi yang cukup kuat dan kita dapat membentuk
N-oksida. Kondisi nitrasi (asam nitrat dan asam sulfat) sangat
asam.
Protonasi nitrogen pada anilin membuatnya menjadi kelompok
penonaktif yang sangat kuat, sehingga cincin aromatik kurang
rentan terhadap reaksi dengan agen nitrasi dan kelompok
Maka gugus pelindung acetyl adalah gugus besar dan secara
istimewa mengarahkan nitrasi kepada posisi para daripada
posisi orto.
Mekanisme reaksi dapat dilihat pada Gambar 14.2.
Anhidrida asetat terprotonasisebagian oleh asam asetat.
Hal ini membuat anhidrida menjadi elektrofil yang lebih baik
lagi untuk nitrogen nukleofilik pada anilin.