BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sampel
2.1.1 Kelor
Menurut Kasolo, dkk., (2011), sistematika tumbuhan kelor adalah sebagai berikut:
Kingdom : Plantae
Divisio : Magnoliophyta Kelas : Magnoliopsida Ordo : Brassicales Kelas : Moringaceae Genus : Moringa
Spesies : Moringa oleifera Lam
Kelor merupakan tanaman yang sangat cepat tumbuh, dapat bertahan dan terus menghasilkan ketika kering dan panas, juga tumbuh secara optimal pada lahan kering di seluruh bagian tropis. Selain itu, tanaman ini dapat tumbuh hingga 10 atau 12 m tingginya.. Tanaman ini batangnya berkayu, tegak, berwarna putih kotor, namun batang kayunya lunak atau mudah patah (Roloff, dkk., 2008).
Daun kelor merupakan daun majemuk dimana tangkai daunnya memiliki cabang kedua namun biasanya sampai percabangan ketiga yang memiliki panjang hingga 45 cm. Daun kelor memiliki panjang 1,2 hingga 2,0 cm dan lebar 0,6 hingga 1,0 cm. Bagian permukaan atas helai daun kelor berwarna hijau dan sedangkan bagian permukaan bawah berwarna lebih pucat, juga kedua permukaan halus. Daun kelor berbentuk bulat menyerupai telur, daunnya yang tipis dan lemas membentuk pangkal daun membulat dan ujung yang tumpul (Roloff, dkk., 2008).
2.1.2 Kandungan
Daun kelor yang telah dikarakterisasi diketahui mengandung kaya akan vitamin seperti tiamin dan riboflavin, mineral, asam amino, dan asam lemak. Sebagai tambahan, daun kelor diketahui mengandung berbagai macam senyawa antioksidan, seperti asam askorbat, flavonoid, fenol, dan karotenoid (Stosh dan Hartman, 2015). Menurut Fahey, (2005), daun kelor mengandung lebih banyak vitamin A dibanding wortel, lebih banyak zat besi dibanding bayam, lebih banyak kalium dibanding pisang, serta kualitas protein dari daun kelor dapat menyaingi susu dan telur, hal inilah salah satu alasan mengapa kelor dikatakan mengandung kaya akan nutrisi, sedangkan pada bijinya mengandung 19-47% minyak yang dikenal sebagai ben oil, yang kaya akan palmitat, stearat, dan asam oleat (Roloff, dkk., 2008).
2.1.3 Manfaat
2.2 Mineral
Mineral merupakan bagian tubuh dan memegang peran penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ, maupun fungsi tubuh secara berlainan. Mengonsumsi mineral terlalu sedikit maupun berlebihan dapat menyebabkan gangguan gizi. Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg per hari, sedangkan mineral mikro dibutuhkan tubuh dalam jumlah kurang dari 100 mg per hari (Almatsier, 2008).
Keseimbangan ion-ion mineral dalam tubuh mengatur proses metabolisme, mengatur keseimbangan asam basa, tekanan osmotik, membantu transpor senyawa-senyawa penting pembentuk membran, beberapa diantaranya adalah konstituen pembentuk jaringan tubuh. Secara tidak langsung, mineral banyak yang berperan dalam proses pertumbuhan. Peran mineral dalam tubuh kita berkaitan satu sama lainnya, dan kekurangan atau kelebihan salah satu mineral akan berpengaruh terhadap kerja mineral lainnya (Poedjiadi, 1994).
2.2.1 Mangan
terdapat di dalamnya sebab merupakan bagian dari klororfil, sedangkan daging, susu, ayam, dan makanan laut tidak banyak mengandung mangan (Linder, 1992). 2.2.2 Zink
Zink sebagai suplemen diketahui dapat memperpendek fase sekresi pada kasus diare dan memiliki efek yang besar dalam proses penyembuhan. Zink juga dikaitkan kritis kepada respon imun, ketidakcukupan asupan zink dapat ditandai dengan penurunan imun bahkan dapat sampai terjadi disfungsi imun, hal ini kadang ditandai dengan terjadinya kerusakan pada kulit dan diare. Kondisi seperti ini juga yang dialami pada kasus anak-anak dengan kasus malnutrisi. Namun perlu ditegaskan karena zink adalah nutrisi yang terbatas maka apabila konsumsi zink berlebih akan terjadi interfensi pada metabolisme copper atau tembaga (Golden, 2009).
Zink juga telibat dalam metabolisme vitamin A, dimana mineral ini berikatan dengan suatu enzim yang disebut enzim dihidrogenase untuk metabolismenya. Juga zink diperlukan dalam sintesis ptotein pengikat retinol di dalam hati. Salah satu sumber terbesar zink adalah pada biji-bijian dan sayuran berserat tinggi (Linder, 1992).
2.3 Spektrofotometri Serapan Atom
kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaannya relatif sederhana. Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar oleh atom-atom netral, dan sinar yang diserap biasanya sinar tampak atau sinar ultraviolet (Gandjar dan Rohman, 2008).
Secara garis besar prinsip sepektrofotometri serapan atom ini sama saja dengan spektrofotometri sinar tampak dan ultraviolet. Perbedaannya terletak pada bentuk spektrum, cara pengerjaan sampel dan peralatannya. Metode spektrofotometri serapan atom ini mendasarkan pada prinsip absorbsi cahaya oleh atom. Atom-atom akan menyerap cahaya pada panjang gelombang tertentu, tergantung pada sifat unsurnya (Gandjar dan Rohman, 2008).
Jika suatu larutan yang mengandung suatu garam logam (atau suatu senyawa logam) dialirkan ke dalam suatu nyala maka terbentuklah uap yang mengandung atom-atom logam itu. Atom logam dalam bentuk gas tersebut tetap berada pada keadaan tidak tereksitasi atau dalam kondisi dasar. Jika cahaya dengan panjang gelombang yang khas dengan logam tersebut dilewatkan pada nyala yang mengandung atom yang bersangkutan, maka sebagian cahaya tersebut akan diserap dan penyerapan tersebut menyebabkan elektron tereksitasi ke tingkat yang lebih tinggi. Inilah asas yang mendasari spektrofotometri serapan atom (Gandjar dan Rohman, 2008).
Teknik ini digunakan untuk menetapkan kadar ion logam dan mineral tertentu dengan jalan mengukur intensitas emisi atau serapan cahaya pada panjang gelombang tertentu oleh uap atom unsur yang ditimbulkan dari bahan, misalnya dengan mengalirkan larutan zat ke dalam api (Ditjen POM, 1995).
nyala. Menurut Basset, dkk., (1994), peristiwa yang terjadi secara singkat setelah sampel dimasukkan ke dalam nyala adalah:
1. Penguapan pelarut yang meninggalkan residu
2. Penguapan zat padat dengan dissosiasi menjadi atom-atom penyusunnya, yang mula-mula akan berada dalam keadaan dasar.
3. Beberapa atom dapat tereksitasi oleh energi panas nyala ke tingkatan -tingkatan energi yang lebih tinggi, dan mencapai kondisi dimana atom tersebut akan memancarkan energi.
2.3.1 Instrumentasi Spektrofotometri Serapan Atom
Instrumen spektrofotometri serapan atom meliputi berikut: 1. Sumber Sinar
Sumber sinar yang diapaki adalah lampu katoda berongga (hollow cathode lamp). Lampu katoda ini terdiri ata tabung kaca tertutup yang mengandung katoda dan anoda. Katoda sendiri berbentuk silinder berongga yang terbuat dari logam atau dilapisi dengan logam tertentu yang akan dianalisis (Gandjar dan Rohman, 2008).
2. Tempat Sampel
Sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan azas. Ada berbagai macam alat yang digunakan untuk mengubah sampel menjadi uap atom-atomnya yaitu:
a. Dengan nyala (Flame)
pengoksidasi (Gandjar dan Rohman, 2008). Beberapa temperatur nyala yang lain dapat dilihat pada Tabel 2.1
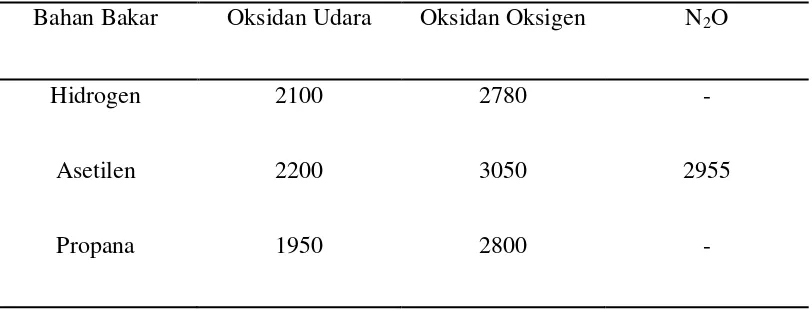
Tabel 2.1 Temperatur Nyala
Bahan Bakar Oksidan Udara Oksidan Oksigen N2O
Hidrogen 2100 2780 -
Asetilen 2200 3050 2955
Propana 1950 2800 -
Sumber: Khopkar (1985). b. Tanpa nyala
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil sedikit (hanya beberapa µl), lalu diletakkan dalam tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu katoda sehingga terjadilah proses penyerapan energi sinar yang memenuhi kaidah kuantitatif (Gandjar dan Rohman, 2008).
3. Monokromator
4. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman (Gandjar dan Rohman, 2008).
5. Amplifier
Amplifier merupakan suatu alat untuk memperkuat signal yang diterima dari detektor sehingga dapat dibaca sebagai alat pencari hasil (Readout) (Gandjar dan Rohman, 2008).
6. Readout
Readout merupakan suatu alat penunjuk atau juga diartikan sebagai pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang menggambarkan absorbansi atau intensitas emisi.
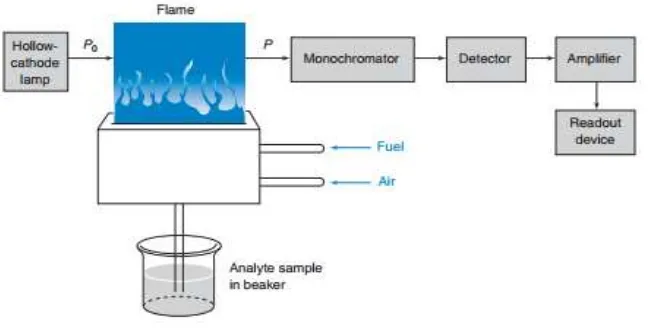
Fungsi nyala adalah untuk memproduksi atom-atom yang dapat mengabsorpsi radiasi yang dipancarkan oleh lampu katoda tabung. Pada umumnya, peralatan yang digunakan untuk mengalirkan sampel menuju nyala adalah nebulizer yang dihubungkan dengan pembakar (burner). Sebelum menuju nyala, sampel mengalir melalui pipa kapiler dan menghasilkan aerosol oleh aliran gas pengoksidasi. Kemudian, aerosol yang terbentuk bercampur dengan bahan bakar menuju burner. Sampel yang menuju burner hanya sekitar 5-10% sedangkan sisanya (90-95%) menuju tempat pembuangan. Sampel yang berada pada nyala lalu diatomisasi dan cahaya dari lampu katoda tabung dilewatkan melalui nyala. Sampel yang berada pada nyala akan menyerap cahaya tersebut (Gandjar dan Rohman, 2008).
Gambar 2.1 Sistem Peralatan Spektrofotometri Serapan Atom (Sumber: Harris, 2007)
2.3.2 Gangguan-gangguan pada Spektrofotometri Serapan Atom
Gangguan-gangguan (interference) pada SSA adalah peristiwa yang menyebebkan pembacaan absorbansi unsur yang dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya dalam sampel. Gangguan-gangguan yang dapat terjadi pada SSA adalah sebagai berikut:
1. Gangguan oleh penyerapan non-atomik (non-atomic absortion)
Gangguan ini terjadi akbat penyerapan cahaya dari sumber sinar yang bukan berasal dari atom - atom yang dianalisis. Penyerapan non - atomik dapat disebabkan adanya penyerapan cahaya-cahaya oleh partikel-partikel pengganggu yang berada di dalam nyala. Cara mengatasi penyerapan non - atomik ini adalah kerja pada panjang gelombang yang lebih besar atau pada suhu yang lebih tinggi (Gandjar dan Rohman, 2008).
a. Dissosiasi senyawa - senyawa yang tidak sempurna
Dissosiasi ini disebabkan oleh terbentuknya senyawa refraktorik (sukar diuraikan dalam api), sehingga akan mengurangi jumlah atom netral yang ada di dalam nyala.
b. Ionisasi atom - atom dalam nyala
Ionisasi terjadi akibat suhu yang digunakan terlalu tinggi. Prinsip dengan spektrofotometri serapan atom adalah mengukur absorbansi atom-atom netral yang berada dalam keadaan asas. Jika terbentuk ion maka akan mengganggu pengukuran absorbansi atom netral karena spektrum absorbansi atom-atom yang mengalami ionisasi tidak sama dengan spektrum atom dalam keadaan netral.
c. Gangguan spektrum
Gangguan spektrum dalam spektrofotometri serapan atom timbul akibat terjadinya tumpang tindih antara frekuensi-frekuensi garis resonansi unsur yang dianalisis dengan garis-garis yang dipancarkan oleh unsur lain. Hal ini disebabkan karena rendahnya resolusi monokromator pada spektrofotometri serapan atom (Gandjar dan Rohman, 2008).
d. Gangguan yang berasal dari matriks sampel yang dapat mempengaruhi banyaknya sampel yang mencapai nyala.
Sifat-sifat matriks sampel yang dapat mengganggu analisis adalah yang mempengaruhi laju aliran bahan bakar/gas pengoksidasi. Sifat-sifat tersebut adalah viskositas dan berat jenis (Gandjar dan Rohman, 2008).
2.4 Validasi Metode Analisis
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis menurut Harmita, (2004) adalah sebagai berikut:
1. Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan dengan dua cara, yaitu:
a. Metode simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya).
b. Metode penambahan baku
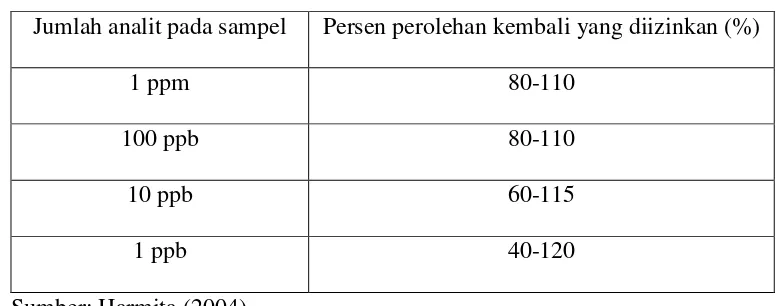
Tabel 2.2 Rentang Persen Perolehan Kembali yang Diizinkan pada Analit Sampel
Jumlah analit pada sampel Persen perolehan kembali yang diizinkan (%)
1 ppm 80-110
100 ppb 80-110
10 ppb 60-115
1 ppb 40-120
Sumber: Harmita (2004) 2. Keseksamaan (precision)
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan.
3 Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang ada di dalam sampel.
4 Linearitas dan Rentang
dapat ditetapkan secara cermat, seksama dan dalam linearitas yang dapat diterima. Menurut Gandjar dan Rohman (2008), linearitas suatu metode merupakan ukuran seberapa baik kurva kalibrasi yang menghubungkan antara respon (Y) dengan konsentrasi (X).
5 Batas Deteksi dan Batas Kuantitasi