Nisbah Bobot Karbon Aktif Ampas Teh dan Sabut Kelapa Teroksidasi sebagai Adsorben Mn (II) dan Zn(II) dalam Limbah Cair Laboratorium Kimia
Weight Ratio of Tea Waste Activated Carbon and Oxidized Coconut Coir Pith as Adsorbent for Mn (II) and Zn (II) on Chemistry Laboratory Waste Water
Oleh : Fitri Nugrahani
652012007
TUGAS AKHIR
Diajukan kepada Program Studi Kimia, Fakultas Sains dan Matematika guna memenuhi sebagian dari persyaratan untuk mencapai gelar Sarjana Sains
Program Studi Kimia Fakultas Sains dan Matematika Universitas Kristen Satya Wacana
Salatiga 2016
ii
Nisbah Bobot Karbon Aktif Ampas Teh dan Sabut Kelapa Teroksidasi sebagai Adsorben Mn (II) dan Zn(II) dalam Limbah Cair Laboratorium Kimia
Weight Ratio of Tea Waste Activated Carbon and Oxidized Coconut Coir Pith as Adsorbent for Mn (II) and Zn (II) on Chemistry Laboratory Waste Water
Oleh Fitri Nugrahani NIM : 652012007
TUGAS AKHIR
Diajukan kepada Program Studi Kimia, Fakultas Sains dan Matematika guna memenuhi sebagian dari persyaratan untuk mencapai gelar Sarjana Sains
Disetujui oleh,
FAKULTAS SAINS DAN MATEMATIKA UNIVERSITAS KRISTEN SATYA WACANA
SALATIGA 2016
Pembimbing Pendamping
Dr. rer. nat. A. Ign. Kristijanto, MS Pembimbing Utama
Ir. Sri Hartini. M. Sc
Disahkan oleh, Dekan
Dr. Suryasatriya Trihandaru., M.Sc. nat Diketahui oleh,
Kaprogdi
iii
PERNYATAAN KEASLIAN KARYA TULIS TUGAS AKHIR
Yang bertanda tangan dibawah ini, Nama : Fitri Nugrahani
NIM : 652012007
Program Studi : Kimia
Fakultas : Sains dan Matematika Universitas Kristen Satya Wacana Menyatakan dengan sesungguhnya bahwa tugas akhir, judul :
Nisbah Bobot Karbon Aktif Ampas Teh dan Sabut Kelapa Teroksidasi Sebagai Adsorben Mn (II) dan Zn (II) dalam Limbah Cair Laboratorium Kimia
Yang dibimbing oleh : 1. Ir. Sri Hartini, M.Sc
2. Dr. rer. nat. A. Ign. Kristijanto, MS Adalah benar – benar hasil karya saya.
Di dalam laporan tugas akhir ini tidak terdapat keseluruhan atau sebagian tulisan atau gagasan orang lain yang saya ambil dengan cara menyalin atau meniru dalam bentuk rangkaian kalimat atau gambar serta symbol yang saya aku seolah – olah sebagai karya saya sendiri tanpa memberikan pengakuan pada penulis atau sumber aslinya.
Salatiga, 20 September 2016 Yang memberi pernyataan,
iv
PERNYATAAN PERSETUJUAN PUBLIKASI TUGAS AKHIR UNTUK KEPENTINGAN AKADEMIS
Sebagai civitas akademika Universitas Kristen Satya Wacana (UKSW), saya yang bertanda tangan dibawah ini :
Nama : Fitri Nugrahani
NIM : 652012007
Program Studi : Kimia
Fakultas : Sains dan Matematika Jenis Karya : Skripsi
demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada UKSW hak bebas royalty non – eksklusif (non – exclusive royalty free right) atas karya ilmiah saya berjudul :
Nisbah Bobot Karbon Aktif Ampas Teh dan Sabut Kelapa Teroksidasi Sebagai Adsorben Mn (II) dan Zn (II) dalam Limbah Cair Laboratorium Kimia
Beserta perangkat yang ada (jika perlu).
Dengan hak bebas royalty non – eksklusif ini, UKSW berhak menyimpan, mengalihmedia / mengalihformatkan, mengolah dalam bentuk pangkalan data, merawat, dan mempublikasikan tugas akhir saya, selama tetap menuliskan nama saya sebagai penulis / pencipta.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di : Salatiga Tanggal : 20 September 2016 Mengetahui, Yang menyatakan Fitri Nugrahani Pembimbing Pendamping
Dr. rer. nat. A. Ign. Kristijanto, MS Pembimbing Utama
v DAFTAR ISI
Halaman
HALAMAN JUDUL... i
HALAMAN PENGESAHAN... ii
PERNYATAAN KEASLIAN KARYA TULIS TUGAS AKHIR... iii
PERNYATAAN PERSETUJUAN PUBLIKASI TUGAS AKHIR UNTUK KEPENTINGAN AKADEMIS... iv DAFTAR ISI... v DAFTAR TABEL... vi ABSTRACT... 1 1. PENDAHULUAN... 2 2. METODE PENELITIAN... 3
2.1. Waktu dan Tempat Penelitian... 3
2.2. Bahan dan Piranti... 3
2.3. Metode... 3
2.3.1. Karakterisasi Limbah Cair Laboratorium Kimia... 3
2.3.2. Preparasi Karbon Aktif Ampas Teh... 3
2.3.3. Preparasi Sabut Kelapa Teroksidasi... 4
2.3.4. Pemberian Perlakuan... 4
2.3.5. Pengukuran Parameter Fisiko-Kimiawi... 4
2.3.6. Isoterm Adsorpsi... 5
2.4. Analisis Data... 6
3. HASIL DAN PEMBAHASAN... 6
3.1. Karakterisasi Awal Parameter Fisiko Kimiawi... 6
3.2. Efektivitas Pengolahan Limbah Cair Laboratorium Kimia dengan Berbagai Penambahan Bobot Karbon Aktif Ampas Teh (g) dalam Waktu Kontak 240 menit... 9
3.3. Rataan Kandungan Parameter Fisko-Kimiawi Limbah Cair Laboratorium Kimia Antar Penambahan Berbagai Bobot Sabut Kelapa Teroksidasi dalam Waktu Kontak 240 menit – 510 menit... 11
3.4. Efektivitas Pengolahan Limbah Cair Laboratorium Kimia Antar Penambahan Berbagai Bobot Sabut Kelapa Teroksidasi dalam Waktu Kontak 240 menit – 510 menit... 13
3.5. Isoterm Adsorpsi Parameter Fisioko-Kimiawi Limbah Cair Laboratorium Kimia dengan Menggunakan Karbon Aktif Ampas Teh dan Sabut Kelapa Teroksidasi dalam Waktu Kontak 510 menit... 14
4. KESIMPULAN... 17
5. SARAN... 18
vi DAFTAR TABEL
Tabel Halaman
1. Parameter Limbah Cair Laboratorium dengan Metode/Piranti Penelitian.. 4 2. Karakteristik Awal Parameter Fisiko-Kimiawi Limbah Cair
Laboratorium Kimia... 7 3. Rataan Kandungan Parameter Fisiko-Kimiawi ( ± SE) Limbah Cair
Laboratorium Kimia Berbagai Penambahan Bobot Karbon Aktif Ampas Teh dalam Waktu Kontak 240 menit... 8 4. Efektivitas (%) Berbagai Bobot Karbon Aktif Ampas Teh (KAAT)
dalam Pengolahan Limbah Cair Laboratorium Kimia dalam Waktu Kontak 240 menit... 10 5. Rataan Kandungan Parameter Fisiko-Kimiawi ( ± SE) Limbah Cair
Laboratorium Kimia Antar Penambahan Berbagai Bobot Sabut Kelapa Teroksidasi dalam Waktu Kontak 240 - 510 menit... 12 6. Efektivitas (%) Berbagai Bobot Sabut Kelapa Teroksidasi (SKT) dalam
Pengolahan Limbah Cair Laboratorium Kimia dalam Waktu Kontak 240 - 510 menit... 14 7. Isoterm Adsorpsi Langmuir dan Freundlich Parameter Fisiko – Kimiawi
Limbah Cair Laboratorium Kimia Menggunakan Karbon Aktif Ampas Teh (KAAT) dan Sabut Kelapa Teroksidasi (SKT)... 15
1
Nisbah Bobot Karbon Aktif Ampas Teh dan Sabut Kelapa Teroksidasi sebagai Adsorben Mn (II) dan Zn(II) dalam Limbah Cair Laboratorium Kimia
Weight Ratio of Tea Waste Activated Carbon and Oxidized Coconut Coir Pith as Adsorbent for Mn (II) and Zn (II) on Chemistry Laboratory Waste Water
Fitri Nugrahani*, Sri Hartini**, dan A.Ign.Kristijanto** *Mahasiswa Program Studi Kimia Fakultas Sains dan Matematika
**Dosen Program Studi Kimia Fakultas Sains dan Matematika Universitas Kristen Satya Wacana, Salatiga
Jln. Diponegoro no 52-60 Salatiga 50711 Jawa Tengah- Indonesia 652012007@student.uksw.edu
Abstract
The objectives of this study are: Firstly, to determine the effectivity of weight ratio of tea waste activated carbon and oxidized coconut coir pith on the decreasing physico-chemical parameters of waste water from Chemistry Laboratory. Second, to determine the isotherm adsorption of weight ratio of tea waste activated carbon and oxidized coconut coir pith. Data were analyzed using Randomized Completely Block Design (RCBD), 5 treatments and 5 replications, and as the block is the time of analysis. As the treatments arethe variations of weight ratio of tea waste activated carbon and oxidized coconut coir pith (gram/gram) which are: (1.25:0); (2.5:10); (3.75:20); (5:30); and (6.25:40), respectively. The treatment of its adsorbent were given separately and both of it is threated with stirring. To test the difference between treatmentmeans, Honestly Significant Differences (HSD) with 5% level of significance were used.
The study showed the following result : In period of 240 minutes, giving of tea waste activated carbon in amount of 1.25 gram effective for COD, while for Mn(II) is 3.75 gram; and 5 gram for Zn (II), respectively. The effectivity of tea waste activated carbon in period of 240 minutes is in the range of 75.29 % (Zn(II)) until 99.27 % (COD). Furthermore, the oxidized coconut coir pith treatment in period of the next 270 minutes give the following result: 10 gram of oxidized coconut coir pith is effective for COD, 20 gram for Mn(II), and 30 gram Zn(II), respectively. The effectivity of oxidized coconut coir pith in period of the next 270 minutes is in the range of 3.71 % (COD) until 48.35 % (Zn(II)).
The maximum adsorption capacity of tea waste activated carbon in period of 240 minutes on giving 1.25 gram for COD = 2,500 mg/g following Langmuir isotherm models; 3.75 gram for Mn (II) = 2.500 mg/g following Freundlich isotherm models; and 5 gram for Zn (II) = 0.807 mg/g following Langmuir isotherm models. While the adsorption capacity of oxidized coconut coir pith in period of the next 270 minutes on giving 10 gram for COD= 1.04×1023 mg/g following Freundlich isotherm models; 20 gram for Mn (II) = 0,0021 mg/g following Langmuir isotherm models; and 30 gram for Zn (II) = 0,1341 mg/g following Freundlich isotherm models.
Key word: tea waste activated carbon, oxidized coconut coir, waste water, isotherm adsorption
2 1. PENDAHULUAN
Meningkatnya kegiatan penelitian telah mengarah pada peningkatan pembuangan limbah kimia dalam lingkungan. Limbah kimia mengandung logam berat dan diklasifikasikan sebagai limbah berbahaya yang tidak dapat dihilangkan dengan perlakuan fisik dan kimia (Lou & Chang (2007) dalam Arbanah et al., 2013). Hasil karakterisasi limbah cair Laboratorium Kimia UKSW mengandung logam berat antara lain Cu, Fe, Cr, Mn, Al, Zn, Pb, Cd, Ni, Hg, dan As sehingga perlu dilakukan upaya pengolahan supaya tidak mencemari lingkungan. Penghilangan kandungan logam berat biasanya dilakukan melalui proses fisik dan kimiawi maupun pembakaran sebelum dibuang ke sungai. Proses tersebut meliputi proses pengendapan kimiawi, elektrokimia, reverse osmosis, dan pertukaran ion. Proses pengolahan tersebut memiliki kekurangan yaitu menghasilkan lumpur beracun yang memerlukan proses pengolahan yang lebih khusus dan memerlukan biaya yang tinggi (Arbanah et al., 2013). Pada tahun 1990-an, biosorpsi dikembangkan untuk perolehan kembali (recovery) logam berat. Laporan pertama melaporkan bahwa materi biologi yang berlimpah seperti teh, sekam, sabut kelapa dan kopi dapat digunakan untuk menghilangkan kandungan logam berat dalam limbah dengan harga yang terjangkau (Volesk (1990) dalam Okafor et al., 2012).
Sabut kelapa yang keberadaannya sangat melimpah dapat dimanfaatkan sebagai adsorben untuk menghilangkan ion logam dari air limbah (Okafor et al., 2012). Kemampuan untuk mengadsorbsi dan pertukaran ion logam berat karena adanya gugus karboksil, fenol, hidroksi siano, dan lain sebagainya ( Abia et al. (2002) dalam Israel & Eduok, 2012). Lignin dan selulosa dalam sabut memiliki sifat serap/pertukaran ion, struktur berpori sabut kelapa tersebut memungkinkan untuk menjerap sejumlah besar air (Okafor et al., 2012). Sabut kelapa yang dimodifikasi dengan cara dioksidasi terbukti memiliki efektivitas lebih besar (75,71%) dibandingkan sabut kelapa tanpa dioksidasi yaitu 29,44% dalam menjerap Cu (II) (Shukla et al., 2009).
Ampas teh juga berpotensi sebagai adsorben yang efektif untuk menghilangkan kandungan logam berat dalam limbah karena strukturnya yang berpori dengan luas permukaan yang besar. Dinding sel teh terdiri dari selulosa dan hemi selulosa, lignin, tanin terkondensasi dan protein struktural sehingga limbah teh
3
memiliki potensi yang baik sebagai penjerap logam dari larutan dan air limbah (Hu &Srinivasan (1999) dalam Wankhade & Ganvir, 2013). Ampas teh juga dapat digunakan sebagai perkursor karbon aktif. Banyak penelitian yang telah membuktikan bahwa karbon aktif ampas teh mampu menjerap pewarna sintetis (Gao et al., 2013), logam berat (Duran et al., 2011) serta digunakan dalam pemurnian biodisel (Fadhil et al., 2012).
Berdasarkan latar belakang di atas maka tujuan dari penelitian ini adalah:
1. Menentukan nisbah bobot karbon aktif ampas teh dan sabut kelapa teroksidasi yang optimal dan kapasitas penjerapan maksimal dalam menjerap Mn(II) dan Zn(II).
2. Menentukan model isotherm adsorpsi nisbah karbon aktif ampas teh dan sabut kelapa teroksidasi.
2. METODE PENELITIAN 2.1. Waktu dan Tempat Penelitian
Penelitian dilakukan di Laboratorium Kimia Lingkungan, Fakultas Sains dan Matematika, Universitas Kristen Satya Wacana dari bulan Februari – Juni 2016.
2.2. Bahan dan Piranti
Ampas teh diperoleh dari salah satu kedai minuman di kampus UKSW dan sabut kelapa diperoleh dari Pasar Raya I, Salatiga. Limbah cair diperoleh dari Laboratorium Kimia Fakultas Sains dan Matematika UKSW. Bahan kimia ini yang digunakan antara lain akuades, H2O2, K2CO3, NaOH, K2Cr2O7, Ag2SO4, H2SO4, HgSO4, Ferrous
Amonium Sulfat, indikator ferroin, Buffer Citrate, Sodium Periodate dan Zincover 5. Piranti yang digunakan antara lain refluks, Spektrofotometer HACH DR/EL 2000, pH meter HANNA Instrument 9812, dan Neraca Analitis (Mettler H80).
2.3. Metode
2.3.1. Karakterisasi Limbah Cair Laboratorium Kimia
Limbah cair Laboratorium Kimia yang belum diolah dikarakterisasi terlebih dahulu untuk mengetahui parameter fisiko-kimiawi termasuk kandungan logam berat sebelum diberi perlakuan dengan adsorben.
2.3.2. Preparasi Karbon Aktif Ampas Teh (Gurten et al. (2012) yang dimodifikasi) Ampas teh dimasukkan dalam larutan K2CO3 5 M dengan perbandingan ampas
4
bersuhu 110 ˚C selama 24 jam, setelah itu dimasukkan ke dalam furnace bersuhu 400 ˚C selama 10 menit.
2.3.3. Preparasi Sabut Kelapa Teroksidasi (Shukla et al., 2006)
Sabut kelapa direndam dengan H2O2 dan NaOH dengan perbandingan massa
100 : 15 : 1 dalam 2 liter akuades, kemudian dipanaskan dalam waterbath bersuhu 85 ˚C selama 2 jam. Setelah itu disaring dan dibilas dengan air panas, lalu dibilas kembali dengan air dingin dan kemudian dikeringkan dalam oven bersuhu 50 ˚C.
2.3.4. Pemberian Perlakuan
Lima gelas beaker ukuran 1 L masing-masing diisi dengan air limbah sebanyak 1 L. Selanjutnya diberi nisbah bobot adsorben karbon aktif ampas teh sebanyak 1,25; 2,5; 3,75; 5; dan 6,25 gram selama 240 menit dengan diaduk menggunakan Jar Test, setelah 240 menit dilanjutkan dengan penambahan sabut kelapa teroksidasi dengan bobot 0, 10, 20, 30, dan 40 gram dan diaduk kembali menggunakan Jar Test selama 270 menit.
2.3.5. Pengukuran Parameter Fisiko-Kimiawi
Perubahan-perubahan yang terjadi selama perlakuan dapat diketahui dengan melakukan beberapa analisa terhadap parameter fisika dan kimia (Tabel 1).
Tabel 1. Parameter – Parameter Limbah Cair Laboratorium dengan Metode/Piranti Penelitian
Parameter Metoda/Piranti
Fisikawi
TDS (Total Dissolved Solids) (ppm) TDS meter (HANNA Instrument 9812)
TSS (Total Suspended Solid) (mg/l) Spektrofotometer HACH DR/EL 2000 Kimiawi
pH pH meter (HANNA Instrument 9812)
COD (Chemical Oxygen Demand) (mg/L)
Titrimetrik (Alaerts dan Santika, 1987)
Mn (II) (mg/L) HACH DR/EL 2000-Spektrofotometer Zn (II) (mg/L) HACH DR/EL 2000-Spektrofotometer
5
2.3.6. Isoterm Adsorpsi
Untuk menjelaskan isoterm adsorpsi, digunakan 2 isoterm yaitu Langmuir dan Freundlich. Langmuir mendefinisikan bahwa kapasitas adsorpsi maksimum terjadi dengan pembentukan lapisan tunggal (monolayer) dengan persamaan isoterm adsorpsi Langmuir adalah sebagai berikut : (Suseno, 2012)
Keterangan :
Ceq (mg/L) : Konsentrasi akhir parameter fisiko-kimiawi saat kesetimbangan
qeq (mg/g) : Massa parameter yang diserap gram adsorben
: Massa parameter pada saat 1 gram adsorben yang dapat menjerap secara sempurna
b : Konstanta isoterm untuk penjerapan partikel adsorben
Nilai b dan diperoleh dengan membuat grafik hubungan antara Ceq/qeq versus Ceq.
Dari persamaan Langmuir berdasarkan nilai faktor pemisahan (RL) dapat
diindikasikan tipe dari isoterm Langmuir yaitu: RL = 0 menunjukkan tipe irreversible; 0
< RL < 1 menunjukkan tipe favourable; RL = 1 menunjukkan tipe linier, dan RL > 1
menunjukkan tipe unfavourable. Nilai RL dapat dihitung dengan persamaan sebagai
berikut: (Senthilkumar, 2011 dalam Putra, 2014)
Keterangan :
RL : Nilai Faktor Pemisahan
KL : Konstanta Langmuir
Co : Konsentrasi Awal Logam
Freundlich mengasumsikan bahwa terdapat lebih dari satu lapisan permukaan (multilayer), dan persamaan isoterm adsorpsi Freundlich adalah sebagai berikut : (Suseno, 2012)
6
Keterangan :
qeq : Jumlah adsorbat terjerap per satuan bobot adsorben
Ceq (mg/L) : Konsentrasi akhir parameter fisiko-kimiawi saat kesetimbangan
n : Konstanta empiris Freundlich Kf : Kapasitas adsorpsi (mg/g)
Nilai Kf dan n diperoleh dengan membuat grafik hubungan antara log qeq vs log Ceq.
Selain dengan menelaah R2 untuk masing-masing model maka penentuan model isotherm adsorpsi yang tepat dapat ditentukan dengan melihat besarnya simpangan baku (SD) dari rataan nilai kapasitas adsorpsi dengan rata-rata pada setiap ulangan. Nilai simpangan baku yang lebih kecil menunjukkan persamaan isotherm adsorpsi yang lebih sesuai (Mulyatna dkk., 2003).
2.4. Analisis Data
Data hasil penelitian dianalisis dengan Rancangan Acak Kelompok dengan 5 perlakuan dan 5 kali ulangan. Sebagai perlakuan adalah variasi nisbah bobot karbon aktif ampas teh dan sabut kelapa teroksidasi (gram/gram) yaitu 1,25:0 ; 2,5:10 ; 3,75:20 ; 5:30 dan 6,25:40, sedangkan sebagai kelompok adalah waktu analisis. Pengujian purata antar perlakuan digunakan uji Beda Nyata Jujur (BNJ) dengan tingkat kebermaknaan 5% (Steel and Torie, 1981).
3. HASIL DAN PEMBAHASAN
3.1. Karakterisasi Awal Parameter Fisiko Kimiawi Limbah Cair Laboratorium Kimia
Hasil karakterisasi awal air limbah Laboratorium Kimia, Fakultas Sains dan Matematika, Universitas Kristen Satya Wacana sebelum diberi perlakuan disajikan pada Tabel 2.
7
Tabel 2. Karakteristik Awal Parameter Fisiko-Kimiawi Limbah Cair Laboratorium Kimia
Parameter Awal Baku Mutu *Keterangan
FISIKAWI TDS (ppm) 1.242 2.000 M TSS (mg/L) 8,2 100 M KIMIAWI pH 2,3 6 - 9 TM COD (mg/L) 11.136 100 TM Mn(II) (mg/L) 10,03 2 TM Zn (II) (mg/L) 10,06 5 TM Keterangan :
M = Memenuhi ; TM = Tidak Memenuhi
* Baku Mutu sesuai Peraturan Daerah Provinsi Jawa Tengah No. 5 Tahun 2012 tentang Baku Mutu Limbah Cair yang belum ditentukan Baku Mutunya.
Dari Tabel 2 terlihat bahwa TDS dan TSS sudah memenuhi baku mutu sebelum diberi perlakuan, sedangkan untuk parameter pH, COD, Mn dan Zn belum memenuhi baku mutu. Agar limbah cair Laboratorium Kimia memenuhi baku mutu maka perlu diolah terlebih dahulu dan dalam penelitian ini digunakan berbagai nisbah adsorben karbon aktif ampas teh dan sabut kelapa teroksidasi yaitu : 1,25:0 ; 2,5:10 ; 3,75:20 ; 5:30 dan 6,25:40 (gram/gram). Perlakuan diberikan secara terpisah dengan pengadukan yaitu karbon aktif ampas teh diberikan terlebih dahulu sesuai bobotnya selama 240 menit selanjutnya setelah 240 menit diberikan sabut kelapa teroksidasi sesuai nisbah bobotnya. Kandungan parameter fisiko-kimiawi yaitu TDS, TSS, pH, COD, Mn dan Zn dalam waktu 240 menit disajikan dalam Tabel 3 (dan Lampiran 1).
8
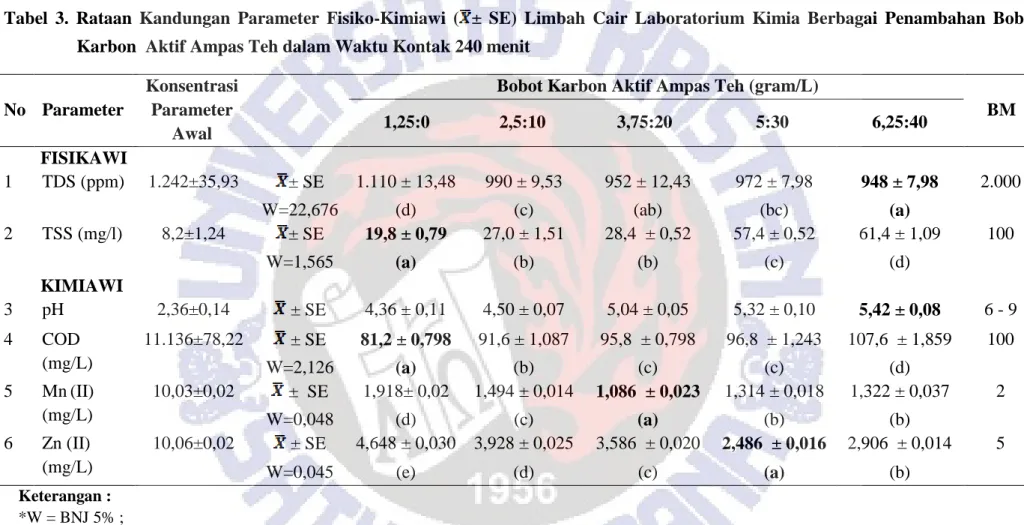
Tabel 3. Rataan Kandungan Parameter Fisiko-Kimiawi ( ± SE) Limbah Cair Laboratorium Kimia Berbagai Penambahan Bobot Karbon Aktif Ampas Teh dalam Waktu Kontak 240 menit
No Parameter
Konsentrasi Parameter
Awal
Bobot Karbon Aktif Ampas Teh (gram/L)
BM 1,25:0 2,5:10 3,75:20 5:30 6,25:40 FISIKAWI 1 TDS (ppm) 1.242±35,93 ± SE 1.110 ± 13,48 990 ± 9,53 952 ± 12,43 972 ± 7,98 948 ± 7,98 2.000 W=22,676 (d) (c) (ab) (bc) (a) 2 TSS (mg/l) 8,2±1,24 ± SE 19,8 ± 0,79 27,0 ± 1,51 28,4 ± 0,52 57,4 ± 0,52 61,4 ± 1,09 100 W=1,565 (a) (b) (b) (c) (d) KIMIAWI 3 pH 2,36±0,14 ± SE 4,36 ± 0,11 4,50 ± 0,07 5,04 ± 0,05 5,32 ± 0,10 5,42 ± 0,08 6 - 9 4 COD (mg/L) 11.136±78,22 ± SE 81,2 ± 0,798 91,6 ± 1,087 95,8 ± 0,798 96,8 ± 1,243 107,6 ± 1,859 100 W=2,126 (a) (b) (c) (c) (d) 5 Mn(II) (mg/L) 10,03±0,02 ± SE 1,918± 0,02 1,494 ± 0,014 1,086 ± 0,023 1,314 ± 0,018 1,322 ± 0,037 2 W=0,048 (d) (c) (a) (b) (b) 6 Zn (II) (mg/L) 10,06±0,02 ± SE 4,648 ± 0,030 3,928 ± 0,025 3,586 ± 0,020 2,486 ± 0,016 2,906 ± 0,014 5 W=0,045 (e) (d) (c) (a) (b) Keterangan : *W = BNJ 5% ;
*Angka-angka yang diikuti dengan huruf yang sama menunjukkan antar perlakuan tidak berbeda nyata, sebaliknya angka-angka yang diikuti huruf yang berbeda menunjukkan perlakuan beda nyata. Keterangan ini juga berlaku untuk Tabel 5.
9
Dari Tabel 3 tampak bahwa pemberian berbagai variasi bobot karbon aktif ampas teh selama 240 menit mampu menurunkan rataan TDS berkisar antara 948 ± 7,98 ppm sampai 1.110 ± 13,48 ppm. Sebaliknya TSS mengalami kenaikan dengan rataan berkisar antara 19,8 ± 0,79 mg/L sampai 61,4 ± 1,09 mg/L, meskipun demikian kenaikannya masih memenuhi baku mutu yang disyaratkan. Untuk pH terjadi kenaikan dengan rentang rataan berkisar antara 4,36 ± 0,11 sampai 5,42 ± 0,08 dan masih belum memenuhi baku mutu yang disyaratkan.
Pemberian 1,25 gram karbon aktif ampas teh mampu menurunkan COD dari 11.136 mg/L menjadi 81,2 ± 0,798 mg/L. Konsentrasi Mn (II) mengalami penurunan pada pemberian karbon aktif ampas teh 3,75 gram dengan rataan konsentrasi 1,086 ± 0,023 mg/L. Konsentrasi Zn (II) mengalami penurunan pada pemberian 5 gram karbon aktif ampas teh dengan rataan konsentrasi 2,486 ± 0,016 mg/L Penurunan Konsentrasi COD, Mn (II) dan Zn (II) disebabkan karena karbon aktif ampas teh memiliki bidang penyerapan yang luas serta dimungkinkan oleh adanya gugus aktif (karboksil) (Lin, 1979).
Hasil penelitian ini sejalan dengan hasil penelitian terdahulu dengan menggunakan adsorben dengan bahan yang sama. Hasil penelitian Nachiappan & Muthukumar (2010) dengan COD awal 29.333 mg/L dan dosis ampas teh teraktivasi 6 g/L mampu menurunkan COD hingga 1319,98 mg/L. Penelitian Khajeh et al. (2013) dengan larutan Mn (II) 1 ppm dan dosis ampas teh 0,2 g/100 ml mampu menurunkan Mn (II) hingga 0,011 ppm. Lebih lanjut, Ahluwalia & Goyal, 2005 melaporkan bahwa dengan menggunakan larutan Zn (II) 10 mg/L dengan dosis ampas teh 4 g/100 ml mampu menurunkan konsentrasi Zn (II) hingga 2,68 mg/L.
3.2. Efektivitas Pengolahan Limbah Cair Laboratorium Kimia dengan Berbagai Penambahan Bobot Karbon Aktif Ampas Teh (g) dalam Waktu Kontak 240 menit
Berikut akan disajikan efektivitas pengolahan limbah cair Laboratorium Kimia antar berbagai nisbah bobot karbon aktif ampas teh (g) dalam waktu kontak 240 menit berkisar antara 23,67% - 99,27% (Tabel 4).
10
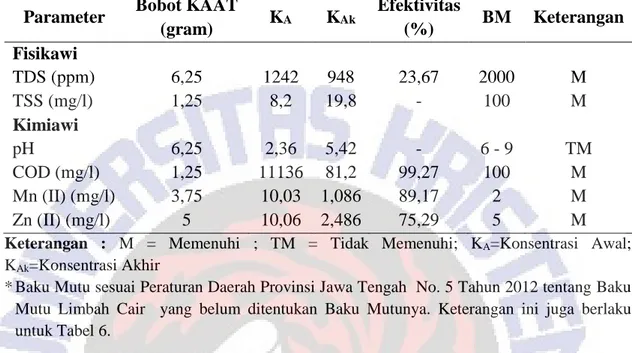
Tabel 4. Efektivitas (%) Berbagai Bobot Karbon Aktif Ampas Teh (KAAT) dalam Pengolahan Limbah Cair Laboratorium Kimia dalam Waktu Kontak 240 menit
Parameter Bobot KAAT
(gram) KA KAk Efektivitas (%) BM Keterangan Fisikawi TDS (ppm) 6,25 1242 948 23,67 2000 M TSS (mg/l) 1,25 8,2 19,8 - 100 M Kimiawi pH 6,25 2,36 5,42 - 6 - 9 TM COD (mg/l) 1,25 11136 81,2 99,27 100 M Mn (II) (mg/l) 3,75 10,03 1,086 89,17 2 M Zn (II) (mg/l) 5 10,06 2,486 75,29 5 M
Keterangan : M = Memenuhi ; TM = Tidak Memenuhi; KA=Konsentrasi Awal;
KAk=Konsentrasi Akhir
* Baku Mutu sesuai Peraturan Daerah Provinsi Jawa Tengah No. 5 Tahun 2012 tentang Baku Mutu Limbah Cair yang belum ditentukan Baku Mutunya. Keterangan ini juga berlaku untuk Tabel 6.
Dari Tabel 4 terlihat bahwa 6,25 gram karbon aktif ampas teh efektif menurunkan TDS 23,67 %, sedangkan pemberian 1,25 gram karbon aktif ampas teh efektif menaikkan pH 56,46% namun masih di bawah baku mutu yang disyaratkan. Pemberian 1,25 gram karbon aktif ampas teh efektif menurunkan COD hingga 99,27%, sedangkan pemberian 3,75 gram karbon aktif ampas teh efektif menurunkan Mn (II) 89,17% dan pemberian 5 gram karbon aktif ampas teh efektif menurunkan Zn (II) 75,29%,
Penelitian ini sejalan dengan penelitian Nachiappan & Muthukumar (2010) dengan COD awal 29.333 mg/L dan dosis ampas teh teraktivasi 6 g/L efektif menurunkan COD hingga 95,5 % dengan menggunakan metode sono-feton-sorption.
Hasil penelitian Khajeh et al. (2013) dengan larutan Mn (II) 1 ppm dan dosis ampas teh 0,2 g/100 ml efektif menurunkan Mn (II) hingga 98,9%. Penelitian oleh Ahluwalia & Goyal, 2005 dengan menggunakan larutan Zn (II) 10 mg dan dosis ampas teh 4 g/100 ml membuktikan bahwa ampas teh efektif menurunkan Zn (II) 73,2%.
11
3.3. Rataan Kandungan Parameter Fisko-Kimiawi Limbah Cair Laboratorium Kimia Antar Penambahan Berbagai Bobot Sabut Kelapa Teroksidasi dalam Waktu Kontak 240 menit – 510 menit
Pada pemberian karbon aktif ampas teh selama 240 menit menunjukkan bahwa pH belum memenuhi baku mutu maka perlu dioptimalkan dengan penambahan sabut kelapa teroksidasi sesuai dengan nisbah bobotnya dengan waktu kontak dari 240 menit sampai 510 menit. Kandungan parameter fisiko-kimiawi dalam waktu kontak dari 240 menit hingga 510 menit disajikan pada Tabel 5 (dan Lampiran 2).
12
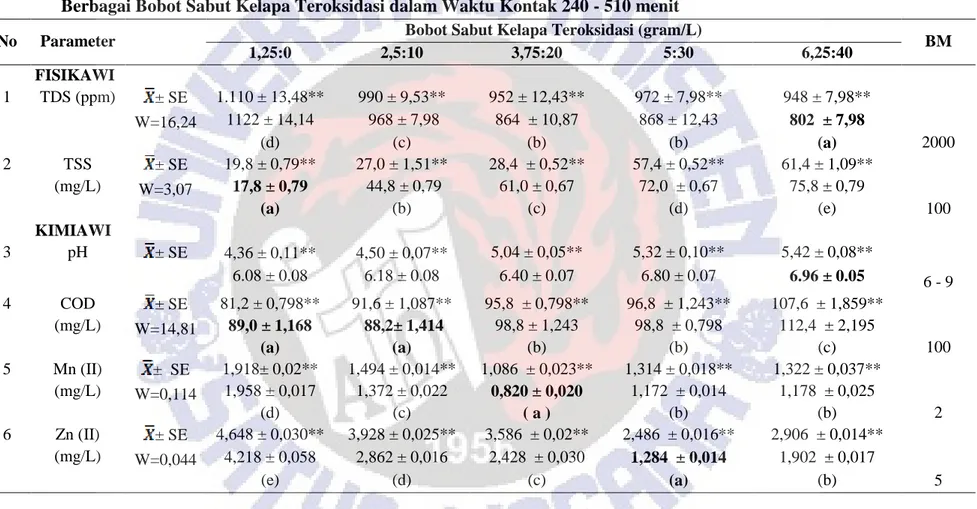
Tabel 5. Rataan Kandungan Parameter Fisiko-Kimiawi ( ± SE) Limbah Cair Laboratorium Kimia Antar Penambahan Berbagai Bobot Sabut Kelapa Teroksidasi dalam Waktu Kontak 240 - 510 menit
No Parameter Bobot Sabut Kelapa Teroksidasi (gram/L) BM
1,25:0 2,5:10 3,75:20 5:30 6,25:40 FISIKAWI 1 TDS (ppm) ± SE W=16,24 1.110 ± 13,48** 990 ± 9,53** 952 ± 12,43** 972 ± 7,98** 948 ± 7,98** 2000 1122 ± 14,14 968 ± 7,98 864 ± 10,87 868 ± 12,43 802 ± 7,98 (d) (c) (b) (b) (a) 2 TSS (mg/L) ± SE W=3,07 19,8 ± 0,79** 27,0 ± 1,51** 28,4 ± 0,52** 57,4 ± 0,52** 61,4 ± 1,09** 100 17,8 ± 0,79 44,8 ± 0,79 61,0 ± 0,67 72,0 ± 0,67 75,8 ± 0,79 (a) (b) (c) (d) (e) KIMIAWI 3 pH ± SE 4,36 ± 0,11** 4,50 ± 0,07** 5,04 ± 0,05** 5,32 ± 0,10** 5,42 ± 0,08** 6 - 9 6.08 ± 0.08 6.18 ± 0.08 6.40 ± 0.07 6.80 ± 0.07 6.96 ± 0.05 4 COD (mg/L) ± SE W=14,81 81,2 ± 0,798** 91,6 ± 1,087** 95,8 ± 0,798** 96,8 ± 1,243** 107,6 ± 1,859** 100 89,0 ± 1,168 88,2± 1,414 98,8 ± 1,243 98,8 ± 0,798 112,4 ± 2,195 (a) (a) (b) (b) (c) 5 Mn (II) (mg/L) ± SE W=0,114 1,918± 0,02** 1,494 ± 0,014** 1,086 ± 0,023** 1,314 ± 0,018** 1,322 ± 0,037** 2 1,958 ± 0,017 1,372 ± 0,022 0,820 ± 0,020 1,172 ± 0,014 1,178 ± 0,025 (d) (c) ( a ) (b) (b) 6 Zn (II) (mg/L) ± SE W=0,044 4,648 ± 0,030** 3,928 ± 0,025** 3,586 ± 0,02** 2,486 ± 0,016** 2,906 ± 0,014** 5 4,218 ± 0,058 2,862 ± 0,016 2,428 ± 0,030 1,284 ± 0,014 1,902 ± 0,017 (e) (d) (c) (a) (b)
13
Dari Tabel 5 terlihat bahwa variasi penambahan sabut kelapa teroksidasi mampu menurunkan TDS dengan kisaran rataan 802 ± 7,98 ppm sampai 1122 ± 14,14 ppm, sedangkan TSS mengalami kenaikan dengan rataan berkisar antara 17,8 ± 0,79 mg/L sampai 75,8 ± 0,79 mg/L tetapi kenaikan TSS masih memenuhi baku mutu. Pemberian 10 gram sabut kelapa teroksidasi mampu menurunkan COD dengan rataan 88,2± 1,414 mg/L. Pemberian 20 gram sabut kelapa teroksidasi mampu menurunkan Mn (II) dengan rataan 0,820 ± 0,020 mg/L. Pemberian 30 gram sabut kelapa teroksidasi mampu menurunkan Zn (II) dengan rataan 1,284 ± 0,014 mg/L.
Penurunan konsentrasi COD, Mn (II) dan Zn (II) terkait dengan terbentuknya gugus –COONa pada permukaan sabut kelapa yang telah dimodifikasi sehingga dapat menurunkan konsentrasi logam (M2+) dengan mekanisme sebagai berikut : (Shukla et al., 2006)
Keterangan : Coir = Sabut Kelapa
Hasil tersebut sejalan dengan hasil penelitian Kumar et al. (2016) dengan dosis sabut kelapa 10 g/ 250 ml limbah tekstil mampu menurunkan COD 33%. Penelitian Mthombeni et al. (2016) dengan dosis sabut kelapa 3 g/L mampu menurunkan Mn (II) dari 100 mg/L menjadi 73,38 mg/L. Israel & Eduok (2012) membuktikan bahwa dengan 0,2 g sabut kelapa termodifikasi (sulphonate toluenediisocynate) dalam 30 ml larutan Zn (II) 10 mg/L mampu menurunkan Zn (II) menjadi 7,83 mg/L.
3.4. Efektivitas Pengolahan Limbah Cair Laboratorium Kimia Antar Penambahan Berbagai Bobot Sabut Kelapa Teroksidasi dalam Waktu Kontak 240 menit – 510 menit
Berikut akan disajikan efektivitas pengolahan limbah cair laboratorium kimia antar penambahan berbagai bobot sabut kelapa teroksidasi (gram) dalam waktu kontak 240 menit – 510 menit berkisar antara 3,71 - 48,35 % (Tabel 6).
14
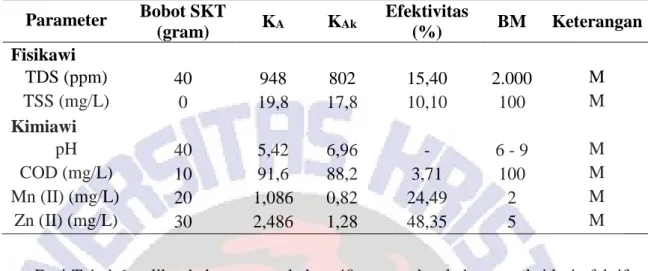
Tabel 6. Efektivitas (%) Berbagai Bobot Sabut Kelapa Teroksidasi (SKT) dalam Pengolahan Limbah Cair Laboratorium Kimia dalam Waktu Kontak 240-510 menit Parameter Bobot SKT (gram) KA KAk Efektivitas (%) BM Keterangan Fisikawi TDS (ppm) 40 948 802 15,40 2.000 M TSS (mg/L) 0 19,8 17,8 10,10 100 M Kimiawi pH 40 5,42 6,96 - 6 - 9 M COD (mg/L) 10 91,6 88,2 3,71 100 M Mn (II) (mg/L) 20 1,086 0,82 24,49 2 M Zn (II) (mg/L) 30 2,486 1,28 48,35 5 M
Dari Tabel 6 terlihat bahwa penambahan 40 gram sabut kelapa teroksidasi efektif menurunkan TDS 15,40%, sedangkan tanpa pemberian sabut kelapa teroksidasi (0 gram) efektif menurunkan TSS 10,10%. Penambahan 40 gram sabut kelapa teroksidasi efektif menaikkan pH 22,13%, sedangkan pada penambahan 10 gram sabut kelapa teroksidasi efektif menurunkan COD 3,71%. Pemberian 20 gram sabut kelapa teroksidasi efektif menurunkan Mn (II) 24,49%. Penurunan Zn (II) 48,35% efektif pada pemberian 30 gram sabut kelapa teroksidasi.
Penelitian ini sejalan dengan hasil penelitian Kumar et al. (2016) dengan dosis 10 gram sabut kelapa dalam 250 ml limbah tekstil selama 60 menit efektif menurunkan COD 33%. Penelitian Mthombeni et al. (2016) dengan dosis adsorben 3 g/L efektif menurunkan Mn (II) 26,62%. Israel & Eduok (2012) melaporkan bahwa dengan 0,2 g sabut kelapa termodifikasi (sulphonate toluenediisocynate) dalam 30 ml larutan Zn (II) 10 mg/L efektif menurunkan Zn (II) 21,7%.
3.5. Isoterm Adsorpsi Parameter Fisioko-Kimiawi Limbah Cair Laboratorium Kimia dengan Menggunakan Karbon Aktif Ampas Teh dan Sabut Kelapa Teroksidasi dalam Waktu Kontak 510 menit.
Hasil perhitungan Isoterm adsorpsi Langmuir dan Freundlich parameter fisiko-kimiawi limbah cair laboratorium kimia di sajikan dalam Tabel 7 (dan Lampiran 2).
15
Tabel 7. Isoterm Adsorpsi Langmuir dan Freundlich Parameter Fisiko – Kimiawi Limbah Cair Laboratorium Kimia Menggunakan Karbon Aktif Ampas Teh (KAAT) dan Sabut Kelapa Teroksidasi (SKT)
Parameter NA (g) Langmuir b Q(mg/g) RL Freundlich n Kf SD
KAAT COD 1,25 y = 0,0004x - 0,1878 -0.0021 2.500 -0,0447 y = -0,1901x + 4,3568 -5,2604 22,74×103 771,41 R² = 0,9422 (r=0,9707) R² = 0,6545 (r=0,8090) Mn (II) 3,75 y = 0,7082x – 0,3663 -1,9334 1,412 -0,0544 y = -0,3054x + 0,398 -3,2744 2,5003 0,4185 R² = 0,931 (r=0,9895) R² = 0,9551 (r=0,9773) Zn (II) 5 y = 1,2388x – 1,5265 -0,8115 0,8072 -0,1396 y = -0,533x + 0,3972 -1,8762 2,4957 2,6346 R² = 0,9951 (r= 0,9975) R² = 0,9778 (r=0,9888) SKT COD 10 y = 10,475x – 872,72 -0,0120 0,0955 -4,1946 y = -11,7x + 23,018 -0,0855 1,04×1023 1,72×1017 R² = 0,9473 (r=0,9733) R² = 0,9523 (r=0,9759) Mn (II) 20 y = 484,24x – 336,45 -1,44 0,0021 -0,0073 y = -3,6098x – 2,1834 -0,277 0,0066 2,5582 R² = 0,9969 (r=0,9984) R² = 0,9803 (r=0,9901) Zn (II) 30 y = 563,46x – 776,42 -0,7257 0,0018 -0,0144 y = -3,7654x – 0,8727 -0,2656 0,1341 1,8065 R² = 0,7189 (r=0,8479) R² = 0,8767 (r=0,9363) Keterangan :
NA = Nisbah Adsorben; KAAT = Karbon Aktif Ampas Teh; SKT = Sabut Kelapa Teroksidasi; b = Konstanta Langmuir; Q = Kapasitas Adsorpsi
Maksimum (mg/g) ; RL = Faktor Pemisah; n = Konstanta Freundlich ; Kf = Kapasitas adsorpsi; SD = Standar Deviasi; R2 = Koefisien Determinasi ; r =
16
Dari Tabel 7 terlihat bahwa model isotherm adsorpsi COD mengikuti model isotherm Langmuir pada pemberian 1,25 gram Karbon Aktif Ampas Teh dengan nilai R2 0,9422 dan kapasitas adsorpsi 2500 mg/g. Sedangkan pada pemberian 10 gram sabut kelapa teroksidasi mengikuti model isotherm Freundlich dengan nilai R² 0,9523 dan kapasitas adsorpsi 1,04×1023 mg/g. Hasil penelitian ini sejalan dengan hasil penelitian terdahulu oleh Aluyor & Badmus (2008) dengan menggunakan karbon aktif dari tanduk binatang menunjukkan bahwa model isotherm untuk COD mengikuti model isotherm Langmuir dengan R2 0,9998 dengan kapasitas adsorpsi 6,46 mg/g dan penelitian Sholeh dkk. (2012) menunjukkan bahwa model isotherm COD menggunakan abu terbang bagas mengikuti model isotherm Freundlich dengan nilai R2 0,93 dan kapasitas adsorpsi
0,4360 mg/g.
Model isotherm untuk Mn (II) mengikuti model isotherm Freundlich dengan nilai R² 0,9551 dan kapasitas adsorpsi 2,5003 mg/g pada pemberian 3,75 gram karbon aktif ampas teh. Sedangkan untuk pemberian 20 gram sabut kelapa teroksidasi mengikuti model isotherm adsorpsi Langmuir dengan nilai R² 0,9969 dan kapasitas adsorpsi 0,0021 mg/g. Hasil penelitian ini sejalan dengan hasil penelitian Khajeh et al. (2013) dengan menggunakan zeolit termodifikasi yang menunjukkan bahwa model isoterm ion logam Mn (II) mengikuti model isoterm Langmuir dengan R2 0,982.
Model isotherm adsopsi untuk Zn (II) mengikuti model isotherm adsorpsi Langmuir pada pemberian 5 gram karbon aktif ampas teh dengan nilai R² 0,9951 dan kapasitas adsorpsi 0,8072 mg/g. Sedangkan pada pemberian 30 gram sabut kelapa teroksidasi mengikuti model isotherm Freundlich dengan nilai R² 0,8767 dan kapasitas adsorpsi 0,1341 mg/g. Hasil penelitian ini sejalan dengan hasil penelitian Ahluwalia & Goyal (2005) dengan penjerap ampas teh, menunjukkan bahwa model isotherm ion logam Zn (II) mengikuti model isotherm Langmuir dengan R² 0,900.
Persamaan Langmuir berdasarkan nilai faktor pemisahan (RL) dapat diindikasikan
tipe dari isoterm Langmuir, (RL = 0) menunjukkan bahwa irreversible, (0 < RL < 1)
menunjukkan bahwa favourable, (RL = 1) menunjukkan bahwa linear dan (RL > 1)
menunjukkan bahwa unfavourable. Nilai RL pada parameter COD, Mn dan Zn (Tabel
2.) tidak dapat diindikasikan karena bernilai negatif.
Pada pemberian Karbon Aktif Ampas Teh untuk parameter COD mengikuti model isoterm adsorpsi Langmuir dan SD = 771,4083; Mn dengan model isotherm
17
adsorpsi Freundlich dan SD = 0,4185; dan Zn dengan model isotherm adsorpsi Langmuir dan SD = 2,6346. Sedangkan pada pemberian Sabut Kelapa Teroksidasi untuk parameter COD mengikuti model isoterm adsorpsi Freundlich dan SD = 1,72×1017; Mn dengan model isoterm adsorpsi Langmuir dan SD = 2,5582; dan Zn dengan model isotherm adsorpsi Freundlich dan SD = 1,8065.
4. KESIMPULAN
Berdasarkan hasil penelitian dapat ditarik kesimpulan sebagai berikut :
1. Pemberian karbon aktif ampas teh selama 240 menit diperoleh nisbah yang efektif pada bobot 1,25 gram untuk COD; 3,75 gram untuk Mn; dan 5 gram untuk Zn dengan efektivitas berkisar antara 75,29% sampai 99,27%. Pemberian sabut kelapa teroksidasi selama 240 – 510 menit yang efektif pada bobot 10 gram untuk COD, 20 gram untuk Mn dan 30 gram untuk Zn dengan efektivitas berkisar antara 3,71% sampai 48,35%.
2. Kapasitas adsorpsi maksimum pada pemberian karbon aktif ampas teh pada pemberian bobot 1,25 gram untuk COD = 2.500 mg/g mengikuti model isotherm Langmuir (SD=771,4083); 3,75 gram untuk Mn = 2,5003 mg/g mengikuti model isotherm Freundlich (SD=0,4185); dan 5 gram untuk Zn = 0,8072 mg/g mengikuti model isotherm Langmuir (SD=2,6346) selama 240 menit. Sedangkan kapasitas adsorpsi pemberian sabut kelapa teroksidasi pada pemberian bobot 10 gram untuk COD= 1,04×1023 mg/g mengikuti model isotherm Freundlich (SD=1,72E+17); 20 gram untuk Mn = 0,0021 mg/g mengikuti model isotherm Langmuir (SD=2,5582); dan 30 gram untuk Zn = 0,1341 mg/g mengikuti model isotherm Freundlich (SD=1,8065) selama 240-510 menit.
18 5. SARAN
Untuk penelitian selanjutnya sebaiknya dilakukan percobaan dengan sabut kelapa yang dikarbonasikan dan ampas teh yang diaktivasi tanpa karbonasi serta dilakukan pengujian lebih lanjut untuk mengetahui gugus aktif dalam adsorben yang digunakan.
DAFTAR PUSTAKA
Ahluwalia, S. S. & Goyal, D., 2005. Removal of Heavy Metals by Waste Tea Leaves from Aqueous Solution. Engineering in Life Sciences 5(2), 158-162.
Alaerts, G. & Santika, S.S., 1987. Metode Penelitian Air. Usaha Nasional. Surabaya. Aluyor, E. O. & Badmus, O. A. M., 2008. COD Removal from Industrial Wastewater
Using Activated Carbon Prepared from Animal Horns. African Journal of Biotechnology 7(21), 3887-3891.
Arbanah, M., Miradatul, M.R.N. & Ku Halim, K.H., 2013. Utilization of Pleurotus ostreatus in the Removal of Cr(VI) from Chemical Laboratory Waste. International Refereed Journal of Engineering and Science (IRJES) 2(4), 29-39. Duran, C. Ozdes, Duygu, Gundogdu, Ali, Imamoglu, Mustafa, Senturk, Hasan Basri,
2011. Tea-industry waste activated carbon, as a novel adsorbent, for separation, preconcentration and speciation of chromium. Elsevier: Analytica Chimica Acta 688(1), 75–83.
Fadhil, A.B., Dheyab, M.M. & Abdul-Qader, A.Q.Y., 2012. Purification of biodiesel using activated carbons produced from spent tea waste. Journal of the Association of Arab Universities for Basic and Applied Sciences 11(1), 45–49.
Gao, J. Kong, Dedong, Wang, Yuefei,Wu, Jing Sun, Shili, Xu, Ping, 2013. Production of mesoporous activated carbon from tea fruit peel residues and its evaluation of methylene blue removal from aqueous solutions. BioResources 8(2), 2145–2160. Gurten, I.I. Ozmak, Meryem, Yagmur, Emine, Aktas, Zeki, 2012. Preparation and
characterisation of activated carbon from waste tea using K 2CO 3. Elsevier: Biomass and Bioenergy 37(1), 73–81.
Israel, A. U. & Eduok, U. M., 2012. Removal of Some Metal Ions from Aqueous Solution Using Coconut Coir Dust and Modified Coconut Coir Dust Extract Resins. Research Jounal of Applied Sciences 7, 481-488.
Khajeh, M., Yazdi, A. S. & Moghadam, A. F., 2013. Modeling of Solid-phase Tea Waste Extraction for Removal of Manganese and Cobalt from Water Samples by Using PSO-artificial Neural Network and Response Surface Methodology. Arabian Journal of Chemistry, 1-11.
19
Kumar, P. S., Kumarand, S. A. & Balamurugan, P., 2016. Comparative Studies on Application of Various Adsorbents in Fire Industry Waste Water. Advances in Natural and Applied Sciences 10(3), 49-57.
Lin, C. 1979. Kinetics and Mechanisms og Adsorption of Heavy Metals Ion on Activated Carbon. Thesis. Texas Tech University.
Mthombeni, N. H., Mbakop, S. & Onyango, M. S., 2016. Adsorptive Removal of Manganese from Industrial and Mining Wastewater. s.l., s.n., 36-45.
Mulyatna, L., H. Pradiko, dan U. K. Nasution. 2003. Pemilihan Persamaan Adsorpsi Isoterm pada Penentuan Kapasitas Adsorpsi Kulit Kacang Tanah terhadap Zat Warna Remazol Golden Yellow 6. INFOTEK 5,131-140.
Nachiappan, S. & Muthukumar, K., 2010. Intensification of Textile Effluent Chemical Oxygen Demand Reduction by Innovative Hybrid Methods. Chemical Engineering Journal 163, 344-354.
Okafor, P.C., Okon, P.U., Daniel, E.F. & Ebenso, E.E., 2012. Adsorption Capacity of Coconut (Cocos nucifera L.) Shell for Lead, Copper, Cadmium and Arsenic from Aqueous Solutions. International Journal of ELECTROCHEMICAL SCIENCE 7, 12354-69.
Putra, A. D. K., 2014. Nisbah Bobot Campuran Kulit Jeruk dan Arang Tongkol Jagung Sebagai Adsorben Dalam Pengolahan Air Limbah Tekstil. Skripsi, Universitas Kristen Satya Wacana, Salatiga.
Sholeh, M., Prasetya, A. & Sarto. 2012. Pengolahan Air Limbah Industri Penyamakan Kulit Menggunakan Abu Terbang Bagas Secara Batch. Majalah Kulit, Karet dan Plastik 28(1), 26-34.
Shukla, S.R., Pai, R.S. & Shendarkar, A.D., 2006. Adsorption of Ni(II), Zn(II) and Fe(II) on modified coir fibres. Elsevier: Separation and Purification Technology 47(3), 141–147.
Shukla, S.R. Gaikar, V. G. Pai, Roshan S. Suryavanshi, Umesh S., 2009. Batch and Column Adsorption of Cu(II) on Unmodified and Oxidized Coir. Separation Science and Technology, 44(1), 40–62.
Steel, R.G.D. and J. H. Torie, 1981. Principle and Procedures of Statistic A Biometrical Approach, 2nd ed. Mc Graw-Hill International. Book Co, Kuga Kusha, Japan.
Suseno, H.P., 2012. Pengurangan Chemical Oxygen Demand (COD) dan Krom Dalam Air Limbah Industri Penyamakan Kulit Menggunakan Abu Terbang Bagas. In Prosiding Seminar Nasional Aplikasi Sains & Teknologi (SNAST) Periode III. Yogyakarta, 2012. ISSN: 1979-911X.
Wankhade Amey, a & Ganvir, V.N., 2013. Preparation of Low Cost Activated Carbon from Tea Waste using Sulphuric Acid as Activating Agent. International Research Journal of Environment Sciences 2(4), 53–55.