Sintesis dan Karakterisasi Nanopartikel Fe-doped
ZnO/Montmorillonite dan Aplikasinya terhadap Fotodegradasi Congo
Red
Nur Afifah
Departemen Fisika, FMIPA-Universitas Indonesia, 16424 Depok, Indonesia
Email: nur.afifah11@ui.ac.id
Abstrak
Nanopartikel Fe- doped ZnO/Montmorillonite dengan empat variasi konsentrasi dopant disintesis menggunakan metode kopresipitasi. Seluruh sampel menunjukkan fase tunggal dari struktur
hexagonal wurzite ZnO pada spektrum X-ray Diffraction (XRD), namun fase sekunder dari
ZnFe2O4 ditemukan pada sampel dengan konsentrasi dopant 12 at.%. Keberadaan dopant Fe dan
montmorillonite dikonfirmasi menggunakan spektroskopi Energy Dispersive X-ray (EDX), Fourier Transform Infrared (FTIR), dan Electron Spin Resonace (ESR). Hasil spektroskopi UV-Vis Diffuse Reflectance (UV-UV-Vis DRS) menunjukkan nilai celah energi yang diperoleh menurun
seiring meningkatnya konsentrasi dopant. Uji aktivitas fotokatalitiik dipelajari dengan menggunakan Congo Red (CR) sebagai model polutan organik di bawah paparan sinar Ultra
Violet (UV). Degradasi CR yang diamati meningkat seiring meningkatnya konsentrasi dopant.
Studi efek dosis katalis dan konsentrasi awal CR menunjukkan hasil optimum dapat tercapai saat menggunakan 0.7g/L Fe-doped ZnO/Montmorillonite 12 at.% untuk mendegradasi 20 mg/L CR pada pH netral. Jenis Reactive Oxygen Species (ROS) yang paling berperan pada aktivitas fotokatalitik ialah elektron (e-)> hole (h+)> OH.
Kata Kunci: Fe-doped ZnO, montmorillonite, aktivitas fotokatalitik, congo red.
Synthesis and Characterization of Fe-doped ZnO/Montmorillonite Nanoparticles and Their Application for Congo Red Photodegradation.
Abstract
Four variations in dopant concentration of Fe-doped ZnO/Montmorillonite nanoparticles were synthesized using co-precipitation method. X-Ray Diffraction spectrum are shown hexagonal wurzite structure for all samples, while at 12 at.% doping concentration the secondary fase of ZnFe2O4 is detected. The existence of Fe dopant and montmorillonite are confirmed by Energy
Dispersive X-Ray, Fourier Transform Infrared, and Electron Spin Resonance Spectroscopies. Results of UV-Vis Diffuse Reflectance Spectroscopy shows tendency of energy gap decreases with increasing dopant concentration. Photocatalytic activities were evaluated by using Congo Red (CR) as a model of organic pollutants under UV light irradiation. The optimum condition to degrade 20 mg/L CR obtains for 0.7 g/L of 12 at.% Fe-doped ZnO/Montmorillonite in neutral condition. The type of Reactive Oxygen Species (ROS) that most contribute on photocatalytic activity is as followed electron (e-)> hole (h+)> OH.
1. Pendahuluan
Fotokatalisis, merupakan “green” teknik yang menawarkan potensi tinggi terhadap rehabilitasi lingkungan dalam proses fotodegradasi polutan organik yang terkandung dalam air limbah [1]. Fotokatalisis sendiri dinilai sebagai teknik yang efisien karena menyediakan cara yang ramah lingkungan untuk secara langsung mengkonversi energi matahari menjadi energi kimia [2]. Pada praktiknya, energi kimia tersebut dapat menyelesaikan serangkaian proses reduksi dan oksidasi untuk menginisiasi zat pewarna dan mengubahnya menjadi senyawa organik dengan gugus kimia yang lebih sederhana serta tidak berbahaya [3, 4]. Beberapa peneliti melaporkan bahwa semikonduktor sebagai fotokatalis memiliki performa fotokatalitik yang baik dan patut untuk diperhitungkan [5, 6].
ZnO merupakan salah satu semikonduktor yang telah berhasil digunakan untuk mendegradasi polutan organik di bawah paparan sinar ultra violet (UV) [7]. ZnO yang telah dimodifikasi dengan menggunakan doping logam transisi, menunjukkan aktivitas fotokatalititik yang lebih baik dibandingkan dengan ZnO tanpa modifikasi [8, 9, 10]. Doping dengan menggunakan logam transisi dipercaya dapat menurunkan nilai celah energi ZnO dan memperbanyak trapping state yang dapat meningkatkan aktivitas fotokatalitik [1, 11]. Zhang et
al. [12] dan Ba-Abbad et al. [13] telah melaporkan aktivitas fotokatalitik ZnO yang diberi dopant Fe. Logam transisi Fe dipilih sebagai dopant karena nilai radius ioniknya yang tidak
berbeda jauh dari radius ionik Zn pada ZnO [13].
Performa fotokatalitik juga bergantung pada kapasitas penyerapan dari suatu katalis karena reaksi fotokatalitik terjadi pada permukaan suatu katalis [14]. Material clay seperti
montmorillonite (MMT) diketahui dapat meningkatkan aktivitas fotokatalitik ZnO dengan
menyediakan luas permukaan aktif yang besar dan kemampuan adsorpsi yang tinggi [15]. Pembuatan katalis dengan cara menambahkan MMT pada semikonduktor TiO2 telah dilaporkan
oleh Djellabi et al. [16] dan Dvininov et al. [17], sedangkan untuk semikonduktor TiO2 yang
diberi dopant logam transisi telah dilaporkan oleh Quan et al. [18]. Penelitian semikonduktor ZnO yang diberi dopant logam transisi Fe dan ditambahkan MMT sebagai katalis masih belum banyak dilakukan sehingga menarik dan perlu diteliti lebih lanjut.
Fe-doped ZnO/Montmorillonite (Fe:ZnO/MMT) pada penelitian ini disintesis dengan menggunakan metode kopresipitasi. Komposisi unsur-unsur penyusun sampel dan kehadiran MMT dipelajari dengan menggunakan spektroskopi Energy Dispersive X-ray (EDX). Struktur
dari sampel dikarakterisasi dengan menggunakan spektroskopi X-ray Diffraction (XRD),
Fourier Transform Infrared (FTIR), dan Electron Spin Resonace (ESR). Celah energi optik dari
sampel diperoleh dari pengukuran spektroskopi UV-Vis Diffuse Reflectance (DRS) dengan bantuan relasi Kubelka-Munk [19]. Aktivitas fotokatalitik dari Fe:ZnO/MMT kemudian diuji dengan menggunakan congo red (CR) sebagai model polutan organik dibawah penyinaran cahaya UV. Pengujian aktivitas fotokatalitik juga dilakukan dengan variasi molar Fe/ZnO, jumlah dosis katalis, dan konsentrasi awal CR yang berbeda untuk memperoleh kondisi optimum. Spesies Reactive Oxygen Species (ROS) yang paling berperan juga dipelajari dalam penelitian ini dengan cara menambahkan beberapa scavenger kedalam larutan uji.
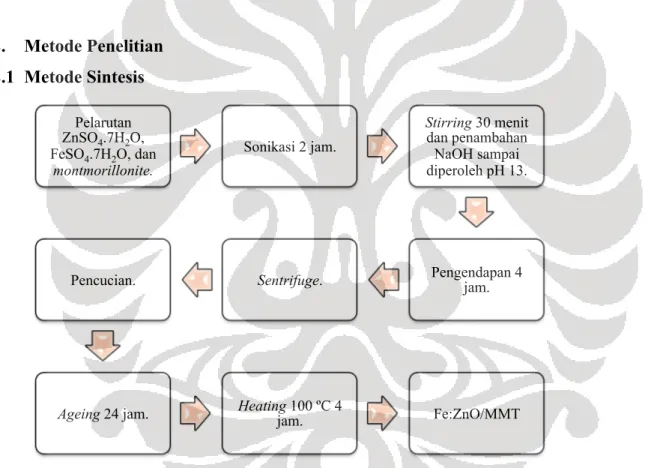
2. Metode Penelitian 2.1 Metode Sintesis
Gambar 2.1. Alur pembuatan sampel Fe-doped ZnO/MMT Nanopartikel.
Sintesis Fe:ZnO/MMT dilakukan dengan menggunakan metode ko-presipitasi. ZnSO!.7H!O (Merck), FeSO!.7H!O (Sigma-Aldrich), dan montmorillonite (Nanomer, U.S.A.) dengan standar analitik (kemurnian 99 %) digunakan sebagai reagen tanpa melalui proses pemurnian terlebih dahulu.
Variasi konsentrasi dopant Fe dari molar ZnO adalah sebesar: 3%, 5%, 10%, dan 15%. Penambahan montmorillonite (MMT) dilakukan dengan perbandingan massa Fe-doped ZnO
Pelarutan ZnSO4.7H2O, FeSO4.7H2O, dan montmorillonite. Sonikasi 2 jam. Stirring 30 menit dan penambahan NaOH sampai diperoleh pH 13. Pengendapan 4 jam. Sentrifuge. Pencucian.
terhadap massa MMT sebesar 10:1. Alur pembuatan sampel yang dilakukan dirangkum pada Gambar 2.1.
2.2 Karakterisasi
Komposisi unsur-unsur yang terkandung dalam sampel dikarakterisasi dengan menggunakan Energy Dispersive X-Ray Spectroscopy LEO 420 Departemen Metalurgi, Fakultas Teknik Universitas Indonesia. Struktur kristal dari sampel yang telah dibuat dianalisis dengan menggunakan spektroskopi XRD Shimadzu Maxima X-7000 Diffractometry Universitas Islam Negeri Syarif Hidayatullah Jakarta dengan sumber radiasi monokromatik CuKα (1.5406Å) yang direkam pada kisaran sudut 20º sampai 80º dengan scan step 0.02º. Gusus fungsional yang terdapat pada nanopartikel Fe:ZnO/MMT dianalisis dengan menggunakan Fourier Transform-
Infrared Shimadzu Prestige-21 Spectrophotometer Departemen Kimia, FMIPA UI yang
beroperasi pada daerah mid infrared 400-4000 cm!! dengan referensi Kalium bromide (KBr).
Keberadaan unsur doping dikonfirmasi dengan menggunakan Electron Spin Resonance JEOL JES-RE1X Spektrometer Badan Tenaga Nuklir Nasional-Pasar Jumat. Nilai reflektansi yang diperoleh dari pengukuran Ultraviolet-Visible Spectrophotometer Shimazu UV-2450 Departemen Kimia, FMIPA UI digunakan untuk mendapatkan nilai celah energi dengan cara mengekstrapolasi persamaan Kubelka-Munk ke nilai energi nol.
2.3 Uji Aktivitas Fotokatalitik
Pengujian aktivitas fotokatalitik dari sampel Fe:ZnO/MMT dilakukan dengan menggunakan dye (zat pewarna) congo red (CR) sebagai indikator polutan organik. Zat pewarna CR dilarutkan ke dalam akuades kemudian ditambahkan fotokatalisator Fe:ZnO/MMT. Campuran antara katalis dan larutan dye diaduk dengan pengaduk magnet dan dikenai cahaya UV selama 2 jam. Untuk mendapatkan fotokatalis dengan efisiensi yang tinggi, pengaruh variasi molar Fe/ZnO, dosis katalis, dan konsentrasi awal CR diamati. Spesies Reactive Oxygen Species (ROS) yang paling berperan pada aktivitas fotokatalitik Fe-doped ZnO/MMT dipelajari dengan menambahkan beberapa scavenger ke dalam larutan uji, yakni Natrium Sulfat (NaSO4),
Ammonium Oksalat (AO), dan tert-Butanol untuk mengikat e-, h+, dan OH. Semua pengukuran dilakukan untuk pH 7. Adapun laju degradasi perubahan warna dye dihitung dengan
Gambar 3.2. Kurva hasil pengukuran EDX sampel Fe:ZnO/MMT untuk empat variasi molar Fe/ZnO.
membandingkan konsentrasi akhir zat pewarna (Ct) dengan konsentrasi awal zat pewarna (C0)
sebagai fungsi waktu.
3. Hasil dan Analisis
Gambar 3.2 menunjukkan komposisi penyusun sampel Fe:ZnO/MMT hasi pengukuran EDX untuk empat variasi molar Fe/ZnO. Berdasarkan hasil kurva tersebut diamati bahwa unsur Zn, Fe, Al, Si, O, dan C terdapat pada semua sampel dengan intensitas puncak yang berbeda-beda. Untuk unsur Zn berada pada puncak dengan kisaran energi 1.01, 8.46, dan 9.35 keV. Untuk unsur O dan C berada pada masing-masing puncak dengan kisaran energi 0.54 dan 0.27 keV. Untuk unsur Al dan Si berada pada puncak dengan kisaran energi 1.46 dan 1.77 keV, dimana kedua unsur tersebut berasal dari MMT dengan rumus kimia (!"!− !"#!) !"!− !"#! !!"(!")!!!!! , !"!! [20] yang ditambahkan pada saat proses pembuatan sampel. Sedangkan, keberadaan doping Fe pada sampel yang telah disintesis dapat dikonfirmasi dengan adanya intensitas puncak unsur Fe yang berada pada kisaran energi 6.33 dan 6.87 KeV.
Setelah ditemukannya unsur-unsur dopant Fe dan MMT pada matriks ZnO, penentuan struktur dan fase kristal dilakukan dengan menganalisis hasil karakterisasi dari alat X-Ray
Diffractometry Spectroscopy seperti yang terlihat pada Gambar 3.3. Sampel Fe:ZnOMMT
menunjukkan fase tunggal dari struktur hexagonal wurtzite untuk variasi molar Fe/ZnO sebesar 3, 5, dan 7 at.%. Hasil ini diperkuat dengan ditemukannya sembilan puncak hexagonal wurtzite hasil representasi dari bidang (100), (002), (101), (102), (110), (103), (200), (112), dan (201) [21]. Namun, untuk variasi molar Fe/ZnO 12 at% ditemukan fase sekunder pada pola difraksi pada sudut 29.80º, 35.06º, 42.76º, 52.62º, dan 61.76º yang merepresentasikan bidang (220), (311), (400) dan (422) dari fase ZnFe2O4 [22].
Pola difraksi dari MMT tidak ditemukan pada analisa XRD dari sampel Fe:ZnO/MMT. Hal ini mungkin dapat disebabakan karena kandungannya yang sangat sedikit pada sampel dengan perbandingan masa Fe-doped ZnO terhadap massa MMT sebesar 10:1. Tidak ditemukannya pola difraksi dari unsur MMT ini dapat mengonfirmasi bahwa penambahan MMT tidak mengubah struktur utama dari ZnO.
Spektrum absorpsi FTIR ditampilkan pada Gambar 3.4 untuk empat variasi molar Fe/ZnO. Puncak dengan bilangan gelombang 562 cm!! dan 1350-1400 cm!! menunjukkan stretching
Gambar 3.3. Kurva hasil fitting data XRD sampel Fe:ZnO/MMT untuk empat
variasi molar Fe/ZnO dengan MAUD. (*: menunjukkan fase sekunder dari ZnFe2O4)
vibration Zn-O [23]. Puncak dengan bilangan gelombang sekitar 600-640 cm!! menunjukkan
vibrasi Fe-O [24]. Keberadaan unsur MMT pada penelitian ini dapat diperkuat dengan adanya mode vibrasi dari unsur Si dan Al. Bilangan gelombang 1090 cm!! menunjukan mode vibrasi antisymmetric dari Si-O-Si, bilangan gelombang 800 cm!! menunjukkan mode vibrasi symmetric
Si-O-Si, dan bilangan gelombang 460 cm!! menunjukkan bending dari Si-O [25, 26]. Puncak
bilangan gelombang 987 cm!! yang menunjukkan vibrasi Si-O-Al dan bilangan gelombang 1050
cm-1 menunjukkan bending Al-OH [27]. Puncak bilangan gelombang pada rentang 1100-1600 cm!! dapat menandakan adanya bending OH, C-OH plane bending and C-OH out-of-plane bending [28]. Sedangkan puncak bilangan gelombang pada rentang 3216-3644 cm!! menandakan
adanya vibrasi O-H [23, 24].
Adanya mode vibrasi unsur Fe, Si dan Al dapat mengonfirmasi hasil pengukuran EDX dan XRD bahwa doping Fe dan MMT berhasil tersubtitusi pada sampel Fe:ZnO/MMT untuk seluruh variasi moral Fe/ZnO.
Degradasi CR oleh Fe:ZnO/MMT untuk empat variasi molar Fe:ZnO, Fe:ZnO 5at.% dan MMT ditunjukkan oleh Gambar 3.5. Dosis katalis dan konsentrasi awal CR yang digunakan ialah 0.5 g/L dan 20 mg/L. Penggunaan dosis katalis dan konsentrasi awal CR ini didasari oleh
Gambar 3.4. Kurva spektrum absorbansi hasil karakterisasi FTIR sampel Fe:ZnO/MMT untuk empat variasi molar Fe/ZnO.
penelitian sebelumnya yang dilakukan oleh Grup Penelitian CENS untuk sampel Fe:ZnO. Hasil yang diperoleh menunjukkan aktivitas fotokatalitik Fe:ZnO/MMT meningkat seiring dengan meningkatnya variasi molar Fe:ZnO. Keberadaan ion dopant yang ditemukan dalam pengukuran EDX dan ESR diketahui dapat membentuk trapping state diantara pita konduksi dan pita valensi yang dapat menghambat laju rekombinasi pasangan elektron dan hole dan meingkatkan aktivitas fotokatalitik. Hal ini dikonfirmasi oleh Saleh dan Djaja [29] dengan menggunakan Fe-doped ZnO sebagai katalis untuk mendegradasi azo dye methyl orange (MO) dan methylene blue (MB). Keberadaan ion Fe2+ dan Fe3+ yang diperoleh pada pengukuran ESR diketahui dapat membentuk 2 level energi baru di dalam celah energi. Satu level energi di atas pita valensi yang mengacu pada orbital 3d dari Fe3+ dan yang lainnya dibawah pita konduksi karena level energi elektron ion Fe2+ lebih rendah dari Zn 3d pada pita konduksi. Ketika cahaya UV diberikan, elektron dapat tereksitasi dari Fe3+ dan pita valensi menuju pita konduksi. Setelah elektron tereksitasi Fe3+ akan dirubah menjadi Fe4+ untuk selanjutnya dapat berinteraksi dengan ion hidroksil dan menghasilkan radikal hidroksil OH.. Secara bersamaan elektron yang tereksitasi ke pita valensi dapat bereaksi
dengan oksigen dan menghasilkan radikal superoksida (.O2-). Fe2+ cenderung memiliki state yang
tidak stabil jika dibandingkan dengan Fe3+, oleh karena itu Fe2+ memiliki kecendrungan untuk melepas elektron sehingga elektron dapat ditransfer untuk mengabsorp oksigen dan menghasilkan radikal superoksida (.O2-) dan Fe3+. Spesies radikal aktif yang terbentuk itulah yang akan
Gambar 3.5. Degradasi CR oleh Fe:ZnO/MMT untuk empat variasi molar Fe:ZnO, Fe:ZnO 5at.% dan MMT.
Gambar 3.5 menunjukkan keberadaan MMT sangatlah mempengaruhi degrasi Fe:ZnO/MMT 5 at.% jika dibandingkan dengan Fe:ZnO 5 at.% dan MMT. Peran MMT sebagai material mesopori dengan luas permukaan aktif yang lebar, serta kemampuan absobsi yang tinggi, dinilai dapat meningkatkan aktivitas fotokatalitik karena menyediakan active site yang banyak untuk dapat bereaksi dengan molekul zat pewarna [20, 24]. Tergabungnya MMT pada Fe:ZnO/MMT yang dikonfirmasi melalui pengukuran EDX dan FTIR dengan adanya unsur Al dan Si dipercaya dapat menambah trapping state yang tersedia pada penelitian ini.
Aktivitas fotokatalitik optimum diperoleh dengan menggunakan Fe:ZnO/MMT 12 at.%. Untuk itu pengaruh dosis katalis, konsentrasi awal zat pewarna dan spesies ROS yang paling berperan pada penelitian ini diamati dengan menggunakan Fe:ZnO/MMT 12 at.%.
Studi mengenai pengaruh konsentrasi awal CR dipelajari dengan menggunakan Fe:ZnO/MMT 12 at./% dengan dosis 0.7 gr/L. Konsentrasi awal CR divariasikan dari 20 mg/L s.d 50 mg/L dengan interval 10 mg/L pada pH netral. Hasil yang diperoleh menunjukkan seiring bertambahnya konsentrasi awal CR, waktu yang dibutuhkan untuk mendegradasi zat pewarna tersebut juga semakin lama. Gambar 3.6 menunjukkan penurunan aktivitas fotokatalitik seiring meningkatnya konsentrasi awal CR 20>30>40>50 mg/L.
Jumlah permukaan aktif katalis yang tersedia untuk dapat berinteraksi dengan molekul
Gambar 3.6. Pengaruh konsentrasi awal CR terhadap aktiftas fotokatalitik
Gambar 3.7 Pengaruh scavanger terhadap degradasi CR dengan Fe:ZnO/MMT sebagai fotokatalisator.
dye
memegang peranan kritis dalam proses fotodegradasi [16, 17]. Semakin tinggi konsentrasi awal CR yang diberikan maka semakin banyak molekul CR yang terserap ke dalam permukaan Fe:ZnO/MMT, sehingga jumlah ion radikal OH· dan O2.- yang dibutuhkan untuk mendegradasi
CR semakin meningkat. Akan tetapi dengan menggunakan jumlah dosis katalis yang dijaga tetap (0.7 g/L) sementara konsentrasi awal CR meningkat, menyebabakan luas permukaan aktif yang tersedia untuk dapat mengabsorp ion hidroksil pun berkurang sehingga jumlah radikal hidroksil OH. yang dapat terbentuk juga cenderung berkurang [30]. Wu et al. [31] mengonfirmasi bahwa berkurangnya pembentukan ion radikal OH· dan O2.-, tidak cukup untuk mendukung proses
fotodegraasi zat pewarna dengan konsentrasi tinggi, sehingga aktivitas fotokatalitiknya pun berkurang.
Pengaruh jenis spesies ROS yang paling berperan dipelajari dengan menambahkan beberapa scavenger yang berbeda. Gambar 3.7 menunjukkan laju degradasi Fe:ZnO/MMT 12 at.% yang berkurang dengan kehadiran scavenger mengikuti: 80% scavenger e-< 85% scavenger
h+< 90% scavenger OH. Dari hasil tersebut dapat diketahui bahwa ketika Natrium Sulfat (NaSO4)
ditambahkan ke dalam larutan dye yang telah berisi fotokatalisator, NaSO4 tersebut dapat
mengindikasikan bahwa spesies yang paling berperan dalam proses fotodegradasi Fe:ZnO/MMT adalah elektron (e-).
4. Kesimpulan
Kehadiran doping besi (Fe) dan MMT pada sampel Fe:ZnO/MMT dikonfirmasi dengan adanya intensitas puncak unsur Fe, Al, dan Si yang diperkuat dengan adanya mode vibrasi dari Fe-O, Si-O-Si, Si-O-Al, dan Al-OH. Seluruh nanopartikel Fe:ZnO/MMT menunjukkan struktur
hexagonal wurzite ZnO, namun fase sekunder dari ZnFe2O4 ditemukan pada konsentrasi dopant
12 at.%. Keberadaan dopant Fe juga diperkuat dengan adanya resonansi ion !"!! dan !"!!.
Nilai celah energi yang diperoleh menunjukkan pergeseran ke energi lebih kecil seiring meningkatnya variasi molar Fe:ZnO. Pengaruh kehadiran MMT pada aktivitas fotokatalitik Fe:ZnO/MMT diperoleh dengan membandingkan aktivitas fotokatalitik Fe:ZnO/MMT 5 at.% yang jauh lebih tinggi jika dibandingkan dengan Fe:ZnO 5 at.%. Degradasi tertinggi ditunjukkan oleh Fe:ZnO/MMT 12 at.%. Efektifitas fotokatalitik yang hampir mencapai 100% diperoleh dengan menggunakan dosis katalis sebesar 0.7gr/L untuk mendegradasi 20 mg/L zat pewarna CR pada pH netral. Jenis ROS yang paling berperan pada penelitian ini berturut-turun ialah e- > h+ >
OH.
Daftar Acuan
[1] V. Chandraboss, L. Natanapatham, B. Karthikeyan, J. Kamalakkannan, S. Prabha and S. Senthilvelan, "Effect of bismuth doping on the ZnO nanocomposite material and study of its photocatalytic activity under UV-light," Materials Research Bulletin, vol. 48, pp. 3707-3712, 2013.
[2] Y. Wei, X. Zhang, J. Xu, J. Wang, Y. Huang, L. Fan and J. Wu, "Enhanchement of photocatalytic activity from HCa2TaxNb3-xO10 (x=0,1), co-intercalated with sulfides particles," Applied Catalysis B: Environmental, vol. 147, pp. 920-928, 2014.
[3] V. Gupta and Suhas, "Application of low-cost adsorbents for dye removal - A review,"
Jornal of Environmental Management, vol. 90, pp. 2313-2342, 2009.
photocatalytic activity of 20 wt%SrO-CuBi2O4 composite," Applied Surface Science, vol. 258, pp. 5010-5024, 2012.
[5] T. Szabo, J. Nemeth and I. Dekany, "Zinc oxide nanaoparticles incorporated in ultrathin layersilicate fils and their photocatalytic properties," Colloids Surface, vol. A 230, pp. 23-35, 2004.
[6] P. Wongkalasina, S. Chavadej and T. Sreethawonga, "Photocatalytic degradation of mixed azo dyes in aqueous wastewater using mesoporous-assambled TiO2 nanao-crystal
synthesized by a modified sol-gel process," Colloids Surface, vol. A 384, pp. 519-528, 2011.
[7] M. Hoffmann, S. Martin, W. Choi and D. Bahnemann, "Environmental application of semiconductor photocatalysis," Chemical Reviews, vol. 95, pp. 69-96, 1995.
[8] T. Jia, W. Wang, F. Long, Z. Fu, H. Wang and Q. Zhang, "Fabrication, characterization and photocatalytic activity of La-doped ZnO nanowires," Journal of Alloys Compounds, vol. 484, pp. 410-415, 2009.
[9] C. Wu and Q. Huang, "Synthesis of Na-doped ZnO nanowires and their photocatalytic properties," Journal of Luminescene, vol. 130, pp. 2136-2141, 2010.
[10] B. Donkova, D. Dimitrov, M. Kostadinov, E. Mitkova and D. Mehandijiev, "Catalytic and photocatalytic activity of lighty doped catalysts M:ZnO (M = Cu, Mn)," Materials
Chemistry and Physics, vol. 123, pp. 563-568, 2010.
[11] K. Apiwong-ngarm, P. Pongwang, B. Inceesungvorn, S. Phanichphant, K. Wetchakun and N. Wetchakun, "Photocatalytic avtivities of Fe-Cu/TiO2 on mineralization of oxalic acid and formic acid under visible light irradiation," Powder Technology, vol. 266, pp. 447-455, 2014.
[12] Y. Zhang, M. Ram, E. Stefanakos and D. Goswami, "Enhanced photocatalytic activity of iron doped zinc oxide nanowires for water decontamination," Surface and Coatings
Technology, vol. 217, pp. 119-123, 2013.
[13] M. M. Ba-Abbad, A. A. H. Kadhum, A. B. Mohamad, M. S. Takriff and K. Sopian, "Visible light photocatalytic activity of Fe3+ -doped ZnO nanoparticle prepared via sol-gel
technique," Chromosphere, vol. 91, pp. 1604-1611, 2013.
[14] D. Bhatkhande, V. Pangarkar and A. Beenackers, "Photocatalytic degradation using TiO2 for environmental application - a review," Journal of Chemical Technology and
Biotechnology, vol. 77, pp. 102-116, 2002.
[15] J. Hu, J. Ma, L. Wang and H. Huang, "Synthesis and photocatalytic properties of LaMnO3-graphene nanacomposites.," Journal of Alloys and Compounds, vol. 583, pp. 539-545, 2014. [16] R. Djellabi, M. Ghorab, G. Cerrato, S. Morandi, S. Gatto, V. Oldani, A. D. Michele and C.
Bianchi, "Photoactive TiO2-Montmorillonite composite for degradation of organic dye in water," Journal of Photochemistry and Photobiology A: Chemistry, vol. 295, pp. 57-63, 2014.
[17] E. Dvininov, E. Popovici, R. Pode, L. Cocheci, P. Barvinschi and V. Nica, "Synthesis and characterization of TiO2-pillared Romania clay and their application for azoic dyes photodegradation," Journal of Hazardous Materials, vol. 167, pp. 1050-1056, 2009. [18] F. Quan, Y. Hu, X. Zhang and C. Wei, "Simple preparation of Mn-N-codoped TiO2
photocatalys and the enhanced photocatalytic activity under visible light irradiation,"
Applied Surface Science, vol. 320, pp. 120-127, 2014.
[19] C. Aydin, M. A. El-sadek, K. Z. Zheng, I. Yahia and F. Yakuphanoglu, "Synthesis, diffused reflectance and electrical properties of nanocrystalline Fe-doped ZnO via sol–gel calcination technique," Optics and Laser Technology., vol. 48, pp. 447-452, 2013.
[20] W. Oueslati, H. B. Rhaiem and A. B. H. Amara, "XRD investigations of hydrated
homoionic montmorillonite saturated by several heavy metal cations," Desalination, vol. 271, p. 139–149, 2011.
[21] N. H. H. Hairom, A. W. Mohammad and A. A. H. Kadhum, "Influence of zinc oxide nanoparticles in the nanofiltration of hazardous Congo red dyes," Chemical Engineering
Journal, vol. 260, pp. 907-915, 2015.
[22] J. Kaur, R. Kotnala, V. Gupta and K. C. Verma, "Anionic polymerization in Co and Fe doped ZnO: Nanorods, magnetism and photoactivity," Current Applied Physics, vol. 14, pp. 749-756, 2014.
[23] Q. Xiao and C. Yao, "Preparation and visible light photocatalytic activity of Zn1−xFexO nanocrystalline," Materials Chemistry and Physics, vol. 130, pp. 5-9, 2011.
[24] N. Khaorapapong, N. Khumchoo and M. Ogawa, "Preparation of zinc oxide– montmorillonite hybrids," Materials Letters , vol. 65, p. 657–660, 2011.
[25] E. Du, S. Yu, L. Zuo, J. Zhang, X. Huang and Y. Wang, "Pb(II) sorption on molecular sieve analogues of MCM-41 synthesized from kaolinite and montmorillonite.," Applied Clay
Science, vol. 51, p. 94–100, 2011.
[26] D. Chen, Z. Honglei and X. Wang, "A facile method to synthesize the photocatalytic TiO2/montmorillonite nanocomposites with enhanced photoactivity," Applied Surface
Science, vol. 319, p. 158–166, 2014.
[27] S. C. Motshekga, S. S. Ray, M. S. Onyango and M. N. Momba, "Microwave-assisted synthesis, characterization and antibacterial activity of Ag/ZnO nanoparticles supported bentonite clay," Journal of Hazardous Materials, vol. 262, p. 439–446, 2013.
[28] J. Das, I. Evans and D. Khushalani, "Zinc glycolate: a precursor to ZnO," Inorganic
Chemistry , vol. 48, pp. 3508-3510, 2009.
[29] R. Saleh and N. F. Djaja, "UV light photocataytic degradation of organic dyes with Fe-doped ZnO nanoparticles," Superlattices and Microstructures, vol. 74, pp. 217-233, 2014. [30] J. C. Joo, C. H. Ahn, D. G. Jang, Y. H. Yoon, J. K. Kim, L. Campos and H. Ahn,
"Photocatalytic degradation of trichloroethylene in aqueous phase usig nano-ZNO/Laponite composites," Journal of Hazardous Materials, vol. 263, pp. 569-574, 2013.
[31] Z.-J. Wu, W. Huang, K.-K. Cui, Z.-F. Gao and P. Wang, "Sustainable synthesis of metals-doped ZnO nanoparticles from zinc-bearing dust for photodegradation of phenol," Journal
of Hazardous Materials, vol. 278, pp. 91-99, 2014.
[32] G. Williamson and W. Hall, "X-ray line broadening from filed aluminium and wolfram,"
Acta Metallurgica, vol. 1, no. 1, p. 22–31, 1953.
[33] A. Mittal, J. Mittal, A. Malviya and V. Gupta, "Adsorptive removal of hazardous anionic dye ‘‘Congo red” from wastewater Adsorptive removal of hazardous anionic dye ‘‘Congo red” from wastewater," Journal of Colloid and Interface Science, vol. 340, p. 16–26, 2009 . [34] T. Pandiyarajan and B. Karthikeyan, "Optical properties of annealing induced post growth
ZnO:ZnFe2O4 nanocomposites," Spectrochimica Acta Part A: Molecular and Biomolecular
Spectroscopy , vol. 106, p. 247–252, 2013.
[35] A. Mishra and D. Das, "Investigation on Fe-doped ZnO nanostructures prepared by chemical rout," Matterial Science and Engineering B, vol. 171, pp. 5-10, 2010. [36] X. Su, Y. Jia, X. Liu, J. Wang, J. Xu, X. He, C. Fu and S. Liu, "Preparation, dielectric
property and infrared emissivity of Fe-doped ZnO powder by coprecipitation method at various reaction time," Ceramics International, vol. 40, no. 4, pp. 5307-5311 , 2014.
[37] T. Rattana, S. Suwanboon, P. Amornpitoksuk, A. Haidoux and P. Limsuwan,
".”Improvement of optical properties of nanocrystalline Fe-doped ZnO powders through precipitation method from citrate-modified zinc nitrate solution.," Journal of Alloys and
Compounds, vol. 480 , p. 603–607, 2009.
[38] K. Kumar, M. Chitkara, I. S. Sandhu, D. Metha and S. Kumar, "Photocatalytic, optical and magnetic properties of Fe-doped ZnO nanoparticles preare by chemical route," Journal of
Alloys and Compounds, vol. 588, pp. 681-689, 2014.
[39] H. Boukhatem, L. Djouadi, N. Abdelaziz and H. Khalaf, "Synthesis, characterization and photocatalytic activity of CdS– montmorillonite nanocomposites," Applied Clay Science, vol. 72, p. 44–48, 2013.
[40] T. An, J. Chen, G. Li, X. Ding, G. Sheng and J. Fu, "Character ization and the photoc atalytic activity of TiO2 immobilized hydrophobic montmorillonite photocatalysts
Degradation of decabromodiphenyl ether (BDE 209)," Catalysis Today, vol. 139, p. 69–76, 2008.
[41] C. Xu, H. Wu and F. L. Gu, "Efficient adsorption and photocatalytic degradation of Rhodamine B under visible light irradiation over BiOBr/montmorillonite composite,"
Journal of Hazardous Materials , vol. 275, p. 185–192, 2014.