VALIDASI METODE ANALISIS RESIDU ANTIBIOTIK
TETRASIKLIN DALAM DAGING AYAM PEDAGING
SECARA KROMATOGRAFI CAIR KINERJA TINGGI
DEDEH SURYANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2009
Ayam Pedaging Secara Kromatografi Cair Kinerja Tinggi Dibimbing oleh HENDRA ADIJUWANA dan RAPHAELLA WIDIASTUTI.
Tetrasiklin (TC), oksitetrasiklin (OTC), dan klortetrasiklin (CTC) ialah antibiotik yang umum digunakan sebagai obat-obatan veteriner yang sering digunakan oleh peternak ayam untuk pencegahan penyakit. Penggunaan yang berlebihan dapat meninggalkan residu antibiotik golongan tetrasiklin dalam produk peternakan tersebut termasuk daging ayam. Implikasi klinis akibat mengonsumsi produk ternak yang mengandung residu antibiotik antara lain alergi, keracunan, dan resistensi terhadap antibiotik tertentu. Residu antibiotik dalam daging ayam pedaging dapat dianalisis dengan kromatografi cair kinerja tinggi (KCKT) secara simultan dengan detektor berkas fotodioda pada panjang gelombang 355 dan 368 nm. Daging ayam pedaging diekstraksi dengan larutan bufer McIlvaine-EDTA dan dihilangkan proteinnya dengan asam trikloroasetat lalu dimurnikan dalam kolom SPE C18. Residu antibiotik tetrasiklin selanjutnya dianalisis dengan KCKT menggunakan kolom C18 Bondapak dan fase gerak asam oksalat 0,0025 M-asetonitril (4:1) dengan laju alir 1 ml/menit. Uji linearitas menghasilkan koefisien korelasi 0,99969 untuk OTC; 0,99947 untuk TC; dan 0,99934 untuk CTC. Hasil uji perolehan kembali berdasarkan metode penambahan standar sebesar 48-116% dengan batas keberterimaan sebesar 80-120%. Batas deteksi untuk OTC, TC, dan CTC berturut-turut sebesar 5,28; 5,09; dan 10,52 ppb dengan batas kuantitasi sebesar 5,93; 5,3; dan 13,52 ppb. Hasil uji analisis sampel daging ayam pedaging yang berasal dari wilayah Jakarta, Bekasi, dan Depok menunjukkan bahwa kadar residu antibiotik golongan tetrasiklin berkisar 5 sampai 68 ppb. Berdasarkan batas maksimum residu antibiotik golongan tetrasiklin dalam daging menurut SNI 01-6066-2000, yaitu 100 ppb, daging ayam tersebut masih relatif aman untuk dikonsumsi.
ABSTRACT
DEDEH SURYANI. Validation of Analytical Method for Tetracyclines Antibiotic Residues in Broiler Chicken Meat by High Performance Liquid Chromatography. Supervised by HENDRA ADIJUWANA and RAPHAELLA WIDIASTUTI.
Tetracyline (TC), oxytetracycline (OTC), and chlortetracycline (CTC) are antibiotics that have been widely used by poultryman to prevent diseases in dairy broiler chicken. Overuse of these antibiotics may lead to the presence of its residues in animal products including meat. Clinic implication which are caused by the consumption of animal products contains antibiotic residues are allergy, intoxication, and spesific of antibiotic resistance. Tetracyclines residue in broiler chicken meat can be analyzed with high performance liquid chromatography (HPLC) simultaneously with photodiode array detector on wavelength of 355 and 368 nm. The meat was extracted with McIlvaine-EDTA buffer solution and trichloroacetic acid to separate its proteins then purified in SPE C18. Tetracyclines residues was further analyzed with HPLC by using C18 Bondapak column and oxalic acid 0,0025 M-acetonitrile (4:1) with flow rate 1 ml/min. The linearity test presented a correlation coefficient of 0.99969 for OTC, 0.99947 for TC, and 0.99934 for CTC. Recovery was 48-116% according to standard addition method with acceptable limit 80-120%. The limit of detection for OTC, TC, and CTC were 5.28, 5.09, and 10.52 ppb and limit of quantitation for OTC, TC, and CTC were 5.93, 5.3, and 13.52 ppb, respectively. The analysis of broiler chicken meat from Jakarta, Bekasi, and Depok showed the amount of tetracyclines residue were from 5 to 68 ppb. According to the maximum residue limit stipulated by SNI 01-6066-2000 (100 ppb), therefore, these broiler chicken meat samples were relatively safe to be consumed.
SECARA KROMATOGRAFI CAIR KINERJA TINGGI
DEDEH SURYANI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2009
Judul : Validasi Metode Analisis Residu Antibiotik Tetrasiklin dalam Daging
Ayam Pedaging secara Kromatografi Cair Kinerja Tinggi
Nama : Dedeh Suryani
NIM : G44052693
Menyetujui:
Pembimbing I,
Pembimbing II,
Ir. Hendra Adijuwana, MST.
Dr. Raphaella Widiastuti
NIP 19440717 196703 1 001
NIP 19621023 198603 2 0001
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor,
Dr. drh. Hasim, DEA
NIP 19610328 198601 1 002
PRAKATA
Segala puji bagi Allah SWT berkat limpahan rahmat dan karunia-Nya penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini dilaksanakan dari bulan Maret sampai Juli 2009 yang bertempat di Laboratorium Toksikologi Balai Besar Penelitian Veteriner (Bbalitvet) Bogor.
Penulis mengucapkan terima kasih kepada Bapak Ir. Hendra Adijuwana, MST selaku Pembimbing Utama dan Ibu Dr. Raphaella Widiastuti selaku Pembimbing Kedua dari Bbalitvet yang telah banyak memberikan petunjuk dan dukungan kepada penulis. Penulis juga mengucapkan terima kasih kepada Mbak Yessy Anastasia, Bapak Rahmat, dan Ibu Siti Djuariah yang telah membantu penulis dalam menggunakan instrumen serta pemakaian alat dan bahan di laboratorium.
Ungkapan terima kasih kepada Ayah, Ibu, adik, dan seluruh keluarga atas semangat, kasih sayang, dan dukungannya. Ucapan terima kasih untuk Mochamad Luqmanul Hakim, Kak Tuti, serta temanku Savitri, Fajar, Yogie, Ired, teman-teman Pinoyers yang telah memberikan semangat, motivasi, dan dorongan dalam menyusun karya ilmiah ini.
Semoga tulisan ini bermanfaat dan dapat menambah wawasan ilmu pengetahuan bagi penulis khususnya dan pembaca umumnya.
Bogor, Oktober 2009
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 24 September 1987 sebagai anak pertama dari dua bersaudara, anak dari pasangan Suryana dan Endah.
Tahun 1999 penulis menyelesaikan sekolah di SDN Mulya Jaya dan pada tahun 2002 penulis menyelesaikan sekolahnya di SLTPN 5 Tambun. Pada tahun yang sama penulis diterima di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) IPB melalui jalur USMI (Undangan Seleksi Masuk IPB).
Selama mengikuti perkuliahan, penulis pernah menjadi asisten praktikum mata kuliah kimia lingkungan pada tahun ajaran 2007/2008. Penulis juga pernah mengikuti kegiatan Praktik Lapangan di Laboratorium Mikrobiologi, Bagian Pengawetan Kayu, Balai Penelitian dan Pengembangan Biomaterial LIPI Cibinong selama periode bulan Juli-Agustus 2008.
DAFTAR ISI
Halaman DAFTAR GAMBAR ... vi DAFTAR TABEL ... vi DAFTAR LAMPIRAN ... vi PENDAHULUAN ... 1 TINJAUAN PUSTAKA Tetrasiklin ... 1Daging Ayam Pedaging ... 2
Residu Antibiotik Golongan Tetrasiklin ... 2
Kromatografi Cair Kinerja Tinggi... 3
Validasi Metode Analisis... 3
BAHAN DAN METODE Alat dan Bahan ... 4
Metode ... 4
HASIL DAN PEMBAHASAN Parameter KCKT-Detektor PDA ... 5
Presisi ... 6
Linearitas ... 6
Batas Deteksi dan Batas Kuantitasi ... 7
Perolehan Kembali (Akurasi) ... 7
Residu Antibiotik Golongan Tetrasiklin dalam Daging Ayam Pedaging ... 8
SIMPULAN DAN SARAN Simpulan ... 10
Saran ... 10
DAFTAR PUSTAKA ... 10
DAFTAR TABEL
Halaman
1 Presisi antibiotik golongan tetrasiklin konsentrasi 1 dan 2 ppm ... 6
2 Batas terendah antibiotik golongan tetrasiklin... 8
3 Perolehan kembali oksitetrasiklin (OTC), tetrasiklin (TC), dan klortetrasiklin (CTC) ... 8
4 Residu antibiotik golongan tetrasiklin dalam daging ayam pedaging ... 9
DAFTAR GAMBAR
Halaman 1 Struktur kimia tetrasiklin ... 12 Struktur kimia oksitetrasiklin ... 2
3 Struktur kimia klortetrasiklin ... 2
4 Spektrum serapan sinas UV-VIS tetrasiklin (a), oksitetrasiklin (b), dan klortetrasiklin (c) ... 6
5 Linearitas antibiotik golongan tetrasiklin... ... 7
DAFTAR LAMPIRAN
Halaman 1 Kromatogram presisi OTC, TC, dan CTC ... 142 Kromatogram linearitas OTC,TC, dan CTC ... 19
3 Kromatogram batas deteksi OTC,TC, dan CTC ... 24
PENDAHULUAN
Daging ayam merupakan salah satu komoditas peternakan yang memiliki nilai gizi sejajar dengan nilai gizi daging lainnya. Konsumsi daging ayam masyarakat Indonesia meningkat 10% per tahun (Rumiati 2003).
Oleh karena itu, pengawasan untuk
menghasilkan daging ayam bermutu tinggi, bebas dari cemaran maupun residu bahan kimia terutama obat-obatan serta aman dikonsumsi perlu dilakukan.
Antibiotik selama ini digunakan untuk pengobatan dan sebagai imbuhan pakan agar hewan ternak tersebut bebas dari penyakit
sehingga pertumbuhan badannya tidak
terhambat. Pemakaian antibiotik yang tidak beraturan dapat menyebabkan residu dalam jaringan organ yang dapat menyebabkan reaksi alergi, resistensi dan mungkin keracunan sehingga cukup berbahaya bagi kesehatan manusia (Yuningsih 2004). Salah satu antibiotik yang digunakan ialah tetrasiklin yang berfungsi sebagai antibakteri (Castellari & Regueiro 2003). Tetrasiklin merupakan antibiotik yang dihasilkan oleh
Streptomyces sp. dan umum digunakan untuk
melawan beberapa jenis bakteri (Berrensen & Rhijn 2006). Tetrasiklin bekerja secara bakteriostatik dan dapat mencegah penyakit yang ditimbulkan baik oleh bakteri gram positif maupun negatif seperti Sphirocete,
Actynomycetes, Ricketsia, dan Mycoplasma
(Cherlet et al. 2003).
Antibiotik tetrasiklin yang ditambahkan ke
dalam pakan ayam pedaging dapat
menimbulkan residu dalam daging ayam tersebut. Adanya residu antibiotik ini pada daging ayam dapat mengganggu kesehatan manusia antara lain timbulnya resistensi terhadap antibiotik tersebut (Oktateria 2008). Untuk memastikan produk pangan aman
untuk dikonsumsi, Badan Standarisasi
Nasional (BSN 2000) menetapkan batas maksimal residu (BMR) yang tercantum dalam SNI 01-6366-2000 yang menetapkan bahwa batas cemaran residu tetrasiklin pada produk hewan ternak ialah 100 ppb pada daging, 50 ppb pada telur, dan 50 ppb pada susu.
Residu antibiotik tetrasiklin dalam bahan pangan jumlahnya sangat kecil sehingga diperlukan suatu metode analisis yang baik
dan teliti. Berbagai metode telah
dikembangkan dalam penentuan residu
antibiotik ini. Pengembangan metode
dilakukan untuk mendapatkan metode deteksi yang lebih cepat dan teliti. Salah satunya ialah
yang dikembangkan oleh Cinquina et al. (2003) serta Castellari dan Regueiro (2003) yang melaporkan bahwa metode KCKT dengan detektor berkas fotodioda dapat digunakan untuk penentuan residu antibiotik tetrasiklin dalam daging ternak.
Hipotesis yang diajukan dalam penelitian ini ialah bahwa metode KCKT dengan detektor berkas fotodioda (PDA) UV dapat
digunakan untuk menganalisis residu
antibiotik tetrasiklin pada daging ayam pedaging.
Penelitian ini bertujuan memvalidasi metode analisis dan menentukan tingkat residu antibiotik golongan tetrasiklin pada sampel lapang daging ayam pedaging asal Jakarta, Bekasi, dan Depok secara KCKT.
TINJAUAN PUSTAKA
Tetrasiklin
Tetrasiklin ialah antibiotik yang umum digunakan sebagai obat-obatan veteriner dan diisolasi dari bakteri Streptomyces sp.. Penggunaan tetrasiklin sebagai obat-obatan veteriner umumnya dicampurkan ke dalam pakan. Tetrasiklin merupakan antibiotik yang bersifat bakteriostatik dan bekerja dengan jalan menghambat sintesis protein kuman. Tetrasiklin memiliki spektrum yang luas, artinya antibiotik ini memiliki kemampuan melawan sejumlah bakteri patogen (Yuningsih 2004).
Tetrasiklin merupakan senyawa kristal berwarna kuning dan sedikit larut dalam air. Pada suhu 28°C kelarutan tetrasiklin dalam air sebesar 1,7 mg/ml sedangkan dalam metanol lebih dari 20 mg/ml (Schunack et al. 1990).
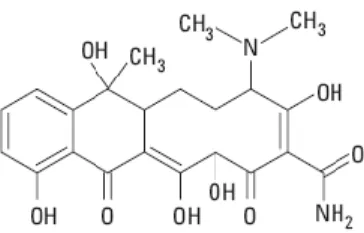
Tetrasiklin memiliki rumus molekul
C22H24N2O8 dan memiliki nama IUPAC [4s-(4α,4aα,5aα,6β,12aα)] -4- (dimetilamino) 1,4,4a,5,5a, 6-11,12a-oktahidro-3,6,10,12,12a- pentahidroksi- 6- metil -1,11-diokso- 2- naftasenkarboksamida dengan bobot molekul 444,44 g/mol (Gambar 1).
Gambar 1 Struktur kimia tetrasiklin Oksitetrasiklin merupakan tetrasiklin dengan tambahan satu gugus OH pada
struktur cincinnya. Oksitetrasiklin dengan rumus molekul C22H24N2O9 memiliki nama IUPAC [ 4s - (4α,4aα,5α,5aα,6β,12aα)] – 4 - (dimetilamino) 1 ,4 ,4 a,5 ,5a ,6 11,12a -oktahidro-3, 5, 6, 10, 12, 12a- heksahidroksi-6-metil-1,11-diokso- 2- naftasenkarboksamida dan bobot molekul 460,44 g/mol (Gambar 2). Oksitetrasiklin berbentuk serbuk halus berwarna kuning muda dan tidak berbau. Oksitetrasiklin memiliki kelarutan yang lebih besar dibandingkan tetrasiklin, yaitu 1g/ml pada suhu 28°C dan sangat mudah larut dalam etanol.
Gambar 2 Struktur kimia oksitetrasiklin Klortetrasiklin merupakan tetrasiklin dengan tambahan satu atom klor pada struktur cincinnya. Klortetrasiklin berbentuk serbuk halus berwarna kuning keemasan dan sedikit larut dalam air (8,6 mg/ml). Klortetrasiklin dapat larut dalam alkali hidroksida, dioksan, karbitol, etanol, butanol, aseton, etil asetat, benzena, dan sedikit larut dalam metanol. Klortetrasiklin memiliki nama IUPAC [4s - (4α, 4aα, 5aα, 6β, 12aα) ] - 7 - kloro – 4 - (dimetilamino)- 1, 4, 4a, 5, 5a, 6 - 11, 12a – oktahidro - 3, 6, 10, 12, 12a – pentahidroksi - 6-metil-1,11-diokso-2- naftasenkarboksamida dengan bobot molekul 478,89 g/mol (Gambar 3).
Gambar 3 Struktur kimia klortetrasiklin Selain keempat jenis antibiotik yang telah disebutkan masih ada turunan lain dari antibiotik tetrasiklin antara lain doksisiklin, demeklosiklin, metasiklin, minosiklin, dan rolitetrasiklin.
Daging Ayam Pedaging
Daging didefinisikan sebagai semua
jaringan hewan dan semua hasil pengolahan jaringan-jaringan tersebut yang sesuai untuk
dimakan serta tidak menimbulkan gangguan kesehatan bagi yang memakannya (Soeparno 1994). Daging ayam merupakan jenis bahan pangan yang bernilai gizi tinggi dan
berperanan penting dalam memperbaiki
kualitas sumberdaya manusia. Daging ayam yang beredar di Indonesia sebagian besar berasal dari ayam pedaging. Ayam pedaging ialah ayam ras yang mampu tumbuh cepat sehingga dapat menghasilkan daging dalam waktu relatif singkat, yaitu 5-7 minggu. Ayam pedaging memiliki peranan yang penting sebagai sumber protein hewani asal ternak (Resnawati 2005).
Daging ayam yang sehat memiliki ciri bersih/terang dan lapisan luarnya kering, daging yang sudah ditiriskan tidak berdarah, aroma baunya tidak amis, tidak kaku, dan tidak bau asam. Daging ayam pedaging memiliki kadar kolesterol yang rendah dan kaya vitamin B dan mineral sehingga sangat diperlukan untuk kesehatan sistem syaraf dan pertumbuhan.
Residu Antibiotik Golongan Tetrasiklin Residu antibiotik dalam makanan asal hewan erat kaitannya dengan penggunaan antibiotik untuk pencegahan dan pengobatan
penyakit serta penggunaannya sebagai
imbuhan pakan (Riti et al. 2002). Penambahan obat hewan antibakteri (antibiotik) ke dalam ransum pakan ternak bertujuan meningkatkan
laju pertumbuhan berat badan atau
meningkatkan laju efisiensi pakan.
Penggunaan obat-obatan tersebut
meningkat tajam khususnya bagi ternak sapi pedaging dan ayam pedaging agar laju
pertumbuhan badannya semakin cepat.
Antibiotik pada ternak juga diberikan dalam bentuk suntikan. Apabila hewan ternak yang baru saja mendapatkan suntikan antibiotik atau ransum tersebut segera dipotong, dapat meninggalkan residu obat-obatan di dalam daging ternak, telur, susu atau produk ternak lainnya. Menurut Rico (1986), keberadaan residu antibiotik dalam pangan asal hewan dapat mengakibatkan efek yang buruk bagi manusia, diantaranya alergi, keracunan, karsinogen, dan resistensi terhadap antibiotik tertentu.
Konsumsi pangan asal hewan yang diberikan antibiotik tidak dilarang asalkan berada di bawah batas maksimum residu (BMR). BMR antibiotik golongan tetrasiklin dalam daging dan susu tidak boleh melebihi
100 ppb menurut SNI 01-6366-2000.
Berbagai metode telah dikembangkan utuk menganalisis residu antibiotik dalam pangan 2
hasil ternak diantaranya metode KCKT untuk analisis tetrasiklin dan oksitetrasiklin dalam susu (Fletouris et al. 1990) dan daging (Moats & Khan (1995). Analisis residu tetrasiklin dalam madu (Martel et al. (2006) dan ikan salmon (Rupp & Anderson (2005).
Kromatografi Cair Kinerja Tinggi Kromatografi cair kinerja tinggi (KCKT), merupakan suatu teknik kromatografi dengan fase gerak cairan dan fase diam cairan atau padat. Parameter KCKT yang digunakan untuk analisis kuantitatif ialah waktu retensi atau volume retensi. Perhitungan kuantitatif didasarkan pada pengukuran tinggi puncak atau luas puncak suatu komponen zat.
Populernya penggunaan KCKT
disebabkan teknik ini memiliki beberapa
keunggulan, yaitu mampu memisahkan
molekul-molekul dari suatu campuran,
kecepatan analisis, kepekaan yang tinggi dan resolusi yang baik. Selain itu, kolom dapat digunakan kembali, dapat menggunakan
bermacam-macam detektor, dan dapat
menghindari terjadinya dekomposisi atau kerusakan bahan yang dianalisis (Adnan 1997).
Berdasarkan perbedaan fase, KCKT
terbagi menjadi dua, yaitu fase normal dan fase terbalik. Fase normal ialah fase diam yang berupa senyawa polar dan fase gerak senyawa nonpolar. Sementara fase terbalik ialah fase diam yang berupa senyawa nonpolar dan fase gerak senyawa polar (Adnan 1997). Menurut Gritter et al. (1991), kromatografi menggunakan fase terbalik sehingga senyawa polar akan lebih baik
pemisahannya, senyawa ionik dapat
dipisahkan, dan air dapat digunakan sebagai salah satu komponen pada fase gerak. Susunan peralatan KCKT tidak banyak berbeda dengan kromatografi gas-cair. Komponen utama pada KCKT antara lain reservoir pelarut untuk fase gerak, pompa, pencampur gradien, injektor, kolom, detektor, rekorder, dan integrator.
Detektor dibutuhkan untuk mendeteksi adanya komponen sampel di dalam kolom (analisis kualitatif) dan menghitung kadarnya (analisis kuantitatif). Detektor yang baik memiliki sensitivitas yang tinggi, derau (noise) yang rendah, kisaran respon linear yang luas, dan memberi respons untuk semua tipe senyawa. Detektor KCKT yang umum digunakan ialah detektor UV 254 nm. Variabel panjang gelombang dapat digunakan untuk mendeteksi banyak senyawa dengan kisaran yang lebih luas. Detektor indeks
refraksi juga digunakan secara luas, terutama pada kromatografi eksklusi, tetapi umumnya kurang sensitif jika dibandingkan dengan detektor UV. Detektor-detektor lain yang digunakan antara lain detektor fluororesensi, spektroskopi massa, dan berkas fotodioda (Putra 2004). Detektor berkas fotodioda (PDA) UV telah banyak digunakan untuk menganalisis residu antibiotik berdasarkan serapan pada daerah spektrum ultraviolet sampai sinar tampak.
Validasi Metode Analisis
Validasi metode analisis ialah suatu
tindakan penilaian terhadap parameter
tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk digunakannya. Validasi metode analisis merupakan suatu proses pembuktian melalui pengujian analisis di laboratorium untuk memberikan data tentang keandalan suatu metode dari suatu prosedur yang digunakan.
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis diuraikan dan didefinisikan sesuai dengan cara penentuannya (Harmita 2004). Parameter yang digunakan ialah batas deteksi dan kuantitasi, presisi, akurasi, dan linearitas.
Selain itu digunakan pula parameter
keterulangan (repeatability) dan ketangguhan (rudgedness) (CDER 1994).
Batas deteksi ialah jumlah terkecil analit dalam sampel yang dapat dideteksi yang
masih memberikan respon signifikan
dibandingkan dengan blangko. Batas deteksi
merupakan parameter uji batas. Batas
kuantitasi merupakan parameter pada analisis renik dan diartikan sebagai kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan saksama.
Presisi ialah ukuran yang menunjukkan derajat kesesuaian antarhasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran yang homogen. Menurut CDER (1994), presisi dibagi menjadi tiga, yaitu keterulangan (repeatability), ketertiruan (reproducibility), dan presisi antara (intermediate precision). Keterulangan ialah presisi metode jika dilakukan berulang kali oleh analis yang sama pada kondisi sama dan
dalam interval waktu yang pendek.
Ketertiruan ialah presisi metode jika dilakukan berulang kali oleh analis yang berbeda pada kondisi berbeda. Presisi antara merupakan ukuran ketertiruan pada kondisi
operasi normal antara laboratorium dan antaranalis.
Akurasi ialah ukuran yang menunjukkan kedekatan nilai hasil analisis dengan kadar analit yang sebenarnya (CDER 1994).
Kecermatan dinyatakan sebagai persen
perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan dengan dua cara yaitu, metode simulasi
(spiked-placebo recovery) dan metode penambahan
standar (standard addition method).
Linearitas ialah kemampuan metode
analisis yang memberikan respons secara langsung atau dengan bantuan transformasi matematika yang baik dan proporsional terhadap konsentrasi analit dalam sampel. Linearitas biasanya dinyatakan dalam variansi sekitar arah garis regresi yang dihitung
berdasarkan persamaan matematika
menggunakan data yang diperoleh dari hasil uji analit dalam sampel dengan berbagai konsentrasi analit. Persamaan dinyatakan dengan rumus y = a + bx, dengan a ialah intersep, b ialah kemiringan garis dengan koefisien korelasi 0,9995 (Harmita 2004).
BAHAN DAN METODE
Alat dan Bahan
Alat–alat yang digunakan dalam penelitian ini ialah KCKT Shimadzu LC 20AD, kolom C18 Bondapak Waters Polaris 5, SPE Cartdrige Bond Elut C18 Varian, mikropipet Socorex 10-100 µl dan 100-1000 µl, mikropipet syringe 50 µl, kertas saring 0.45 µm Waters, dan sentrifus Beckman model Tj-6.
Bahan-bahan yang digunakan dalam penelitian ini ialah daging ayam pedaging, standar tetrasiklin, oksitetrasiklin, dan klortetrasiklin (Vetranal®), SIGMA), dan metanol HPLC Grade. Sampel daging ayam pedaging berasal dari wilayah Jakarta, Bekasi, dan Depok baik dari pasar tradisional maupun swalayan yang diambil secara acak dan tidak mengikuti kaidah statistik.
Metode
Ekstraksi dan Pemurnian Sampel
Metode ekstraksi yang digunakan diadopsi
dari metode yang dikembangkan oleh
Cinquina et al. (2003). Sementara metode
pemurnian sampel yang digunakan
dikembangkan dari Castellari dan Reguiro (2003) berdasarkan referensi dari AOAC
Official Method 995.09 tentang residu
klortetrasiklin, oksitetrasiklin, dan tetrasiklin dalam jaringan hewan.
Sebanyak 5,0 gr daging ayam yang telah diseragamkan ukurannya ditempatkan dalam tabung sentrifus. Setelah itu ditambahkan 2 ml larutan asam trikloroasetat 20% kemudian dikocok menggunakan vorteks. Setelah itu sampel ditambahkan 18 ml larutan bufer McIlvaine-EDTA kemudian diputar pada kecepatan 3000 rpm selama 10 menit. Larutan supernatan hasil sentrifus dipisahkan dari residunya kemudian dimasukkan ke dalam kolom. Ekstraksi diulangi kembali dengan menambahkan 10 ml larutan bufer McIlvaine-EDTA, lalu dikocok menggunakan vorteks. Setelah itu sampel yang telah diekstrak tersebut diputar pada kecepatan 3000 rpm selama 10 menit. Larutan supernatan hasil sentrifus dipisahkan dari residunya kemudian dimasukkan ke dalam kolom. Proses ekstraksi selesai, selanjutnya dilanjutkan dengan
pemurnian sampel menggunakan SPE
Cartridge (kolom) C18.
Kolom sebelumnya diaktifkan terlebih dahulu dengan 20 ml metanol dan 20 ml air. Setelah itu dimasukkan sebanyak 10 ml sampel, kolom dicuci dengan 20 ml metanol 5% dan didiamkan selama 5 menit. Kemudian kolom tersebut dielusi dengan 6 ml metanol oksalat. Setelah itu, filtrat dipindahkan dalam aliran gas nitrogen kemudian dilarutkan dengan 200 µl metanol oksalat. Sebanyak 40 µl sampel dianalisis dengan KCKT.
Larutan Standar Tetrasiklin, Oksitetrasiklin, dan Klortetrasiklin
Sebanyak 10 mg standar tetrasiklin, oksitetrasiklin, dan klortetrasiklin dilarutkan
masing-masing dengan metanol lalu
dimasukkan ke dalam labu takar dan ditepatkan hingga 5 ml untuk mendapatkan konsentrasi larutan standar 2000 ppm. Sebanyak 250 µl larutan standar standar
tetrasiklin, 250 µl larutan standar
oksitetrasiklin, dan 500 µl larutan standar
klortetrasiklin konsentrasi 2000 ppm
dimasukkan ke dalam labu takar 5 ml
kemudian ditepatkan dengan metanol
sehingga didapat konsentrasi larutan standar campuran antibiotik tetrasiklin, oksitetrasiklin, dan klortetrasiklin (1:1:2) 100:100:200 ppm. Larutan tersebut dapat diencerkan kembali untuk pengujian parameter-parameter analisis. Analisis menggunakan KCKT
Sebanyak 40 µl alikuot diinjeksikan ke dalam KCKT Shimadzu seri LC 20AD. Kondisi KCKT sebagai berikut:
Kolom : Bondapak C18 Varian 150×4,6 mm
Sistem : Fase Terbalik
Fase Gerak : Asam oksalat 0.0025 M - asetonitril (4:1, v/v) Laju Alir : 1 ml/menit
Detektor : Berkas fotodioda
355 nm dan 368 nm
Atenuasi : 4 kali
Perhitungan Kadar
Kadar residu antibiotik golongan
tetrasiklin dihitung dengan rumus:
Cs ialah konsentrasi sampel, Cst ialah konsentrasi standar, As ialah luas puncak sampel, Ab ialah luas puncak standar, Vt ialah volume akhir sampel (µl), dan ms ialah bobot sampel (g).
Presisi: Keterulangan (Repeatability) Larutan standar campuran tetrasiklin, oksitetrasiklin, dan klortetrasiklin konsentrasi 1000, 1000, dan 2000 ppb sebanyak 40 µl dianalisis dengan KCKT. Analisis dilakukan sebanyak lima kali ulangan dan dilakukan oleh tiga orang pelaksana. Luas puncak yang diperoleh kemudian ditentukan simpangan baku (SD) dan simpangan baku relatifnya (RSD).
Akurasi: Uji Perolehan Kembali (Recovery
Test)
Sebanyak 5,0 gram sampel daging ayam dimasukkan ke dalam tabung sentrifus lalu ditambahkan 250 µl larutan standar campuran tetrasiklin (1:1:1) konsentrasi 1000 ppb. Perlakuan selanjutnya sama seperti preparasi
sampel. Percobaan diulangi untuk
penambahan 500 µl dan 750 µl larutan standar campuran yang sama. Nilai % perolehan kembali (recovery) dihitung menggunakan rumus:
Ct merupakan konsentrasi tetrasiklin, oksitetrasiklin, dan klortetrasiklin total setelah penambahan standar; Cu ialah konsentrasi tetrasiklin, oksitetrasiklin, dan klortetrasiklin dalam larutan uji (sampel); dan Cs ialah konsentrasi tetrasiklin, oksitetrasiklin, dan klortetrasiklin standar.
Uji Linearitas
Dibuat larutan standar campuran antibiotik tetrasiklin dengan konsentrasi 125, 250, 500, 1000, 2000, dan 4000 ppb. Sebanyak 40 µl larutan dianalisis dengan KCKT. Linearitas ditentukan menggunakan metode regresi kuadrat terkecil sebanyak tiga kali ulangan untuk setiap konsentrasi. Persamaan linearitas yang digunakan ialah y = a + bx dengan a ialah titik potong dan b ialah kemiringan. Penentuan Batas Konsentrasi Terendah
Larutan standar tetrasiklin, oksitetrasiklin, dan klortetrasiklin dengan konsentrasi 50, 25, 10, 5, dan 1 ppb sebanyak 40 µl dianalisis dengan KCKT. Dihitung respons simpangan standarnya menggunakan rumus:
Q ialah batas deteksi dan batas kuantitasi dengan x = luas puncak rata rata konsentrasi terendah, SD atau standar deviasi simpangan standar luas puncak blangko, nilai k = 3 untuk batas deteksi dan 10 untuk batas kuantitasi.
HASIL DAN PEMBAHASAN
Parameter KCKT-Detektor PDA Metode analisis residu antibiotik golongan tetrasiklin dalam daging ayam pedaging secara KCKT diambil dari metode yang dikembangkan oleh Cinquina et al. (2003) serta Castellari dan Reguiro (2003) berdasarkan referensi dari AOAC Official Method 995.09. KCKT yang digunakan ialah KCKT Shimadzu LC-20AD dengan detektor PDA. Detektor tersebut dapat mendeteksi senyawa yang memiliki spektrum serapan pada daerah UV (200-380 nm) dan sinar tampak (380-780 nm). KCKT tersebut juga dapat digunakan untuk menganalisis lebih dari 1 senyawa yang memiliki 2 panjang gelombang yang berbeda secara simultan.
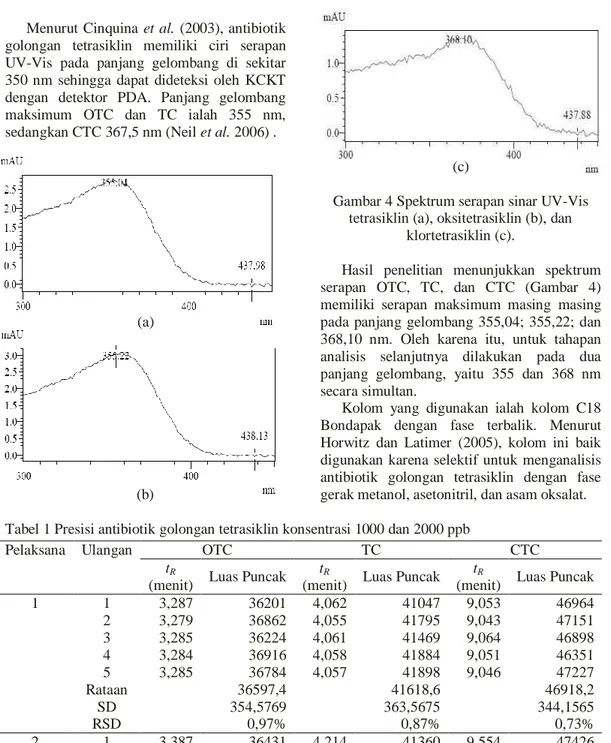
Menurut Cinquina et al. (2003), antibiotik golongan tetrasiklin memiliki ciri serapan UV-Vis pada panjang gelombang di sekitar 350 nm sehingga dapat dideteksi oleh KCKT dengan detektor PDA. Panjang gelombang maksimum OTC dan TC ialah 355 nm, sedangkan CTC 367,5 nm (Neil et al. 2006) .
(a)
(b)
(c)
Gambar 4 Spektrum serapan sinar UV-Vis tetrasiklin (a), oksitetrasiklin (b), dan
klortetrasiklin (c).
Hasil penelitian menunjukkan spektrum serapan OTC, TC, dan CTC (Gambar 4) memiliki serapan maksimum masing masing pada panjang gelombang 355,04; 355,22; dan 368,10 nm. Oleh karena itu, untuk tahapan analisis selanjutnya dilakukan pada dua panjang gelombang, yaitu 355 dan 368 nm secara simultan.
Kolom yang digunakan ialah kolom C18 Bondapak dengan fase terbalik. Menurut Horwitz dan Latimer (2005), kolom ini baik digunakan karena selektif untuk menganalisis antibiotik golongan tetrasiklin dengan fase gerak metanol, asetonitril, dan asam oksalat. Tabel 1 Presisi antibiotik golongan tetrasiklin konsentrasi 1000 dan 2000 ppb
Pelaksana Ulangan OTC TC CTC
tR
(menit) Luas Puncak
tR
(menit) Luas Puncak
tR
(menit) Luas Puncak
1 1 3,287 36201 4,062 41047 9,053 46964 2 3,279 36862 4,055 41795 9,043 47151 3 3,285 36224 4,061 41469 9,064 46898 4 3,284 36916 4,058 41884 9,051 46351 5 3,285 36784 4,057 41898 9,046 47227 Rataan 36597,4 41618,6 46918,2 SD 354,5769 363,5675 344,1565 RSD 0,97% 0,87% 0,73% 2 1 3,387 36431 4,214 41360 9,554 47426 2 3,334 36201 4,127 40891 9,289 46306 3 3,337 36475 4,131 40890 9,293 45979 4 3,346 36391 4,139 40908 9,301 45653 5 3,347 36867 4,140 41422 9,307 45891 Rataan 36473 41094,2 46251 SD 243,7786 271,9195 697,2872 RSD 0,67% 0,66% 1,51% 3 1 3,272 36445 4,048 41657 9,035 47160 2 3,273 36036 4,047 40909 9,033 46949 3 3,294 36416 4,070 40783 9,083 47234 4 3,288 36248 4,064 41245 9,068 46786 5 3,278 36472 4,056 41247 9,079 47218 Rataan 36323,4 41168,2 47069,4 SD 182,8436 341,5395 195,0610 RSD 0,50% 0,83% 0,41% 6
Presisi
Presisi untuk KCKT dilakukan dengan cara menganalisis satu seri larutan standar oleh pelaksana yang berbeda. Presisi pada penelitian ini dilakukan oleh 3 orang pelaksana yang berbeda. Kromatogram presisi dapat dilihat di Lampiran 1. Presisi dikatakan baik jika memiliki nilai simpangan baku relatif kurang dari 2% dengan konsentrasi
0-150% kadar analat (IUPAC 2002).
Berdasarkan hasil pada Tabel 1, simpangan baku relatif OTC, TC, dan CTC masing masing 0,97; 0,87; dan 0,73%. Hal ini menunjukkan bahwa kondisi KCKT telah sesuai dan dapat digunakan untuk analisis residu antibiotik golongan tetrasiklin.
Linearitas
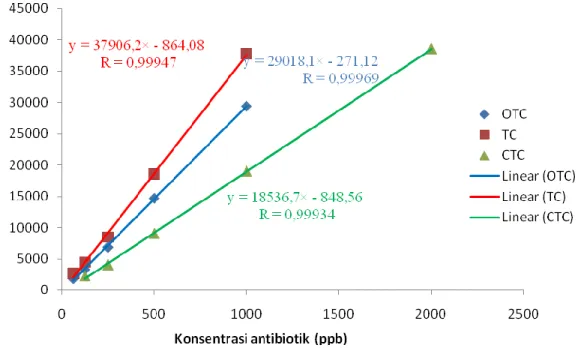
Uji linearitas merupakan suatu metode analisis yang menggambarkan kemampuan suatu alat untuk memperoleh hasil pengujian yang sebanding dengan kadar analat dalam zat uji pada rentang kadar tertentu. Uji linearitas dilakukan dengan membuat kurva kalibrasi dari serangkaian konsentrasi larutan standar antibiotik golongan tetrasiklin. Setelah diperoleh kurva kalibrasi, persamaan regresi dihitung untuk mengetahui hubungan antara konsentrasi antibiotik dengan luas puncak. Kromatogram linearitas OTC, TC, dan CTC dapat dilihat pada Lampiran 2. Persamaan regresi linear yang diperoleh ialah y = 29018,1x - 271,12 untuk OTC, y = 37906,2x - 864,08 untuk TC, dan y =18536,7x - 848,58
untuk CTC. Nilai koefisien korelasi 0,99969 untuk OTC, 0,99947 untuk TC, dan 0,99934 untuk CTC (Gambar 5).
Nilai ini telah memenuhi persyaratan metode yang baik dari segi linearitas, yaitu koefisien korelasi lebih dari 0,9995 (IUPAC 2002). Oleh karena itu, analisis antibiotik golongan tetrasiklin dapat dilakukan secara simultan oleh KCKT.
Batas Deteksi dan Batas Kuantitasi Menurut IUPAC (2002), batas deteksi ialah batas konsentrasi terendah yang masih dapat dideteksi oleh instrumen. Batas deteksi dan batas kuantitasi merupakan ukuran sensitivitas dari KCKT. KCKT tidak dapat mendeteksi keberadaan OTC, TC, dan CTC pada konsentrasi 1 dan 2 ppb (Tabel 2). Hal ini disebabkan pada konsentrasi 1 dan 2 ppb sinyal yang dihasilkan oleh KCKT sangat rendah dan tidak terbaca sebagai sinyal OTC, TC, dan CTC. Oleh karena itu, penentuan batas deteksi dilakukan pada konsentrasi 5 dan 10 ppb. Kromatogram batas deteksi dan batas kuantitasi dapat dilihat di Lampiran 3.
Batas deteksi yang diperoleh untuk OTC, TC, dan CTC berturut turut ialah 5,28; 5,09; dan 10,52 ppb. Oleh karena itu pada konsentrasi di bawah 5,28 ppb, 5,09 ppb, dan 10,52 ppb, kadar OTC, TC, dan CTC tidak dapat ditentukan. Batas kuantitasi yang diperoleh untuk OTC, TC, dan CTC berturut turut ialah 5,93; 5,30; dan 13,52 ppb.
Gambar 5 Linearitas antibiotik golongan tetrasiklin
Tabel 2 Batas terendah antibiotik golongan tetrasiklin Luas Puncak ulangan OTC TC CTC 1 358 367 297 2 352 356 298 3 356 355 302 4 343 356 292 5 361 360 306 rerata 354 358,80 299 SD 6,6106 2,1279 5,1769 LOD (ppb) 5,28 5,09 10,52 LOQ (ppb) 5,93 5,3 13,52
Menurut Badan Standarisasi Nasional (BSN 2000), BMR antibiotik golongan tetrasiklin yaitu 100 ppb, sedangkan nilai batas deteksi yang diperoleh lebih kecil dari nilai BMR tersebut. Hal ini menunjukkan bahwa metode KCKT dapat digunakan untuk
mendeteksi residu antibiotik golongan
tetrasiklin dalam jumlah yang relatif sedikit. Perolehan Kembali (Akurasi) Uji perolehan kembali dilakukan untuk mengetahui kemampuan metode dan untuk mengetahui berapa persen analat yang
ditambahkan dapat ditemukan.kHasil
perolehan kembali untuk OTC 107,3-113,2%, TC 40,8-46,9%, dan CTC 88,2-110,3% (Tabel 3).
Tabel 3 Perolehan kembali oksitetrasiklin (OTC), tetrasiklin (TC), dan klortetrasiklin (CTC)
Antibiotik Standar yang
ditambahkan (ppb) tR (menit) Luas Puncak Konsentrasi yang diperoleh (ppb) % Perolehan kembali Rataan % Perolehan kembali OTC 50 3,198 8045 56,46 113,1 107,3 3,186 8143 57,18 114,6 3,214 6758 46,67 94,1 100 3,183 16069 114,94 115,9 113,2 3,223 15738 113,20 113,4 3,172 15302 109,31 110,2 150 3,198 23218 167,36 112,5 110,5 3,242 22867 166,12 110,7 3,216 22386 160,93 108,4 TC 50 3,911 4425 25,05 50,2 44,7 3,897 4795 27,31 54,7 3,935 2706 14,42 29,1 100 3,907 8655 50,65 51,1 46,9 3,959 9057 53,43 53,5 3,876 6216 35,79 36,1 150 3,914 10070 59,27 39,8 40,8 4,059 11785 70,29 46,9 3,968 9080 53,13 35,8 CTC 50 8,55 9141 56,88 114,0 110,3 8,549 9225 57,43 115,1 8,542 8190 50,44 101,7 100 8,561 17950 112,96 113,9 106,9 8,565 18531 117,39 117,6 8,482 14140 88,56 89,3 150 8,542 20281 127,89 85,9 88,2 8,765 20674 131,47 87,6 8,729 21442 135,06 90,9 8
Menurut Center for Drugs Evaluation and Research (CDER), nilai perolehan kembali ialah 80-120% (CDER 1994). Berdasarkan ketetapan tersebut, nilai perolehan kembali untuk oksitetrasiklin dan klortetrasiklin memenuhi persyaratan. Namun tetrasiklin tidak memenuhi persyaratan nilai perolehan
kembali yang dianjurkan. Hal ini
kemungkinan disebabkan oleh metode analisis yang dilakukan tidak cukup untuk mengurangi pengaruh matriks sampel yang mengganggu.
Residu Antibiotik Golongan Tetrasiklin dalam Daging Ayam Pedaging
Residu antibiotik dalam makanan dan minuman kemungkinan merupakan salah satu faktor penyebab resistensi kuman terhadap antibiotik. Penggunaan antibiotik sebagai bahan pengobatan dan tambahan pakan ternak saat ini masih banyak dilakukan.
Adanya residu dalam daging ayam disebabkan ayam tersebut telah dipotong sebelum dicapai waktu henti (withdrawal Tabel 4 Residu antibiotik golongan tetrasiklin dalam daging ayam pedaging
*tt berarti tidak terdeteksi oleh alat KCKT (untuk OTC ≤ 5,93; TC ≤ 5,3; dan CTC ≤ 13,52 ppb).
Lokasi Kode sampel Konsentrasi Antibiotik (ppb)
OTC TC CTC Jakarta A1 5,98 14,28 35,95 A2 tt tt 38,68 A3 7,35 tt 19,46 A4 22,42 tt 18,09 A5 10,31 tt 14,72 A6 tt tt 44,37 A7 tt tt 19,00 A8 8,69 tt 13,68 A9 tt tt 26,26 A10 10,37 tt 16,34 Bekasi B1 tt tt 18,24 B2 tt tt 15,55 B3 tt tt tt B4 tt tt 15,33 B5 15,35 tt 33,24 B6 tt tt 16,71 B7 12,58 tt 29,45 B8 tt tt 38,98 B9 tt tt 38,96 B10 tt tt 18,71 Depok C1 41,55 tt 31,07 C2 tt tt 26,45 C3 tt tt 43,13 C4 7,88 tt 58,92 C5 6,85 tt 32,34 C6 tt tt 25,70 C7 8,53 58,01 37,69 C8 tt tt 23,81 C9 13,42 tt 46,76 C10 8,40 tt 53,87 9
time), yakni lima hari. Kadar residu oksitetrasiklin dalam daging ayam pedaging asal daerah Jakarta cukup rendah, yaitu sekitar 5-20 ppb (Tabel 4). Begitu juga dengan daging ayam asal daerah Bekasi dan Depok, residu oksitetrasiklin masing-masing sebesar 12-15 ppb dan 6-68 ppb.
Kadar residu tetrasiklin dalam hampir semua sampel daging ayam pedaging berada di bawah nilai batas kuantitasi OTC, TC, dan CTC sehingga tidak terdeteksi oleh alat KCKT atau daging ayam pedaging tersebut tidak mengandung residu tetrasiklin.
Kadar residu klortetrasiklin dalam daging ayam pedaging dari daerah Jakarta, Bekasi, dan Depok ialah yang paling banyak, yaitu 13-58 ppb. Perhitungan kadar OTC, TC, dan CTC dapat dilihat di Lampiran 4. Jumlah kadar residu antibiotik golongan tetrasiklin dalam semua sampel daging ayam pedaging yang dianalisis berada di bawah BMR, yaitu 100 ppb sehingga masih aman untuk dikonsumsi. Kadar residu obat yang melewati BMR yang ditetapkan akan menyebabkan daging tersebut tidak aman dikonsumsi karena
dapat mengakibatkan reaksi alergis,
keracunan, dan resistensi mikrob tertentu.
SIMPULAN DAN SARAN
Simpulan
Kromatografi cair kinerja tinggi dengan detektor PDA layak digunakan untuk analisis residu antibiotik golongan tetrasiklin secara simultan pada panjang gelombang 355 dan 368 nm dengan fase gerak asam oksalat 0,0025 M-asetonitril (4:1) dan laju alir 1 ml/menit. Batas deteksi yang diperoleh KCKT untuk OTC, TC, dan CTC berturut turut ialah 5,28; 5,09; dan 10,52 ppb. Batas kuantitasi OTC, TC, dan CTC berturut turut ialah 5,93; 5,30; dan 13,52 ppb.
Hasil uji-uji parameter validasi yang dilakukan berupa uji presisi, linearitas, batas deteksi, dan batas kuantitasi telah memenuhi persyaratan validasi metode analisis dan memiliki kelayakan yang bagus untuk antibiotik golongan tetrasiklin. Namun untuk uji perolehan kembali, antibiotik tetrasiklin tidak memenuhi persyaratan validasi metode analisis menurut CDER (1994) karena di luar kisaran 80-120%. Nilai perolehan kembali yang didapatkan untuk oksitetrasiklin sebesar 107,3 sampai 113,2 %, tetrasiklin 40,8 sampai 46,9 %, dan klortetrasiklin 88,2 sampai 110,3 %.
Penelitian terhadap 30 sampel daging ayam pedaging asal Jakarta, Bekasi, dan Depok menunjukkan bahwa kadar residu antibiotik golongan tetrasiklin berada di bawah BMR (100 ppb) sehingga masih aman untuk dikonsumsi. Semua sampel daging ayam tersebut positif mengandung antibiotik klortetrasiklin, sedangkan hampir semuanya tidak mengandung residu tetrasiklin.
Saran
Hasil uji perolehan kembali untuk
tetrasiklin masih kurang baik yaitu di bawah 80%. Oleh karena itu, perlu dipelajari dan
dikembangkan metode ekstraksi untuk
mengurangi pengaruh matriks sampel agar tetrasiklin dapat terekstrak dengan baik
sehingga analisis antibiotik golongan
tetrasiklin (oksitetrasiklin, tetrasiklin, dan klortetrasiklin) secara simultan dapat lebih optimal.
DAFTAR PUSTAKA
Adnan M. 1997. Teknik Kromatografi untuk
Analisis Bahan Makanan. Yogyakarta:
Andi Pr.
[AOAC] Association of Official Analytical
Chemists. 2002. Chlortetracycline,
Oxytetracycline, and Tetracycline in edible animal tissues. Washington: AOAC Int.
Bahri S, Masbulan E, Kusumaningsih A. 2005. Proses praproduksi sebagai faktor penting dalam menghasilkan produk
ternak yang aman untuk manusia.
[terhubung berkala]. http://www.pustaka-deptan.go.id/publication/p3241054.pdf [10 Agu 2009].
Berendsen BJA, Rijhn JAV. 2006. Residue analysis of tetracycline in poultry muscle, shortcomings revealed by a proficiency test. Food Additives and Contaminants 23(11):1141-1148.
[BSN] Badan Standarisasi Nasional. 2000. Batas maksimal cemaran mikroba dan batas residu dalam bahan makanan asal hewan. Dalam Standar Nasional Indonesis No. 01-6366-2000.
Castellari M, Reguiero JAG. 2003. HPLC determination of tetracycline in lamb muscle using an RP-C18 monolithic type column. Chromatographia 58:789-792. [CDER] Center for Drug Evaluation and
Research. 1994. Reviewer Guidance: Validation of Chromatographic Methods. Geneva: Food and Drug Administration. Cherlet M, Baere S, Backer P. 2003.
Quantitative analysis of oxytetracycline and its 4-epimer in calf tissues by
high-performance liquid chromatography
combined with positive electrospray ionization mass spectrometry. Analyst 128:871-878.
Cinquina Al, Longo F, Anastasi G, Giannetti L, Cozzani R. 2003. Validation of a high
performance liquid chromatography
method for oxytetracyline, tetracycline, and chlortetracycline in bovine milk and muscle. Journal of Chromatography A 987:227-233.
Fletouris DJ, Psomas JE, Botsoglon NA. 1990. Trace analysis of oxytetracycline and tetracycline in milk by high performane of liquid chromatography.
Journal of Agricultural and Food
Chemistry 38:1913-1917.
Gritter RJ, Bobbit JM, Schwartig AE. 1991.
Pengantar Kromatografi. Padmawinata K,
penerjemah; Niksolihin S, editor.
Bandung: Penerbit ITB. Terjemahan dari:
Introduction to Chromatography
Harmita. 2004. Petunjuk pelaksanaan validasi metode dan cara perhitungannya. Majalah
Ilmu Kefarmasian 1(3):117-135.
J’Oneil et al. 2006. The Merck Index 14th
Edition, An Encyclopedia of Chemicals, Drugs, and Biologicals. New Jersey:
Merck Research Laboratories.
Horwitz W, Latimer GW, editor. 2005. Official Methods of Analysis of AOAC International. Ed ke-18. Maryland: AOAC International Pub.
[IUPAC] International Union Of Pure And Applied Chemistry. 2002. Harmonized
Guidelines For Single-Laboratory
Validation Of Methods Of Analysis (IUPAC Technical Report). London: IUPAC.
Martel AC, Zeggane S, Drajnudel P, Faucon JP Aubert M. 2006. Tetracycline residues in honey after hive treatment. Food
Additives and Contaminants
23(3):265-273.
Moats WA, Khan RH. 1995. Rapid HPLC determination of Tetracycline antibiotics in milk. Journal of Agricultural and Food
Chemistry. 43: 931-934.
Oktateria L. 2008. Deteksi residu antibodi oksitetrasiklin dengan metode ELISA [skripsi]. Jakarta: Fakultas Farmasi, Universitas Pancasila.
Putra EDL. 2004. Kromatografi cair kinerja tinggi dalam bidang farmasi [skripsi]. Medan: Fakultas Farmasi Universitas Sumatera Utara. [terhubung berkala]. http://digilib.usu.ac.id/skripsi/farmasi.pdf. [11 Feb 2009].
Resnawati H. 2005. Preferensi konsumen terhadap daging dada ayam pedaging yang diberi ransum menggunakan tepung cacing tanah (Lumbricus rubellus). Di dalam:
Seminar Nasional Teknologi Peternakan dan Veteriner. Bogor: Balai Penelitian
Ternak. Hlm 744-748.
Rico, AG. 1986. Drug Residues in Animal. Toulose: Academic Press.
Riti N, Handayani N, Dewi A. 2002. Survei residu antibiotika asal hewan di kabupaten Badung tahun 2002. [terhubung berkala].
http://poultryindonesia.com/antibiotik-dalam-pakan-ternak.pdf. [10 Feb 2009] Rumiati. 2003. Pengaruh lama pembekuan
terhadap mutu daging ayam ditinjau dari kadar protein, jumlah total koloni bakteri dan organoleptik [abstrak] JIPTUMM.
[terhubung berkala]. http://
digilib.umm.ac.id/JIPTUMM/gdl/s1/rumia ti.htm. [11 Feb 2009].
Rupp H, Anderson CR. 2005. Determination of oxytetracycline in salmon by liquid
chromatography with metal-chelate
fluorescence detection. Journal of AOAC
International 88:505-510.
12
Schunack W, Mayer K, Haake M. 1990.
Senyawa Obat, Buku Pelajaran Kimia
Farmasi. Wattimena J, Soebito S,
penerjemah; Padmawinata, editor.
Yogyakarta: UGM Pr. Terjemahan dari:
Arzneistoffe, Lehrburch der
Pharmazeutischen Chemle. .
Soeparno. 1994. Ilmu dan Teknologi Daging. Yogyakarta: Gajah Mada Univ. Pr.
Yuningsih. 2004. Keberadaan residu
antibiotika dalam produk peternakan (susu dan daging). Di Dalam: Lokakarya
Nasional Keamanan Pangan Produk
Peternakan. Bogor: Balai Penelitian
13
LAMPIRAN
Lampiran 1 Kromatogram presisi OTC, TC, dan CTC
A. Pelaksana 1
Ulangan ke-1, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.287 36201 4.062 41047 9.053 46964
Ulangan ke-2, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.279 36862 4.055 41795 9.043 47151
Ulangan ke-3, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.285 36224 4.061 41469 9.064 46898 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2
15
B. Pelaksana 2
Ulangan ke-4, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.284 36916 4.058 41884 9.051 46351
Ulangan ke-5, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.285 36224 4.061 41469 9.064 46898
Ulangan ke-1, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.387 36431 4.214 41360 9.554 47426 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 15
Ulangan ke-2, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.334 36201 4.127 40891 9.289 46306
Ulangan ke-3, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.337 36475 4.131 40890 9.293 45979
Ulangan ke-4, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.346 36391 4.139 40908 9.301 45653 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2
17
C. Pelaksana 3
Ulangan ke-5, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.347 36867 4.140 41422 9.307 45891
Ulangan ke-1, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.272 36445 4.048 41657 9.035 47160
Ulangan ke-2, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.273 36036 4.047 40909 9.033 46949 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2
Ulangan ke-3, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.294 36416 4.070 40783 9.083 47234
Ulangan ke-4, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.288 36248 4.064 41245 9.068 46786
Ulangan ke-5, standar OTC 1 ppm. TC 1 ppm, dan OTC 2 ppm
OTC TC CTC
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.278 36472 4.056 41247 9.079 47218 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2
8
Lampiran 2 Kromatogram linearitas OTC,TC, dan CTC Ulangan 1
Standar OTC 1 ppm Standar TC 1 ppm Standar CTC 2 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.159 28916 3.896 38855 8.719 35293
Standar OTC 0,5 ppm Standar TC 0,5 ppm Standar CTC 1 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.175 14217 3.911 19139 8.744 18021
Standar OTC 0,25 ppm Standar TC 0,25 ppm Standar CTC 0,5 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.177 6920 3.915 8611 8.754 8880 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 19
Ulangan 2
Standar OTC 0,125ppm Standar TC 0,125 ppm Standar CTC 0,25 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.174 3391 3.913 4611 8.758 3769
Standar OTC 0,0625 ppm Standar TC 0,0625 ppm Standar CTC 0,125 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.154 1693 3.901 1961 8.747 2169
Standar OTC 1 ppm Standar TC 1 ppm Standar CTC 2 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.161 29436 3.900 39451 8.742 38602 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2
8
Standar OTC 0,5 ppm Standar TC 0,5 ppm Standar CTC 1 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.160 14698 3.900 18764 8.747 19013
Standar OTC 0,25 ppm Standar TC 0,25 ppm Standar CTC 0,5 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.164 6860 3.902 8556 8.745 9048
Standar OTC 0,125 ppm Standar TC 0,125 ppm Standar CTC 0,25 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.154 3280 3.899 4270 8.723 4016 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 21
Ulangan 3
Standar OTC 0,0625 ppm Standar TC 0,0625 ppm Standar CTC 0,125 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.172 1835 3.916 2189 8.753 2262
Standar OTC 1 ppm Standar TC 1 ppm Standar CTC 2 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.172 28932 3.907 37753 8.728 36621
Standar OTC 0,5 ppm Standar TC 0,5 ppm Standar CTC 1 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.173 13936 3.909 18500 8.723 16832 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2
8
Standar OTC 0,25 ppm Standar TC 0,25 ppm Standar CTC 0,5 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.167 6686 3.904 8445 8.734 8407
Standar OTC 0,125 ppm Standar TC 0,125 ppm Standar CTC 0,25 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.179 3587 3.911 4410 8.729 3876
Standar OTC 0,0625 ppm Standar TC 0,0625 ppm Standar CTC 0,125 ppm
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.170 1726 3.906 2625 8.751 1851 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 23
Lampiran 3 Kromatogram batas deteksi OTC,TC, dan CTC
Standar OTC 100 ppb Standar TC 100 ppb Standar CTC 200 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.179 3498 3.911 4091 8.729 3400
Standar OTC 50 ppb Standar TC 50 ppb Standar CTC 100 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.224 1685 3.996 1893 9.040 1800
Standar OTC 25 ppb Standar TC 25 ppb Standar CTC 50 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.179 931 3.910 1083 8.742 911 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2
8
Standar OTC 10 ppb Standar TC 10 ppb Standar CTC 20 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.196 548 3.876 530 8.687 537
Standar OTC 5 ppb Standar TC 5 ppb Standar CTC 10 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.191 358 3.903 367 9.520 297
Standar OTC 5 ppb Standar TC 5 ppb Standar CTC 10 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.193 352 3.917 356 9.335 298 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 25
Standar OTC 5 ppb Standar TC 5 ppb Standar CTC 10 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.202 356 3.921 355 8.793 302
Standar OTC 5 ppb Standar TC 5 ppb Standar CTC 10 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.215 343 3.932 356 9.426 292
Standar OTC 5 ppb Standar TC 5 ppb Standar CTC 10 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
3.240 361 3.927 360 9.262 306 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2 1 PDA Multi 1 2 PDA Multi 2
8
Standar OTC 1 ppb Standar TC 1 ppb Standar CTC 2 ppb
tR Luas Puncak tR Luas Puncak tR Luas Puncak
- - - - 1 PDA Multi 1 = λ 355 nm 2 PDA Multi 2 = λ 368 nm 1 PDA Multi 1 2 PDA Multi 2 27
Lampiran 3 Contoh perhitungan A. Perhitungan LOD dan LOQ OTC
Q = LOD atau LOQ χ = rerata luas puncak k = 3 (LOD) dan 10 (LOQ)
SD = simpangan baku luas puncak blangko Diketahui Puncak Luas ulangan OTC 1 358 2 352 3 356 4 343 5 361 rerata 354 SD 6,6106 LOD = 354 + 3(6,6106) = 373,83
Konsentrasi LOD OTC = 373,83 × konsentrasi standar OTC, TC, dan CTC (ppb)
354 = 373,83 × 5 ppb 354 = 5,28 ppb LOQ = 354 + 10 (6,6106) = 420,11
Konsentrasi LOQ OTC = 420,11 × konsentrasi standar OTC, TC, dan CTC (ppb)
354
= 420,11 × 5 ppb
354
= 5,93 ppb
B. Penentuan perolehan kembali (Recovery) OTC
Konsentrasi standar (Cst) OTC = 1 ppm = 1 ng/µL
Konsentrasi standar yang ditambahkan (Ci) = 1 ppm = 1 ng/µL
Luas puncak standar (Ab) OTC = 32472
Volume standar yang ditambahkan (Vs) = 250 µL
8
Konsentrasi sebenarnya (Cs) = Ci×Vs
ms
= 1 ng/µL × 250 µL 5,01 g = 49,90 ng/g (ppb)
Luas puncak larutan uji/sampel (As) = 8045
Volume akhir = 400 µL
Faktor pengenceran = 30/10 = 3
Konsentrasi larutan uji/sampel (Ct) =
=
= 59,34 ppb
Konsentrasi larutan uji (blanko) (Cu) =
=
= 2,89 ppb
Persen perolehan kembali =
=
= 107,3 %
C. Penentuan konsentrasi sampel =
=
= 5,9792 ppb