2.1. Lemak dan Minyak
jenuh atau tidak jenuh , dapat sama atau berbe Asam lemak alamiah
lemak adalah triasilgliserol (TAG) atau trigliserida bahwa lemak adalah ester dari gliserol dan berbagai
rantai lurus yang dikenal sebagai asam lemak. Asam memiliki 4 ~ 24 atom karbon dan masing-masing memiliki tergantung dari jumlah atomnya. Asam lemak dapat klasifikasikan
(12 atau lebih karbon) ; rantai pendek (kurang dari i sedang / medium (8-10 karbon).
pemanasan yang bergantung pada derajat kejenuhannya ; asam ikatan rangkap.
geometrik ; asam lemak cis dan asam lemak trans pada asam
Struktur lemak / minyak secara umum (R1, R2 dan R3 adalah jenuh atau tidak jenuh , dapat sama atau berbeda
lemak alamiah didapati berbentuk cis. Isomer trans biasanya reaksi kimia seperti hidrogenasi atau oksidasi. Asam lebur yang lebih rendah daripada asam lemak trans dengan
Panjang rantai karbon juga mempengaruhi titik lebur. kenaikan titik lebur bergantung kepada panjangnya rantai nuh yang panjang rantainya sama memiliki titik lebur dibandingkan dengan asam lemak tidak jenuh trans (Weiss, 1983
Tersedia tiga posisi pada molekul gliserol untuk esterifikasi asam lemak. Karakter dan sifat-sifat asam lemak ditentukan berdasarkan jenis asam lemak yang teresterifikasi dalam molekul trigliserida (Silalahi, 1999).Selanjutnya jenis, komposisi dan pembagian dari asam lemak pada backbone gliserol memiliki fungsi penting tidak hanya sifat-sifat fisiknya tetapi juga sifat kimia pada bahan makanan itu (Kritcheusky, 1995 ; Haumann, 1997). Hal ini sangat penting dalam peleburan lemak coklat dan pengkristalan struktur dari lemak. Titik lebur dari campuran lemak berubah secara random (acak) dengan adanya reaksi interesterifikasi untuk menghasilkan lemak dengan titik lebur rendah atau tinggi. Sebagai contoh, campuran 30 persen tripalmitin dan 70 persen triolein yang memiliki titik lebur 58 0C sebelum interesterifikasi dan 48 o
C setelah interesterifikasi (Weiss, 1983 ; List et al, 1997 ; Silalahi, 1999).
Trigliserida tidak dapat larut dalam air dan pada temperatur kamar akan berubah dari padat menjadi cair. Panjang asam lemak beberapa minyak yang dapat dikonsumsi 16 ~ 18. Meskipun demikian minyak kelapa dan minyak init sawit termasuk yang tinggi karena memiliki asam laurat. Secara umum lemak mengandung suatu campuran trigliserida yang akan berbeda setiap komposisi dan posisi asam lemaknya pada molekul trigliserida, hal ini menyebabkan molekul dalam lemak dapat melembut atau mengeras. Oleh karena itu, semua lemak dapat berbentuk cair pada temperatur kamar tetapi umumnya mengandung molekul lemak padat (suspended solid) pada minyak cairnya. Jika lemak cair didinginkan, beberapa molekul lemak akan memadat dan sebagian membentuk kristal lemak dari bagian yang cair. Oleh karena itu, titik lebur dari lemak dapat sebagai karakter fisik dari lemak murni (Weiss, 1983).
Penggunaan minyak nabati secara umum dapat dimodifikasi dengan mencari sifat-sifat yang biasanya terdapat pada minyak tersebut, sepert: sifat-sifat peleburan, daya tahan terhadap oksidasi, kandungan lemak poliena tidak jenuh (poliunsaturated), sifat kristalisasinya dan kalori lemak yang rendah dengan penyerapan yang cepat (Silalahi, 1999). Modifikasi dari lemak dapat berhasil dengan mengubah komposisi pada molekul asam lemak trigliserida untuk membentuk lemak baru misalnya lemak dengan titik lebur yang tinggi, ataupun dengan titik lebur yang rendah.
manusia, pelarut vitamin A, D, E, K dan pengontrol serum lipida dan lipoprotein (Melton, 1996). Lemak dan minyak dengan konsentrasi 9 kkal/g merupakan sumber energi, selain itu sebagai penyerap bagi vitamin yang larut dalam lemak seperti vitamin A, D, E dan K. Oleh karena, itu asam lemak merupakan prekursor pada prostaglandin yang merupakan senyawa seperti hormon yang berfungsi sebagai pengatur variasi fisiologi. Lemak mempunyai fungsi utama bagi pertumbuhan dan perkembangan tubuh manusia (Geise, 1996).
Di samping fungsinya pada nutrisi, lemak juga merupakan komponen makananan dan pemberi rasa dalam makanan. Lemak memberikan citarasa yang merupakan suatu kombinasi yang memberikan rasa lembut, lezat, bentuk dan aroma pada makanan. Lemak juga sebagai pembawa senyawa citarasa lipophilik yang disebabkan oleh adanya prekursor untuk pembentuk cita rasa (Akoh, 1995).
Selain mempunyai efek positif sebaliknya lemak juga mempunyai efek negatif, kebanyakan lemak akan menyebabkan meningkatnya resiko kegemukan dan beberapa jenis penyakit kanker, kolesterol yang tinggi di dalam darah dan penyakit jantung koroner (Akoh, 1995 ; Geise, 1996). Pengurangan konsumsi lemak dapat menurunkan resiko terkena penyakit jantung dan jika manusia yang memiliki kelebihan berat badan melakukan diet lemak dapat menurunkan resiko penyakit jantung koroner (Geise, 1996). Akibatnya banyak permintaan untuk mengurangi lemak dari makanan. Industri makanan mencari variasi pengganti lemak dalam bahan makanan ataupun dengan cara memodifikasi lemak itu sendiri (O’Brien, 1998 ; Silalahi, 1999).
Refined Bleached Deodorized Palm Kernel Stearin (RBDPKS) merupakan suatu bentuk fraksi padat dari Palm Kernel Oil diperoleh setelah dikristalisasi pada temperatur yang terkontrol. Fraksi ini dapat digunakan untuk membuat CBS (Dunford, 2012).
2.2.Proses Hidrogenasi
ikatan rangkap minyak atau lemak dengan bantuan katalisator akan menaikkan titik cair (Ketaren, 1986).
Hidrogenasi minyak dan lemak merupakan salah satu reaksi kimia terbesar dalam industri pengolahan minyak dan lemak. Secara sederhana, hidrogensi merupakan proses penambahan hidrogen ke dalam rantai etilen atau ikatan rangkap asam lemak dengan bantuan katalis logam (Swern, 1982). Proses hidrogenasi merupakan proses penambahan hidrogen pada ikatan rangkap di minyak atau lemak dengan menggunakan bantuan katalis, biasanya nikel. Hidrogenasi menghasilkan dua hal, yaitu meningkatkan titik cair (melting point) lemak atau minyak dan meningkatkan ketahanan terhadap proses oksidasi dan penurunan rasa. Hidrogenasi yang dilakukan untuk mengubah minyak dari bentuk cair menjadi bentuk semi padat ataupun lemak plastis, biasa digunakan pada industri shortening atau mentega (Gunstone dan Norris, 1983 ; Ketaren, 1986).
Reaksi hidrogenasi dilakukan dengan menggunakan hidrogen murni dan ditambahkan katalisator. Setelah proses hidrogenasi selesai, minyak didinginkan dan katalisator dipisahkan dengan cara penyaringan. Hasilnya adalah minyak yang bersifat plastis atau keras, tergantung pada derajat kejenuhannya (Ketaren, 1986).
Faktor-faktor yang mempengaruhi rendemen dan kecepatan reaksi hidrogenasi adalah tekanan dan suhu, kemurnian gas hidrogen, katalis dan bahan baku minyak.
a. Tekanan dan suhu
Kedua faktor ini paling mempengaruhi proses hidrogenasi. Jika waktu hidrogenasi yang diinginkan sangat singkat maka tekanan yang digunakan minimal 20 atm. Pada suhu antara 100 ~ 180oC kecepatan reaksi meningkat dengan cepat, namun peningkatan kecepatan reaksi ini akan terhenti pada suhu 220oC.
b. Kemurnian hidrogen dan waktu kontak minyak dengan hidrogen
Gas hidrogen yang digunakan harus dalam keadaan kering dan semurni mungkin. Kecepatan reaksi sangat dipengaruhi oleh distribusi hidrogen dalam massa lemak yang akan dihidrogenasi. Semakin banyak gelembung-gelembung hidrogen terdispersi dalam massa semakin cepat proses hidrogenasi berlangsung. Hidrogen cair murni dapat diperoleh secara komersial.
c. Jenis katalis
Katalisator yang dapat digunakan pada proses hidrogenasi adalah Palladium, Platina, Copper Chromite dan Nikel. Namun katalis Nikel telah terbukti sebagai tipe katalis yang paling cocok untuk hidrogenasi dan sering digunakan dalam proses hidrogenasi karena lebih ekonomis dan lebih efisien.
Katalis sangat rentan mengalami keracunan yang disebabkan oleh komponen sulfur, asam lemak bebas, sabun, dan fosfatida dalam minyak. Dalam beberapa kasus, keracunan tersebut dapat diminimisasi melaluli penambahan bleaching earth teraktivasi.
d. Sifat-sifat kemurnian minyak yang akan dihidrogenasi
Biasanya minyak dihidrogenasi jika sifat-sifat fisik dan kimia gliserida pada suatu minyak yang ingin dimodifikasi menjadi lebih padat (pengerasan). Minyak yang akan dihidrogenasi adalah minyak atau asam-asam lemak yang telah mengalami proses pemurnian. Minyak yang akan dihidrogenasi seharusnya adalah minyak yang telah dinetralisasi dan dipucatkan, mengandung sabun dalam jumlah yang sangat sedikit (di bawah 25 ppm), serta kering. Hal ini untuk mencegah keracunan katalis dan mengurangi selektivitas. Asam lemak bebas, sabun dan air bersifat racun bagi katalis sehingga mengurangi aktivitas katalis dan selektivitas.
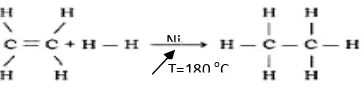
Hidrogenasi minyak dan lemak meliputi penambahan hidrogen (berupa gas) ke dalam ikatan tidak jenuh di rantai asam lemak, yang menyebabkan asam lemak tidak jenuh menjadi jenuh dengan penambahan satu mol hidrogen pada masing-masing ikatan rangkap. Reaksi tersebut secara sederhana dapat dilihat pada Gambar 2.2.
Gambar 2.2. Reaksi hidrogenasi Ni
Proses hidrogenasi dilakukan untuk menjenuhkan ikatan rangkap di dalam rantai asam lemak, namun gas hidrogen dapat juga bereaksi dengan komponen non gliserida dalam minyak seperti karoten. Hal ini sangat tidak menguntungkan. Masalah yang harus diperhatikan selanjutnya adalah reaksi selektivitas.
Pada reaksi selektivitas, pertama-tama hidrogen akan menjenuhkan ikatan rangkap pada minyak yang mengandung tiga atau lebih ikatan rangkap (polyunsaturated). Selanjutnya secara berurutan hidrogen menjenuhkan komponen minyak dengan dua ikatan rangkap (diunsaturated) dan satu ikatan rangkap (monounsaturated). Dengan cara ini maka asam linoleat akan berubah seluruhnya menjadi asam linoleat, sebelum beberapa asam linoleat dihidrogenasi menjadi oleat. Demikian seharusnya hingga terjadi perubahan oleat menjadi asam jenuh, yaitu asam stearat (Gunstone dan Norris ,1983).
Ikatan rangkap dengan bentuk ciscenderung labil dibandingkan dengan bentuk trans. Ketidakstabilan bentuk cis ini menyebabkan gas hidrogen dapat dengan mudah menjenuhkan ikatan rangkap. Perubahan lain yang mungkin terjadi selama proses hidrogenasi adalah perubahan bentuk cis ikatan rangkap menjadi bentuk trans yang memiliki titik leleh lebih tinggi. Stereo-isomerisasi ini selalu mengikuti peningkatan selektivitas. Hal ini tidak diinginkan karena dapat meningkatkan titik leleh (melting point) tanpa mengurangi asam lemak tidak jenuh (Ketaren, 1986).
2.3. Mentega Coklat
Biji coklat diubah menjadi coklat cair melalui proses pemanggangan,
pemisahan dan pendinginan. Sejak tahun 1828 Van Houten di Holand menyatakan
bahwa kelebihan lemak yang ada pada coklat dapat diterima. Coklat cair diproses
sedemikian rupa dengan cara penekanan menjadi mentega coklat dan tepung coklat,
mentega coklat selanjutnya diproduksi menjadi coklat makan dan coklat cair
(Pushparajah dan Soon, 1986).
Total kandungan lemak padat pada biji coklat kering sekitar 48 ~ 49%, dengan
trigliserida sebagai komponen utama. Mentega coklat adalah komponen termahal
dalam formula coklat. Dalam komposisi mentega coklat secara perdominan (>75
persen) merupakan trigliserida simetris dengan asam oleat pada posisi dua. Kira-kira
20 persen trigliserida cair pada temperatur kamar dan memiliki titik lebur antara
32~35 oC, ini sangat penting dalam fungsinya sebagai mentega coklat. Hal ini disebabkan mentega coklat mengandung trigliserida yang non simetris (seperti PPO,
PSO dan SSO ; P = asam palmitat, O = asam oleat, dan S = asam stearat; posisi dari
huruf menunjukkan susunan asam lemak di dalam molekul trigliserida (O’Brien,
1998). Seperti yang diperlihatkan pada tabel 2.1 sebagai berikut:
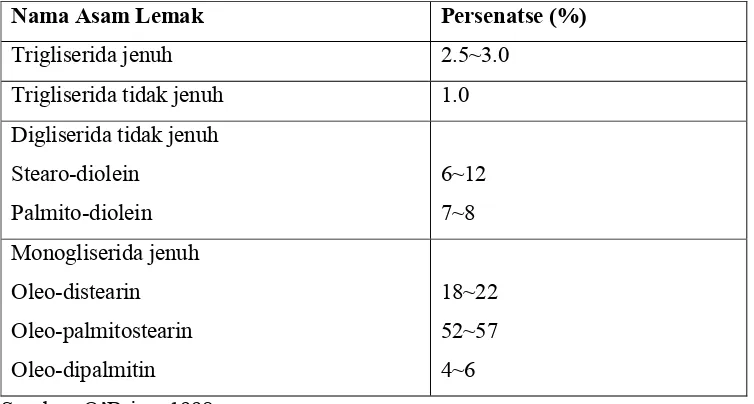
Tabel 2.1. Persentase konstituen gliserida dalam lemak coklat
Nama Asam Lemak Persenatse (%)
Keistimewaan komposisi trigliserida, bersama trigliserida yang rendah
menghasilkan mentega coklat dengan sifat fisik yang memberikan kemampuan selama
proses rekristalisasi dalam modifikasi kristal yang stabil. Komposisi trigliserida pada
Tabel 2.2. Komposisi asam lemak berbagai variasi mentega coklat dengan analisa GLC
Asal Negara 16:0 18:0 18:1 18:2 20:0
Ghana 24.8 37.1 33.1 2.6 1.1
India 25.3 36.2 33.5 2.8 1.1
Brazil 23.7 32.9 37.8 4.0 1.0
Nigeria 25.5 35.8 33.2 3.1 1.1
Ivory Coast 25.4 35.0 34.1 3.3 1.0
Malaysia 24.8 37.1 33.2 2.6 1.1
Sumber : Shukla, 1995
Dari tabel 2.2 menunjukkan mentega coklat Malaysia memiliki diena terbanyak, sedang mentega coklat Brazil mengandung sedikit diena dan banyak trigliserida tidak jenuh lainnya. Mentega coklat yang keras lebih gampang mengembang (bloom) daripada mentega coklat yang lembut. Mentega coklat dari Malaysia, Srilangka dan India adalah keras sedangkan mentega coklat Brazil lembut, yang lainnya berada diantara keduanya. Kualitas mentega coklat Brazil dapat diperbaiki dengan mencampurnya dengan mentega coklat Malaysia, yang dapat menaikkan kandungan lemak padat. Untuk mendapatkan kualitas mentega coklat yang baik dapat dengan cara mengurangi digliserida, Beberapa usaha dapat dibuat untuk memperbaiki sifat-sifat coklat. Penghilangan bau (deodorisasi) dari mentega coklat biasanya dilakukan pada temperatur yang relatif rendah, yang dapat memberikan hasil yang memuaskan dalam pencampuran citarasa. Penghilangan bau dapat dilakukan dengan menggunakan eliminasi klorinasi. Temperatur untuk penghilangan bau (deodorisasi) yang normal antara 150~180 oC (Shukla, 1995 ; O’Brien, 1998).
Penambahan lemak susu pada mentega coklat akan menurunkan titik lebur, yang
mengakibatkan perubahan kristalisasi pada kekerasan mentega coklat dan dapat
menurunkan kandungan lemak padat.
Ada empat macam kristal polimorfis yang bisa dibentuk mengikuti sifat-sifat
sebagai berikut:
Pembentukan γ: diproduksi dengan temperatur yag sangat dingin pada lemak cair, titik leburnya kira-kira 17 oC ini sangat tidak stabil dan sangat
mudah berubah bentuk,
Pembentukan α : cepat terjadi pada temperatur rendah, titik leburnya 21~24 oC,
Pembentukan β’ : perubahan dari bentuk αpada temperatur normal ke bentuk β, titik
leburnya 27~29 oC,
Pembentukan β : terbentuk dari β’ yang stabil yang mempunyai titik lebur 34~35 oC.
Stabilitas dari pembentukan kristal yang berbeda dari γ ke β, terjadi pada
semua proses coklat, secara objektif inilah yang membentuk mentega coklat dan
coklat lebih stabil kristalnya. Beberapa penelitian menemukan bentuk polimorfis
lainnya, tetapi dari suatu nilai yang praktis menjadi empat nilai seperti di atas itu lebih
diutamakan. Kecepatan kristalisasi merupakan suatu faktor terjadinya peningkatan
kualitas. Pada pembentukan lemak ekuivalen sifat ini menjadi suatu ketergantungan
dengan struktur gliserida (Minifie, 1989).
Penurunan kandungan lemak padat ketika lemak susu dicampurkan ke mentega
coklat dengan berbagai variasi menyebabkan penurunan kekerasan. Ada dua hal yang
menyebabkannya terjadinya campuran yang tidak sesuai yaitu penurunan titik lebur
dari campuran dan penurunan kelembutan, yang membentuk senyawa pada lemak itu
sendiri, yang ditunjukkan dengan fluiditas, dan komponen lemak padat yang
membentuk trigliserida mentega coklat. Penggunaan lemak susu dalam berbagai
variasi yang sesuai pada coklat akan memperbaiki permukaan campuran menjadi
semangkin halus yang memberikan pengaruh pada citarasa, warna dan bentuk
(Shukla, 1995).
Tabel 2.3 Komposisi asam lemak mentega coklat
Asam Lemak Rumus Kimia Persentase
(%)
Asam Palmitat (16:0) C15H31COOH 25.4
Asam Palmitoleat (16:1) C15H29COOH 0.2
Asam Stearat (18:0) C17H35COOH 33.2
Asam Oleat (18:1) C17H33COOH 32.6
Asam Linoleat (18:2) C17H31COOH 2.8
Asam Linolenat (18:3) C17H30COOH 0.1
Sumber : O’Brien, 1998
2.4 Pengganti Mentega Coklat
Lemak yang mempunyai kompabilitas yang sangat terbatas dengan mentega coklat
yang mempengaruhi rheologi dari mentega coklat. Derajat kompabilitas lemak dengan mentega coklat adalah keras pada suhu kamar, mempunyai titik lebur yang sama dengan temperatur tubuh dan mempunyai derajat kompabilitas dengan mentega coklat dan lemak susu (Sara, 1997).
Untuk mendapatkan mentega coklat yang murah dan mudah diperoleh dicari alternatif
lain dengan mengganti mentega coklat dengan minyak nabati dalam pembuatan penyalut coklat.
Sejak awal tahun 1930, dicoba menggunakan lemak lain selai mentega coklat. Eksperimen ini tidak berhasil karena terjadi kontabilitas yang buruk antara campuran
lemak yang digunakan, dan perbandingan yang tidak sesuai, dimana terjadi penghilangan warna dan pengembangan lemak (bloom). Penelitian kemudian ditujukan pada sifat fisik mentega coklat. Diketahui bahwa lemak dari mentega coklat berupa mentega keras (Shukla, 1995 ; O’Brien, 1998).
Lemak nabati dapat dipakai sebagai bahan dasar untuk membuat pengganti mentega coklat dalam pembuatan penyalut coklat. Produk yang dihasilkan ini disebut juga mentega keras dan dapat diperoleh dengan menggunakan minyak kelapa sawit, kelapa, dan minyak khusus lainnya seperti sal, shea dan illipe yang dipakai sebagai
bahan material dasar. Proses pembuatan mentega keras meliputi hidrogenasi lemak, interesterifikasi, fraksinasi dan blending. Beberapa mentega keras dapat diperoleh dengan mengkombinasi proses hidrogenasi dan fraksinasi (Shukla, 1995). Mentega keras dapat dibuat dengan menggunakan palm kernel, kelapa dan minyak esotik lainnya seperti sal, shea dan illipe yang merupakan material dasar. Proses lainnya
menggantikan sebahagian dari mentega coklat, menggantikan secara keseluruhan dan
memodifikasinya (Shukla, 1995 ; O’Brien, 1998, Basiron, 2000).
Mentega keras berdasarkan sifat dan material dasar yang digunakan dapat
digolongkan menjadi tiga:
2.4.1. Pengganti Mentega Coklat dari Laurat (LauricCBS)
Mentega coklat laurat merupakan lemak yang tidak sesuai dengan mentega coklat,
tetapi memiliki sifat fisik yang mirip dengan mentega coklat. Kategori ini termasuk ke
dalam industri lemak berdasarkan persamaan sifat fisika, tetapi kesemua komposisi
trigliserida membuatnya tidak sesuai dengan mentega coklat, antara lain mereka selalu
digunakan dalam formula tepung coklat untuk menghasilkan penyalut. Pengganti
mentega coklat yang diperoleh dari lemak laurat didapatkan dari berbagai variasi
spesies pohon kelapa dimana yang termasuk di dalamnya minyak kelapa sawit dan
minyak kelapa. Minyak kelapa digunakan pertama sekali dalam pembuatan pengganti
mentega coklat dari laurat (lauric CBS) pada tahun 1897. Aarhus pertama sekali
membat suatu lemak laurat dengan stearin ke permen coklat Danish. Sejak saat itu
dilakukan penelititan-penelitian untuk mengkaji rahasia mentega coklat dalam
meningkatkan supremasi lemak. Minyak kelapa kandungan asam lauratnya 47~48
persen, bersama dengan sejumlah kecil rantai asam lemak medium pendek (Shukla,
1995 ; O’brien, 1998).
Dari penelitian yang berkelanjutan ternyata stearin kelapa sawit lebih baik
dipakai daripada olein kelapa sawit, karena stearin padat dan titik leburnya di atas
suhu kamar, jarak antara titik leburnya pendek. Sifat yang simpel ini dapat digunakan
sebagai penyalut coklat yang merupakan lemak padat pada saat pendinginan, tetapi
tidak pernah melebur dibawah 30 oC. Teknik hidrogenasi yang digunakan
menyebabkan terjadinya selang seling pada posisi lemak laurat, khususnya pada
stearin kelapa sawit yang menunjukkan suatu sifat yang lebih baik daripada dengan
menggunakan hidrogenasi minyak kelapa sawit (HPKO). Lemak nabati dapat
mengkristal pada beberapa keadaan polimorfik, beberapa diantaranya seperti α, β’ dan β, pada jenis yang sama menunjukkan pertambahan stabilitas, titik lebur, panas peleburan dan densitas. Secara umum lemak laurat adalah stabil di dalam bentuk β’.
Sumber lainnya untuk industri lauric CBS adalah dengan menambahkan minyak
kelapa, minyak kelapa sawit Amerika Selatan, Tukum, Cohune, Babasu dan Auri-curi.
Prinsip pemakaian laurat CBS untuk mendapatkan stabilitas terhadap oksidasi, waktu
paruh yang panjang, ini berpengaruh terhadap kualitas dan citarasa yang lezat, tidak
memiliki rasa lilin, teksturnya sangat mirip dengan mentega coklat, seperti kekerasan,
bisa dikatakan tidak lembut, kepadatan terjadi dengan cepat dan kompatibel
permukaan yang dapat dikitalkan mempermudah pencetakan dan kehalusan
permukaan selama penyimpanan dan memiliki harga yang jauh lebih murah daripada
mentega coklat. Dilain pihak lauric CBS juga memiliki kelemahan diantaranya:
Campuran lauric CBS dengan mentega menyebabkan keadaan eutectic, jika dalam
industri coklat berubah ke industri penyalut, tangki dalam sistem proses harus
dibersihkan kembali karena lemak yang terjadi tidak boleh lebih 6 persen dari
mentega coklat.
Ketika lauric CBS dimasukkan ke campuran terjadi pemecahan oleh enzim lipase,
ini sangat berbahaya pada hidrolisa lemak, karena menyebabkan rasa sabun pada
konsentrasi yang rendah, Secara bebas asam lemak memiliki citarasa yang rendah
dalam senyawannya, ini disebabkan panjang rantai asam lemak asam butirat (C4)
0,6 ppm ; asam kaproat (C6) 2,5 ppm ; asam kaprilat (C8) 350 ppm ; asam kaprat
(C10) 200 ppm, asam laurat (C12) 700 ppm dan asam stearat (C18) 5 ppm.
Kelemahan lainnya memiliki toleransi yang relatif rendah dengan lemak susu (Shukla, 1995 ; O’Brien, 1998 ; Silalahi, 1999).
2.4.2. Pengganti Mentega Coklat Non Laurat (Non LauricCBS)
Mentega coklat non laurat merupakan lemak yang sebagian sesuai dengan mentega
coklat. Pengganti mentega coklat non laurat merupakan proses fraksinasi pada
hidrogen minyak, kacang kedelai, kapas, jagung, kacang tanah, bunga matahari.
Minyak ini dihidrogenasi pada posisi tertentu untuk mendapatkan pembentukan dari
asam lemak trans, dimana terjadi kenaikan kandungan padat. Titik lebur dari asam
oleat yang merupakan konfigurasi cis pada 14oC yang merupakan suatu isomer asam
eliadat yang titik leburnya 51.5oC (Shukla, 1995 ; Basiron, 2000). Pengganti mentega
coklat non laurat biasanya dibuat dari minyak cair pada temperatur kamar, yang
sebelumnya dihidrogenasi untuk membuat minyak cair menjadi kental dengan mutu
minyak kapas dan minyak kacang tanah. Hasil ini sangat baik sebagai penyalut biskuit
dan coklat yang memberikan tekstur yang rapuh. Formulasi senyawa pengganti
mentega coklat non laurat tidak cocok untuk makanan yang meleleh dalam mulut,
seperti berbagai bentuk coklat. Selain itu mentega non laurat juga digunakan untuk
meningkatkan kualitas makanan dengan citarasa yang tidak enak dan harganya mahal.
Dengan kata lain pengganti mentega coklat non laurat tidak begitu baik digunakan
karena harganya mahal, dan dalam prinsip pembuatan pengganti mentega coklat
pertimbangan harga lebih penting daripada kualitas makanan, karena ada alternatif
pengganti mentega coklat lain yang dapat digunakan (Basiron, 2000).
2.4.3. Cocoa Butter Equivalentatau Extenders (CBE)
Lemak ini sepenuhnya sesuai dengan mentega coklat baik sifat fisik maupun kimia.
Mentega coklat ekuivalen adalah suatu lemak khusus yang tidak dihidrogenasi
mengandung asam lemak yang sama dan memiliki kemiripan diena pada mentega
coklat. Kesemuanya ini akan sesuai dengan mentega coklat dan dapat dicampur pada
mentega coklat dengan beberapa perbandingan. Mentega coklat merupakan sistem tiga
komponen yaitu POP, POS, SOS pada trigliseridanya. Fraksi minyak sawit
menghasilkan suatu campuran yang kaya akan POP, dan lemak yang eksotik seperti
shea, sall dan illipe. Fraksinasi dilakukan untuk mendapatkan trigliserida yang kaya
akan POS dan SOS. Suatu kelemahan mentega coklat ekuivalen yaitu stabilitas
produksi yang tidak tetap dan prosesnya menggunakan biaya yang besar sehingga
harganya mahal. Selain itu juga mempunyai kelebihan diantaranya toleransi dengan
lemak susu sangat baik karena efektif mengadisi lemak susu dan membentuk kristal
polimorfis β, sedangkan dengan lemak susu anhidrat (AMF) dan lemak susu keras
(HMF) membentuk kristal polimorfis β’ memiliki daya tahan tinggi terhadap
temperatur sehinggga sukar terjadi pengembangan lemak (bloom) (Sabariah, 1998). Teknologi ini memiliki keuntungan dalam kesesuaian lemak dengan mentega coklat
Pada umumnya CBE adalah formula yang merupakan fraksi tengah minyak sawit
(PMF) yang dicampur dengan lemak nabati seperti illipe dan lemak shea. PMF kaya
akan miasilgliserol POP dan dua lemak lainnya kaya akan SOS dan triasilgliserol POS
(Shukla, 1995 ; Basiron, 2000).
Kelapa sawit dikenal memiliki 4 macam varietas yakni: macrocarya, dura, tenera dan
pesifera yang dibedakan berdasarkan tempurung buah kelapa sawit (Kaban, 1997).
Kelapa sawit merupakan sumber dua jenis minyak yang berbeda, dan daging buahnya
mengandung minyak kelapa sawit disebut MKS dan tempurung buah kelapa sawit
disebut MIS (Palm Kernel Oil). Kedua minyak ini memiliki sifat yang berbeda
wlaupun berasal dari sumber yang sama. MIS mirip dengan minyak kelapa,
sama-sama memiliki warna yang jernih, titik leburnya tajam, mengandung asam lemak
laurat dan miristat yang tinggi, cukup stabil terhadap oksidasi karena mengandung
asam lemak tidak jenuh yang rendah (O’Brien, 1998 ; Kaban, 1997). Stearin adalah
padat dan dapat digunakan untuk memperbaiki kualitas kelembutan cocoa. Seperti
memperbaiki kualitas dari mentega coklat Brazil melalui proses fraksinasi. Stearin
diperoleh dari pemurnian minyak sawit dari sabut (mesocarp) kelapa sawit yang
diproses dengan beberapa tahap.
2.5.1. Penghilangan Getah (Degumming)
Degumming merupakan suatu proses pemisahan getah atau lendir-lendir yang terdiri
dari posfatida, protein, residu karbohidrat, air dan resin tanpa mengurangi asam lemak
bebas dalam minyak. Proses degumming dilakukan dalam dua tahap, pada tahap
pertama air sebanyak 4 persen ditambahkan ke dalam minyak kasar, campuran
kemudian dipanaskan sampai 60 oC diaduk selama 30 menit kemudian dibiarkan
selama 24 jam sehingga air dan minyak mudah dipisahkan. Pada tahap kedua, 10
persen air dan 1 persen asam oksalat (katalis) ditambahkan ke dalam minyak kasar
kemudian dipanaskan sampai 40oC dan diaduk selama 20 menit dan dibiarkan selama
24 jam. Untuk mengilangkan asam dilakukan netralisasi menggunakan NaOH.
Minyak yang telah netral kemudian diaduk selama 1 jam pada suhu 35~60 oC lalu
didinginkan lagi selama 24 jam agar air terpisah di bawah lapisan minyak sehingga
mudah dipisahkan (Pushparajah dan Soon, 1986).
2.5.2. Pemucatan(Bleaching)
Untuk mendapatkan lemak dan minyak yang berwaarna cerah perlu dilakukan
pemucatan dengan cara penyerapan zat warna. Penyerapan zat warna yang sering
dilakukan adalah menggunakan tanah pemucat (Fuller’s Earth) dan arang (Charcoal)
2.5.3. Penghilangan Bau (Deodorization)
Proses deodorisasi dilakukan dengan menggunakan uap panas. Minyak dipanaskan
pada suhu 230 ~240oC. Bau yang tidak dikehendaki dapat dihilangkan dengan uap air
dan dikeluarkan dengan proses vakum, proses ini biasanya berlangsung 90 menit
(O’Brien, 1998).
2.5.4. Pendinginan (Winterization)
Proses pendinginan dilakukan dengan pemisahan bagian trigliserda jenuh atau bertitik
cair tinggi dari trigliserida bertitik cair rendah. Minyak yang belum mengalami
pendinginan masih mengandung sejumlah asam stearat yang menyebabkan minyak
membeku atau kelihatan seperti susu pada suhu rendah. Dengan mendinginkan
minyak pada temperatur rendah dapat diperoleh bagian yang membeku pada suhu
rendah yang dipisahkan dengan penyaringan, sehingga menghasilkan minyak yang
tidak dapat membeku pada temperatur sangat rendah disebut olein atau winter oil,
sedangkan yang berbentuk padat disebut sebagai stearin kelapa sawit (Pushparajah
dan Soon, 1986). Dengan mendinginkan minyak pada suhu rendah yang disebut
stearin, sedangkan yang berbentuk cair disebut sebagai olein.
Stearin mempunyai komposisi trigliserida yang mirip dengan mentega coklat,
yang merupakan campuran dari POP, POS dan SOS dan tidak ada komponen yang
cair pada temperatur kamar. Dengan penambahan stearin, kristalisasi mentega coklat
semakin baik dan kompleks dan panas peleburan bertambah.
Gambar 2.3. Skema pemurnian minyak sawit
Dari gambar 2.3, untuk stearin (misalnya RBDPKS) dilakukan pengolahan yang sama
dengan menggunakan bahan dasar CPKO.
Stearin adalah padat dan dapat digunakan untuk memperbaiki kelembutan
mentega coklat Brazil dengan fraksinasi dalam susunan komposisi trigliseridanya CPO
(Degumming)
Minyak Hasil Pemisahan Gum
Netralisasi dengan Basa
Pemucatan (Bleaching)
Fraksinasi
ternyata mirip dengan mentega coklat, sehingga kemungkinan besar dapat digunakan
sebagai pengganti mentega coklat.
Beberapa sifat fisika dan kimia yang penting pada stearin kelapa sawit, diantaranya:
Bilangan asam untuk semua metil ester adalah rendah, normalnya kurang dari 0,8 mg KOH/g,
Bilangan penyabunan metil ester adalah tinggi, menurut dengan pertambahan atom karbon dalam molekulnya,
Kandungan air metil ester rendah, normalnya dibawah 0,2 persen, Bilangan hidroksil rendah, antara 0~2.5 persen (Basiron, 2000).
Dalam susunan komposisi trigliseridanya ternyata mirip dengan mentega
coklat sehingga kemungkinan besar dapat digunakan sebagai pengganti mentega
coklat. Stearin kelapa sawit diketahui memiliki kemiripan dengan mentega coklat
yang dapat dilihat dari kurva NMR, yang menunjukkan tekstur yang sangat rapuh,
jarak peleburan yang dekat yang memastikan cepat melebur dan meleleh di dalam
mulut. Interval diantara kepadatan dan titik leburnya pendek. Ini merupakan suatu
keuntungan tambahan pada mentega coklat. Sifat yang simpel ini dapat digunakan
sebagai penyalut. Komposisi asam lemak serta beberapa sifat fisika kimia dari MKS
dan MIS dapat dilihat pada tabel 2.4 dan tabel 2.5.
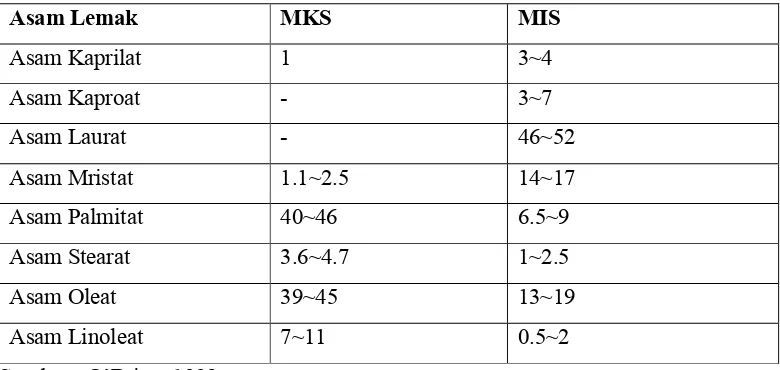
Tabel 2.4. Komposisi asam lemak minyak kelapa sawit dan minyak inti sawit
Asam Lemak MKS MIS
Asam Kaprilat 1 3~4
Asam Kaproat - 3~7
Asam Laurat - 46~52
Asam Mristat 1.1~2.5 14~17
Asam Palmitat 40~46 6.5~9
Asam Stearat 3.6~4.7 1~2.5
Asam Oleat 39~45 13~19
Asam Linoleat 7~11 0.5~2
Tabel 2.5. Beberapa nilai sifat fisiko kimia minyak kelapa sawit dan minyak inti sawit
Karakteristik MKS MIS
Bobot Jenis (25 oC) 0.900 0.900~0.913
Indeks Bias (40 oC) 1.4565~1.4585 1.415~1.495
Bilangan Iodium 48~56 14~20
Bilangan Penyabunan 196~206 244~254
Sumber : O’Brien, 1998
Minyak sawit banyak digunakan dalam oleokimia. Oleokimia merupkan suatu
senyawa kimia yang dibuat dari minyak atau lemak alami melalui proses peruraian
ester trigliserida menjadi gliserin dan asam lemak bebas beserta turunannya.
2.6. Kandungan Lemak Padat
2.6.1. Dilatometri
Dilatasi dari suatu lemak merupakan ekspansi isotermal yaitu perubahan dari keadaan
padat menjadi keadaan cair, yang mana sebelumnya lemak telah dipadatkan pada
kondisi yang tepat. Pada prinsipnya dilatasi adalah pengukuran volume dari suatu
lemak yang sudah diketahui beratnya diukur dibawah temperatur 60 oC (Paquot,
1987). Dialtasi lemak ini memberikan suatu petunjuk perbandingan antara lemak
padat dan lemak cair dalam sampel semi padat (Hamilton,1986).
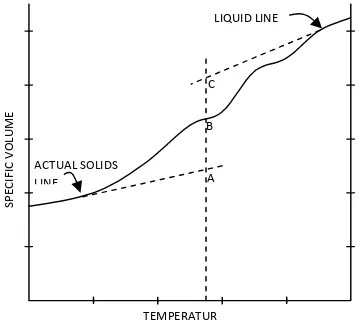
Gambar 2.4. Kurva dilatometri dari lemak
Gambar 2.4 menunjukkan hipotesa kurva dilatometri. Plot umum spesifik
temperatur yang diberikan. Persentase pada sama dengan fraksi yang tidak mencair
dari seluruh massa lemak. Persentse lemak padat = BC / AC.
Solid Fat Index(SFI) dapat dibandingkan dengan kurva dilatometri, yaitu SFI
= BC / AC, dimana SFI dianggap lebih besar dari ukuran perluasan garis lemak padat.
Temperatur yang digunakan untuk pengkuran garis pada keadaan padat adalah sangat
rendah dan sulit untuk dikontrol. Garis pada SFI memberikan slopeyang sama dengan
garis pada keadaan cair yang mudah untuk diukur.
2.6.2. Spektrometer NMR
Pada umunya, jika suatu sampel lemak cair, ditempatkan dalam tempat sampel pada
spektrometer NMR yang kemudian diikuti integrasi selama kira-kira 30 detik suatu
nilai diperoleh yaitu perbandingan jumlah lemak yang ada. Nilai ini merupakan signal
yang terintegrasi pada spektrum absorbsi yaitu suatu fungsi linier dari jum lah minyak
yang diperoleh dari peralatan yang dioperasikan pada kondisi yang benar-benar murni
dari kejenuhan, Nilai yang diperoleh dari spektrum ini bagaimanapun juga suatu
fungsi minyak (komposisi gliserida-gliseridanya) dengan temperatur sampel. Nilai ini
akan memeprlihatkan bahwa dasar untuk suatu metode pengukuran kandungan lemak
cair berbeda dengan metode pengukuran kandungan lemak padat. Jika signal yang
diukur dari Wo gram minyak adalah So Volt dan signal yang diukur dari Wf gram
lemak semi padat adalah Sf, maka signalper gram minyak adalah So/Wo. Signalper
gram lemak dalam sampel lemak semi padat adalah Sf /Wf, maka:
% minyak cair dalam lemak semi padat = 100 x
Wo
diukur pada temperatur yang sama dengan sampel lemak. Kedua bahwa stkitar minyak
atau referensi yang digunakan adalah komposisinya sama dengan minyak yang ada
dalam sampel. Metode yang didasarkan pada prinsip-prinsip ini telah diperoleh dan
pada umumnya memberikan hasil yang memuaskan. Metode ini mempunyai
kekurangan yaitu bahwa sampel yang diukur menggunakan termostat untuk
pengaturan temperatur. Prosedur ini adalah prosedur yang tidak langsung sehingga
percobaan telah dibuat dengan maksud untuk memperoleh pengukuran langsung
”direct” dari perbandingan padat cair. Jika signal dan wide line spektrometer
continuous wavediplotkan terhadap panjang medan maka kuva:
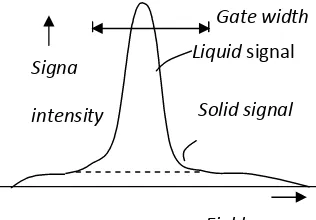
Gambar 2.5. Signal wide line dari campuran fase padat dan fase cair dari lemak
(Marangoni dan Roessau, 1982).
2.6.3. PulsedNMR
Kandungan lemak padat adalah suatu ukuran dari sejumlah padatan yang ada dalam
lemak dan diukur sebagai perbandingan jumlah proton cair yang ada pada temperatur
tertentu, yang diberikan dengan jumlah total proton dalam suatu sampel. Dengan
mengukur signal pada dua waktu yang berbeda maka persen kandungan lemak padat
dapat ditentukan. Berdasarkan prinsip ini telah diperkenalkan Spektrometer Pulsed
NMR resolusi rendah yang dirancang untuk analisa lemak. Pulsed NMR banyak
digunakan untuk menentukan jumlah kandungan minyak dalam biji-bijian dan produk
bahan makanan. Pemakaian pulsed NMR dalam analisa lemak yaitu penentuan
kandungan lemak padat. Pulsed NMR memberikan pengukuran yang langsung
daripadatan yang terdapat dalam lemak yang diukur di bawah temperatur 40 oC
(Hamilton, 1986).
Jika suatu sampel yang mengandung proton ditempatkan dalam suatu medan
magnet yang sangat kuat, proton-proton bersifat seperti magnet batang yang sangat
kecil dan cederung searah dengan arah medan. Bila medan yang kedua digunakan
dalam bentuk pulse gelombang radio penjajaran elektron dapat diubah 90o, energi
yang diserap oleh proton-proton memberikan gaya dorong untuk proses istirahat
tertentu yang memungkinkan energi berubah antara proton-proton mereka sendiri atau
antara proton-proton dengan kisi-kisi. Itu adalah merupakan proses yang penting
dalam pengembangan suatu metode untuk menentukan perbandingan padat dan cair.
Kecepatan yang mana sistem istirahat dan kecepatan dimana proton-proton
mengubah energinya dapat dikarakterisasi oleh waktu istirahat T2. Waktu istirahat T2 Gate width
Liquidsignal
Solid signal
Field Signa
berbeda untuk proton-proton fase padat dan proton fase cair. Maka untuk fase padat,
proton-proton mengubah ernerginya dengan cepat sebab jarak antara molekulnya
relatif pendek dan kisi-kisi yang keras memudahkan perpindahan energi. Untuk fase
cair, oleh karena proton-protonnya lebih menyebar dan kisi-kisinya tidak keras,
sehingga menyebabkan sistem istirahat lebih lama. Khususnya T2 untuk proton-proton
lemak padat adalah 30 μs sedangkan T2 untuk proton-proton minyak cair adalah 200
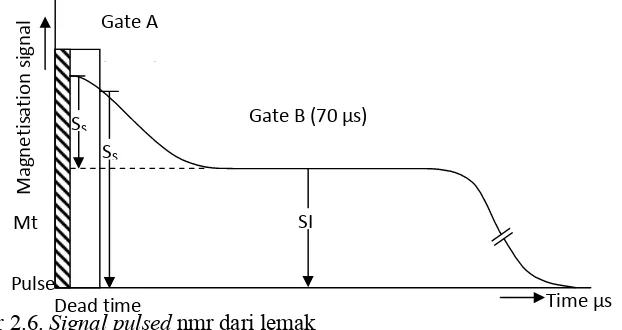
μs. Sinyal yang disebabkan pada coil penerima dari spektrometer pulseduntuk suatu campuran lemak padat dan cair dapat dilihat dalam gambar 2.6.
Gambar 2.6. Signal pulsednmr dari lemak
Tinggi mula-mula dari signal pulse90o adalah perbandingan dari jumlah total
proton-proton dalam kedua fase padat dan cair karena tidak ada terjadi waktu istirahat.
Misalnya besarnya signal dari fase padat adalah Ss dan fase cair adalah SI maka
amplitudo signalmula-mula akan menjadi Ss + SI.
Pada waktu tertentu, signaldari fase padat akan turun kurang dari 1 persen dari tinggi asalnya, biasanya kira-kira 50 ~ 70 μs. Oleh karena itu, jika signal diukur pada 70 μs ini akan sebanding dengan jumlah total proton pada fase cair dari sampel,
persentase fase padat dapat dihitung dari persamaan berikut:
% Fase Padat = x 100
sebagai perbandingan jumlah proton – proton fase padat dengan jumlah proton-proton
dalam sampel, Tidak ada koreksi yang dibuat untuk membedakan proton antara fase
padat dan fase cair, Nlainya dinyatakan sebagai persentase, yang selalu disertai
dengan penentuan temperatur, Pada tabel 2.6 diperlihatkan kandungan lemak padat
dan hubungannya dengan titik lebur.
Tabel 2.6. Titik lebur dan kandungan lemak padat interesterifikasi hidrogenasi
minyak kelapa sawit
Lemak
Indeks Kandungan Lemak Padat
Titik Lebur
(oC)
10oC 20oC 35oC 38oC
HPKO 46.8 74.2 67.0 15.4 11.7
Interersterifikasi HPKO 35.0 65.0 49.9 1.4 1.1
50%HPKO : 50%HPKO 41.7 70.0 54.7 8.7 5.2
65%HPKO : 35%HPKO 44.2 71.0 59.7 10.2 6.7
80%HPKO : 20%HPKO 46.0 72.4 62.6 12.4 8.5
Sumber : Swern, 1982
Berdasarkan data tersebut maka kandungna lemak padat semakin rendah jika
titik lebur rendah dan pada pengukuran kandungan lemak padat pada berbagai
temperatur tampak semangkin tinggi temperatur pengukuran, kandungan lemak padat
juga menurun. Hal ini menunjukkan bahwa kandungna lemak padat merupakan fungsi
temperatur.
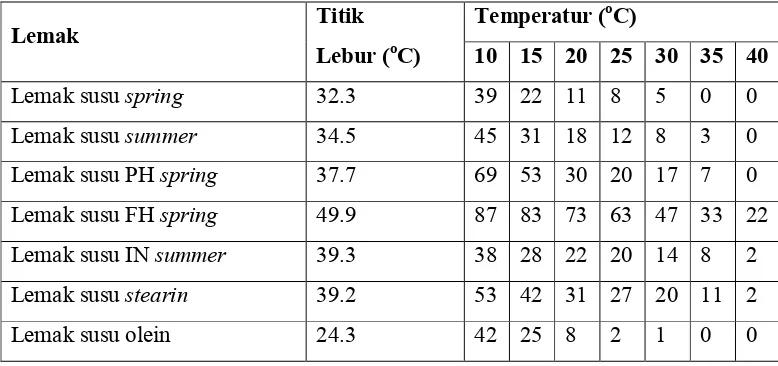
Tabel 2.7. Titik lebur dan kandungan lemak padat (%) antara lemak susu dan lemak
lainnya yang dianalisa dengan NMR
Lemak Titik Temperatur (
o C)
Lebur (oC) 10 15 20 25 30 35 40
Lemak susu spring 32.3 39 22 11 8 5 0 0
Lemak susu summer 34.5 45 31 18 12 8 3 0
Lemak susu PH spring 37.7 69 53 30 20 17 7 0
Lemak susu FH spring 49.9 87 83 73 63 47 33 22
Lemak susu IN summer 39.3 38 28 22 20 14 8 2
Lemak susu stearin 39.2 53 42 31 27 20 11 2
Lemak susu olein 24.3 42 25 8 2 1 0 0
PH = Padat Sebahagian; FH = Semuanya Padat ; IN = Interesterifikasi
Demikian juga pada tabel 2.7 juga memperlihatkan kondisi yang sama, hanya
pada percampuran antara lemak susu dengan stearin yang memiliki titik lebur (39.2
o
C) memiliki kandungan lemak padat yang lebih besar (11 %) dari percampuran yang
memiliki titik lebur lebih tinggi (39.3 oC) yaitu kandungan lemak padatnya (8 %)
(Marangoni dan Roessau, 1982).
2.7. Titik Lebur pada Lemak
Titik lebur lemak merupakan suatu sifat empiris yang berhubungan dengan sifat fisik
lemak. Titik lebur berhubungan langsung terhadap temperatur dimana lemak
mengkristal atau memadat. Semangkin tinggi temperatur maka titik lebur semangkin
tinggi, tergantung dari perubahan sifat polimorfis kristal lemak. Titik lebur lemak atau
tidak merupakan suhu yang tepat, tetapi merupakan kisaran suhu tertentu. Hal ini
disebabkan minyak atau lemak disusun dari campuran gliserida dan komponen
lainnya. Asam lemak selalu menunjukkan kenaikan titik lebur, dengan semangkin
panjangnya rantai karbon dan semangkin jenuhnya lemak tersebut.
Lemak yang berstruktur trans mempunyai titik lebur yang lebih tinggi daripada bentuk
cis. Ada beberapa penentuan titik lebur, namun yang umum digunakan untuk
penentuan titik lebur lemak adalah dengan cara sebagai berikut:
Lemak dicairkan terlebih dahulu, kemudian pipa kapiler dicelupkan sehingga cairan
masuk ke dalam pipa. Ujung pipa ditutup dan diangkat dan ujung yang lain ditutup
dengan jalan memanaskan sehingga ujung pipa meleleh dan tertutup. Selanjutnya
dibekukan dalam freezer dengan temperatur 4~10 oC. Pipa kapiler yang digunakan
berdiameter 1 mm dan panjang 5~10 cm. Kemudian pada pipa kapiler diikatkan
termometer dan dicelupkan ke dalam air dingin yang suhunya dinaikkan bertahap
sekitar 0.5 oC. Lemak akan berangsur-angsur menjadi jernih sebelum mencair
sempurna. Pemanasan air diteruskan sampai isi pipa kapiler jernih. Suhu yang
menunjukkan dalam pipa kapiler jernih adalah merupakan titik lebur lemak
(Sudarmadji, 1996).
2.8. Kromatografi Gas
Secara etimologi, kromatografi berasal dari bahasa yunani yang berarti ‘warna’ dan
‘tulis’. Kromatografi Gas (GC), merupakan jenis kromatografi yang digunakan dalam
kimia organik untuk pemisahan dan analisis, Oleh karena itu, senyawa-senyawa kimia
menguji kemurnian dari bahan tertentu, atau memisahkan berbagai komponen dari
campuran. Kromatologi gas memisahkan suatu campuran berdasarkan kecepatan
migrasinya di dalam fasa diam yang dibawa oleh fasa gerak. Sedangkan perbedaan
migrasi ini disebabkan oleh adanya perbedaan interaksi diantara senyawa-senyawa
kimia tersebut (di dalam campuran) dengan fasa diam dan fasa geraknya.
Sebagaiman dalam dalam fase gas-cair, GC fase gerak dan fase diamnya
diantaranya :
Fase gerak adalah gas dan zat terlarut terpisah sebagai uap. Pemisahan tercapai
dengan partisi sampel antara fase gas bergerak
Fase diam berupa cairan dengan titik didih tinggi (tidak mudah menguap) yang
terikat pada zat padat penunjangnya.
Dalam GC, fase yang bergerak (atau "mobile phase") adalah sebuah operator
gas, yang biasanya gas murni seperti helium atau yang tidak reactive seperti gas
nitrogen. Stationary atau fasa diam merupakan tahap mikroskopis lapisan cair atau
polimer yang mendukung gas murni, di dalam bagian dari sistem pipa-pipa kaca atau
logam yang disebut kolom
GC mirip dengan pecahan penyulingan, karena kedua proses memisahkan
komponen dari campuran terutama berdasarkan titik didih (atau tekanan uap)
perbedaan. Namun, pecahan penyulingan biasanya digunakan untuk memisahkan
komponen campuran pada skala besar, sedangkan GC dapat digunakan pada skala
yang lebih kecil (yakni microscale).
GC terkadang juga dikenal sebagai uap-tahap kromatografi (VPC), atau
gas-cair kromatografi partisi (GLPC). Alternatif nama ini, serta masing-masing singkatan,
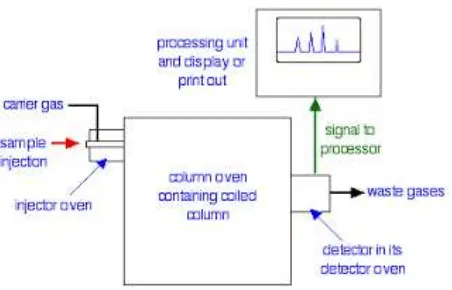
Gambar 2.7. Diagram alir kromatografi gas-cair
Mekanisme kerja GC dan komponen dalam GC :
2.8.1. Fase Mobil (Gas Pembawa)
Fasa mobil (gas pembawa) dipasok dari tanki melalui pengaturan pengurangan
tekanan. Kemudian membawa cuplikan langsung ke dalam kolom. Jika hal ini terjadi,
cuplikan tidak menyebar sebelum proses pemisahan. Cara ini cocok untuk cuplikan
yang mudah menyerap.
Gas pembawa ini harus bersifat inert dan harus sangat murni. Seringkali gas
pembawa ini harus disaring untuk menahan debu uap air dan oksigen. Gas sering
digunakan adalah N2, H2 He dan Ar (Hendrayati, 2010).
2.8.2. Injeksi Sampel
Sejumlah kecil sampel yang akan dianalisis diinjeksikan pada mesin menggunakan
semprit kecil. Jarum semprit menembus lempengan karet tebal (Lempengan karet ini
disebut septum) yang mana akan mengubah bentuknya kembali secara otomatis ketika
semprit ditarik keluar dari lempengan karet tersebut.
Injektor berada dalam oven yang mana temperaturnya dapat dikontrol. Oven
tersebut cukup panas sehingga sampel dapat mendidih dan diangkut ke kolom oleh gas
pembawa misalnya helium atau gas lainnya.
Fase bergerak dalam kromatografi ini adalah gas, yang paling lazim adalah
helium, hidrogen, atau nitrogen. Kompenen pilihan gas pembawa terutama tergantung
pada karakteristik detektor. GC komersial biasanya menyediakan katup pengatur
tambahan untuk pengendalian tekanan yang baik pada inlet kolom. Dekat inlet kolom
Sampel-sampel tersebut bisa berupa gas atau cairan yang mudah menguap. Lubang
injeksi dipanaskan agar sampel cair teruapkan dengan cepat (Hendrayati, 2010).
2.8.3. Kolom
Aliran gas selanjutnya menemui kolom yang diletakkan dalam oven bertemperatur
konstan. Ini adalah jantung instrumen tesebut, tempat dimana proses kromartgrafi
dasar berlangsung. Kolom memilki variasi dalam hal ukuran dan bahan isian. Tabung
diisi dengan bahan padat halus dengan luas permukaan besar yang relatif inert.
Padatan itu sebenarnya hanya sebuah penyangga mekanik untuk cairan, sebelum diisi
kedalam kolom, padatan tersebut diimpregnasi dengan cairan yang diinginkan yang
berpareran sebagai fasa stasioner sesungguhnya. Cairan ini harus stabil dan nonfolatil
pada temperatur kolom, pemisahan dan harus sesuai untuk pemisahan tertentu.
Ada dua tipe utama kolom dalam kromatografi gas-cair. Tipe pertama, kolom
Partisi, berisi bahan padat inertmenyangga lapisan tipis cairan, disebut Kromatografi
Gas Cair (GLC). Tipe kedua, kolom adsorbsi berisi partikel penyerap yang umumnya
digunakan untuk analisa gas permanen dan hidro karbon rendah, biasa disebut
Kromatograrfi Gas Padat (GSC).
Kolom biasanya dibuat dari baja tak berkarat dengan panjang antara 1 sampai
4 meter, dengan diameter internal sampai 4 mm. Kolom digulung sehingga dapat
disesuaikan dengan oven yang terkontrol secara termostatis. Kolom dipadatkan
dengan tanah diatomae, yang merupakan batu yang sangat berpori. Tanah ini dilapisi
dengan cairan bertitik didih tinggi dan biasanya polimer lilin.
Temperatur kolom dapat bervariasi antara 50oC sampai 250oC. Temperatur
kolom lebih rendah daripada gerbang injeksi pada oven, sehingga beberapa komponen
campuran dapat berkondensasi pada awal kolom. Kolom memulai pada temperatur
rendah dan kemudian terus menerus menjadi lebih panas dibawah pengawasan
komputer saat analisis berlangsung.
Ada tiga hal yang dapat berlangsung pada molekul tertentu dalam campuran
yang diinjeksikan pada kolom:
a. Molekul dapat berkondensasi pada fase diam.
b. Molekul dapat larut dalam cairan pada permukaan fase diam
Dari ketiga kemungkinan itu, tak satupun yang bersifat permanen. Senyawa
yang mempunyai titik didih yang lebih tinggi dari temperatur kolom secara jelas
cenderung akan berkondensasi pada bagian awal kolom. Namun, beberapa bagian dari
senyawa tersebut akan menguap kembali dengan dengan jalan yang sama seperti air
yang menguap saat udara panas, meskipun temperatur dibawah 1000 oC. Peluangnya
akan berkondensasi lebih sedikit selama berada di dalam kolom.
Sama halnya untuk beberapa molekul dapat larut dalam fase diam cair. Beberapa
senyawa akan lebih mudah larut dalam cairan dibanding yang lainnya. Senyawa yang
lebih mudah larut akan menghabiskan waktunya untuk diserap pada fase diam,
sedangkan senyawa yang suka larut akan menghabiskan waktunya lebih banyak dalam
fase gas.
Proses dimana zat membagi dirinya menjadi dua pelarut yang tidak
bercampurkan karena perbedaan kelarutan, dimana kelarutan dalam satu pelarut satu
lebih mudah dibanding dengan pelarut lainnya disebut sebagai partisi. Sekarang, kita
bisa beralasan untuk memperdebatkan bahwa gas seperti helium tidak dapat dijelaskan
sebagai pelarut. Tetapi, istilah partisi masih dapat digunakan dalam kromatografi
gas-cair.
Substansi antara fase diam cair dan gas. Beberapa molekul dalam substansi
menghabiskan waktu untuk larut dalam cairan dan beberapa lainnya menghabiskan
waktu untuk bergerak bersama-sama dengan gas (Hendrayati, 2010).
2.8.4. Detektor
Setelah muncul dari kolom itu, aliran gas lewat melalui sis lain detektor. Maka elusi
zat terlarut dari kolom itu mengatur ketidakseimbangan antaradua sisi detektor yang
direkam secara elektrik. Laju aliran gas pembawa adalah hal yang sangat penting, dan
biasanya pengukur aliran untuk itu tersedia. Secara normal gas-gas yang muncul
dialirkan keluar pada tekanan atmosfir. Karena pekerja laboratorium secara terus
menerus terpapar oleh uap senyawa-senyawa yang terkromatogafi yang mungkin tak
baik walaupun kadarnya biasanya kecil maka ventilasi pada keluaran instrumen harus
diperhatikan. Ketentuan bisa dibuat untuk menjebak zat terlarut yang dipisahkan
setelah muncul dari kolom jika hal ini dibutuhkan untuk penyelidikan lebih lanjut.
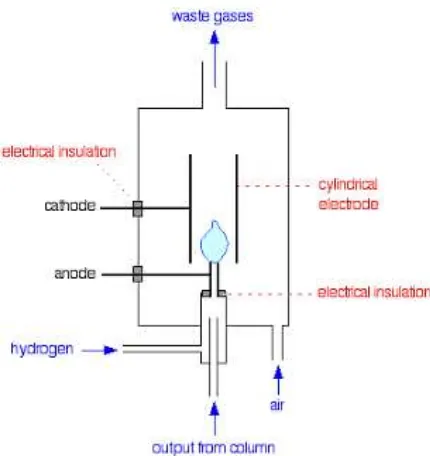
Ada beberapa tipe detektor yang biasa digunakan. Detektor ionisasi nyala
dijelaskan pada bagian bawah penjelasan ini, merupakan detektor yang umum dan
Gambar 2.8. Detektor ionisasi nyala
Dalam mekanisme reaksi, pembakaran senyawa organik merupakan hal yang
sangat kompleks. Selama proses, sejumlah ion-ion dan elektron-elektron dihasilkan
dalam nyala. Kehadiran ion dan elektron dapat dideteksi.
Seluruh detektor ditutup dalam oven yang lebih panas dibanding dengan
temperatur kolom. Hal itu menghentikan kondensasi dalam detektor. Jika tidak
terdapat senyawa organik datang dari kolom, kita hanya memiliki nyala hidrogen yang
terbakar dalam air. Sekarang, anggaplah bahwa satu senyawa dalam campuran kita
analisa mulai masuk ke dalam detektor.
Ketika dibakar, itu akan menghasilkan sejumlah ion-ion dan elektron-elektron
dalam nyala. Ion positif akan beratraksi pada katoda silinder. Ion-ion negatif dan
elektron-elektron akan beratraksi pancarannya masing-masing yang mana merupakan
anoda.Hal ini serupa dengan apa yang terjadi selama elektrolisis normal.
Pada katoda, ion positif akan mendatangi elektron-elektron dari katoda dan
menjadi netral. Pada anoda, beberapa elektron dalam nyala akan dipindahkan pada
elektroda positif; ion-ion negatif akan memberikan elektron-elektronnya pada
elektroda dan menjadi netral.
Kehilangam elektron-elektron dari satu elektroda dan perolehan dari elektroda
lain, akan menghasilkan aliran elektron-elektron dalam sirkuit eksternal dari anoda ke
Arus yang diperoleh tidak besar, tetapi dapat diperkuat. Jika senyawa-senyawa
organik lebih banyak dalam nyala, maka akan banyak juga dihasilkan ion-ion, dan
dengan demikian akan terjadi arus listrik yang lebih kuat. Ini adalah pendekatan yang
beralasan, khususnya jika kita berbicara tentang senyawa-senyawa yang serupa, arus
yang kita ukur sebanding dengan jumlah senyawa dalam nyala.
Kekurangan utama dari detektor ini adalah pengrusakan setiap hasil yang
keluar dari kolom sebagaimana yang terdeteksi. Jika kita akan mengrimkan hasil ke
spektrometer massa, misalnya untuk analisa lanjut, kita tidak dapat menggunakan
detektor tipe ini (Hendrayati, 2010).
2.8.5. Pencatat (Recorder)
Fungsi recordersebagai alat untuk mencetak hasil percobaan pada sebuah kertas yang
hasilnya disebut kromatogram (kumpulan puncak grafik).
Hasil akan direkam sebagai urutan puncak-puncak, setiap puncak mewakili
satu senyawa dalam campuran yang melalui detektor. Sepanjang kita mengontrol
secara hati-hati kondisi dalam kolom, kita dapat menggunakan waktu retensi untuk
membantu mengidentifikasi senyawa yang tampak-tentu saja kita atau seseorang lain
telah menganalisa senyawa murni dari berbagai senyawa pada kondisi yang sama.
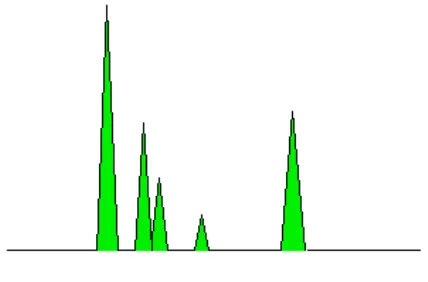
Gambar 2.9. Peak areakromatogram
Area dibawah puncak sebanding dengan jumlah setiap senyawa yang telah
melewati detektor, dan area ini dapat dihitung secara otomatis melalui komputer yang
dihubungkan dengan monitor. Area yang akan diukur tampak sebagai bagian yang
berwarna hijau dalam gambar yang disederhanakan.
Perlu dicatat bahwa tinggi puncak tidak merupakan masalah, tetapi total area
tertinggi dan memiliki area yang paling luas. Hal ini tidak selalu merupakan hal
seharusnya.
Mungkin saja sejumlah besar satu senyawa dapat tampak, tetapi dapat terbukti
dari kolom dalam jumlah relatif sedikit melalui jumlah yang lama. Pengukuran area
selain tinggi puncak dapat dipergunakan dalam hal ini (Hendrayati, 2010).
2.8.6. Waktu Retensi
Waktu yang digunakan oleh senyawa tertentu untuk bergerak melalui kolom menuju
ke detektor disebut sebagi waktu retensi. Waktu ini diukur berdasarkan waktu dari saat
sampel diinjeksikan pada titik dimana tampilan menunujukkan tinggi puncak
maksimum untuk senyawa itu.
Setiap senyawa memiliki waktu retensi yang berbeda. Untuk senyawa tertentu,
waktu retensi sangat bervariasi dan bergantung pada titik didih senyawa. Senyawa
yang mendidih pada temperatur yang lebih tinggi daripada temperatur kolom, akan
menghabiskan hampir seluruh waktunya untuk berkondensasi sebagai cairan pada
awal kolom. Dengan demikian, titik didih yang tinggi akan memiliki waktu retensi
yang lama.
Kelarutan dalam fase cair. Senyawa yang lebih mudah larut dalam fase cair,
akan mempunyai waktu lebih singkat untuk dibawa oleh gas pembawa.. Kelarutan
yang tinggi dalam fase cair berarti memiliki waktu retensi yang lama.
Temperatur kolom. Temperatur tinggi menyebakan pergerakan
molekul-molekul dalam fase gas, baik karena molekul-molekul-molekul-molekul lebih mudah menguap, atau
karena energi atraksi yang tinggi cairan dan oleh karena itu tidak lama tertambatkan.
Temperatur kolom yang tinggi mempersingkat waktu retensi untuk segala sesuatunya
di dalam kolom.
Untuk memberikan sampel dan kolom, tidak ada banyak yang bisa dikerjakan
menggunakan titik didih senyawa atau kelarutannya dalam fase cair, tetapi kita dapat
mempunyai pengatur temperatur.
Semakin rendah temperatur kolom semakin baik pemisahan yang akan kita
dapatkan, tetapi akan memakan waktu yang lama untuk mendapatkan senyawa karena
kondensasi yang lama pada bagian awal kolom.
Dengan kata lain, menggunakan temperatur tinggi, segala sesuatunya akan
melalui kolom lebih cepat, tetapi pemisihannya kurang baik. Jika segala sesuatunya
puncak-puncak dalam kromatogram. Solusinya adalah dimulai dengan kolom dengan
suhu yang rendah kemudian perlahan-lahan secara teratur temperaturnya dinaikkan.
Pada awalnya, senyawa yang menghabiskan lebih banyak waktunya dalam
fase gas akan melalui kolom secara cepat dan dapat dideteksi. Dengan adanya sedikit
pertambahan temperatur akan memperjelas perlekatan senyawa. Peningkatan
temperatur masih dapat lebih `melekatan` molekul-molekul fase diam melalui kolom.
Salah satu kegunaan GC adalah untuk mengetahu susunan komposisi asam
lemak pada minyak sehingga Asam Lemak Trans (TFA) yang terkandung dalam
minyak tersebut dapat diketahui. Jumlah TFA yang dikonsumsi pada umumnya