Yahdiana Har ahap, Umar M ansur , Ther esia Sinandang Depar temen Far masi FM IPA - UI
AN ALISIS GLIM EPIRIDA DALAM
PLASM A TIKUS
Majalah Ilmu Kefarmasian, Vol. III, No.1, A pril 2006, 22 - 37 ISSN : 1693-9883
ABSTRACT
The aim of this research is to find the method for analyze glimepiride and it’ s metabolite. Glimepiride is the second generation of antidiabetic oral from the sulphonyl urea that works by stimulating the insulin secretion from beta cells of pancreas. Glimepiride is isolated from plasma the using chloroform. Using the high perfor-mance liquid chromatography method which include C
18 reversed phase column,
using mixture of methanol:water (50:50, v/v) as a mobile phase, flow rate 1.0 ml/ minutes, detection at wavelenght 228 nm with photo diode array detector gives reten-tion times of glimepiride in 17 minutes without any interference from endogen com-ponent of plasma and from it’ s metabolite. Linearity with added internal standard gliclazide was established for the range concentration 100-1000 ng/ml with coeffi-cient of correlation (r) is 0.9977 and give the limit of quantitation of glimepiride in 50 ng/ml. The results of validation method fulfilled for the given criterias.
Key W ords : Glimepiride, blood plasma, HPLC
PEN D A HULUA N
A . LA TA R BELA KA NG
Glimep irid a merup akan anti-diabetes oral dari golongan sulfonil urea generasi II yang terbaru. Obat ini bekerja dengan cara menstimulasi sekresi insulin dari sel beta pankreas. Belakangan p enggunaan o bat ini sebagai antid iabetes semakin me-ningkat, karena keuntungannya yaitu dosis terapi yang rendah dan risiko timbulnya efek hipoglikemia yang lebih kecil dibandingkan golongan sulfonil urea lainnya. Pada pengguna-an jpengguna-angka ppengguna-anjpengguna-ang, kadar glimepirida dalam darah perlu dipantau untuk mend eteksi gejala d ini terjad inya efek samping, sehingga diperlukan
m eto d e y ang terp ercay a untuk kepentingan analisis secara rutin. Selain itu suatu metode analisis obat d alam cairan bio lo gis juga sangat diperlukan untuk tujuan lain seperti p erhitungan p arameter farmako -kinetika, bio availabilitas, bio ekui-valen dan yang lainnya ((Kahn, CR (Ed) 1995),(Shargel et al. 1988)).
Metode kromatografi cair kinerja tinggi (KCKT) sejak tahun 1990 sudah dimanfaatkan untuk analisis glime-pirida dalam cairan biologis (Lehr, Damn P. 1990). Mengingat kad ar glimepirida dalam darah yang cukup kecil (dalam kisaran ng/ mL) maka metode analisis glimepirida semakin berkembang untuk mend ap atkan sensitivitas yang tinggi, sehingga identifikasi glimepirida dapat dilaku-kan dengan akurat. Kromatografi cair dengan spketrometer massa merupa-kan meto d e yang saat ini banyak d ig unakan untuk m eng analisis glimepirida dalam cairan bio lo gis karena sensitivitasnya yang cukup tinggi ((Ismail et al. 2004),(Hon Yun Kim et al. 2004),(Ho, Emmie, et al. 2004)) d an sud ah d im anfaatkan untuk studi biavailabilitas dan bio-ekuivalen. Meto d e ini melibatkan seperangkat instrumen yang lebih canggih dan ko mpleks jika diban-dingkan dengan metode-metode lain yang sering digunakan dalam rangka analisis obat dalam cairan biologis di Indo nesia. Di lingkungan Depar-temen Farmasi FMIPA Universitas Indonesia sendiri sudah ada pene-litian mengenai analisis glimepirida dalam plasma secara in vitro dengan menggunakan meto d e yang lebih sed erhana d an lebih eko no m is dibandingkan metode-metode yang telah d ipublikasikan, yaitu secara KCKT dengan detektor uv-vis (Wu-landari, Mahi 2004). Secara in vivo
meto d e ini belum teruji. Berbekal metode ini, maka pada penelitian ini akan dilakukan analisis glimepirida
in vivo dalam plasma dengan meng-gunakan hew an coba. Dalam pene-litian akan diamati apakah dalam p ro ses analisis glimep irid a tid ak terganggu baik oleh metabolit dari glimepirida atau komponen endogen lain dalam plasma.
B. TUJUA N PENELITIA N
Melakukan analisis glimepirida secara in vivo dengan menggunakan meto d e yang telah d ivalid asi d an mengamati seberapa jauh gangguan yang dapat muncul dalam analisis glimepirida.
C. BA HA N DA N CA RA KERJA
BA HA N
Glim ep irid a (Kalbe Farm a), Glipizida (BPOM), Gliklazida Gli-benklam id a, M etano l p ro H PLC (Merck), Etanol pro HPLC (Merck), Aqua bidestilata Kloroform (Merck), Gas nitro gen Heparin (Inviclo t ®), Dietil eter (Merck), Tikus putih jantan strain Spraque–Dawley berumur 2-3 bulan dan dengan berat badan 150-200 gram. (BPOM)
A LA T
KCKT A lliance W aters 2695 d engan d etekto r Photodiode A rray
dengan integrator UV-PC v.39, Pipet volume, Timbangan analitik Ultra-sonik Branson, Shaker, Sentrifugator,
V ortex , Transfer p et (Effendorf, Turbovap evaporator)
PROSEDUR KERJA
1. Penetapan kondisi analisis Larutan induk glimepirida di-encerkan hingga didapat konsen-trasi 1 µg/ ml, kemudian disuntikkan sebanyak 20 µl ke dalam alat KCKT d eng an fase g erak m etano l:air masing –masing d eng an p erban-dingan 80:20, 70:30, 60:40, dan 50:50. Diamati kondisi analisis yang paling o p tim um d ari berbag ai p erban-dingan komposisi fase gerak.
2. Pemilihan baku dalam yang cocok
Larutan ind uk g lip izid a, g li-klazida, dan glibenklamida diencer-kan d eng an fase g erak terp ilih hingga didapat konsentrasi masing-masing 1 µg/ ml. Masing-masing-masing larutan baku dalam disuntikkan 20 µl ke d alam KCKT d eng an ko nd isi terpilih. Kemudian diamati w aktu retensi m asing -m asing z at d an dibandingkan dengan waktu retensi glimepirida.
3. Uji Linearitas
Larutan stand ar g lim ep irid a diencerkan dengan fase gerak hingga didapat ko nsentrasi 100, 200, 300, 400, 800 dan 1000 ng/ ml. Kemudian disuntikkan sebanyak 20 ml ke dalam
alat KCKT dengan kondisi terpilih, dan dibuat kurva persamaan garis regresi linier luas puncak terhadap ko nsentrasi glimepirid a. Langkah yang sama dilakukan pada larutan glimep irid a d engan p enambahan baku dalam 1000ng/ ml pada masing-masing konsentrasi. Kemudian di-buat kurva persamaan garis regresi linier p erband ingan luas p uncak terhad ap ko nsentrasi glimepirid a. Dihitung nilai koefisien korelasi dari kedua kurva tersebut.
4. A nalisis glimepirida dalam plasma in vitro
a. uji spesifisitas (selektivitas) Sebany ak 0,5 m l p lasm a ko so ng (tanp a p enam bahan glimepirida) diekstraksi dengan 2,5 ml klo ro fo rm d engan cara d iko co k menggunakan shaker
mengandung glimepirida 100, 400, 1000 ng/ ml dan baku dalam terpilih 1000 ng/ ml.
b. Uji perolehan kembali Sebany ak 0,5 m l p lasm a yang mengandung glimepirida 100, 400, d an 1000 ng/ ml d i-ekstraksi dengan 2,5 ml kloro-form dengan cara dikocok meng-gunakan shaker pada kecepatan 100 rpm selama 15 menit. Pisah-kan fase o rg anik, kem ud ian ekstraksi kembali dengan cara yang sama sebanyak dua kali. Semua larutan kloroform dikum-pulkan dan diuapkan dengan gas nitrogen pada temperatur 37°C hingga kering. Kemudian residu dilarutkan dalam 1,0 ml metanol,
vorteks selama 30 detik. Masing-masing larutan yang diperoleh d isuntikkan secara berulang sebany ak 20 µl p ad a KCKT dengan kondisi terpilih, dihitung persentase pero lehan kembali dengan membandingkan luas puncak yang diperoleh dengan larutan standard. Uji perolehan kembali juga d ilakukan p ad a plasma yang mengandung glime-pirida 100, 400, 1000 ng/ ml dan baku dalam terpilih 1000 ng/ ml.
c. Uji limit deteksi dan limit kuantitasi
Larutan ekstrak p lasma yang mengandung glimepirida dengan konsentrasi 100 ng/ ml disuntikkan sebanyak 20 ml ke dalam alat KCKT dengan kondisi
terp ilih, kem ud ian d ihitung tinggi p uncak p ad a kro mato -gram. Dihitung nilai p erban-d ingan tinggi puncak erban-d engan tinggi derau (S/ N’ = signal to noise ratio). Untuk tinggi derau (noise) disuntikkan pelarut metanol:air (50:50), kemudian pada kroma-to gram d ihitung tinggi d erau tertingginya.
d. Uji Linearitas
e. Uji akurasi dan presisi Sebany ak 0,5 m l p lasm a yang mengandung glimepirida 100 , 400, dan 1000 ng/ ml di-ekstraksi dengan 2,5 ml kloro-form sebanyak dua kali. Semua fraksi kloroform dikumpulkan dan diuapkan dengan gas nitro-gen pada temperatur 37°C hingga kering. Kemudian residu dilarut-kan dalam 1,0 ml metanol, vorteks
selama 30 detik. Masing-masing larutan yang diperoleh disuntik-kan sebanyak 20 ml secara ber-ulang (minimal lima kali) pada KCKT dengan kondisi terpilih. Dihitung nilai persentase akurasi d an ko efisien v ariasiny a. Uji akurasi dan presisi juga dilaku-kan pada plasma yang mengan-dung glimepirida 100, 400, 1000 ng/ ml dan baku dalam terpilih 1000 ng/ ml dengan mengulangi langkah-langkah seperti di atas.
5. A nalisis glimepirida dalam plasma tikus
a. Perhitungan dosis untuk tikus
Dosis yang akan digunakan adalah 4 mg pada manusia.
Untuk d o sis tikus/ 200g = dosis manusia x faktor konversi x faktor farmakokinetik
= 4 mg x 0.018 x 6 = 0.432 mg/200 g tikus
b. A klimatisasi hewan coba Hewan coba diaklimatisasi-kan dalam lingkungan sekitar
selama dua minggu. Pada tahap ini dilakukan pengamatan ter-hadap keadaan umum, seperti penimbangan berat badan, tikus yang sakit tidak diikutkan dalam percobaan.
c. H ew an co ba d ibag i ke dalam dua kelompok. Kelompok I diberi perlakuan pemberian glimepirida 0,432 mg/ 200 g (per o ral) p ad a tikus no rmal, d an kelompok II diberi placebo (air). Masing-masing tikus ditimbang dan atur pemberian dosis sesuai dengan berat tikus.
terpilih. Pad a kelo mpo k yang diberi perlakuan placebo diamati adanya gangguan/ interferensi pada kromatogram dari ekstrak plasma blangko. Pada kelompok yang d iberi p erlakuan glime-p irid a d iam ati m unculny a puncak glimepirida dan meta-bolitnya pada kromatogram.
HA SIL DA N PEM BA HA SA N
1. Penetapan panjang gelombang analisis
Panjang gelombang maksimum untuk larutan glimepirid a ad alah 228 nm,. larutan gliklazida pada 228,5 nm, larutan glipizida pada 227,4 nm, dan larutan glibenklamida pada 229,7 nm. Berdasarkan spektrum serapan yang diperoleh, glimepirida memiliki panjang gelombang maksimum pada 228 nm.
Pad a p anjang g elo mbang ini metanol masih memberikan serapan yang cukup besar meskipun begitu hal ini tidak mengganggu analisis glimepirida. Serapan metanol dapat d iminimalkan d engan menggeser panjang gelo mbang ke arah yang lebih besar hanya saja mengakibat-kan menurunnya respon glimepirida. Selanjutny a d iamati sp ektrum serapan dari ketiga zat yang akan d ig unakan sebag ai baku d alam . Panjang gelombang maksimum dari ketiga zat ini d engan glimepirid a tidak berbeda jauh, sehingga dapat ditetapkan bahw a panjang gelo m-bang analisis adalah pada 228 nm.
2. Penetapan kondisi analisis Pada fase gerak metanol : air (80: 20; v / v ) d ip ero leh w aktu retensi g limep irid a 3,753 menit, d eng an jumlah pelat teoritis 2748, dan faktor ikutan 1,13. Pada fase gerak metanol: air (70 : 30; v/ v) dipero leh w aktu retensi g lim ep irid a 5,83 m enit, dengan jumlah pelat teoritis 3054, dan faktor ikutan 1,16. Pada fase gerak metanol : air (60 : 40; v/ v) diperoleh waktu retensi glimepirida 8,93 menit, dengan jumlah pelat teoritis 1852, dan faktor ikutan 1,85. Pada fase gerak metanol:air (50:50) diperoleh waktu retensi glimep irid a 17,064 menit, dengan jumlah pelat teoritis 2954, dan faktor ikutan 1,08. Dari kedua kondisi terakhir yang menunjukkan pemi-sahan yang baik, pad a ko mpo sisi metano l : air (50 : 50) d ip ero leh jumlah lempeng teoritis yang lebih besar dan nilai HETP yang lebih kecil. Sehing g a fase g erak y ang akan d igunakan d alam analisis ad alah metanol : air (50 : 50; v/ v) hanya saja w aktu analisis untuk ko nd isi ini cukup lama yaitu sekitar dua puluh menit.
waktu analisis sehingga mengurangi keefisienan w aktu. Sedangkan jika laju alir dipercepat maka akan terjadi kenaikan tekanan sistem yang akan meng akibatkan semakin p end ek umur kolom.
3. Pemilihan baku dalam
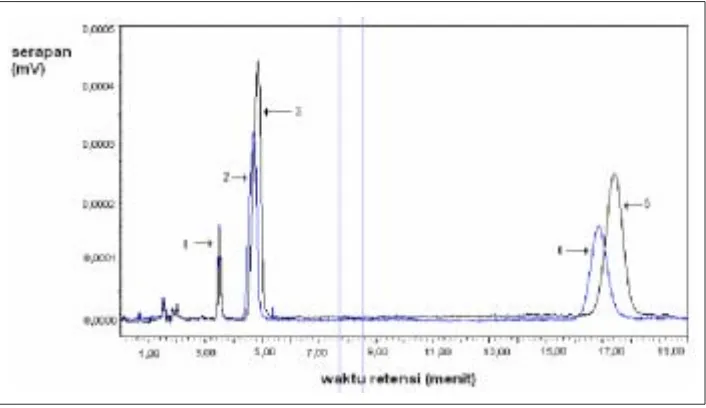
Pad a ko nd isi terp ilih y aitu dengan fase gerak metanol : air (50: 50), laju alir 1,0 m l/ m enit d an temperatur kolom 500 C disuntikkan ketiga larutan baku dalam.
Dari literatur yang ada ((Ismail et al. 2004)(H o n Yun Kim et al. 2004)(Ho, Emmie, et al. 2004),(Rafael E 2001)) glibenklamida merupakan baku dalam terpilih untuk analisis glimepirida dalam plasma. Hal ini m eny ang kut struktur d an sifat farmakokinetik yang hampir sama dengan glimepirida. Pada ko ndisi terpilih glibenklamida muncul pada 16,9 m enit d ekat d eng an w aktu retensi glimepirida. Hal ini menan-dakan glibenklamida memiliki sifat kepolaran yang paling mirip dengan glimepirida, tetapi puncak gliben-klamida berhimpit dengan puncak g lim ep irid a sehing g a tid ak bisa d ig unakan sebag ai baku d alam . Glip izid a d an gliklazid a masing-masing cukup terpisah baik dengan glimepirida dengan masing-masing nilai reso lusiny a 4,52 d an 4,43, resolusi merupakan parameter untuk menunjukkan apakah dua komponen terpisah dengan baik. Sebagai baku dalam dipilih gliklazida meskipun nilai reso lusi sed ikit lebih kecil daripada glipizida tapi waktu retensi
lebih lama daripada glipizida. Hal ini untuk menghindari puncak-puncak yang dapat muncul pada menit-menit aw al dalam analisis plasma. (lihat gambar 1)
4. Uji linearitas
Pada larutan glimepirida tanpa baku dalam diperoleh kurva kalibrasi dengan persamaan garis y = 65,743 x + 2772,635 d engan nilai ko efisien ko relasi (r) 0,9998. Pad a larutan glimep irid a d engan p enambahan baku dalam diperoleh kurva kalibrasi dengan persamaan garis y = 0,0014 x + 0,0619 dan nilai koefisien korelasi (r) 0,9993. Hal ini menunjukkan untuk bahw a m eto d e y ang d ig unakan sudah memenuhi kriteria linearitas. Rentang ko nsentrasi yang d ipilih untuk uji linearitas didasarkan pada ko nsentrasi minimum glimepirida dalam darah yaitu 100 ng/ ml, dan konsentrasi maksimum glimepirida dalam darah yaitu 1000 ng/ ml.
5. U ji limit deteksi dan limit kuantitasi
dalam darah diperlukan suatu me-tode yang cukup sensitif yang dapat mengukur hingga satuan ng/ ml.
Perhitungan limit deteksi dan limit kuantitasi glimepirida dilakukan dengan menghitung perbandingan luas p uncak g limep irid a d eng an tinggi derau (noise) pada kromato-gram pelarut metanol : air (50 : 50) (S/ N). Berdasarkan pustaka (Wulan-dari, Mahi 2004), nilai LOD adalah tiga kali nilai S/ N dan LOQ adalah sepuluh kali nilai S/ N. LOD didapat-kan pada konsentrasi glimepirida di bawah 20 ng/ ml, dan LOQ didapat-kan pada konsentrasi glimepirida 50 ng/ ml.
M eto d e analisis g lim ep irid a dalam plasma secara kromatografi cair d eng an sp ektro meter massa
dapat menghasilkan limit kuantitasi 5-10 ng/ ml. Metode KCKT dengan detektor uv-vis (Yun Kyoung Song. et al. 2004) juga menghasilkan limit kuantitasi 10 ng/ ml. Limit kuantitasi yang dipero leh dari penelitian ini tidak sama (tidak lebih baik), walau-pun detektor yang digunakan sama yaitu uv-vis. Hal ini kemungkinan terjadi akibat perbedaan perangkat instrumen.
Meskipun demikian limit deteksi d an kuantitasi d ari meto d e yang d igunakan sud ah cukup sensitif, mengingat kad ar terend ah glime-pirida dalam darah ialah 100 ng/ ml, nilai ini di atas limit kuantitasi. Hasil ini jug a memp erbaiki nilai limit deteksi dan kuantitasi yang diper-oleh dari penelitian terakhir
menge-Gambar 1. Kromatogram berbagai macam larutan baku dalam (overlay) dengan fase gerak metanol-air (50:50); kecepatan alir 1,0 ml/menit; T kolom 50o C; volume
penyuntikan 20 µl; pada panjang gelombang 228 nm.
nai glimepirida dengan KCKT yang menggunakan fase gerak metanol : air (80 : 20; v/ v) dengan laju alir 0,8 ml/ menit (Wulandari, Mahi 2004). Pada tinggi puncak yang dihasilkan oleh gliklazida 1000 ng/ ml adalah 280 mm dan didapatkan nilai S/ N 93,33. Hasil ini sud ah memenuhi limit kuantitasi yang dipersyaratkan.
6. Uji akurasi dan presisi
Pada larutan glimepirida tanpa baku dalam pada konsentrasi 100 ng/ ml memberikan nilai akurasi d an presisi 99,08 ± 1,47 %, pada konsen-trasi 400 ng/ ml memberikan nilai akurasi dan presisi 101,59 ± 2,02 %, pada konsentrasi 1000 ng/ ml mem-berikan nilai akurasi dan presisi 95,54 ± 0,84 %.
Pada larutan glimepirida dengan baku dalam 1000 ng/ ml, pada kon-sentrasi 100 ng/ ml memberikan nilai akurasi dan presisi 93,51 ± 4,14 %, pada konsentrasi 400 ng/ ml mem-berikan nilai akurasi d an p resisi 107,09 ± 3,84 %, pada konsentrasi 1000 ng/ ml memberikan nilai akurasi dan presisi 100,36 ± 0,39 %. Akurasi atau kecermatan merupakan ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya, sedangkan presisi atau keterulangan merupakan keseksa-maan meto d e jika d ilakukan o leh analis yang sama dan dalam interval waktu yang pendek. Uji akurasi dan p resisi d ilakukan untuk menilai ketepatan meto de analisis dengan ketelitiannya.
Pengujian akurasi d an presisi
d ilakukan d engan menyuntikkan larutan stand ar secara berulang , minimal lima kali. Uji ini dilakukan pada tiga konsentrasi yaitu 100, 400 dan 1000 ng/ ml baik untuk larutan glimepirida tanpa baku dalam atau dengan penambahan baku dalam.
Kriteria akurasi untuk suatu metode adalah 90 -110 %, dan untuk kriteria presisi dinyatakan dengan ko efisien v ariasi atau simp angan baku relatif yaitu sebesar 2 % atau kurang. Untuk larutan glimepirida dengan baku dalam pada konsentrasi 100 dan 400 ng/ ml memberikan nilai koefisien variasi di atas 2 %, hal ini kemungkinan d isebabkan karena larutan yang tidak homogen. Tetapi p ad a ko nsentrasi lainny a sud ah memberikan nilai koefisien variasi di bawah 2 %. Dari hasil ini dapat di-katakan bahwa metode analisis yang digunakan sudah memenuhi kriteria akurasi dan presisi.
7. Uji kestabilan
Larutan glimepirida tanpa baku dalam stabil selama periode tujuh hari. Untuk larutan g lim ep irid a d engan penambahan baku d alam gliklazida stabil hingga hari keempat, pada hari kelima bentuk komatogram dari gliklazida berubah lebih lebar dan terdapat puncak-puncak tambah-an ytambah-ang sebelumnya tidak muncul.
8. A nalisis glimepirida dalam plasma in vitro
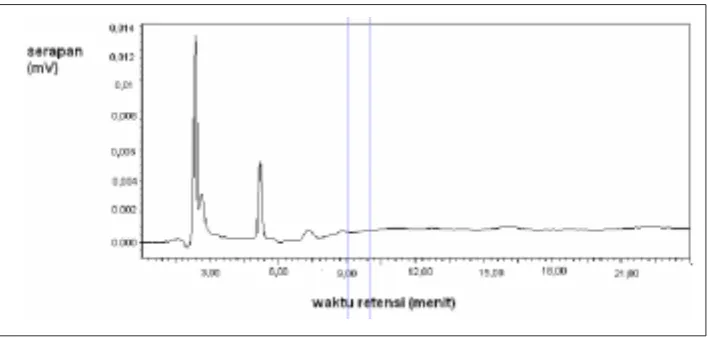
a. Uji spesifisitas
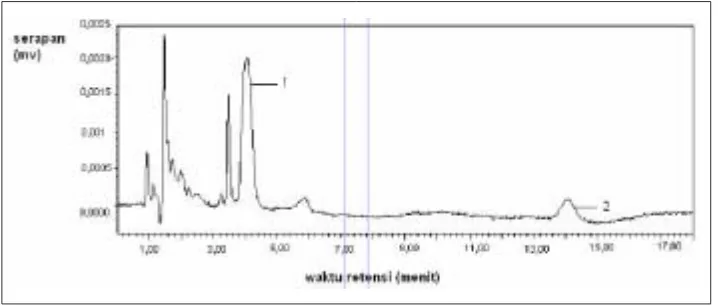
suatu meto d e analisis untuk ko mpo nen-ko mpo nen lain da-lam suatu sampel (cuplikan). Uji spesifisitas d ilakukan d engan m eny untikkan larutan d ari ekstrak blanko plasma (tanpa penambahan glimepirida) pada Gambar 2, terlihat bahwa tidak ada gangguan dari ko mpo nen end o gen plasma pad a sekitar w aktu analisis glimepirida dan baku dalam gliklazida. Kroma-to g ram ekstrak p lasma y ang mengand ung glimep irid a 400 ng/ ml dan baku dalam 1000 ng/ ml dapat dilihat pada Gambar 3. Hasil ini memperlihatkan bahwa metode analisis yang digunakan sud ah cukup sp esifik untuk analisis glimepirida.
b. Uji perolehan kembali Cara ekstraksi yang diguna-kan pada penelitian ini adalah
berdasarkan penelitian terakhir mengenai analisis glimepirida dalam plasma yang dilakukan di departemen Farmasi FMIPA UI (W uland ari, Mahi 2004) yaitu dengan pengocokan mengguna-kan shaker pada kecepatan 100 rp m selama 15 menit d engan klo ro fo rm . Deng an cara ini, pada konsentrasi glimepirida 250 ng/ ml tanpa baku dalam meng-hasilkan persentase pero lehan kembali sebesar 77,0 %. Dengan penambahan baku dalam dapat meningkatkan nilai persentase p ero lehan kem bali m enjad i 86,09%. Kriteria persentasi per-o lehan kembali menurut FDA (11) adalah 80-120 %, pada uji perolehan kembali tanpa baku dalam tidak memenuhi kriteria tersebut. Oleh karena itu dicoba meningkatkan persentase per-olehan kembali dengan
menam-Gambar 2. Kromatogram ekstrak blangko plasma dengan fase gerak metanol-air
(50:50; v/v); kecepatan alir 1,0 ml/menit; T kolom 50o C; volume penyuntikan 20 µl;
bah variasi kecep atan p engo -co kan d an lama p engo -co kan, yakni pada 125 rpm selama 25 menit. Dengan cara ini ternyata dapat meningkatkan hasil per-o lehan kem bali baik untuk larutan glimepirida tanpa dan dengan baku dalam, berturut-turut ialah 101,01 % dan 93,82 %. Selanjutnya d ilakukan uji p ero lehan kembali p ad a tig a ko nsentrasi glimepirid a yaitu 100, 400, dan 1000 ng/ ml dengan atau tanpa baku dalam, masing-masing dilakukan triplo. Pada larutan glimepirida tanpa baku dalam, dari konsentrasi 100 ng/ ml d ihasilkan nilai pero lehan kembali 94,175 ± 3,83 %, pada konsentrasi 400 ng/ ml dihasilkan nilai perolehan kembali 92,70 ± 7,9 % dan pada konsentrasi 1000 ng/ ml dihasilkan nilai perolehan
kembali 97,21 ± 9,94 %. Sedang-kan pad a larutan glimepirid a dengan baku dalam 9920 ng/ ml pada konsentrasi 100, 400, dan 1000 ng / m l d ihasilkan nilai p ero lehan kem bali berturut-turut 83,54 ± 1,96 %, 91,66 ± 2,19 %, dan 88,85 ± 3,08 %. Di sini tampak bahwa penggunaan baku dalam dapat meningkatkan akurasi dan presisi.
Kriteria keterulangan dari meto d e ekstraksi d iny atakan d engan ko efisien v ariasi d ari perolehan persentasi nilai pero-lehan kembali, koefisien variasi y ang d ip erbo lehkan ad alah kurang dari 15 %. Dari masing-masing konsentrasi baik larutan glimepirida tanpa atau dengan baku dalam menghasilkan koe-fisien variasi kurang dari 15 %. Dengan d emikian meto d e
ek-Gambar 3. Kromatogram ekstrak plasma yang mengandung glimepirida 100 ng/ml
dan baku dalam gliklazida 1020 ng/ml dengan fase gerak metanol-air (50:50; v/v); kecepatan alir 1,0 ml/menit; T kolom 50o C; volume penyuntikan 20 µl; pada panjang
gelombang 228 nm.
straksi yang digunakan sudah memenuhi kriteria untuk metode yang valid.
c. Uji linearitas
Pada ekstrak plasma yang sudah ditambahkan glimepirida pada rentang ko nsentrasi 100-1000 ng/ ml dapat dibuat kurva kalibrasi d eng an p ersam aan garis y = 64,8560 x + 3514,95 dan koefisien korelasi (r) 0,9960.
Pada ekstrak plasma yang sudah ditambahkan glimepirida dan baku dalam gliklazida pada rentang ko nsentrasi 100-1000 ng/ ml dapat dibuat kurva kali-brasi dengan persamaan garis y = 1,2134x10-3 x + 0,0656 d an ko efisien ko relasi (r) 0,9977. Untuk metode bioanalisis yang valid, kriteria linieritas dipenuhi d eng an m eng hasilkan harg a koefisien variasi r = 0,998 (Ismail et al. 2004). Sehing g a d ap at disimpulkan bahwa hanya kurva kalibrasi larutan g limep irid a dengan penambahan baku dalam y ang m em enuhi kriteria uji linieritas.
d. Uji limit deteksi dan limit kuantitasi
Pad a ko nsentrasi g lim e-pirida 100 ng/ ml dalam plasma didapat tinggi puncak sebesar 62 mm, dan memberikan nilai S/ N 20,67. Dari hasil ini d apat d i-asumsikan bahwa limit kuantitasi berada di bawah konsentrasi 100 ng/ ml. Tinggi puncak gliklazida
1000 ng/ ml dalam plasma adalah 230 mm dan memberikan nilai S/ N 76,67, hal ini sudah memenuhi kriteria limit kuantitasi yang d ip ersyaratkan. Dengan limit kuantitasi glimepirida di bawah 100 ng/ ml menunjukkan bahwa metode ini sudah cukup sensitif, dan diharapkan dapat diaplika-sikan untuk analisis glimepirida secara in vivo dalam manusia.
e. Uji akurasi dan presisi Rentang akurasi yang diper-bo lehkan untuk suatu meto de analisis dalam matriks biologis adalah 80-120 % dan untuk pre-sisi ad alah memberikan nilai ko efisien variasi sebesar 15 % atau kurang (11).
Uji akurasi dan presisi di-lakukan pada konsentrasi glime-pirida 100, 400, dan 1000 ng/ ml baik dengan penambahan baku dalam dan tanpa baku dalam.
Pad a larutan g limep irid a tanpa baku dalam pada konsen-trasi 100 ng/ ml memberikan nilai akurasi dan presisi 91,12 ± 4,60%, p ad a ko nsentrasi 400 ng / m l memberikan nilai akurasi dan presisi 87,77 ± 7,13 %, dan pada ko nsentrasi 1000 ng/ ml mem-berikan nilai akurasi dan presisi 101,82 ± 1,47 %.
nilai akurasi dan presisi 104,72 ± 1,32 %, pada ko nsentrasi 1000 ng/ ml memberikan nilai akurasi dan presisi 100,13±3,13 %.
Dari hasil di atas memper-lihatkan bahwa metode analisis yang digunakan sudah meme-nuhi kriteria akurasi dan presisi untuk suatu metode bioanalisis y ang v alid , d im ana rentang akurasi yang dihasilkan masih dalam batas 80 % hingga 120 % dan nilai koefisien variasi masih di bawah 15 % pada tiap konsen-trasi larutan uji.
9. A nalisis glimepirida dalam plasma tikus
Metode yang digunakan dalam penelitian ini dapat mengidentifikasi glimepirida tanpa adanya gangguan baik dari metabolit yang terbentuk atau dari komponen endogen plasma. Dari data-data yang didapat dari analisis g lim ep irid a baik d alam larutan standar atau dalam plasma in v itro, d ap at d iambil kesimp ulan bahw a analisis glimepirida secara kuantitatif dilakukan dengan metode penambahan baku d alam. Karena terbukti dari hasil validasi metode bahw a d engan penambahan baku dalam lebih baik dibandingan pada analisis g lim ep irid a tanp a baku d alam . Pad a analisis kuantitatif glimepirida pada plasma tikus di-gunakan metode penambahan baku dalam
Dosis yang akan diberikan ada-lah dosis 4 mg manusia. Data dosis suatu obat pada manusia tidak dapat
d ip ro y eksikan beg itu saja p ad a hewan coba hanya berdasarkan berat bad an (m g d o sis o bat/ kg berat badan). Menurut pustaka (Harmita dan Radji M. 2004) faktor konversi dari dosis manusia untuk tikus per 200 gram adalah 0,018. Selain itu ada juga hal lain yang harus diperhitung-kan dalam penentuan dosis, meng-ing at ad any a p erbed aan sp esies maka metabo lisme akan berbed a pula, hal ini diperhitungkan sebagai faktor farmakokinetika. Penentuan fakto r farmako kinetik p ad a tikus didasarkan pada jumlah enzim yang berperan pada proses metabolisme. Glimepirida secara sempurna dimeta-bo lisme p ad a fase I (reaksi o ksi-datif). Pada tikus, jumlah enzim yang berperan pada fase ini adalah lebih bany ak emp at hing g a enam kali dibandingkan pada manusia. Faktor farmakokinetika yang diambil adalah 6 (Williams, RT. 1979).
jernih (supernatan) dan dipisahkan untuk tahap analisis selanjutnya.
Mengingat ikatan protein glime-pirida dengan plasma sangat besar (hampir 100 %), cara pengendapan protein yang sering sekali digunakan untuk memisahkan obat dari kom-ponen plasma tidak dapat digunakan karena glimepirida akan ikut mengen-dap akibatnya penarikan glimepirida tid ak akan berhasil. Cara y ang digunakan pada penelitian ini adalah melalui ekstraksi cair-cair meng-gunakan larutan kloroform. Metode ini didasarkan nilai koefisien partisi (KD) antara cairan dengan fase orga-nik, nilai KD maksimum merupakan dasar pemilihan jenis larutan peng-ekstraksi. Pada penelitian sebelum-ny a (Ism ail et al. 2004) sud ah dilakukan optimasi pada pemilihan jenis larutan pengekstraksi, yaitu didapatkan bahwa kloroform memi-liki nilai KD paling besar diantara jenis larutan pengekstraksi lainnya.
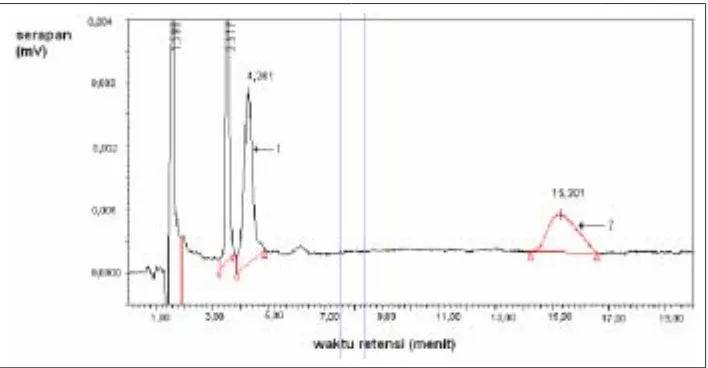
Larutan kloroform yang didapat diuapkan untuk memekatkan kon-sentrasi dari glimepirida. Penguapan dengan bantuan gas nitrogen dila-kukan untuk menghindari terjadinya d eko mpo sisi analit selama pro ses penguapan. Terlihat bahw a metode ini d apat mengid entifikasi glime-pirida yang muncul pada 15,301 menit dan gliklazida pada 4,261 menit. Pada pemberian dosis glimepirida dalam tubuh akan terbentuk metabolit, dari meto de analisis ini baik pada jam kelima atau pada jam ketujuh tidak muncul adanya metabolit pada kro-m ato g rakro-m . Dalakro-m hal ini d ap at
terjadi kemungkinan, yaitu karena metabolit tidak ikut terekstraksi oleh kloroform, atau metabolit ikut ter-ekstraksi hanya saja p ad a w aktu pelarutan dengan metanol metabolit tid ak ikut terlarut sehingga tid ak muncul pada kromatogram. Meta-bo lit suatu o bat pasti lebih po lar dibandingkan dengan obat induk-nya, karena perbedaan kepolaran ini maka terjadi perbedaan pula baik p ad a w aktu ekstraksi atau p ad a pro ses pelarutan dengan metano l. Jika tidak diperlukan untuk meng-hitung kadar metabolit glimepirida maka metode ini dapat digunakan untuk analisis glimepirid a d alam plasma, tetapi jika diinginkan untuk menghitung metabolit secara kuan-titatif, maka d ip erlukan meto d e ekstraksi yang tepat agar metabolit ikut terekstraksi dan teridentifikasi. A tau d eng an menambah w aktu pengambilan darah agar konsentrasi metabolit bertambah. Dari hasil ini dapat dihitung dari pemberian empat mg glimepirida dosis manusia, pada jam kelima kadar glimepirida dalam p lasm a (p ad a d ua tikus) ad alah 389,24 – 628,32 ng/ ml. Pad a jam ketujuh d id ap atkan kad ar glime-pirida dengan dan tanpa baku dalam sebesar 75,03 d an 95,93 %. (lihat gambar 4)
KESIM PULA N
metanol:air (50:50; v/ v), laju alir 1,0 ml/ menit, d an d id eteksi p ad a panjang gelombang 228 nm dengan detektor photo diode array, glimepirida dapat dianalisis dengan penambahan baku dalam gliklazida tanpa adanya gangguan baik dari metabolit atau komponen endogen plasma. Waktu retensi glimepirida diperoleh pada 17 menit.
2. Hasil valid asi meto d e me-nunjukkan bahw a meto de analisis yang digunakan sudah memenuhi kriteria akurasi, presisi, selektivitas dan sensitivitas.
DA FTA R PUSTA KA
A nonim,G uidance for industry bioanaly tical method validation.
2001. Center for Drug Evaluation and Research (CDER). http:/ / w w w .fda.gov/ cder/ guidance/ index.htm, 1 Mei 2005, pk. 20.00 WIB.
Harmita, Radji M. Buku A jar A nalisis H ay ati. Dep o k: Dep artem en Farmasi Fakultas Matematika d an Ilmu Pengetahuan A lam, 2004:74-78.
Ho n Yun Kim, Kyu Yo ung Chan, Chang Hun Park, M o o n Sun Jang. Determinatio n o f glime-piride in human plasma using liquid chro mato g rap hy electro -spray ionization tandem mass. spectrometry (LC-ESI/ MS/ MS).
Buletin of the Korean Chemical So-ciety, 25 No. 1. 2004.
Ho, Emmie, Yiu K, Wan T, Stew art B, Watkins K. Detection of anti
Gambar 4. Kromatogram ekstrak sampel plasma pada jam ke-5 setelah pemberian
dosis glimepirida dengan penambahan baku dalam dengan fase gerak metanol-air (50:50; v/v); kecepatan alir 1,0 ml/menit; T kolom 50o C; volume penyuntikan 20 µl;
diabetics in equine plasma and urine by liquid chromatography-tand em mass sp ectro metry. J Chromatogr B 811. 2004:65-73. Ismail, Isam, Jafer I, Tamimi J.
De-termination of glimepiride in hu-man plasma by liquid chromatog-raphy electro spray io nizatio n tand em mass spectro metry. J. Chromatogr B, 5. 2004 : 103-109. Kahn, CR (Ed ). Diso rd ers o f Fuel
Metabolism.Dalam: Becker, FL (Ed ). Princip les & p ractise o f endo cryno lo gy & metabo lism. 2nd ed. Philadelphia : J.B.
Lippin-cott Company, 1995.
Kelly, MT. Drug Analysis in Biologi-cal Fluid s. Dalam : ChemiBiologi-cal analysis in co mplex matrices. Dublin, Ireland, 1990 : 17-97. Lehr, Damn P. Simultaneous
deter-mination of the sulphonylurea glimepiride and it’s metabolites in human serum and urine by high performance liquid chroma-tography after pre-column deri-vatization. J. Chromatogr B : bio-medical sciences and application 526. 1990 : 497-505.
Rafael Elisio Barrientes Astifgarraga. The determination glimepiride in human plasma LC-MS-MS using
glibenclamid e as the internal standard. Brazil : Institute of Bio-m ed ical Sciences-USP. 2001.
Http://www.cartecius.com, tanggal 20 November 2004 pukul 15.30 WIB.
Shargel, Leon and A ndrew BC Yu. A p p lied Bio p harmaceutics & Pharmacokinetics second edition.
A ppleton & Lange, 1988 : 33-110. Williams, RT. Species Variations in
Drug Biotransformation. Dalam: La Du, BN, Mandel HG and Way EL (Eds). Fundamentals of Drug Metabolism and Drug Disposi-tion. Huntington, New York : The W illiams and W ilkins Company,
1979: 187-203.