PENGENDALIAN INFEKSI CACING HATI PADA TERNAK : KONTROL BIOLOGI
FASCIOLA GIGANTICA
DENGAN TREMATODA LAIN PADA SIPUT
LYMNAEA
RUBIGINOSA
PENDAHULUAN
Masalah fasciolosis pada ternak ruminansia
di Indonesia cenderung ticlak berubah dari
waktu ke waktu . Tingkat kejadian fasciolosis
berkisar antara
42-100 % (ANONIMOUS, 1992),dapat mengakibatkan kerugian ekonomi sebesar
Rp.
513milyar setiap tahunnya
(ANONIMOUS, 1991)sehingga perlu penanganan yang serius
mengingat pada umumnya ternak yang
terse-rang tersebar di pedesaan . Pada negara-negara
yang sudah maju walau masih ditemukan kasus
fasciolosis namun masalahnya sudah dapat
di-tangani, baik dengan cara-cara pencegahan
ter-hadap terjadinya infeksi maupun pengobatan
pada ternak. Sedang di negara-negara yang
sedang berkembang, seperti halnya Indonesia,
masih banyak kendala yang dihadapi.
Kemam-puan ekonomi peternak, sistem usaha
peter-nakan, pengetahuan tentang penyakit berkaitan
dengan sistem usaha lainnya (misalnya
perta-nian), serta program pemerintah di dalam
me-nangani penyakit clan ketersediaan/harga obat
yang masih belum memadai merupakan contoh
kendala yang memungkinkan kejadian
fasciolo-sis pads ternak tidak berubah sejak penyakit ini
ditemukan.
Pengendalian fasciolosis pada ternak dapat
dilakukan dengan berbagai macam cara,
misal-nya program pengobatan dipadukan dengan
pencegahan terhadap terjadinya penyakit
berda-sarkan data epidemiologi parasit . Pengobatan
fasciolosis pada ternak di daerah yang
mempu-nyai empat musim, pemberian obat cacing biasa
diberikan paling kurang dua kali setahun
(ANONIMOUS, 1977; FAWCETT,1990; REIDclan
ARMOUR, 1978)clan dipadukan dengan
pro-gram-program
pencegahan.
Sedang
untuk
daerah tropis program pengobatan masih
bera-gam . Seperti di Thailand misalnya, pengobatan
dilakukan setelah populasi siput L . rubiginosa di
lapangan
menonjukkan
angka
terrendah
(SRIKITJAKARN, 1986)clan dilakukan sekali lagi
pada saat populasi siput tertinggi. Di Filipina
SUHARDONO
Balai Penelitian Veteriner
Jalan R. E. Martadinata 30, P.O. Box 151, Bogor 16114
(TONGSON, 1978)
pernah membuat program
nasional untuk pengobatan fasciolosis
berclasar-kan atas periode prepaten cacing hati, yakni
3bulan, sehingga pemberian obat cacing
diberi-kan sampai empat kali setahun .
BORAY (1991)memperkirakan pemberian obat cacing hati pada
ternak di wilayah Asia Tenggara dapat
dilaku-kan dua kali setahun pada setiap akhir musim
kemarau clan penghujan. Pencegahan fasciolosis
dimaksudkan untuk menghinclarkan /
mengu-rangi kemungkinan ternak menclapatkan infeksi
atau menghindari bersatunya telur cacing
dengan siput. Pencegahan ini dapat dilakukan
misainya dengan cara memisahkan ternak dari
lahan yang cocok untuk hidupnya siput,
mem-bunuh/menurunkan populasi siput clan kontrol
biologi
(ANONIMOUS, 1977; BORAY, 1991 ; OVER, 1982; WILSONet al.,
1982; WRIGHT, 1968) .Pengendalian fasciolosis dengan cara
pengo-batan clan dipadukan dengan perbaikan
tata-lak-sana sistem usaha peternakan telah
disampai-kan oleh
SUHARDONOet al. pada Seminar
Nasional Peternakan clan Veteriner
1997di
Ciawi, Bogor. Pada kesempatan ini penulis
bermaksud menguraikan pengendalian
fasciolo-sis melalui kontrol biologi .
PENGERTIAN KONTROL BIOLOGI
Kontrol biologi merupakan cara
pengenda-lian penyakit dengan menggunakan makhluk
hidup lain dimana agen tersebut dapat berperan
sebagai predator, parasit/patogen, kompetitor
atau pengubah habitat
(STURROCK, 1995 ; WRIGHT, 1968) .Untuk fasciolosis, kontrol
biologi dapat ditargetkan pada siput yang
ber-peran sebagai incluk semang antara cacing hati
(Lymnaea spp .) atau ditujukan pada larva cacing
hati yang masih berada di dalam siput tersebut.
MURTISARIclan
EVANS (1982)melaporkan bahwa
itik yang clipelihara dengan cara digembalakan
mengkonsumsi siput sebanyak
17%dari total
pakan yang ada di dalam temboloknya . Hal
yang senada juga dilaporkan oleh BORAY (1991) bahwa sehubungan dengan banyaknya itik yang digembalakan di sawah-sawah di Indonesia, di-cluga dapat menurunkan populasi siput . Laporan dari Zambia (LOCKE, 1969) clan Inggris (HANCOCK, 1969) menduga bahwa dengan menggembalakan sejumlah angsa (geese) atau itik selama beberapa minggu di pastur sebelum sapi digembalakan clapat menghabiskan siput di tempat itu. SRI WIDJAJANTI (1990) melaporkan hasil penelitian laboratoriumnya bahwa seekor ikan mas
(Cyprinus carpio)
mampu memangsa paling seclikit 10 siputL. rubiginosa
setiap hari, seclang ikan gurami(0sphromenus gouraini)
clan ikan sepat(Trichogaster sp.)
potensinya sebagai pemangsa siput lebih rendah daripada ikan mas . Contoh-contoh di atas merupakan kontrol biologi dimana unggas clan ikan berpe-ran sebagai predator langsung dalammenurun-kan populasi siput .
Kontrol biologi dengan Cara antagonis dari dua atau lebih larvae trematoda di dalam siput sempat menclapat perhatian yang serius di Malaysia baik oleh peneliti dari dalam maupun luar negeri, seperti yang dilaporkan oleh LIE
et
al.
(1968), Kwoet al.
(1970) clan Lim clan HEYNEMAN (1972) . Konsepnya sendiri didasar-kan pads beberapa pengamatan bahwa bebera-pa spesies cacing trematoda menggunakan siput yang sama sebagai incluk semang antara (BASCH, 1966), akan tetapi jarang sekali ditemu-kan satu siput melepasditemu-kan lebih dari satu tipe serkariae (LIEet al.,
1966) . BASCHet al.
(1970) di dalam mencari penjelasan terhadap fenomena tersebut mengemukakan suatu teori bahwa larvae trematoda secara langsung atau tidak langsung berantagonis dengan larvae trematoda lainnya clan sebagai akibatnya adalah lenyapnya parasit yang lemah (subordinate) . Mereka menemukan bahwaEchinostoma audyi
(seka-rang spesies ini menurut KANEV (1994) identik dengan E.revolutum
bersifat antagonis domi-nan terhadap larva F.gigantica
(Kwoet al.,
1970; LIEet al.,
1971) . Di Indonesia sifat dominan dari larvaE. revolutum
terhadap F.gigantica
di dalam siputL . rubiginosa
juga dila-porkan oleh ESTUNINGSIH (1991) . Bentuk dewasa cacing E.revolutum
biasa ditemukan di dalam saluran pencernaan itik clan ayam buras Lebih lanjut ESTUNINGSIH melaporkan dari hasil penelitian laboratoriumnya bahwa infeksiL.
rubiginosa
denganE. revolutum
mengakibatkan sterilitas dari siput yang terinfeksi, sehingga siput tersebut menurun atau bahkan berhentiTrematoda Lain pada Siput Lymnaea Rubiginosa
memproduksi telur . Penemuan ini senada dengan pengamatan yang dilakukan oleh SLUITERS (1981) clan COMES (1982) bahwa ter-jadi gangguan fungsi reproduksi dari siput yang terinfeksi oleh larva trematoda . Beberapa gambaran ini lebih lanjut memperkuat dugaan tentang kemampuan dari E.
revolutum
sebagai agen untuk pengendalian secara biologi larva cacing F.gigantica
dalam siputL. rubiginosa.
Namun untuk memastikan dugaan ini perlu dilakukan uji di lapangan . Sehubungan dengan hal ini, maka penulis melakukan uji lapang pada tahun 1995 (SUHARDONO, 1997) . Sebelum melaksanakan uji lapang tersebut di atas, penulis telah melakukan penelitian biologi siputL. rubiginosa
clan infeksi larvae trematoda pada siput di daerah yang sama .BIOLOGI SIPUT
LYMNAEA RUBIGINOSA
DAN KEJADIAN INFEKSI OLEH TREMATODA LAIN Di Indonesia telah dilaporkan tentang dina-mika populasi siputL. rubiginosa
di beberapa habitat (SRI WIDJAJANTI, 1989; VAN BENTHEM JUTTING, 1956; SUHARDONO, 1997) . Habitat yang paling cocok untuk siput tersebut adalah sawah irigasi yang ditanami padi . Habitat ini memberikan fasilitas maksimum bagi siputL.
rubiginosa,
antara lain : air yang selalu ada, mengalir dengan lamban, dangkal, teduh dari sinar matahari clan banyak biota lain yang hidup di situasi seperti ini .Pengamatan penulis menunjukkan bahwa populasi siput, akan naik dengan cepat pada saat padi tumbuh clan bertahan tetap tinggi hingga panen padi berakhir . Pengeringan sawah sekitar seminggu sebelum padi dipanen ticlak membunuh siput. Namun populasi siput akan cepat berkurang segera setelah panen padi selesai clan lahan clibiarkan 'bero' atau ditanami palawija . Sehingga selama musim penghujan boleh clikatakan populasi siput akan tetap tinggi. Pada musim kemarau populasi siput relatif rendah clan habitat yang cocok pada musim kemarau ini antara lain : selokan/sungai yang aliran airnya sangat pelan, daerah sekitar sumber mata air clan kolam .
Dari penelitian yang dilakukan di propinsi Jawa Tengah, DIY clan Jawa Barat cliketahui bahwa angka prevalensi kejadian infeksi oleh larva F.
gigantica
pada siputL . rubiginosa
sangat rendah (0,07 %) clan oleh trematoda lain sebesar 22 % dari 9000 lebih siput yangdiperiksa (SUHARDONO
et al., 1989) .
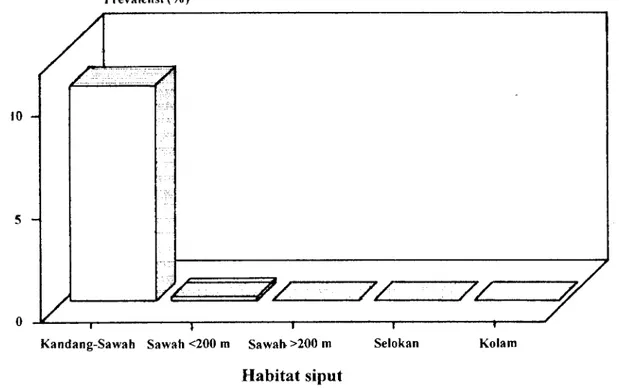
Hasil pengamatan penulis tentang kejadian infeksi oleh larva cacing trematoda pada siput tersebut menunjukkan tingkat prevalensi yang tidak sama di setiap habitat siput yang diambil contohnya. SUHARDONO(1997)
berhasil mengi-dentifikasi daerah/habitat siput L.rubiginosa
dengan tingkat infeksi oleh larva cacing trematoda yang berbeda-beda (Gambar 1) . Dari Gambar 1 tersebut terlihat bahwa kejadian infeksi tertinggi oleh F.
gigantica
pada siput ditemukan pada habitat sawah/kolam yang letaknya bersebelahan dengan kandang sapi, habitat yang jaraknya < 200 meter dari pemu-kiman tingkat kejadiannya lebih renclah clan boleh dikatakan tidak ditemukan siput terinfeksi olehF. gigantica
pada habitat yang jaraknya > 200 meter dari pemukiman . Demikian juga infeksi oleh larvae trematoda lain pada siput yang sama tingkat kejadiannya mirip dengan hal di atas .Secara umum clapat dikatakan bahwa semakin dekat dengan pemukiman penclucluk maka tingkat infeksi larva cacing trematoda pada siput semakin tinggi . Dengan
teridentifika-10
Prevalensi (%)
WARTAZOA Vol. 7 No. 1 Th. 1998
Kandang-Sawah Sawah <200 m SawA >200 m Habitat siput
sinya habitat-habitat siput dengan tingkat kejadian infeksi oleh
F. gigantica
yang berbeda satu sama lain, maka secara teoritis kontrol biologi dengan cara antagonisme antar larva trematoda dalam siput dapat diterapkan pada salah satu habitat dengan prevalensi fasciolosis tertinggi yakni sawah/kolam yang bersebelahan dengan kandang sapi . Habitat semacam itu ti-dak seclikit ditemukan di pedesaan dimana populasi ternak cukup tinggi . Diperkirakan dengan menurunkan prevalensi infeksi oleh larva cacing hati pada siput di lokasi-lokasi seperti tersebut di atas clapat menurunkan tingkat pencemaran pada hijauan, yang lebih lanjut akan menurunkan kemungkinan bagi ter-nak untuk mendapatkan infeksi . Untuk menguji dugaan ini maka dilakukan penelitian lapangan, dimana pada sekelompok kandang sapi yang letaknya 'berdekatan' dengan sawah/kolam juga dibuat kandang itik sedemikian sehingga koto-ran itik jatuh clan 'menyatu' dengan feses sapi clan akhirnya feses tersebut masuk ke dalam petak sawah tanaman padi yang sama. Uji lapang ini dilakukan pada tahun 1995 di Kecamatan Surade, Sukabumi .Selokan Kolam
Gambar 1 . Angka prevalensi infeksi larva
Fasciola gigantica
pada siputLymnaea rubiginosa
dari berbagai habitatTrematoda Lain pada Siput Lymnaea Rubiginosa UJI LAPANG KONTROL BIOLOGI
Dua puluh enam petak sawah yang ditanami padi, berumur antara 2-6 minggu, bersebelahan dengan kandang sapi dipakai untuk penelitian . Empat belas petak sebagai kontrol clan 11 petak lainnya sebagai perlakuan . Pada kelompok perlakuan dibuat kandang itik sedemikian rupa sehingga feses itik tersebut dapat masuk/bercampur dengan feses sapi di petak sawah tersebut. Sebanyak 10 ekor itik dibandangkan setiap malam selama penelitian berlangsung, sebelum percobaan dimulai telah diperiksa bahwa 70% dari itik-itik tersebut terinfeksi oleh cacing trematoda; selama perco-baan berlangsung juga telah diperiksa bahwa antara 700-1200 telur cacing trematoda pada itik ditemukan dalam feses/kandang/malam . Sedang telur cacing hati yang ada pada feses sapi sekitar 20.000 butir/kandang/malam . Sela-ma padi tumbuh hingga panen, feses yang ber-asal dari kedua jenis ternak tersebut masuk ke sawah . Telur-telur cacing trematoda tersebut akan menetas clan menemukan siput di sawah tersebut .
Tabel 1 . Tingkat prevalensi infeksi oleh larvae trematoda pada siput Lymnaea rubiginosa pada kedua kelompok
petak sawah tanaman padi
= Jumlah siput L . rubiginosa diperiksa Sumber : SUHARDONO, 1997
Selama penelitian berlangsung ada bebera-pa ekor itik yang mati/hilang, sehingga rata-rata akhir dari itik yang ada di masing-masing kelompok perlakuan tinggal 8 ekor, terrenclah 5 ekor clan tertinggi 10 ekor. Waktu sekitar padi dipanen, siput L. rubiginosa pada petak sawah diambil semua baik di kelompok kontrol maupun perlakuan . Hasil pemeriksaan siput L. rubiginosa terhadap adanya infeksi larvae cacing trematoda disajikan dalam Tabel 1 . Dari Tabel 1 tersebut terlihat bahwa tingkat infeksi oleh larva F. gigantica pada siput yang diambil dari
petak-petak perlakuan (0,18 %) 10 kali lebih renclah (P<0,00) dibandingkan pada kelompok kontrol (1,75 %) . Sebaliknya, tingkat infeksi pada siput oleh larvae trematoda lain (Echinostoma clan Furcocercous) pada kelompok perlakuan lebih tinggi (46,73%) dibanding pada kelompok kontrol (11,2 %) (P<0,01) . Terjadi penurunan (P<0,05) jumlah siput yang ticlak terinfeksi oleh larvae cacing trematoda pada kelompok perla-kuan (48,16 %) dibandingkan pada kelompok kontrol (86,86 %) .
Penjelasan dari penurunan kejadian infeksi oleh larva F. gigantica pada siput L. rubiginosa adalah sebagai berikut : Pengandangan itik yang secara alami terinfeksi oleh cacing trematoda memungkinkan masuknya feses itik clan sapi secara bersamaan ke sawah tanaman padi dimana banyak ditemukan siput di sini. Selanjut-nya terjadi kompetisi antara larva yang menetas dari telur-telur cacing trematoda yang berasal dari itik clan dari sapi didalam menggunakan siput L. rubiginosa sebagai incluk semang antara. Dari Tabel 1 di atas terlihat jelas bahwa derajad infeksi larvae trematoda lain (Echinostoma clan Furcocercous) dalam siput meningkat. Kenaikan tingkat infeksi ini dapat terjadi karena sifat dominan dari larvae cacing tersebut, namun mungkin juga clibarengi dengan kecepatan pertumbuhan larva yang lebih tinggi (khususnya larva Furcocercous) bila dibanding-kan dengan pertumbuhan larva F. gigantica. Dengan demikian, hasil penelitian laboratorium yang dilakukan oleh ESTUNINGSIH (1991) tentang antagonisme antar larvae trematoda pada siput terbukti pada penelitian ini. Namun berclasarkan jumlah populasi siput yang ada di petak sawah dimana penelitian dilakukan, pengaruh sterilisasi dari siput yang terinfeksi oleh E. revolutum (ESTUNINGSIH, 1991 ; SLUITERS et al., 1980; SLUITERS, 1981) ticlak terlihat dalam penelitian ini (P>0,05) . Hal ini erat sekali dengan sifat biologi dari siput yang mempunyai kemampuan berreproduksi sangat besar, jumlah siput yang terinfeksi oleh larvae cacing trematoda kurang dari setengahnya sedangkan sisanya bebas dari infeksi, sehingga secara keseluruhan populasi siput yang ada di petak sawah tempat peneliti-an ticlak terlihat adpeneliti-anya perbeclapeneliti-an populasi . Dengan demikian pemanfaatan parasit trema-toda pada unggas sebagai agen biologik untuk pengendalian fasciolosis hanya clitekankan pada daerah-daerah dimana terjadi derajad infeksi yang tinggi oleh larva F. gigantica pada siput L. rubiginosa, misalnya pada sawah tanaman padi Larvae Trematoda Tingkat prevalensi (%)
Kontrol Perlakuan F. gigantica 1,75 0,18 Echinostoma 11,2 46,73 Furcocercous 0,19 4,93 Negatif 86,86 48,16 10,179* 5,641*
atau kolam yang bersebelahan dengan kandang sapi/ kerbau . Kontrol biologi yang ditawarkan ini bukan untuk menurunkan populasi siput
L.
rubiginosa
melainkan menekan derajad infeksi oleh larvaF.
gigantica
pada siput tersebut.APLIKASI KONTROL BIOLOGI
Kontrol biologi terhadap fasciolosis dapat diterapkan di daerah dimana penanaman padi dilakukan baik secara intensif maupun semi intensif, ternak khususnya sapi dan kerbau ber-peran utama sebagai sumber tenaga kerja untuk mengolah sawah, dan unggas (khususnya ung-gas air) dipelihara secara ekstensif. Lingkungan seperti tersebut di atas banyak tersebar di pede-saan . Apabila unggas air (misalnya itik) tidak/ jarang dipelihara di suatu daerah yang diduga merupakan daerah endemik fasciolosis, maka itik dapat diintroduksi di daerah tersebut dengan tata laksana pemeliharaan yang dilakukan seca-ra ekstensif atau semi intensif. Sehingga intro-duksi itik tersebut berperan ganda, yaitu mem-bantu mengendalikan kasus fasciolosis pada ternak dan menambah sumber pendapatan bagi peternak .
Kontrol biologi terhadap fasciolosis ini dapat tercapai dengan mengandangkan itik seki-tar 5 - 10 ekor, yang merupakan jumlah yang dapat dipelihara oleh petani hampir tanpa mem-berikan pakan tambahan kecuali sisa-sisa dapur dan makanan yang diperoleh pada saat dilepas . Ada sedikit perubahan yang harus dilakukan dari tatalaksana sistem pengandangan itik yang sebelumnya, yakni dengan memindahkan kan-dang itik ke tempat yang bersebelahan dengan kandang sapi. Cara lainya yaitu dengan me-ngumpulkan feses itik kemudian dicampurkan dengan feses sapi yang akan dipakai sebagai pupuk tanaman padi .
KESIMPULAN
Dengan diidentifikasinya daerah-daerah sumber siput
L. rubiginosa
dengan tingkat prevalensi yang tinggi oleh larva casing hati maka kontrol biologi dengan cara antagonisme antar parasit dapat diaplikasikan di lapangan . Memahami sifat biologi dan daur hidup cacing hatiF.
gigantica
dan kejadian infeksi secara alami pada itik oleh cacing trematoda lain kemu-dian dikaitkan dengan tatalaksana baik dalam cara bercocok tanam padi maupun carabeter-WARTAZOA Vol. 7 No. 1 Th. 1998
nak sapi di daerah lahan dengan sistem irigasi intensif maka peternak sapi sebaiknya juga memelihara itik dengan menempatkan kandang bersebelahan satu sama lain sedemikian sehing-ga feses dari kedua jenis ternak tersebut mudah bercampur. Cara beternak ini akan memberikan keuntungan bahwa fasciolosis pada sapi dapat ditekan melalui penurunan pencemaran hijauan oleh metaserkaria cacing hati, disamping itu ada keuntungan tambahan dari pemeliharaan itik itu sendiri baik berupa penghasilan maupun protein .
Mekanisme kontrol biologi ini terjadi dengan oercampurnya feses sapi dan itik masuk ke sawah tanaman padi memungkinkan terjadinya kompetisi antara larva trematoda yang menetas dari telur yang ada pada feses didalam menggunakan siput
L. rubiginosa
sebagai induk semang antara . Kontrol biologi ini dapat diterapkan di daerah pedesaan dimana kedua jenis ternak ini sudah sejak lama ada di daerah seperti itu . Jumlah itik yang hanya berkisar antara 5-10 ekor untuk setiap keluarga pemilik sapi/kerbau tidak akan banyak mengganggu kerja tambahan bagi keluarga tersebut namun sebaliknya lebih memperkecil ternak dari kemungkinan mendapatkan infeksi cacing hati.DAFTAR PUSTAKA
ANONIMOUS. 1977 . Fascioliasis in Australia. Bulletin of
International Office of Epizootic87 : 675-691 .
ANONIMOUS. 1991 . Data ekonomi akibat penyakit
hewan 1990. Direktorat Kesehatan Hewan, Direktorat Jenderal Peternakan, Departemen Pertanian .
ANONIMOUS. 1992. Dwi windu P41 (Beberapa masalah
parasitosis pada hewan di Indonesia) . Buku peringatan 16 tahun P41 (13 Januari 1976 - 31 Januari 1992) . P41, Jakarta .
BASCH, P. F. 1966. The life cycle of Trichobilharzia
brevis, n.sp., an avian schistosome from Malaya . Zeitschrift fur Parasitenkunde27 : 242-251 .
BASCH, P. F., LIE, K . J. and HEYNEMAN, D. 1970.
Experimental double and triple infections of snails with larval trematodes. The Southeast Asian Journal of Tropical Medicine and Public Health 1 : 129-137 .
BORAY, J. C. 1991 . Current status of the control of
trematode infections in livestock in developing countries. Working paper for expert consultation on helminth infections of livestock in developing countries. FAO Rome pp. 1-33.
COMBES, C. 1982. Trematodes : antagonism between species and sterilizing effects on snails in biological control . Parasitology84: 151-175 . ESTUNINGSIH, S. E. 1991 . Studies on trematodes
infecting Lymnaea rubiginosa in West Java. M.Sc thesis, Tropical Veterinary Sciences and Agriculture, James Cook University, Townsville, Australia .
FAWCETT, A. R. 1990 . A study of a restricted programme of strategic dosing against Fasciola hepatica with triclabendazole . The Veterinary
Record Nov. : 492-493 .
HANCOCK, R. C. G . 1969. Controllin g liver-fluke . The Veterinary Record 84 : 228.
KANEV, I. 1994. Life-cycle, deLIMination and redescription of Echinostoma revolutum (Froelich, 1802) (Trematoda : Echinostomatidae) . Systematic Parasitology 28 : 125-144 .
Kwo, E. H ., LIE, K. J. and Ow-Yang, C. K. 1970 . Predation of sporocysts of Fasciola gigantica by rediae of Echinostoma audyi. The Southeast Asian Journal of Tropical Medicine and Public Health 1 :429 .
LIE, K. J ., BASCH, P. F. and Umathevy, T. 1966 . Studies on echinostomatidae (trematoda) in Malaya . XII. Antagonism between two species of echinostome trematodes in the same lymnaeid snail. The Journal of Parasitology 52: 454-457.
LIE, K. J., BASCH, P. F., HEYNEMANN, D., BECK, A. J. and AUDY, J . R. 1968. Implications for trematode control of interspecific larval antagonism within snail hosts. Transaction of the Royal Society of Tropical Medicine and Hygiene 62: 299-319 .
LIE, K. J., Kwo, E. H. and OW-YANG, C. K. 1971 . Further trial to control Schistosoma spindale by trematode antagonism . Southeast Asian Journal of Tropical Medicine and Public Health 2:237-243.
LIM, H. K. and HEYNEMAN, D. 1972. Intramolluscan inter-trematode antagonism : a review of factors influencing the host parasite system and its possible role in biological control . Advances in Parasitology 10:191-268.
LOCKE, R. D . 1969 . Controlling liver-fluke . The Veterinary Record Mar:260.
MURTISARI, T. and EVANS, A. J . 1982. The importance of aquatic snails in the diet of fully herded ducks. Research Report 1982, Balai Penelitian Ternak Ciawi pp.59-61 .
OVER, H. J . 1982. Ecological basis of parasite control: Trematodes with special reference to fascioliasis . Veterinary Parasitology 11 : 85-97 . REID, J. F. S. and ARMOUR, J . 1978. An economic
appraisal of helminth parasites in sheep. The Veterinary Records 102:4-7.
SLUITERS, J . F., BRUSAARD-WUST, C. M. and MEULEMAN, E. A. 1980. The relationship between miracidial dose, production of cercariae, and reproductive activity of the host in the combination Trichobilharzia ocellata and Lymnaea stagnalis. Zeitschrift for Parasitenkunde 63:13-26 .
SLUITERS, J. F. 1981 . Development of Trichobilharzia ocellata in Lymnaea stagnalis and the effect of infection on the reproductive system of the host. Zeitschrift fur Parasitenkunde64 : 303-319. SRIKITJAKARN, L. 1986. Strategic treatment of
Fasciola gigantica in the North-East of Thailand. Proceedings of the 5th International Conference on Livestock Production and Disease in the Tropics. Edited by M R Jaenudin, M Mahyuddin and J E Huhn, pp 95-96.
SRI WIDJAJANTI . 1989 . Studies on the biology of Lymnaea rubiginosa . M .Sc. Thesis, Tropical Veterinary Sciences and Agriculture, James Cook University of North Queensland, Townsville, Australia .
SRI WIDJAJANTI . 1990 . Ikan air tawar sebagai predator siput Lymnaea Rubiginosa . Seminar Parasitologi Nasional VI dan Konggres P41 V di Pandaan, Pasuruan, 23-25 Juni 1990 .
STURROCK, R. F. 1995 . Current concept on snail control. Memorias do Instituto Oswaldo Cruz Rio de Janeiro 90:241-248 .
SUHARDONO . 1997 . Epidemiology and control of fasciolosis by Fasciola gigantica in ongole cattle in West Java . Ph.D . thesis. James Cook University of North Queensland, Australia . SUHARDONO, BACHRI, S. and WAHYUNING, K.S. 1989 .
Usaha pengendalian fascioliasis secara biologis . Warta Penelitian dan Pengembangan Pertanian . 11 : 6.
TONGSON, M . S. 1978 . A national fascioliasis control program for the Philippines (A professorial lecture) . The annual convention of the Veterinary Practitioners Association of the Philippines, 22-23 June. pp. 106-117 .
VAN BENTHEM JUTTING, W. S . S. 1956 . Systemati c studies on the non-marine mollusca of the Indo-Australian archipelago . V. Critical revision of the Javanese fresh water gastropods. Treubia 23: 454-461 .
WILSON, R. A., SMITH, G.
and
THOMAS, M. R.1982.
Fascioliasis. In: The population dynamic of
infectious diseases: Theory and applications
pp262-319 (Edited by
R MAnderrson) Chapman
and Hall, London, New York.
WARTAZOA Vol. 7 No. 1 Th. 1998
WRIGHT,