BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian ini dilakukan dari bulan Juni-Nopember 2010. Tempat penelitian di Pilot Plant, Bread Unit, Laboratorium Rekayasa Proses Pangan, Laboratorium
Kimia Pangan, dan Laboratorium Evaluasi Sensori SEAFAST Center IPB serta
Laboratorium Biokimia Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian IPB.
Bahan dan Alat
Bahan utama yang digunakan dalam penelitian ini adalah jagung NK 33 yang diperoleh dari kabupaten Banyuwangi, Jawa Timur. Bahan lain yang digunakan adalah bahan untuk pembuatan cookies dan bahan kimia untuk analisis.
Bahan pembuatan cookies yaitu tepung jagung, gula halus, margarin, susu skim,
kuning telur, baking soda dan vanili. Bahan kimia untuk analisis amilosa murni, NaOH 1N, asam asetat 1N, larutan iod, HCl 0,02N, K2SO4, HgO, H2SO4 pekat,
H3BO3, methylene red, methylene blue, dan NaOH-Na2S2O3,
Alat yang digunakan yaitu seperangkat alat pembuatan tepung jagung dan tepung jagung pragelatinisasi diantaranya hummer mill, disc mill, cabinet dryer
(H.ORTH.GmbH D-6700, tipe ITHU, West Germany), pengayak 100 mesh, dan retort (Korimat tipe KA 120/1,6 Christian Wagner, Germany). Alat-alat analisis
meliputi Differential Scanning Calorimetry (DSC-60, Shimadzu, Japan),
Brabender Amilograph (Brabender® OHG Duisburg 1Amylograph, Kulturstraβe
51-55.D-4100, Germany), spektrofotometer (UV-Visible Recording Spectrophotometer, UV-160, Shimadzu, Japan), alat sentrifugasi (Hettich Zentrifugen D-7200 Tuttlingen, Hettich Universal), tabung setrifugasi, pipet mikro, tanur, oven (Thelco model 15, Precision Scietific Company, Chicago Illionis) , desikator, waterbath (GFL tipe 1008, Germany), cawan porselin,
timbangan, dan alat alat gelas. Alat-alat yang digunakan untuk pembuatan cookies
loyang, mixer, timbangan, alat cetak cookies, mangkok, piring, sendok, nampan
saji, plastik, dan lainnya.
Metode Penelitian
Penelitian dilakukan melalui tiga tahap yaitu (1) Proses pembuatan tepung jagung (2) Kajian pengaruh pengukusan bertekanan terhadap sifat fisikokimia tepung jagung (3) Aplikasi tepung jagung dalam pembuatan cookies.
Proses Pembuatan Tepung Jagung
Proses pembuatan tepung jagung mengacu pada Suarni (2009). Tahapan yang dilakukan adalah biji jagung pipilan kering disortasi kemudian biji bersih digiling menggunakan hummer mill. Biji jagung yang sudah digiling dipisahkan
lembaga, perikarp dan pangkal biji dengan cara dicuci sehingga diperoleh grits jagung. Grits jagung direndam selama 4 jam kemudian grits jagung dicuci, ditiriskan dan dikeringkan hingga kadar air sekitar 14%. Grits jagung ditepungkan
dengan mesin penepung (disc mill). Tepung yang dihasilkan kemudian
dikeringkan dengan cabinet dryer sampai kadar airnya kurang dari 10%, lalu
tepung diayak dengan ayakan 100 mesh sehingga diperoleh tepung jagung yang mempunyai ukuran partikel seragam, lolos ayakan 100 mesh. Tahapan proses pembuatan tepung jagung disajikan pada Gambar 6.
Pengamatan yang dilakukan pada tepung jagung yang dihasilkan adalah sebagai berikut:
1) Rendemen tepung jagung
2) Analisis thermal tepung jagung menggunakan DSC
3) Sifat amilografi tepung jagung menggunakan Brabender Amilograph 4) Swelling volume tepung jagung
5) Kelarutan tepung jagung
6) Kapasitas penyerapan air tepung jagung 7) Kandungan pati tepung jagung
9) Analisis proksimat: kadar air, kadar abu, kadar protein, kadar lemak, dan kadar karbohidrat
Gambar 6 Proses pembuatan tepung jagung (Suarni 2009) Jagung pipilan kering
Sortasi
Jagung grit
Perendaman dalam air selama 4 jam
Penepungan dengan disc mill
Pengayakan dengan ayakan 100 mesh
Tepung jagung
Jagung digiling dengan hummer mill
Pengeringan dengan cabinet dryer suhu
55oC sampai kadar air kurang dari 10%
Pemisahan lembaga, perikarp dan pangkal biji dengan pencucian
Pencucian dan penirisan
Pengeringan dengan cabinet dryer suhu
Kajian Pengaruh Pengukusan Bertekanan Terhadap Sifat Fisikokimia Tepung Jagung
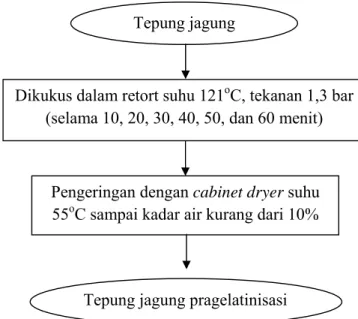
Tujuan dari proses ini adalah mendapatkan tepung jagung pragelatinisasi dengan beberapa tingkat gelatinisasi. Perlakuan yang dilakukan pada tahap ini adalah tepung jagung dikukus dengan retort suhu 121oC, tekanan 1,3 bar selama 10, 20, 30, 40, 50, dan 60 menit (Gambar 7). Penghitungan lama pengukusan bertekanan dimulai ketika tekanan telah mencapai 1,3 bar kemudian tekanan dipertahankan sesuai lama perlakuan pengukusan bertekanan.
Gambar 7 Proses pembuatan tepung jagung pragelatinisasi Pengamatan yang dilakukan pada tahap ini adalah:
1) Analisis thermal tepung jagung pragelatinisasi menggunakan DSC
2) Sifat amilografi tepung jagung pragelatinisasi menggunakan Brabender Amilograph
3) Swelling volume tepung jagung pragelatinisasi
4) Kelarutan tepung jagung pragelatinisasi
5) Kapasitas penyerapan air tepung jagung pragelatinisasi 6) Kadar air tepung setelah pengukusan bertekanan
7) Kadar amilosa dan amilopektin tepung jagung pragelatinisasi Tepung jagung
Dikukus dalam retort suhu 121oC, tekanan 1,3 bar (selama 10, 20, 30, 40, 50, dan 60 menit)
Tepung jagung pragelatinisasi Pengeringan dengan cabinet dryer suhu
Aplikasi Tepung Jagung Dalam Pembuatan Cookies
Tujuan dari tahap ini adalah mengetahui hubungan tingkat gelatinisasi dengan karakteristik berpasir cookies. Berdasarkan penelitian Suarni (2009),
substitusi tepung jagung terhadap tepung terigu dalam pembuatan cookies dapat
dilakukan di atas 50%. Hal ini sama dengan hasil penelitian Lopulalan (2008) dalam pembuatan biskuit. Pada penelitian ini dipilih penggunaan tepung jagung 100%. Tepung jagung yang digunakan adalah tepung jagung yang telah mendapat perlakuan pengukusan bertekanan selama 10, 20, 30, 40, 50 dan 60 menit. Komposisi bahan dalam pembuatan cookies mengacu pada formulasi Belinda
(2009) dengan modifikasi (Tabel 8). Modifikasi dilakukan pada jumlah margarin yang digunakan dan penggunaan 100% bahan baku tepung jagung pragelatinisasi.
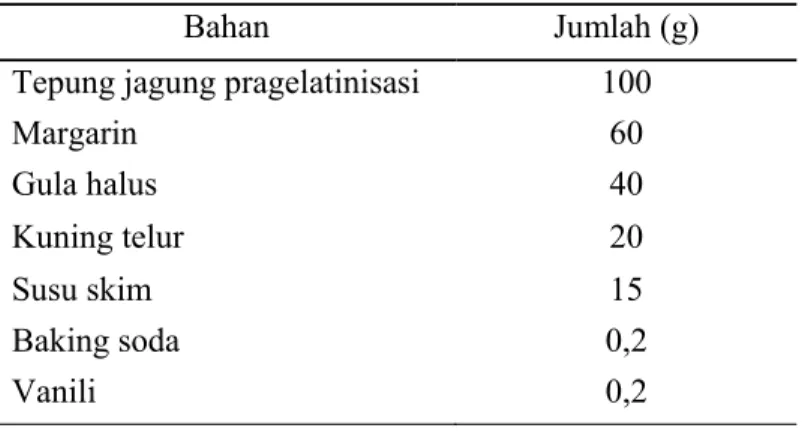
Tabel 8 Bahan-bahan pembuatan cookies per 100 g tepung
Bahan Jumlah (g)
Tepung jagung pragelatinisasi 100
Margarin 60 Gula halus 40 Kuning telur 20 Susu skim 15 Baking soda 0,2 Vanili 0,2
Tahapan proses pembuatan cookies adalah gula halus, margarin, vanili
dicampur dengan mixer dengan kecepatan tinggi selama 10 menit sehingga
diperoleh krim. Krim ditambahkan kuning telur kemudian dicampur dengan kecepatan tinggi selama 1 menit. Tepung jagung, susu skim, baking soda ditambahkan dalam campuran krim dan kuning telur kemudian dicampur dengan kecepatan rendah selama 5 menit sehingga dihasilkan adonan cookies. Adonan cookies dicetak kemudian dipanggang dalam oven pada suhu 125oC selama 25
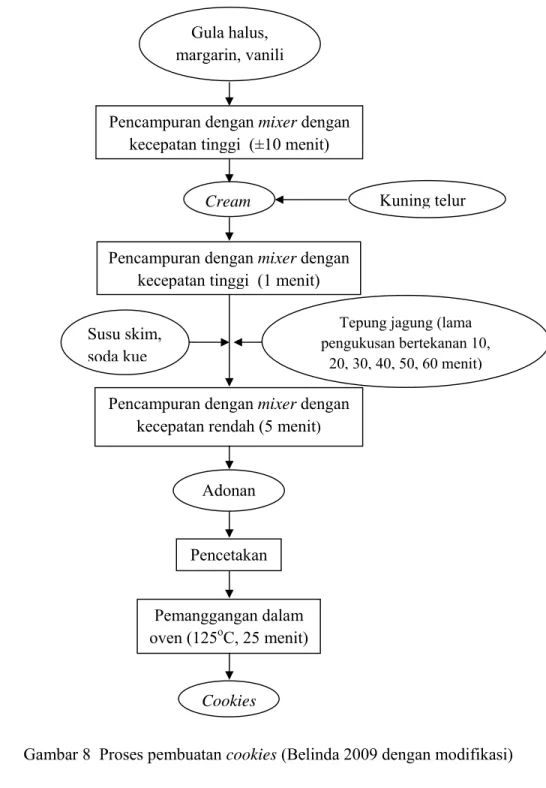
menit sehingga diperoleh cookies jagung matang. Tahapan proses pembuatan cookies disajikan pada Gambar 8. Analisis yang dilakukan pada tahap ini adalah
kepada panel semi terlatih yang berjumlah 50 orang. Uji organoleptik yang digunakan adalah uji skoring. Tahapan pengujian yang dilakukan adalah panelis diminta memberikan skor mutu dari sampel yang disajikan.
Gambar 8 Proses pembuatan cookies (Belinda 2009 dengan modifikasi)
Gula halus, margarin, vanili
Pencampuran dengan mixer dengan
kecepatan tinggi (±10 menit)
Cream Kuning telur
Pencampuran dengan mixer dengan
kecepatan rendah(5 menit)
Tepung jagung (lama pengukusan bertekanan 10,
20, 30, 40, 50, 60 menit)
Pencampuran dengan mixer dengan
kecepatan tinggi (1 menit)
Adonan Pencetakan Pemanggangan dalam oven (125oC, 25 menit) Cookies Susu skim, soda kue
Prosedur Analisis
Analisis Thermal Tepung (Yu dan Christie 2001, Wang et al. 2008)
Alat DSC yang digunakan adalah DSC-60, thermal analyzer (TA 600 WS)
dan flow control (FC-60A) merk Shimadzu, Japan (Gambar 9). DSC dikalibrasi
menggunakan indium dan pan alumunium kosong digunakan sebagai referens. 2,5
mg sampel ditimbang dalam alumunium pan kemudian ditambahkan 7,5 µL
aquades menggunakan mikrosiringe. Pan yang berisi sampel diseal secara
hermetis kemudian disimpan pada suhu ruang selama 24 jam. Kemudian pan
dipanaskan dalam alat DSC dari suhu 30-120 oC dengan kenaikan suhu yang telah di-scan 10 oC/menit. To,Tp, Tc, (T onset, T peak, T conclusion) dan ΔH
dihitung dari area peak pada thermogram. Tingkat gelatinisasi dihitung dengan
membandingkan ΔH tepung jagung pragelatinisasi dengan ΔH tepung jagung tanpa perlakuan pengukusan bertekanan.
Tingkat gelatinisasi (%) = (1 - [ΔHa/ ΔHb]) x 100%
Range suhu gelatinisai (R) = 2(Tp – To)
Keterangan:
ΔHa: ΔH tepung jagung pragelatinisasi
ΔHb: ΔH tepung jagung tanpa perlakuan pengukusan bertekanan Sifat Amilografi Tepung
Pengamatan sifat amilografi tepung dilakukan dengan menggunakan Brabender Amilograph (Brabender® OHG Duisburg 1Amylograph, Kulturstraβe
51-55.D-4100, Germany) (Gambar 9). Tahapan yang dilakukan sebagai berikut: larutan tepung jagung dibuat dengan konsentrasi 10% (b/v), sehingga setiap 400 ml aquades diperlukan tepung jagung sebanyak 40 g. Sebanyak 40 g tepung jagung dimasukkan dalam gelas piala 500 ml dan ditambah 300 ml aquades, kemudian diaduk selama 1,5 menit. Campuran tersebut dipindahkan ke dalam mangkuk amilograph yang sudah dipasang pada alat Brabender Amilograph, sisa yang tertinggal dalam gelas dicuci dengan 100 ml aquades dan air bilasan tersebut
d s s 9 s B G dimasukkan sampel dipu sampai 95oC 95oC selama suhu 1,5oC Brabender A Gambar 10. dalam ma utar dengan C dengan la a 20 menit, k per menit. Amilograph Gambar 9 D angkok ami kecepatan aju kenaikan kemudian di Perubahan pada kertas DSC-60 (kir Gambar 10 ilograph. M 75 rpm dan n suhu 1,5oC iturunkan sa viskositas grafik kont ri), Brabende Profil gelati Mangkuk am n suhunya d C per meni ampai 50oC d pasta tepun tinyu seperti er Amilograp inisasi pati milograph y ditingkatkan t. Suhu dip dengan laju ng jagung d i yang terca ph (kanan) yang berisi dari 30oC ertahankan penurunan dicatat oleh antum pada
Suhu awal gelatinisasi (SAG) = suhu pada saat kurva mulai naik
Suhu puncak gelatinisasi (SPG) = suhu pada saat viskositas maksimum dicapai (kurva mencapai puncak)
Suhu ditentukan berdasarkan perhitungan berikut = suhu awal + (waktu dalam menit x 1,5 menit)
Viskositas puncak/maksimum = pada puncak gelatinisasi dinyatakan dalam Amilograph atau Brabender Unit (BU) Viskositas pasta panas (VPP) = viskositas pasta setelah dipertahankan
selama 20 menit pada suhu 95oC
Viskositas breakdown (VB) = viskositas maksimum – viskositas pasta
panas
Viskositas pasta dingin (VPD) = viskositas pasta setelah dipertahankan selama 20 menit pada suhu 50oC
Viskositas setback (VS) = viskositas maksimum – viskositas pasta
dingin
Swelling Volume dan Kelarutan (Collado dan Corke 1999)
Prinsip pengukuran swelling volume adalah seberapa besar kemampuan
mengembang tepung jagung (ml) setelah dilakukan pemanasan pada suhu dan waktu tertentu. Satuan dari swelling volume adalah ml/g sampel.
Sampel ditimbang sebanyak 0,35 g basis kering [(0,35[(100/(100-kadar air)] di dalam tabung sentrifuse kemudian ditambahkan 12,5 ml aquades. Sampel divorteks hingga campuran merata. Selanjutnya sampel dipanaskan dalam
waterbath bersuhu 92,5oC selama 30 menit sambil sesekali diaduk. Sampel
didinginkan dalam air es selama 1 menit kemudian didiamkan selama 5 menit pada suhu ruang. Selanjutnya sampel disentrifugasi dengan kecepatan 3500 rpm selama 30 menit. Gel yang terbentuk diukur volumenya dan dinyatakan sebagai
swelling volume (ml/g bk). Kelarutan diperoleh dengan cara supernatan yang
dihasilkan dituang ke dalam cawan yang telah diketahui beratnya dan dikeringkan pada suhu 110oC selama semalam.
Kelarutan (%) = x 100%
Kapasitas Penyerapan Air(KPA) (Metode Sathe dan Salunke 1981)
Prinsip pengukuran kapasitas penyerapan air adalah seberapa besar kemampuan tepung jagung untuk menyerap air, sehingga satuannya g/g sampel (bk). Kapasitas penyerapan air ditentukan dengan cara sentrifugasi. 1 g contoh dicampur dengan 10 ml aquades kemudian diaduk selama 30 detik. Campuran yang sudah terbentuk didiamkan selama 30 menit pada suhu kamar. Selanjutnya campuran disentrifugasi dengan kecepatan 4000 rpm selama 30 menit. Kapasitas penyerapan air dihitung dengan rumus:
Absorbs air = Keterangan:
a : bobot air mula-mula b : bobot supernatant c : bobot sampel
Kadar Pati (SNI 01-2891-1992)
Sampel sebanyak 5 g ditimbang di dalam tabung erlenmeyer 500 ml. Sebanyak 200 ml larutan HCl 3% ditambahkan ke dalam erlenmeyer. Erlenmeyer dididihkan selama 3 jam dengan pendingin tegak. Larutan dalam erlenmeyer dinetralkan dengan larutan NaOH 30% (dilihat dengan lakmus atau fenolftalein) dan ditambahkan sedikit CH3COOH 3% agar suasana menjadi sedikit asam.
Larutan dipindahkan ke dalam labu ukur 500 ml dan ditepatkan hingga tanda tera kemudian disaring. Sebanyak 10 ml filtrat dipipet ke dalam erlenmeyer 500 ml dan ditambah dengan 25 ml larutan luff, batu didih dan 15 ml aquades. Erlenmeyer dipanaskan dengan nyala api tetap. Setelah mendidih selama 10 menit erlenmeyer didinginkan ke dalam bak berisi es. Setelah campuran dingin, ditambahkan 15 ml larutan KI 20% dan 25 ml H2SO4 25% secara perlahan-lahan.
Larutan dititrasi dengan larutan Na2S2O3 0,1N. Titik akhir titrasi ditentukan
dengan indikator pati 0,5%. Prosedur analisis yang sama dilakukan terhadap duplo.
Perhitungan kadar pati sampel ditentukan berdasarkan kadar glukosa yang terkuantifikasi pada titrasi sampel. Kadar glukosa dihitung berdasarkan volume dan normalitas larutan Na2S2O3 yang digunakan. Rumusnya sebagai berikut:
Na2S2O3 yang diperlukan = (Vb – Vs) x N Na2S2O3 x 10
keterangan:
Vb : Volume Na2S2O3 yang digunakan untuk titrasi blanko
Vs : Volume Na2S2O3 yang digunakan untuk titrasi sampel
Jumlah (mg) gula yang terkandung untuk ml Na2S2O3 yang digunakan
ditentukan dengan daftar Luff Schrool (Tabel 9). Dari tabel tersebut dapat diketahui hubungan antara volume Na2S2O3 0,1N yang dipergunakan dengan
jumlah glukosa yang ada pada sampel yang dititrasi. Tabel 9 Penetapan gula menurut Luff Schrool
Na2S2O3
0,1 N (ml)
Glukosa, fruktosa dan gula inversi
(mg)
Na2S2O3
0,1 N (ml)
Glukosa, fruktosa dan gula inversi
(mg) 1 2,4 13 33,0 2 4,8 14 35,7 3 7,2 15 38,5 4 9,7 16 41,3 5 12,2 17 44,2 6 14,7 18 47,1 7 17,2 19 50,0 8 19,8 20 53,0 9 22,4 21 56,0 10 25,0 22 59,1 11 27,6 23 62,2 12 30,3
Selanjutnya kadar glukosa dan pati dihitung dengan menggunakan rumus sebagai berikut:
G = 100
Keterangan:
G : kadar glukosa sampel (%)
w : glukosa yang terkandung (mg) untuk ml Na2S2O3 yang digunakan dari tabel.
w1 : bobot sampel (mg) fp : faktor pengenceran P : kadar pati (%)
Kadar Amilosa, Metode IRRI (AOAC 1995) a) Pembuatan kurva standar
Amilosa murni ditimbang sebanyak 40 mg kemudian dimasukkan ke dalam tabung reaksi bertutup, ditambahkan dengan 1 ml etanol 95% dan 9 ml NaOH 1N. Campuran dipanaskan dalam air mendidih selama 10 menit sampai terbentuk gel. Gel yang terbentuk dipindahkan ke dalam labu takar 100 ml dan ditambahkan aquades sampai tanda tera. Gel yang telah diencerkan diambil 1, 2, 3, 4, 5, 6 dan 7 ml lalu dimasukkan ke dalam labu takar 100 ml. Masing-masing labu takar tersebut ditambahkan asam asetat 1N sebanyak masing-masing 0,2; 0,4; 0,6; 0,8; 1,0; 1,2 dan 1;4 ml, lalu ditambahkan larutan iod sebanyak 2 ml. Masing-masing labu takar kemudian ditambahkan aquades sampai tanda tera, dikocok, dan didiamkan selama 20 menit. Tahap selanjutnya adalah pengukuran intensitas warna yang terbentuk dengan spektrofotometer (UV-Visible Recording Spectrophotometer, UV-160, Shimadzu, Japan) pada panjang gelombang 625 nm.
b) Penetapan sampel
Sampel sebanyak 100 mg ditimbang kemudian ditambahkan 1 ml etanol 95% dan 9 ml NaOH 1N. Selanjutnya campuran dipanaskan dalam air mendidih selama 10 menit sampai terbentuk gel. Gel yang terbentuk dipindahkan ke dalam labu takar 100 ml, kemudian ditepatkan sampai tanda tera dengan aquades dan dikocok. Gel yang telah diencerkan dipipet sebanyak 5 ml dan dimasukkan ke dalam labu takar 100 ml kemudian ditambahkan 1 ml asam asetat 1N dan 2 ml larutan iod. Larutan ditambah aquades dan ditepatkan sampai tanda tera, dikocok dan didiamkan selama 20 menit. Tahap selanjutnya adalah pengukuran intensitas warna yang terbentuk dengan spektrofotometer (UV-Visible Recording
Spectrophotometer, UV-160, Shimadzu, Japan) pada panjang gelombang 625 nm. Kurva standar dibuat sebagai hubungan antara kadar amilosa (sumbu x) dengan absorbansi (sumbu y).
Kadar amilosa (% bk) = x x 100%
Keterangan:
A : konsentrasi amilosa dari kurva standar (mg/ml) Fp : faktor pengenceran
ka : kadar air
b : berat sampel (mg) v : volume mula-mula (ml)
Rendemen
Pengukuran rendemen tepung jagung berdasarkan berat jagung pipilan kering. Rumus yang digunakan adalah:
Rendemen tepung jagung (%) = x 100%
Kadar Air, Metode Oven (AOAC 1995)
Kadar air diukur dengan metode oven biasa karena kandungan bahan volatil pada sampel rendah dan sampel tidak terdegradasi pada suhu 100oC. Cawan alumunium kosong dikeringkan dalam oven suhu 105oC selama 15 menit lalu didinginkan dalam desikator selama 5 menit atau sampai tidak panas lagi. Berat cawan ditimbang dan dicatat. Sampel ditimbang sebanyak 5 g di dalam cawan tersebut. Sampel kemudian dikeringkan dalam oven sampai beratnya konstan (perubahan berat tidak lebih dari 0.0003 g). Setelah itu cawan yang berisi sampel kering didinginkan dalam desikator. Berat akhir cawan berisi sampel kering ditimbang. Dihitung kadar air dengan persamaan sebagai berikut:
Kadar air (% bb) = x 100% Keterangan:
x : berat cawan dan sampel sebelum dikeringkan (g) y : berat cawan dan sampel setelah dikeringkan (g) A : berat cawan alumunium kosong (g)
Kadar Abu, Metode Gravimetri (AOAC 1995)
Cawan porselin dibakar dalam tanur selama 15 menit kemudian didinginkan di dalam desikator. Setelah dingin, berat cawan kosong ditimbang. Sampel sebanyak 5 g ditimbang di dalam cawan lalu diabukan di dalam tanur hingga diperoleh abu berwarna putih dan beratnya tetap. Pengabuan dilakukan dalam 2 tahap yaitu tahap pertama suhu 400oC lalu dilanjutkan pada tahap kedua dengan suhu 550oC. Cawan kemudian didinginkan di dalam desikator lalu ditimbang. Perhitungan kadar abu dilakukan sebagai berikut:
Kadar abu (% bb) = x 100% Keterangan:
W1 : berat sampel (g) W2 : berat abu (g)
Kadar Protein, Metode Mikro Kjeldahl (AOAC 1995)
Sampel sebanyak ± 0,2 g ditimbang (kira-kira membutuhkan 3-10 ml HCl 0,01N/0,02N) dan dimasukkan dalam labu Kjeldahl 30 ml. Lalu ditimbang 2 g K2SO4, 50 mg HgO, 2 ml H2SO4 pekat dan batu didih. Sampel didekstrusi
(dididihkan) selama 1-1,5 jam hingga jernih, lalu didinginkan. Lalu ditambahkan 2 ml air secara perlahan dan didinginkan kembali. Cairan hasil dekstrusi (cairan x) dipindahkan ke dalam alat destilasi dan labu kemudian dibilas dengan air. Air bilasan juga dipindahkan ke dalam alat destilasi. Erlenmeyer 125 ml berisi 5 ml H3BO3 dan 2 tetes indicator (methylene red:methylene blue = 2:1) diletakkan
diujung kondensor alat destilasi dengan ujung selang kondensor terendam dalam larutan H3BO3. Cairan x ditambahkan 10 ml NaOH-Na2S2O3 dan destilasi
dilakukan hingga larutan dalam Erlenmeyer ± 50 ml. kemudian larutan dalam Erlenmeyer dititrasi dengan HCl 0,02N. Titik akhir titrasi ditandai dengan perubahan warna larutan dari hijau menjadi abu-abu. Prosedur yang sama dilakukan juga untuk penetapan blanko. Blanko dibuat dengan tahapan yang sama dengan pembuatan sampel dengan mengganti sampel dengan air destilat. Perhitungan kadar protein dilakukan melalui persamaan sebagai berikut:
% N = , x 100%
Kadar protein (% bb) = 6,25 x %N Keterangan:
Vs : volume HCl untuk titrasi sampel (ml) Vb : volume HCl untuk titrasi blanko (ml) C : konsentrasi HCl (N)
W : berat sampel (mg)
Kadar Lemak, Metode Soxhlet (AOAC 1995)
Labu lemak yang telah bebas lemak dikeringkan di dalam oven kemudian ditimbang setelah dingin. Sampel sebanyak 5 g dibungkus dalam kertas saring kemudian ditutup kapas yang bebas lemak. Sampel dimasukkan dalam alat ekstraksi Soxhlet, kemudian kondensor dan labu dipasang di ujung-ujungnya. Pelarut heksana dimasukkan ke dalam alat lalu sampel direfluks selama 5 jam. Setelah itu pelarut didestilasi dan ditampung pada wadah lain. Labu lemak dikeringkan di dalam oven pada suhu 105oC sampai diperoleh berat tetap. Labu lemak kemudian dipindahkan ke desikator, didinginkan, dan ditimbang. Perhitungan kadar lemak dilakukan berdasarkan persamaan:
Kadar Karbohidrat (by difference) (Apriyantono et al. 1989)
Kadar karbohidrat dihitung berdasarkan analisis by difference dengan
persamaan:
Kadar karbohidrat (% bk) = 100% - (a + b + c ) Keterangan:
a : kadar abu (% bk) b : kadar protein (% bk) c : kadar lemak (% bk)
Uji Organoleptik (Rahayu 1998)
Uji organoleptik yang digunakan adalah uji skoring. Format uji terlampir dalam Lampiran 1. Skor yang digunakan 5. Lima skor mutu setara dengan skala mutu sebagai berikut:
5 sangat tidak berpasir 4 tidak berpasir 3 agak berpasir 2 berpasir
1 sangat berpasir
Rancangan Percobaan dan Analisis Data Rancangan Percobaan
Rancangan percobaan yang digunakan pada tahap kajian pengaruh pengukusan bertekanan terhadap sifat fisikokimia tepung jagung pragelatinisasi adalah rancangan acak lengkap satu faktor dengan dua kali ulangan duplo. Faktor dari tahap ini adalah lama pengukusan bertekanan yang terdiri dari 6 level yaitu 10, 20, 30, 40, 50 dan 60 menit. Menurut Mattjik dan Sumertajaya (2000), model linier rancangan acak lengkap seperti rumus di bawah ini:
Keterangan:
Yij : Nilai pengamatan respon akibat lama pengukusan level ke-i dari ulangan
ke-j
µ : Nilai rata-rata pengamatan
βi : Pengaruh lama pengukusan bertekanan level ke-i (i = 1, 2, 3, 4, 5, 6) ij : Galat percobaan
Analisis Data
Data yang dihasilkan dari tahap kajian pengaruh pengukusan bertekanan terhadap sifat fisikokimia tepung jagung pragelatinisasi dianalisis dengan menggunakan analisis ragam, apabila berbeda nyata (P<0,05) dilanjutkan dengan uji Duncan menggunakan program SPSS versi 15. Data yang dihasilkan dari uji organoleptik karakteristik berpasir (sandiness) cookies dianalisis dengan statistik
nonparametrik menggunakan uji Kruskal-Wallis H, apabila berbeda nyata (P<0,05) dilanjutkan dengan uji lanjut multiple comparisons dengan uji LSD
(Least Square Differences) menggunakan program SPSS versi 15. Analisis
korelasi (r) antara dua parameter dilakukan dengan program Microsoft Excel. Ukuran korelasi mengacu pada Hasan (2008) seperti di bawah ini:
r = 0 tidak ada korelasi
0<r≤0,20 korelasi sangat rendah/lemah sekali 0,20<r≤0,40 korelasi rendah/lemah tapi pasti 0,40<r≤0,70 korelasi cukup berarti 0,70<r≤0,90 korelasi tinggi, kuat
0,90<r≤1,0 korelasi sangat tinggi r = 1,0 korelasi sempurna