BAB II
TINJAUAN PUSTAKA
2.1 Minuman Berenergi
Minuman energi adalah minuman yang mengandung satu atau lebih bahan
yang mudah dan cepat diserap oleh tubuh untuk menghasilkan energi dengan atau
tanpa bahan tambahan makanan yang diizinkan (Standar Nasional Indonesia,
2002).
Minuman berenergi bertujuan memberi peningkatan energi melalui
kombinasi zat stimulan seperti kafein, ginseng, vitamin B kompleks, asam amino
dan gula. Asupan makanan antara lain berfungsi untuk menggantikan energi tubuh
yang hilang akibat beraktivitas.Jika energi tersebut tidak segera diganti maka
orang tersebut akan kekurangan energi sehingga tubuhnya akan menjadi lemas
dan kurang bersemangat (Tautua, dkk., 2013).
2.2 Uraian Bahan
2.2.1 Kafein
Kafein merupakan komponen utama minuman berenergi selain asam
amino, vitamin B dan suplemen herbal yang memberikan efek terhadap tubuh
yaitu dapat menstimulasi sistem saraf pusat sehingga memberi efek “alert” dan
meningkatkan denyut jantung, tekanan darah serta menyebabkan dehidrasi tubuh.
Kafein atau 1,3,7-trimetilxantin cepat dan komplit terabsorbsi setelah pemberian
oral, dengan kecepatan bioavaibilitas 100% (Louisa dan Dewoto, 2007).
Rumus struktur
:
Rumus Molekul
: C
8H
10N
4O
2Berat Molekul
: 194,19
Nama Kimia
: Coffein
Kandungan
: Tidak kurang dari 98,5% dan tidak lebih dari
101,0% C
8H
10N
4O
2, dihitung terhadap zat anhidrat.
Pemerian
: Serbuk putih atau bentuk jarum mengkilat putih;
biasanya menggumpal; tidak berbau; rasa pahit.
Larutan ini bersifat netral pada kertas lakmus.
Bentuk hidratnya mekar di udara.
Kelarutan
: Agak sukar larut dalam air, dalam etanol, mudah
larut dalam kloroform; sukar larut dalam eter.
Kafein merupakan derivat xantin, terdapat dalam kopi yang didapat dari
biji Coffea arabica, dalam satu cangkir kopi rata-rata mengandung 1 – 2% kafein,
kadar kafein dalam daun teh lebih kurang 2% dari daun Camelia sinensis, dan dari
biji Theobroma cacao kadar kafein sekitar 0,7% - 2 %. Kadar kafein yang tinggi
menyebabkan aritmia. Penggunaan kafein sebagai zat penyegar yang bila
digunakan terlampau banyak (lebih dari 20 cangkir sehari) dapat bekerja adiktif.
Minum kopi lebih dari 4 -5 cangkir sehari meningkatkan kadar homosistein dalam
darah dan dapat menimbulkan resiko penyakit jantung namun bila dihentikan
sekaligus dapat mengakibatkan sakit kepala (Louisa dan Dewoto, 2007).
jantung, gangguan lambung, tangan gemetaran, gelisah dan ingatan berkurang
serta sukar tidur, sebaiknya jangan minum lebih dari 3 cangkir kopi dalam sehari
(Tan dan Rahardja, 2007). Menurut Standar Nasional Indonesia (2002), batas
maksimum kandungan kafein dalam minuman berenergi adalah 50 mg persaji.
2.2.2 Vitamin C
Vitamin C adalah suatu zat organik yang merupakan ko-enzim atau
askorbat ko-faktor pada berbagai reaksi biokimia tubuh. Vitamin C termasuk
golongan vitamin yang larut dalam air. Dari semua jenis vitamin yang ada,
vitamin C merupakan yang paling mudah rusak dan sangat mudah teroksidasi
terutama apabila ada panas, cahaya, alkali, dan adanya enzim-enzim oksidasi.
Karena mudah dioksidasi inilah, maka vitamin C merupakan suatu zat reduktor
yang kuat (Tjokronegoro, 1985).
Menurut Ditjen POM (1995), vitamin C memiliki:
Rumus Struktur
:
Rumus molekul
: C
6H
8O
6Berat Molekul
: 176,13
Nama Kimia
: L-Asam Askorbat
Kandungan
: Tidak kurang dari 99,0% dan tidak lebih dari
100,5% C
6H
8O
6pengaruh cahaya lambat laun menjadi berwarna
gelap. Dalam keadaan kering stabil di udara,
dalam larutan cepat teroksidasi. Melebur pada
suhu lebih kurang 190
o.
Kelarutan
: Mudah larut dalam air; agak sukar larut dalam
etanol; tidak larut dalam kloroform, dalam eter
dan dalam benzena.
Fungsi dari vitamin C yaitu salah satunya adalah sebagai antiskorbut.
Kekurangan asupan vitamin C dapat menyebabkan penyakit sariawan atau
skorbut. Vitamin C juga berperan dalam pembentukan kolagen. Kolagen adalah
sejenis protein yang merupakan salah satu komponen utama dari jaringan ikat,
tulang-tulang rawan, matriks tulang dan gigi (Tjokronegoro, 1985).
Kekurangan vitamin C akan menyebabkan penyakit sariawan atau skorbut.
Gejala-gejala penyakit skorbut ialah terjadinya pelunakan ikatan kolagen, infeksi,
dan demam. Pada orang dewasa skorbut terjadi setelah beberapa bulan menderita
kekurangan vitamin C dalam makanannya. Gejala-gejalanya ialah pembengkakan
dan pendarahan pada gusi, anemia, deformasi tulang dan yang terparah adalah
adalah gigi menjadi goyah dan dapat lepas (Winarno, 1992).
Kelebihan asupan vitamin C akan diekskresikan melalui urine apabila
kadar dalam darah melebihi batas normal, tetapi apabila hal ini berjalan terus,
khususnya pada vitamin C dosis tinggi bagi seseorang yang mengalami gangguan
metabolisme urat dan atau oksalat dapat meningkatkan kemungkinan terjadinya
batu saluran kemih (Tjokronegoro, 1985).
atau yang diekskresi. Pada manusia sehat kebutuhan ini 3-4% dari persediaan
tubuh (1500 mg), yaitu berkisar 60 mg/hari (Tjokronegoro, 1985).
2.3 Spektrofotometri
Spektrofotometer adalah alat untuk mengukur transmitan atau serapan
suatu sampel sebagai fungsi panjang gelombang. Spektrofotometer merupakan
penggabungan dari dua fungsi alat yang terdiri dari spektrometer yang
menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan
fotometer sebagai alat pengukur intensitas cahaya yang ditransmisikan atau yang
diabsorpsi. Jika suatu molekul sederhana dikenakan radiasi elektromagnetik maka
molekul tesebut akan menyerap radiasi elektromagnetik. Interaksi antara molekul
dengan radiasi elektromagnetik ini akan meningkatkan energi dari tingkat dasar ke
tingkat tereksitasi (Rohman, 2007).
Teknik analisis spektrofotometri berdasarkan interaksi radiasi
elektromagnet dengan komponen atom atau molekul yang menghasilkan
fenomena bermakna sebagai parameter analisis (Satiadarma, dkk., 2004).
Bagian molekul yang bertanggung jawab terhadap penyerapan cahaya
disebut kromofor dan terdiri atas ikatan rangkap dua atau rangkap tiga, terutama
jika ikatan rangkap tersebut terkonjugasi. Semakin panjang ikatan rangkap dua
atau rangkap tiga terkonjugasi di dalam molekul, molekul tersebut akan lebih
mudah menyerap cahaya (Cairns, 2008).
Gugus fungsi seperti –OH, –O, –NH
2dan –OCH
3yang memberikan
arah yang lebih besar atau pergeseran batokromik (Rohman, 2007).
Radiasi ultraviolet diabsorpsi oleh molekul organik aromatik, molekul
yang mengandung elektron-
π terkonjugasi atau atom yang mengandung elektron
-n, menyebabkan transisi elektron di orbit terluarnya dari tingkat energi elektron
dasar ke tingkat energi tereksitasi lebih tinggi. Besarnya absorbansi radiasi
tersebut berbanding dengan banyaknya molekul analit yang mengabsorpsi dan
dapat digunakan untuk analisis kuantitatif (Satiadarma, dkk., 2004).
2.3.1 Hukum Lambert-Beer
Menurut Hukum Lambert, serapan berbanding lurus terhadap ketebalan sel
yang disinari. Sedangkan menurut Beer, serapan berbanding lurus dengan
konsentrasi. Kedua pernyataan ini dapat dijadikan satu dalam Hukum
Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus terhadap konsentrasi
dan ketebalan sel, hukum Lambert-Beer menyatakan bahwa intensitas yang
diteruskan oleh larutan zat penyerap berbanding lurus dengan tebal dan
konsentrasi larutan (Rohman, 2007).
Hukum Lambert-Beer umumnya dikenal dengan persamaan sebagai
berikut:
A = abc
Dimana: A = absorbansi
a = absorptivitas
b = tebal kuvet (cm)
c = konsentrasi
Absorptivitas tergantung pada suhu, pelarut, struktur molekul dan panjang
gelombang radiasi (Rohman, 2007).
2.3.2 Kegunaan Spektrofotometri
Kegunaan spektrofotometri ultraviolet dalam analisis kualitatif sangat
terbatas karena rentang daerah radiasi yang relatif sempit hanya dapat
mengakomodasi sedikit sekali puncak absorpsi maksimum dan minimum, karena
itu identifikasi senyawa yang tidak diketahui tidak memungkinkan untuk
dilakukan (Satiadarma, dkk., 2004). Akan tetapi, jika digabung dengan cara lain
seperti spektroskopi inframerah, resonansi magnet inti dan spektroskopi massa,
maka dapat digunakan untuk identifikasi atau analisis kualitatif senyawa tersebut
(Rohman, 2007).
Metode spektrofotometri memiliki beberapa keuntungan antara lain
kepekaan yang tinggi, ketelitian yang baik, mudah dilakukan, cepat pengerjaannya
dan dapat digunakan untuk menentukan senyawa campuran (Munson, 1984).
Pada analisis kuantitatif dengan cara penetapan kadar, larutan standar obat
yang akan dianalisis disiapkan, serapan sampel dan standar dapat ditentukan
(Cairns, 2008), dimana konsentrasi zat dalam sampel dihitung dengan rumus
sebagai berikut:
Penentuan kadar senyawa organik yang mempunyai struktur kromofor
atau mengandung gugus kromofor, serta mengabsorpsi radiasi ultraviolet
penggunaannya cukup luas (Satiadarma, dkk., 2004).
2.4 Spektrofotometri derivatif
Spektrofotometri derivatif berkaitan dengan transformasi spektrum
serapan menjadi spektrum derivatif pertama, kedua atau spektrum derivatif
dengan order yang lebih tinggi. Spektrum derivat pertama dibuat dengan
memplotkan dA / dλ dengan panjang gelombang, derivat kedua dibuat dengan
memplotkan d
2A / dλ
2dengan panjang gelombang dan seterusnya (Ditjen POM,
1995).
Konsep derivatif telah diperkenalkan pertama kali pada tahun 1950,
dimana terlihat memberikan banyak keuntungan. Aplikasi utama spektrofotometri
derivatif ultraviolet – visibel adalah untuk identifikasi kualitatif dan analisis
senyawa dalam sampel. Metode spektrofotometri derivatif sangat cocok untuk
analisis pita absorpsi yang overlapping atau tumpang tindih (Owen, 1995).
Spektrum derivatif diperoleh dengan membuat absorban dan transmitan
derivatif orde pertama atau orde lebih tinggi yang terkait dengan panjang
gelombang (ΔA / Δλ) sebagai fungsi dari panjang gelombang. Spektrum dapat
sehingga berguna jika analit adalah dua komponen yang mengabsorpsi radiasi
pada sisi pita absorpsi dari komponen yang mengganggu (Satiadarma, dkk.,
2004).
Pada spektrofotometri konvensional, spektrum serapan merupakan plot
serapan (A) terhadap panjang gelombang (λ). Pada spektrofotometri derivatif, plot
serapan terhadap panjang gelombang dimana:
A = f (λ)
, order nol
dA
/ dλ =
f’ (λ), order pertama
d
2A
/ dλ
2=
f” (λ)
, order kedua
dan seterusnya (Owen, 1995).
Menurut Talsky (1994), sesuai dengan hukum Lambert-Beer, maka ada
hubungan linier antara konsentrasi dengan absorbansi untuk semua orde pada
spektrofotometri derivatif adalah:
dA
/ dλ =
�� (1%, 1 ��)��
x bc
d
2A
/ dλ
2=
�²� ( 1%,1 ��) d�²x bc
d*A
/ dλ* =
�˟∗� ( 1%,1 ��)d�∗˟
x bc
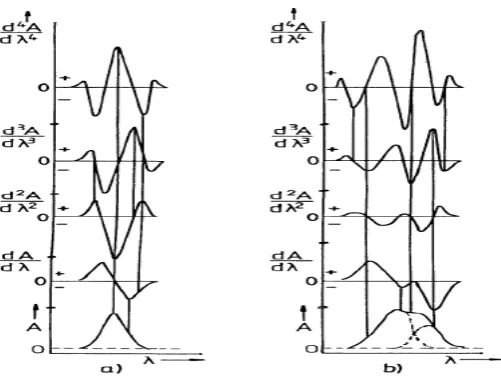
Gambar 2.1Kurva serapan derivat pertama sampai derivat keempat(Talsky, 1994).
Ada tiga aplikasi spektrofotometri derivatif yang sering digunakan dalam
analisa kuantitatif antara lain metode zero crossing, metode peak to peak dan
metode multivariate spectrophotometric calibration (Talsky, 1994).
Panjang gelombang zero crossing adalah panjang gelombang dimana
senyawa tersebut mempunyai serapan nol dan menjadi panjang gelombang
analisis untuk zat lain dalam campurannya. Metode zero crossing memisahkan
campuran dari spektrum derivatifnya pada saat panjang gelombang komponen
pertama tidak ada sinyal. Pengukuran pada zero crossing tiap komponen dalam
campuran merupakan fungsi tunggal konsentrasi dari yang lainnya (Nurhidayati,
2007).
Panjang gelombang serapan maksimum suatu senyawa pada spektrum
normal akan menjadi panjang gelombang zero crossing pada spektrum derivatif
pertama, panjang gelombang tersebut tidak mempunyai serapan atau dA / dλ = 0
(Munson, 1984).
satu, maka yang dipilih untuk dijadikan panjang gelombang analisis adalah
panjang gelombang zero crossing yang serapan pasangannya dan campurannya
persis sama, karena pada panjang gelombang tersebut dapat secara selektif
mengukur serapan senyawa pasangannya dan memiliki serapan yang paling besar.
Pada serapan yang paling besar, serapannya lebih stabil sehingga kesalahan
analisis dapat diperkecil (Nurhidayati, 2007). Kurva sederhana aplikasi zero
crossing dapat dilihat pada Gambar 2.2.
Gambar 2.2Kurva sederhana aplikasi zero crossing (Talsky, 1994).
Metode spektrofotometri derivatif dapat digunakan untuk analisis
kuantitatif zat dalam campuran dimana spektrumnya mungkin tersembunyi dalam
suatu bentuk spektrum besar yang saling tumpang tindih dengan mengabaikan
proses pemisahan zat terlebih dahulu. Spektrum dalam bentuk ini menghasilkan
profil yang lebih rinci yang tidak terlihat pada spektrum normal (Connors, 1982).
2.4.1 Komponen Spektrofotometer derivatif
Biasanya spektrofotometer telah mempunyai software untuk mengolah
data yang dapat dioperasikan melalui komputer yang telah terhubung dengan
spektrofotometer. Spektrofotometri derivatif merupakan metode manipulatif
terhadap spektra pada spektrofotometri UV-Visibel (Moffat, dkk., 2005).
2.4.2 Kegunaan spektrofotometri derivatif
Teknik spektrofotometri derivatif menawarkan beberapa keuntungan
dibandingkan dengan spektrofotometri konvensional seperti spektrum derivatif
yang diukur dapat digunakan untuk meningkatkan perbedaan antara spektrum
yang dianalisis, untuk menyelesaikan pita serapan analit yang tumpang tindih
dalam analisis kualitatif dan yang paling penting untuk mengurangi efek
interferensi dari hamburan sinar, matriks, atau senyawa menyerap lainnya dalam
analisis kuantitatif (Owen, 2000).
Spektrofotometri derivatif banyak digunakan untuk zat-zat dalam suatu
campuran yang spektrumnya saling mengganggu dan saling tumpang tindih atau
overlapping dimana zat-zat tersebut dapat larut dalam pelarut yang sama serta
memiliki serapan maksimum pada panjang gelombang yang berdekatan (Watson,
2005).
Beberapa keuntungan dari spektrofotometri derivatif antara lain yaitu
spektrum derivatif memberikan gambaran struktur yang terinci dari spektrum
serapan dan gambaran ini makin jelas dari spektrum derivatif pertama hingga ke
derivatif keempat (Munson, 1984).
derivatif relatif lebih sederhana, alat dan biaya operasionalnya lebih murah dan
waktu analisisnya lebih cepat (Nurhidayati, 2007).
2.5 Validasi Metode Analisis
Tujuan utama yang harus dicapai dari suatu kegiatan analisis kimia adalah
dihasilkannya data hasil uji yang absah (valid). Secara sederhana hasil uji yang
absah dapat digambarkan sebagai hasil uji yang mempunyai akurasi (accuracy)
dan presisi (precission) yang baik. Validasi adalah suatu tindakan penilaian
terhadap parameter tertentu pada prosedur penetapan yang dipakai untuk
membuktikan bahwa parameter tersebut memenuhi persyaratan untuk
penggunaannya (Harmita, 2004).
Validasi metode analisis dilakukan dengan uji laboratorium, dengan
demikian dapat ditunjukkan bahwa karakteristik kinerjanya telah memenuhi
persyaratan untuk diterapkan dalam analisis senyawa atau sediaan yang
bersangkutan (Satiadarma, dkk., 2004). Parameter analisis yang ditentukan pada
validasi adalah akurasi, presisi, limit deteksi, limit kuantitasi, kelinieran dan
rentang (Rohman, 2007).
2.5.1 Akurasi
Akurasi (kecermatan) adalah ukuran yang menunjukkan derajat kedekatan
hasil analisis dengan kadar analit sebenarnya. Akurasi dinyatakan sebagai persen
perolehan kembali (recovery) analit yang ditambahkan dan dapat ditentukan
melalui dua cara yaitu metode simulasi (spiked placebo recovery) dan metode
penambahan bahan baku atau standard addition method (Harmita, 2004).
(plasebo), lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan
kadar standar yang ditambahkan atau kadar sebenarnya. Jika plasebo tidak
memungkinkan untuk disiapkan, maka sejumlah analit yang telah diketahui
konsentrasinya dapat ditambahkan langsung ke dalam sediaan farmasi. Ini
dinamakan metode penambahan baku standar (Harmita, 2004).
Menurut Harmita (2004) dalam metode adisi (penambahan bahan baku),
sejumlah sampel yang dianalisis ditambah analit dengan konsentrasi biasanya
80% sampai 120% dari kadar analit yang diperkirakan, dicampur dan dianalisis
kembali. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya.
Menurut Harmita (2004), dalam kedua metode tersebut, persen perolehan
kembali dinyatakan sebagai rasio antara hasil yang diperoleh dengan hasil yang
sebenarnya:
%
Perolehan Kembali
=
CF- CACA*