BAB 3
METODOLOGI PENELITIAN
3.1 Jenis Penelitian
Penelitian ini merupakan penelitian eksperimental laboratorium.
3.2 Tempat dan Waktu Penelitian 3.2.1 Tempat penelitian
Pembuatan gel Metronidazol berbasis kitosan 0,125%, 0,25%, 0,5%, 1%, 2%, gel
Metronidazol 0,25% dalam media agar, gel kitosan tanpa Metronidazol dan uji
efektifitas antibakteri P. gingivalis, A. actinomycetemcomitans dan F. nucleatum
dilakukan di Laboratorium Mikrobiologi Oral, Universitas Airlangga, Surabaya.
3.3 Sampel dan Besar Sampel 3.3.1 Sampel penelitian
Sampel penelitian adalah biakan murni A. actinomycetemcomitans (ATCC
29522), P. gingivalis (ATCC 33277) dan F. nucleatum (ATCC 25586) dan dibiakkan
dengan media Mueller Hinton Agar (MHA).
Penentuan besar sampel dilakukan berdasarkan standar Laboratorium
Mikrobiologi Oral, Fakultas Kedokteran Gigi, Universitas Airlangga, Surabaya.
Jumlah pengulangan yang dilakukan pada penelitian ini menggunakan rumus Federer,
yaitu:
(6-1)(r-1) ≥ 15
5r-5 ≥ 15
5r ≥ 20
r ≥ 4
Jumlah perlakuan ulang (r) yang digunakan dalam penelitian ini adalah 4
kali pengulangan.
3.4.1 Variabel bebas: 3.4 Variabel Penelitian
Gel Metronidazol 0,125%, 0,25%, 0,5%, 1% dan 2% berbasis kitosan, gel
Metronidazol 0,25% dalam media agar, gel Metronidazol komersil dan gel kitosan
tanpa Metronidazol.
3.4.2 Variabel tergantung:
Diameter daya hambat dari Metronidazol berbasis kitosan terhadap bakteri
Aggregatibacter actinomycetemcomitans, Porphyromonas gingivalis dan
Fusobacterium nucleatum.
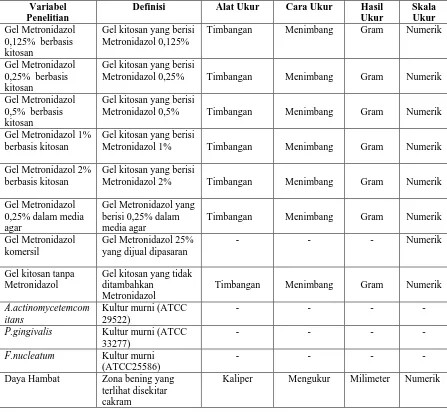
3.5 Definisi Operasional, Cara Ukur, Hasil Ukur dan Alat Ukur
Definisi operasional, cara ukur, hasil ukur, dan alat ukur dari masing-masing
variabel penelitian dapat dijelaskan pada Tabel 2.
(t-1)(r-1) ≥ 15 Keterangan:
Tabel 2. Definisi operasional variabel penelitian.
Gel kitosan yang berisi Metronidazol 0,125%
Timbangan Menimbang Gram Numerik
Gel Metronidazol 0,25% berbasis kitosan
Gel kitosan yang berisi
Metronidazol 0,25% Timbangan Menimbang Gram Numerik
Gel Metronidazol 0,5% berbasis kitosan
Gel kitosan yang berisi
Metronidazol 0,5% Timbangan Menimbang Gram Numerik
Gel Metronidazol 1% berbasis kitosan
Gel kitosan yang berisi
Metronidazol 1% Timbangan Menimbang Gram Numerik
Gel Metronidazol 2% berbasis kitosan
Gel kitosan yang berisi
Metronidazol 2% Timbangan Menimbang Gram Numerik
Gel Metronidazol
Timbangan Menimbang Gram Numerik
Gel Metronidazol
Gel kitosan yang tidak ditambahkan
Metronidazol
Timbangan Menimbang Gram Numerik
A.actinomycetemcom itans
Kultur murni (ATCC 29522)
- - - -
P.gingivalis Kultur murni (ATCC 33277)
- - - -
F.nucleatum Kultur murni (ATCC25586)
- - - -
Daya Hambat Zona bening yang terlihat disekitar cakram
Kaliper Mengukur Milimeter Numerik
3.6 Alat dan Bahan Penelitian 3.6.1 Alat penelitian
Lumpang dan stamfer, neraca analitik (Boeco), laminar airflow cabinet (Astec
labu tentukur 1000 ml (Pyrex), labu tentukur 25 ml (Pyrex), beaker glass (Pyrex),
pipet volume 1 ml (Pyrex), pipet volume 2 ml (Pyrex), gelas ukur (Pyrex), pipet tetes,
bola karet, botol, batang pengaduk, kaliper, kertas Whatmann no.1, tabung reaksi dan
rak petri dish, lampu spiritus, ose, kabin cabinet dan alat-alat laboratorium yang biasa
digunakan.
3.6.2 Bahan penelitian
1. Kitosan adalah produk laboratorium Fakultas MIPA USU
2. Metronidazol (PT Mutifa)
3. Asam laktat (Merck)
4. MHA (Mueller Hinton Agar) (Oxoid)
5. Aquabidestillata Steril (PT Ikapharmindo Putramas Pharmaceutical
Laboratories)
6. Biakan murni bakteri A.actinomycetemcomitans (ATCC29522), P. gingivalis
(33277) dan F.nucleatum (ATCC25586).
3.7 Prosedur Penelitian
3.7.1 Pembuatan gel Metronidazol 0,125%, 0,25%, 0,5%, 1% dan 2% berbasis kitosan, gel Metronidazol 0,25% dalam media agar, dan gel kitosan tanpa Metronidazol
Gel Metronidazol 0,25% berbasis kitosan dibuat dengan metode pembuatan gel
R/ Metronidazol 0,25 g
Kitosan 3 g
Asam laktat 2 g
Akuades bebas CO2 ad 100 ml
Kemudian diikuti dengan pembuatan gel Metronidazol berbasis kitosan dengan
konsentrasi 0,125%, 0,5%, 1% dan 2%, pembuatan gel Metronidazol 0,25% dalam
media agar dan pembuatan gel kitosan tanpa Metronidazol.
Semua alat yang akan digunakan telah disterilkan dalam oven pada suhu 170°C
selama 1 jam. Pembuatan gel Metronidazol secara aseptik dilakukan di dalam lemari
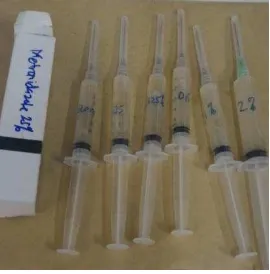
laminar air flow. Masing-masing bahan ditimbang. Kitosan sebanyak 3 g
ditambahkan larutan Asam laktat dan ditambahkan bubuk Metronidazol sebanyak
0,125 g, 0,25 g, 0,5 g, 1 g dan 2 g kemudian diaduk di dalam beaker glass sampai
berbentuk gel dan homogen, kemudian dimasukkan kedalam spuit steril (Gambar 10).
3.7.2 Uji sensitivitas bakteri
3.7.2.1 Sterilisasi alat dan bahan.
3.7.2.2
Alat-alat yang digunakan dalam uji aktivitas
antibakteri ini, disterilkan terlebih dahulu sebelum dipakai. Alat-alat dan media
disterilkan di autoklaf pada suhu 121°C selama 15 menit.
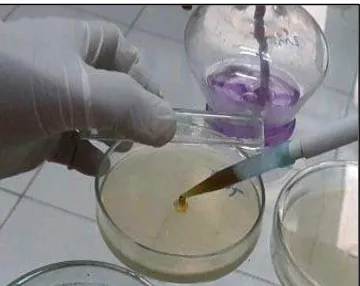
Pembuatan media. Sebelum spesimen dibiakkan, dibuat media Mueller Hinton Agar, sebanyak 12 gram bubuk dilarutkan ke dalam 240 ml aquadest untuk 40
petri (20 ml/Petri), lalu dipanaskan di atas tungku pemanas magnetik sampai
Gambar 8. Bubuk Metronidazol Gambar 9. Gel Metronidazol 0,25%
berbasis kitosan
mendidih (Gambar 11). Kemudian media yang telah masak, disterilkan di dalam
autoklaf selama 15 menit dengan tekanan udara 2 atm suhu 121°C. Setelah
disterilkan, media disimpan dalam lemari pendingin. Jika akan digunakan kembali,
media dipanaskan kembali hingga mendidih lalu dituangkan ke dalam masing-masing
petri dan dibiarkan hingga dingin.
Gambar 11. a. Bahan pembuat Media Muller Hinton Agar (MHA)
b. Media Muller Hinton Agar (MHA) Plate
3.7.2.3 Pembiakan spesimen. Kegiatan pembiakan spesimen dilakukan dalam
suasana anaerob pada inkubator CO2. A actinomycetemcomitans, P gingivalis dan F
nucleatum yang digunakan adalah spesimen stem-cell masing-masing bakteri yang
telah dibiakkan secara murni pada media MHA yang telah disiapkan pada prosedur
sebelumnya dalam suasana anaerob (Gambar 12). Sebanyak 1-2 ose dari biakan
murni bakteri uji yang telah dikultur dan tumbuh dengan subur disuspensikan dengan
menggunakan larutan NaCl 0,9 % sampai diperoleh kekeruhan sesuai standard 0,5 Mc
Farland atau sebanding dengan jumlah bakteri 1 x 106 CFU/ml. BHI (Brain Heart
Infusion) Broth steril diambil di dalam kulkas dan dikeluarkan dan dibiarkan di dalam a
ruangan. Hidupkan bunsen lalu panaskan ose sampai membara agar ose dapat steril.
Setelah itu A actinomycetemcomitans, P gingivalis dan F nucleatum diambil dari BHI
(Brain Heart Infusion) Broth dan pada saat dibuka harus didekat dengan bunsen agar
bakteri A actinomycetemcomitans, P gingivalis dan F nucleatum tidak terkontaminasi
(Gambar 13). Setelah itu diinkubator dalam suhu 37o
C selama 24 jam (Gambar 14).
Gambar 12. Kultur murni Bakteri
Gambar 14. Bakteri diinkubasi selama 24 jam
Gambar 13. a. Pengambilan bakteri dengan menggunakan ose
b. Pengkulturan bakteri kedalam BHI
a
3.7.2.4 Penentuan daya hambat menggunakan metode difusi cakram. Bakteri
yang telah diencerkan dengan mencampur 1 ose suspensi bakteri ke dalam tabung
raksi yang telah berisi larutan NaCL dan telah di standarisasi sesuai konsentrasi 0,5
Mc Farland, bakteri tersebut dioleskan kedalam Mueller Hinton Agar (MHA),
penanaman dilakukan dengan metode swaping (pemerataan bakteri dengan swab)
(Gambar 15). Petri disk dibagi beberapa bagian sesuai konsentrasi yang diuji yaitu
0,125%, 0,25%, 0,5%, 1% dan 2% serta kontrol, kemudian tetesi kertas cakram steril
dengan diameter +6 mm dengan masing-masing bahan uji sebanyak 10 µl (Gambar
17). Setiap tindakan tersebut diulangi sebanyak 4 kali dan kemudian diinkubasikan ke
dalam inkubator pada suhu 37
o
C secara anaerob selama 48 jam (Gambar 18), amati
dan ukur diameter zona terang (clear zone) yang berbentuk di sekitar cakram dengan
menggunakan penggaris dan jangka sorong.
Gambar 15. Inokulasi bakteri ke media Mueller Hinton Agar (MHA)
dengan metode swaping
Gambar 17. Penempatan bahan uji diatas kertas cakram
3.8Alur Penelitian
- Gel Metronidazol
0,125% berbasis kitosan. - Gel Metronidazol 0,25% berbasis kitosan.
- Gel Metronidazol 0,5% berbasis kitosan.
- Gel Metronidazol 1% berbasis kitosan.
- Gel Metronidazol 2% berbasis kitosan.
- Gel Metronidazol 0,25% dalam media agar.
- Gel Metronidazol
komersil.
- Gel kitosan tanpa
Metronidazol .
Media bakteri P.gingivalis ditetesi:
- Gel Metronidazol
0,125% berbasis kitosan. - Gel Metronidazol 0,25% berbasis kitosan.
- Gel Metronidazol 0,5% berbasis kitosan.
- Gel Metronidazol 1% berbasis kitosan.
- Gel Metronidazol 2% berbasis kitosan.
- Gel Metronidazol 0,25% dalam media agar.
- Gel Metronidazol
komersil.
- Gel kitosan tanpa
Metronidazol.
Media bakteri
F.nucleatum ditetesi:
- Gel Metronidazol
0,125% berbasis kitosan. - Gel Metronidazol 0,25% berbasis kitosan.
- Gel Metronidazol 0,5% berbasis kitosan.
- Gel Metronidazol 1% berbasis kitosan.
- Gel Metronidazol 2% berbasis kitosan.
- Gel Metronidazol 0,25% dalam media agar.
- Gel Metronidazol
komersil.
- Gel kitosan tanpa
Metronidazol. Pembuatan gel Metronidazol 0,125%, 0,25%,
0,5%, 1% dan 2% berbasis kitosan, gel Metronidazol 0,25% dalam media agar dan gel
kitosan tanpa Metronidazol
Pembuatan Media Bakteri Mueller
Hinton Agar (MHA)
3.9Analisis Data
Pengolahan data pada penelitian ini akan dilakukan dengan menggunakan sistem
komputerisasi yang ditampilkan dalam bentuk tabel. Analisis data pada penelitian ini
dilakukan setelah pengujian efektifitas gel Metronidazol 0,125%, 0,25%, 0,5%, 1%
dan 2% berbasis kitosan, gel Metronidazol 0,25% dalam media agar, gel
Metronidazol komersil, gel kitosan tanpa Metronidazoldi Laboratorium Mikrobiologi
Oral FKG UNAIR. Uji normalitas menggunakan Shapiro-Wilk untuk melihat
distribusi data kelompok dan dilakukan uji Mann-Whitney untuk melihat perbedaan
efektifitas masing-masing konsentrasi gel Metronidazol 0,125%, 0,25%, 0,5%, 1%
dan 2% berbasis kitosan, gel Metronidazol 0,25% dalam media agar, gel
Metronidazol komersil dan gel kitosan tanpa Metronidazol terhadap pertumbuhan
BAB 4
HASIL PENELITIAN
Pada penelitian ini, dilakukan uji daya hambat gel Metronidazol 0,125%,
0,25%, 0,5%, 1% dan 2% berbasis kitosan sebagai kelompok uji serta gel
Metronidazol 0,25% dalam media agar, gel Metronidazol komersil dan gel kitosan
tanpa Metronidazol sebagai kontrol terhadap bakteri A.actinomycetemcomitans, P.
gingivalis dan F. nucleatum. Masing-masing gel tersebut diteteskan kedalam media Mueller Hinton Agar yang berisi bakteri A.actinomycetemcomitans, P.gingivalis dan F.nucleatum, kemudian diinkubasi selama 1, 2 dan 3 hari, perlakuan tersebut
dilakukan sebanyak 4 kali. Efektifitas gel Metronidazol dievaluasi melalui diameter
daya hambat yang berupa zona bening pada media Mueller Hinton Agar yang diukur
menggunakan Kaliper.
4.1. Diameter Daya Hambat Gel Metronidazol 0,125%, 0,25%, 0,5%, 1% dan 2% Berbasis Kitosan, Gel Metronidazol 0,25% Dalam Media Agar, gel Metronidazol Komersil dan Gel Kitosan Tanpa Metronidazol Pada Bakteri A.actinomycetemcomitans, P.gingivalis, F.nucleatum
Diameter zona bening yang terbentuk pada media Mueller Hinton Agar
menunjukkan adanya daya hambat aktivitas antibakteri gel Metronidazol 0,125%,
0,25%, 0,5%, 1% , 2% berbasis kitosan, gel Metronidazol 0,25% dalam media agar
P.gingivalis dan F.nucleatum. Diameter daya hambat diukur dengan menggunakan
kaliper. Gambaran dari zona bening ini berbentuk lingkaran yang menunjukan tidak
adanya pertumbuhan bakteri di daerah sekitar obat. Semakin luas diameter zona
bening maka semakin besar daya hambat antibakteri gel tersebut terhadap bakteri
(Gambar 19, 20, 21).
Gambar 19. Daya hambat masing-masing gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri A.actinomycetemcomitans.
Gambar 21. Daya hambat masing-masing gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri F.nucleatum
Dari gambar 19, 20 dan 21 menunjukkan bahwa gel Metronidazol 0,125%,
0,25%, 0,5%, 1% , 2% berbasis kitosan, gel Metronidazol 0,25% dalam agar dan gel
Metronidazol komersil membentuk suatu zona bening di sekitaran kertas cakram pada
media Mueller Hinton Agar sehingga terlihat bahwa bahan-bahan tersebut efektif
dalam menghambat pertumbuhan bakteri A.actinomycetemcomitans, P.gingivalis dan
F.nucleatum (Tabel 3, 4, 5). Gel kitosan tanpa Metronidazol tidak membentuk zona
bening di sekitaran kertas cakram pada media Mueller Hinton Agar sehingga bahan
tersebut tidak efektif dalam menghambat pertumbuhan bakteri
A.actinomycetemcomitans, P.gingivalis dan F.nucleatum, oleh sebab itu tidak
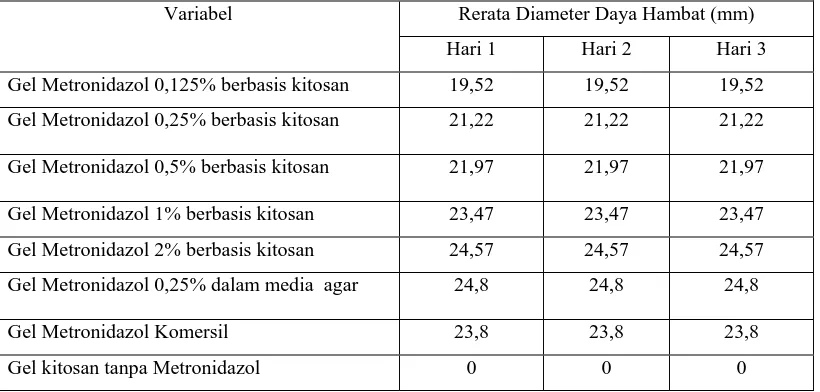
Tabel 3. Rerata diameter daya hambat masing-masing gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri A.actinomycetemcomitans pada hari 1, 2 dan 3
Variabel Rerata Diameter Daya Hambat (mm)
Hari 1 Hari 2 Hari 3
Gel Metronidazol 0,125% berbasis kitosan 19,52 19,52 19,52
Gel Metronidazol 0,25% berbasis kitosan 21,22 21,22 21,22
Gel Metronidazol 0,5% berbasis kitosan 21,97 21,97 21,97
Gel Metronidazol 1% berbasis kitosan 23,47 23,47 23,47
Gel Metronidazol 2% berbasis kitosan 24,57 24,57 24,57
Gel Metronidazol 0,25% dalam media agar 24,8 24,8 24,8
Gel Metronidazol Komersil 23,8 23,8 23,8
Gel kitosan tanpa Metronidazol 0 0 0
Tabel 4. Rerata diameter daya hambat masing-masing gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri P. gingivalis pada hari 1, 2 dan 3
Variabel Rerata Diameter Daya Hambat (mm)
Hari 1 Hari 2 Hari 3
Gel Metronidazol 0,125% berbasis kitosan 18,52 18,52 18,52
Gel Metronidazol 0,25% berbasis kitosan 20,95 20,95 20,95
Gel Metronidazol 0,5% berbasis kitosan 22,17 22,17 22,17
Gel Metronidazol 1% berbasis kitosan 23,45 23,45 23,45
Gel Metronidazol 2% berbasis kitosan 24,55 24,55 24,55
Gel Metronidazol 0,25% dalam media agar 24,8 24,8 24,8
Gel Metronidazol Komersil 23,87 23,87 23,87
Tabel 5. Rerata diameter daya hambat masing-masing gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri F. nucleatum pada hari 1, 2 dan 3
Variabel Rerata Diameter Daya Hambat (mm)
Hari 1 Hari 2 Hari 3
Gel Metronidazol 0,125% berbasis kitosan 18,02 18,02 18,02
Gel Metronidazol 0,25% berbasis kitosan 20,07 20,07 20,07
Gel Metronidazol 0,5% berbasis kitosan 21,72 21,72 21,72
Gel Metronidazol 1% berbasis kitosan 22,9 22,9 22,9
Gel Metronidazol 2% berbasis kitosan 23,95 23,95 23,95
Gel Metronidazol 0,25% dalam media agar 24,82 24,82 24,82
Gel Metronidazol Komersil 23,15 23,15 23,15
Gel kitosan tanpa Metronidazol 0 0 0
Dari tabel 3, 4 dan 5 diatas menunjukkan bahwa tidak ada perbedaan diameter
daya hambat masing-masing gel Metronidazol dan gel kitosan tanpa Metronidazol
pada bakteri A.actinomycetemcomitans, P.gingivalis dan F.nucleatum pada hari 1, 2
dan 3.
4.2 Perbandingan Diameter Daya Hambat Masing-Masing Gel Metronidazol 0,125%, 0,25%, 0,5%, 1% dan 2% Berbasis Kitosan, Gel Metronidazol 0,25% Dalam Agar, Gel Metronidazol Komersil dan Gel Kitosan Tanpa Metronidazol Pada A.actinomycetemcomitans, P.gingivalis, F.nucleatum
Dilakukan Uji Kruskal-Wallis untuk melihat perbandingan daya hambat
masing-masing konsentrasi gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap
Tabel 6. Hasil analisis uji Kruskal-Wallis perbandingan daya hambat masing-masing konsentrasi gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri A.actinomycetemcomitans
Variabel Perlakuan Median
± Interquartile range
Nilai p 0,5% berbasis kitosan
22,3 22,0 21,9 21,7 21,95 ± 0,48
Dari tabel 6 terlihat diameter daya hambat terbesar terhadap bakteri
A.actinomycetemcomitans ada pada gel Metronidazol 0,25% dalam media agar,
sedangkan yang terkecil ada pada gel Metronidazol 0,125% berbasis kitosan. Daya
hambat yang terbentuk oleh seluruh konsentrasi gel Metronidazol memiliki perbedaan
Tabel 7. Hasil analisis Uji Kruskal-Wallis perbandingan daya hambat masing-masing konsentrasi gel Metronidazol dan gel kitosan tanpa Metronidazol pada bakteri P. gingivalis
Variabel Perlakuan Median
± Interquartile range
Nilai p 0,5% berbasis kitosan
22,5 22,1 21,3 21,8 22,17 ± 0,57
Dari tabel 7 terlihat diameter daya hambat terbesar terhadap bakteri P.gingivalis
ada pada gel Metronidazol 0,25% dalam media agar, sedangkan yang terkecil ada
pada gel Metronidazol 0,125% berbasis kitosan. Daya hambat yang terbentuk oleh
Tabel 8. Hasil analisis Uji Kruskal-Wallis perbandingan daya hambat masing-masing konsentrasi gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri F. nucleatum
Variabel Perlakuan Median
± Interquartile range
Nilai p
Dari tabel 8 terlihat diameter daya hambat terbesar terhadap bakteri F.nucleatum
ada pada gel Metronidazol 0,25% dalam media agar, sedangkan yang terkecil ada
pada gel Metronidazol 0,125% berbasis kitosan. Daya hambat yang terbentuk oleh
seluruh konsentrasi gel Metronidazol memiliki perbedaan signifikan (p = 0,000).
Data yang diperoleh dilakukan uji normalitas dengan menggunakan Uji
Shapiro-Wilk. Hasilnya menunjukkan distribusi data tidak normal (p<0,05), sehingga
konsentrasi gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri
A.actinomycetemcomitans, P.gingivalis dan F.nucleatum (Tabel 9, 10, 11).
Tabel 9. Hasil analisis Uji Mann-Whitney perbandingan daya hambat masing-masing konsentrasi gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri A.actinomycetemcomitans
Gel Metronidazol 0,25% berbasis kitosan
(*) Tidak signifikan p>0,05
Dari tabel 9 terlihat adanya perbedaan daya hambat yang signifikan antara
terhadap bakteri A. actinomycetemcomitans, P. gingivalis dan F. nucleatum. Namun
tidak ada perbedaan daya hambat yang signifikan antara Metronidazol 1% berbasis
kitosan dengan gel Metronidazol komersil.
Tabel 10. Hasil analisis Uji Mann-Whitney perbandingan daya hambat masing-masing konsentrasi gel Metronidazol dan gel kitosan tanpa Metronidazol terhadap bakteri P.gingivalis
Variabel 0,25% berbasis kitosan
0,021 0,021 0,021 0,021 0,021 0,014
Dari tabel 10 terlihat adanya perbedaan daya hambat yang signifikan antara
masing-masing konsentrasi gel Metronidazol dan gel kitosan tanpa Metronidazol
terhadap bakteri A. actinomycetemcomitans, P. gingivalis dan F. nucleatum. Namun
tidak ada perbedaan daya hambat yang signifikan antara Metronidazol 1% berbasis
kitosan dengan gel Metronidazol komersil dan antara gel Metronidazol 2% berbasis
kitosan dengan gel Metronidazol komersil.
Gel kitosan tanpa Metronidazol
Uji Mann-Whitney
(*) Tidak signifikan p>0,05
Dari tabel 11 terlihat adanya perbedaan daya hambat yang signifikan antara
masing-masing konsentrasi gel Metronidazol dan gel kitosan tanpa Metronidazol
terhadap bakteri A. actinomycetemcomitans, P. gingivalis dan F. nucleatum. Namun
tidak ada perbedaan daya hambat yang signifikan antara Metronidazol 1% berbasis
BAB 5 PEMBAHASAN
Penelitian ini bertujuan untuk mengetahui dan menganalisis efektifitas gel
Metronidazol berbasis kitosan dalam menghambat pertumbuhan bakteri
A.actinomycetemcomitans, P.gingivalis dan F.nucleatum yang merupakan bakteri
patogen periodontal. Penelitian ini adalah penelitian eksperimental laboratorium.
Peracikan Metronidazol 0,125 %, 0,25%, 0,5%, 1% dan 2% berbasis kitosan dan gel
kitosan tanpa Metronidazol serta uji aktivitas antibakteri terhadap bakteri
A.actinomycetemcomitans, P.gingivalis
Pada penelitian ini dilakukan uji efektifitas Metronidazol berbasis kitosan dan gel
kitosan tanpa Metronidazol pada bakteri
dan F.nucleatum dilakukan di Laboratorium
Mikrobiologi Oral, Universitas Airlangga, Surabaya. Sampel bakteri di dapat dari
biakan murni A.actinomycetemcomitans (ATCC29522), P. gingivalis (33277) dan
F.nucleatum (ATCC25586) yang dikembangbiakan dalam media Mueller Hinton Agar kemudian dilanjutkan dengan pemberian kertas cakram diatas media dan
masing-masing kertas cakram ditetesi bahan uji, hal ini dilakukan pengulangan
sebanyak empat kali untuk mengurangi kesalahan penelitian. Selanjutnya
masing-masing media diinkubasi pada hari 1, 2 dan 3 dalam inkubator anaerob dan diukur
daya hambatnya dengan menggunakan kaliper.
A.actinomycetemcomitans, P.gingivalis dan F. nucleatum, karena pada 25 tahun terakhir ini telah ada lebih dari 100 penelitian
Hasil-hasil penelitian tersebut menunjukkan bahwa bakteri anaerob seperti
A.actinomycetemcomitans lebih mendominasi di dalam plak dan erat hubungannya
dengan terjadinya periodontitis. P.gingivalis adalah salah satu bakteri patogen
periodontal utama yang memiliki kemampuan untuk melekat dan menginvasi epitel
rongga mulut. Bakteri ini juga merupakan patogen periodontal yang sangat penting
sehingga sering dijadikan topik penelitian yang bertujuan untuk pengembangan
vaksin yang dapat menghasilkan sistem imun sehingga penyakit periodontal kronis
dapat dicegah.1,3 F. nucleatum berperan sebagai microbial bridge antara koloni awal
dan koloni akhir karena dapat melakukan koagregrasi dengan berbagai bakteri plak.
Selain itu Fusobacterium nucleatum juga merupakan inisiator organisme yang
penting karena dapat menciptakan perubahan psycho-chemical pada sulkus gingiva
yang membantu patogen lain untuk berkembang dan proliferasi.
Penelitian ini menggunakan basis kitosan dengan konsentrasi 3% dan asam laktat
2%, karena sesuai dengan
3
penelitian Popa L dkk 2013 menyatakan bahwa semakin
tinggi konsentrasi kitosan akan mengurangi kemampuan pelepasan obat. Basis
kitosan 3% dapat berperan sebagai penghantar obat dengan modulasi yang paling
optimal.18 Penelitian yang dilakukan oleh Yellanki dkk dengan menggunakan
Metronidazol 0,25% yang dicampur dengan asam laktat 2% dan kitosan 3% hasilnya
menunjukkan konsentrasi obat lebih tinggi, bioadhesive lebih baik dan pelepasan obat
lebih terkontrol. Gel Metronidazol yang dipersiapkan menggunakan polimer alami
kitosan dapat digunakan untuk perawatan penyakit periodontal dan juga dapat
mengurangi frekuensi dosis, meningkatkan bioavabilitas dari Metronidazol yang bisa
Bahan yang digunakan pada penelitian ini adalah gel Metronidazol 0,125 %,
0,25%, 0,5%, 1% dan 2% berbasis kitosan, Metronidazol 0,25% dalam media agar,
gel Metronidazol komersil dan gel kitosan tanpa Metronidazol. Kitosan merupakan
biopolimer hidrofilik diperoleh dari diasetilisasi kitin dalam keadaan basa, komponen
utamanya berasal dari kerang arthropoda, telah diakui dapat berperan baik sebagai
bioadhesive dan permeabilizer. Kitosan memiliki sifat yang menguntungkan seperti
non toksisitas, biokompatibilitas dan biodegradasi. Kitosan itu sendiri memiliki
aktivitas antimikroba, penyembuhan luka, hemostatik, dan sifat regenerasi jaringan,
sehingga menimbulkan ketertarikan yang besar di bidang kedokteran gigi.51 Kitosan
dapat dilarutkan dalam asam organik seperti asam laktat dan asam asetat sebelum
dibentuk menjadi film. Kitosan memiliki kemampuan untuk membentuk film, hal
tersebut memungkinkan penggunaan yang luas dalam aplikasi pada bidang kesehatan
seperti pada sistem pengantar obat.41
Kitosan hidrogel telah dikembangkan untuk pelepasan obat secara lokal di rongga
mulut. Selain untuk pelepasan obat, kitosan hidrogel dan lapisannya mampu
membatasi perlekatan patogen umum seperti Candida albicans ke sel manusia.
Sistem pelepasan obat secara lokal juga mampu mempertahankan pelepasan obat
(chlorhexidine gluconate). Kitosan hidrogel juga mampu memberikan zat ipriflavone
, obat lipofilik yang meningkatkan kepadatan tulang, yang berada didalam jaringan
periodontal.
Penelitian George dan Abraham pada tahun
2006 mengenai sifat toksik kitosan menyatakan bahwa kitosan merupakan polimer
hidrofilik yang tidak bersifat toksik dan biodegradable.
Metronidazol merupakan kelompok obat Nitroimidazol, bertindak secara khusus
terhadap bakteri anaerob dan jarang terjadi resistensi. Banyak penelitian menyatakan
bahwa penggunaan Metronidazol dengan dosis yang direkomendasikan untuk
digunakan dalam kedokteran gigi baik untuk pengobatan lokal dan sistemik adalah
sangat aman. Metronidazol sebagai local drug delivery telah terbukti lebih aman
(konsentrasi serum yang lebih rendah) bila dibandingkan dengan pemberian secara
sistemik.51 Cara kerja Metronidazol adalah setelah menembus membran sel bakteri
Metronidazol akan mengikat DNA dan merusak struktur heliks dari molekul.
Kerusakan DNA akan menyebabkan kematian sel, dan hasil proses ini sangat cepat
membunuh mikroorganisme anaerob. Metronidazol adalah agen kemoterapi yang
efektif terhadap patogen periodontal termasuk P.intermedia, P.gingivalis, dan
Fusobacterium sp. 8,30 Menurut Drisko 2001 dan Pedrazzoli 1992 setelah waktu paruh 8 jam, konsentrasi Metronidazol sangat tinggi sekitar 128µg/ml yaitu sekitar 100 x
kadar hambat minimal dari bakteri paling anaerob sekalipun, dapat menghambat
>90% bakteri subgingiva, dengan resiko efek samping non oral, sensitivitas dan
resistensi minmal. Setelah 24 jam konsentrasi Metronidazol tetap diatas KHM 50%
untuk membunuh kuman periodontal patogen.53
Sato dkk. melakukan pengujian
sediaan lokal gel Metronidazol pada periodontal secara in vivo yang dilakukan pada
Anjing Mongrel telah menunjukkan bahwa Metronidazol dapat dilepaskan di cairan
krevikular gingiva beberapa kali lipat lebih tinggi dari konsentrasi hambat minimum
patogen periodontal yang tumbuh dalam biofilm subgingiva.
Berdasarkan teori pemberian Metronidazol, Metronidazol secara sistemik efektif
terhadap bakteri A.actinomycetemcomitans Metronidazol efektif bila dikombinasikan
dengan antibiotik lainnya.54 Namun pada penelitian ini, gel Metronidazol tanpa
dikombinasi dengan antibiotik lain efektif dalam menghambat pertumbuhan bakteri
A.actinomycetemcomitans. Hal ini kemungkinan karena pemberian obat secara
langsung yang diaplikasikan terhadap bakteri uji sehingga konsentrasi obat yang lebih
tinggi dapat dicapai. Telah diamati oleh beberapa peneliti bahwa pemberian obat
secara lokal dapat mencapai konsentrasi 100 kali lipat lebih tinggi pada daerah yang
diberikan obat dibandingkan dengan pemberian secara sistemik, hal ini akan
mengurangi total dosis lebih dari 400 kali lipat yang diberikan pada pasien sehingga
dapat menghindari terjadinya resistensi obat.
Hasil uji daya hambat Metronidazol 0,125 %, 0,25%, 0,5%, 1% dan 2% berbasis
kitosan dan gel Metronidazol komersil serta Metronidazol dalam agar terhadap
bakteri A.actinomycetemcomitans, P.gingivalis dan F.nucleatum menunjukan adanya
zona bening pada media Mueller Hinton Agar yang berbentuk lingkaran disekitar
kertas cakram. Zona bening tersebut mengindikasikan adanya efektifitas antibakteri
dari masing masing bahan obat. Hasil pengukuran diameter daya hambat masing
-masing bahan obat dengan rerata diatas 22 mm yang menunjukan -masing--masing
bahan obat memiliki daya hambat yang kuat terhadap bakteri
A.actinomycetemcomitans, P.gingivalis dan F.nucleatum. Kesimpulan tersebut berdasarkan penelitian Greenwood 1995 yang menyatakan bahwa apabila daya
hambat yang terbentuk pada uji difusi agar berukuran <10 mm, maka aktivitas
penghambatannya dikategorikan kurang efektif. Apabila daya hambat berukuran
dikategorikan kuat.56 Berdasarkan pernyataan tersebut, gel Metronidazol 0,125%,
0,25%, 0,5%, 1% dan 2% berbasis kitosan memiliki efek antibakteri yang kuat.
Sedangkan gel kitosan tanpa Metronidazol tidak efektif dalam menghambat
pertumbuhan bakteri A.actinomycetemcomitans, P.gingivalis dan F.nucleatum. Hasil
penelitian ini sesuai dengan pernyataan Goy dkk yang menyatakan bahwa kitosan
memiliki efek antibakterial yang lebih tinggi terhadap bakteri gram positif
dibandingkan bakteri gram negatif, seperti yang diketahui bakteri-bakteri yang diuji
dalam penelitian ini merupakan bakteri gram negatif.57
Hasil uji daya hambat Metronidazol 2% berbasis kitosan memiliki daya hambat
paling besar diantara semua konsentrasi Metronidazol yang diuji terhadap bakteri A.
actinomycetemcomitans, P. gingivalis dan F. nucleatum. Metronidazol 1% berbasis
kitosan menunjukkan daya hambat hampir sama atau tidak berbeda secara signifikan
dengan gel Metronidazol komersil terhadap masing-masing bakteri yang diuji dengan
daya hambat >23 mm.
Pada penelitian ini telah terlihat efektifitas antimikroba Metronidazol berbasis
kitosan terhadap bakteri
Walaupun terdapat perbedaan yang signifikan antara daya
hambat gel Metronidazol komersil dibandingkan Metronidazol 0,25% berbasis
kitosan, tetapi Metronidazol 0,25% berbasis kitosan menghasilkan daya hambat >20
mm sehingga dikategorikan kuat.
A.actinomycetemcomitans, P.gingivalis dan F.nucleatum
yang merupakan bakteri patogen periodontal. Berdasarkan hasil penelitian ini,
menjadi dasar untuk melakukan penelitian selanjutnya, sehingga nantinya gel
Metronidazol berbasis kitosan dapat diaplikasikan secara klinis sebagai penunjang
BAB 6
KESIMPULAN DAN SARAN
6.1 Kesimpulan
Pada penelitian ini diperoleh kesimpulan bahwa gel Metronidazol berbasis
kitosan mempunyai efektifitas dalam menghambat pertumbuhan beberapa bakteri
A.actinomycetemcomitans, P.gingivalis dan F.nucleatum secara in vitro. Rerata
diameter daya hambat semua gel Metronidazol berbasis kitosan lebih dari 22 mm
yang menunjukan adanya aktifitas antibakteri Metronidazol 0,125%, 0,25%, 0,5%,
1% dan 2% berbasis kitosan adalah kuat sedangkan gel kitosan tanpa Metronidazol
tidak memiliki aktifitas antibakteri. Gel Metronidazol 2% berbasis kitosan memiliki
aktifitas antibakteri yang paling baik karena menunjukkan diameter daya hambat
yang paling besar dibandingkan dengan gel Metronidazol 0,125%, 0,25%, 0,5% dan
1% berbasis kitosan dan gel kitosan tanpa Metronidazol. Gel Metronidazol 0,25%
berbasis kitosan menghasilkan daya hambat >20 mm sehingga daya hambatnya juga
dikategorikan kuat. Kitosan dapat digunakan sebagai media untuk penghantar obat
secara topikal karena bahan kitosan dapat melepaskan Metronidazol yang ada di
dalam gel kitosan.
6.1 Saran
1. Perlu dilakukan penelitian lanjutan untuk menguji efektifitas gel Metronidazol
2. Perlu dilakukan penelitian lanjutan dengan penambahan variabel waktu yang
lebih lama.
3. Perlu dilakukan penelitian lanjutan secara in vitro untuk mengetahui efek
sitotoksik gel Metronidazol berbasis kitosan.
4. Perlu dilakukan penelitian lanjutan secara in vivo untuk mengetahui efektifitas
gel Metronidazol berbasis kitosan.
5. Perlu dilakukan penelitian mengenai perbandingan antibiotik Metronidazol
secara sistemik dan lokal.