BAB II
TINJAUAN PUSTAKA
II.1. STROKE II.1.1. Definisi
Stroke adalah suatu episode disfungsi neurologi akut disebabkan oleh
iskemik atau perdarahan berlangsung ≥24 jam atau meninggal, tapi tidak
memiliki bukti yang cukup untuk diklasifikasikan (Sacco dkk, 2013).
Stroke iskemik adalah episode disfungsi neurologis disebabkan
infark fokal serebri, spinal dan infark retinal. Dimana infark SSP adalah
kematian sel pada otak, medulla spinalis, atau sel retina akibat iskemia,
berdasarkan:
- Patologi, imaging atau bukti objektif dari focal injury iskemik pada
serebral, medulla spinalis atau retina pada suatu distribusi vaskular
tertentu.
- Atau bukti klinis dari focal injury iskemik pada serebral, medulla
spinalis atau retina berdasarkan symptom yang bertahan ≥ 24 jam
atau meninggal dan etiologis lainnya telah dieksklusikan (Sacco dkk,
2013).
Stroke hemoragik adalah disfungsi neurologis yang berkembang
dengan cepat yang disebabkan oleh perdarahan di parenkim otak atau
II.1.2. Epidemiologi
Insiden stroke bervariasi di berbagai negara di eropa, diperkirakan
terdapat 100-200 kasus stroke baru per 10.000 penduduk per tahun
(Hacke dkk, 2003). Insiden stroke pada pria lebih tinggi dari pada wanita,
pada usia muda, namun tidak pada usia tua. Rasio insiden pria dan wanita
adalah 1,25 pada kelompok usia 55-64 tahun, 1,50 pada kelompok usia
65-74 tahun, 1,07 pada kelompok usia 75-84 tahun dan 0,76 pada
kelompok usia diatas 85 tahun. Negara Amerika diperkirakan terdapat
lebih dari 700.000 insiden stroke per tahun, yang menyebabkan lebih dari
160.000 kematian per tahun, dengan 4,8 juta penderita stroke yang
bertahan hidup (Goldstein dkk, 2006).
Di Indonesia, insiden stroke sebesar 51.6/100.000 penduduk.
Penderita laki-laki lebih banyak dari pada perempuan, dan profil usia di
bawah 45 tahun: 11,8 %, usia 45-64 tahun: 54,2% dan usia lebih dari 65
tahun: 33,5%. Stroke menyerang usia produktif dan usia lanjut, yang
berpotensi menimbulkan masalah baru dalam pembangunan kesehatan
secara nasional di kemudian hari (Misbach dkk, 2011).
II.1.3. Faktor Risiko
Penelitian prospektif stroke telah mengidentifikasi berbagai
faktor-faktor yang dipertimbangkan sebagai risiko yang kuat terhadap timbulnya
stroke. Faktor risiko timbulnya stroke (Sjahrir, 2003)
1. Non modifiable risk factors
a. Usia
b. Jenis Kelamin
c. Keturunan/genetik
2. ModifiableRisk Factors
a. Behavioural Risk Factors
- Merokok
- Unhealthy diet : lemak, garam berlebihan, asam urat,
kolesterol, kurang buah
- Alkoholik
- Obat-obatan: narkoba (kokain), antikoagulansia, anti
platelet, obat kontrasepsi
- Aktifitas yang rendah
b. PhysiologicalRisk Factors
- Penyakit hipertensi
- Penyakit jantung
- Diabetes mellitus
- Infeksi/lues, arthritis, traumatik, AIDS, lupus
- Gangguan ginjal
- Kegemukan (obesitas)
- Polisitemia, viskositas darah meninggi & penyakit
perdarahan
- Kelainan anatomi pembuluh darah
II.1.4. Klasifikasi
Dasar klasifikasi yang berbeda-beda diperlukan, sebab setiap jenis
stroke mempunyai cara pengobatan, pencegahan dan prognosa yang
berbeda, walaupun patogenesisnya sama.
1. Berdasarkan patologi anatomi dan penyebabnya :
a. Stroke Iskemik
- Transient Ischemic Attack (TIA)
- Thrombosis serebri
- Emboli serebri
b. Stroke Hemoragik
- Perdarahan intraserebral
- Perdarahan subarachnoid
2. Berdasarkan stadium / pertimbangan waktu
a. Transient Ischemic Attack (TIA)
b. Stroke inevolution
c. Completed stroke
3. Berdasarkan jenis tipe pembuluh darah
a. Sistem karotis
b. Sistem vertebrobasiler
4. Klasifikasi Bamford untuk tipe infark yaitu
a. Partial Anterior Circulation Infarct (PACI)
b. Total Anterior Circulation Infarct (TACI)
d. Posterior Circulation Infarct (POCI)
5. Klasifikasi stroke iskemik berdasarkan kriteria kelompok peneliti
TOAST (Sjahrir, 2003).
a. Aterosklerosis Arteri Besar
Gejala klinik dan penemuan imejing otak yang signifikan
(>50%) stenosis atau oklusi arteri besar di otak atau cabang
arteri di korteks disebabkan oleh proses aterosklerosis.
Gambaran computed tomography (CT) sken kepala/MRI
menunjukkan adanya infark dikortikal, serebellum, batang
otak, atau subkortikal yang berdiameter lebih dari 1,5 mm
dan potensinya berasal dari aterosklerosis arteri besar.
b. Kardioembolisme
Oklusi arteri disebabkan oleh embolus dari jantung. Sumber
embolus dari jantung terdiri dari :
1. Risiko tinggi
- Prostetik katub mekanik
- Mitral stenosis dengan atrial fibrilasi
- Fibrilasi atrial
- Atrial kiri/atrial appendage thrombus
- Sick sinus syndrome
- Miokard infark baru (<4 minggu)
- Thrombus ventrikel kiri
- Segmen ventricular kiri akinetik
- Atrial myxoma
- Infeksi endokarditis
2. Risiko sedang
- Prolaps katub mitral
- Kalsifikasi annulus mitral
- Mitral stenosis tanpa fibrilasi atrial
- Turbulensi atrial kiri
- Aneurisma septal atrial
- Paten foramen ovale
- Atrial flutter
- Lone atrial fibrillation
- Katub kardiak bioprostetik
- Trombotik endokarditis non bacterial
- Gagal jantung kongestif
- Segmen ventrikuler kiri hipokinetik
- Miokard infark (>4 minggu, <6 bulan)
c. Oklusi Arteri kecil
Sering disebut juga infark lakunar, dimana pasien harus
mempunyai satu gejala klinis sindrom lakunar dan tidak
mempunyai gejala gangguan disfungsi kortikal serebral.
normal atau infark lakunar dengan diameter < 1,5 mm di
daerah batang otak atau subkortikal.
d. Stroke akibat dari Penyebab lain yang menentukan
1. Non-Aterosklerosis vaskulopati
- Non inflamasi
- Inflamasi non infeksi
- Infeksi
2. Kelainan Hematologi atau Koagulasi
e. Stroke Akibat dari Penyebab lain yang Tidak Dapat
ditentukan
II.1.5. Patofisiologi
Pada stroke iskemik, berkurangnya aliran darah ke otak
menyebabkan hipoksemia daerah regional otak dan menimbulkan reaksi
berantai yang berakhir dengan kematian sel-sel otak dan unsur-unsur
pendukungnya (Misbach, 2011).
Secara umum daerah regional otak yang iskemik terdiri dari bagian
inti (core) dengan tingkat iskemik terberat dan berkorelasi di sentral.
Daerah ini akan menjadi nekrotik dalam waktu singkat jika tidak ada
reperfusi. Diluar daerah core iskemik terdapat daerah penumbra iskemik.
Sel-sel otak dan jaringan pendukungnya belum mati akan tetapi sangat
berkurang fungsi-fungsinya dan menyebabkan juga defisit neurologis.
(luxury perfusion area). Daerah penumbra iskemik inilah yang menjadi
sasaran terapi stroke iskemik akut supaya dapat direperfusi dan sel-sel
otak berfungsi kembali. Reversibilitas tergantung pada faktor waktu dan
jika tidak terjadi reperfusi, daerah penumbra dapat berangsur-angsur
mengalami kematian (Misbach, 2011).
Iskemik otak mengakibatkan perubahan dari sel neuron otak secara
bertahap, yaitu: (Sjahrir, 2003)
Tahap 1 :
a. Penurunan aliran darah
b. Pengurangan O2
c. Kegagalan energi
d. Terminal depolarisasi dan kegagalan homeostasis
ion
Tahap 2 :
a. Eksitoksisitas dan kegagalan homeostasis ion
b. Spreading depression
Tahap 3 : Inflamasi
Respon inflamatorik pada stroke iskemik akut mempunyai
pengaruh buruk yang memperberat bagi perkembangan infark
serebri. Berbagai penelitian menunjukkan adanya perubahan
kadar sitokin pada penderita stroke iskemik akut. Mikroglia
merupakan makrofag serebral yang merupakan sumber sitokin
merupakan protein atau glikoprotein yang dikeluarkan oleh suatu
sel dan mempengaruhi sel lain dalam suatu proses inflamasi,
contohnya limfokin dan interleukin (IL-1 beta, IL-6, IL-8,
TNF-yang merupakan sitokin pro-inflamatorik. Adanya IL-8 tersebut
merupakan diskriminator terkuat yang membedakan kasus stroke
dengan non stroke. Produksi sitokin yang berlebih mengakibatkan
plugging mikrovaskuler serebral dan pelepasan mediator
vasokontruktif endothelin sehingga memperberat penurunan aliran
darah, juga mengakibatkan eksaserbasi kerusakan blood brain
barier dan parenkim melalui pelepasan enzim hidrolitik, proteolitik
dan produksi radikal bebas yang akan menambahkan neuron
yang mati.
Tahap 4 : Apoptosis
II.2. LEUKOSIT
Leukosit adalah sistem pertahanan tubuh yang merupakan
kumpulan unit yang bergerak. Sistem daya tahan tubuh ini adalah
kemampuan tubuh untuk bertahan dan menyingkirkan material yang
berbahaya dan sel-sel abnormal dalam tubuh (Sherwood dkk, 2012).
Leukosit atau sel darah putih berfungsi untuk membantu tubuh
melawan berbagai penyakit infeksi dan sebagian dari sistem kekebalan
tubuh, leukosit tidak berwarna, memiliki inti, dapat bergerak secara
terdiri dari neutrofil, basofil, eosinofil, monosit dan limfosit (Baratawidjaja,
2004).
Leukosit dan turunannya serta protein plasma membentuk sistem
imun yang merupakan sistem yang dapat mengenal, menghancurkan dan
menetralisir material yang seharusnya tidak terdapat dalam tubuh
(Sherwood dkk, 2012).
Jumlah normal leukosit adalah 4000-11.000/µl darah manusia,
dimana diantara ini semua sel granulosit (sel polimorfonuklear/PMS)
adalah yang paling banyak. Sel granulosit muda ini memiliki bentuk seperti
tapal kuda dan akan berubah menjadi sel multilobus. Sebagian besar dari
sel polimorfonuklear ini terdiri dari granul (neutrophil), dan sebagian kecil
lagi adalah eusinofil, basophil, limposit yang memiliki inti sel yang lebar
dengan sedikit sitoplasma serta monosit dengan sitoplasma dalam jumlah
besar dan nukleus berbentuk ginjal. Seluruh sel ini akan melindungi tubuh
dengan bekerja sama melawan tumor, virus, bakteri dan infeksi parasit
(Ganong, 2003).
II.2.1. Peranan Leukosit pada Stroke
Tingkat awal dari inflamasi dimulai beberapa jam sesudah awitan
(onset) iskemik dengan karakteristik munculnya ekspresi adhesi molekul di
endotel pembuluh darah dan leukosit di sirkulasi. Leukosit bergerak
melewati endotel keluar dari sirkulasi dan penetrasi ke jaringan parenkim
Infiltrasi leukosit pada iskemik serebral telah diuji secara
eksperimental pada hewan percobaan. Jumlah leukosit yang tinggi pada
darah perifer dinyatakan sebagai prediktor risiko stroke berikutnya (Wang
dkk, 2015).
II.3. MONOSIT
Monosit adalah leukosit fagositik yang juga berperan penting dalam
pertahanan terhadap organisme patogenik dan antigen. Sel yang paling
awal dibentuk monoblas, mengalami proses pematangan melalui
promonosit untuk menjadi monosit matang. Disumsum tulang normal,
prekusor monosit biasanya tidak tampak mencolok. Monosit keluar dari
sumsum tulang setelah matang dan masuk ke sinusoid-sinusoid vena
untuk bersirkulasi dalam darah perifer. Sel-sel ini beredar selama sekitar
12 sampai 14 jam sebelum bermigrasi ke jaringan (Sacher dkk, 2002).
Monosit di bentuk 5 sampai 8% dari leukosit di dalam darah. Setiap
saat, hanya sejumlah kecil monosit yang beredar. Sel-sel ini berasal dari
sel bakal yang sama dengan asal neutrofil, tetapi jalur pematangannya
kemudian terpisah. Sel prekursor (monoblas) mudah terlihat dengan
pewarnaan esterase. Monosit matang beredar secara singkat di dalam
darah perifer dan kemudian masuk ke jaringan untuk menjadi makrofag
(Sacher dkk, 2002).
Peradangan dapat merangsang monosit bermigrasi dari darah ke
Migrasi ini paling mencolok pada peradangan subakut atau kronis. Sel-sel
ini berperan penting dalam banyak mekanisme pertahanan pejamu.
Sel-sel ini sangat aktif dalam fagositosis dan pemusnahan mikroorganisme,
serta dalam banyak interaksi kompleks dengan imunogen dan dengan
konstituen selular dan protein sistem imun. Sel ini mungkin memulai dan
mengatur tingkat respon imun. Sel ini juga bertanggung jawab dalam
pengenalan dan pengolahan antigen. Dengan mengolah dan menyajikan
antigen kepada limfosit-T dan B, monosit memulai respons imun selular
dan humoral. Juga mensekresikan berbagai substansi larut yang aktif
secara biologis yang disebut monokin, diantaranya adalah interleukin -1.
Faktor ini meningkatkan respons proliferative dan ekspresi reseptor
membran sel T. Interaksinya dengan limfosit, terutama limfosit-T, sangat
terintegrasi dan kompleks (Sacher dkk,2002).
II.3.1. Peranan Monosit/Makrofag pada Stroke
Monosit/makrofag mempunyai peranan langsung pada stroke. Sel
mikroglia yang berasal dari makrofag dan blood-derived monocyte/
macrophages mempunyai peranan morfologi dan fungsional pada stroke.
Sel mikroglia diaktivasi cepat sebagai respon dari kerusakan otak.
Aktivasi terjadi dalam beberapa menit dari onset iskemik dan menginduksi
produksi dari sitokin inflamasi yaitu interleukin-1-β (IL-1β) dan Tumor
Necrosis Factor-
/macrophages menginfiltrasi ke jaringan otak dalam beberapa jam sampai
beberapa hari. Studi lain ada yang menunjukkan bahwa blood-derived
monocyte/macrophages banyak terdapat pada jaringan yang mengalami
iskemik, pada hari ke-3 sampai ke-7 setelah stroke. Sebaliknya sel
mikroglia meningkat pada hari pertama setelah iskemik serebri. Sel
mikroglia bisa bertahan pada lesi iskemik hari ke-4 sampai ke-7 (Chiba
dan Umegaki, 2013).
II.4. PROCALCITONIN
Procalcitonin (PCT) adalah precursor peptida dari hormon calcitonin
dan disentesis secara fisiologis oleh sel tyroid. Pada kondisi normal nilai
procalcitonin sangat rendah (0.1 ng/ml) akan tetapi pada infeksi bakteri,
procalcitonin akan disintesis pada jaringan neuroendokrin extratyroid.
Procalcitonin adalah komponen sel inflamasi yang berespon secara
spesifik terhadap infeksi bakteri sitemik. Infeksi bakteri sistemik akan
menimbulkan peningkatan nilai procalcitonin yang tinggi terutama pada
infeksi bakteri gram negatif. Pada infeksi virus ataupun infeksi bakteri
intraseluler seperti mycoplasma pneumonia hanya akan menimbulkan
peningkatan yang tidak berarti. Pada keadaan sepsis nilai procalcitonin ini
tidak terpengaruh terhadap penggunaan steroid secara signifikan. Pada
infeksi bakteri, nilai serum procalcitonin akan meningkat dalam waktu 4
jam setelah onset infeksi dan mencapai puncaknya setelah 8-24 jam (Kibe
II.5. OUTCOME STROKE
Tahun 1890 World Health Organization (WHO) membuat definisi
impairments, disabilitas dan handicaps sebagai berikut (Misbach, 2011):
1. Impairments adalah suatu kehilangan atau abnormalitas fungsi
atau struktur psikologis, fisiologis anatomis.
2. Disabilitas adalah hambatan atau ketidakmampuan akibat
impairments untuk melakukan suatu aktivitas dalam rentang
waktu tertentu dengan cara atau yang dianggap normal untuk
orang sehat.
3. Handicaps adalah gangguan yang dialami oleh individu akibat
“impairment” atau “disabilitas” tersebut, sehingga seseorang
terbatas dalam melakukan suatu perannya sebagai manusia
normal.
Untuk kemudahan dan keseragaman pengukuran kemajuan dari
fungsi otak terdapat beberapa penilaian berdasarkan skoring yang telah
digunakan secara luas didunia. Skoring atau skala yang telah dipakai di
unit stroke dan sudut stroke Rumah Sakit Cipto Mangunkusumo adalah
National Institute of Health Stroke Scale (NIHSS), Barthel Index dan
modified Rankin Scale. Penelitian klinis tentang stroke secara rutin
menggunakan mortalitas sebagai outcome, namun terdapat outcome
lainnya yang penting untuk investigasi klinis dan relevan dengan pasien,
Modified Rankin Scale (mRS) mengukur tingkat keterbatasan
fungsional pasca stroke. Hasil penelitiannya adalah secara umum, terdiri
dari 0-6 dimana 0 berarti tidak ada gejala dan 5 berarti
cacat/ketidakmampuan yang berat, 6 berarti meninggal (Jood dkk, 2008).
Bila mRS 1-3, dikelompokkan sebagai outcome baik sedangkan
mRS 4-6 dikelompokkan sebagai outcome jelek (Painthakar dkk, 2003).
II.6. INFEKSI PADA STROKE FASE AKUT II.6.1. Inflamasi dan Infeksi
Inflamasi SSP memegang peranan penting dalam proses
patofisiologi setelah onset iskemik serebral pada stroke iskemik,
subarachnoid hemorrhage, dan head injury. Selain itu, inflamasi pada SSP
atau perifer dapat menjadi faktor risiko untuk pengembangan awal iskemik
serebral ( Emsley dan Tyrrell, 2002).
Inflamasi setelah proses iskemik ditandai oleh aktivasi cepat sel
mikroglia dan proses infiltrasi dari sel neutrofil serta makrofag pada daerah
yang mengalami kerusakan, beberapa mekanisme antara lain second
messenger yang teraktivasi oleh ion kalsium, peningkatan radikal bebas
oksigen dan hipoksia akan mencetuskan beberapa gen proinflamasi
melalui beberapa faktor transkripsi (Amantea dkk, 2008).
Mediator inflamasi seperti platelet activating faktor, tumor necrotic
faktor- (TNF- interleukin- 1β (IL-1β) dan IL-6 dihasilkan dari sel
endotel seperti ICAM-1, P-selectin, dan E-selectin. Adhesion molecule
akan berinteraksi dengan komplemen pada permukaan reseptor sel
neutrofil. Proses selanjutnya adalah neutrofil teraktivasi dan melakukan
perlekatan pada endotel, menembus dinding pembuluh darah, dan
akhirnya menuju pada parenkim otak yang mengalami iskemik. Masuknya
neutrofil akan diikuti oleh makrofag dan monosit. Sel pertahanan lokal juga
ikut teraktivasi pada proses inflamasi, sekitar 4-6 jam pasca iskemik, sel
astrosit akan menjadi hipertrofik, kemudian sel mikroglia dengan tonjolan
atau prosesusnya akan membentuk struktur ameboid yang berarti menjadi
bentuk aktif (Dirnagl dkk, 2005).
Setelah stroke fase akut, infeksi sistemik dapat mempersulit proses
pemulihan dan menyebabkan outcome klinis yang lebih buruk, termasuk
risiko kematian yang lebih tinggi. Post Stroke Infection (PSI)
bertanggungjawab terutama pada kejadian mortalitas yang terjadi antara 1
minggu dan 1 bulan setelah stroke, puncaknya pada akhir minggu kedua.
Efek dari PSI pada outcome jangka panjang dan aspek lain dari
pemulihan, seperti kognisi, mood dan kualitas hidup sebagian besar tidak
diketahui. Meskipun telah ada kemajuan dalam pemahaman dasar
tentang mekanisme patofisiologi PSI, studi klinis belum memberikan
guidline dengan metode terbaik untuk manajemen atau preventif dari PSI.
(Kwan dkk, 2008).
Setelah stroke fase akut, pasien memiliki risiko tinggi
paling umum adalah PSI. Komplikasi ini serius dapat memperpanjang dan
mempersulit proses pemulihan serta meningkatkan risiko mortalitas dan
morbiditas. Pada penelitian dalam jumlah besar pada RS di Jerman,
komplikasi medis yang serius yang paling sering terjadi pada minggu
pertama rawat inap adalah stroke berulang dan pneumonia. Dalam
sebuah penelitian yang berbasis besar di Inggris, pneumonia dan infeksi
saluran kemih (ISK) adalah komplikasi medis yang paling sering terjadi.
(Kwan dkk, 2008).
II.6.2. Efek inflamasi pada status imunologis
Otak dan sistem kekebalan tubuh secara fungsional dihubungkan
melalui jalur sistem saraf dan sistem humoral, penurunan fungsi sistem
kekebalan tubuh dan tingginya kejadian infeksi telah ditunjukkan pada
keadaan-keadaan yang disebabkan gangguan fungsi saraf akut. Cedera
pada SSP, baik di otak maupun medulla spinalis dapat mengakibatkan
pelepasan mediator-mediator inflamasi pada SSP, atau gangguan dalam
pengontrolan sirkuit neural-immune, keduanya mengakibatkan penurunan
sistem imunitas, baik innate immunity maupun adaptive immunity, hal ini
menyebabkan defisiensi dari sistem kekebalan tubuh, sehingga individu
tersebut menjadi rentan terhadap invasi mikroorganisme. Walaupun
respon awal lokal terhadap kerusakan otak adalah pelepasan
pasien-pasien dengan lesi di SSP juga menunjukkan adanya tanda-tanda
immunodepresi (Meisel dkk, 2005).
II.6.3. Stroke sebagai faktor risiko untuk mengembangkan infeksi
Meskipun infeksi sering terjadi setelah stroke dan beberapa studi
menemukan hubungan antara stroke dan infeksi yang didapat ketika
dirawat di rumah sakit. Tidak ada bukti yang jelas, apakah stroke akut
secara tidak langsung meningkatkan risiko infeksi sistemik, atau apakah
peningkatan risiko infeksi sebagai akibat dari konsekuensi kondisi yang
tidak baik (misalnya, imobilitas dan status gizi buruk). Hal ini juga diketahui
bahwa kondisi medis akut non-stroke lainnya juga dapat menyebabkan
infeksi didapat di rumah sakit, dan studi telah melaporkan variasi yang
sangat luas dalam frekuensi terjadinya infeksi, dari sangat rendah (2-10%)
untuk tingkat yang ditemukan diantara studi stroke dengan cohort (~20%)
(Kwan dkk, 2008).
II.6.4. Kondisi yang dapat menyebabkan infeksi setelah stroke
Setelah stroke akut, defisit neurologis dan fungsional yang
menyebabkan tingkat ketergantungan yang tinggi dapat berpotensi
mengalami kecendrungan untuk terjadinya PSI. Dalam satu penelitian
terbaru, disfagia, inkontinensia urin (dan kateterisasi urin) dan penurunan
kesadaran yang ditemukan merupakan faktor predisposisi PSI. Disfagia
malnutrisi. Penelitian sebelumnya telah menunjukkan bahwa sekitar
setengah dari semua pasien stroke dengan disfagia akan mengalami
aspirasi, dan lebih dari sepertiga dari pasien ini akan mengembangkan
aspirasi pneumonia dan sekitar setengah akan berkembang menjadi
malnutrisi. Pasien dengan penurunan kesadaran dapat meningkatkan
risiko aspirasi oleh karena menurunnya pengaturan refleks batuk pasien,
sehingga menyebabkan rendahnya pembersihan sekresi. Intervensi
seperti nasogastrik, yang secara tradisional dianggap sebagai metode
yang aman memberikan nutrisi bagi pasien yang berisiko aspirasi, telah
terbukti hanya memberikan perlindungan yang terbatas terhadap aspirasi
pneumonia (Kwan dkk, 2008).
Inkontinensia urin, yang sangat umum setelah stroke akut, dapat
menyebabkan maserasi perineum dan kerusakan kulit. Meskipun
hubungan sebab akibat yang jelas antara kateterisasi urin dan urinary
tract infection (UTI), pasien stroke akut umumnya masih dikelola dengan
menggunakan kateter urin, terutama selama periode awal. Kateterisasi
urin tidak hanya mendorong pertumbuhan bakteri, tetapi pembentukan
biofilm yang terbentuk pada bagian dalam kateter juga berfungsi untuk
melindungi bakteri dari pertahanan tubuh dan terapi antibiotik, dan ini
merupakan keuntungan terhadap kelangsungan hidup bakteri. Pada tahun
2007, Kwan dkk menunjukkan bahwa kateterisasi urin meningkatkan
kemungkinan pengembangkan UTI pasca stroke tiga sampai empat kali
cenderung mengalami PSI termasuk malnutrisi, penggunaan kateter vena
perifer atau pusat, hiperglikemia dan bedrest berkepanjangan (Kwan dkk,
2008).
II.6.5. Diagnosis Infeksi Pada Stroke Fase Akut
Deteksi dan pengobatan dini PSI telah disorot sebagai salah satu
alasan mengapa stroke unit care terorganisir sehingga didapatkan
kelangsungan hidup dan outcome yang lebih baik, dan tentu saja telah
dimasukkan sebagai salah satu elemen utama dalam manajemen stroke
fase akut. Aspek yang paling penting dari manajemen dari PSI adalah
ambang yang rendah untuk menegakkan diagnosis PSI. Namun, dalam
praktek klinis dapat sangat sulit untuk memastikan diagnosis, terutama
karena gejala klinis dan tanda-tanda bisa sulit untuk didapatkan, dan apa
yang mungkin dianggap sebagai temuan klinis yang abnormal dari infeksi
sebenarnya bisa merupakan sequele yang sering setelah stroke (tidak
terkait dengan infeksi). Misalnya, gejala pneumonia biasanya termasuk
batuk produktif dan demam. Namun, setelah stroke, refleks batuk mungkin
ditekan, suara ditransmisikan saluran nafas bagian atas dapat sering
didengar karena sulit menelan dan demam yang sering dapat diamati
tanpa adanya infeksi (Kwan dkk, 2008).
Di Copenhagen Stroke Study, 25% pasien stroke akut mengalami
demam, dan ini hanya 16% telah membuktikan terjadinya infeksi
pneumonia, seperti crackles inspirasi dan penurunan suara napas, sangat
tidak spesifik dan sering bisa ditemukan pada pasien tanpa pneumonia
(Kwan dkk, 2008).
A. Pneumonia setelah stroke
Diagnosis pneumonia ditentukan oleh :
1. Pemeriksaan paru yang abnormal, infiltrasi paru pada foto thorak
2. Batuk yang produktif dengan sputum purulen, pada kultur
ditemukan mikrobiologi positif ataupun kultur darah (Harms dkk,
2010).
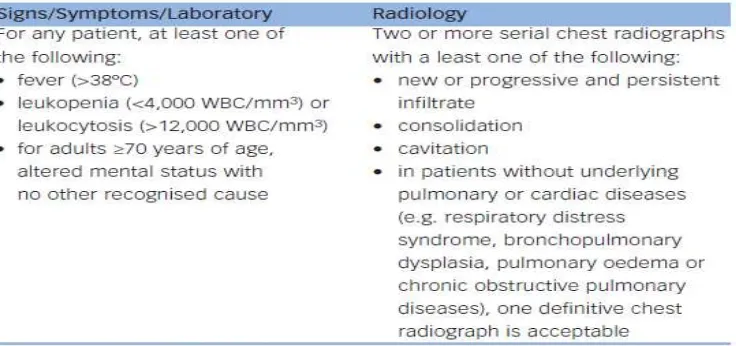
Tabel 1. Kriteria untuk Definisi Klinis Pneumonia berdasarkan Centers for Disease Control
Dikutip dari : Harms H, Halle E, Andreas Meisel A. 2010. Post-Stroke Infections – Diagnosis, Prediction, Prevention And Treatment To Improve Patient Outcomes. European Neurological Review;5(1):39–43
B. Infeksi Saluran Kemih
Diagnosis infeksi saluran kemih ditentukan oleh :
1. Demam ≥ 380
C
3. Leukosituria > 40/µL ataupun ada bakteriuria ≥ 104
/mL
Tabel 2. Kriteria untuk Infeksi Saluran Kemih berdasarkan Centers for Disease Control
Dikutip dari: Dikutip dari : Harms H, Halle E, Andreas Meisel A. 2010. Post-Stroke Infections – Diagnosis, Prediction, Prevention And Treatment To Improve Patient Outcomes. European Neurological Review;5(1):39–43
C. Infeksi lainnya
Diagnosis ini ditentukan oleh :
1. Suhu ≥ 380 C
2. Leukosit ≥ 11.000/mL
II.7. HUBUNGAN KADAR LEUKOSIT DAN MONOSIT DENGAN INFEKSI PADA STROKE FASE AKUT
Beberapa tahun ini, infeksi seperti pneumonia telah diketahui
merupakan komplikasi tersering pada stroke iskemik. Namun, studi
terbaru menunjukkan bahwa inflamasi sistemik mungkin juga menjadi
faktor risiko untuk terjadinya stroke iskemik. Secara khusus, leukositosis
awal dan neutrofilia yang ditemukan terkait dengan volume jaringan infark
sebagaimana dinilai dengan diffusion-weighted magnetic resonance
imaging di antara pasien dengan stroke iskemik akut. Limfopenia dan
monositosis yang terjadi pada awal stroke berkorelasi dengan volume
infark dan juga mungkin meningkatkan kerentanan pasien terhadap
infeksi. Selain itu, peningkatan jumlah leukosit dan neutrofil perifer
dilaporkan dikaitkan dengan kejadian stroke iskemik berulang yang lebih
tinggi. Sampai saat ini, tidak ada penelitian yang secara definitive
menunjukkan bahwa tingkat peradangan sistemik pada saat masuk rumah
sakit dikaitkan dengan kelangsungan hidup, derajat kerusakan dan
kecacatan setelah stroke iskemik akut karena ada beberapa perancu
potensial untuk leukositosis (Furlan dkk, 2013).
Infeksi peripheral, yang biasanya mempengaruhi saluran kemih dan
pernapasan pada beberapa hari dan beberapa minggu setelah stroke
iskemik akut, telah dihubungkan dengan tingkat keparahan stroke, usia
yang lebih tua, disfagia dan aspirasi. Disregulasi respon imun setelah
infeksi pasca stroke. Data dasar peneliti mengkonfirmasi bahwa pasien
dengan peningkatan leukosit pada awal masuk lebih rentan terhadap
infeksi saluran kemih atau pernapasan dan sepsis pada hari-hari
berikutnya setelah stroke iskemik akut. Cross-talk antara sistem saraf
pusat dan sistem kekebalan tubuh dikenal dengan baik dan setidaknya
sebagian dapat menjelaskan penurunan kemampuan sistem imun akibat
stimulus stress yang diikuti perburukan dari sistem saraf pusat termasuk
cedera otak traumatik, cedera tulang belakang traumatik dan stroke.
Sementara mediator inflamasi yang ditemukan pada tingkat rendah pada
jaringan otak yang sehat, insult otak iskemik menginduksi sitokin
proinflamasi, kemokin dan perekrutan sel imun ke dalam sistem saraf
pusat. Sel-sel inflamasi yang telah diaktivasi terlibat dalam perkembangan
sekunder lesi otak dan prognosis kurang menguntungkan setelah insult
dari sistem saraf pusat. Ini adalah penjelasan yang paling mungkin untuk
temuan penelitian Furlan J.C dkk yang sebagian besar menunjukkan
hubungan antara tingginya leukosit dalam darah dan outcome yang lebih
buruk setelah stroke iskemik akut (Furlan dkk, 2013).
Imunitas dan peradangan memainkan peran penting dalam
patogenesis stroke akut. Berbagai elemen dari sistem kekebalan tubuh
yang terlibat dalam semua tahap kaskade iskemik, dari peristiwa
intravaskular akut proses parenkim, menyebabkan kerusakan otak dan
memperbaiki jaringan. Sebagai contoh, ekspresi berbagai sitokin di lokasi
tumor necrosis factor (TNF) -
dan faktor pertumbuhan. Di perifer setelah stroke, aktivasi sistemik dari
sistem kekebalan tubuh terjadi dengan tingkat peningkatan sitokin seperti
IL-1β, IL-6, TNF- -10, IL-17 dan transforming growth factor (TGF)-sS.
Selain itu, studi sebelumnya telah menyarankan bahwa masuknya sel
kekebalan yang berbeda, termasuk sel-sel T, sel B, monosit, dan sel
dendritik, serta sitokin yang diproduksi di otak dapat memberi efek
imunomodulator pada peradangan paska-iskemik (Kaito dkk, 2013).
Ada konsensus yang menyatakan bahwa stroke dapat
menyebabkan imunosupresi dalam tahap awal, meningkatkan risiko
infeksi dan juga akan memberikan kontribusi untuk mencegah
perkembangan kerusakan otak selanjutnya. Beberapa studi menunjukkan
bahwa monosit beredar sebagai antigen-presenting leukosit, memainkan
peran yang penting dalam inflamasi, diferensiasi sel T, fagositosis, dan
imunitas bawaan. Data eksperimen telah menunjukkan bahwa monosit
perifer akut direkrut ke daerah infark dalam 24 jam pertama iskemia
jaringan berasal dari reservoir limpa dan mungkin bermanfaat untuk
mengurangi stroke yang disebabkan cedera otak. Selain itu, deactivation
fungsional monosit cepat dan berkepanjangan telah diamati setelah stroke
akut pada manusia, yang ditandai dengan berkurangnya ekspresi human
leukocyte antigen (HLA)-Dr dan rendahnya produksi TNF-
II.8. HUBUNGAN KADAR PROCALCITONIN DENGAN RISIKO TERJADI INFEKSI PADA STROKE FASE AKUT
Mekanisme tentang sintesa dan peran PCT setelah peradangan
sampai sekarang sama sekali tidak diketahui. Selama infeksi mikroba,
akan terjadi peningkatan ekspresi gen CALC-I yang menyebabkan
pelepasan PCT dari seluruh jaringan parenkim dan seluruh sel
terdeferensiasi di seluruh tubuh. Pelepasan PCT pada saat peradangan
diinduksi dalam dua jalur utama yaitu: cara langsung diinduksi oleh toksin
atau lipopolisakarida yang dilepaskan oleh mikroba, dan induksi tidak
langsung melalui respon imun penjamu yang bersifat cell-mediated yang
dimediasi oleh sitokin inflamasi (seperti interleukin-1β [IL-1β], interleukin-6
[IL-6], tumor necrosis factor- -
Procalcitonin meningkatkan prediksi terjadinya SAI dibandingkan
dengan penanda prognostik kuat yang lainnya. Kombinasi biomarker
mungkin lebih baik dari pada pemeriksaan satu biomarker saja sehingga
dapat memprediksi terjadinya infeksi yang lebih akurat dari awal terjadinya
infeksi walaupun klinisnya belum jelas. Biomarker diselidiki untuk
mendeteksi infeksi sebelum tanda-tanda klinis atau paraclinical di
diagnosis lanjut sampai mengarah ke diagnosis infeksi. Dengan demikian,
tanda tersebut dapat membantu dalam stratifikasi risiko dan dapat memilih
pasien berisiko tinggi untuk studi intervensi (Fluri dkk, 2012).
Sebagai biomarker diagnostik pada sepsis bakteri, substansi yang
infeksi bakteri, konsentrasi PCT serum akan mulai naik sejak 4 jam
setelah onset infeksi, dan mencapai puncaknya 8 atau 24 jam setelahnya.
Kebalikannya, CRP dengan leukosit sebagai pengecualiannya merupakan
biomarker infeksi yang paling sering digunakan di Inggris ditentukan
meningkat secara perlahan dan mencapai puncaknya hingga 36 jam
setelah terjadinya perubahan endotoksin (Kibe dkk, 2011).
II.9. HUBUNGAN KADAR LEUKOSIT DENGAN OUTCOME FUNGSIONAL
Menurut penelitian yang dilakukan Nardi K dkk (2012) menunjukkan
bahwa jumlah leukosit meningkat pada awal fase akut stroke yang
merupakan prediktor independent yang signifikan pada tingkat keparahan
yang jelek pada awal stroke, dan outcome klinis yang buruk setelah 72
jam, dan menimbulkan kecacatan. Untuk pertama kalinya, penelitian ini
mendukung nilai prognostik leukositosis pada fase akut iskemik untuk
outcome awal. Studi ini menjelaskan leukositosis pada awal fase akut
stroke.
Pada penelitian yang dilakukan Nardi K dkk (2012), pada 811
pasien, outcome fungsional menunjukkan interaksi yang kuat dengan level
leukosit pada saat masuk. Sebuah korelasi yang kuat antara jumlah
leukosit yang lebih tinggi dan kecacatan ditemukan dengan menggunakan
Spearman rank correlation (r=0,21; p<001). Korelasi tetap baik dalam
independen mRS, seperti usia (NS), jenis kelamin (NS), dan NIHSS (p
<0,0001). Berfokus pada berbagai syndrome klinis stroke, pasien total
Anterior Cerebral Stroke (TACS) dengan tingkat leukosit yang lebih tinggi
saat masuk lebih cenderung memiliki outcome fungsional yang jelek. Pada
pasien TACS, korelasi antara tingkat leukosit dan mRS kuat
menggunakan Spearman rank correlation (r=0,27; p=0,003). Sebaliknya,
pasien Partial Anterior Cerebral Stroke (PACS), Posterior Cerebral Stroke
(POCS), dan Lacunar Cerebral Stroke (LACS) tidak memiliki interaksi
yang signifikan antara jumlah leukosit dan mRS (p = NS).
Peng Y dkk (2011) melakukan penelitian dengan sampel yang
besar pada hubungan antara jumlah leukosit saat masuk dan outcome
jangka pendek pada pasien infark serebral akut. Peningkatan jumlah
leukosit pada saat masuk ditemukan secara independen berkaitan
dengan kematian di rumah sakit dan dependency antara pasien dengan
infark serebral akut. Jumlah leukosit lebih tinggi pada kasus kematian dari
pada kasus dependency, dan lebih tinggi dalam kematian dan kasus
dependency dari kasus non-dependent. Hasil pengamatan menunjukkan
bahwa jumlah leukosit saat masuk mungkin memprediksi terjadinya
outcome yang buruk di jangka pendek antara pasien infark serebral akut.
Pada 763 pasien stroke yang tidak diseleksi, datang dalam waktu
24 jam dari onset, Kammersgaard dkk, secara prospektif mempelajari
hubungan antara jumlah leukosit dan outcome klinis. Temuan mereka
keparahan stroke tapi tidak dengan outcome, jumlah leukosit saat masuk
tampaknya hanya menggambarkan keparahan awal stroke dan biasanya
ini merupakan respon stress tanpa pengaruh independen pada outcome.
Studi Kazmierski dkk (2004) menunjukkan bahwa peningkatan
jumlah leukosit dalam waktu 12 jam sejak onset stroke iskemik merupakan
faktor prognostik yang kuat untuk mortalitas di rumah sakit pada 400
penderita stroke akut.
Di Northern Manhattan Stroke Study (Elkind dkk, 2004), 655 pasien
dengan stroke iskemik dilakukan uji prospektif selama 5 tahun untuk
mengetahui terjadinya stroke berulang, infark miokard atau kematian.
Temuan mereka menunjukkan bahwa jumlah leukosit tinggi pada saat
stroke iskemik memprediksi terjadinya stroke berulang, infark miokard
atau kematian.
Studi T Uraj dkk (2006), menunjukkan bahwa jumlah leukosit
adalah prediktor independen dari kasus fatalitas selama satu tahun pada
900 pasien dengan stroke iskemik yang datang ke rumah sakit dalam
waktu 24 jam setelah timbul gejala.
Dalam penelitian Agnihotri dkk (2011), jumlah leukosit perifer
secara independen memprediksi outcome fungsional yang buruk dalam
pengurangan Modified Barthel Index (MBI) pada 3 bulan. Hal ini
menunjukkan bahwa aktivasi sistem kekebalan tubuh perifer dapat
meningkatkan cedera setelah ICH. Namun, perubahan jumlah leukosit
terpanjang yang berkorelasi dengan biomarker sampai saat ini pada
pasien ICH.
II.10. HUBUNGAN KADAR MONOSIT DENGAN OUTCOME FUNGSIONAL
Dalam studi klinis, total jumlah leukosit perifer telah dikaitkan
dengan volume awal perdarahan, awal kerusakan neurologis, dan
outcome fungsional setelah Intracerebral hemorrhage (ICH). Neutrofil dan
monosit adalah leukosit yang dominan, neutrofil perifer dan infiltrasi
monosit telah ditemukan berkontribusi terhadap secondary injury pada
percobaan yang menggunakan hewan yang mengalami ICH. Monosit
dalam aliran darah memainkan peran utama dalam patogenesis
aterosklerosis dan penyakit kardiovaskular. Peredaran monosit juga
mengungkapkan sejumlah besar faktor jaringan berinteraksi dengan
trombosit dan memodulasi trombosis dan hemostasis. Sebuah studi klinis
terbaru menemukan bahwa peningkatan ekspresi TLR2 dan TLR4 di
monosit dikaitkan dengan outcome yang buruk setelah ICH (Adeoye dkk,
2014).
Jika tersedia biomarker yang langsung bisa digunakan untuk
menghitung jumlah monosit dan neutrofil perifer, yang dapat digunakan
sebagai prediktif yang kuat terhadap luasnya perdarahan, edema serebral,
dan/atau outcome pada ICH, hal ini dapat menimbulkan pertanyaan dalam
jumlah leukosit. Dalam penelitian Adeoye dkk, ditemukan hubungan
leukosit perifer, monosit dan jumlah neutrofil dengan baseline volume ICH
dan mengalami perburukan dalam 30 hari. Penelitian Adeoye dkk,
berhipotesis bahwa jumlah leukosit, absolute monocyte count (AMC) dan
absolute neutrophil count (ANC) pada presentasi dan perubahan monosit
dan neutrofil yang dihitung dari presentasi sampai 24 jam pertama
dikaitkan dengan menyajikan volume ICH dan mengalami perburukan
dalam 30 hari (Adeoye dkk, 2014).
Hal ini menunjukkan bahwa hubungan jumlah monosit dengan
kasus kematian mungkin karena kontribusi monosit pada secondary injury
setelah ICH. Temuan baru ini dapat meningkatkan pemahaman tentang
patofisiologi dan klinis ICH dan menyebabkan penyelidikan lebih lanjut jika
dikonfirmasi dalam sebuah set data independen (Adeoye dkk, 2014).
Secondary injury setelah ICH dapat dihasilkan dari ekspansi
hematoma atau edema serebral. Meskipun Adeoye dkk tidak menemukan
hubungan jumlah monosit dengan ekspansi hematoma dalam laporan ini,
studi prospektif yang cukup kuat diperlukan untuk menyelidiki hubungan
jumlah monosit dan kasus kematian ICH. Terkecuali ada hubungan yang
jelas antara jumlah monosit dengan ekspansi hematoma dan/atau edema
serebral, mekanisme monosit dapat berkontribusi untuk outcome yang
jelek dan kasus yang fatal setelah ICH termasuk peningkatan perlekatan
monosit pada endotel pembuluh darah, sehingga merusak sawar darah
chemoattractant monosit yang diekspresikan dalam pembuluh darah otak
dan dikenal untuk memfasilitasi kematian neuronal dan mencetuskan
terjadinya cedera pembuluh darah setelah berikatan dengan monosit dan
total ekspresi dari TLRs 2 dan 4 (antara molekul pro-inflamasi lainnya)
berkontribusi terhadap edema serebral dan outcome yang buruk (Adeoye
dkk, 2014).
Seperti yang telah diuraikan sebelumnya, Adeoye dkk; menemukan
bahwa jumlah leukosit dan neutrofil awal yang lebih tinggi berhubungan
secara signifikan dengan volume ICH awal yang lebih besar. Berbeda
dengan laporan sebelumnya, ini tidak independen terkait dengan outcome
setelah disesuaikan dengan jumlah monosit. Adeoye dkk tidak
menemukan hubungan antara perubahan awal leukosit, neutrofil atau
jumlah monosit dan volume ICH atau kasus kematian. Namun, hasil ini
mungkin karena ukuran sampel yang kecil, dan data untuk pemeriksaan
laboratorium ulang tidak tersedia, hanya data awal yang tersedia,
sehingga tidak ada data untuk perbandingan (Adeoye dkk, 2014).
II.11. HUBUNGAN KADAR PROCALCITONIN DENGAN OUTCOME FUNGSIONAL
Miyakis dkk (2004) pada studi percontohan pada nilai prognostik
PCT pada stroke akut. Kadar serum serial tidak berkorelasi dengan
Procalcitonin telah digunakan dalam guidline terapi penggunaan
antibiotik, tetapi tidak pada stroke akut. Pada pasien di ruang gawat
darurat dengan gejala infeksi saluran pernapasan bawah, PCT diukur dan
hanya pasien dengan konsentrasi PCT >0,25 ng/mL atau >0,5 ng/mL
yang diberikan terapi antibiotik (Christ-Crain dkk, 2004).
Dengan latar belakang terganggunya fungsi kekebalan tubuh pada
pasien stroke disatu sisi dan adanya respon inflamasi sistemik setelah
stroke pada sisi lainnya, hal ini benar-benar menjelaskan apakah
konsentrasi PCT berubah pada pasien dengan infeksi pasca stroke. Pada
penelitian dari tingkat PCT serum pada pasien stroke akut tidak
menunjukkan perbedaan yang signifikan antara hari rawat inap dan hari
II.12. KERANGKA TEORI
STROKE AKUT
Misbach dkk, 2011: glukosa & O2 (-) gangguan
homeostasis kematian sel secara tidak langsung
MIsbach dkk, 2011: stroke iskemik aliran darah ke otak hipoksemia kematian sel-sel otak.
KERUSAKAN JARINGAN
Amantea dkk, 2008: daerah yang mengalami kerusakan inflamasi aktivasi cepat sel mikroglia & proses infiltrasi dari sel netrofil serta makrofag
Misbach dkk, 2011: inflamasi dimulai beberapa jam sesudah awitan iskemik ekspresi adhesi molekul di endotel pembuluh darah & leukosit di sirkulasi.
Caplan , 2009: sitokin komponen kunci pada aktivasi dan pengerahan leukosit di SSP.
Dirnagl dkk, 2005: inflamasi neutrofil teraktivasi & melakukan perlekatan pada endotel dinding pembuluh darah & akhirnya parenkim otak yang mengalami iskemik. Masuknya neutrofil akan diikuti oleh makrofag & monosit.
Watenberg dkk, 2011: leukosit, CRP, edema serebal & outcome yang buruk
Chamorro et inflamasi & makrofag akan menyerbu & memfagositosis sisa-sisa sel.
PROSES INFLAMASI
Amantea dkk,2005: inflamasi aktivasi cepat sel mikroglia & proses infiltrasi dr sel neutrofil serta makrofag daerah yang mengalami kerusakan
Suzuki dkk : terdpt hubungan linear antara jumlah leukosit & volume hematoma.
II.13. KERANGKA KONSEP
STROKE AKUT
KADAR LEUKOSIT, MONOSIT DAN PROCALCITONIN
INFEKSI PADA STROKE FASE AKUT