SKRIPSI
MONIKA KLARIZCA SARAGIH 170801032
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN 2021
PENGARUH SUHU TERHADAP SINTESIS DAN KARAKTERISASI Fe
3O
4DENGAN METODE KOPRESIPITASI
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
MONIKA KLARIZCA SARAGIH 170801032
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN 2021
PERNYATAAN ORISINALITAS
PENGARUH SUHU TERHADAP SINTESIS DAN KARAKTERISASI Fe3O4 DENGAN METODE KOPRESIPITASI
SKRIPSI
Saya menyatakan bahwa skripsi ini adalah hasil karya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, 18 Agustus 2021
Monika Klarizca Saragih 170801032
PENGARUH SUHU TERHADAP SINTESIS DAN KARAKTERISASI FE
3O
4DENGAN METODE KOPRESIPITASI
ABSTRAK
Proses pembuatan Fe3O4 dilakukandengan metode kopresipitasi dan dilakukan variasi suhu yang bertujuan untuk mengetahui pengaruh suhu terhadap Fe3O4. Telah disintesis dan dikarakterisasi morfologi, struktur kristal dan sifat magnetik material magnetik Fe3O4 dengan menggunakan metode kopresipitasi, di kalsinasi pada suhu 100 °C, 125 °C, 150 °C selama 10 jam. Morfologi, struktur kristal, dan sifat magnet dikarakterisasi menggunakan X-ray Diffraction (XRD), Scanning Electron Microscope (SEM). Bahan baku sintesis Fe3O4 adalah FeCl2.4H2O dan FeCl3.6H2O. Struktur kristal hasil analisis XRD menyatakan bahwa peningkatan suhu pada proses kalsinasi material Fe3O4mempengaruhi puncak difraksi yang dihasilkan dan dapat dilihat semakin tinggi suhu maka semakin tinggi puncak difraksinya. Kemudian hasil analisis SEM menyatakan hasil tidak Homogen dikarenakan waktu penggerusan sampel kurang lama sehingga sampel tidak homogen.
Kata Kunci :Fe3O4, Kopresipitasi, Struktur Kristal, Sifat Magnet.
EFFECT OF TEMPERATURE ON SYNTHESIS AND CHARACTERIZATION OF FE
3O
4WITH COPRECIPITATION METHOD
ABSTRACT
The process of making Fe3O4 is carried out by the coprecipitation method and temperature variations are carried out which aim to determine the effect of temperature on Fe3O4. It has been synthesized and characterized by morphology, crystal structure and magnetic properties of Fe3O4 magnetic material using coprecipitation method, calcined at 100 °C, 125 °C, 150 °C for 10 hours. Morphology, crystal structure, and magnetic properties were characterized using X- ray Diffraction (XRD), Scanning Electron Microscope (SEM). The raw materials for the synthesis of Fe3O4 are FeCl2.4H2O and FeCl3.6H2O. The crystal structure of the XRD analysis states that the increase in temperature in the calcination process of Fe3O4 material affects the resulting diffraction peak and it can be seen that the higher the temperature, the higher the diffraction peak. Then the results of the SEM analysis stated that the results were not homogeneous because the grinding time of the sample was not long enough so that the sample was not homogeneous.
Keywords: Fe3O4, Coprecipitation, Crystal Structure, Magnetic Properties.
PENGHARGAAN
Puji dan Syukur penulis ucapkan Kehadirat Tuhan Yang Maha Esa dimana atas berkat dan kasih karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini dengan judul “Pengaruh Suhu Terhadap Sintesis dan Karakterisasi Fe3O4 dengan Metode Kopresipitasi”. Penelitian ini di laksanakan di Laboratorium Ilmu Dasar dan Umum Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara (USU) Medan,Laboratorium Pusat Survey Geologi Bandung, dan Laboratorium Terpadu Universitas Sumatera Utara, Medan. Skripsi ini disusun sebagai syarat akademis dalam menyelesaikan studi program sarjana (S1) Jurusan Fisika Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Penulisan ini tidak dapat terselesaikan jika tidak adanya dukungan serta saran yang penulis terima selama penyelesaian Skripsi ini.Ucapan terimakasih yang tak terhingga kepada Bapakku Tercinta Alm.Riahman Saragih Garingging dan Mamakku tersayang Eva Erstayana Sitopu yang selalu menjadi alasan penulis untuk semangat dan berjuang, selalu menguatkan dan memberi dukungan penuh kepada penulis, baik dalam hal materi dan nasihat yang luar biasa.Penulis juga mengucapkan terimakasih kepada kakaku tersayang Alm.Amanda Eria Saragih Garingging, SE yang telah meberikan penulis banyak hal baik.memberikan nasihat dan dukungan yang luar biasa, kakaku Chyntya Yolanda Saragih Garingging, S,Th yang juga memberikan dukungan luar biasa dan setia mengingatkanku. Terimakasih kepada adik-adik saya Yohana Tresya Saragih Garingging, Josua Priadinata Saragih Garingging, Keysa Putlima Saragih Garingging, Chassey Widya Damanik, Dea Dwi Putri Damanik, Tesalonika Cindy Try Ayu Damanik, dan Bapan Godang saya Jonri Damanik. Penulis juga ingin menyampaikan rasa terimakasih yang sebesar-besarnya atas segala bantuan, dukungan serta saran yang penulis dapatkan :
1. Ibu Dr. Nursahara Pasaribu M.Sc selaku Dekan FMIPA Universitas Sumatera Utara 2. Bapak Perdinan Sinuhaji, MS, sebagai Ketua Departemen Fisika USU, Bapak Awan
Maghfirah, M. Si, sebagai Sekretaris Departemen Fisika USU, serta seluruh Dosen, Staf, dan Pegawai Departemen Fisika USU
3. Kepada Bapak Prof. Dr. Timbangen Sembiring,M.Scselaku Dosen Pembimbing yang telah memberikan kesempatan, motivasi, ilmu, nasihat serta dukungan dalam membimbing penulis selama ini.
4. Bapak Dr. Syahrul Humaidi, M.Sc selaku dosen penguji yang telah memberikan pengarahan dan bimbingan kepada penulis.
5. Ibu Prof. Dr. Zuriah Sitorus, MS, selaku dosen penguji yang telah memberikan pengarahan dan bimbingan kepada penulis.
6. Kepada Ibu Hariyati Lubis dan Bapak Ridwan Yusub Lubis yang selalu setia dan sabar, sudah membimbing dan mengarahkan penulis hingga menyelesaikan Skripsi ini.
7. Kepada Yoki Aldona Damanik yang selalu sabar dan setia mengingatkan saya dan selalu memberi semangat serta dukungan.
8. Kepada Jeprin Tua Sihite, David Arianto Hutajulu, Yosalina Br.Tumorang teman seperdopingan dan seperjuangan saya, yang selalu menerima keluh kesah saya.
9. Sahabat yang telah memberikan semangat, doa dan dukungan nya dalam menyelesaikan tugas akhir iniMaria Sihombing, Mitra.
10. Terimakasih kepada Kelompok Kecil saya Mitra, Jusnartik, Dewi, Naomi dan Kaka PKK saya Kak Nova Lubis.
11. Kepada Yosua Sirait yang banyak membantu saya.
12. Kepada segenap Physic Infinity yang mengisi waktu kuliah saya dengan tidak membosankan selama di USU.
13. Kepada Fisika USU 2017 yang mengisi 4 tahun saya di Fisika.
14. Kepada Keluarga Besar Ikatan Mahasiswa Simalungun Universitas Sumatera Utara (IMAS-USU) yang sudah banyak membimbing saya hingga sampai saat ini sehingga saya bisa menjadi mahasiswa yang lebih bertanggung jawab.
Dan untuk seluruh orang-orang yang selalu mendoakan dan memberikan dukungan serta motivasi yang tidak dapat penulis sebutkan satu persatu. Penulis menyadari sepenuhnya bahwa dalam penyelesaian skripsi ini masih jauh dari sempurna, untuk itu kritik dan saran yang bersifat membangun sangat diharapkan dari para pembaca.
Medan, 18 Agustus 2021
Monika Klarizca Saragih
DAFTAR ISI
LEMBAR PENGESAHAN ... i
ABSTRAK ... ii
ABSTRACT ... iii
PENGHARGAAN ... iv
DAFTAR ISI ... vi
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR SINGKATAN ... x
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 2
1.3 Batasan Masalah ... 2
1.4 Tujuan Penelitian ... 2
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ...4
2.1 Besi (II,III) Oksida (Fe3O4) ...4
2.2 Amonium Hidroksida (NH4OH) ...5
2.3 Metode Kopresipitasi ...6
2.4X-Ray Diffraction Spectroscopy (XRD) ...7
2.5 Scanning Electron Microscopy(SEM) ...9
BAB III METODOLOGI PENELITIAN ...12
3.1 Tempat dan Waktu Penelitian ... 12
3.1.1 Tempat Penelitian ... 12
3.1.2 Waktu Penelitian ... 12
3.2 Peralatan dan Bahan Penelitian ... 12
3.2.1 Peralatan Penelitian ... 12
3.2.2 Bahan Penelitian ... 13
3.3 Prosedur Penelitian ... 13
3.4 DiagramAlir Penelitian... 15
BAB IVHasil dan Pembahasan ... 16
4.1 Analisis Hasil Karakterisasi Sintesis Fe3O4 ... 16
4.1.1 Sintesis Fe3O4melalui metode akaopresipitasi ... 16
a) Hasil XRD sampel V : 100 oC b) Hasil XRD sampel V : 125 oC c) Hasil XRD sampel V : 150 oC 4.2 Analisis Hasil Struktur Fe3O4 Menggunakan SEM ... 19
a) Hasil SEM Sampel Fe3O4 V : 100 oC ... 19
b) Hasil SEM Sampel Fe3O4 V : 125 oCError! Bookmark not defined.
c) Hasil SEM Sampel Fe3O4 V : 150oCError! Bookmark not defined.
BAB V KESIMPULAN DAN SARAN
5.1 Kesimpulan ... 22 5.2 Saran ... 22 DAFTAR PUSTAKA ... 23 LAMPIRAN
DAFTAR TABEL
Nomor Tabel
Judul 2.1 Sifat-Sifat Magnetit Fe3O4
2.2 Sifat-Sifat Magnetit NH4OH 3.1 Peralatan Sintesis Fe3O4
3.2 Peralatan Karakterisasi Fe3O4
DAFTAR GAMBAR
No. Judul Halaman
1 Struktur ikatan kimia Fe3O4 4
2 Prinsip kerja x-ray diffraction (XRD) 7
3 Grafik contoh analisis sampel dari uji XRD 7
4 Spektrum XRD Fe3O4 8
5 Sinyal karakteristik yang dihasilkan SEM 9
6 Skema Dasar SEM 9
7 Pola SEM Fe3O4 10
3.1 Diagram Alir Penelitian 14
4.1 Identifikasi XRD dari fasa yang terbentuk dalam sampel
yang dikalsinasi pada V:100oC 16
4.2 Identifikasi XRD dari fasa yang terbentuk dalam sampel
yang dikalsinasi pada V:125oC 17
4.3 Identifikasi XRD dari fasa yang terbentuk dalam sampel
yang dikalsinasi pada V:150oC 18
4.4 Hasil SEM Sampel sampel V : 100 oC 19
4.5 Hasil SEM Sampel sampel V : 125oC 20
4.6 Hasil SEM Sampel sampel V : 150 oC 21
DAFTAR SINGKATAN
FeCl3 : Iron (III) Oxyde
XRD : X-Ray Diffraction
SEM : Scanning Eletron Microscopy
LIPI : Lembaga Penelitian dan Ilmu Pengetahuan
NH4OH : Amonium hidroksida
Fe3O4 : Besi (II,III) Oksida (Fe3O4)
BAB I PENDAHULUAN
1.1 Latar Belakang Masalah
Teknologi nanopartikel akhir-akhir ini telah berkembang pesat untuk diaplikasikan dibidang industri.Teknologi ini telah membuat perubahan yang signifikan diberbagai kehidupan.Material magnetit telah menjadi material menarik yang dikembangkan karena sifatnya yang terkenal dan sangat potensial dalam aplikasinya di berbagai bidang. Aplikasi Fe3O4 diantaranya sebagai penyimpan informasi dengan densitas yang tinggi, pembentukan gambar dengan resonansi magnetit, sistem pengiriman untuk obat–obatan, kosmetik, pewarna, tinta serta berperan dalam berbagai proses pemisahan, termasuk adsorpsi. Selain itu juga digunakan untuk menghilangkan katalis, dan unsur-unsur beracun dari limbah industri sedangkan nanomagnetik film secara luas digunakan dalam perangkat listrik dan elektronik, sensor, penyimpanan digital yang memiliki kerapatan tinggi, dan melindungi elektromagnetit. Fe3O4 (magnetit), merupakan salah satu fase dari oksida besi yang bersifat amfoter dan memiliki daya serap yang tinggi (Nurdin Bukit, 2015 ; Suryani Taib, 2015).
Senyawa Fe3O4 terdiri dari FeO.Fe2O3, berwarna hitam dengan struktur berbentuk inversi spinel dan mengandung ion Fe2+ dan Fe3+. Senyawa Fe3O4, berwarna hitam dengan struktur berbentuk inversi spinel dan mengandung ion Fe2+ dan Fe3+(Pintor Simamora, 2015).
Sifat-sifat fisika dan kimia dari nanopartikel Fe3O4 sangat menarik dan memiliki potensi untuk diaplikasikan dalam berbagai bidang. Sifat-sifat fisika partikel Fe3O4 meliputi struktur kristal, sifat mekanik, optik, akustik, termodinamik, elektromagnetik, listrik, dan vibrasi. Sementara itu, sifat-sifat kimia Fe3O4 meliputi laju reaksi, ikatan kimia, dan stabilitas dalam reaksi kimia.Kemudian, partikel Fe3O4 juga mampu menunjukkan sifat biokompatibel ketika difungsionalisasi dengan polimer yang biokompatibel. Sifat-sifat fisika maupun kimia partikel Fe3O4 tersebut dipengaruhi oleh beberapa faktor, yaitu teknik sintesis, parameter sintesis, fungsionalisasi, dan perlakuan tambahan sintesis (Sholihah, 2010 ; Marlisa, 2017).
Fe3O4 memiliki aplikasi pada bidang industri seperti keramik, katalis, energy storage,magnetite data storage, ferofluida, maupun dalam diagnosis medis.
Partikel Fe3O4 biasanya di dapat dengan beberapa metode sintesis kimia, seperti, reverse micelle method, sintesis microwaveplasmateknik sol–gel, freeze drying, ultrasound irradiaton, metode hidrotermal, teknik pirolisis laser, metode kopresipitasi, dan lain–lain.
Dalam penelitian ini metode yang akan digunakan adalah metode kopresipitasi. Metode kopresipitasi merupakan proses kimia yang membawa suatu zat terlarut ke bawah sehingga terbentuk endapan yang dikehendaki. Teknik ini sering dipakai untuk memisahkan analitik dari pengotornya (Sholihah, 2010). Keunggulan dari metode kopresipitasi ialah dapat digunakan dengan mudah, bahan–bahan dan cara kerja yang digunakan juga lebih sederhana.
Selain itu, kelebihan dari metode ini adalah prosesnya menggunakan suhu rendah dan mudah
untuk mengontrol ukuran partikel sehingga waktu yang dibutuhkan relatif singkat (Nurjannah, 2018).
Karakterisasi hasil sintesis menggunakan alat X-Ray Diffraction (XRD), Scanning Electron Microscope (SEM).
1.2 Rumusan Masalah
Dalam penelitian ini dipaparkan beberapa perumusan masalah yang akan diselesaikan yaitu :
Bagaimana pembuatan Fe3O4 dengan metode kopresipitasi?
Bagaimana pengaruh Suhu terhadap Sintesis Fe3O4 dengan metode kopresipitasi ?
Bagaimana karakterisasiSEM, XRD terhadap Fe3O4 dengan metode kopresipitasi?
1.3 Batasan Masalah
Batasan masalah dalam penelitian ini adalah :
Suhu yang digunakan dalam proses sintering adalah 100 oC, 5 C 5 C
Asam yang digunakan untuk sintesis Fe3O4 adalah Amonium Hidroksida (NH4OH) 3,2M.
Karakterisasi Fe3O4 menggunakan SEM, dan XRD.
1.4 Tujuan Penelitian
Berdasarkan rumusan masalah diatas dapat ditentukan tujuan dari penelitian ini, yaitu:
Mengetahui pembuatan Fe3O4 dengan metode kopresipitasi.
Mengetahui pengaruh suhu terhadap sintesis Fe3O4 dengan metode kopresipitasi.
MengetahuikarakterisasiSEM, XRD terhadap Fe3O4 dengan metode kopresipitasi.
1.5 Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini adalah :
Degradasi dan penanganan air limbah methylene blue.
Untuk menangani air limbah (methylene blue) diperlukan partikel yang dapat mendegradasi dengan baik, diantaranya partikel Fe3O4(Besi Oksida)ialah salah satu partikel yang mampu mendegradasi air limbah dengan baik.
BAB II
TINJAUAN PUSTAKA
2.1 Besi (II,III) Oksida (Fe3O4)
Magnetit ialah senyawa kimia anorganik dengan rumus Fe3O4 yang mengandung baik ion Fe2+ maupun Fe3+ dan terkadang dirumuskan sebagai FeO.Fe2O3. Fe3O4 material nano yang mempunyai sifat magnetit yang banyak dipelajari karena memiliki bermacam-macam sifat kimia dan sifat fisik (Merdekani, 2013).Salah satu ciri magnetit yaitu berwarna hitam, bersifat non- toxic, biokompatibel, memiliki medan koersivitas yang tinggi dan dalam ukuran nanopartikel bersifat superparamagnetis. Sifat magnetit tersebut membuat magnetit dapat dimanfaatkan dalam banyak aplikasi (Firnando, 2015).
Partikel magnetit memiliki sifat fisis yang unik, salah satunya terkait dengan sifat kemagnetan yang dimiliki. Sifat magnetiknya sebagian besar dipengaruhi oleh morfologi, ukuran, karakteristik fisika dari partikel tunggal daninteraksi antarmuka. Selain itu luas permukaan partikel yang besar juga menjadi salah satu keunggulan partikel magnetik sehingga memiliki kapasitas besar untuk mengapsorpsi ion logam berat (Marlisa, 2017 ; Rahimah, 2019).
Tabel 2.1. Sifat-Sifat Magnetit Fe3O4 Sifat-Sifat Fe3O4
Kategori Mineral Oksida
Rumus Kimia Besi (II, III) Oksida
Warna Hitam
Sistim Kristal Isometrik, Heksoktahedral
Sifat Dalam Rapuh
Kelarutan Larut perlahan pada asam klorida
Kekerasan 5.5 – 6.5
[ Wei, Y, 2013]
Magnetit Fe3O4 merupakan oksida besi yang paling banyak ditemukan dan memiliki sifat kemagnetan yang paling kuat dibandingkan oksida-oksida besi lainnya (Wey, Y, 2013).
Gambar 2.1. Struktur ikatan kimia Fe3O4
Gambar 1 merupakan struktur ikatan kimia sel satuan dari mineral magnetit yang terdiri dari atom Fe3+, Fe2+, O2. Reaksi kimia dari magnetit ini adalah :
Fe3O4→FeO.Fe2O3………...(2.1)
Aplikasi partikel magnetit banyak digunakan untuk mengatasi masalah pencemaran lingkungan. Salah satunya sebagai absorben penyerapan logam berat. Aplikasi ini menarik
o
Fe Fe
o o o
Fe
perhatian besar karena lebih murah dari sisi biaya, lebih efisien waktu, mudah diproduksi serta mampu menanggulangi pencemaran air oleh logam berat. Untuk menghasilkan partikel yang efisien digunakan untuk menyerap logam maka dalam beberapa penilitian sering diteliti tentang karakteristik partikel kemudian dilanjutkan dengan aplikasi partikel magnetit Fe3O4 secara elektrokimia.Partikel yang dihasilkan selanjutnya dikarakterisasi dengan menggunakan difraktometer sinar-x (XRD) sehingga dapat diketahui serta mampu diidentifikasi fasanya (Marlisa, 2017).Suhu dan waktu reaksi mempengaruhi pertumbuhan kristal nonomagnetit dan kristalinitasnya. Semakin tinggi suhu, semakin cepat reaksi pembentukan magnetit. Semakin lama waktu reaksi, semakin meningkat ukuran kristal magnetit yang terbentuk. Serta semakin tinggi suhu reaksi dan bertambahnya waktu sintesis juga meningkatkan kristalinitas magnetit.Morfologi magnetit yang dihasilkan masih teraglomerasi dan partikelnya berukuran semakin besar seiring bertambahnya suhu dan waktu sintesis (Firnando, 2015).
2.2 Amonium Hidroksida (NH4OH)
Amonium hidroksida (NH4OH) adalah senyawa basa bentuk dari amonia (NH3) yang terionisasi dan terlarut dalam air.Amonia bereaksi secara reversibel dengan air menghasilkan ion amonium (NH4+) dan ion hidroksida (OH-). Amonia adalah senyawa kimia dengan rumus NH3 yang merupakan salah satu indikator pencemaran udara pada bentuk kebauan. Gas ammonia adalah gas yang tidak berwarna dengan bau menyengat, biasanya ammonia berasal dari aktifitas mikroba, industri ammonia, pengolahan limbah dan pengolahan batu bara. Amonia di atmosfer akan bereaksi dengan nitrat dan sulfat sehingga terbentuk garam ammonium yang sangat korosif (Cahyaninggalih, 2015 ; Amalia, 2015).
Tabel 2.2. Sifat-Sifat NH4OH Sifat-Sifat NH4OH
Massa jenis dan fase ( g/L ) 0,6942
Kelarutan dalam air ( gr/100 ml pada 00C) 89,9
Titik lebur ( 0C ) -77,73
Titik didih ( 0C ) -33,34
Keasaman ( PKa ) 9,25
Kebasaan (PKb) 4,75
[ Hari Gusti Firnando, 2015]
Larutan NH4OH dapat digunakan sebagai pengendap. Penggunaan NH4OH yang mengotori endapan dapat dihilangkan dengan jalan pemanasan. Hasil endapan yang terbentuk dipengaruhi oleh konsentrasi pelarut dan pengendap, suhu pemanasan, serta durasi pengadukan (Siti, 2016).
2.3 Metode Kopresipitasi
Kopresipitasi merupakan salah satu metode yang digunakan untuk membuat preparasi material nanopartikel. Metode kopresipitasi merupakan metode yang paling efektif karena metode ini dapat dilakukan pada kondisi lingkungan yang normal. Dalam sintesisnya metode ini
menggunakan pasangan asam dan basa. Asam berfungsi sebagai perlarut dan basa membawa zat terlarut kebawah sehingga terbentuk endapan yang dikehendaki. Sintesis nanopartikel magnetit dengan metode kopresipitasi diharapkan memiliki sifat monodispersif. Sifat monodispersif artinya partikel magnetit terdistribusi secara merata atau seragam. Prinsip kerja metode ini adalah dengan mengubah suatu garam logam menjadi endapan dengan menggunakan pengendap basa hidroksida atau karbonat yang kemudian diubah ke bentuk oksidanya dengan cara pemanasan (Nurjannah, 2016).Metode kopresipitasi merupakan salah satu metode sintesis senyawa organic yang didasarkan pada pengendapan lebih dari satu substansi secara bersama- sama ketika melewati titik jenuhnya. Kopresipitasi merupakan metode yang menjanjikan karena prosesnya menggunakan temperature rendah sehingga waktu yang dibutuhkan relatif lebih singkat, yaitu sekitar 12 jam (Susilo, 2016).Kopresipitasi merupakan proses kimia yang diawali dengan adanya zat terlarut yang mengendap sehingga menghasilkan endapan yang diinginkan.
Pengendapan terjadi sebagai akibat pembentukan kristal campuran.
Pembuatan Fe3O4 menggunakan metode kopresipitasi, yaitu melakukan transformasi fasa besi oksida dengan temperatur. Tujuan awal penggunaan metode kopresipitasi ini adalah untuk mempelajari sifat magnetit dalam struktur domain tunggal, tetapi dalam sintesis partikel nano magnetit difokuskan pada potensi aplikasi dan peningkatan kualitas dari partikel (Siti, 2016).
Prosedur yang sama juga digunakan untuk sintesis tipe ferit yang lain, seperti MnFe2O4 dan CoFe2O4, dengan mengubah prekusor yang digunakan. Pada umumnya metode kopresipitasi pada partikel Fe3O4 (ukuran kurang dari 20 nm) hanya difokuskan pada satu variabel atau dideskripsikan satu kondisi proses yang menghasilkan partikel dengan sifat-sifat tertentu (Merdekani, 2013).
Akan tetapi, metode ini memiliki beberapa kelemahan seperti tidak dapat berjalan dengan baik apabila menggunakan reaktan yang mempunyai kelarutan berbeda, proses ini tidak tepat untuk pembuatan material dengan tingkat kemurnian yang tinggi, selain itu metode ini tidak memiliki kondisi sintesis yang umum dalam pembentukan beberapa oksida logam (Cahyaninggalih, 2015).
2.4 X-Ray Difraction (XRD)
XRD pertama kali ditemukan oleh Max von Laue tahun 1913 dan pengembangannya dilakukan oleh Bragg. Difraksi sinar-x merupakan salah satu metode baku yang penting untuk mengkarakterisasi material. Sampai saat ini, metode difraksi sinar-x digunakan untuk mendapatkan informasi struktur Kristal material logam maupun paduan, mineral, polimer, material organik, dan superkonduktor (Suharyana, 2012).XRD memberikan data-data difraksi dan kuantisasi intensitas difraksi pada sudut dari suatu bahan.Data yang diperoleh dari XRD
berupa intensitas difraksi sinar-x yang terdifraksi dan sudutsudut θ Tiap pola yang muncul pada pola XRD mewakili satu bidang kristalyang memiliki orientasi tertentu (Widyawati, 2012).
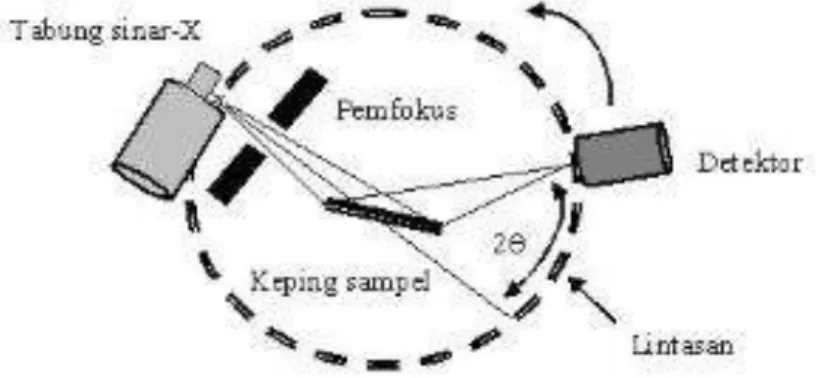
X-Ray Diffraction (XRD) merupakan salah satu metode karakteristik material yang paling tua dan paling sering digunakan hingga sekarang. Teknik ini digunakan untuk mengidentifikasi fasa kristalin dalam material dengan cara menentukan parameter struktur kisi serta untuk mendapatkan ukuran partikel. Bahan yang dianalisa adalah tanah halus, homogenized, dan rata- rata komposisi massal ditentukan (Ratnasari, 2009). Prinsip kerja X-Ray Diffraction (XRD) yang digunakan untuk menentukan struktur suatu padatan kristalin adalah dengan menggunakan metode difraksi sinar-x serbuk (X-raypowder diffraction) seperti terlihat pada gambar 2 berikut:
Gambar 2: Prinsip kerja x-ray diffraction (XRD) (Beiser, 1992).
Dari gambar di atas dapat dijelaskan bahwa, jika seberkas sinar-x ditembakkan pada sampel padatan kristalin, maka bidang kristal ini akan membiaskan sinar-x yang memiliki panjang gelombang yang sama dengan jarak kisi dalam kristal (yang memenuhi hukum Bragg).
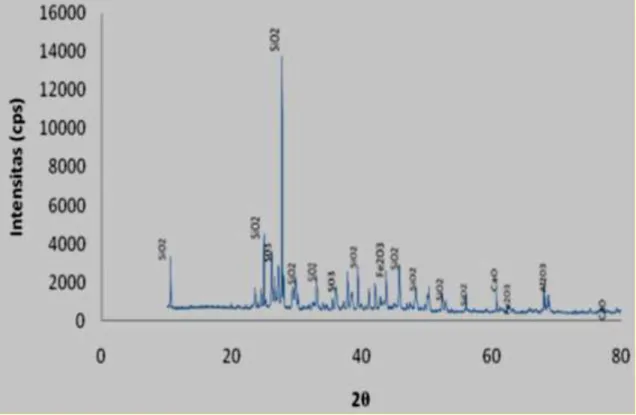
Kemudian sinar yang dibiaskan akan ditangkap oleh detektor, detektor kemudian akan mencatat puncak intensitas yang bersesuaian dengan orde pembiasan (orde-n) yang digunakan, yang kemudian akan ditampilkan dalam bentuk grafik yaitu grafik difraktogram yang merupakan grafik hubungan antara intensitas (cps) dengan 2, yang dapat dilihat pada grafik berikut:
Gambar 3. Grafik contoh analisis sampel dari uji XRD
Dari grafik di atas, besarnya intensitas relatif dari deretan puncak-puncak tersebut bergantung pada jumlah atom atau ion yang ada dalam sampel. Dimana semakin banyak bidang kristal yang terdapat dalam sampel, maka semakin kuat intensitas pembiasan yang dihasilkan.
Tiap puncak yang muncul pada pola XRD mewakili satu bidang kristal yang memiliki orientasi tertentu dalam sumbu tiga dimensi. Prinsip kerja XRD secara umum adalah XRD terdiri dari tiga bagian utama, yaitu tabung sinar-x, tempat objek yang diteliti dan detektor sinar-x.Sinar-x dihasilkan di tabung sinar-x yang berisi katoda memanaskan filamen, sehingga menghasilkan elektron. Perbedaan tegangan menyebabkan percepatan elektron akan menembaki objek. Ketika elektron mempunyai tingkat energi yang tinggi dan menabrak elektron dalam objek sehingga dihasilkan pancaran sinar-x.Objek dan detektor berputar untuk menangkap dan merekam intensitas refleksi sinar-x.Detektor merekam dan memproses sinyal sinar-x dan mengolahnya dalam bentuk grafik (Ratnasari, 2009).
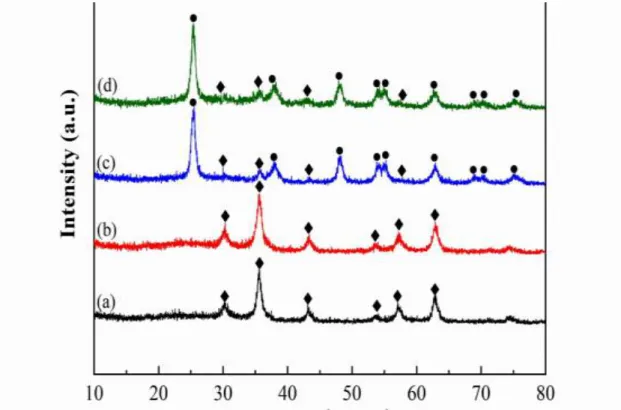
Gambar 4. Spektrum XRD Fe3O4 (a) (Havancsak, 2016)
Seperti yang ditunjukkan pada Gambar 4 (a), puncak difraksi karakteristik muncul pada 30,0, 35.3, 43.0, 53.5, 56.9 dan 62.8, sesuai dengan (220), (311), (400), (422), (511) dan (440) bidang kristal (JCPDS No.26 - 1136), mereka termasuk dalam puncak karakteristik difraksi Fe3O4.
2.5 Sistem Kristal Cubic
Struktur kristal merupakan susunan atom-atom, ion atau molekul di dalam suatu material.
Struktur kristal dibagi menjadi lebih kecil lagi yang disebut dengan unit cell. Sedangkan unit cell merupakan kelompok partikel terkecil di dalam material yang membentuk pola berulang dalam sumbu x, y, z. Panjang lengan sumbu x, y, z pada unit cell disebut dengan konstanta kisi (a) (Hook & Hall, 2010).
a. Simple cubic
Struktur kristal simple cubic merupakan unit cell yang terdiri dari satu atom yang terbagi di delapan sudut kubus seperti yang ditunjukkan pada gambar 2.1 dibawah ini. Oleh karena itu, sel satuan simple cubic mengandung total satu atom (1/8 × 8).
Gambar 5 Konfigurasi stuktur kristal simple cubic (Mayer, 2007) b. Body-centered cubic
Pada gambar 6 di bawah ini menunjukkan konfigurasi struktur kristal body centered- cubic yang terdiri dari satu atom yang berada di tengah kubus dan 1/8 atom terletak di delapan sudut kubus. Struktur kristal body centered-cubic ini memiliki total bersih 2 atom per unit cell (1/8 × 8 +1).
Gambar 6 Konfigurasi struktur kristal body-centered cubic (Mayer, 2007) c. Face-centered cubic
Gambar 7 Konfigurasi struktur kristal face-centered cubic (Mayer, 2007)
Gambar 7 diatas menunjukan konfigurasi struktur kristal face-centered cubic yang terdiri dari ½ atom yang terletak disetiap sisi kubus dan 1 atom yang terbagi di 8 sudut kubus. Jumlah seluruh atom pada struktur face-centered cubic adalah 4 atom.
2.5 Scanning Electron Microscope (SEM)
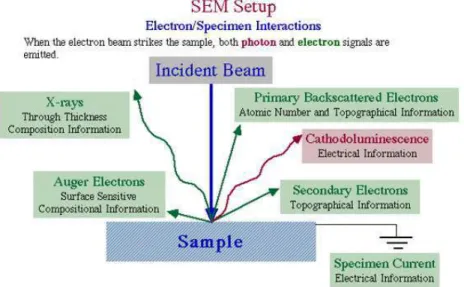
Mikroskop pemindaian elektron (Scanning Electron Microscope) adalah jenis mikroskop electron yang mencitrakan permukaan sampel oleh pemindaian dengan pancaran tinggi elektron.Elektron yang berinteraksi dengan atom yang membentuk sampel menghasilkan sinyal yang berisi informasi tentang sampel dari permukaan topografi, komposisi dan sifat lainnya seperti daya konduksi listrik. SEM terdiri dari seberkas electron yang memindai permukaan sampel yang akan dianalisis dimana sebagai tanggapan, kembali memancarkan partikel tertentu.
Partikel dianalisis oleh detektor yang berbeda yang memungkinkan untuk merekonstuksi tiga dimensi dari permukaan.SEM digunakan untuk mengetahui morfologi permukaan suatu bahan.Karakteristik bahan menggunakan SEM dimanfaatkan untuk melihat struktur topografi permukaan, ukuran butir, cacat struktural, dan komposisi pencemaran suatu bahan.Hasil yang diperoleh berupa scanning electron macrograph yang menyajikan bentuk tiga dimensi berupa gambar atau foto. Ada beberapa sinyal penting yang dihasilkan oleh SEM. Dari pantulan inelastis didapatkan sinyal elektron sekunder dan karakteristik sinar x sedangkan dari pantulan elastis didapatkan sinyal backscattered electron. Sinyal -sinyal tersebut dijelaskan pada gambar di bawah ini.
Gambar 5.Sinyal karakteristik yang dihasilkan SEM (Goldstein et al, 2007).
Gambar 5 menunjukkan bahwa elektron sekunder menghasilkan topografi dari benda yang dianalisa dengan permukaan yang tinggi berwarna lebih cerah dari permukaan rendah.
Sedangkan primary backscattered elektron memberikan perbedaan berat molekul dari atom-atom yang menyusun permukaan. Atom dengan berat molekul tinggi akan berwarna lebih cerah daripada atom dengan berat molekul rendah (Goldstein et al, 2007). Skema dasar SEM disajikan pada gambar 6.
Gambar 6.Skema dasar SEM (Havancsak, 2016)
Elektron sekunder adalah elektron yang dipancarkan dari permukaan kulit atom terluar yang dihasilkan dari interaksi berkas elektron jatuh dengan padatan sehingga mengakibatkan terjadinya loncatan elektron yang terikat lemah dari pita konduksi. Elektron Auger adalah elektron dari kulit orbit terluar yang dikeluarkan dari atom ketika elektron tersebut menyerap energi yang dilepaskan oleh elektron lain yang jatuh ke tingkat energi yang lebih rendah. Apabila berkas elektron mengenai sampel padat maka sebagian berkas yang jatuh tersebut akan dihamburkan kembali dan sebagian lagi akan menembus sampel.
Untuk sampel yang tipis maka sebagian besar elektron akan diteruskan, beberapa elektron akan dihamburkan secara elastis tanpa kehilangan energi dan sebagian lagi akan dihamburkan secara tak elastis. Teknik ini juga dapat dimanfaatkan untuk mengamati unsur-unsur pada daerah kecil permukaan bahan secara kualitatif dan semi kuantitatif.Hal ini karena masing-masing unsur menyebar pada panjang gelombang spesifik.
Gambar 7. Pola SEM Fe3O4
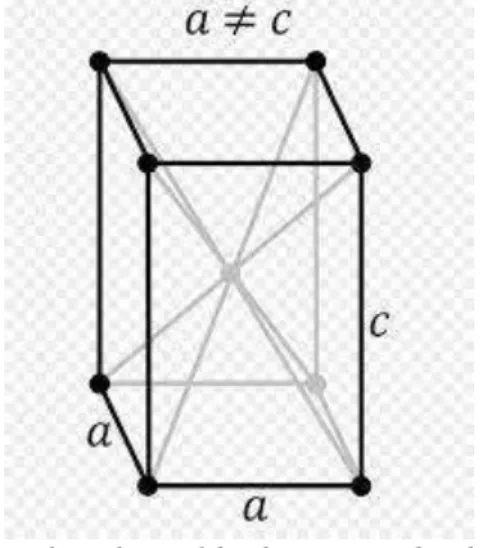
Gambar 7 menunjukkan bahwa partikel Fe3O4 memiliki bentuk tetragonal struktur, Ukuran partikel sekitar 400nn dan terdistribusi merata.
Prinsip kerja dari SEM berupa suatu sumber elektron dari filamen yang terbuat dari tungsten memancarkan berkas elektron.Tungsten biasanya digunakan pada elektron gun karena memiliki titik lebur tertinggi dan tekanan uap terendah dari semua logamsehingga memungkinkan dipanaskan untuk emisi elektron. Berkas electrondifokuskan oleh satu atau dua lensa kondensor ke titik yang diameternya sekitar0,4 nm sampai 5 nm. Permukaan bahan yang dikenai berkas elektron akanmemantulkan kembali berkas tersebut atau menghasilkan elektron sekunder kesegala arah arah. Scanning pada permukaan bahan yang dikehendaki dapat dilakukan dengan mengatur scanning generator dan scanning coils. Elektron sekunder hasil interaksi antara elektron dengan permukaan spesimen ditangkap oleh detektor secondary electron (SE) yang kemudian diolah dan diperkuat oleh amplifier dan kemudian divisualisasikan dalam monitor sinar katoda (Havancsak, 2016).
BAB III
METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian
3.1.1 Tempat Penelitian
1. Laboratorium Ilmu Dasar dan Umum Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara (USU) Medan, untuk sintesis dan karakterisasi Fe3O4. 2. Laboratorium Pusat Survey Geologi Bandung, untuk pengujian/karakterisasi sampel.
3. Laboratorium Terpadu Universitas Sumatera Utara, untuk pengujian/karakterisasi sampel.
3.1.2 Waktu Penelitian
Penelitian ini dilaksanakan pada bulan Januari 2021 sampai dengan bulan Juli 2021.
3.2 Alat dan Bahan Penelitian 3.2.1 Alat
Alat-alat yang digunakan padapenelitian ini adalah:
Tabel 3.1 Peralatan Sintesis Fe3O4
No Nama Alat Fungsi
1 Neraca Analitik Untuk menimbang massa sejumlah bahan kimia 2 Gelas ukur Untuk mengukur volume dari bahan baku 3 Spatula Untuk mengambil bahan
4 Cawan Mortar Untuk menggerussampel yang sudah dikeringkan sehingga berbentuk serbuk
5 Oven Untuk memanaskan sampel
6 Magnetic stirrer Untuk mengaduk larutan campuran agar terjadi homogenisasi.
7 Kertas timbang Untuk tempat bahan ketika ditimbang
8 Gelas beaker Untuk wadah penampung yang digunakan untuk mengaduk, mencampur, dan memanaskan cairan yang biasanya digunakan dalam laboratorium.
9 Sarung tangan Untuk melindungi tangan dari bahan kimia 10 Masker mulut Untuk melindungi mulut dari bahan kimia 11 Tissue Untuk membersihkan peralatan
12 Magnetic Bar Untuk pengaduk larutan campuran pada magnetic stirrer 13 Alumunium foil Untuk menutupi larutan
14 Pipet Tetes Untuk memindahkan larutan dari suatu wadah ke wadah lain 15 Cawan Porselin Sebagai wadah untuk memanaskan sampel
16 Lemari Asam Sebagai tempat reaksi kimia yang menggunakan bahan-bahan yang mudah menguap atau gas yang berbahaya
Tabel 3.2 Peralatan Karakterisasi Fe3O4 No Nama Alat Fungsi 1 X-Ray Difraction
(XRD)
Untuk mengetahui mikrostruktur dari sampel 2 Scanning
Electron Microscopy (SEM)
Untuk menganalisa morfologi nanopartikel sampel
3.2.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah
Besi (II,III) Oksida (Fe3O4) (ID Merck : 637106-100G)
Prekursor FeCl2.4H2O (ID Merck : 1.03861.0250)
Prekursor FeCl3.6H2O (ID Merck : 1.00731.1000)
NH4OH (3.2 M) (ID Merck : A-1011.1336.216)
Etanol
Aquabides 3.3 Prosedur Percobaan
3.3.1 Sintesis dan karakterisasi Fe3O4 dengan metode kopresipitasi dengan suhu 100oC, 125oC, 150oC.
Dilakukan penimbangan FeCl3.6H2O sebanyak 5,2001 gr dan FeCl2.4H2O sebanyak 2,0002 gr. Kemudian penambahan Aquabides sebanyak 80ml dan dilakukan proses pengadukan menggunakan hotplate dan magnetit stirrer dengan t = 1 jam. Kemudian, penambahan larutan NH4OH (3,2 M) sebanyak 20 ml. Dilakukan pengadukan dengan t = 1 jam untuk menyempurnakan reaksi. Kemudian pencucian endapan menggunakan Etanol dengan V = 10ml selama t = 20 menit dan 10 ml Aquabides denganV = 10ml selama t = 20 menit. Setelah proses pencucian selesai, terjadi proses pemisahan larutan dari magnetit tersebut dan larutan dimasukkan ke dalam wadah untuk dilakukan proses pemanasan bahan. Kemudian dilakukan proses Kalsinasi / oven dengan T = 100oC, 125o, 150oC dengan T = 6 jam. Setelah bahan tersebut sudah kering, dilakukan proses penggerusan menggunakan mortar dengan t = 1 jam.
Penggerusan dilakukan dengan tujuan untuk menghasilkan sifat magnet pada sampel tersebut dan dapat diuji langsung. Kemudian untuk karakterisasi dilakukan dengan uji X-Ray Difraction (XRD), SEM.
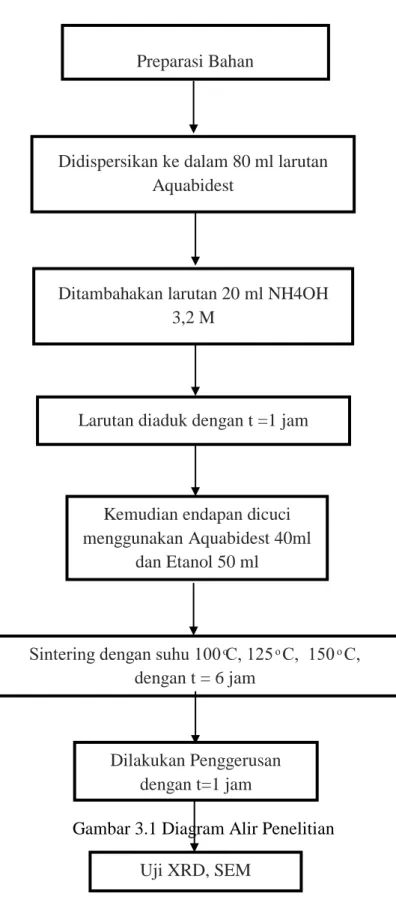
Gambar 3.1 Diagram Alir Penelitian Preparasi Bahan
Didispersikan ke dalam 80 ml larutan Aquabidest
Ditambahakan larutan 20 ml NH4OH 3,2 M
Larutan diaduk dengan t =1 jam
Kemudian endapan dicuci menggunakan Aquabidest 40ml
dan Etanol 50 ml
inte ing dengan su u C 5 C 5 C dengan t = 6 jam
Dilakukan Penggerusan dengan t=1 jam
Uji XRD, SEM
Diagram Alir Penelitian
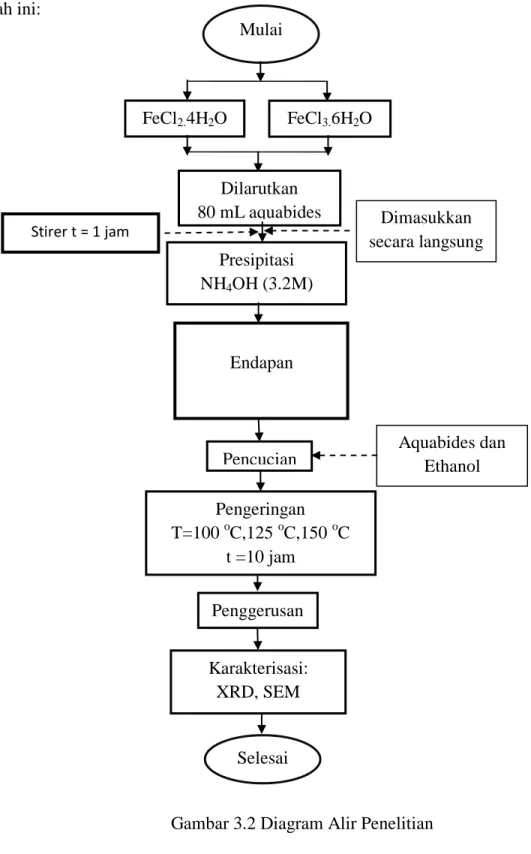
Alur proses kerja yang dilakukan dalam penelitian ini ditunjukkan oleh diagram alir dibawah ini:
ss
Gambar 3.2 Diagram Alir Penelitian Mulai
Presipitasi NH4OH (3.2M)
Dilarutkan 80 mL aquabides
FeCl3.6H2O FeCl2.4H2O
Pengeringan T=100 oC,125 oC,150 oC
t =10 jam Pencucian
Selesai Penggerusan
Karakterisasi:
XRD, SEM
Dimasukkan secara langsung
Aquabides dan Ethanol Stirer t = 1 jam
Endapan
BAB 4
HASIL DAN PEMBAHASAN 4.1 Analisis Hasil Karakterisasi Sintesis Fe3O4
4.1.1 Sintesis Fe3O4 melalui Metode Kopresipitasi a.Hasil XRD sampel V : 100 oC
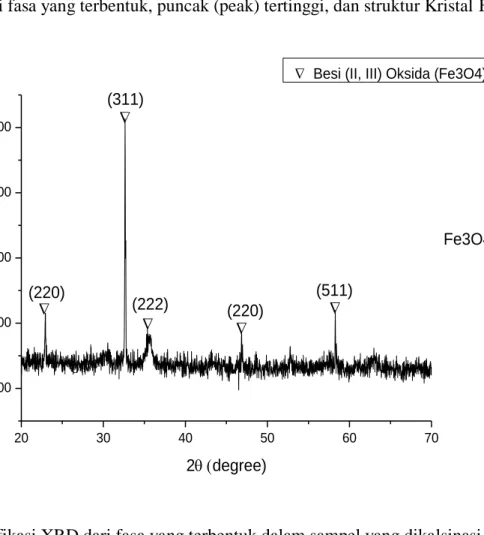
Pola-pola difraksi yang merupakan puncak-puncak karakteristik dari suatu sampel dilakukan pengujian X-Ray Diffraction (XRD). Pengujian XRD dilakukan untuk mengetahui fasa yang terbentuk, puncak (peak) tertinggi, dan struktur Kristal Fe3O4
Gambar 4.1 Identifikasi XRD dari fasa yang terbentuk dalam sampel yang dikalsinasi pada V:
100oC
Pola XRD dari sampel ditunjukkan pada Gambar 4.1. Hasil karakterisasi XRD menunjukkan bahwa sampel Fe3O4mengkristal baik dengan puncak-puncak utama pada daerah 2ϴ sekitar 32,65ᵒ yang merupakan puncak bidang (311) diperkuat dengan kemunculan puncak- puncak lain, yaitu pada bidang (311), (511), (220), (222) hasil menunjukkan kesesuaian dengan standard Join Committee on Powder Difraction Standard (JCPDS 04-002-3668) dimana, puncak-puncak lain yang teridentifikasi dalam sampel secara berturut-turut adalah pada bidang (222), (220), (311), (400), (422), (155), (511), (440). Pada penelitian ini terbentuk struktur kristal Cubic yang ditunjukkan pada hasil pengolahan data XRD menggunakan aplikasi Match.
20 30 40 50 60 70
200 400 600 800 1000
(222)
Fe3O4
(220) (511)
(311)
Intensity(cps)
2(degree)
Besi (II, III) Oksida (Fe3O4)
(220)
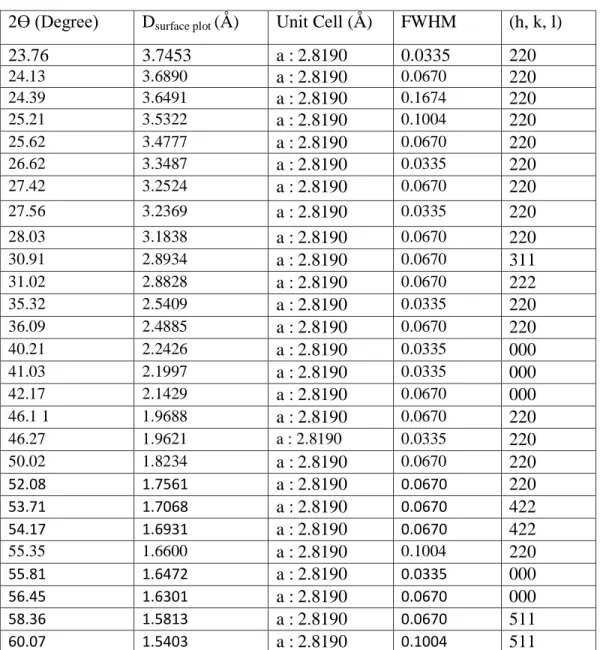
Tabel 4.1 Pe gese an θ (deg ee) sampel Fe3O4 dengan suhu 100oC
Ө (Deg ee) Dsurface plot (Å) Unit Cell (Å) FWHM (h, k, l)
23.76 3.7453 a : 2.8190 0.0335 220
24.13 3.6890 a : 2.8190 0.0670 220
24.39 3.6491 a : 2.8190 0.1674 220
25.21 3.5322 a : 2.8190 0.1004 220
25.62 3.4777 a : 2.8190 0.0670 220
26.62 3.3487 a : 2.8190 0.0335 220
27.42 3.2524 a : 2.8190 0.0670 220
27.56 3.2369 a : 2.8190 0.0335 220
28.03 3.1838 a : 2.8190 0.0670 220
30.91 2.8934 a : 2.8190 0.0670 311
31.02 2.8828 a : 2.8190 0.0670 222
35.32 2.5409 a : 2.8190 0.0335 220
36.09 2.4885 a : 2.8190 0.0670 220
40.21 2.2426 a : 2.8190 0.0335 000
41.03 2.1997 a : 2.8190 0.0335 000
42.17 2.1429 a : 2.8190 0.0670 000
46.1 1 1.9688 a : 2.8190 0.0670 220
46.27 1.9621 a : 2.8190 0.0335 220
50.02 1.8234 a : 2.8190 0.0670 220
52.08 1.7561 a : 2.8190 0.0670 220
53.71 1.7068 a : 2.8190 0.0670 422
54.17 1.6931 a : 2.8190 0.0670 422
55.35 1.6600 a : 2.8190 0.1004 220
55.81 1.6472 a : 2.8190 0.0335 000
56.45 1.6301 a : 2.8190 0.0670 000
58.36 1.5813 a : 2.8190 0.0670 511
60.07 1.5403 a : 2.8190 0.1004 511
b. Hasil XRD sampel V : 125oC
Berdasarkan hasil pengamatan XRD diperoleh grafik, kemudian dilakukan untuk mengetahui fasa dan hkl. Data yang dihasilkan akan disesuaikan dengan Join Committee on Powder Difraction Standarduntuk mengidentifikasi kandungan senyawa dari sampelFe3O4
Gambar 4.2 Identifikasi XRD dari fasa yang terbentuk dalam sampel dikalsinasi pada V : 125oC Pola XRD dari sampel ditunjukkan pada Gambar 4.2. Hasil karakterisasi XRD menunjukkan bahwa sampel Fe3O4mengkristal baik dengan puncak-puncak utama pada daerah 2ϴ sekitar 32,07ᵒ yang merupakan puncak bidang (311) diperkuat dengan kemunculan puncak- puncak lain, yaitu pada bidang (400), (422), (511), (220) hasil menunjukkan kesesuaian dengan standard Join Committee on Powder Difraction Standard (JCPDS 04-002-3668) dimana, puncak-puncak lain yang teridentifikasi dalam sampel secara berturut-turut adalah pada bidang (222), (220), (311), (400), (422), (155), (511), (440). Pada penelitian ini terbentuk struktur kristal Cubic yang ditunjukkan pada hasil pengolahan data XRD menggunakan aplikasi Match.
20 30 40 50 60 70
0 500 1000 1500 2000 2500
(311)
Fe3O4
(511) (400)
(422)
Intensity(cps)
2 (degree)
Besi (II, III) Oksida (Fe3O4)
(220)
Tabel 4.2 Pe gese an θ (deg ee) sampel Fe3O4 dengan suhu 125oC
Ө (Deg ee) Dsurface plot (Å) Unit Cell (Å) FWHM (h, k, l)
23.76 3.7453 a : 2.8190 0.0335 220
24.13 3.6890 a : 2.8190 0.0670 220
24.39 3.6491 a : 2.8190 0.1674 220
25.21 3.5322 a : 2.8190 0.1004 220
25.62 3.4777 a : 2.8190 0.0670 220
26.62 3.3487 a : 2.8190 0.0335 220
27.42 3.2524 a : 2.8190 0.0670 220
27.56 3.2369 a : 2.8190 0.0335 220
28.03 3.1838 a : 2.8190 0.0670 220
30.91 2.8934 a : 2.8190 0.0670 311
31.02 2.8828 a : 2.8190 0.0670 222
35.32 2.5409 a : 2.8190 0.0335 220
36.09 2.4885 a : 2.8190 0.0670 220
40.21 2.2426 a : 2.8190 0.0335 000
41.03 2.1997 a : 2.8190 0.0335 000
42.17 2.1429 a : 2.8190 0.0670 000
46.1 1 1.9688 a : 2.8190 0.0670 220
46.27 1.9621 a : 2.8190 0.0335 220
50.02 1.8234 a : 2.8190 0.0670 220
52.08 1.7561 a : 2.8190 0.0670 220
53.71 1.7068 a : 2.8190 0.0670 422
54.17 1.6931 a : 2.8190 0.0670 422
55.35 1.6600 a : 2.8190 0.1004 220
55.81 1.6472 a : 2.8190 0.0335 000
56.45 1.6301 a : 2.8190 0.0670 000
58.36 1.5813 a : 2.8190 0.0670 511
60.07 1.5403 a : 2.8190 0.1004 511
c. Hasil XRD sampel V : 150oC
Berdasarkan hasil pengamatan XRD diperoleh grafik, kemudian dilakukan untuk mengetahui fasa dan hkl. Data yang dihasilkan akan disesuaikan dengan Join Committee on Powder Difraction Standarduntuk mengidentifikasi kandungan senyawa dari sampelFe3O4
Gambar 4.3 Identifikasi XRD dari fasa yang terbentuk dalamsampel yang dikalsinasi pada V : 150oC
Pola XRD dari sampel ditunjukkan pada Gambar 4.3. Hasil karakterisasi XRD menunjukkan bahwa sampel Fe3O4mengkristal baik dengan puncak-puncak utama pada daerah 2ϴ sekitar 34,52ᵒ yang merupakan puncak bidang (311) diperkuat dengan kemunculan puncak- puncak lain, yaitu pada bidang (400), (422), (511) hasil menunjukkan kesesuaian dengan standard Join Committee on Powder Difraction Standard (JCPDS 04-002-3668) dimana, puncak-puncak lain yang teridentifikasi dalam sampel secara berturut-turut adalah pada bidang (222), (220), (311), (400), (422), (511), (440). Pada penelitian ini terbentuk struktur kristal Cubic yang ditunjukkan pada hasil pengolahan data XRD menggunakan aplikasi Match.
20 30 40 50 60 70
200 400 600 800 1000 1200 1400 1600
(400)
(220) (511)
(422)
Fe3O4
Intensity (cps)
2 (degree)
Besi (II, III) Oksida (Fe3O4) (311)
Tabel 4.3 Pe gese an θ (deg ee) sampel Fe3O4 dengan suhu 150oC
Ө (Deg ee) Dsurface plot (Å) Unit Cell (Å) FWHM (h, k, l)
23.76 3.7453 a : 2.8190 0.0335 220
24.13 3.6890 a : 2.8190 0.0670 220
24.39 3.6491 a : 2.8190 0.1674 220
25.21 3.5322 a : 2.8190 0.1004 220
25.62 3.4777 a : 2.8190 0.0670 220
26.62 3.3487 a : 2.8190 0.0335 220
27.42 3.2524 a : 2.8190 0.0670 220
27.56 3.2369 a : 2.8190 0.0335 220
28.03 3.1838 a : 2.8190 0.0670 220
30.91 2.8934 a : 2.8190 0.0670 311
31.02 2.8828 a : 2.8190 0.0670 222
35.32 2.5409 a : 2.8190 0.0335 220
36.09 2.4885 a : 2.8190 0.0670 220
40.21 2.2426 a : 2.8190 0.0335 000
41.03 2.1997 a : 2.8190 0.0335 000
42.17 2.1429 a : 2.8190 0.0670 000
46.1 1 1.9688 a : 2.8190 0.0670 220
46.27 1.9621 a : 2.8190 0.0335 220
50.02 1.8234 a : 2.8190 0.0670 220
52.08 1.7561 a : 2.8190 0.0670 220
53.71 1.7068 a : 2.8190 0.0670 422
54.17 1.6931 a : 2.8190 0.0670 422
55.35 1.6600 a : 2.8190 0.1004 220
55.81 1.6472 a : 2.8190 0.0335 000
56.45 1.6301 a : 2.8190 0.0670 000
58.36 1.5813 a : 2.8190 0.0670 511
60.07 1.5403 a : 2.8190 0.1004 511
4.2 Hasil Analisis Struktur Menggunakan SEM (Scanning Electron Microscopy) a. Hasil SEM Sampel Fe3O4dengan V : 100oC
Scanning Electron Microscope merupakan jenis mikroskop electron yang mencitrakan permukaan sampel oleh pemindaian dengan pancaran tinggi electron, SEM dimanfaatkan untuk melihat struktur topografi permukaan, ukuran butir, cacat struktural, dan komposisi pencemaran suatu bahan.
(a) (b)
Gambar 4.4 (a) Hasil SEM Sampel sampel V : 100 oC Perbesaran 500x (b) Hasil SEM Sampel A1 Perbesaran 5000x
Scanning Electron Microscopy (SEM) dilakukan untuk mengetahui mikrostruktur permukaan sampel yang dihasilkan. Sampelyang dikalsinasi denganV : 100 oC dianalisis menggunakan SEM dengan perbesaran 500 kali dan 5000 kali, masing-masing ditunjukkan pada gambar 4.4 (a) dan (b). Dari hasil analisis menunjukkan bahwa sampel V : 100 oC tidak homogen yang ditunjukkan oleh adanya celah pada permukaan sampel. Hal ini disebabkan oleh waktu penggerusan sampel yang terlalu singkat yang mengakibatkan adanya jarak antar partikel, sehingga persebaran partikel sampel tidak merata dan permukaan sampel tidak homogen.
X500 200um X5000 20um
b. Hasil SEM sampel Fe3O4 V : 125 oC
(a) (b)
Gambar 4.5 (a) Hasil SEM Sampel V : 125 oC Perbesaran 500x (b) Hasil SEM Sampel V : 125 oC Perbesaran 5000x
Scanning Electron Microscopy (SEM) dilakukan untuk mengetahui mikrostruktur permukaan sampel yang dihasilkan. Sampel V : 125oC dianalisis menggunakan SEM dengan perbesaran 500 kali dan 5000 kali, masing-masing ditunjukkan pada gambar 4.5 (a) dan (b). Dari hasil analisis menunjukkan bahwa sampel dengan suhu V : 125oC tidak homogen yang ditunjukkan oleh adanya celah pada permukaan sampel. Hal ini disebabkan oleh waktu penggerusan sampel yang terlalu singkat yang mengakibatkan adanya jarak antar partikel, sehingga persebaran partikel sampel tidak merata dan permukaan sampel tidak homogen.
X500 200um X5000 20um
c. Hasil SEM Sampel Fe3O4 V : 150oC
(a) (b)
Gambar 4.6 (a) Hasil SEM Sampel V : 150oC Perbesaran 500x (b) Hasil SEM Sampel V : 150oC Perbesaran 5000x
Scanning Electron Microscopy (SEM) dilakukan untuk mengetahui mikrostruktur permukaan sampel yang dihasilkan. Sampel dengan suhu kalsinasi V : 150oC dianalisis menggunakan SEM dengan perbesaran 500 kali dan 5000 kali, masing-masing ditunjukkan pada gambar 4.6 (a) dan (b). Dari hasil analisis menunjukkan bahwa sampel dengan V : 150oC tidak homogen yang ditunjukkan oleh adanya celah pada permukaan sampel. Hal ini disebabkan oleh waktu penggerusan sampel yang terlalu singkat yang mengakibatkan adanya jarak antar partikel, sehingga persebaran partikel sampel tidak merata dan permukaan sampel tidak homogen.
X500 200um X500020um
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian dan pembahasan yang telah dilakukan, dapat diperoleh kesimpulan sebagai berikut :
1. Sintesis Fe3O4telah berhasil dilakukan dengan dengan metode kopresipitasi.
2. Pengaruh variasi suhu pada sintesis Fe3O4menunjukkan bahwa semakin tinggi suhu yang digunakan tidak mempengaruhi srtuktur partikel tetapi berpengaruh terhadap sifat magnet.
3. Karakterisasi sampel yang dihasilkan bergantung dengan senyawa yang terbentuk, struktur kristal dan puncak (peak) tertinggi yaitu :
a. Hasil identifikasi sampel menggunakan X-Ray Difraction (XRD) menunjukkan bahwa sampel mengkristal baik dengan puncak-puncak utama pada daerah 2ϴ sekitar 32,65ᵒ, 32,07ᵒdan 32,67ᵒ dengan puncak bidang (311).
b. Dari hasil karakterisasi sampel menggunakan Scanning Electron Microscopy (SEM) menunjukkan bahwa sampel tidak homogen yang ditunjukkan oleh adanya celah dan penggumpalan partikel pada permukaan sampel.
5.2 Saran
1. Untuk pengembangan penelitian ini, sebaiknya melakukan penelitian dengan mengunakan bahan dengan timbangan yang sesuai agar menghasilkan hasil yang baik
2. Untuk penelitian berikutnya sebaiknya proses penggerusan dilakukan lebih lama agar hasil tidakhomogen.
3. Untuk penelitian berikutnya sebaiknya suhu kalsinasi lebih di perhatikan agar tidak mempengaruhi sifat magnet yang di hasilkan
DAFTAR PUSTAKA
Amalia Putri Lubis. 2015. Interaksi MolekulerAmonium Hidroksida. FMIPA, State University of Padang. Padang
Ariswan.(2016). Kuliah Scanning Electron Microscope. Yogykarta: FMIPA UNY.
Asadina Kusma Cahyaninggalih. Recovery Amonium Hidroksida (NH4OH) Dari Limbah Regenerasi Mengandung (NH4)2SO4 Dengan Menggunakan Distilasi Vakum.
Politeknik Perkapalan Negeri Surabaya, Surabaya.
B akti Henny Dwi dkk “Penga u uku an Pa tikel Fe3O4 da i pasi Besi ebagai Bahan Penyerap Pada Frekuensi X-Band dan Ku-Band” Fisika : Jakarta.
Beiser, Arthur. 1992. Modernt Technical Physics. Malang.
Goldstein, Joseph.,et al. (2007). Scanning Electron Microscopy and X-Ray Microanalysis: Third Edition. USA. Springer.
Hari Gusti Firnando. 2015. Pengaruh suhu pada proses sonikasi terhadap morfologi partikel dan kristalinitas nanopartikel Fe3O4. Unand, Padang.
Havancsak, Kalory. (2016). High-Retolution Scanning Electron Microscopy
http://www.technoorg.hu/news-and- events/articles/highresolutionscanning-electron- microscopy-1/ diunduh pada tanggal 6 Desember 2017.
Lia Kurnia Sholihah. 2010. Sintesis dan Karakterisasi Partikel Nano Fe3O4 yang Berasal dari Pasir Besi dan Fe3O4 Bahan Komersial (Aldrich). Institut Teknologi Sepuluh November, Surabaya.
Lisa Marlisa. 2017. Uji Karakterisasi Nanopartikel Magnetit Fe3O4 Menggunakan X- RAY Diffraction Dan Scanning Electron Microscopy.Universitas Islam
Alauddin. Makassar
Mathews N.R., Erik R., Cortes M.A., Toledo J.A. 2009. TiO2 thin films influence of annealing temperature on structural, optical and photocatalytic properties.
Programa de ingenieria Molecular IMP.Mexico D.F.C.P 07730.
Merdekani, Sera. 2013. Sintesis Partikel Nanokomposit Fe3O4/SiO2 Dengan Metode Kopresipitasi. BATAN Bandung.
Nurdin Bukit, Erna Frida, Pintor Simamora, Tresia Sinaga. 2015. Analisis Difraksi Nanopartikel Fe3O4 Metode Kopresipitasi Dengan Polietilen Glikol 6000.
Fakultas MIPA, Universitas Negeri Jakarta.
Nurhidayah.2016. Karakteristik Material Pasir Besi Dengan Menggunakan X-Ray Diffraction (XRD).UIN : Makasar.
Nurjannah, Siti. 2018. Sintesis Dan Karakterisasi Nanopartikel Magnetik Fe3O4
Pasir Besi Glagah Kulon Progo Dengan Metode Kopresipitasi. Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta.
Yogyakarta.
Pintor Simamora, Krisna. 2015. Sintesis Dan Karakterisasi Sifat Magnetik Nanokomposit Fe3o4 – Montmorilonit Berdasarkan Variasi Suhu. Universitas Negeri Jakarta.
Rahimah. 2019. Synthesis and Characterization Nanomagnetite by Coprecipitation.
Science and Tegnology, Medan.
Ratnasa i Dina dkk 9 “X-Ray Diffraction (XRD)”. Tugas Kimia Fisika. (2009):
h. 2-3. http:// kimia.ft.uns.ac.id/ file/ kuliah/ kimia%20Fisika/.../XRD% 20III.
ania dkk 4 “Ka akte istik dan Kandungan Mine al Pasi Pantai L ok Mee Beureunut dan Leunga Kabupaten Ace Besa ” Mate ial
Siti, W., W. Ari, S. Winatapura. 2016. The SiO2 addition effect to Fe3O4/TiO2
photocatalytic characteristic and performance on methylene blue degradation.
Pusat sains dan teknologi bahan maju, BATAN. Gedung 42, puspiptek Serpong, Tangerang Selatan.
Suharyana.(2012). Dasar-Dasar dan Pemanfaatan Metode Difraksi Sinar-X. Surakarta:
Universitas Sebelas Maret.
Suryani Taib. 2015. Sintesis Nanopartikel Magnetite (Fe3O4) dengan Template Silika (SiO2) dan Karakterisasi Sifat Kemagnetannya. Fakultas MIPA, Universitas Gadjah Mada. Yogyakarta
Wei Y., Han B., Xiaoyang H., Lin Y., Wang X., Deng X. 2012. Syntesi of Fe3O4 nanoparticles and their magnetic properties.Chinese materialsconference. China.
Widyawati, N. 2012.Analisa Pengaruh Heating Rate terhadap tingkat Kristal dan Ukuran Butir Lapisan BZT yang Ditumbuhkan dengan Metode Sol Gel.Surakarta:
Universitas Sebelas Maret.
Simamora Pintor, 2015. Sintesis Dan Karakterisasi Sifat Magnetik Nanokomposit Fe3o4 – Montmorilonit Berdasarkan Variasi Suhu. Medan
HASIL PENGUJIAN X-RAY DIFRACTION (XRD) 1. Grafik Hasil XRD sampel Fe3O4 dengan V : 100 oC
20 30 40 50 60 70
200 400 600 800 1000
Fe3O4
Intensity(cps)
2(degree)
Besi (II, III) Oksida (Fe3O4)
2. Grafik Hasil XRD sampel Fe3O4 dengan V : 125 oC
20 30 40 50 60 70
0 500 1000 1500 2000 2500
Fe3O4
Intensity(cps)
2 (degree)
Besi (II, III) Oksida (Fe3O4)
20 30 40 50 60 70 200
400 600 800 1000 1200 1400 1600
Fe3O4
Intensity (cps)
2 (degree)
Besi (II, III) Oksida (Fe3O4)
HASIL PENGUJIAN SCANNING ELECTRON MICROSCOPY (SEM) 1. Hasil SEM Sampel dengan V : 100oC dengan perbesaran 200x
2. Hasil SEM Sampel dengan V : 100oC dengan perbesaran 5000x
X500 200um
X5000 20um
4. Hasil SEM Sampel dengan V : 125oC dengan perbesaran 5000x
X500 200um
X5000 20um
6. Hasil SEM Sampel dengan V : 150oC dengan perbesaran 5000x
X500 200um
X500020um
RUMUS PEMBUATAN NH4OH 3,2 MOLAR
Proses pencampuran NH4OH pekat dengan Aquabides NH4OH = 7+4+16+1 = 28
M = ,𝑔𝑟-𝑀𝑟. × , −𝑉.
3.2 = ,𝑔𝑟-28. × ,1000-100.
89.6 = 10 gr gr = ,89.6-10.
= 8.96 gram
Massa NH4OH = 8.96 gram = 8.96 mililiter 1 gram = 1 milimeter
Proses pencampuran NH4OH pekat dengan Etanol M1V1 = M2V2
3,2 . V1 (ml) = 98% . 1000 (ml) 3,2 . V1 = 1,73 . 1000 ml
V1 =,1,73-3,2.
V1 = 5,4 ml
Etanol = mol = 0,173 ml M = mol × ,100-𝑃.
M = 0,173 × ,1000-100.
M = 1,73
Maka, V NH4OH = 5,4 mililiter
GAMBAR PERALATAN DAN BAHAN PENELITIAN 1.Alat Penelitian
2.Bahan Penelitian
NH4OH (3.2 M)
Etanol Aquabidest
Prekursor FeCl3.6H2O Prekursor FeCl2.4H2O