Prosiding Pertemuan dan Presentasi llmiah
P3TM-BATAN, Yogyakarta 14 -15 Juli 1999 Buku II 239
PEMISAHAN
CAMPURAN URANIUM DAN MOLIBDENUM
DENGAN ZEOLIT
So II
R. Subagiono, Kris Tri Basuki, Imam Prayogo, Supriyanto C P3TM-BATAN. Jl. BabarsariKotak Pas 1008. Yogyakarta 55010
ABSTRAK
PEMISAHAN CAMPURAN URANIUM DAN MOL/BDENUM DENGAN ZEOL/T. Zeolit a/am daTi Gunung Kidul, YO!7yakarta dicuci dengan larutan HCI 0,1 M. Kation-kation alkali atau alkali tanah ditukar dengan ,IVH4+ dengan menggunakan larutan NH4CI 0,5 M dan dikeringkan pada suhu 200 DC dapat digunakan untuk memisahkan campuran (U,Mo) dengan cara pertukaran kation. Pemisahan carnpuran (U,Mo) dilakukan dengan menggunakan zeolit berukuran butir -200 +325 mesh untukkadar U = 31.000ppm dan Mo = 100ppm di da/am larutan H2SO4 0,05 M dengan waktu pemisahan 1 jam. Melalui cara ini diperoleh hasil faktor pemisahan (U,Mo) = 0,4.
ABSTRACT
THE SEPARATION OF URANIUM AND MOLlBDENUM MIXTURE USING ZEOLITE.. The natural zeolite from Gunung Kidul, Yogyakarta, Indonesia was washed with 0.1 M HCI solution. Alkali or alkaline earth <:ations was exchanged with NH4+ by using 0.5 M of NH4CI and was dried at 200 DC. The separation of (U,Mo) mixture was done by using zeolite of -200 +325 mesh for U = 31,000 ppm and Mo = 100 ppm in 0.05 M H2SO4 solution with time extraction of 1 hour. By using this method a se{.laration factor of U,Mo gained was 0.4.
PENDAHULUAN
I
ndonesia sebagai negara yang mempunyai
berbagai jenis tambang mineral, salah satunya adalah zeolit. Potensi zeolit alam di Indonesia cukup besar clan telah dike,tahui oleh para ahli geologi sekitar 47 lokasi (kota), terbanyak tersebar di sekitar pulau Jawa< 1 ). Di Daerah Istimewa Yogyakarta diperkirakan terdapat deposit mineral zeolit sekitar 490 juta ton yang tersebar di daerah kabupaten Gunung Kidul dan Kulon Progo (BKPMD, Propinsi DIY, Informasi Potensi Bahan Galian Zeolit, Pemetaan Semi Mikro Bahan Galian Golongan C , Kabupaten Gunung Kidul, 1997). Zeolit alam selain dapat digunakan untuk bidang petemakan, perikanan, pertanian, kedokteran/kesehatan, juga dapat dimanfaatkan untuk menangani proses olah ulang bahan bakar reaktor clan limbah industri nuklir. Di dalam bahan bakar bekas reaktor nuklir terutama jenis PWR pada umumnya masih banyak mengandung uranium (U) yang perlu dipisahkan daTi unSUT-lffisur radioaktif hasil belah dari reaksi inti di dalam reaktor nuklir hila diinginkan untuk dipakai lagi. Molibdinium (Mo) adalah salah satu hasil belah yang mempunyai sifat kimia mirip dengan uranium. Teknik pemisahan U clan Mo telah banyak dilakukan misalnya dengan cara pengendapan, ekstraksi cair-cair atau memakai resin
penukar ion. Kajian kemungkinan pemanfaatan
zeolit untuk memisahkan
U dari Mo merupakan hal
yang sangat menarik, karena zeolit alam mudah
diperoleh dengan harga yang murah dan dalam
jumlah yang berlimpah. Zeolit adalah senyawa
kristalin dengan struktur kerangka
tiga dimensi yang
berongga,
kerangka tiga dimensi ini terbentuk oleh
tetrahedral aluminat (AIo4)5- dan silikat (SiO4)4-.
Dalam struktur kristal tersebut terdapat sisi aktif
yang dapat menjadikan zeolit berlaku sebagai
fenukar kation dan seb~gai
adsorben
yang selektif.(
3). Berdasarkan suat tersebut maka zeollt
diharapkan dapat digunakan untuk memisahkan
uranium dan molibdenum. Reaksi pertukaran ion
antara ion dalam padatan dengan ion dalam larutan
berlangsung
secara
stoikiometri. Pertukaran ion-ion
hanya terjadi antara ion-ion sejenis. Pacta keadaan
seimbang,
sisi aktif dalam padatan
penukar ion telah
jenuh dengan ion penukar sehingga pertukaran ion
tidak terjadi lagi. Persamaan keseimbangan
pertukaran ion antara zeolit dengan ion uranium
atau ion molibdenum secara umum dinyatakan
dalam persamaan
Z--Mn+(p)+Nn+(I)~Z--Nn+(p)+Mn+(I) (1)
Z adalah padatan
zeolit, Mn+ ion yang tertukar, Nn+
ion penukar ( U atau Mo ) dan n adalah valensi ion.
ISSN 0216-3128 Teknologi Proses
Prosiding Perlemuan dan Presentasi Ilmiah P3TM-BA TAN, Yogyakarla 14 -15 Juli 1999 Buku II
Efisiensi penyerapan (E zeolit adalah :
ion penukar ke dalam
Eu
(2)
EM'
(3)
Keberhasilan pemisahan antara U daD Mo menurut Tompkins, E.R ( 4 ) ditunjukkan oleh nilai faktor pemisahan
-~
_A~
(4)
~
B-XB
Diman~ A, B masing-masing adalah berat ion penukar U dan Mo di dalam larutan sebelum proses pemisahan dilakukan. XA, XB masing-masing adalah berat ion penukar U dan Mo di dalam padatan zeolit. Berdasarkan mekanisme tersebut di atas maka dilakukan pengkajian proses untuk memanfaatkan zeolit alam dalarn upaya memisahkan uranium dari molibdenum, yaitu pengaruh. suhu kalsinasi zeolit, keasaman larutan campuran U dan Mo, ukuran butir zeolit dan waktu pemisahan.
CARA
KERJA
Bahan
Bahan yang dipakai untuk penelitian ini adalah HCI, ~CI, UO2(NO3h. 6 H2O, (NH4)6Mo7O24. 4 H2O, H2SO4 dari E. Merck, air suling daD zeolit alam dari desa Sum, Gedang sari, kabupaten Gunung Kidul yang mempunyai kandungan SiO2 = 62,75 % , Al2O3 = 13,63 %, Fe203 = 2,12 %, CaD = 3,42 %, MgO = 0,87 %, Na20= 1,32 %, K2O = 1,39 %.
sebanyak I I , diaduk dan direndam selama 24 jam. Setelah itu zeolit dicuci dengan air suling dan selanjutnya direndam dengan ~CI 0,5 M selama 24 jam. Zeolit dicuci kembali dengan air suling , selanjutnya dikalsinasi pacta suhu bervariasi sampai 800 DC selama 4 jam.
2. Kajian pengaruh suhu kalsinasi
Zeolit dengan ukuran butir -100 +200 mesh yang dipreparasi kimia di alas dikalsinasi pacta suhu 100, 200, 300, 400, 500, 600, 700, dan 800 DC selama 4 jam, ditimbang sebanyak 5 g untuk masing-masing suhu kalsinasi dan ditambahkan 20 ml larutan campuran U = 31.000 ppm , Mo = 100 ppm di dalam H2SO4 0,05 M. Campuran zeolit dan larutan (U,Mo) diaduk menggunakan alat homogenisasi yang berputar dengan kecepatan 30 rpm selama 4 jam. Setelah itu campuran disaring untuk memisahkan rasa padat dan rasa cair atau fiJtratnya yang kemudian filtrat ditentukan kadar U, Mo nya dengan alat spektrometer pendar sinar -X dan spektrometer serapan nyaJa atom.
3. Kajian
pengaruh
keasaman
larutan
campuran (U,Mo)
ZeoJit dengan ukuran butir -100 +200 mesh, suhu kalsinasi 200 DC sebanyak 5 g ditambahkan masing-masing larutan campuran CU,Mo) dengan U = 31.000ppm, Mo = 100 ppm di dalam H2SO4: 0,05 ; I ; 2 ; 3 ; 4; dan 5 M. Selanjutnya dikerjakan seperti cara kerja no.2. 4. Kajian pengaruh ukuran butir zeolit
Zeolit basil kalsinasi pacta suhu 200 DC dengan ukuran butir yang bervariasi : 50 +100, -100 +200, -200 +325, -325 +400, dan -400 mesh masing-masing sebanyak 5 g ditambah 20 ml larutan campuran (U,Mo) dengan U = 31.000 ppm , Mo = 100 ppm di dalam H2SO4 0,05 M. Selanjutnya dikerjakan seperti cara kerja no.2.
5. Kajian pengaruh waktu pemisahan
Zeolit dengan ukuran butir basil kondisi optimum kajian no.4 yang dikalsinasi pacta suhu 200 DC sebanyak 5 g ditambah 20 ml larutan campuran (U,Mo) dengan U = 31.000 ppm, Mo = 100 ppm di dalam H2SO4 0,05 M. Masing-masing campuran zeolit dan larutan (U,Mo) diaduk menggunakan alat homogenisasi yang berputar dengan kecepatan 30 rpm selama : I, 2, 3, 4 dan 5 jam. Selanjutnya dikerjakan seperti cara kerja no.2.
Alat
Penggojok
putar : R.R Mini, Karl Kolb,
D-6072, neraca Sartorius 2462, spektrometer
pendar
sinar -X
(MCA-ORTEC-7010), spektrometer
serapan nyala atom (AAS) tipe AA-300 P buatan
Varian Tehtron, Austria, tungku Logotherm
(program controller C-19), pengayak
HAVER EML,
mortir agate clan
peralatan
gelas.
HASIL DAN PEMBAHASAN
Aktivasi zeolit yang telah dilakukan
dimaksudkan untuk meningkatkan aktivitas zeolit,
baik sebagai adsorb
en maupun sebagai penukar
kation. Pada percobaan
ini dilakukan dengan 2 cara,
yaitu secara
kimia daD
fisis.
Tata kerja
1. Aktifasi zeolit
Zeolit alarn dari Gunung Kidul yang telah
digerus berukuran antara 50 sarnpai 200 mesh
ditimbang sebanyak 1 kg kemudian dimasukkan
ke
dalam bekerglas clan ditambahkan HCI 0,1 M
Subaaiono. dkk Teknologi Proses
Prosiding Perlemuan dan Presentasi llmiah
P3TM-BA TAN, Yogyakarla 14 -15 Ju/i 1999 Buku II 241
dengan naiknya nilai suhu kalsinasi sedang untuk molibdenum adalah sebaliknya. Pada suhu 200 DC terjadi selisih nilai yang terbesar antara efisiensi penyerapan uranium daD molibdenum atau dengan kata lain nilai faktor pemisahan (U ,Mo ) adalah terkecil yaitu 0,5 , hal ini karena molekul air yang menutupi permukaan/ rongga zeolit telah menguap, menurut Keer ( S ) pada suhu 200 DC ion amonium di dalam zeolit mulai terdekomposisi (deaminasi) dengan persamaan reaksi sebagai berikut :
200 DC
NH4AI Si 06 200.C ~ Cara kimia dengan menambahkan bahan
kimia, pertama mencuci zeolit dengan larutan HCI 0, I M yang bertujuan menghilangkan bahan-bahan organik clan logam-logam pengotor yang ada pada mineral zeolit. Kedua dengarl menambahkan larutan N~CI 0,5 M bertujuan untuk mengganti ion logam yang terikat dalam zeolit pada ikatan Si, Al dengan N~ + (sebagai kation).
Perubahan yang tampak dengan adanya
perlakuan aktivasi secara kimia adalah perubahan wama zeolit, daTi coklat kehijauan menjadi coklat
muda, hal ini dikarenakan unsur pengotor yang terikut telah dipisahkan.
Aktivasi secara fisis adalah kalsinasi, yaitu memanaskan zeolit yang telah melalui tahap pencucian/aktivasi kimiawi, dengan menggunakan tungku listrik, pada suhu sampai 800 DC selama
beberapajam.
Pengaruh suhu kalsinasi pada pemisahan U, Mo Kalsinasi terhadap 2:eolit bertujuan untuk meningkatkan derajat kekristalan, menguapkan molekul air yang menutupi pentlukaan/rongga zeolit clan menghilangkan bahan organik. Suhu kalsinasi zeolit dikaji pada penelitian ini bervariasi dari 100 DC sampai 800 DC, selama 4 jam. Larutan umpan campuran (U,Mo) yang akan dipisahkan mengandung U = 31.000 ppm clan Mo = 100 ppm, keasaman 0,05 M H2SO4. Pemisahan dikerjakan dengan alat homogenisasi yang berputar 30 (pm selama 4 jam. Hasil pemisahan dapat disajikan pada gambar I.
HAl Si 06+ NH3t (5) asam Bronsted
Pacta suhu kalsinasi lebih tinggi dari 200 °c zeolit yang mempunyai sifat sebagai asam Bronsted akan berubah secara sempuma menjadi zeolit yang bersifat basa Bronsted dan asam Lewis dengan melepaskan air pacta suhu 400 -500 °c, maka nampak pacta basil penelitian ini bahwa adanya perubahan tersebut nilai dari efisiensi penyerapan uranium cenderung turun dan efisiensi penyerapan molibdenum bertambah besar. Oleh karena itu untuk pemisahan campuran CU,Mo) menggunakan zeolit ini dipilih suhu pemanasan 200 °C.
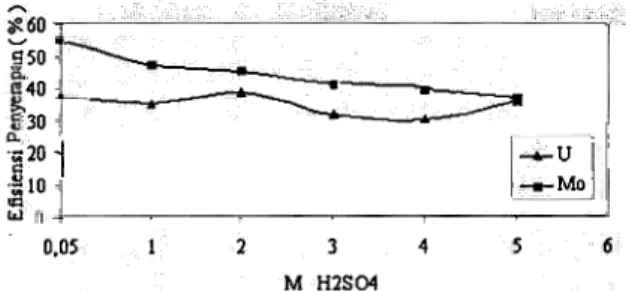
Pengaruh keasaman larutan umpan (U,Mo) Keasaman larutan umpan dinyatakan dalam molar H2SO4. Larutan umpan campuran (O,Mo), 0 = 31.000 ppm dan Mo = 100 ppm dibuat dalam kondisi asam sulfat dengan konsentrasi bervariasi dari 0,05 sampai 5 M, dengan tujuan agar unsur yang akan dipisahkan mempunyai bentuk spesies yang berlainan pacta tiap-tiap konsentrasi keasaman dan terjadi kompetisi dari dua unsur tersebut. Hal ini berdasarkan sifat daripada uranium dan molibdenum yaitu bahwa pacta konsentrasi H2SO4, yang rendah mereka berada dalam spesies 00;+ dan MoO;+, tetapi hila konsentrasi H2SO4. tinggi mereka berada dalam spesies 002(S04)3-4 dan MoOiS04)3-4 yang tidak dapat dipisahkan dengan cara ini. Perlakuan variasi keasaman menggunakan zeolit dengan suhu kalsinasi 200 °c dan ukuran butiran -100 +200 mesh. Hasil penyerapan pacta pengaruh keasaman disajikan pacta gambar 2.
""
~'60
~ 550 40 ;.30 ,1
.;:20"
.~10...
w 0) 23456189 SuhuKalsms (x 100 C)Gambar 1 a. Hubungan suhu kalsinasi dengan
efisiensi
penyerap,::n
U dan Mo
1 .: ~ 0,9
'"
.~ 0,6" ~ 0,4 ~ 0,2...
0 3 SuhuKalsmsi (1: 100 C)Gambar lb. Hubungan suhu kalsinasi dengan
faktor pemisahan U-Mo
Dari gambar 1 terlihat bahwa nilai efisiensi penyerapan uranium cenderun;g bertambah besar
~
~
I~
,~
0,05 1 2 3 4 5 6
M H2SO4
Gambar 2a. Hubungan keasaman umpan (U; Ma)
dengan efisiensi
penyerapannya
ISSN 0216-3128 Teknologi Proses
Subagiono, dkk
U Mo'
Prosiding Pertemuan dan Presentasi llmiah P3TM-BA TAN, Yogyakarta 14 -15 Juli 1999
242 Buku II
Gambar lb. Pengaruh keasaman umpan (u; Mo)
terhadap
faktor pemisahan
Pada konsentrasi
keasaman
0,05 M terlihat
nilai
efisiensi penyerapan uranium maupun
molibdenum menunjukkan basil yang tertinggi ,
namun hila dilakukan pada konsentrasi keasaman
yang lebih rendah (misainya 0,00 1M), maka akan
terjadi sedikit endapan putih kekuning-kuningan
pada larutan campuran,
diperkirakan adalah endapan
H2MoO4
karena UO/+ sangat stabil pada pH 2 -2,5
atau lebih rendah. Hal ini tidak dikehendaki
karena
pengkajian pemisahan dengan menggunakan
zeolit
tidak dapat dilakukan. Pada konsentrasi keasaman
0;05 M H2SO4 terjadi selisih nilai yang terbesar
antara efisiensi penyerapan uranium clan
molibdenum dan nilai faktor pemisahan yang
terkecil yaitu 0,5 , maka pacta
konsentrasi
keasaman
0,05 M bisa disebut sebagai konsentrasi
keasaman
optimum.
Dari tabel di atas terlihat bahwa semakin kecil ukuran butir maka efisiensi penyerapan uranium maupun molibdenum akan semakin besar, hat ini karena luas permukaan dari zeolit bertambah besar, sehingga daya serapnya meningkat. Kondisi penyerapan yang optimum terjadi pada ukuran butir -200 +325 mesh, karena pada kondisi ini terjadi selisih nilai efisiensi penyerapan uranium clan molibdenum yang terbesar serta ni1ai faktor pemisahan yang terkecil yaitu 0,3917. Pada kondisi ukuran butir -325 +400 mesh menunjukkan efisiensi penyerapan uranium maupun molibdenum yang tertinggi, namun tidak bisa diambil sebagai titik optimum karena nilai selisihnya lebih kecil dibandingkan pada kondisi ukuran butir -200 +325
mesh
Pengaruh waktu pemisahan
Semakin lama kontak antara rasa air yang terdiri dari larutan umpan (U ,Mo) dengan rasa padat yaitu zeolit maka efisiensi penyerapan uranium maupun molibdenum akan semakin besar, akan tetapi pada suatu saat tertentu nilai faktor pemisahan akan tetap karena telah tercapai keseimbangan sistem. Larutan umpan campuran (U,Mo), U = 31.000 ppm clan Mo = 100 ppm, keasaman 0,05 M H2SO4 dicampur di dalam alat homogenisasi dengan zeolit berukuran butir -200 +325 mesh, pada kecepatan putar 30 rpm selama waktu yang divariasi hingga 5 jam.. Hasi1 yang diperoleh adalah seperti terlihat pada gambar 3.
~
~
~ " .. 0-~~
~
5~
~Efisiensi penyerapan
molibdenum
menun-jukkan cenderung
turun dengan
bertambah
besarnya
konsentrasi
keasaman,
hal ini dimungkinkan
karena
zeolit tidak stabil dengan keasaman
yang makin
tinggi. Untuk meningkatkan kesetabilan zeolit
dalam suasana
asam maka dapat dilakukan dengan
jalan mengurangi kandungan aluminium dalam
struktur dasar zeolit (dealuminasi).
Pengaruh Ukuran Butir Zeolit
Ukuran butir sangat berpengaruh
terhadap
proses penyerapan, semakin halus partikel zeolit
maka akan mempunyai luas permukaan yang
semakin besar, sehingga mampu menyerap lebih
banyak partikel yang akan dipisahkan. Variasi
ukuran butir dikerjakan daTi -50 sampai -400 mesh
menggunakan zeolit yang dikalsinasi dengan suhu
200 DC. Umpan larutan campuran (U,Mo), U =
31.000 ppm daD Mo = 100 ppm, dengan keasaman
0,05M H2SO4-
Hasil percobaan
variasi ukuran butir
dapat dilihat pacta
tabel dibawah ini.
0123456
Waklu PenisalJan(j am)
Gambar 3a. Hubungan antara waktu pemisahan
dengan efisiensi penyerapan U dan
Mo
0,42 0=0,4(.~
.IX 0,4 ~ 039.
(l, "03 8"~ '
..
0c~37 ~ ' 0..36Ukuran Butir Faktor Pemisahan
Zeolit (Mesh) U,Mo
-50+100 -100 +200 -200 +325 -325 -+400 -400 34,96 37,48 37,51 41,24 47,31 54,64 54,76 60,51 63,67 64,67 0,4463 0,4953 0,3917 0,4005 0!4~ .1 3 4 5 6 Wiliu Periisahan(jam)
Gambar 3b. Hubungan antara waktu pemisahan
denganfaktor pemisahan U-Mo
Prosiding Peltemuan dan Presentasi Ilmiah
P3TM-BA TAN, Yogyakalta 14 -15 Juli 1999 Buku II 243
Melihat garnbar 3b maka pemisahan campuran (U,Mo) dengan waktu pemisahan selarna I jam dan seterusnya memberikan nilai faktor pemisahan yang dapat dianggap tetap, maka kondisi pemisahan yang optimum dipilih I jam dengan faktor pemisahan 0,4.
products of ammonium zeolite Y, J. Catal. 15 (1969),200 -204
TANYA
-JAWAB
KESIMPULAN
Zeolit alam dari desa Suru, Gedang sari, kabupaten Gunung Kidul dapat digunakan untuk memisahkan campuran (U,Mo) dengan cara batuan zeolit dihancurkan menjadi butiran kemudian dicuci dengan larutan HCI 0,1 M, diaktitkan melalui pertukaran ion menggunakan larutan N~CI 0,5 M clan selanjumya dikeringkan .lewat pemanasan pad a suhu 200 °C. Adapun pemisahan campuran (U,Mo) dilakukan dengan menggun,tkan zeolit berukuran butir -200 +325 mesh untuk kadar U = 31.000 ppm clan Mo = 100 ppm di dalam larutan H2SO4 0,05 M dengan waktu pemisahan 1 jam. Melalui cara ini diperoleh hasil faktor pemisahan (U,Mo) = 0,4.
UCAP AN TERIMA
KASIH
Bersama ini diucapkan
terima kasih kepada
Sdr. Purwoto dan Mulyono (teknisi senior
BTFK-P3TM), Sdr. Atok Suhartanto (mahasiswa
PA1N-BAT AN
Yogyakarta) yan,g telah membantu
penelitian ini.
DAFTAR
PUSTAKJ~
Sahat Simbolon :
» Kation apa saja yang digantikan oleh NH.j+?
» Apakah mungkin kation NH.j + dapat mengganti
Al dan Si ?
R. Subagiono :
~ Kation yang digantikan oleh NH4+ adalah
kation logam alkali dan alkali tanah (K,
Na+, Bal+, C~+ dan Mi+) yang terikat
zeolit.
~ Tidak dapat, karena Al don Si adalah
pembentuk struktur kerangka tiga dimensi
yang mempunyai
sisi aktif sehingga berlaku
sebagai
penukar kation.
Djoko Sardjono :
» Mengapa efisiensi pemisahan U lebih rendah
daripada Mo, mengingat
ukuran partikel U lebih
besar daripada Mo dan muatan U (Uoli
dan
Mo (MoO221 sarna?
R. Subagiono :
~ Betul I, efisiensi pemisahan U lebih rendah
daripada Mo, disebabkan
karena muatan U
(UO/+) dan Mo (MOO11+)
sarna sedangkan
ukuran partikel U lebih besar daripada Mo
maka kemampuan
tarik dari zeolit sebagai
penukar ion lebih besar terhadap Mo
daripada U
Iswani
» Bagaimana efektifitas pemisahan carnpuran U
dan Mo dengan zeolit ? Dari nilai ekonominya
apakah pemisahan
ini menguntungkan
, mohon
dijelaskan.
R. Subagiono :
~ Berdasarkan
hasil penelitian di alas dimana
laktor pemisahan (u; Mo) = 0,4 ,. ini
menunjukkan bahwa campuran tersebut
dapat dipisahkan secara bertingkat.
Mengingat harga zeolit murah don dapat
diregenerasi maka proses ini
cukup
ekonomis
dan menguntungkan.
1. HARJANTO dan SARNO, , Lempung Zeolit
Dolomit dan Magnesit, Pusat Pengembangan
Teknologi Mineral, Bandung (1987)
2. MINA TO, H., Zeolite: Its Natural Resources
and Utilization, Ceramic Japan, 10 (1975), 941
-957
3. BARRER, R.M., Zeolite and Clay Minerals as
Sorbents and Moleculair Sieves, Academic
Press, London (1978)
4. NACHOD, F.C. and JACK SCHUBERT, Ion
Exchange Technology, Academic Press Inc.
Publishers,
New York (195~5)
5. KEER, G.T.,
"Chemistry of ,crystalline
aluminosilicates VII", Thermal decomposition
T eknologi Proses ISSN 0216-3128