BAB 2
TINJAUAN PUSTAKA
2.1. Kitin
Kitin merupakan poli (2-asetamido-2-deoksi-β-(1 4)-D-glukopiranosa) dengan rumus molekul (C8H13NO5)n yang tersusun atas 47% C, 6% H, 7% N, dan 40% O. Struktur kitin menyerupai struktur selulosa dan hanya berbeda pada gugus yang terikat diposisi atom C-2. Gugus pada selulosa adalah gugus hidroksil, sedangkan pada C-2 kitin adalah gugus N-asetil(-NHCOCH3asetamida).
Seperti yang tampak pada (gambar 2.1) dibawah ini:
O
Gambar 2.1. Struktur polimer selulosa (R= -OH) dan kitin (R= -NHCOCH3) (Sugita, 2009)
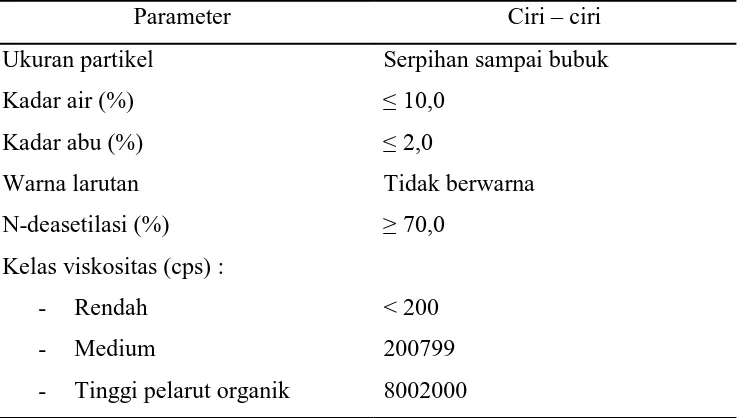
Spesifikasi Kitin dapat dilihat pada tabel 2.1 berikut: Tabel 2.1. Spesifikasi kitin
Parameter Ciri – ciri
Ukuran partikel Serpihan dalam bentuk serbuk
Kadar air (%) ≤ 10,0
- Pelarut organik Tidak larut - LiCl2/ dimetilasetamida Sebagian larut
Enzim pemecah Lisozim dan kitinase
(Sugita, 2009)
2.2. Kitosan
Kitosan adalah poli-(2-amino-2-deoksi-β-(1 4)-D-glukopiranosa) dengan rumus molekul (C6H11NO4)n yang dapat diperoleh dari deasetilasi kitin. Kitosan juga dijumpai secara alamiah di beberapa organisme. Struktur polimer kitosan dapat dilihat pada gambar (Gambar 2.2.) di bawah ini :
O
Gambar 2.2. Struktur polimer kitosan (Sugita, 2009)
2.3. Transformasi kitin menjadi kitosan secara kimia
2.3.1. penghilangan protein
Deproteinasi kitin merupakan reaksi hidrolisis dalam suasana asam atau basa. Lazimnya, hidrolisis dilakukan dalam suasana basa dengan menggunakan larutan NaOH 2-3% pada suhu 63-65oC selama 1-2 jam (Johnson et al,1982). Efisiensi deproteinasi tidak hanya bergantung pada konsentrasi basa dan suhu, tetapi juga spesies sumber kitin pada tahap deproteinasi, protein diubah menjadi garam natrium proteinat yang larut air
Kerangka luar Crustacea mengandung kitin yang berikatan dengan kalsium karbonat (CaCO3) dan protein (Austin, 1988), terkadang juga dengan lapisan lilin, kadar protein yang terikat dalam matriks kulit sekitar 30-40% dari komponen organik totalnya (Johnson et al, 1982). protein terikat secara fisik dan sebagian lainnya terikat secara kovalen yang kadarnya beragam untuk setiap jenis crustacea. Austin (1988) menyatakan, bahwa dari jumlah protein total dalam udang (34%) dengan kontribusi protein yang terikat secara kovalen dan fisik berturut-turut adalah sekitar 16 dan 18%.
2.3.2. Penghilangan Mineral
Hal yang terpenting dalam tahap penghilangan mineral adalah jumlah asam yang digunakan (Shadidi et al, 1991). Ion mineral ditentukan melalui destruksi dengan asam kuat HCl terhadap abu dari endapan yang diperoleh pada tahap pemisahan mineral, selanjutnya penetapan ion mineral dilakukan menggunakan metode Spektroskopi Serapan Atom (AAS).
2.3.4. Penghilangan gugus asetil (Deasetilasi)
2.4. Sifat Fisika-Kimia pada Kitosan
Kitosan merupakan padatan amorf yang berwarna putih kekuningan dengan rotasi spesifik [ ] -3 ingga -10 pada kon ent a i a am a etat 2 ito an la ut pada kebanyakan larutan asam organik (Tabel 2.2.) pada pH sekitar 4,0, tetapi tidak larut pada pH lebih besar dari 6,5, juga tidak larut dalam pelarut air, alkohol, dan aseton. Dalam asam mineral pekat seperti HCl dan HNO3, kitosan larut pada konsentrasi 0,15-1,1 %, tetapi tidak larut pada konsentrasi 10%. Kitosan tidak larut dalam H2SO4 pada berbagai konsentrasi, sedangkan didalam H3PO4 tidak larut pada konsentrasi 1% sementara pada konsentrasi 0,1% sedikit larut. Perlu untuk kita ketahui,bahwa kelarutan kitosan dipengaruhi oleh bobot molekul, derajat deasetilasi, dan rotasi spesifiknya yang beragam bergantung pada sumber dan metode isolasi serta transformasinya.
Tabel 2.2. Kelarutan kitosan pada berbagai pelarut asam organik
Konsentrasi asam organik Konsentrasi asam organik (%)
10 50 >50
Asam asetat + ± -
Asam adipat - - -
Asam sitrat + - -
Asam format + + +
Asam laktat + - -
Asam maleat + - -
Asam malonat + - -
Asam oksalat + - -
2.5. Keterkaitan Sifat Fisik –Kimia pada Kitosan
Kitosan dalam bentuk terprotonasi menunjukkan kerapatan muatan yang tinggi dan bersifat sebagai polielektrolit kationik, seperti yang dapat dilihat pada Gambar 2.3 dan sangat efektif berinteraksi dengan biomolekul bermuatan negatif dan biomolekul permukaan. Sedangkan dalam bentuk netralnya, kitosan mampu mengompleks ion logam berat berbahaya seperti Cu, Cr, Cd, Mn, Co, Ph, Hg, Zn, dan Pd.
Gambar 2.3. Kitosan sebagai polielektrolit kationik (Sugita, 2009) Spesifikasi Kitin dapat dilihat pada tabel 2.3 dibawah ini:
Tabel 2.3. Spesifikasi kitosan
Parameter Ciri – ciri
Ukuran partikel Serpihan sampai bubuk
Kadar air (%) ≤ 10,0
- Tinggi pelarut organik 8002000
2.6. Modifikasi Kitosan
Kitosan dapat dimodifikasi, kitosan sebagai adsorben dapat berada dalam berbagai bentuk, antara lain bentuk butir, serpih, hidrogel, dan membran (film). Kitosan sebagai adsorben sering dimanfaatkan untuk proses adsorpsi ion logam berat. Besarnya afinitas kitosan dalam mengikat ion logam sangat bergantung pada karakteristik makrostruktur kitosan yang dipengaruhi oleh sumber dan kondisi pada luas permukaannya. Semakin kecil ukuran kitosan akan semakin besar dan proses adsorpsi pun dapat berlangsung dengan baik. Modifikasi kimia kitosan menjadi gel kitosan dapat meningkat kapasitas jerapnya, keunggulan ini disebabkan oleh bentuk butiran gel mempunyai volume pori yang lebih besar dibandingkan dengan bentuk serpihan. Kitosan dengan bobot molekul tinggi akan menghasilkan larutan dengan viskositas yang tinggi pula (Rao, 1993)
2.6.1. Glutaraldehida
Glutaraldehida merupakan agen penaut silang kitosan yang paling banyak digunakan. Glutaraldehida dapat menautsilangkan rantai kitosan melalui reaksi pembentukan basa Schiff (imina tersubstitusi ,-CH=NR) antara gugus aldehida glutaraldehida dan guggus –NH2 kitosan. Jumlah tautan silang tersebut meningkat seiring dengan bertambahnya jumlah glutaraldehida yang ditambahkan. Tautan silang tersebut telah terbukti dapat menghilangkan stabilitas adsorben kitosan dalam asam. Namun derajat tautan silang yang terlalu tinggi juga akan menurunkan jumlah –NH2, sehingga kapasitas adsorpsi maksimumnya juga menurun. Selain itu reaksi glutaraldehida dan kitosan juga dapat melemahkan ikatan antara atom nitrogen dan ion logam yang akan dijerap (Osifo et al, 2008). Struktur kimia glutaraldehida dapat dilihat pada gambar 2.4 berikut;
O O
H H
2.7. Aplikasi Kitosan dalam Bidang Lingkungan
Lingkungan sangat berpotensi tercemar zat organik, anorganik, maupun logam berat. Keberadaan zat-zat pencemar tersebut akan mengganggu ekosistem yang ada, termasuk juga manusia. Oleh sebab itu, kelestarian lingkungan dari zat pencemar harus dijaga dan terus mendapatkan perhatian dari masyarakat sekitar, yang merupakan elemen dari lingkungan hidup itu sendiri. Salah satu cara yang dapat digunakan untuk mengurangi zat pencemar pada lingkungan adalah dengan menggunakan kitosan sebagai adsorben.
Kitosan lazimnya disintesis dari deasetilasi kitin yang berasal dari limbah kulit udang atau kepiting. Oleh karena itu, penggunaan kitosan sejak awal telah berperan dalam mengurangi pencemaran lingkungan. Manfaat kitosan dalam bidang lingkungan adalah untuk menjerap logam berat maupun zat warna yang banyak dihasilkan dari industri tekstil atau kertas. Logam berat merupakan limbah yang sangat berbahaya. Hal tersebut dikarenakan logam berat dapat menimbulkan toksisitas akut pada manusia maupun habitat yang ada di lingkungan perairan.
2.7.1. Logam Berat
2.7.2. Zat Warna
Pada umumnya zat warna yang masuk ke dalam lingkungan berasal dari limbah tekstil dan kertas. Zat warna kedua industri tersebut menimbulkan warna yang sangat pekat walaupun dalam konsentrasi yang rendah,sehingga dampaknya dapat mengurangi estetika lingkungan, selain itu limbah zat warna bersifat karsinogenik jika dikonsumsi dan sulit terdegradasi.
Berdasarkan muatannya, zat warna dapat dibedakan menjadi 2, yaitu zat warna anionik dan kationik. Kedua zat warna tersebut dapat dijerap dengan kitosan dan modifikasinya (Singh et al.,2008). Zat warna anionik dan asam,zat warna anionik sebagian besar merupakan senyawaan azo yang mengandung gugus sulfonat,sebagaimana diketahui,bahwa zat warna tersebut lebih banyak digunakan dalam industri tekstil. zat warna kationik. Berbeda dengan zat warna anionik, muatan positif pada zat warna kationik disebabkan oleh keberadaan garam kuartener sekunder. Karena muatannya yang positif, zat warna kationik akan terjerap dengan baik pada kitosan dengan kitosan dengan kondisi netral atau basa untuk mencegah protonasi pada gugus amino kitosan.
2.7.3. Pestisida
2.7.4. Senyawaan Fenolik
Fenol merupakan polutan organik yang berbahaya bagi organisme perairan dan manusia walaupun dalam konsentrasi yang rendah, bahkan hanya dalam konsentrasi 0,005 mg/L saja sudah dapat merubah rasa dan bau pada air minum,sehingga tidak baik untuk dikonsumsi, manusia yang mengkonsumsi air yang terkontaminasi fenol akan mengalami beberapa nyeri yang memicu kerusakan pembuluh kapiler dan berakibat pada kematian, selain itu proses klorinasi pada air yang tercemar akan berakibatkan pembentukan klorofenol (Aksu,2005).
2.8. Kandungan logam berat
I tila “logam” eca a k a membe ikan un u yang me upakan kondukto li t ik yang baik dan mempunyai konduktivitas panas, rapatan, kemudahan ditempa, kekerasan dan keelektropositifan yang tinggi. (Connel, 1995) Logam berat (heavy metal) atau logam (toxic metals) adalah bentuk umum yang digunakan untuk menjelaskan sekelompok elemen-elemen logam yang kebanyakan tergolong berbahaya bila masuk ke dalam tubuh mahkluk hidup. Logam berat yang terdapat baik di lingkungan maupun di dalam tubuh manusia dalam konsentrasi yang sangat rendah disebut sebagai trace metals. Trace metals seperti Cadmium(Cd), Timbal (Pb), dan Merkuri (Hg) (Nugroho, 2006).
2.8.1 Efek Toksik Kadmium
2.9. Spektrofotometri Serapan Atom
Spektrofotometri serapan atom adalah metoda pengukuran kuantitatif suatu unsur yang terdapat dalam suatu cuplikan berdasarkan penerapan cahaya pada panjang gelombang tertentu oleh atom – atom bentuk gas dalam keadaan dasar. telah lama ahli kimia menggunakan pancaran radiasi oleh atom yang dieksitasikan dalam suatu nyala sebagai alat analisi. fraksi atom – atom yang tereksitasi berubah secara eksponensial dengan temperatur. tekni ini digunakan untuk penetapan sejumlah unsur, kebanyakan logam dan sampel yang sangat beraneka ragam (Walsh , 1955).
2.9.1 Prinsip dan Teori
Spektrofotometri serapan atom didasarkan pada bahwa atom – atom pada suatu unsur dapat mengabsropsi energi sinar pada panjang gelombang tertentu. banyak energi sinar yang di absropsi berbanding lurus dengan jumlah atom – atom unsur yang mengabsropsi. Atom terdiri atas inti atom yang mengandung proton bermuatan positif dan neutron berupa pertikel netral, dimana inti atom dikelilingi oleh elektron –elektron bermuatan negatif pada tingkat energi yang berbeda – beda. Jika energi diabsropsi oleh atom, maka elektron yang berada di kulit terluar ( electron valensi ) akan tereksitasi dan bergerak dari keadaan dasar atau tingkat energi yang terendah kekeadan tereksitasi dengan tingkat energi yang terendah. Jumlah energi yang dibutuhkan untuk memindahkan elektron ke tingkat energi tertentu dikenal sebagai potensial eksitasi untuk tingkat energi tersebut (Clark, 1979).
2.9.2 Instrumentasi
Ada beberapa cara untuk melarutkan sampel, yaitu:
Langsung dilarutkan dengan pelarut yang sesuai
Sampel dilarutkan dalam suatu asam
Sampel dilarutkan dalam suatu basa atau dilebur dahulu dengan basa kemudian hasil leburan dilarutkan dengan pelarut yang sesuai
Metode pelarutan apapun yang akan dipilih untuk dilakukan analisis dengan spektrofotometer serapan atom, yang terpenting adalah bahwa larutan yang dihasilkan harus jernih, stabil dan tidak mengganggu zat-zat yang akan dianalisis. Pelarutan juga dimaksudkan untuk destruksi sampel dimana sampel dimana biasanya digunakan asam-asam seperti asam nitrat pekat (Rohman, 2007)
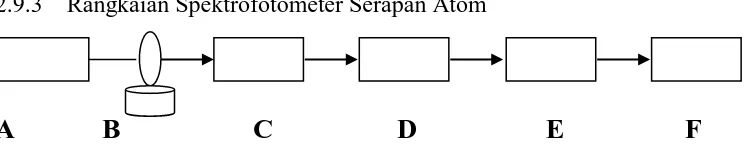
Komponen penting yang membentuk spektrofotomter serapan atom diperlihatkan pada gambar 2.5 dibawah ini.
2.9.3 Rangkaian Spektrofotometer Serapan Atom
A
B
C
D E
F
Gambar 2.5. Rangkaian ringkas Spektrofotometer Serapan Atom Keterangan Gambar :
A = Lampu Katoda Berongga
B = Nyala
C = Monokromator
D = Detektor
E = Amplifier
F = Recorder ( Sony.2009)
a. Sumber sinar
b. Tempat sampel
Dalam analisis dengan spektofotometri serapan atom, sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan asas. Ada berbagai macam yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu dengan nyala dan tanpa nyala.
1. Nyala (flameless)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi.
2. Tanpa nyala(flameless)
Pengatoman dapat dilakukan dalam tungku dari grafit. Sampel diletakkan dalam tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik grafit. Akibat pemanasan ini,maka gas yang akan dianalisis berubah menjadi atom-atom netral (Rohman, 2007).
c. Monokromator
Monokromator memisahkan,mengisolasi dan mengontrol intensitas dari radiasi energi yang mencapai detektor (Haswell, 1991).
d. Detektor
Detektor dapat diatur sedemikian rupa pada nilai frekuensi tertentu, sehingga tidak memberikan respon terhadap nilai emisi yang berasal dari eksitasi termal.(Khopkar, 2007).
e. Read Out
2.9.4 Gangguan pada SSA dan cara mengatasinya
Gangguan nyata pada SSA adalah seringkali didapatkan suatu harga yang tidak sesuai dengan konsentrasi sampel yang ditentukan. Penyebab dari gangguan ini adalah faktor matriks sampel dan faktor kimia karena adanya gangguan molekuler yang bersifat radiasi.
Sampel dalam bentuk molekul karena disosiasi yang tidak sempurna akan cenderung mengabsorpsi radiasi dari sumber radiasi. Demikian juga terjadinya ionisasi atom akan menjadi kesalahan pada SSA oleh karena spektrum radiasi oleh ion jauh berbeda denga spektrum absorpsi atom netral yang memang akan ditentukan. Ada beberapa usaha untuk mengurangi gangguan kimia pada SSA yaitu dengan cara:
1. Menaikkan temperatur nyala agar mempermudah penguraian untuk itu dipakai gas pembakar campuran C2H2 + N2O yang memberikan nyala dengan temperatur yang tinggi.
2. Menambahkan elemen pengikat gugus atom penyangga, sehingga terikat kuat akan tetapi atom yang ditentukan bebas sebagai atom netral. Misalnya penentuan logam yang terikat sebagai garam, dengan penambahan logam yang lainnya akan terjadi ikatan lebih kuat dengan anion pengganggu. 3. Pengeluaran unsur pengganggu dari matriks sampel dengan cara eksitasi
(Mulja, 1995).
2.10. FTIR (Fourier Transform Infra Red)
Salah satu hasil kemajuan instrumentasi IR adalah pemrosesan data seperti Fourier Transform Infra Red (FTIR). Teknik ini memberikan informasi dalam hal kimia, seperti struktur dan konformasional pada polimer dan polipaduan, perubahan induksi tekanan dan reaksi kimia. Dalam teknik ini padatan diuji dengan cara merefleksikan sinar infra merah yang melalui tempat kristal sehingga terjadi kontak dengan permukaan cuplikan. Sensitivitas FTIR adalah 80-200 kali lebih tinggi dari instrumentasi dispersi standar karena resolusinya lebih tinggi (Kroschwitz, 1990).
Teknik pengoperasian FTIR berbeda dengan spektrofotometer infra merah. Pada FTIR digunakan suatu interferometer Michelson sebagai pengganti monokromator yang terletak di depan monokromator. Interferometer ini akan memberikan sinyal ke detektor sesuai dengan intensitas frekuensi vibrasi molekul yang berupa interferogram (Bassler, 1986).
Interferogram juga memberikan informasi yang berdasarkan pada intensitas spektrum dari setiap frekuensi. Informasi yang keluar dari detektor diubah secara digital dalam komputer dan ditransformasikan sebagai domain, tiap-tiap satuan frekuensi dipilih dari interferogram yang lengkap (fourier transform). Kemudian sinyal itu diubah menjadi spektrum IR sederhana. Spektrofotometer FTIR digunakan untuk :
1. Mendeteksi sinyal lemah.
2.11 Reaksi Ikat Silang
Ikatan silang merupakan ikatan yang menghubungkan rantai polimer yang satu dengan rantai polimer yang lain di mana ikatan tersebut berupa ikatan kovalen atau ionik. Reaksi ikat silang memberikan pengaruh yang besar baik dalam sifat kimia maupun sifat mekanik dari polimer (Nicholson, 2006). Pembentukan ikat silang dilakukan dengan penambahan suatu agen pengikat silang ke dalam larutan bahan yang akan dimodifikasi (Berger et al, 2004).
Ikatan silang dapat terjadi dengan dua cara, yaitu dengan membentuk ikatan kovalen dan dengan membentuk ikatan ionik. Dalam reaksi pembentukan ikatan silang kovalen, agen pengikat silang yang umum digunakan adalah dialdehid, contohnya glioksal dan glutaraldehid (Monteiro et al, 1999).
Akan tetapi, kedua agen pengikat silang tersebut bersifat toksik. Glutaraldehid bersifat neurotoksik, sedangkan glioksal bersifat mutagenik. Meskipun hasil modifikasi tersebut dimurnikan sebelum pemberian, keberadaan dialdehid bebas yang tidak ikut bereaksi tidak seluruhnya dapat dihilangkan dan dapat memberikan efek toksik.
Agen pengikat silang kovalen lainnya yang dapat digunakan untuk membentuk reaksi ikat silang dengan kitosan telah banyak diteliti sebagai alternatif pilihan. Di samping dialdehid, asam oksalat dan genipin terbukti dapat digunakan sebagai agen pengikat silang. Akan tetapi, sampai saat ini belum ada data yang lengkap mengenai biokompatibilitas dari senyawa-senyawa tersebut.