21
IV. METODOLOGI
A. DESKRIPSI MAGANG
Kegiatan magang ini dilakukan di Departemen Quality Control PT Frisian Flag Indonesia, yang beralamat di Jalan Raya Bogor Km 26, Ciracas, Jakarta Timur selama empat bulan dari bulan Maret hingga Juni 2012. Kegiatan magang dilakukan setiap hari kerja dengan mengikuti jam kerja perusahan. Salah satu kegiatan magang yang dilakukan adalah pembuatan model kalibrasi sampel
recovery produk susu dengan metode spektroskopi inframerah. Kegiatan tersebut meliputi
pembuatan model kalibrasi untuk penentuan komposisi sampel recovery produk A (produk susu yang memiliki total padatan > 15%) dengan metode spektroskopi Near Infrared Reflectance (NIR) dan penyesuaian model kalibrasi produk B (produk susu yang memiliki total padatan ≤ 15%) untuk penentuan komposisi sampel recovery produk B dengan metode spektroskopi Fourier
Transform Infrared (FTIR).
B. BAHAN DAN ALAT
Bahan baku utama yang digunakan pada kegiatan magang ini adalah sampel recovery dari dua jenis produk susu yaitu produk A yang berasal dari tangki recovery produk A dan produk B dari tangki recovery produk B di PT Frisian Flag Indonesia. Bahan untuk analisis total padatan adalah air destilata. Bahan untuk analisis kadar lemak yaitu air destilata, ammonia 20%, etanol 96%, etanol yang dicampur indikator Brom Cresol Purple (BCP), dietil eter, dan petroleum benzena. Bahan untuk analisis kadar sukrosa yaitu amonia 7%, asam asetat 25%, larutan K4Fe(CN)6, larutan seng asetat, HCl 30%, dan air destilata. Bahan untuk analisis kadar protein
yaitu tablet Kjeldahl (mengandung K2SO4 dan CuSO4), H2SO4 pekat, H2O2 pekat, NaOH 40%,
asam borat 3%, HCl 0.1 N, dan air destilata.
Alat yang digunakan secara umum antara lain neraca analitik, buret, dan pipet Mohr. Instrumen NIRS yang digunakan adalah FOSS NIRSystems 5000 dan instrumen FTIRS yang digunakan adalah FOSS MilkoScan FT120. Alat untuk analisis total padatan meliputi syringe, aluminium dish, dan fiber paper. Alat yang digunakan untuk analisis kadar lemak meliputi tabung Mojonnier, rak tabung Mojonnier, sumbat tabung Mojonnier, shaker, sentrifuge, cawan aluminium, pemanas (hot plate), gegep, oven vakum, dan desikator. Alat untuk analisis kadar sukrosa meliputi labu takar 200 ml, labu takar 50 ml, erlenmeyer 300 ml, thermometer, corong, kertas saring, waterbath, dan polarimeter. Alat yang digunakan untuk analisis kadar protein meliputi syringe, tabung pedal, digestion block, FOSS Digestor, dan alat Kjeltech.
C. METODE PENELITIAN
Kegiatan magang di PT Frisian Flag Indonesia difokuskan pada pembuatan model kalibrasi sampel recovery produk susu dengan metode spektroskopi inframerah. Pembuatan model kalibrasi tersebut terdiri atas (1) pembuatan model kalibrasi untuk penentuan komposisi sampel recovery produk A dengan metode spektroskopi Near Infrared Reflectance (NIR) dan (2) pembuatan model kalibrasi untuk penentuan komposisi sampel recovery produk B dengan metode spektroskopi
22
1. Spektroskopi Near Infrared Reflectance (NIR)
Pembuatan model kalibrasi sampel recovery produk A (produk susu yang memiliki total padatan > 15%) dengan metode spektroskopi NIR dibagi menjadi empat tahap, yaitu (1) persiapan sampel recovery produk A; (2) analisis parameter komposisi sampel recovery produk A menggunakan instrumen FOSS NIRSystems 5000 dan metode konvensional; (3) pembuatan model kalibrasi; dan (4) verifikasi model kalibrasi dengan menggunakan uji t. Garis besar tahap penelitian ini dapat dilihat pada Gambar 10.
Gambar 10. Bagan alir tahapan pembuatan model kalibrasi sampel recovery produk A dengan metode spektroskopi NIR
a. Persiapan Sampel
Persiapan sampel yang dilakukan meliputi pengambilan sampel recovery produk A yang diproduksi oleh PT Frisian Flag Indonesia. Sampel recovery produk A yang digunakan terdiri atas dua varian yaitu varian X dan Y. Sampel recovery produk A yang
Persiapan sampel recovery produk A
Analisis kadar lemak, protein, total padatan, dan sukrosa
Metode konvensional Instrumen FOSS NIRSystems 5000
Data spektrum sampel recovery
produk A
Model kalibrasi
Verifikasi model kalibrasi
Model kalibrasi terverifikasi Pembuatan model kalibrasi
Data analisis konvensional Sampel recovery produk A
varian-X dan varian-Y
23 dibutuhkan untuk pembuatan model kalibrasi metode spektroskopi NIR dengan menggunakan instrumen FOSS NIRSystems 5000 minimal 30 sampel (Mark & Campbell 2008) dan untuk verifikasi minimal 10 sampel (Santoso 2009). Pada penelitian ini digunakan 2/3 sampel recovery produk A varian X dan 1/3 sampel recovery produk A varian Y. Pengambilan sampel dilakukan selama 8 minggu.
Sampel recovery produk A yang dianalisis berasal dari tangki recovery. Tangki
recovery yang terdapat di PT Frisian Flag dikelompokan berdasarkan jenis produk dan
varian rasa. Pada penelitian ini sampel recovery yang dianalisis berasal dari tangki recovery A. Sampel recovery diambil dari dalam tangki recovery dengan sample cock. Sebelum sampel diambil, sample cock harus dipastikan dalam keadaan bersih untuk menghindari kontaminasi. Selanjutnya isi dalam tangki recovery dihomogenkan, diambil sampel
recoverynya, dan diisikan ke dalam botol steril.
b. Analisis Parameter Komposisi Sampel
Analisis dilakukan terhadap parameter komposisi seperti total padatan, kadar lemak, sukrosa, dan protein pada sampel recovery produk A dengan menggunakan instrumen dan metode konvensional.
i. Instrumen
Sampel recovery produk A dianalisis menggunakan instrumen NIRS yaitu FOSS NIRSystems 5000. Hal ini dikarenakan sampel recovery produk A memiliki total padatan > 15% dan dikhawatirkan apabila dianalisis menggunakan instrumen FTIRS dapat menyebabkan kerusakan pada pompa di instrumen tersebut. Analisis menggunakan instrumen NIRS diawali dengan dihomogenkannya sampel recovery produk A yang akan dianalisis. Kemudian program ISIscan dipilih untuk analisis/pembacaan komposisi sampel. Selanjutnya dipilih equation yang digunakan untuk pembuatan model kalibrasi. Sampel recovery produk A varian X dan Y di scan menggunakan equation yang sama. Sebelum pembacaan dimulai, terlebih dahulu
ceramic reference dipastikan telah berada pada tempat scan. Selanjutnya tombol “Scan”
diklik, kode sampel yang dianalisis diisikan pada kotak yang tersedia, dan tombol “Continue” diklik. Pembacaan reference dilakukan terlebih dahulu kemudian dilanjutkan pembacaan sampel.
Pembacaan sampel dilakukan setelah muncul kotak dialog pada layar komputer “Sample”. Sampel diletakkan pada kuvet sampel dan ditekan dengan fiber-optic probe. Kuvet harus dipastikan dalam keadaan bersih dan tidak terdapat gelembung saat ditekan dengan fiber-optic probe. Hal ini dikarenakan gelembung tersebut dapat mengganggu pembacaan sampel saat dianalisis. Kemudian reference dipindahkan dari tempat scan, diganti dengan kuvet yang berisi sampel, dan tombol “Enter” ditekan. Instrumen NIRS dipastikan dalam keadaan tertutup pada saat pembacaan reference dan sampel. Sampel
recovery dilewati oleh sinar inframerah dekat (NIR) yang memiliki panjang gelombang
780 – 2500 nm (Cen & He 2007). Setelah pembacaan sampel selesai, kuvet selanjutnya dikeluarkan dari instrumen NIRS dan dibersihkan.
Data yang dihasilkan dari pembacaan sampel recovery produk A menggunakan instrumen NIRS berupa data kuantitatif parameter komposisi. Hal ini dikarenakan penggunaan model kalibrasi yang sudah ada pada instrumen NIRS untuk pembacaan
24 komposisi sampel recovery produk A. Namun, data kuantitatif ini hanya digunakan untuk melihat apakah hasil pembacaan instrumen NIRS berbeda dengan hasil metode konvensional. Data yang akan digunakan untuk pembuatan model kalibrasi adalah data spektrum masing-masing sampel yang juga terekam oleh instrumen NIRS saat pembacaan sampel.
ii. Metode Konvensional
Setelah sampel recovery produk A dianalisis dengan instrumen NIRS, selanjutnya dilakukan analisis menggunakan metode konvensional yang dilakukan secara duplo setiap sampel. Metode konvensional yang digunakan antara lain metode Roese-Göttlieb atau metode Mojonnier untuk analisis kadar lemak (AOAC 2006), metode Kjeldahl untuk analisis kadar protein (AOAC 2006), total padatan dengan fiber
paper (AOAC 2006), dan metode polarimetri untuk pengukuran kadar sukrosa (IDF
2004). Karena digunakan dua varian sampel recovery produk A, hasil analisis metode konvensional selanjutnya dilakukan uji t pada keempat parameter komposisi sampel
recovery produk A. Hal ini bertujuan untuk melihat apakah kedua data analisis
konvensional tesebut dapat digabungkan untuk membuat model kalibrasi sampel
recovery produk A.
Sebelum dilakukan uji t, terlebih dahulu dilakukan uji kenormalan data analisis menggunakan SPSS 16.0. Uji t yang digunakan adalah uji t: two-sample assuming
unequal variances dengan P (two tail) karena selisih mean yang signifikan dapat
bersifat negatif atau positif. Apabila hasil uji t menunjukkan Thitung ≤ Ttabel ( α;df) atau nilai
P (two tail) > 0.05, maka H0 diterima (Efendi & Miranto 2008).
Hipotesis dari uji t varian sampel recovery produk A adalah:
H0 : hasil analisis konvensional sampel recovery produk A varian X tidak
berbeda nyata dengan sampel recovery produk A varian Y
H1 : hasil analisis konvensional sampel recovery produk A varian X berbeda
nyata dengan sampel recovery produk A varian Y
c. Pembuatan Model Kalibrasi
Setelah diperoleh data spektrum dari pembacaan instrumen NIRS dan data analisis metode konvensional, selanjutnya dilakukan pembuatan model kalibrasi dengan menggunakan software bawaan instrumen NIRS yaitu WinISI. Data spektrum panjang gelombang dari masing-masing sampel yang mencakup empat parameter komposisi (kadar lemak, protein, total padatan, dan sukrosa) terekam oleh instrumen NIRS dan diperlukan untuk pengolahan data. Data spektrum metode spektroskopi NIR dan data analisis metode konvensional selanjutnya diolah menjadi model kalibrasi dengan bantuan software WinISI berdasarkan analisis multivariate. Model kalibrasi tersebut merupakan hubungan antara data analisis metode konvensional dan data yang diperoleh menggunakan metode spektroskopi NIR (Restaino et al. 2009). Model kalibrasi selanjutnya dievaluasi berdasarkan koefisien determinasi kalibrasi (R2), standard error of calibration (SEC),
standard error of cross validation (SECV), dan koefisien determinasi pada cross validation
25
d. Verifikasi Model Kalibrasi
Model kalibrasi yang telah diperoleh selanjutnya diverifikasi menggunakan sampel
recovery produk A varian X dan Y. Tahap verifikasi model kalibrasi dilakukan dengan
membandingkan data masing-masing parameter komposisi sampel recovery produk A yang dihasilkan instrumen NIRS menggunakan model kalibrasi baru dengan data analisis metode konvensional. Data pembacaan instrumen diperoleh dengan men-scan sampel recovery produk A dengan instrumen NIRS. Kemudian sampel recovery produk A dianalisis menggunakan metode konvensional untuk keempat parameter komposisi. Jumlah sampel
recovery yang digunakan pada tahap verifikasi ini adalah 10 sampel (Santoso 2009).
Verifikasi model kalibrasi dilakukan dengan analisis bivariate menggunakan uji t untuk menganalisis dan melihat perbedaan atau hubungan antara dua variabel (Santoso 2009). Analisis bivariate digunakan untuk mengetahui perbedaan antara data instrumen NIRS dengan data analisis metode konvensional. Sebelum dilakukan uji t, terlebih dahulu dilakukan uji kenormalan data analisis menggunakan SPSS 16.0. Sebaran data analisis yang normal selanjutnya dihitung nilai uji t dengan Microsoft Excel 2007. Uji t yang digunakan adalah uji t berpasangan (paired t-test) dengan P (two tail) karena selisih mean yang signifikan dapat bersifat negatif atau positif. Apabila hasil uji t menunjukkan Thitung ≤ Ttabel ( α;df) atau nilai P (two tail) > 0.05, maka H0 diterima (Efendi & Miranto 2008).
Hipotesis dari verifikasi model dengan uji t adalah:
H0 : hasil analisis NIRS tidak berbeda nyata dengan hasil analisis metode
konvensional
H1 : hasil analisis NIR berbeda nyata dengan hasil analisis metode konvensional
2. Spektroskopi Fourier Transform Infrared (FTIR)
Pembuatan model kalibrasi sampel recovery produk B (produk susu yang memiliki total padatan ≤ 15%) dengan metode spektroskopi FTIR dibagi menjadi lima tahap, yaitu (1) persiapan sampel recovery produk B; (2) analisis parameter komposisi sampel recovery produk B menggunakan instrumen FOSS MilkoScan FT120 dan metode konvensional; (3) verifikasi awal model kalibrasi yang digunakan dengan uji t; (4) penyesuaian model kalibrasi; dan (5) verifikasi model kalibrasi yang telah sesuai dengan menggunakan uji t. Garis besar tahap penelitian ini dapat dilihat pada Gambar 11.
26
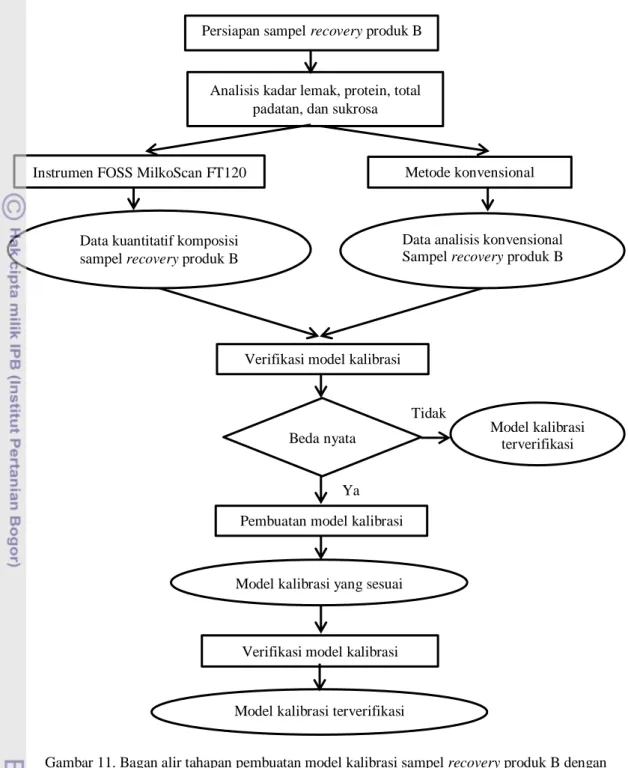
Gambar 11. Bagan alir tahapan pembuatan model kalibrasi sampel recovery produk B dengan metode spektroskopi FTIR
a. Persiapan Sampel
Persiapan sampel yang dilakukan meliputi pengambilan sampel recovery produk B yang diproduksi oleh PT Frisian Flag Indonesia. Sampel recovery produk B yang dibutuhkan untuk verifikasi model kalibrasi metode spektroskopi FTIR minimal 10 sampel (Santoso 2009) menggunakan instrumen FOSS MilkoScan FT120. Pengambilan sampel dilakukan selama 2 minggu.
Sampel recovery yang dianalisis berasal dari tangki recovery B yang terdapat di PT Frisian Flag Indonesia. Sampel recovery diambil dari dalam tangki recovery dengan sample
cock. Sebelum sampel diambil, sample cock harus dipastikan dalam keadaan bersih untuk
Persiapan sampel recovery produk B
Analisis kadar lemak, protein, total padatan, dan sukrosa
Metode konvensional Instrumen FOSS MilkoScan FT120
Data kuantitatif komposisi sampel recovery produk B
Model kalibrasi yang sesuai
Verifikasi model kalibrasi
Model kalibrasi terverifikasi Verifikasi model kalibrasi
Data analisis konvensional Sampel recovery produk B
Beda nyata
Tidak
Ya
Model kalibrasi terverifikasi
27 menghindari kontaminasi. Selanjutnya isi dalam tangki recovery dihomogenkan, diambil sampel recoverynya, dan diisikan ke dalam botol steril.
b. Analisis Parameter Komposisi Sampel
Analisis dilakukan terhadap parameter komposisi seperti total padatan, kadar lemak, sukrosa, dan protein pada sampel recovery produk B dengan menggunakan instrumen dan metode konvensional.
i. Instrumen
Sampel recovery produk B dianalisis menggunakan instrumen FTIRS yaitu FOSS MilkoScan FT120. Hal ini dikarenakan sampel recovery produk B memiliki total padatan ≤ 15%. Persiapan sampel recovery produk B dilakukan sebelum dianalis menggunakan instrumen FTIRS. Sampel yang berada dalam botol steril selanjutnya dikocok terlebih dahulu agar homogen. Kemudian program ISIscan dipilih untuk analisis/pembacaan komposisi sampel. Selanjutnya dipilih equation yang digunakan untuk pembuatan model kalibrasi. Menu “Analysis” dipilih, kode sampel yang dianalisis diisikan pada kotak yang tersedia, pompa dimasukkan ke dalam botol sampel, dan tombol “Scan” diklik. Hasil pembacaan instrumen FTIRS terlihat di layar komputer yang tersambung dengan instrumen FTIRS.
Data yang dihasilkan dari pembacaan sampel recovery produk B menggunakan instrumen FTIRS berupa data kuantitatif parameter komposisi. Hal ini dikarenakan penggunaan model kalibrasi yang sudah ada pada instrumen FTIRS untuk pembacaan komposisi sampel recovery produk B. Data kuantitatif parameter komposisi ini selanjutnya dibandingkan dengan hasil metode konvensional sebagai tahapan verifikasi awal.
ii. Metode Konvensional
Setelah sampel recovery produk B dianalisis dengan instrumen FTIRS, selanjutnya dilakukan analisis menggunakan metode konvensional yang dilakukan secara duplo setiap sampel. Metode konvensional yang digunakan antara lain metode Roese-Göttlieb atau metode Mojonnier untuk analisis kadar lemak (AOAC 2006), metode Kjeldahl untuk analisis kadar protein (AOAC 2006), total padatan dengan fiber
paper (AOAC 2006), dan metode polarimetri untuk pengukuran kadar sukrosa (IDF
2004).
c. Verifikasi Awal Model Kalibrasi
Verifikasi awal dilakukan terhadap data kuantitatif masing-masing parameter komposisi sampel recovery produk B dari pembacaan instrumen FTIRS dan data analisis metode konvensional yang diperoleh. Data pembacaan instrumen diperoleh dengan
men-scan sampel recovery produk B menggunakan model kalibrasi yang telah ada sebelumnya.
Kemudian sampel recovery produk B dianalisis menggunakan metode konvensional untuk keempat parameter komposisi. Jumlah sampel recovery yang digunakan pada tahap verifikasi ini minimal 10 sampel.
28 Sebelum dilakukan uji t, terlebih dahulu dilakukan uji kenormalan data analisis menggunakan SPSS 16.0. Sebaran data analisis yang normal selanjutnya dihitung nilai uji t dengan Microsoft Excel 2007 dengan menggunakan uji t berpasangan (paired t-test) dengan P (two tail) karena selisih mean yang signifikan dapat bersifat negatif atau positif. Apabila hasil uji t menunjukkan Thitung ≤ Ttabel (α;df) atau nilai P (two tail) > 0.05, maka H0 diterima
(Efendi & Miranto 2008).
Hipotesis dari verifikasi model dengan uji t adalah:
H0 : hasil analisis FTIRS tidak berbeda nyata dengan hasil analisis metode
konvensional
H1 : hasil analisis FTIRS berbeda nyata dengan hasil analisis metode konvensional.
Apabila verifikasi model kalibrasi yang digunakan untuk menentukan parameter komposisi sampel recovery produk B menunjukkan hasil analisis FTIR tidak berbeda nyata dengan hasil analisis metode konvensional, maka model kalibrasi tersebut sesuai digunakan untuk penentuan parameter komposisi sampel recovery produk B. Namun, apabila verifikasi model kalibrasi yang digunakan untuk menentukan parameter komposisi sampel
recovery produk B tersebut menunjukkan hasil analisis FTIR berbeda nyata dengan hasil
analisis metode konvensional, maka model kalibrasi tersebut tidak sesuai digunakan untuk penentuan parameter komposisi sampel recovery produk B. Oleh sebab itu, perlu dilakukan penyesuaian model kalibrasi yang digunakan dengan sampel recovery produk B agar dapat digunakan untuk penentuan parameter komposisi sampel recovery produk B.
d. Pembuatan Model Kalibrasi
Penyesuaian model kalibrasi dilakukan apabila verifikasi model kalibrasi yang digunakan untuk menentukan parameter komposisi sampel recovery produk B tersebut menunjukkan hasil analisis FTIR berbeda nyata dengan hasil analisis metode konvensional. Sampel recovery produk B memiliki spektrum, sifat fisik dan komposisi kimia yang hampir sama dengan produk produk B. Oleh sebab itu, pembuatan model kalibrasi sampel recovery produk B tidak dilakukan dengan menggunakan spektrum sampel melainkan dengan penyesuaian model kalibrasi yang telah yang digunakan. Jumlah sampel yang diperlukan minimal 10 sampel (FOSS 2005).
Data analisis sampel recovery produk B menggunakan instrumen FTIRS dan data analisis metode konvensional selanjutnya diolah menjadi model kalibrasi dengan bantuan
software WinISI. Metode yang digunakan untuk pembuatan model kalibrasi baru pada
metode spektroskopi FTIR adalah adjustment slope and intercept. Model kalibrasi baru tersebut selanjutnya dievaluasi berdasarkan koefisien determinasi kalibrasi (R2) dan
standard error of calibration (SEC) (Decandia et al. 2009).
e. Verifikasi Model Kalibrasi
Model kalibrasi yang telah sesuai untuk sampel recovery produk B selanjutnya diverifikasi. Tahap verifikasi model kalibrasi dilakukan dengan membandingkan data yang dihasilkan instrumen FTIRS menggunakan model kalibrasi baru dengan data analisis metode konvensional. Jumlah sampel recovery yang digunakan pada tahap verifikasi ini adalah 10 sampel. Tahap verifikasi model kalibrasi yang telah sesuai ini menggunakan uji t berpasangan (paired t-test) seperti yang digunakan pada tahap verifikasi awal.
29
3. Prosedur Analisis
a. Total Padatan (AOAC 990.19, 2006)
Penetapan total padatan pada sampel recovery dilakukan dengan menggunakan fiber
paper yang selanjutnya dikeringkan di oven. Total padatan sampel recovery ditentukan
dengan menimbang sampel, mengeringkannya, dan menimbang residu sampel yang telah dikeringkan. Terlebih dahulu dua lembar fiber paper dibuat persegi (2 x 2 cm) dan diletakkan di atas aluminium dish yang selanjutnya dimasukkan ke dalam oven bersuhu 102°C selama 15 menit. Selanjutnya fiber paper beserta aluminium dish dikeluarkan dan didiamkan selama 2 menit, kemudian ditimbang. Sebanyak 1 gram sampel recovery dari botol sampel diambil menggunakan syringe, ditimbang dengan bantuan alat penyangga
syringe, dan kemudian tekan tanda “Tare”. Sampel kemudian diteteskan pada selembar fiber paper dan ditutup dengan lembar fiber paper lainnya. Selanjutnya syringe ditimbang
kembali dan dicatat sebagai Bobot sampel. Fiber paper beserta aluminium dish yang telah berisi sampel selanjutnya dikeringkan dalam oven bersuhu 102°C selama 30 menit, dikeluarkan, aluminium dish dilipat, dan didiamkan selama 2 menit. Bobot sampel yang telah dikeringkan kemudian ditimbang. Total padatan dalam sampel dihitung dengan persamaan :
%
Total Padatan=
A-BBobot sampel setelah pengenceran
x FP x 100%
(7)dimana :
A = bobot dish setelah pengeringan B = bobot dish sebelum pengeringan FP = Bobot (sampel air)
Bobot sampel
b. Kadar Lemak (AOAC 989.05, 2006)
Metode yang digunakan pada penetapan kadar lemak adalah metode Roese- Göttlieb atau metode Mojonnier. Prinsip metode ini adalah gravimetri dengan menggunakan alat
Mojonnier Tester. Sampel recovery ditimbang sebanyak 10 gram dengan bantuan syringe
dan dimasukkan ke dalam tabung Mojonnier. Selanjutnya ditambahkan 2 ml ammonia 20% yang berfungsi untuk melarutkan protein dan 10 ml etanol yang dicampur dengan indikator
Brom Cresol Purple (BCP) kemudian diekstrak dengan 20 ml dietil eter dan 20 ml
petroleum benzena, lalu disentrifugasi selama 2 menit dengan kecepatan 530 rpm. Setiap penambahan pereaksi, tabung Mojonnier disumbat lalu dikocok dengan shaker. Pada proses sentifugasi dihasilkan dua lapisan, yaitu lapisan atas (supernatan) yang jernih dan lapisan bawah. Tahapan ekstraksi pada lapisan bawah dilakukan dua kali lagi untuk memperbesar ketelitian. Tahapan ekstraksi kedua dan ketiga sama seperti tahapan ekstraksi pertama hanya berbeda pada penambahan pereaksi. Pada ekstraksi kedua, lapisan bawah hasil ekstraksi pertama ditambahkan 5 ml etanol 96%, 20 ml dietil eter, dan 20 ml petroleum benzena sedangkan pada ekstraksi ketiga ditambahkan 15 ml dietil eter dan 15 ml petroleum benzena. Supernatan dari setiap hasil ekstraksi dimasukkan ke cawan aluminium yang telah diketahui berat kosongnya, dipanaskan di atas pemanas (hot plate) hingga hanya
30 terdapat residu lemak. Selanjutnya cawan aluminium dimasukkan ke dalam oven vakum selama 10 menit dan didinginkan di dalam desikator hingga mencapai berat konstan. Berat residu dinyatakan sebagai persentase lemak yang terdapat dalam sampel susu dan dihitung dengan persamaan:
%
Lemak (w/w)=
–(8)
c. Kadar Sukrosa (IDF 35:2004, 2004)
Metode yang digunakan pada penetapan kadar sukrosa adalah metode polarimetri. Prinsip metode ini adalah mengukur perubahan rotasi optik dengan menggunakan polarimeter. Sampel recovery ditimbang 16.3 gram dan dimasukkan ke dalam labu takar 200 ml. Selanjutnya ditambahkan 50 ml air destilata dan diaduk. Selanjutnya ammonia 7% ditambahkan sebanyak 1 ml, diaduk, dan didiamkan selama 20 menit. Setelah 20 menit, sampel selanjutnya ditambahkan 5 ml asam asetat 25%, 5 ml larutan K4Fe(CN)6, 5 ml
larutan seng asetat, dan air destilata hingga tanda tera pada labu ukur. Larutan sampel tersebut dipastikan harus dikocok setiap penambahan pereaksi.
Sampel yang telah ditambahkan pereaksi selanjutnya disaring melalui kertas saring ke dalam erlenmeyer 300 ml. Erlenmeyer yang digunakan dipastikan dalam keadaan bersih dan kering. Larutan yang disaring disebut P1. Sebanyak 50 ml larutan hasil penyaringan dipindahkan ke dalam labu takar 50 ml, ditambahkan 5 ml HCl 30% untuk menghidrolisis sukrosa sehingga menghasilkan laktosa dan beberapa gula yang tidak mempengaruhi pengukuran, dan dikocok. Larutan sampel dalam labu ukur 50 ml disebut P2. Selanjutnya P2 direndam dalam waterbath 60oC selama 15 menit dan didinginkan hingga suhunya sama dengan suhu larutan P1. Seluruh larutan P2 harus dipastikan terendam. Kadar sukrosa sampel selanjutnya dibaca dengan menggunakan polarimeter pada λ = 546 nm. Adapun perhitungan kadar sukrosa :
%
( )(9)
dimana :
P1 = larutan sampel hasil penyaringan di Erlenmeyer P2 = larutan sampel hasil penyaringan di labu ukur 50 ml K = konstanta (susu cair = 0.00)
1.0402 = gaya berat sukrosa 1.1 = faktor konversi sukrosa
d. Kadar Protein (AOAC 991.20, 2006)
Metode yang digunakan adalah metode Kjeldahl. Metode ini menganalisis kadar protein kasar dalam bahan makanan secara tidak langsung berdasarkan kadar nitrogennya. Persen protein dihitung dengan mengalikan hasil analisis dengan faktor konversi (6.38). Nilai faktor konversi 6.38 berdasarkan pada protein murni yang mengandung 15.67% nitrogen pada produk susu (Winarno 2008). Prinsip metode ini adalah destruksi, destilasi dan titrasi. Dekomposisi senyawa nitrogen organik melalui tahap destruksi dengan asam sulfat pekat dan katalis membentuk ammonium sulfat, kemudian didestilasi dengan natrium hidroksida membentuk gas ammonia yang bereaksi dengan asam borat. Banyaknya asam
31 borat yang bereaksi dengan ammonia dapat diketahui melalui tahap titrasi menggunakan larutan asam klorida dengan indikator Conway (Brom Cresol Green : Metil Merah 1:1). Titik akhir titrasi ditandai dengan terbentuknya warna merah muda.
Sebanyak 2.5 g sampel recovery dimasukkan ke dalam tabung pedal dan diletakkan pada digestion block, kemudian ditambahkan 2 butir tablet Kjeldahl (mengandung K2SO4
dan CuSO4), 20 ml asam sulfat pekat, larutan dikocok hingga larut dan didiamkan selama 5
menit. Scrubber cup dipasangkan pada digestion block dan digestion block diletakkan pada FOSS Digestor, kemudian sampel didestruksi selama 3 jam (1 jam pada suhu 200oC dan 2 jam pada suhu 400oC). Setelah dingin ditambahkan 50 ml air destilata. Tahap selanjutnya yaitu destilasi dilakukan dengan penambahan natrium hidroksida 40%. Gas ammonia yang dihasilkan ditampung dengan menggunakan larutan asam borat 3%. Sampel dititrasi menggunakan HCl 0.1 N dan hasil titrasi ditampilkan di layar alat Kjeltech. Penetapan blanko dilakukan dengan cara yang sama tanpa menggunakan sampel. Adapun perhitungan kadar protein:
Protein
( - )
(10) dimana: N HCl = normalitas HCl 0.1 N BM = berat molekul protein
FK = Faktor konversi (untuk susu = 6.38)
4. Analisis Statistik
a. Standard Error of Calibration (SEC) (EMEA 2012)
Standard Error of Calibration (SEC) adalah perhitungan statistik yang menghitung
perbedaan antara nilai prediksi NIRS dengan nilai hasil pengukuran menggunakan metode konvensional pada tahap kalibrasi. Pada tahap kalibrasi metode spektroskopi NIRS digunakan 2/3 data dari keseluruhan sampel. SEC < 1% menunjukkan model yang semakin baik. Standard Error of Calibration (SEC) diperoleh dengan menggunakan persamaan sebagai berikut:
√
∑-
-
(11)
dimana:
Ylab = nilai hasil analisis metode konvensional
YNIR = nilai hasil analisis metode NIR
n = jumlah sampel
32
b. Standard Error of Cross Validation (SECV) (EMEA 2012)
Standard Error of Cross Validation (SECV) adalah perhitungan statistik yang
menghitung perbedaan antara nilai prediksi NIRS dengan nilai hasil pengukuran menggunakan metode konvensional untuk pembuatan validasi silang. Cross Validation merupakan teknik validasi internal yang digunakan untuk optimasi/memilih model kalibrasi. Validasi merupakan tahap untuk meyakinkan model kalibrasi yang telah terbentuk. Validasi internal dilakukan dengan melakukan sampling ulang data statistik secara acak (1/3 data dari keseluruhan sampel) yang digunakan untuk kalibrasi dan diberlakukan berbagai macam proses statistik untuk mengidentifikasi model kalibrasi (dilakukan oleh software) yang sesuai dengan data yang ada (EMEA 2012). SECV < 1% menunjukkan model yang semakin baik. Standard Error of Cross Validation (SECV) diperoleh dengan menggunakan persamaan sebagai berikut:
√
∑ - (12)dimana:
Ylab = nilai hasil analisis metode konvensional
YNIR = nilai hasil analisis metode NIR
n = jumlah sampel
c. Koefisien Determinasi Kalibrasi (R
2) dan Cross Validation (1-VR)
(Wahyono 2010)
Koefisien determinasi menunjukkan kemampuan model menerangkan keragaman nilai peubah tak bebas. Semakin besar nilai R2 dan 1-VRmaka model semakin mampu menerangkan perilaku peubah tidak bebas. Data yang digunakan untuk perhitungan nilai R2 adalah data yang digunakan untuk perhitungan pada tahap kalibrasi, sedangkan data yang digunakan untuk perhitungan nilai 1-VR adalah data untuk perhitungan validasi silang (cross validation). Kisaran nilai R2 dan 1-VRmulai dari 0 hingga 1 (Wahyono 2010). Koefisien determinasi diperoleh dengan menggunakan persamaan sebagai berikut:
Koefisisen Determinasi
(
∑ - ̅ - ̅ √∑ - ̅ ∑ - ̅)
(13) R2 = 1- (SEC/SD)2 (14) 1-VR = 1- (SECV/SD)2 (15) dimana:Ylab = nilai hasil analisis metode konvensional
YNIR = nilai hasil analisis metode NIR
̅
= rata-rata hasil analisis metode konvensional̅
= rata-rata hasil analisis metode NIR R2 = koefisien determinasi kalibrasi 1-VR = koefisien determinasi cross validation33 SEC = Standard Error of Calibration
SECV = Standard Error of Cross Validation SD = standar deviasi
d. Bias (EMEA 2012)
Bias adalah rata-rata error yang dihasilkan antara hasil analisis metode spektroskopi
dengan hasil analisis metode konvensional. Kisaran nilai bias adalah 0-1 dan dapat dihitung dengan persamaan:
Bias
=
∑ ̅ (16)dimana:
Ymanual = nilai hasil analisis metode konvensional
ȲFTIR = nilai rata-rata hasil analisis metode FTIR
n = jumlah sampel
e. Uji T: Two Sample Assuming Unequal Variances (Shier 2004)
Uji t ini sering disebut juga Welch‟s t-test dan digunakan untuk membandingkan dua varian populasi yang dianggap berbeda (jumlah sampel mungkin tidak sama) (Shier 2004). Rumus yang digunakan untuk perhitungan Welch‟s t-test adalah:
t
̅̅̅̅
̅̅̅̅
̅̅̅̅ ̅̅̅̅ (17) dimana:̅ =
rata-rata sampel X̅̅̅̅ X1 ̅̅̅̅2=√
f. Uji T Berpasangan/ Paired T-Test (Shier 2004)
Uji t berpasangan digunakan untuk membadingkan dua populasi rata-rata yang dihasilkan dari satu sampel yang mengalami dua perlakuan berbeda (Shier 2004). Rumus yang digunakan untuk perhitungan uji t berpasangan adalah:
t =
S
d̅
d
√n
⁄
(18)dimana: