DAFTAR PUSTAKA DAFTAR PUSTAKA Anggraeny, Dian, (2005),
Anggraeny, Dian, (2005), Pengaruh Cu(II) dalam Penentuan FePengaruh Cu(II) dalam Penentuan Fe pada pH 4,5 dan pH 8,0 dengan pengompleks pada pH 4,5 dan pH 8,0 dengan pengompleks Ortofeantrolin secara Spektrofotometri UV-Vis, Ortofeantrolin secara Spektrofotometri UV-Vis, Skripsi, Jurusan Kimia, FMIPA, ITS, Surabaya
Skripsi, Jurusan Kimia, FMIPA, ITS, Surabaya Amelia, (2004),
Amelia, (2004), Optimasi pH Buffer Asetat dan KonsentrasiOptimasi pH Buffer Asetat dan Konsentrasi Larutan Pereduksi Natrium Tiosulfat dalam Penentuan Larutan Pereduksi Natrium Tiosulfat dalam Penentuan
Kadar Besi Secara Spektrofotometri UV-Vis,
Kadar Besi Secara Spektrofotometri UV-Vis, TugasTugas Akhir Kimia ITS, Surabaya
Akhir Kimia ITS, Surabaya Arsyad, M. Natsir, (2000),
Arsyad, M. Natsir, (2000), Kamus Kimia Arti dan PenjelasanKamus Kimia Arti dan Penjelasan Istilah
Istilah, PT. Gramedia Pustaka Utama, Jakarta, PT. Gramedia Pustaka Utama, Jakarta Brady, James E., (1999),
Brady, James E., (1999), Kimia Universitas: Asas dan Struktur,Kimia Universitas: Asas dan Struktur, Jilid 1, Binarupa Aksara, Jakarta
Jilid 1, Binarupa Aksara, Jakarta Cotton, F.A, dan Wilkinson G., (1989),
Cotton, F.A, dan Wilkinson G., (1989), Kimia Anorganik Dasar Kimia Anorganik Dasar ,, UI-Press , Jakarta
UI-Press , Jakarta
Day, F.A., Underwood A.L., (1993),
Day, F.A., Underwood A.L., (1993), Analisa Kimia Kuantitatif Analisa Kimia Kuantitatif ,, Terjemahan Oleh Pudjaatmaka, A.H., Edisi Keempat, Terjemahan Oleh Pudjaatmaka, A.H., Edisi Keempat, Erlangga, Jakarta
Erlangga, Jakarta Friest, J., H. Getrost, (1977),
Friest, J., H. Getrost, (1977), Organic Reagent For TraceOrganic Reagent For Trace Analysis
Analysis, Darmstadt, E.Merck , Darmstadt, E.Merck Harris, Daniel C. (2003).
Harris, Daniel C. (2003). Quantitative Chemical AnalysisQuantitative Chemical Analysis, , 66thth Edition. Saunders College Publishing. Santa Barbara Edition. Saunders College Publishing. Santa Barbara Iswanto, Mansuri, A. (2003).
Iswanto, Mansuri, A. (2003). Besi Nutrisi yang BergunaBesi Nutrisi yang Berguna Sekaligus Berbahaya
Sekaligus Berbahaya. Tugas Akhir Kimia ITS.. Tugas Akhir Kimia ITS. Surabaya
Surabaya Khopkar, S.M., (1990),
Khopkar, S.M., (1990),Konsep Kimia Analitik Konsep Kimia Analitik , UI-Press, Jakarta, UI-Press, Jakarta Kumar, T.N Kiran, Revanasiddappa, H. D., (2005), Kumar, T.N Kiran, Revanasiddappa, H. D., (2005), Spectrophotometric Determination of Vanadium Using Spectrophotometric Determination of Vanadium Using Variamine Blue and Its Application to Synthetic, Variamine Blue and Its Application to Synthetic, Environmental and Biological Sample,
Environmental and Biological Sample,Journal of TheJournal of The Iranian Chemical Society, Vol. 2, No.2
Iranian Chemical Society, Vol. 2, No.2 Malik, Ashok Kumar, (2000),
Malik, Ashok Kumar, (2000), Direct Spectrophotometric Direct Spectrophotometric Determination of Ferbam Iron (III) Determination of Ferbam Iron (III)
39 39
Dimethyldithiocarbanat In Commercial Sample and Dimethyldithiocarbanat In Commercial Sample and
Wheat Grains Using
4,7-Diphenyl-1,10-Wheat Grains Using
4,7-Diphenyl-1,10-Phenanthroline
Phenanthroline, Joiurnal of Agricultural and Food, Joiurnal of Agricultural and Food Chemistry, Vol. 48, No.12, pp
Chemistry, Vol. 48, No.12, pp 5808-5811, India5808-5811, India Miller, J.C., dan Miller J.N. (1991).
Miller, J.C., dan Miller J.N. (1991). Statistik Untuk KimiaStatistik Untuk Kimia Analitik
Analitik . Edisi Kedua. Penerbit ITB. Bandung. Edisi Kedua. Penerbit ITB. Bandung Othmer, Kirk, (1978),
Othmer, Kirk, (1978), Encyclopedia of Chemical Technology Encyclopedia of Chemical Technology, 3, 3rdrd Edition, Vol. 13, John Willey and Sons Inc,
Edition, Vol. 13, John Willey and Sons Inc, New York New York Rivai, Harrizul, (1995),
Rivai, Harrizul, (1995), Asas Pemeriksaan Kimia Asas Pemeriksaan Kimia, UI-Press,, UI-Press, Jakarta
Jakarta
Sandell, E.B., (1959),
Sandell, E.B., (1959), Colorimetric Determination Trace of Colorimetric Determination Trace of Metal
Metal, , 33rdrd Edition, Inter Science Publisher Inc., NewEdition, Inter Science Publisher Inc., New York
York
Singh, Mono M., Ronald M. Pike, Zvi Scafran, (1995), Singh, Mono M., Ronald M. Pike, Zvi Scafran, (1995),
Microscale and Selected Macroscale Experiments for Microscale and Selected Macroscale Experiments for General and Advanced General Chemistry; An General and Advanced General Chemistry; An Innovative Approach
Innovative Approach, Willey, Seoul, Korea, Willey, Seoul, Korea
Skoog, Douglas A.; West, Donald M.; Holler J., (1996), Skoog, Douglas A.; West, Donald M.; Holler J., (1996),
Fundamentals of Analytical Chemistry,
Fundamentals of Analytical Chemistry, Edisi Ketujuh,Edisi Ketujuh, Saunders College Publishing, New York
Saunders College Publishing, New York Subiyakto, Markus G., (2001),
Subiyakto, Markus G., (2001), Kimia dan Fotografi Hitam PutihKimia dan Fotografi Hitam Putih,, Harian Kompas, Jakarta
Harian Kompas, Jakarta Thomas, M., (1996),
Thomas, M., (1996), Ultraviolet and Visible SpectroscopyUltraviolet and Visible Spectroscopy, John, John Willey and Sons Inc., Ukraina
Willey and Sons Inc., Ukraina Vogel, (1985),
Vogel, (1985), Buku Teks Analisa Anorganik Kualitatif MakroBuku Teks Analisa Anorganik Kualitatif Makro dan Semimikro (Terjemahan oleh Setiono L., dan Semimikro (Terjemahan oleh Setiono L., Pudjaatmaka A.H)
Pudjaatmaka A.H), Edisi Kelima, PT. Kalman Media, Edisi Kelima, PT. Kalman Media Pustaka, Jakarta
Pustaka, Jakarta
39 39
Dimethyldithiocarbanat In Commercial Sample and Dimethyldithiocarbanat In Commercial Sample and
Wheat Grains Using
4,7-Diphenyl-1,10-Wheat Grains Using
4,7-Diphenyl-1,10-Phenanthroline
Phenanthroline, Joiurnal of Agricultural and Food, Joiurnal of Agricultural and Food Chemistry, Vol. 48, No.12, pp
Chemistry, Vol. 48, No.12, pp 5808-5811, India5808-5811, India Miller, J.C., dan Miller J.N. (1991).
Miller, J.C., dan Miller J.N. (1991). Statistik Untuk KimiaStatistik Untuk Kimia Analitik
Analitik . Edisi Kedua. Penerbit ITB. Bandung. Edisi Kedua. Penerbit ITB. Bandung Othmer, Kirk, (1978),
Othmer, Kirk, (1978), Encyclopedia of Chemical Technology Encyclopedia of Chemical Technology, 3, 3rdrd Edition, Vol. 13, John Willey and Sons Inc,
Edition, Vol. 13, John Willey and Sons Inc, New York New York Rivai, Harrizul, (1995),
Rivai, Harrizul, (1995), Asas Pemeriksaan Kimia Asas Pemeriksaan Kimia, UI-Press,, UI-Press, Jakarta
Jakarta
Sandell, E.B., (1959),
Sandell, E.B., (1959), Colorimetric Determination Trace of Colorimetric Determination Trace of Metal
Metal, , 33rdrd Edition, Inter Science Publisher Inc., NewEdition, Inter Science Publisher Inc., New York
York
Singh, Mono M., Ronald M. Pike, Zvi Scafran, (1995), Singh, Mono M., Ronald M. Pike, Zvi Scafran, (1995),
Microscale and Selected Macroscale Experiments for Microscale and Selected Macroscale Experiments for General and Advanced General Chemistry; An General and Advanced General Chemistry; An Innovative Approach
Innovative Approach, Willey, Seoul, Korea, Willey, Seoul, Korea
Skoog, Douglas A.; West, Donald M.; Holler J., (1996), Skoog, Douglas A.; West, Donald M.; Holler J., (1996),
Fundamentals of Analytical Chemistry,
Fundamentals of Analytical Chemistry, Edisi Ketujuh,Edisi Ketujuh, Saunders College Publishing, New York
Saunders College Publishing, New York Subiyakto, Markus G., (2001),
Subiyakto, Markus G., (2001), Kimia dan Fotografi Hitam PutihKimia dan Fotografi Hitam Putih,, Harian Kompas, Jakarta
Harian Kompas, Jakarta Thomas, M., (1996),
Thomas, M., (1996), Ultraviolet and Visible SpectroscopyUltraviolet and Visible Spectroscopy, John, John Willey and Sons Inc., Ukraina
Willey and Sons Inc., Ukraina Vogel, (1985),
Vogel, (1985), Buku Teks Analisa Anorganik Kualitatif MakroBuku Teks Analisa Anorganik Kualitatif Makro dan Semimikro (Terjemahan oleh Setiono L., dan Semimikro (Terjemahan oleh Setiono L., Pudjaatmaka A.H)
Pudjaatmaka A.H), Edisi Kelima, PT. Kalman Media, Edisi Kelima, PT. Kalman Media Pustaka, Jakarta
Pustaka, Jakarta
39 39
LAMPIR LAMPIR SKEMA SKEMA AN A AN A K KEERRJJA A ((UU UUMM)) 41 41
LAMPIRAN B SKEMA KERJA
1. Penentuan Panjang Gelombang Maksimum
* Tiap prosedur diulangi sebanyak 3 kali Larutan Standar Fe(III) 100 ppm
•
Dimasukkan sebanyak 0,5 ml ke dalam labu ukur 10 ml•
Ditambah 1,1 ml Na2S2O3100 ppm•
Ditambah 1,5 ml 1,10-fenantrolin 1000 ppm•
Ditambah 1,5 ml larutan buffer asetat pH 4,5•
Ditambah 5 ml aseton•
Diencerkan dengan aqua DM hingga tanda batas•
Dikocok dan didiamkan selama 5 menit•
Diukur absorbansinya pada panjang gelombang 500-600 nm2. Pembuatan Kurva Kalibrasi
a)
Prosedur yang sama juga dilakukan pada volume 0,2; 0,3; 0,4; 0,5 ml larutan standar Fe(III) 100 ppm
* Tiap prosedur diulangi sebanyak 3 kali Larutan Standar Fe(III) 100 ppm a)
•
Dimasukkan sebanyak 0,1 ml ke dalam labu ukur 10 ml•
Ditambah 1,1 ml Na2S2O3100 ppm•
Ditambah 1,5 ml 1,10-fenantrolin 1000 ppm•
Ditambah 1,5 ml larutan buffer asetat pH 4,5•
Ditambah 5 ml aseton•
Diencerkan dengan aqua DM hingga tanda batas•
Dikocok dan didiamkan selama 5 menit•
Diukur absorbansinya pada panjang gelombang maksimum3. Pengaruh ion Co(II)
a)
Prosedur yang sama juga dilakukan pada 0,05 ml; 0,06 ml; 0,07 ml; 0,08 ml; 0,09 ml; 0,10 ml larutan Co(II) 10 ppm. 0,02 ml; 0,04 ml; 0,06 ml; 0,08 ml larutan Co(II) 100 ppm. 0,02 ml; 0,04 ml; 0,06 ml; 0,08 ml; 0,10 ml larutan Co(II) 1000 ppm.
* Tiap prosedur diulangi sebanyak 3 kali. Larutan Standar Fe III 100 m
•
Dimasukkan sebanyak 0,5 ml ke dalam labu ukur 10 ml•
Ditambah 0,00 ml larutan Co(II) 10 ppma)•
Ditambah 1,1 ml Na2S2O3100 ppm•
Ditambah 1,5 ml larutan buffer asetat pH 4,5•
Ditambah 1,5 ml 1,10-fenantrolin 1000 ppm•
Ditambah 5 ml aseton•
Diencerkan dengan aqua DM hingga tanda batas•
Di dikocok dan didiamkan selama 5 menit•
Diukur absorbansinya pada panjang gelombangmaksimum Diperoleh % Recovery
LAMPIRAN C
PEMBUATAN LARUTAN STANDAR BESI (III) 100 ppm Larutan standar dibuat dengan melarutkan 0,0483 gr FeCl3.6H2O dalam 10 ml aqua DM, kemudian diencerkan hingga
volume larutan 100 ml sehingga diperoleh larutan standar besi(III) 100 ppm. Larutan stok 100 ppm diperoleh dengan perhitungan sebagai berikut:
100 ppm = 100 mg/ L = 10 mg/100 mL 3 MrFeCl ArFe = O H beratFeCl beratFe 2 3
.
6
mol gr x x mol gr / )) 18 6 ( ) 5 , 35 3 ( 56 ( / 56+
+
= x mg 10 mol gr mol gr / 5 , 270 / 56 = x mg 10 x = 0,0483 gr FeCl3.6H2OLarutan kerja yang digunakan adalah larutan standar kerja dengan kandungan Fe 5, 10, 20, 30, 40, dan 50 mg, yang dibuat dengan mengencerkan karutan kerja Fe 100 ppm dengan volume ambil sesuai perhitungan hingga volume menjadi 10 mL, perhitungannya sebagai berikut:
V1.M1= V2.M2
Dimana, V1= volume larutan standar Fe 100 ppm
V2= volume larutan kerja Fe
M1= konsentrasi larutan standar Fe 100 ppm
Jadi, volume ambil larutan kerja Fe 100 ppm adalah seperti pada Tabel B.1.
Tabel B.1 Pembuatan larutan kerja Fe(III) Konsentrasi Larutan
Standar Fe(III) (ppm)
Kandungan Fe (mg) Volume ambil Larutan kerja Fe 100 ppm (mL) 1,0 2,0 3,0 4,0 5,0 10 20 30 40 50 0,10 0,20 0,30 0,40 0,50
LAMPIRAN D
PEMBUATAN LARUTAN KERJA Na2S2O3100 ppm
Larutan Na2S2O3 dibuat dengan cara melarutkan kristal Na2S2O3 sebanyak 100 mg dengan aqua DM hingga volume 1 L, sehingga diperoleh larutan kerja Na2S2O3 100 ppm. Perhitungan untuk pembuatan larutan standar adalah sebagai berikut:
a. Na2S2O3100 ppm ppm = mg/L
volume akhir yang diinginkan adalah 1L, maka banyaknya Na2S2O3yang dibutuhkan adalah:
100 ppm = x mg/L
100 ppm = 100 mg/L x 1L 100 ppm = 100 mg
= 0,1 gr
Jadi, banyaknya kristal Na2S2O3yang harus dilarutkan untuk mendapatkan 100 ppm Na2S2O3dalam 1L adalah 0,1 gr.
b. Na2S2O311 ppm
Larutan kerja 11 ppm dibuat dengan cara pengenceran dari larutan 100 ppm dengan perhitungan sebagai berikut:
V1.M1= V2.M2
Dimana, V1= volume larutan standar Na2S2O3100 ppm V2= volume larutan kerja Na2S2O311 ppm
M1= konsentrasi larutan standar Na2S2O3100 ppm M2= konsentrasi larutan kerja Na2S2O311 ppm Untuk memperoleh larutan Na2S2O3 11 ppm dalam 10 mL larutan dihitung sebagai berikut:
V1.M1 = V2.M2
V1.100 ppm = 10 mL.11 ppm V1 = 110 /100 V1 = 1,1 mL
Jadi, volume larutan standar Na2S2O3 100 ppm yang diambil untuk membuat larutan standar Na2S2O3 11 ppm adalah 1,1 mL.
LAMPIRAN E
PEMBUATAN LARUTAN PENGOMPLEKS
1,10-FENANTROLIN 1000 ppm
Larutan 1,10-Fenantrolin dibuat dengan melarutkan padatan 1,10-Fenantrolin dengan aqua DM hingga volume 100
mL. Perhitungannya adalah sebagai berikut: Fenantrolin 1000 ppm = 1000 mg/L
= 100 mg/100mL = 0,1 gr/100mL
LAMPIRAN F
PEMBUATAN LARUTAN Co(II) 1000 ppm
Larutan Co(II) dibuat dengan cara melarutkan kristal 0,4037 gr CoCl2.6H2O dalam aqua DM hingga volume 100 mL, sehingga diperoleh larutan Co(II) 1000 ppm. Perhitungannya adalah sebagai berikut:
1000 ppm = 1000 mg/L = 100 mg/1000 mL O H MrCoCl ArCo 2 2.6 = O H beratCoCl beratCo 2 2.6 mol gr x x mol gr / )) 18 6 ( ) 5 , 35 2 ( 93 , 58 ( / 93 , 58
+
+
= x mg 100 mol gr mol gr / 93 , 237 / 93 , 58 = x mg 100 x = 0,4037 gr CoCl2.6H2OLAMPIRAN G
PEMBUATAN LARUTAN BUFFER ASETAT pH 4,5
Larutan buffer asetat pH 4,5 dibuat dengan melarutkan 6,5765 gram Natrium asetat trihidrat (CH3COONa.3H2O) dan 5
ml CH3COOH 99,9% (Ka = 1,75.10-5) dengan Aqua DM sampai
volume 100 ml. Hasil tersebut diperoleh berdasarkan perhitungan sebagai berikut :
99,9% CH3COOH = 99,9 x densitas CH3COOH
100
= 99,9 x 1,049 Kg/L 100
= 1,04795 Kg/L = 1047,95 gr/L Konversi ke molaritas CH3COOH :
[CH3COOH] = 1047,95 gr/L = 17,4658 mol/L
60 gr/mol = 17,4658 M
Konsentrasi CH3COOH dalam 100 ml larutan :
M1.V1 = M2.V2
17,4658.5 = M2. 100
pH = 4,5 +[H] = K a x
[ ]
[ ]
s a C C 10-4,5 = 1,75.10-5 x 0,87329 CgaramC
garam= 0.4833 M
Mol CH3COONa.3H2O dalam 1 L larutan = 0,4833 mol,
Maka massa CH3COONa.3H2O dalam 100 ml larutan adalah :
Massa
CH3COONa.3H2O = mol x Mr x 100 ml1000 ml
= 0.4833 x 136,08083 x 100 ml 1000 ml
= 6,5765 gram
Sehingga, dengan melarutkan 6,5765 gram CH3COONa.3H2O
dan 5 ml CH3COOH 99,9% (Ka = 1,75.10-5) dengan Aqua DM
sampai volume larutan mencapai 100 ml, didapatkan larutan buffer asetat pH 4,5.
LAMPIRAN H
PERHITUNGAN PERSAMAAN REGRESI LINEAR
KURVA KALIBRASI PADA pH 4,5
Berdasarkan hukum Lambert-Beer yang menyatakan bahwa :
A =ε.b.c Dengan : A adalah absorbansi
ε adalah tetapan absorbtivitas molar (apabila c dalam mol/liter)
b adalah tebal medium penyerap (dalam cm) c adalah konsentrasi besi (II) (dalam ppm)
Jika absorbansi (A) sebagai sumbu x dan konsentrasi besi (II) sebagai sumbu y pada kurva larutan standar besi, maka :
B
=∑. ∑.∑
∑
∑
A
=∑∑
Tabel F.1 Perhitungan Persamaan Regresi Linear Kurva Kalibrasi pH 4,5 Konsentrasi Fe(II) (ppm) (X) Absorbansi (Y) X 2 X.Y 0 0.000 0 0 1 0.051 1 0.051 2 0.101 4 0.202 3 0.155 9 0.465 4 0.213 16 0.852 5 0.273 25 1.365 ΣX=15 ΣY= 0.793 ΣX2=55 ΣX.Y=2.935 B =
∑. ∑.∑
∑
∑
= 6 (2,935) – (15.0,793) 6.55 – (15)2 = 0,0544 A =∑∑
= 0,793 – 0,0544.15 6 = -0,003Persamaan Regresi Linear Kurva Kalibrasi Larutan Standar Besi : y = Bx + A
LAMPIRAN I
PERHITUNGAN KOEFISIEN KORELASI KURVA
KALIBRASI PADA pH 4,5
Koefisien Korelasi (r) digunakan untuk memakai seberapa baik kumpulan titik percobaan sesuai dengan garis lurus. Nilai r dihitung dengan menggunakan persamaan :
r =
( )( )
( ) ( )
2 2∑
∑
∑
−
−
−
−
y y x x y y x x Keterangan : r : koefisien korelasi y : absorbansi _x : rata-rata konsentrasi besi (III) _
C(x) A(y) x− x y− y
( )
x− x 2(
y− y)
2 (x
−
x
). ( y−
y) 0 0,000 -2,5 -0,132 6,25 0,01742 0,33 1 0,051 -1,5 -0,081 2,25 0,00656 0,1215 2 0,101 -0,5 -0,031 0,25 0,00096 0,0155 3 0,155 0,5 0,023 0,25 0,00053 0,0115 4 0,213 1,5 0,081 2,25 0,00656 0,1215 5 0,273 2,5 0,141 6,25 0,01988 0,3525x
= 2,5 y= 0,132 Σ= 17,5 Σ= 0,05191 Σ= 0,9525 r =( )( )
( ) ( )
2 2∑
∑
∑
−
−
−
−
y y x x y y x x r = 0,952500 0,2171551 r= 0,999 r 2= 0,998LAMPIRAN J
PERHITUNGAN UJI-t TERHADAP KURVA KALIBRASI Uji t (uji keberartian) digunakan untuk mengetahui apakah koefisien korelasi memang berarti dengan persamaan berikut : t =
(
)
(
2)
1
2
r n r−
−
dimana :H0: tidak ada korelasi antara absorbansi (y) dengan konsentrasi (x)
Hi: ada korelasi antara absorbansi (y) dengan konsentrasi (x) Dengan nilai r = 0,999 dan r 2= 0,998,
t =
(
)
(
1
0
,
998
)
2
6
999
,
0
−
−
= 44,68Sehingga nilai thitungdiatas kemudian dibandingkan dengan nilai ttabeldari nilai kritik sebaran t yaitu 2,78 untuk selang kepercayaan 95% dengan derajat kebebasan (n-2). Karena nilai thitung lebih besar daripada ttabel, maka H0 ditolak dan disimpulkan bahwa ada
LAMPIRAN K
DATA ABSORBANSI DENGAN ADANYA ION PENGGANGGU Co(II)
[Fe(III)] (ppm) [Co] (ppm) Absorbansi
5 0.00 0.273 0.273 0.273 5 0.05 0.267 0.267 0.266 5 0.06 0.265 0.265 0.265 5 0.07 0.263 0.262 0.262 5 0.08 0.259 0.259 0.26 5 0.09 0.256 0.256 0.258 5 0.10 0.255 0.256 0.255
[Fe(III)] (ppm) [Co] (ppm) Absorbansi 5 0.2 0.254 0.255 0.25 5 0.4 0.253 0.252 0.248 5 0.6 0.246 0.244 0.243 5 0.8 0.243 0.243 0.243 5 1 0.242 0.24 0.241 5 2 0.236 0.234 0.235 5 4 0.233 0.233 0.23
[Fe(III)] (ppm) [Co] (ppm) Absorbansi 5 6 0.229 0.228 0.228 5 8 0.227 0.225 0.225 5 10 0.224 0.222 0.221
LAMPIRAN L
PERHITUNGAN KONSENTRASI, PROSEN RECOVERY, RSD DAN CV
Konsentrasi larutan kompleks besi yang terukur dapat dihitung dengan cara memasukkan harga absorbansi pada persamaan kurva kalibrasi y = 0,0544x – 0,003 dengan absorbansi (A) sebagai sumbu y dan konsentrasi besi (III) sebagai sumbu x pada kurva kalibrasi, maka :
Untuk absorbansi = 0,273, maka x = 0,273+0,003 0,0544 = 5,07 ppm
Prosen recovery merupakan ukuran ketepatan/keterdekatan hasil penentuan suatu metode analisis dengan harga sebenarnya. Prosen recovery dapat dihitung dengan persamaan :
% recovery = konsentrasi Fe(III) terukur x 100% Konsentrasi Fe(III) mula-mula
Diketahui konsentrasi cuplikan sebesar 5,07 ppm, maka : % recovery = 5,07 ppm x 100%
5 ppm = 101,47%
RSD (Relative Standard Deviation) dan CV (Coefficient of Variant) digunakan untuk menyatakan kecermatan atau kepresisian dari hasil penelitian dengan suatu metode tertentu. Untuk harga RSD < 20 ppt atau CV < 2%, dapat dikatakan
metode tersebut memiliki presisi yang bagus. RSD dan CV dihitung dengan persamaan :
RSD = x ppt x s
1000
⎟
⎠
⎞
⎜
⎝
⎛
CV = x100
%
x s⎟
⎠
⎞
⎜
⎝
⎛
Dengan s = simpangan baku
x
= rata-rata hasil penentuan dengan metode tertentu Simpangan baku dapat dihitung dengan persamaan :s =
∑
x
dengan : x adalah hasil penentuan dengan suatu metode tertentu
x
adalah rata-rata hasil penentuan n adalah jumlah pengulanganRSD = x
1000
ppt2667
,
0
000578
,
0
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
= 2,17 pptCV =
100
%
2667
,
0
000578
,
0
x⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
= 0,217%[Fe(III)] (ppm) [Co(II)] (ppm) Absorbansi Rata-rata Absorbansi [Fe(III)] terukur (ppm) %recovery RSD (ppt) CV (%) 5 0.00 0.273 0.273 5.0735 101.47 0 0 0.273 0.273 5 0.05 0.267 0.2667 4.9577 99.15 2.17 0.217 0.267 0.266 5 0.06 0.265 0.265 4.9265 98.53 0 0 0.265
[Fe(III)] (ppm) [Co(II)] (ppm) Absorbansi Rata-rata Absorbansi [Fe(III)] terukur (ppm) %recovery RSD (ppt) CV (%) 5 0.00 0.273 0.273 5.0735 101.47 0 0 0.273 0.273 5 0.05 0.267 0.2667 4.9577 99.15 2.17 0.217 0.267 0.266 5 0.06 0.265 0.265 4.9265 98.53 0 0 0.265 0.265 63 [Fe(III)] (ppm) [Co(II)] (ppm) Absorbansi Rata-rata Absorbansi [Fe(III)] terukur (ppm) %recovery RSD (ppt) CV (%) 5 0.07 0.263 0.2623 4.8768 97.54 2.21 0.221 0.262 0.262 5 0.08 0.259 0.2593 4.8217 96.43 2.23 0.223 0.259 0.26 5 0.09 0.256 0.2567 4.7739 95.47 4.50 0.450 0.256 0.258 5 0.1 0.256 0.2556 4.7537 95.07 2.27 0.227 0.257 64
(ppm) (ppm) Absorbansi Absorbansi terukur (ppm) %recovery (ppt) (%) 5 0.07 0.263 0.2623 4.8768 97.54 2.21 0.221 0.262 0.262 5 0.08 0.259 0.2593 4.8217 96.43 2.23 0.223 0.259 0.26 5 0.09 0.256 0.2567 4.7739 95.47 4.50 0.450 0.256 0.258 5 0.1 0.256 0.2556 4.7537 95.07 2.27 0.227 0.257 0.257 [Fe(III)] (ppm) [Co(II)] (ppm) Absorbansi Rata-rata Absorbansi [Fe(III)] terukur (ppm) %recovery RSD (ppt) CV (%) 5 0.2 0.254 0.253 4.7059 94.11 10.46 1.046 0.255 0.25 5 0.4 0.253 0.251 4.6691 93.38 10.54 1.054 0.252 0.248 5 0.6 0.246 0.2443 4.546 90.92 6.25 0.625 0.244 0.243 5 0.8 0.243 0.243 4.5221 90.44 0 0 0.243
5 0.2 0.255 0.253 4.7059 94.11 10.46 1.046 0.25 5 0.4 0.253 0.251 4.6691 93.38 10.54 1.054 0.252 0.248 5 0.6 0.246 0.2443 4.546 90.92 6.25 0.625 0.244 0.243 5 0.8 0.243 0.243 4.5221 90.44 0 0 0.243 0.243 65 [Fe(III)] (ppm) [Co(II)] (ppm) Absorbansi Rata-rata Absorbansi [Fe(III)] terukur (ppm) %recovery RSD (ppt) CV (%) 5 1 0.242 0.241 4.4853 89.71 4.15 0.415 0.24 0.241 5 2 0.236 0.235 4.375 87.5 4.25 0.425 0.234 0.235 5 4 0.233 0.232 4.3198 86.40 7.47 0.747 0.233 0.23 5 6 0.229 0.2283 4.2518 85.04 2.53 0.253 0.228 66
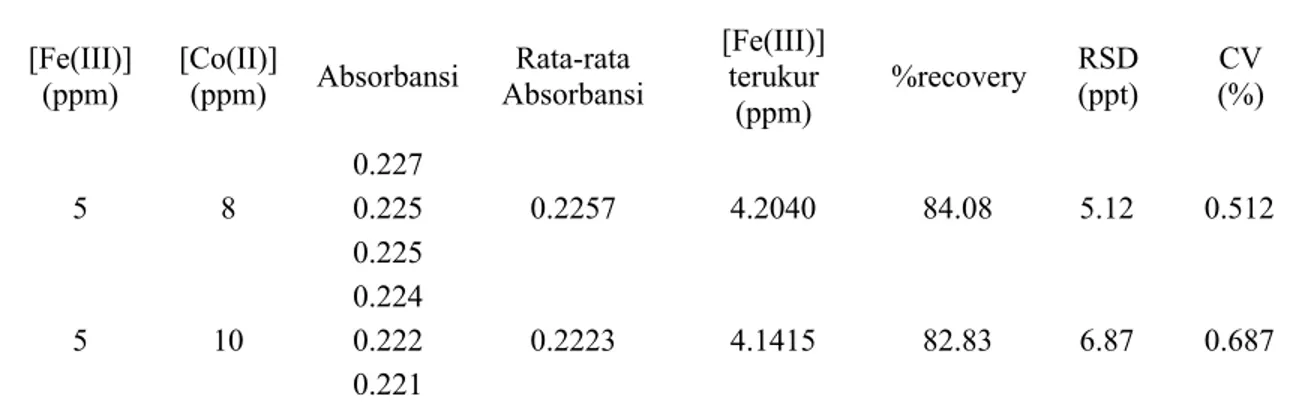
[Fe(III)] (ppm) [Co(II)] (ppm) Absorbansi Rata-rata Absorbansi [Fe(III)] terukur (ppm) %recovery RSD (ppt) CV (%) 5 1 0.242 0.241 4.4853 89.71 4.15 0.415 0.24 0.241 5 2 0.236 0.235 4.375 87.5 4.25 0.425 0.234 0.235 5 4 0.233 0.232 4.3198 86.40 7.47 0.747 0.233 0.23 5 6 0.229 0.2283 4.2518 85.04 2.53 0.253 0.228 0.228 [Fe(III)] (ppm) [Co(II)] (ppm) Absorbansi Rata-rata Absorbansi [Fe(III)] terukur (ppm) %recovery RSD (ppt) CV (%) 5 8 0.227 0.2257 4.2040 84.08 5.12 0.512 0.225 0.225 5 10 0.224 0.2223 4.1415 82.83 6.87 0.687 0.222 0.221
5 8 0.225 0.2257 4.2040 84.08 5.12 0.512 0.225 5 10 0.224 0.2223 4.1415 82.83 6.87 0.687 0.222 0.221 67 LAMPIRAN N
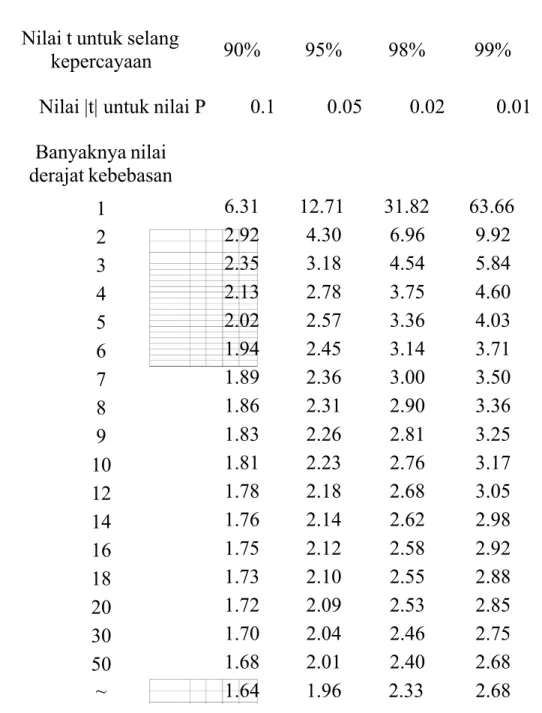
TABEL NILAI KRITIK SEBARAN t
Nilai t untuk selang
kepercayaan 90% 95% 98% 99% Nilai |t| untuk nilai P 0.1 0.05 0.02 0.01
Banyaknya nilai derajat kebebasan 1 6.31 12.71 31.82 63.66 2 2.92 4.30 6.96 9.92 3 2.35 3.18 4.54 5.84 4 2.13 2.78 3.75 4.60 5 2.02 2.57 3.36 4.03 68
LAMPIRAN N
TABEL NILAI KRITIK SEBARAN t
Nilai t untuk selang
kepercayaan 90% 95% 98% 99%
Nilai |t| untuk nilai P 0.1 0.05 0.02 0.01
Banyaknya nilai derajat kebebasan 1 6.31 12.71 31.82 63.66 2 2.92 4.30 6.96 9.92 3 2.35 3.18 4.54 5.84 4 2.13 2.78 3.75 4.60 5 2.02 2.57 3.36 4.03 6 1.94 2.45 3.14 3.71 7 1.89 2.36 3.00 3.50 8 1.86 2.31 2.90 3.36 9 1.83 2.26 2.81 3.25 10 1.81 2.23 2.76 3.17 12 1.78 2.18 2.68 3.05 14 1.76 2.14 2.62 2.98 16 1.75 2.12 2.58 2.92 18 1.73 2.10 2.55 2.88 20 1.72 2.09 2.53 2.85 30 1.70 2.04 2.46 2.75 50 1.68 2.01 2.40 2.68 ~ 1.64 1.96 2.33 2.68