BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
2.1.1 Penyebaran dan Habitat
Toona sinensis (sinonim.Cedrella sinensis A. Juss.) adalah spesies Toona
yang terdapat di Asia Tenggara, Korea Selatan dan Utara, bagian tenggara India, Myanmar, Malaysia, dan bagian barat Indonesia. Dalam bahasa Malaysia disebut suren. Jenis ini dijumpai di hutan-hutan primer maupun sekunder, dan banyak tumbuh di hutan pedesaan sering dijumpai disepanjang sungai di daerah bukit dan lereng-lereng pada ketinggian 1.200 – 2.700 m dpl (Dharmawati, 2002).
2.1.2 Meliaceae
Tumbuhan yang tergolong dalam suku Meliaceae biasanya berupa semak atau pohon, mempunyai kelenjar resin atau kelenjar minyak, daun majemuk, menyirip, duduknya tersebar, tanpa daun penumpu, bunga aktinomorf. Kelopak sering kali kecil, terdiri dari 4-5 daun kelopak. Buahnya berupa buah kendaga atau buah batu. Biji dengan atau tanpa endosperm, seringkali bersayap. Sekitar 750 jenis tumbuhan merupakan warga suku ini terbagi dalam kurang lebih 50 marga, tersebar di daerah- daerah iklim panas. Misalnya Melia azedarach, Aglaia odorata sebagai tanaman hias, bunga sering digunakan sebagai pewangi pakaian. Cedrella
odorata, penghasil kayu sedar (Gembong, 1991).
2.1.3 Deskripsi Tumbuhan
Pohon berukuran sedang sampai besar, dapat mencapi tinggi 25 meter. Diameter batang dapat mencapai 70 cm. Kulit batang berwarna coklat dan
kelihatan licin pada pohon yang muda, menjadi pecah dan terasa kasar pada pohon yang sudah tua. Daunnya lebar, kadang-kadang mengelompok diujung cabang, panjangnya 50-70 cm, dengan 8-20 pasang anak daun. Permukaan dan tulang daun sebelah atas umumnya berbulu. Bunga dihasilkan pada musim panas, bunga dijumpai diujung cabang, berukuran kecil, dengan diameter 4-5 mm, berwarna putih atau pink pucat. Buah berupa kapsul dengan panjang 2-3,5 cm, buah terdiri dari beberapa ruang yang didalamnya terdapat beberapa benih (Dharmawati, 2002).
2.1.4 Sistematika Tumbuhan
Menurut hasil identifikasi tanaman dari LIPI Bogor, diperoleh: Dunia : Plantae Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledonae Ordo : Sapindales Famili : Meliaceae Genus : Toona
Spesies : Toona sinensis (A.Juss.) M.Roem 2.1.5 Nama Daerah
Nama daerah dari pohon ingul adalah ingul (Karo), suren (Malaysia). 2.1.6 Kegunaan
Daun-daun muda digunakan sebagai sumber sayur di Cina dan Malaysia. Daunnya memiliki aroma sehingga dapat menggantikan bawang, selain itu daunnya juga digunakan sebagai karminatif, namun perlu diketahui bahwa
daunnya mengandung racun yang dapat menyebabkan kejang hebat dan kematian. Buah, kulit batang dan akarnya, digunakan sebagai obat tradisional yaitu diare kronik dan anemia, astringen. Bubuk akar digunakan sebagai minuman penyegar dan peluruh seni (diuretik). Kayunya sangat keras, berwarna kemerahan, bernilai tinggi, serta memiliki sifat kayu yang baik. Banyak digunakan untuk pembuatan furniture atau perabot rumah (Bocker dan Backhuizen, 1963).
2.2 Uraian kimia
2.2.1 Senyawa Flavonoida
Flavonoida adalah suatu kelompok senyawa fenol terbesar yang ditemukan di alam dan yang memiliki potensial sebagai antioksidan serta bioaktifitas sebagai obat. Senyawa flavonoida sebenarnya terdapat pada semua bagian tumbuhan termasuk daun, akar, kayu, kulit, tepung sari, bunga, buah, dan biji. Kebanyakan flavonoida ini berada di dalam tumbuh-tumbuhan, kecuali alga. Namun ada juga flavonoida yang terdapat pada hewan, misalnya dalam kelenjar berang-berang dan sekresi lebah. Dalam sayap kupu - kupu dengan anggapan bahwa flavonoida berasal dari tumbuh-tumbuhan yang menjadi makanan hewan tersebut dan tidak dibiosintesis di dalam tubuh mereka. Penyebaran jenis flavonoida pada golongan tumbuhan yang tersebar yaitu angiospermae, chlorophyta, fungi, bryophyta (Markham, 1988).
Sekitar 2% dari seluruh karbon yang difotosintesis oleh tumbuhan (atau kira-kira 1 x 109 ton/tahun) diubah menjadi flavonoida atau senyawa yang berkaitan dengannya. Sebahagian besar tanin pun berasal dari flavonoida. Jadi flavonoida merupakan salah satu golongan fenol alam yang terbesar. Flavonoida
merupakan senyawa 15 karbon yang umumnya tersebar di seluruh dunia tumbuhan. Lebih dari 2000 flavonoida yang berasal dari tumbuhan telah diidentifikasi. Kerangka dasar flavonoida biasanya diubah sedemikian rupa sehingga terdapat lebih banyak ikatan rangkap, menyebabkan senyawa itu dapat menyerap cahaya tampak, dan ini yang membuatnya berwarna. Sebagian besar flavonoida yang terdapat pada tumbuhan terikat pada molekul gula sebagai glikosida dan dalam bentuk campuran, jarang sekali dijumpai berupa senyawa tunggal. Disamping itu sering ditemukan campuran yang terdiri dari flavonoida yang berbeda kelas. Misalnya antosianin dalam mahkota bunga yang berwarna merah, ungu dan biru. Pigmen ini juga terdapat di berbagai bagian tumbuhan lain, misalnya buah tertentu, batang, daun, dan bahkan akar. Sering flavonoida terikat di sel epidermis. Flavonoida dalam tumbuhan mempunyai fungsi sebagai pigmen warna. Senyawa flavonoida dalam tubuh manusia berfungsi sebagai antioksidan, antibakteri, dan anti inflamasi sehingga baik untuk pencegahan kanker. Manfaat lain dari flavonoida ini adalah untuk melindungi sel, meningkatkan efektivitas vitamin C, anti inflamasi, anti bakteri, anti diabetes, diuretik dan sebagai antibiotik (Markham, 1988).
2.2.2 Struktur Dasar Senyawa Flavonoida
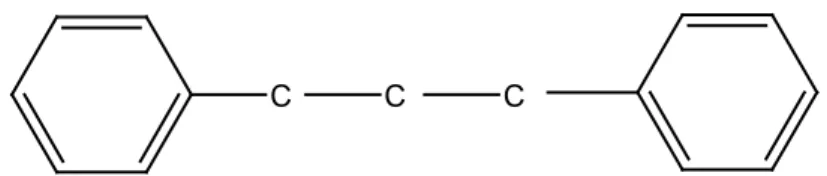
Senyawa flavonoida mempunyai kerangka dasar karbon yang terdiri dari 15 atom karbon, dua cincin benzen (C6) terikat pada suatu rantai propana (C3) sehingga bentuk susunan C6 –C3 – C6 (Markham, 1988). Struktur dasar flavonoida dapat digambarkan sebagai berikut:
C C C
Gambar 1. Kerangka dasar senyawa flavonoida 2.2.3 Biosintesa dari Flavonoida
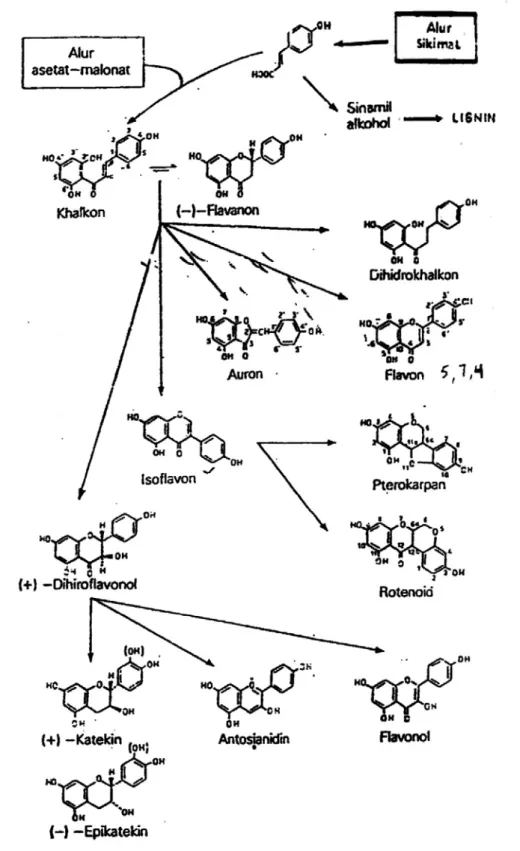
Pola biosintesa flavonoida pertama kali disarankan oleh Birch. Menurut Birch, pada tahap-tahap pertama dari biosintesa flavonoida suatu unit C6-C3 berkombinasi dengan tiga unit C2 menghasilkan unit C6-C3-(C2 + C2 + C2). Kerangka C15 yang dihasilkan dari kombinasi ini telah mengandung gugus-gugus fungsi oksigen pada posisi-posisi yang diperlukan. Adapun cincin A dari struktur flavonoida berasal dari jalur poliketida, yakni kondensasi dari tiga unit asetat atau malonat, sedangkan cincin B dan tiga atom karbon dari rantai propan berasal dari jalur fenilpropanoid (jalur shkimat). Dengan demikian, kerangka dasar karbon dari flavonoida dihasilkan dari kombinasi antara dua jalur biosintesa yang utama untuk cincin aromatik, yakni jalur shkimat dan jalur asetat malonat (Harbone, 1987).
Senyawa-senyawa flavonoida terdapat dalam semua bagian tumbuhan tinggi, seperti bunga, daun, ranting, buah, kayu, kulit kayu, dan akar. Akan tetapi, senyawa flavonoida tertentu seringkali terkonsentrasi dalam suatu jaringan tertentu, misalnya antosianidin adalah zat warna dari bunga, buah dan daun. Sebagian besar dari flavonoida alam ditemukan dalam bentuk glikosida, dimana unit flavonoida terikat pada suatu gula. Oleh karena itu, ada baiknya bila pada kesempatan ini diingatkan kembali bahwa secara umum, suatu glikosida adalah kombinasi antara suatu gula dan suatu alkohol yang saling berikatan melalui
ikatan glikosida. Pada prinsipnya ikatan glikosida terbentuk apabila gugus hidroksil dari alkohol beradisi kepada gugus karbonil dari gula (Harbone, 1987).
Pada hidrolisa oleh asam, suatu glikosida terurai kembali atas komponen- komponennya menghasilkan gula dan alkohol yang sebanding, dan alkohol yang dihasilkan ini disebut aglikon. Lazimnya, residu gula dari glikosida flavonoida alam ialah glukosa, ramnosa, galaktosa, dan gentibiosa sehingga glikosida tersebut masing-masing disebut glukosida, ramnosida, galaktosida dan gentiobiosida. Flavonoida dapat ditemukan sebagai mono, di atau triglikosida, dimana satu, dua atau tiga gugus hidroksil dalam molekul flavonoida terikat oleh gula. Poliglikosida larut dalam air dan hanya sedikit larut dalam pelarut-pelarut organik seperti eter, benzen, klorofom, dan aseton. Dari segi struktur, senyawa-senyawa flavonoida turunan flavon dapat dianggap sebagai 2-arilkromon. Oleh sebab itu, sebagaimana kromon dan kumarin, flavonoid dapat dideteksi berdasarkan warnanya dibawah sinar tampak atau sinar ultraviolet. Oleh karena itu, karakterisasi flavonoida akhir-akhir ini lazimnya dilakukan dengan pengukuran-pengukuran spektrofotometri (Harbone, 1987).
2.2.4 Klasifikasi Senyawa Flavonoida
Flavonoida merupakan senyawa metabolit sekunder yang terdapat pada tanaman hijau kecuali alga. Flavonoida yang lazim ditemukan pada tumbuhan tingkat tinggi (angiospermae) adalah flavon dan flavonol dengan C- dan O- glikosida, isoflavon C dan O-glikosida dan dihidrokhalkon, proantosinidin dan antosianin. Golongan flavon, flavonol, khalkon, flavanon, dan isoflavon juga sering ditemukan dalam bentuk aglikonnya. Istilah flavonoida diberikan untuk senyawa-senyawa fenol yang berasal dari kata flavon, yaitu nama dari salah satu flavonoid yang terbesar jumlahnya dalam tumbuhan. Senyawa-senyawa flavon ini mempunyai kerangka 2-fenilkroman, dimana posisi orto dari cincin A dan atom
karbon yang terikat pada cincin B dari 1,3-diarilpropana dihubungkan oleh jembatan oksigen sehingga membentuk cincin heterosiklik yang baru (cincin C). Senyawa-senyawa flavonoida terdiri dari beberapa jenis, tergantung pada tingkat oksidasi dari rantai propan dari sistem 1,3 diarilpropana. Dalam hal ini, flavon mempunyai tingkat oksidasi yang terendah sehingga senyawa ini dianggap sebagai senyawa induk dalam tatanama senyawa-senyawa turunan flavon. Dari berbagai jenis flavonoid tersebut, flavon, flavonol, dan antosianin adalah jenis yang banyak ditemukan di alam, sehingga seringkali dinyatakan sebagai flavonoida utama. Sedangkan jenis-jenis flavonoida yang tersebar di alam dalam jumlah yang terbatas ialah khalkon, flavanon dan leukoantosianidin. Flavonoida mengandung sistem aromatik yang terkonjugasi sehingga menunjukkan pita serapan kuat pada daerah spektrum sinar ultraviolet dan spektrum sinar tampak, umumnya dalam tumbuhan terikat pada gula yang disebut dengan glikosida (Harborne, 1987).
Flavonoida biasanya terdapat sebagai O-glikosida, pada senyawa tersebut satu gugus hidroksil flavonoida (atau lebih) terikat pada satu gula dengan ikatan hemiasetal yang tidak tahan asam. Pengaruh glikosilasi menyebabkan flavonoida menjadi kurang reaktif dan lebih mudah larut dalam air (cairan). Sifat terakhir ini memungkinkan penyimpanan flavonoida di dalam vakuol sel. Walaupun gugus hidroksil pada setiap posisi dalam inti flavonoida dapat diglikosilasi. Glukosa merupakan gula yang sangat penting umum terlibat, walaupun galaktosa, ramnosa, xilosa dan arabinosa sering juga terdapat. Gula lain yang kadang-kadang ditemukan ialah alosa, manosa, fruktosa, apiosa dan asam glukuronat serta galakturonat (Markham, 1988).
Gula juga terikat pada atom karbon flavonoida dan dalam hal ini gula tersebut terikat langsung pada inti benzena dengan suatu ikatan karbon-karbon yang tidak tahan asam. Glikosida yang demikian disebut C-glikosida. Sekarang gula yang terikat pada atom C hanya ditemukan pada atom C nomor 6 dan 8 dalam inti flavonoida. Jenis gula yang terlibat ternyata jauh lebih sedikit daripada jenis gula pada O-glikosida, biasanya dari jenis glukosa yang paling umum (misalnya viteksin, orientin), dan juga galaktosa (misalnya apigenin 8-C galaktosida), ramnosa (misalnya violantin), xilosa (misalnya visenin -1) dan arabinosa. Jenis aglikon flavonoida yang terlibat juga sangat terbatas. Walaupun isoflavon, flavanon, dan flavonol kadang-kadang terdapat dalam bentuk C-glikosida, sebegitu jauh hanya flavon C- glikosida yang paling lazim ditemukan (Markham, 1988).
Selain itu flavonoida dapat dikelompokkan berdasarkan keragaman pada rantai C3 yaitu:
a. Flavonol
Flavonol paling sering terdapat sebagai glikosida, biasanya 3-glikosida, dan aglikon flavonol yang umum yaitu kamferol, kuersetin, dan mirisetin yang berkhasiat sebagai antioksidan dan anti inflamasi. Flavonol lain yang terdapat di alam bebas kebanyakan merupakan variasi struktur sederhana dari flavonol. Larutan flavonol dalam suasana basa dioksidasi oleh udara tetapi tidak begitu cepat sehingga penggunaan basa pada pengerjaannya masih dapat dilakukan (Harborne, 1987).
O
O
OH
Gambar 3. Struktur flavonol
b. Flavon
Flavon berbeda dengan flavonol dimana pada flavon tidak terdapat gugusan 3-hidroksi. Hal ini mempunyai serapan UV-nya, gerakan kromatografi, serta reaksi warnanya. Flavon terdapat juga sebagai glikosidanya lebih sedikit daripada jenis glikosida pada flavonol. Flavon stabil terhadap asam kuat dan eternya yang mudah didealkilasi dengan penambahan HI atau HBr, atau dengan aluminium klorida dalam pelarut inert. Flavon yang paling umum dijumpai adalah apigenin dan luteolin. Luteolin merupakan zat warna yang pertama kali dipakai di Eropa. Jenis yang paling umum adalah 7-glukosida dan terdapat juga flavon yang terikat pada gula melalui ikatan karbon-karbon. Contohnya luteolin 8-C-glikosida. Flavon dianggap sebagai induk dalam nomenklatur kelompok senyawa flavonoid (Harborne, 1987). O O 1 2 3 4 5 6 7 8 9 10 2' 3' 4' 5' 6' 1'
c. Isoflavon
Isoflavon merupakan isomer flavon, tetapi jumlahnya sangat sedikit dan sebagai fitoaleksin yaitu senyawa pelindung yang terbentuk dalam tumbuhan sebagai pertahanan terhadap serangan penyakit. Isoflavon sukar dicirikan karena reaksinya tidak khas dengan pereaksi warna manapun. Beberapa isoflavon (misalnya daidzein) memberikan warna biru muda cemerlang dengan sinar UV bila diuapi amonia, tetapi kebanyakan yang lain tampak sebagai bercak lembayung yang pudar dengan amonia berubah menjadi coklat (Harborne, 1987).
O
O
Gambar 5. Struktur Isoflavon
d. Flavanon
Flavanon (biasanya sebagai glikosida) terdistribusi luas di alam. Flavanon terdapat di dalam kayu, daun dan bunga. Flavanon glikosida merupakan konstituen utama dari tanaman genus prenus dan buah jeruk. Dua glikosida yang paling lazim adalah neringenin dan hesperitin, terdapat dalam buah anggur dan jeruk (Harborne, 1987).
O
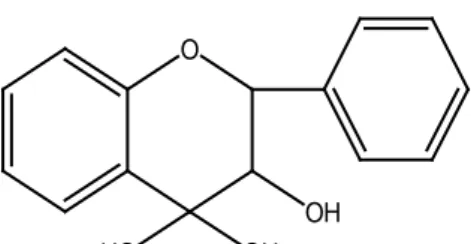
e. Flavanonol
Senyawa ini berkhasiat sebagai antioksidan dan hanya terdapat sedikit sekali jika dibandingkan dengan flavonoida lain. Sebagian besar senyawa ini diabaikan karena konsentrasinya rendah dan tidak berwarna (Harborne, 1987).
O
O
OH
Gambar 7. Struktur flavanonol f. Katekin
Katekin terdapat pada seluruh dunia tumbuhan, terutama pada tumbuhan berkayu. Senyawa ini mudah diperoleh dalam jumlah besar dari ekstrak kental
Uncaria gambir dan daun teh kering yang mengandung kira-kira 30% senyawa
ini. Katekin berkhasiat sebagai antioksidan (Harborne, 1987).
O OH HO OH OH OH
Gambar 8. Struktur katekin 7. Leukoantosianidin
Leukoantosianidin merupakan senyawa tan warna, terutama terdapat pada tumbuhan berkayu. Senyawa ini jarang terdapat sebagai glikosida, contohnya melaksidin, apiferol (Harborne, 1987).
O
HO OH
OH
Gambar 9. Struktur leukoantosianidin 8. Antosianin
Antosianin merupakan pewarna yang paling penting dan paling tersebar luas dalam tumbuhan. Pigmen yng berwarna kuat dan larut dalam air ini adalah penyebab hampir semua warna merah jambu, merah marak , ungu, dan biru dalam daun, bunga, dan buah pada tumbuhan tinggi. Secara kimia semua antosianin merupakan turunan suatu struktur aromatik tunggal yaitu sianidin, dan semuanya terbentuk dari pigmen sianidin ini dengan penambahan atau pengurangan gugus hidroksil atau dengan metilasi atau glikosilasi. Antosianin ini umumnya tidak terdapat di lumut hati, ganggang, dan tumbuhan tingkat rendah lainnya, walaupun beberapa antosianin dan flavonoida ada di lumut tertentu. Antosianin jarang ditemui di gimnospermae, walaupun gimnospermae mengandung jenis lain dari flavonoida (Harborne, 1987).
O
OH
Gambar 10. Struktur antosianin 9. Khalkon
Khalkon adalah pigmen fenol kuning yang berwarna coklat kuat dengan sinar UV bila dikromatografi kertas. Aglikon flavon dapat dibedakan dari
glikosidanya, karena hanya pigmen dalam bentuk glikosida yang dapat bergerak pada kromatografi kertas dalam pengembang air (Harborne, 1987).
O
Gambar 11. Struktur khalkon 10. Auron
Auron berupa pigmen kuning emas yang terdapat dalam bunga tertentu dan briofita. Dalam larutan basa senyawa ini berwarna merah ros dan tampak pada kromatografi kertas berupa bercak kuning, dengan sinar ultraviolet warna kuning kuat berubah menjadi merah jingga bila diberi uap amonia (Harborne, 1987).
O
C H
O
Gambar 12. Struktur auron
2.3 Metode Ekstraksi
Ekstraksi adalah suatu kegiatan penelitian kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut sehingga menggunakan pelarut cair.
Ada beberapa cara ekstraksi menggunakan pelarut antara lain: 1. Cara dingin
a. Maserasi
Maserasi adalah proses pengekstraksian simplisia menggunakan pelarut dengan beberapa kali pengadukan dan pendiaman pada temperatur ruangan. Sedangkan remaserasi adalah pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama dan seterusnya (Ditjen POM, 1979).
b. Perkolasi
Perkolasi adalah ekstraksi menggunakan pelarut yang selalu baru sampai sempurna yang umumnya dilakukan pada temperatur ruangan, serbuk simplisia yang akan diperkolasi tidak langsung dimasukkan kedalam bejana perkolator, tetapi dibasahi atau dimaserasi terlebih dahulu dengan cairan penyari sekurang-kurangnya 3 jam. Bila serbuk simplisia tersebut langsung dialiri dengan cairan penyari, maka cairan penyari tidak dapat menembus ke seluruh sel dengan sempurna (Ditjen POM, 1979).
2. Cara panas a. Refluks
Refluks adalah ekstraksi menggunakan pelarut pada temperatur titik didihnya selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingan balik (Ditjen POM, 1979).
b. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru, mumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dan
jumlah pelarut relatif konstan dengan adanya pendingin balik (Ditjen POM, 1979).
c. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur yang lebih tinggi dari temperatur ruangan (kamar) yaitu secara umum dilakukan pada temperatur 40-500C (Ditjen POM, 1979).
d. Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas air (bejana infus tercelup dalam penangas air mendidih, temperatur terukur 96-980C) selama waktu tertentu (15-20 menit) (Ditjen POM, 1979).
e. Dekok
Dekok adalah infus pada waktu yang lebih lama (≥ 30 0C) dan temperatur sampai titik didih air (Ditjen POM, 1979).
2.4 Kromatografi
Kromatrografi adalah metode pemeriksaan berdasarkan proses migrasi dari komponen-komponen senyawa diantara dua fase yaitu fase diam dan fase gerak. Fase gerak membawa zat terlarut melalui media sehingga terpisah dari zat terlarut lainnya yang terelusi lebih awal atau lebih akhir. Umumnya zat terlarut dibawa melalui media pemisah oleh aliran suatu pelarut berbentuk cairan atau gas. Fase diam dapat bertindak sebagai penyerap, seperti alumina dan slika gel atau dapat bertindak melarutkan zat terlarut sehingga terjadi partisi antara fase diam dan fase gerak. Dalam proses ini suatu lapisan cairan pada penyangga yang inert berfungsi sebagai fase diam (Ditjen POM, 1995).
Cara-cara kromatografi dapat digolongkan sesuai dengan sifat-sifat dari fase diam, yang dapat berupa zat padat atau zat cair. Jika fase diam berupa zat padat disebut kromatografi serapan, jika berupa zat cair disebut kromatografi partisi. Karena fase gerak dapat berupa zat cair atau gas maka terdapat empat macam sistem kromatografi, yaitu :
1. Fase gerak cair-fase diam dan padat (kromatografi serapan) : • Kromatografi lapis tipis
• Kromatografi kolom
2. Fase gerak gas-fase diam padat : • Kromatografi gas padat
3. Fase gerak cair-fase diam cair (kromatografi partisi) : • Kromatografi kertas
4. Fase gerak gas-fase diam cair : • kromatografi gas cair
Semua pemisahan dengan kromatografi tergantung pada kenyataan bahwa senyawa-senyawa yang dipisahkan terdistribusi diantara fase gerak dan fase diam dalam perbandingan yang sangat berbeda-beda dari satu senyawa terhadap senyawa yang lain (Sastrohamidjojo, 1991).
Kromatografi kertas merupakan kromatografi partisi dimana fase geraknya adalah cair yang disokong oleh molekul-molekul selulosa dari kertas. Kertas yang digunakan adalah kertas Whatman No.1 dan kertas yang lebih tebal Whatman No. 3 biasanya untuk pemisahan campuran dalam jumlah yang lebih besar karena dapat menampung lebih banyak cuplikan (Sastrohamidjojo, 1991).
Fase gerak yang digunakan biasanya campuran dari suatu komponen organik yang utama air dan berbagai tambahan seperti asam-asam, basa atau pereaksi-pereaksi kompleks dengan tujuan untuk memperbesar kelarutan dari beberapa senyawa atau untuk mengurangi kelarutan yang lainnya (Sastrohamidjojo, 1991). Fase gerak terdiri dari satu atau beberapa pelarut dan bila diperlukan dapat menggunakan sistem pelarut multi komponen, berupa suatu campuran sederhana mungkin yang terdiri atas maksimum tiga komponen. Pada pemisahan senyawa organik selalu menggunakan pelarut campur, tujuannya untuk memperoleh polaritas yang tepat sehinga diperoleh pemisahan senyawa yang baik. Kombinasi pelarut berdasarkan atas polaritas masing-masing pelarut sehingga dengan demikian diperoleh sistem penggabung yang cocok (Stahl, 1985).
Jarak pengembang senyawa pada kromatogram biasanya dinyatakan dengan harga Rf (Stahl, 1985).
Rf = Jarak perambatan bercak dari titik pentotolan
Jarak perambatan pelarut dari titik pentotolan
Jarak yang ditempuh oleh tiap bercak dari titik pentotolan diukur dari pusat bercak dan harga Rf berada antara 0,00–1,00. Harga Rf sangat beguna untuk mengidentifikasi suatu senyawa (Eaton, 1989).
Faktor-faktor yang mempengaruhi harga Rf adalah sebagai berikut: (Sastrohamidjojo, 1991).
1. Struktur kimia senyawa yang dipisahkan 2. Sifat penyerap
3. Tebal dan kerataan lapisan penyerap 4. Pelarut dan drajat kemurniannya
6. Teknik percobaan
7. Jumlah cuplikan yang digunakan
Menurut Sastrohamidjojo (1991), kromatografi kertas dapat dikembangkan dengan cara:
1. Menurun (desendens)
Dilakukan dengan membiarkan fase gerak merambat turun pada kertas kromatografi, kertas digantungkan dalam bejana menggunakan batang kaca dan batang kaca lain menahan ujung atas kertas yang tercelup dalam fase gerak. Setelah bejana ditutup, fase gerak dibiarkan merambat turun pada kertas.
2. Menaik (esendens)
Kertas digantung pada penggantung berbentuk kail yang dipasang pada penutup bejana kromatografi. Pelarut diletakkan pada bagian bawah dari bejana lalu ujung bawah kertas dicelupkan ke dalam fase gerak sehingga fase gerak merambat naik pada kertas.
3. Mendatar
Kertas yang digunakan berbentuk bulat dan ditengahnya diberi lubang tempat untuk meletakkan sumbu yang terbuat dari gulungan kertas atau benag. Fase gerak akan naik membasahi kertas dan merambat melingkar memisahkan senyawa yang ditotolkan.
Kromatografi kertas merupakan metode yang paling sering digunakan dalam hal analisis senyawa polar (flavonoida). Untuk tujuan isolasi, hanya memerlukan sejumlah bahan yang sedikit. Komponen senyawa flavonoid umumnya mudah dipelajari dengan metode kromatografi karena sifatnya yang menghasilkan warna dari hubungan sifat kelarutannya. Adapun kelebihan
kromatografi kertas yaitu senyawa flavonoida dapat menghasilkan warna alami dari berbagi komponen senyawa bila dilihat dibawah sinar ultraviolet yang mudah diamati pada kertas. Kedua, tekniknya mudah dipelajari, memberikan hasil yang cepat dan memerlukan peralatan yang tidak mahal. Selain itu, metode kromatografi kertas merupakan cara terbaik untuk mengidentifikasi campuran senyawa flavonoida dengan jumlah yang sedikit (Geissman, 1962).
2.5 Spektrofotometri Ultraviolet
Spektrofotometri ultraviolet adalah suatu metode spektrofotometri serapan dengan cara mengukur serapan radiasi elektromagnetik suatu larutan pada panjang gelombang tertentu. Spktrum ultraviolet digambarkan sebagai hubungan antara panjang gelombang (frekuensi serapan) dengan insensitas serapan (transmitansi atau absorbansi) (Sastrohamidjojo, 1985).
Apabila suatu molekul menyerap radiasi ultraviolet, maka didalam molekul tersebut terjadi perpindahan atau tranmisi tingkat energi elektron-elektron ikatan di orbital molekul paling luar dari tingkat energi yang lebih mudah (orbital ikatan π) ketingkat energi yang lebih tinggi (orbital anti ikatan π*). Keuntungan dari serapan ultraviolet adalah selektifnya dimana gugus-gugus yang khas dapat dikenal dalam molekul-molekul yang sangat kompleks. Serapan molekul didalam daerah ultraviolet bergantung pada struktur elektronik dari molekul, apabila suatu molekul menyerap radiasi ultraviolet, di dalam molekul terjadi perpindahan tingkat energi elektron-elektron ikatan pada orbital molekul paling luar dari tingkat energi yang lebih rendah ketingkat energi yang lebih tinggi (Noerdin, 1985).
2.5.1 Pereaksi Geser (Shift Reagent)
Spektrofotometri UV adalah cara yang paling berguna untuk menganalisis struktur flavonoida, biasanya ditentukan dalam larutan dengan pelarut metanol atau etanol. Spektrum senyawa flavonoida terdiri atas dua pita absorbsi maksimum, yaitu pita I pada rentang 300-550 nm dan pita II pada 240-285 nm. Pita I menunjukkan absorbsi sistem benzoil pada cincin A (Markham, 1988).
Kedudukan gugus hidroksi fenol bebas pada inti flavonoida dapat ditentukan dengan menambahkan pereaksi geser ke dalam larutan cuplikan dan mengamati puncak serapan yang terjadi (Markham, 1988). Langkah pertama yang dilakukan dalam menafsirkan spektrum yaitu menentukan jenis flavonoida dengan memperhatikan:
1. Bentuk umum spektrum dalam metanol 2. Panjang gelombang pita serapan
3. Data kromatografi kertas
Langkah kedua adalah memperhatikan arti perubahan spektrum yang disebabkan oleh penembahan berbagai pereaksi geser (Markham, 1988).
2.5.2 Spektrum Natrium Metoksida
Natrium metoksida merupakan basa kuat yang dapat mengionisasi hampir semua gugus hidroksi pada inti flavonoida. Spektrum ini biasanya merupakan petunjuk sidik jari pola hidroksilasi dan juga bermanfaat untuk mendeteksi gugus hidroksi yang lebih asam dan tidak tersubstitusi. Degradasi atau pengurangan kekuatan spektrum setelah waktu tertentu merupakan petunjuk baik akan adanya gugus yang peka terhadap basa. Pereaksi pengganti natrium metoksida yang cocok ialah larutan NaOH 2 M dalam air (Mabry dkk, 1970).
2.5.3 Spektrum AlCl3 dan AlCl3/ HCl
AlCl3 membentuk kompleks tahan asam dengan gugus hidroksi (pada C3 atau C5) dan keton, juga membentuk kompleks tak tahan asam dengan gugus orto-dihidroksi, sehingga dapat digunakan untuk mendeteksi kedua gugus tersebut. Spektrum AlCl3/HCl hanya berguna untuk mendeteksi gugus hidroksi yang bertetangga dengan gugus keton, karena gugus tersebut dengan AlCl3 akan membentuk senyawa kompleks yang tahan asam (Mabry dkk, 1970).
2.5.4 Spektrum Natrium Asetat
Natrium asetat hanya menyebabkan pengionan yang berarti pada gugus hidroksil flavonoida yang paling asam. Jadi natrium asetat digunakan terutama untuk mendeteksi adanya gugus 7-hidroksil bebas (atau yang setara) (Mabry dkk, 1970).