Uji Efek Ekstrak Air dari Daun Avokad (
Persea gratissima
) terhadap
Streptococcus Mutans
dari Saliva dengan Kromatografi Lapisan Tipis (TLC)
dan Konsentrasi Hambat Minimum (MIC)
Fauzia*, Astari Larasati **
* Departemen Farmasi Kedokteran, Fakultas Kedokteran Universitas Indonesia, Jakarta **Fakultas Kedokteran Gigi Universitas Indonesia, Jakarta
dekok yang terdiri dari: konsentrasi 100%; 50%; 25%; 12,5%. Daun Avokad mengandung antara lain: flavonoid, alkaloid dan saponin yang memiliki efek antibakteri, yang ditunjukkan dengan penelitian memakai Metoda Khromatografi lapisan tipis. Efek anti bakteri ditentukan dengan mengukur zona hambatan Konsentrasi Hambat Minimum, dan Konsentrasi Bakteri Minimum. Mikroorganisme yang diujikan adalah Streptococcus mutans yang terdiri dari 6 koloni yang disolasi dari saliva. Hasil penelitian menunjukkan Ekstrak air daun Avokad memiliki efek antibakteri terhadap Streptococcus mutans asal saliva.
Kata kunci: kromatografi lapisan tipis, konsentrasi hambat minimum, konsentrasi bakterisidal minimum
Abstract: It has been done anti bacterial agent of aqueous extract from avokado leaves. Avokado leaves have active substance compound such as flavonoid, alkaloid, and saponin, it showed by Thin Layer Chromatography. An aqueous extract of avocado (Persea gratissima) was examined in inhibiting the bacterial growth by determining the inhibition zone (disk with drug in solid media method), Minimum Inhibition Concentration (MIC) and Minimum Bactericidal Concentration (MBC).The microorganisms tested were composed 6 strains of salivary mutans streptococci isolated from volunteers of dental student in University of Indonesia, Jakarta. The result showed that the aqueous extract from avocado (Persia gratissima) has anti bacterial activity against local strain of Streptococcus mutans isolated from saliva.
Keywords: thin layer chromatography, minimum inhibitory concentration, minimum bactericidal concentration
PENDAHULUAN
Indonesia termasuk salah satu negara yang banyak menggunakan tumbuhan sebagai obat tradisional. Akhir-akhir ini pemakaiannya semakin meningkat sejalan dengan majunya pengetahuan tentang khasiat tumbuh-tumbuhan. Salah satu khasiat yang banyak mendapat perhatian adalah tumbuhan untuk mengatasi sakit gigi.
Avokad merupakan tumbuhan yang mudah didapat dan harganya relatif murah telah lama dikenal masyarakat sebagai bahan minuman dan campuran makanan. Tetapi ternyata Avokad juga berkhasiat untuk pengobatan, termasuk gigi dan mulut1
.
Dari suatu penelitian, daun Avokad mengandung flavonoid, alkaloid dan saponin
yang mempunyai aktivitas antibakteri dan mampu menghambat pertumbuhan bakteri. Flavonoid, alkloid, dan saponin termasuk senyawa fenol, dan banyak ditemukan pada tumbuhan. Dalam dunia kedokteran, senyawa fenol diketahui mempunyai efek antiseptik. Dalam usaha untuk mengetahui kebenaran khasiatnya, dilakukan penelitian untuk dapat membuktikan penggunaan air rebusan daun Avokad untuk mengatasi sakit gigi2
.
BAHAN DAN METODE PENELITIAN Bahan:
• Untuk pembuatan ekstrak air - Daun Avokat
- Cushing - Panci infus
• Untuk kromatografi lapisan tipis: - Fase stasioner/fase diam = Adsorben
yang dipakai silica gel.
- Fase mobil/fase gerak = Eluen • Untuk Konsentrasi Hambat Minimum
- Tabung reaksi - Saliva
- Streptococcus mutans
- Brain Heart Infussion Broth
- Anaerobic jar
METODE PENELITIAN
I. Pembuatan Ekstrak Daun Avokad
1. 50 gram daun Avokad dan 500 ml air dimasukkan ke dalam panci infus dipanaskan selama 15 menit setelah itu disaring, didapatkan cairan infus sebanyak 50 ml.
2. Menimbang cushing dengan tujuan mendapatkan berat awal cushing tanpa ekstrak.
3. Cairan infus ditempatkan di cushing dan dipanaskan dengan suhu 900
C selama + 45 menit sampai diperoleh cairan infus yang sangat pekat.
4. Massa ekstrak (gram) ditimbang dengan cara mengurangi berat cushing tambah cairan infus pekat dengan berat cushing dalam keadaan kosong. 5. Lalu ditambahkan cairan BHI (Brain
Heart Infussion Broth) sebanyak massa ekstrak, dalam satuan millimeter.
6. Hasil campuran ini dianggap 100% massa ekstrak.3 Dibuat konsentrasi: 50% : 2 ml ekstrak 100% diencerkan dalam 2 ml BHI 25% : 2 ml ekstrak 50% diencerkan dalam 2 ml BHI 12.5% : 2 ml ekstrak 25% diencerkan dalam 2 ml BHI
II. Kromatografi Lapisan Tipis
Pengerjaan Kromatografi Lapisan Tipis4
1. Pembuatan campuran cairan chamber
Campuran dibuat dengan memakai butanol, asam asetat anhidrid dengan perbandingan 4 : 1 : 5.
2. Mempersiapkan plate dan bahan
percobaan
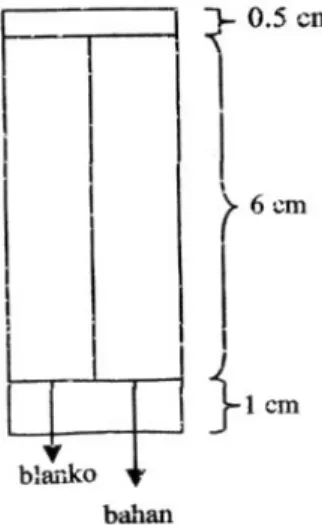
Teteskan blanko (untuk fenol gunakan
quercetine, sedangkan untuk flavonoid gunakan asam salisilat yang dilarutkan dalam alkohol) di sebelah kiri, dan bahan percobaan di sebelah kanan.
Gambar 1. Plate kromatografi lapisan tipis
3. Menyinari plate dengan sinar UV 4. Melakukan penyemprotan
Untuk percobaan fenol, FeCl3 digunakan untuk penyemprotan. Sedangkan untuk percobaan flavonoid, cukup diuapkan di atas amoniak pekat selama beberapa detik.
Fenol
Rf blanko (quersetine) = 4.55/6 = 0.758 Rf bahan = 2.4/6 = 0.4
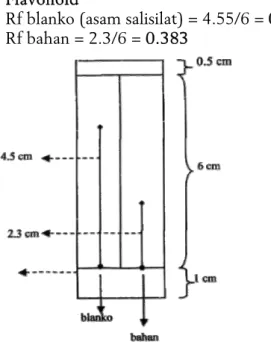
Flavonoid
Rf blanko (asam salisilat) = 4.55/6 = 0.75 Rf bahan = 2.3/6 = 0.383
Gambar 3. Hasil kromatografi flavonoid
Teknik kromatografi lapisan tipis, yaitu: a. Pembuatan pelat
b. Penotolan sampel c. Elusi
d. Deteksi noda Cara identifikasi
Dengan cara membandingkan komponen-komponen yang terpisah dengan senyawa-senyawa standar atau senyawa murni/blangko yang dikromatografi dengan kondisi yang identik. Jarak yang ditempuh suatu komponen dinyatakan oleh Rf (Ratio of front atau Related to front)
Gambar 4. Kromatografi lapisan tipis
x Rf =
y
Hasil Identifikasi Fenol
Dalam melakukan uji fenol, dipergunakan juga blanko berupa asam salisilat. Uji fenol dilakukan dengan penambahan larutan FeCl3 ke dalam sampel.
Jika terbentuk warna hijau atau biru setelah penambahan FeCl3 maka hal ini menunjukkan
keberadaan fenol di dalam sampel tersebut. Setelah dilakukan penetesan FeCl3 diperoleh
hasil berupa warna yang berubah menjadi kehijauan. Perubahan warna yang terjadi menunjukkan keberadaan fenol pada ekstrak air avokad (Persea gratissima). Beberapa senyawa fenol yang terkandung dalam tumbuhan Persea gratissima, yaitu flavonoid, alkaloid, dan saponin.5
Hasil Identifikasi Flavonoid6
Pengujian flavonoid dilakukan dengan menambahkan metanol, logam Mg, dan HCl. Adapun tujuan penambahan logam Mg dan HCl pekat pada pengujian ini adalah untuk mereduksi inti benzopiron yang terdapat dalam struktur flavonoid sehingga terjadi perubahan warna menjadi jingga atau merah. Setelah penambahan metanol dan logam Mg, dilakukan pemanasan terhadap sampel, untuk kemudian diteteskan HCl. Penetesan HCl menyebabkan didapatkan hasil bahwa sampel berubah warna menjadi jingga. Hal ini menunjukkan terjadi reaksi oksidasi reduksi antara logam Mg sebagai pereduksi, dengan sampel flavonoid. Reaksi oksidasi reduksi antara logam Mg dan flavonoid, menyebabkan terbentuknya senyawa kompleks yang menimbulkan warna jingga pada sampel.
Klasifikasi Alkaloid7
Alkaloid umumnya diklasifikasikan berdasarkan struktur molekul atau jalur metabolis yang digunakan untuk membentuk molekul tersebut. Dahulu, mereka dikelompokkan ke dalam suatu jenis campuran. Saat ini, pengelompokkan tersebut didasarkan pada golongan amin yang terlibat pada proses sintesis protein.
Saponin7
Saponin berasal dari bahasa latin sapo, yang berarti sabun. Senyawa ini dapat mengeluarkan cairan seperti buih dan mempunyai khasiat serupa deterjen yaitu bersifat antiseptik. Saponin dapat mengurangi pembengkakan, memperkuat pembuluh darah, mengurangi permeabilitas dan kerapuhan pembuluh darah.
III. Konsentrasi Hambat Minimum8
1. Subjek penelitian meludah ke dalam tabung yang telah dipersiapkan.
2. Ambil 0,5 ml saliva yang telah diencerkan, lalu letakkan pada medium pembiakan, yaitu agar TYS20B. Setelah itu agar dibiak pada suhu 37o
C selama 3 x 24 jam.
3. Setelah 3 hari dibiakkan, dilakukan identifikasi koloni Streptococcus mutans berdasarkan diameter, warna, permukaan, tepi dan opasitas dari koloni
4. Kemudian Streptococcus mutans yang telah diidentifikasi dibiakkan lagi pada medium cair dengan menggunakan BHI (Brain Heart Infussion Broth) dan disimpan dalam anaerobic jar selama 3 x 24 jam pada suhu 37o
C.
5. Setelah 3 hari dibiakkan, bandingkan
kekeruhan antara Streptococcus
mutans yang dikultur dalam medium cair dengan larutan standar McFarland 0.5.
6. Jika Streptococcus mutans yang
dikultur pada BHI lebih keruh, maka perlu ditambahkan larutan NaCl sedikit demi sedikit hingga kekeruhannya sama dengan larutan standar McFarland 0.5
7. Jika kekerurahan keduanya sudah sama, maka tahap selanjutnya adalah melakukan tes sensitivitas.
Tes Sensitivitas
Berdasarkan Schaube et al (1958) tes sensitivitas bakteri bisa dilakukan dengan 2 metode yaitu:
1. Metode serial dilution
2. Metode disk with drug in solid media
Metode Serial Dilution9
1. Disiapkan 6 tabung reaksi untuk masing-masing jenis koloni
Streptococcus mutans yaitu untuk tabung 1 untuk konsentrasi 100%, tabung 2 untuk konsentrasi 50%, tabung 3 untuk konsentrasi 25%, tabung 4 untuk konsentrasi 12.5% serta tabung 5 untuk kontrol negatif (-) dan tabung 6 untuk kontrol positif (+)
2. Masing-masing tabung diisi 1 ml BHI, kecuali tabung 1 yang diisi dengan 2 ml ekstrak daun avokad.
3. Dari tabung 1, diambil 1 ml ekstrak lalu diteteskan ke tabung 2 dengan menggunakan eppendorf.
4. Dari tabung 2 diambil 1 ml lalu diteteskan ke tabung 3, lakukan sampai tabung 5.
5. Streptococcus mutans yang dibiakkan dalam BHI dan telah disetarakan kekeruhannya dengan larutan standar McFarland 0.5 diteteskan ke masing-masing tabung kecuali pada tabung 5. 6. Setelah itu, tabung disimpan di
anaerobic jar selama 3 x 24 jam pada suhu 7. Setelah 3 hari, diamati apakah terjadi
kekeruhan pada masing-masing tabung.
Metode Disk with Drug in Solid Media10
1. Streptococcus mutans yang telah sama kekeruhannya dengan larutan standar McFarland 0.5 diratakan ke seluruh permukaan agar TYS20B.
2. Disk dicelupkan ke ekstrak daun avokad dengan konsentrasi tertentu lalu diletakkan di media agar TYS20B 3. Setelah itu, agar TYS20B tersebut
dimasukkan ke dalam anaerobic jar selama 3 x 24 jam pada suhu 37o
C 4. Setelah 3 hari lalu diukur zona
hambatan yang terlihat pada masing-masing konsentrasi
Diagram Kerja11
Tabel 1.
Daun avokad
Streptococcus mutans asal saliva zona hambatan
Using disk with drug method
Tes sensitivitas
Daun avokad
Streptococcus mutans asal saliva MIC/MBC
Hasil tes sensitivitas Streptococcus mutans
terhadap ekstrak daun avokad12
Konsentrasi (% ml) Tipe bakteri 100% 50% 25% 12.50% K (+) K (-) S.mutans 1 + + + + + - S.mutans 2 - - - + + - S.mutans 3 - - + + + - S.mutans 4 - + + + + - S.mutans 5 - - + + + - S.mutans 6 - - + + + - (-) Tidak tumbuh (+) Tumbuh
K (+): tanpa ekstrak daun avokad K (-): dengan ekstrak daun avokad
Tes sensitivitas dengan metode disk with drug in solid media menunjukkan adanya zona hambatan pada area sekitar disk yang telah diberikan ekstrak dengan konsentrasi tertentu, sedangkan zona hambatan tidak ditemukan pada media kultur tanpa ekstrak daun avokad. Hasil pengukuran zona hambatan pada media agar TYS20B dapat dilihat pada Tabel 2.
Tabel 2.
Hasil pengukuran zona hambatan Streptococcus
mutans Konsentrasi (% ml) Tipe bakteri 100% 50% 25% 12.50% S.mutans 1 2.8 1.2 0.2 - S.mutans 2 7.3 5.0 3.5 - S.mutans 3 6.0 4.8 2.5 - S.mutans 4 5.8 3.0 2.5 - S.mutans 5 8.0 4.0 2.4 - S.mutans 6 69 4.8 1.9 - 6.13 3.8 2.16 - PEMBAHASAN
Dari hasil penelitian, dapat dilihat bahwa
Streptococcus mutans 2, Streptococcus mutans 3, Streptococcus mutans 4, Streptococcus mutans 5 dan Streptococcus mutans 6 sensitif terhadap ekstrak daun avokad dengan konsentrasi 100%, sedangkan
Streptococcus mutans tidak sensitif terhadap ekstrak daun avokad dengan konsentrasi 100%. Zona hambatan masing-masing
Streptococcus mutans pun berbeda.
Streptococcus mutans 1 memiliki zona hambatan 2.8 mm, Streptococcus mutans 2 memiliki zona hambatan 7.3 mm,
Streptococcus mutans 3 memiliki zona hambatan 6.0 mm, Streptococcus muntas 4 memiliki zona hambatan 5.8 mm,
Streptococcus mutans 5 memiliki zona hambatan 8.0 mm, dan Streptococcus mutans
6 memiliki zona hambatan 6.9 mm.
Studi ini dilakukan terhadap
Streptococcus mutans, dikarenakan dalam dunia kedokteran gigi Streptococcus mutans
dikenal sebagai agen primer yang dapat menyebabkan terjadinya karies gigi. Selain itu, berdasarkan penelitian sebelumnya daun avokad mengandung senyawa aktif flavonoid, alkaloid dan saponin yang mempunyai aktivitas antibakteri dan menghambat pertumbuhan Staphylococcus aureus strain A dan B. Staphylococcus albus, Pseudomonas sp., Proteus sp., Escherichia coli dan Bacillus subtilis (E.O. Ognulans dan E. Ramstad, 1975).
Berdasarkan hasil penelitian yang telah dilakukan, maka bisa diasumsikan bahwa ekstrak daun avokad dengan kadar 100% dan 50% cukup efektif untuk menghambat pertumbuhan Streptococcus mutans. Sehingga diharapkan daun avokad dapat digunakan sebagai salah satu metode pencegahan karies di masa yang akan datang.
KESIMPULAN
Dari hasil uji yang telah dilakukan, ekstrak air dari daun avokad memiliki efek antibakteri yang dapat menghambat aktivitas dan pertumbuhan Streptococcus mutans yang diisolasi dari saliva. Pengujian dilakukan dengan cara kromatografi dan secara mikrobiologi.
SARAN
Perlu dilakukan penelitian lebih lanjut mengenai kandungan fenol, flavonoid, dan zat kimia lain pada tumbuhan daun Avokad (Persea gratissima) semakin dikembangkan.
DAFTAR PUSTAKA
1. Yohana Arisandi, Yovita Andriani.: Khasiat Tanaman Obat. Ed. 2. Jakarta. Pustaka Buku Murah, 2006.
2. Wijayakusuma, Hembing dkk.: Tanaman Obat di Indonesia Jilid ke-4. Jakarta Pustaka Kartini. 1996.
3. Chatri, Moralita Dra.: Pemanfaatan Ekstrak Daun Avokad (Persea gratissima) untuk menghambat Pertumbuhan Bakteri. Puslit Fisika LIPI. 2000.
4. Departemen Kesehatan Republik. Indonesia: Materiae Medika Indonesia Jakarta: Dep.Kes. R.I.: 1995: X-XVIII, 309-318.
5. Louis Friedli, George Dr. Phenolicinterms: Alkaloid.
http://www.alkaloid.htm/17/10/2006. 20:08:02.
6. Naim, Rochman. Senyawa antimikroba dari tanaman. http:// www.kompas.com/ kompas.cetak/0409/15/sorotan/1265264. htm/10/11/2006.23.18
7. http://www.herbs2000/com/h_menu/sap onins.htm/18/09/2006:21/26 WIB.
8. Balows A., Current Techniques for Antibiotic Susceptibility Testing. Charles C. Thomas Publisher-Springfield-Illinois, 1984; 7-8: 65.
9. Schuster, George S.: Oral Microbiology and Infectious Disease, hal. 171. 1978.
10. Samaranayake, L.P.: Essential Microbiology for Dentistry, 2 nd
ed. hal. 52. Hongkong: Churchill Livingstone. 2002.
11. http://www.ncl.ac.uk..Streptococcus mutans/dental/oralbiol/oralenv/tutorial/ mutans.htm
12. Wikipedia, the free encyclopedia. Streptococcus mutans. http;//en.wikipeda. org//wiki/camellia sinensis. 2006/10/09/2006