REFERAT
Gangguan Keseimbangan Asam Basa
dan Elektrolit
Diajukan Sebagai Salah Satu Tugas Dalam Menjalani Kepanitraan Klinik Senior Pada Bagian/SMF Ilmu Penyakit Dalam Program Studi Pendidikan Dokter
Universitas Malikussaleh Rumah Sakit Umum Cut Meutia Aceh Utara
Nama : Putri Azka Rinanda, S.Ked
NIM : 090610041
Preseptor : Dr. Suhaemi, SpPD, Finasim
Bagian : Ilmu Penyakit Dalam
PROGRAM STUDI PENDIDIKAN DOKTER UNIVERSITAS MALIKUSSALEH BAGIAN/SMF ILMU PENYAKIT DALAM
RUMAH SAKIT UMUM CUT MEUTIA ACEH UTARA TAHUN AJARAN
KATA PENGANTAR
Puji syukur kepada Tuhan Yang Maha Esa, akhirnya penyusunan referat yang berjudul “Gangguan Keseimbangan Asam Basa Dan Elektrolit” dapat saya selesaikan penulisannya dalam rangka memenuhi salah satu tugas sebagai ko-asisten yang sedang menjalani kepaniteraan klinik pada bagian Ilmu Penyakit Dalam di Rumah Sakit Umum Cut Meutia.
Dalam menyelesaikan tugas ini, saya mengucapkan terima kasih kepada Dr. Suhaemi, Sp.PD, Finasim selaku pembimbing dalam penulisan referat dan sebagai pembimbing selama menjalani kepaniteraan ini. Apabila terdapat kekurangan dalam menyusun referat ini, saya akan menerima kritik dan saran. Semoga tulisan ini bermanfaat bagi kita semua.
Lhokseumawe, Mei 2014
DAFTAR ISI
KATA PENGANTAR... i
DAFTAR ISI... ii
BAB 1. PENDAHULUAN ... 1
1.1 Latar Belakang... 1
BAB 2. TINJAUAN PUSTAKA ... 4
2.1 Asam Basa... 4
2.2 Mekanisme Kompensasi... 5
2.3 Gangguan Keseimbangan Asam Basa ... 10
2.3.1 Asidosis... 13
2.3.2 Alkalosis... 24
2.4 Keseimbangan Elektrolit... 24
2.4.1 Natrium... 29
2.4.2 Kalium... 38
2.4.3 Kalsium... 46
2.4.4 Magnesium... 57
2.4.5 Klorida... 60
BAB 3. PENUTUP ... 64
3.1 Kesimpulan... 64 DAFTAR PUSTAKA
PENDAHULUAN
1.1 Latar Belakang
Keseimbangan asam basa adalah homeostasis dari kadar ion hydrogen
([H+]). Pada cairan tubuh asam terus menerus diproduksi dalam metabolisme
yang normal. Meskipun terbentuk banyak asam sebagai hasil metabolisme, namun
[H+] cairan tubuh tetap rendah. Kadar H normal dari arteri adalah 4 x 10-8 mEq/L
atau sekitar 1 per sejuta dari kadar Na+. meskipun rendah, kadar [H+] yang stabil
perlu dipertahankan agar fungsi sel dapat berjalan normal, karena sedikit fluktuasi
(naik turun) sangat mempengaruhi aktivitas enzim sel sehingga merubah seluruh
fungsi sel dan tubuh. Karena konsentrasi ion hydrogen normalnya adalah rendah
dan karena jumlahnya yang kecil ini tidak praktis, biasanya konsentrasi ion
hydrogen disebut dalam skala logaritma dengan menggunakan satuan pH. 1,3
Pengaturan keseimbangan ion hydrogen dalam beberapa hal sama dengan
pengaturan ion-ion lain dalam tubuh. Sebagai contoh, untuk mencapai
homeostasis, harus ada keseimbangan antara asupan dan produksi ion hydrogen
dan pembuangan ion hydrogen dari tubuh. Dan seperti pada ion-ion lain, ginjal
memainkan peranan kunci dalam pengaturan konsentrasi ion hydrogen. Terdapat
juga mekanisme penyangga asam basa yang melibatkan darah, sel-sel, dan
paru-paru yang perlu untuk mempertahankan konsentrasi ion hydrogen normal dalam
Gangguan keseimbangan asam basa disebut dengan istilah asidosis bila pH
darah bersifat asam dan alkalosis jika pH darah bersifat basa. Tergantung proses
primernya dapat dibagi menjadi asidosis atau alkalosis respiratorik (proses
primernya pada pernapasan) dan asidosis atau alkalosis metabolic (proses
primernya adalah gangguan metabolic). Akhiran osis pada asidosis ataupun
alkalosis menunjukkan proses primer yang menghasilkan asam atau basa tanpa
melihat nilai pH darah. Pada asidosis atau alkalosis ringan yang terkompensasi
sempurna, pH darah dapat tetap normal. Pada setiap gangguan keseimbangan
asam basa, selalu akan diikuti kompensasi untuk mempertahankan pH normal.
Kompensasi dari asidosis respiratorik adalah alkalosis metabolic, sedangkan
kompensasi dari alkalosis respiratorik adalah asidosis metabolic dan demikian
juga sebaliknya. 4,5
Elektrolit merupakan molekul ionisasi yang ditemukan dalam darah,
jaringan dan sel-sel tubuh. molekul ini, baik bemuatan positif (kation) dan negatif
(anion), mengkonduksi aliran listrik serta membantu keseimbangan Ph dan nilai
asam basa dalam tubuh. elektrolit juga memfasilitasi aliran cairan diantar dan
didalam sel melalui proses yang dikenal sebagai osmosis, serta berperan dalam
fungsi regulasi sistem neuromuscular. 12,13
Gangguan elektrolit merupakan ketidakseimbnagan antara garam ionisasi
tertentu ( seperti natrium, kalium, dan magnesium) dalam darah.
Obat-obatan, penyakit kronik dan trauma (seperti luka barar, fraktur, dan
atau terlalu rendah (hipo-). Jika hal ini terjadi dapat menghasilkan
BAB 2
TINJAUAN PUSTAKA
2.1 Asam dan Basa
Asam adalah setiap senyawa kimia yang melepaskan ion hidrogen ke suatu larutan atau ke senyawa biasa. Sedangkan basa adalah senyawa kimia yang menerima ion hidrogen. Adapun beberapa definisi oleh para pakar dimana menurut Bronsted-Lowry, Asam didefinisikan sebagai senyawa kima yang dapat bertindak sebagai proton donor (H+), sedangkan basa adalah senyawa kimia yang
dapat bertindak sebagai akseptor proton. Dalam solusi fisiologis, mungkin lebih baik menggunakan definisi dari Arrhenius, dimana dia mendefinisikan asam sebagai senyawa yang mengandung hidrogen dan bereaksi dengan air untuk membentuk ion hidrogen dan basa adalah senyawa yang menghasilkan ion hiroksida dalam air. 1,2
Asam kuat adalah asam yang berdiosiasi dengan cepat terutama melepaskan sejumlah besar ion H+ dalam larutan, contohnya HCl. Asam lemah
mempunyai lebih sedikit kecenderungan untuk berdisosiasikan ion-ionnya dan oleh karena itu kurang melepaskan H+, contohnya adalah H2CO3. 1
Basa kuat adalah suatu basa yang secara cepat dan kuat dengan H+ dan
oleh karena itu dengan cepat menghilangkannya dari larutan. Contohnya adalah ion hirdoksil (OH-) yang bereaksi dengan cepat membentuk air (H
2O). Basa lemah
adalah basa yang secara lemah bereaksi dengan ion H+, contohnya adalah HCO 3-.1
Keseimbangan asam-basa terkait dengan pengaturan konsentrasi ion H+
vena 7,35. Jika pH <7,35 dikatakan asidosis, dan jika pH darah >7,45 dikatakan alkalosis. Ion H+ terutama diperoleh dari aktivitas metabolik tubuh. H+ secara
normal dan kontinyu akan ditambahkan ke cairan tubuh dari 3 sumber, yaitu: 1. Pembentukan asam karbonat dan sebagian akan berdisosiasi menjadi H+
dan bikarbonat.
2. Katabolisme zat organik
3. Disosiasi asam organik pada metabolismme intermedia, misalnya pada metabolisme lemak terbentuk asam lemak dan laktat, sebagian asam ini akan berdisosiasi melepaskan ion H+. 1,2
Fluktuasi konsentrasi ion H+ dalam tubuh akan mempengaruhi fungsi normal sel,
antara lain :
1. Perubahan eksitabilitas saraf dan otot. Pada asidosis terjadi depresi susunan saraf pusat, sebaliknya pada alkalosis terjadi hiperekstabilitas. 2. Mempengaruhi enzim-enzim dalam tubuh.
3. Mempengaruhi konsentrasi ion K+
Bila terjadi perubahan konsentrasi ion H+ maka tubuh berusaha mempertahankan ion H+ seperti semula dengan cara:
1. Mengaktifkan sistem buffer
2. Mekanisme pengontrolan pH (kompensasi) oleh sistem pernapasan. 3. Mekanisme pengontrolan pH (kompensasi) oleh sistem ginjal. 1,2
2.2 Mekanisme Kompensasi
1. Body buffer
Fisiologis dari buffer penting pada manusia termasuk bikarbonat (H2CO3/HCO3-), hemoglobin (HbH/Hb-), protein intraseluler lainnya
(PrH/Pr), fosfat (H2PO4-/HPO42-) dan ammonia (NH3/NH4+). Efektivitas
dari buffer ini pada berbagai kompertemen cairan berhubungan dengan konsentrasi mereka. Bikarbonat merupakan buffer yang paling penting dalam kompartemen cairan ekstraseluler. Hemoglobin, meskipun dibatasi oleh sel darah merah, juga berfungsi sebagai buffer yang penting dalam darah. Protein lain mungkin memainkan peran utama dalam buffer pada kompartemen cairan intraseluler. Ion fosfat dan ammonium merupakan buffer yang penting pada urine. 3,4
Bikarbonat
Meskipun dalam arti yang ketat, buffer bikarbonat terdiri dari H2CO3 dan HCO3-, tekanan CO2 dapat menggantikan H2CO3
karena:
H2O + CO2 ↔ H2CO3 ↔ H+ +HCO3
-Hidrasi CO2 dikatalis oleh karbonat anhidrase, jika
penyesuaian-penyesuaian yang dibuat untuk buffer bikarbonat dan jika koefisien kelarutan untuk CO2 dipertimbangkan, persamaan
Henderson-Hasselbach untuk bikarbionat dapat ditulis sebagai berikut:
Dicatat bahwa Pk yang baik dihapus dari pH arteri normal 7,40 yang berarti bahwa bikarbonat tidak akan diharapkan untuk menjadi buffer ekstraseluler yang efesien. Sistem bikarbonat bagaimanapun penting karena dua alasan:
1. Bikarbonat hadir dalam konsentrasi tinggi yang relatif pada cairan ekstreseluler.
2. Lebih penting lagi, PaCO2 dan plasma [HCO3-] diatur secara
ketat oleh paru-paru dan ginjal.
Kemampuan dua organ ini untuk mengubah rasio [HCO3-/PaCO2 memungkinkan mereka untuk mengerahkan
pengaruh penting teradap pH arteri.
Derivasi sederhana dan lebih praktis dari persamaan Henderson-hasselbach untuk buffer bikarbonat adalah sebagai berikut :
[H+] = 24 x PaCO2 (HCO3-)
Harus ditekankan bahwa buffer bikarbonat efektif terhadap metabolisme tetapi tidak pada gangguan asam basa pernapasan. 1,3,4,5
2. Kompensasi Respiratorik
Perubahan pada ventilasi alveolar berespon terhadap kompensasi respiratorik dari PaCO2 pada brainstem. Respon reseptor ini untuk mengubah pH
dari cairan CSF. Minute ventilation meningkat 1-4 L/menit untuk setiap (akut) 1 mmHg peningkatan PaCo2. Kenyataannya, paru-paru berespon untuk eliminasi
metabolisme lemak. Respon kompensasi respiratorik juga penting dalam melindungi penanda perubahan pH selama gangguan metabolik.
Disamping itu kemoreseptor pada arkus aorta dan sinus carotid yang mengatur frekuensi dan dalamnya nafas juga dipengaruhi oleh perubahan O2, pH
dan CO2 dalam darah. Kompensasi respiratori dalam mempertahankan
keseimbangan asam basa adalah dengan pengaturan konsentrasi CO2 cairan
ekstraseluler oleh paru. Dengan menyesuaikan PCO2 meningkat atau menurun,
paru secara efektif akan mengatur konsentrasi ion hydrogen cairan ekstraseluler. Peningkatan ventilasi akan mengurangi CO2 dan mengurangi konsentrasi ion
hidrogen demikian juga sebaliknya.
Pengaturan konsentrasi ion hidrogen dengan ventilasi paru ini diatur oleh sistem sirkulasi darah. Bila terjadi kenaikan pCO2, CO2 akan bereaksi dengan H2O
dan menghasilkan ion H+. Ion H+ ini akan merangsang kemoreseptor diarkus aorta
dan sinus carotid, kemudian N.IX dan X akan mengirimkan sinyal ke pusat pernapasan untuk meningkatkan ventilasi. Akibatnya, kadar CO2 berkurang dan
pH bertambah.
Selain CO2, penurunan kadar oksigen (hipoksemia) yaitu bila pO2 < 60
mmHg juga menstimulasi reseptor sinus carotid. Dan ion H+ dari produksi asam (misalnya asam laktat) selain hasil disosiasi CO2 juga bisa merangsang
Kompensasi respiratorik selama asidosis metabolik
Penurunan ph darah arteri menstimulasi pusat pernapasan pada brainsterm. Hasil peningkatan ventilasi alveolar menurunkan PaCO2 dan
cenderung untuk mengembalikan pH arteri ke nilai normal.
Kompensasi respiratorik dalam alkalosis metabolik
Peningkatan pH arteri menekan pusat pernapasan. Hasil dari hipoventilasi alveolar cenderung meningkatkan PaCO2 dan
mengembailkan pH arteri kenilai normal. 6,7
3. Kompensasi Ginjal
Regulasi ginjal untuk mengatur keseimbangan asam basa dilakukan dengan mengeluarkan urine yang asam atau basa. Pengeluaran urine asam akan mengurangi jumlah asam dalam cairan ekstraseluler dan meningkatkan pH. Sedangkan pengeluran urine basa akan menghilangkan basa dari cairan ekstraseluler dan menurunkan pH. 6,7
Ginjal mengatur konsentrasi ion hidrogen cairan ekstraseluler melalui tiga mekanisme, yaitu sekresi ion hdrogen dan reabsorbsi ion bikarbonat, asidifikasi
buffer dan eksresi ammonia. 6,7
Kompensasi Ginjal selama Asidosis
Respon ginjal terhadap keadaan asam terdiri dari 3 langkah: - Peningkatan reabsorbsi HCO3- yang difiltrasi
Kompensasi ginjal selama alkalosis
Jumlah HCO3- yang banyak secara normal difiltrasi dan
kadang-kadang direabsorbsi karena ginjal butuh eksresi bikarbonat dalam jumlah yang banyak jika dibutuhkan. Sebagai hasilnya, ginjal sangat efektif dalam proteksi terhadap keadaan metabolic alkalosis yang secara umum terjadi karena defisiensi sodium atau mineral kortikoid berlebih. Deplesi dari sodium akan menurunkan volume cairan ekstraseluler dan meningkatkan reabsorbsi Na+ dari tubulus proksimal ginjal. 6,7
2.3 Gangguan Keseimbangan Asam-Basa
Keseimbangan asam-basa darah dikendalikan secara seksama, karena perubahan pH yang sangat kecil pun dapat memberikan efek yang serius terhadap beberapa organ. 6
Tubuh menggunakan 3 mekanisme untuk mengendalikan keseimbangan asam-basa darah: . 7
1. Kelebihan asam akan dibuang oleh ginjal, sebagian besar dalam bentuk
amonia. Ginjal memiliki kemampuan untuk mengatur jumlah asam atau basa yang
dibuang,yang biasanya berlangsung selama beberapa hari.
2. Tubuh menggunakan penyangga pH (buffer) dalam darah sebagai pelindung terhadap perubahan yang terjadi secara tiba-tiba dalam pH darah. Suatu penyangga ph bekerja secara kimiawi untuk meminimalkan perubahan pH suatu larutan. Penyangga pH yang paling penting dalam darah adalah bikarbonat. Bikarbonat (suatu komponen basa) berada dalam kesetimbangan dengan
dalam aliran darah, maka akan dihasilkan lebih banyak bikarbonat dan lebih sedikit karbondioksida. Jika lebih banyak basa yang masuk ke dalam aliran darah, maka akan dihasilkan lebih banyak karbondioksida dan lebih sedikit bikarbonat. 3. Pembuangan karbondioksida. Karbondioksida adalah hasil tambahan penting dari metabolisme oksigen dan terus menerus yang dihasilkan oleh sel. Darah membawa karbondioksida ke paru-paru dan di paru-paru karbondioksida tersebut dikeluarkan (dihembuskan). 6,7
Pusat pernafasan di otak mengatur jumlah karbondioksida yang dihembuskan dengan mengendalikan kecepatan dan kedalaman pernafasan. Jika pernafasan meningkat, kadar karbon dioksida darah menurun dan darah menjadi lebih basa. Jika pernafasan menurun, kadar karbondioksida darah meningkat dan darah menjadi lebih asam. Dengan mengatur kecepatan dan kedalaman pernafasan, maka pusat pernafasan dan paru-paru mampu mengatur pH darah menit demi menit. 6,7
Asidosis adalah suatu keadaan pada saat darah terlalu banyak mengandung asam (atau terlalu sedikit mengandung basa) dan sering menyebabkan menurunnya pH darah.
Alkalosis adalah suatu keadaan pada saat darah terlalu banyak mengandung basa (atau terlalu sedikit mengandung asam) dan kadang menyebabkan meningkatnya pH darah.
Asidosis dan alkalosis bukan merupakan suatu penyakit tetapi lebih merupakan suatu akibat dari sejumlah penyakit. Terjadinya asidosis dan alkalosis merupakan petunjuk penting dari adanya masalah metabolisme yang serius. Asidosis dan alkalosis dikelompokkan menjadi metabolik atau respiratorik, tergantung kepada penyebab utamanya. 3
2.3.1 Asidosis
a. Definisi
Asiodos adalah suatu keadaan dimana adanya peningkatan asam didalam darah yang disebabkan oleh berbagai keadaan dan penyakit tertentu yang mana tubuh tidak bisa mengeluarkan asam dalam mengatur keseimbangan asam basa. Hal ini penting untuk menjaga keseimbangan fungsi sistem organ tubuh manusia. Gangguan keseimbangan ini dapat dikelompokkan dalam dua kelompok besar yaitu metabolik dan respiratorik. Ginjal dan paru merupakan dua organ yang berperan penting dalam pengaturan keseimbangan ini. 5
b. Patogenesis
Pada keadaan asidosis yang berperan adalah sistem buffer (penyangga) pada referensi ini akan dibahas tentang sistem buffer bikarbonat. Sistem penyangga bikarbonat terdiri dari larutan air yang mengandung bikarbonat yang terdiri dari larutan air yang mengandung dua zat yaitu asam lemah (H2CO3) dan
garam bikarbonat seperti NaHCO3. H2CO3 dibentuk dalam tubuh oleh reaksi CO2 dengan H2O.
CO2 + H2O <—-> H2CO3
Reaksi ini lambat dan sangat sedikit jumlah H2CO3 yang dibentuk kecuali
bila ada enzim karbonik anhidrase. Enzim ini terutama banyak sekali di dinding alveoli paru dimana CO2 dilepaskan, karbonik anhidrase juga ditemukan di sel-sel
epitel tubulus ginjal dimana CO2 bereaksi dengan H2O untuk membentuk H2CO3
H2CO3 berionisasi secara lemah untuk membentuk sejumlah kecil H+ dan HCO3-
-Komponen kedua dari sistem yaitu garam bikarbonat terbentuk secara dominan sebagai Natrium Bicarbonat (NaHO3) dalam cairan ekstraseluler.
NaHCO3 berionisasi hampir secara lengkap untuk membentuk ion-ion bicarbonat (HCO3-) dan ion-ion natrium (Na+) sebagai berikut :
NaHCO3 <—-> Na+ + HCO3
-Sekarang dengan semua sistem bersama-sama, kita akan mendapatkan sebagai berikut :
CO2 + H
2O <—-> H2CO3 <—-> H+ + HCO3- + Na+
Akibat disosiasi H2CO3 yang lemah, konsentrasi H+ menjadi sangat kuat
bila asam kuat seperti HCl ditambahkan ke dalam larutan penyangga bicarbonat, peningkatan ion hidrogen yang dilepaskan oleh asam disangga oleh HCO3 :
H + + HCO3- H
2CO3 CO2 + H2O
Sebagai hasilnya, lebih banyak H2CO3 yang dibentuk. Meningkatkan
produksi CO2 dan H2O. Dari reaksi ini kita dapat melihat bahwa ion hidrogen dari
asam kuat HCl, bereaksi dengan HCO3- untuk membentuk asam yang sangat
lemah yaitu H2CO3 yang kemudian membentuk CO2 dan H2O. CO2 yang
berlebihan sangat merangsang pernapasan yang mengeluarkan CO2 dari cairan
ekstraseluler. Ini berpengaruh terjadinya asidosis pada tubuh. 3,5
1. Asidosis Metabolik . 8
sebagai usaha tubuh untuk menurunkan kelebihan asam dalam darah dengan cara menurunkan jumlah karbon dioksida. Pada akhirnya, ginjal juga berusaha mengkompensasi keadaan tersebut dengan cara mengeluarkan lebih banyak asam dalam air kemih. Tetapi kedua mekanisme tersebut bisa terlampaui jika tubuh terus menerus menghasilkan terlalu banyak asam, sehingga terjadi asidosis berat dan berakhir dengan keadaan koma. 8
a. Etiologi 7
Penyebab asidosis metabolik dapat dikelompokkan kedalam 3 kelompok utama:
1. Jumlah asam dalam tubuh dapat meningkat jika mengkonsumsi suatu asam atau suatu bahan yang diubah menjadi asam. Sebagian besar bahan yang menyebabkan asidosis bila dimakan dianggap beracun. Contohnya adalah metanol (alkohol kayu) dan zat anti beku (etilen glikol). Overdosis aspirin pun dapat menyebabkan asidosis metabolik.
ginjal ini dikenal sebagai asidosis tubulus renalis, yang bisa terjadi pada penderita gagal ginjal atau penderita kelainan yang mempengaruhi kemampuan ginjal untuk membuang asam.
Secara umum, Penyebab utama dari asidois metabolik: - Gagal ginjal
- Asidosis tubulus renalis (kelainan bentuk ginjal) - Ketoasidosis diabetikum
- Asidosis laktat (bertambahnya asam laktat)
- Bahan beracun seperti etilen glikol, overdosis salisilat, metanol, paraldehid, asetazolamiatau amonium klorida
- Kehilangan basa (misalnya bikarbonat) melalui saluran pencernaan karena diare, ileostomi atau kolostomi.
Beberapa penyebab yang sering terjadi pada keadaan asidosis metabolik :
Asidosis di Tubulus Ginjal . 8
keadaan normal, ginjal menyerap asam sisa metabolisme dari darah dan membuangnya ke dalam urin. Pada penderita penyakit ini, bagian dari ginjal yang bernama tubulus renalis tidak dapat berfungsi sebagaimana mestinya, sehingga hanya sedikit asam yang dibuang ke dalam urin. Akibatnya terjadi penimbunan asam dalam darah, yang mengakibatkan terjadinya asidosis, yakni tingkat keasamannya menjadi di atas ambang normal. Diduga penyakit ini disebabkan faktor keturunan atau bisa timbul akibat obat-obatan, keracunan logam berat atau penyakit autoimun (misalnya lupus eritematosus sistemik atau sindroma Sjogren). Sejauh ini dunia kedokteran belum menemukan obat atau terapi untuk menyembuhkannya, karena penyakit ini tergolong sebagai kerusakan organ tubuh, sepertipenyakit diabetes mellitus (akibat kerusakan kelenjar insulin).
Sementara ini penanganan ATR baru sebatas terapi untuk mengontrol tingkat keasaman darah, yaitu dengan memberikan obat yang mengandung zat bersifat basa (alkalin) secara berkala (periodik), sehingga tercapai tingkat keasaman netral, seperti pada orang normal. Zat basa ini mengandung bahan aktif natrium bikarbonat (bicnat).
Diare .2
Diabetes Melitus 2
Diabetes melitus disebabkan oleh tidak adanya sekresi insulin oleh pankreas yang menghambat penggunaan glukosa dalam metabolisme.Ini terjadi karena adanya pemecahan lemak menjadi asam asetoasetat dan asam ini di metabolisme oleh jaringan untuk menghasilkan energi, menggantikan glukosa. Pada DM yang berat kadar Asetoasetat dalam darah meningkat sangat tinggi sehingga menyebabkan asidosis metabolik yang berat.
Penyerapan Asam 2
Jarang sekali sejumlah besar asam diserap dari makanan normal akan tetapi asidosis metabolik yang berat kadang-kadang dapat disebabkan oleh keracuan asam tertentu antara lain aspirin dan metil alkohol.
Gagal Ginjal Kronis 2
Saat fungsi ginjal sangat menurun terdapat pembentukan anion dari asam lemak dalam cairan tubuh yang tidak eksresikan oleh ginjal. Selain itu penurunan laju filtrasi glomerulus mengurangi eksresi fosfat dan NH4 + yang mengurangi jumlah bikarbonat.
b. Gejala Klinis 4
asidosis semakin memburuk, tekanan darah dapat turun, menyebabkan syok, koma dan kematian.
c. Diagnosa 4
Diagnosis asidosis biasanya ditegakkan berdasarkan hasil pengukuran pH darah yang diambil dari darah arteri (arteri radialis di pergelangan tangan). Darah arteri digunakan sebagai contoh karena darah vena tidak akurat untuk mengukur pH darah. Untuk mengetahui penyebabnya, dilakukan pengukuran kadar karbon dioksida dan bikarbonat dalam darah. Mungkin diperlukan pemeriksaan tambahan untuk membantu menentukan penyebabnya. Misalnya kadar gula darah yang tinggi dan adanya keton dalam urin biasanya menunjukkan suatu diabetes yang tak terkendali. Adanya bahan toksik dalam darah menunjukkan bahwa asidosis metabolik yang terjadi disebabkan oleh keracunan atau overdosis. Kadang-kadang dilakukan pemeriksaan air kemih secara mikroskopis dan pengukuran pH air kemih.
d. Penatalaksanaan 4
Pengobatan asidosis metabolik tergantung kepada penyebabnya. Sebagai contoh, diabetes dikendalikan dengan insulin atau keracunan diatasi denganmembuang bahan racun tersebut dari dalam darah. Kadang-kadang perlu dilakukan dialisa untuk mengobati overdosis atau keracunan yang berat. Asidosis metabolik juga bisa diobati secara langsung. Bila terjadi asidosis ringan, yang diperlukan hanya cairan intravena dan pengobatan terhadap penyebabnya.
Koreksi asidosis metabolik dapat dilakukan dengan rumus yaltu: 1. (Ki - Ku) x BB x 0.6 = mEq NaHCO3.
Ki = kadar bikarbonat yang ingin dicapai Ku = kadar bikarbonat terukur saat itu. 1. Asidosis Respiratorik . 10
Asidosis Respiratorik adalah keasaman darah yang berlebihan karena penumpukan karbondioksida dalam darah sebagai akibat dari fungsi paru-paru yang buruk atau pernafasan yang lambat. Kecepatan dan kedalaman pernafasan mengendalikan jumlah karbondioksida dalam darah. Dalam keadaan normal, jika terkumpul karbondioksida, pH darah akan turun dan darah menjadi asam. Tingginya kadar karbondioksida dalam darah merangsang otak yang mengatur pernafasan, sehingga pernafasan menjadi lebih cepat dan lebih dalam. Keadaan ini timbul akibat ketidakmampuan paru untuk mengeluarkan CO2 hasil metabolisme (keadaan hipoventilasi). Hal ini menyebabkan peningkatan H2CO3 dan konsentrasi ion hidrogen sehingga menghasilkan asidosis.
a. Etiologi
Penurunan pernapasan. 10
hiperkalemi) juga secara lambat menghalangi depolarisasi neural. Akibat neuron respiratorik juga akan mengurangi keadaan fisik. Trauma sebagai hasil langsung
kerusakan fisik untuk neuron respirasi atau menimbulkan hypoksia sampai iskemik yang dapat mengganggu atau menghancurkan kemampuan neuron untuk membangkitkan dan mengirimkan impuls ke otot skeletal yang membantu dalam respirasi. Neuron respirasi dapat rusak atau hancur secara tidak langsung apabila terdapat masalah di area otak karena meningkatnya tekanan intrakranial. Meningkatnya tekanan intrakranial ini karena adanya edema jaringan,dimana menekan pusat pernapasan (batang otak). Trauma spinal cord, penyakit tertentu seperti polio adalah sebab yang aktual bagi kerusakan diaxon dan penyakit lain seperti mistenia gravis, dan syndrom Guillain-Barre yang mengganggu tranmisi impuls nervous ke otot skele.
Inadequatnya Ekspansi Dada10
membatasi perpindahan pernapasan dalam dinding dada jika terdapat kerusakan tulang atau malformasi tulang yang menyebabkan distorsi dalam fungsi dada. Struktur tulang dada yang tidak berbentuk serasi dapat membentuk deformasi
pada rongga dada dan mencegah penuhnya ekspansi pada satu atau kedua paru.
Deformitas skeletal mungkin congenital: hasil dari kesalahan pertumbuhan tulang
( seperti skoliosis, osteogenesis imperfecta dan syndrome Hurler’s) atau hasil yang tidak seimbang dari degenerasi jaringan tulang (osteoporosis, metastase sel kanker). Kondisi kelemahan otot respirasi berhubungan dengan ketidakseimbangan elektrolit dan kelelahan.
Obstruksi jalan napas10
dan asma) dan dan masuknya bahan-bahan iritan seperti asap rokok, debu batu bara, serat asbes, serat kapas, debu silikon dan beberapa partikel yang
mencapai jalan napas bagian bawah.
Gangguan difusi alveolar-kapiler 10
Pertukaran gas pulmonal terjadi oleh difusi di persimpangan alveolar dan membrane kapiler. Beberapa kondisi dimana mencegah atau mengurangi proses difusi karena dapat meretensi CO2 dan terjadi asidemia. Masalah difusi dapat terjadi pada membran alveolar, membran kapiler atau area diantara keduanya. Asidosis respiratorik sering terjadi akibat kondisi patologis yang merusak pusat pernapasan atau yang menurunkan kemampuan paru untuk mengeliminasikan CO2.
b. Manifestasi Klinik
Meningkatnya nadi dan tingkat pernapasan
Pernapasan dangkal
Dyspnea
Pusing
Convulsi
Letargi
Kelemahan
sakit kepala
c. Penatalaksanaan 5
organik lainnya dalam cairan ektraselular. Koreksi cairan perlu disertai pemeriksaan pH dan analisis gas darah. Pengobatan yang tepat adalah memperbaiki ventilasi dengan respirator. Pengobatan dengan natrium bikarbonat kurang tepat, karena tindakan ini malahan akan menyebabkan hiperosmolalitas dan gagal jantung. Pengobatan ditujukan terhadap etiologi, disamping usaha untuk meningkatkan pCO2 dalam darah. Pemberian amonium kiorida tidak dianjurkan. Bernapas dalam sungkup yang dipasang di wajah (rebreathing,) dapat mengurangi gejala dan kehilangan CO2 pada hiperventilasi akut.
2.3.2 Alkalosis
a. Definisi
Alkalosis adalah suatu keadaan pada saat darah terlalu banyak mengandung basa (atau terlalu sedikit mengandung asam) dan kadang menyebabkan peningkatan pH darah.
b. Etiologi
1. Alkalosis respiratori yang disebabkan rendahnya tingkat karbon. Berada dalam tekanan tinggi atau memiliki penyakit yang menyebabkan bekurangnya kadar oksigen dalam darah dapat mengakibatkan jantung bernafas lebih cepat (hiperventilate), yang menurunkan kadar karbondioksida.
3. Hypokelemik alkalosis disebabkan oleh respon ginjal terhadap kurangnya atau hilangnya potassium, yangg dapat muncul ketika seseorang mengambil pengobatan diuretik.
4. Hipochloremik alkalosis disebabkan oleh kurangnya atau hilangnya klorit, yang muncul disertai dengan muntah berkepanjangan.
1. Alkalosis Respiratorik 4
a. Definisi
Alkalosis Respiratorik adalah suatu keadaan dimana darah menjadi basa karena pernafasan yang cepat dan dalam, sehingga menyebabkan kadar karbondioksida dalam darah menjadi rendah.
b. Etiologi
Penyebab :Pernafasan yang cepat dan dalam disebut hiperventilasi, yang menyebabkan terlalu banyaknya jumlah karbondioksida yang dikeluarkan dari aliran darah. Penyebab hiperventilasi yang paling sering ditemukan adalah kecemasan.
Penyebab lain dari alkalosis respiratorik adalah: - rasa nyeri
- kadar oksigen darah yang rendah - demam
c. Manifestasi Klinis 8
Alkalosis respiratorik dapat membuat penderita merasa cemas dan dapat menyebabkan rasa gatal disekitar bibir dan wajah. keadaannya makin memburuk, bisa terjadi kejang otot dan penurunan kesadaran. d. Diagnosa 6
Diagnosis ditegakkan berdasarkan hasil pengukuran kadar karbondioksida dalam darah arteri. pH darah juga sering meningkat. e. Penatalaksanaan
Biasanya satu-satunya pengobatan yang dibutuhkan adalah memperlambat pernafasan. Jika penyebabnya adalah kecemasan, memperlambat pernafasan bisa meredakan penyakit ini.Jika penyebabnya adalah rasa nyeri, diberikan obat pereda nyeri. Menghembuskan nafas dalam kantung kertas (bukan kantung plastik) bisa membantu meningkatkan kadar karbondioksida setelah penderita menghirup kembali karbondioksida yang dihembuskannya.
2. Alkalosis Metabolik 6
a. Definisi :
Alkalosis Metabolik adalah suatu keadaan dimana darah dalam keadaan basa karena tingginya kadar bikarbonat.
b. Etiologi
Penyebab Alkalosis metabolik terjadi jika tubuh kehilangan terlalu banyak asam. Sebagai contoh adalah kehilangan sejumlah asam lambung selama periode muntah yang berkepanjangan atau bila asam lambung disedot dengan selang lambung (seperti yang kadang-kadang dilakukan di rumah sakit, terutama setelah pembedahan perut).
Pada kasus yang jarang, alkalosis metabolik terjadi pada seseorang yang mengkonsumsi terlalu banyak basa dari bahan-bahan seperti soda bikarbonat. Selain itu, alkalosis metabolik dapat terjadi bila kehilangan natrium atau kalium dalam jumlah yang banyak mempengaruhi kemampuan ginjal dalam mengendalikan keseimbangan asam basa darah.
c. Penatalaksanaan
Pengobatan alkalosis metabolik adalah dengan pemberian ainonium kiorida dengan dosis dihitung menurut rumus:
Amonium kiorida yang diperlukan (mEq) = (Ki - Ku) x BB x fd Keterangan:
Ki = konsentrasi bikarbonat natrikus yang diinginkan
Ku = konsentrasi bikarbonat natrikus yang diukur
BB = berat badan dalam kg
2.4 Keseimbangan Elektrolit
Elektrolit adalah senyawa didalam larutan yang berdisosiasi menjadi partikel yang bermuatan ( ion) positif atau negatif. Ion bermuatan positif disebut kation. Dan ion bemuatan negatif disebut anion. Keseimbangan keduanya disebut sebagai elektronetralitas. 12,15
Sebagian besar proses metabolisme memerlukan dan dipengaruhi oleh elektrolit. Konsentrasi elektrolit yang tidak normal dapat menyebabkan banyak gangguan. Pemeliharaan homeostasis cairan tubuh adalah penting bagi kelangsungan hidup organisme. Pemeliharaan tekanan osmotik dan distribusi beberapa kompartemen cairan tubuh manusia adalah fungsi utama empat elektrolit mayor, yaitu natrium (Na+), kalium (K+), klorida (Cl-) dan bikarbonat (HCO
3).
Pemerikasaan keempat elektrolit tersebut dalam klinis disebut sebagai “profil elektrolit”. 12,14,16
2.4.1 Natrium
A. Fisiologi Natruim
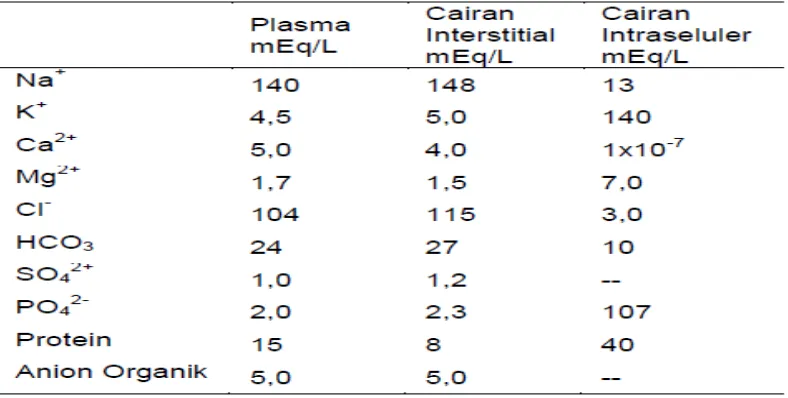
Natrium adalah kation terbanyak dalam cairan ekstrasel, jumlahnya bisa mencapai 60 mEq per kilogram berat badan dan sebagian kecil (sekitar 10-14 mEq/L) berada dalam cairan intrasel. Lebih dari 90% tekanan osmotik didalam ekstrasel ditentukan oleh garam yang mengandung natrium klorida (NaCl) dan natrium bikarbonat (NaHCO3) sehingga perubahan tekanan osmotik pada cairan
ekstrasel menggambarkan perubahan konsentrasi natrium. 14
Perbedaan kadar natrium intravaskuler dan interstitial disebabkan oleh keseimbangan Gibbs-Donnan, sedangkan perbedaan kadar natrium dalam cairan ekstrasel dan intrasel disebabkan oleh adanya transport aktif dari natrium keluar sel yang bertukar dengan masuknya kalium kedalam sel (pompa Na+ K+).14 Kadar
natrium dalam cairan ekstrasel dan cairan intrasel dapat dilihat pada tabel berikut. Jumlah natrium dalam tubuh merupakan gambaran natrium yang masuk dan natrium yang dikeluarkan. Pemasukan natrium yang berasal dari diet melalui epitel mukosa saluran cerna dengan proses difusi dan pengeluarannya melalui ginjal atau saluran cerna atau keringat dikulit. Pemasukan dan pengeluaran natrium perhari mencapai 48-144 mEq. 14
Keringat adalah cairan hipotonik yang berisi natrium dan klorida. Kandungan natrium pada cairan keringat orang normal rerata 50 mEq/L. Jumlah pengeluaran keringat akan meningkat sebanding dengan lamanya periode terpapar pada lingkungan yang panas, latihan fisik dan demam. Eksresi natrium terutama dilakukan oleh ginjal. Pengaturan eksresi ini dilakukan untuk mempertahankan homeostasis natrium, yang sangat diperlukan untuk mempertahankan volume cairan tubuh. natrium difiltrasi bebas diglomelurus, direabsorbsi secara aktif 60-65% ditubulus proksimal bersama dengan H2O dan klorida yang direabsorbsi
secara pasif, sisanya direabsorbsi di lengkung henle (25-30%), tubulus distal (5%) dan duktus koligentes (4%). Sekresi natrium diurine <1%. Aldosteron menstimulasi tubulus distal untuk mereabsorbsi natruim bersama air secara pasif dan mensekresi kalium pada sistem rennin-angiotensin-aldosteron untuk mempertahankan elektroneutralitas. 12,15
Tabel 2. Nilai Rujukan Natrium B. Gangguan Keseimbangan Natrium
1. Hipernatremia
a. Etiologi
Adanya defisit cairan tubuh akibat defisit air melebihi ekresi natrium atau asupan air berkurang. Misalnya pada pengeluaran air tanpa elektrolit melalui “isensible water loss” atau keringat, osmotik diare akibat pemberian laktulosa atau sorbitol, diabetes insipidus sentral maupun nefrogenik, diuresis osmotik akibat glukosa atau manitol. Gangguan pusat rasa haus di hipotalamus akibat tumor atau gangguan vaskular. Deplesi volume dan defisit cairan menyebabkan ekresi Na dalam urin rendah sehingga kadarnya kurang dari 25 mEq/L. 18
Penambahan natrium yang melebihi jumlah cairan dalam tubuh misalnya koreksi bikarbonat berlebihan pada asidosis metabolik. Pada keadaan ini tidak terjadi deplesi volume sehingga natrium yang berlebihan akan diekresikan dalam urine menyebabkan kadar Na dalam urine lebih dari 100 mEq/L. 18
Masuknya air tanpa elektrolit dalam sel. Misalnya pada latihan olahraga yang berat, asam laktat dalam sel meningkat sehingga osmolalitas sel juga meningkat dan air dari ekstrasel akan masuk kedalam intrasel. Biasanya kadar natrium akan kembali normal dalam waktu 5-15 menit setelah istirahat.
kekurangan air tidak diatasi dengan baik misalnya pada orang dengan usia lanjut, diabetes insipidus (volume urine dapat >10L). 18
b. Gejala klinis
Gejala klinis pada hipervolemia timbul pada keadaan peningkatan plasma secara akut hingga diatas 158 meq/L. Gejala yang ditimbulkan akibat mengecilnya volume otak oleh karena air keluar dari dalam sel. Pengecilan volume ini menimbulkan robekan pada vena menyebabkan perdarahan lokal diotak dan perdarahan subarahnoid. Gejala dimulai dari letargi, lemas, kejang dan akhirnya koma. Kenaikan akut diatas 180 meq/L dapat menimbulkan kematian. 18
c. Penatalaksanaan
Langkah pertama yang dilakukan adalah menetapkan etiololgi hipernatremia. Sebagian besar penyebab hipetnremia adalah defisit cairan tanpa elektrolit akibat koreksi air yang tidak cukup akan kehilangan cairan tanpa elektrolit melalui saluran cerna, urin, atau saluran napas.
2. Hiponatremi
a. Definisi
Hiponatremi (kadar natrui darah yang rendah) adalah konsentrasi natruim yang lebih kecil dari 136 mEq/L darah. 14.18
b. Etiologi
Respon fisiologi dari hiponatermia adalah tertekannya pengeluaran ADH dari hipotalamus sehingga ekresi urine meningkat oleh karena saluran air (AQP2) dibagian apikal duktus koligentes berkurang (osmolaritas urine rendah).
Hiponatermi terjadi bila:
Jumlah asupan cairan melebihi kemampuan eksresi
Ketidakmampuan menekan sekresi ADH misalnya pada kehilangan cairan melalui saluran cerna atau gagal jantung atau sirosis hati atau pada SIADH ( syndrome of inappropriate ADH-secretion).
Konsentrasi natrium darah menurun jika natrium telah dilarutkan terlalu banyaknya air dalam tubuh. Pengenceran natrium bisa terjadi pada orang yang minum air dalam jumlah yang sangat banyak (seperti yang kadang terjadi pada kelainan psikis tertentu) dan pada penderita yang dirawat di rumah sakit, yang menerima sejumlah besar cairan intravena. 14,18
Hiponatremia juga sering terjadi pada penderita gagal jantung dan sirosis hati, dimana volume darah meningkat.Pada keadaan tersebut, kenaikan volume darah menyebabkan pengenceran natrium, meskipun jumlah natrium total dalam tubuh biasanya meningkat juga. 14,18
Hiponatremia terjadi pada orang-orang yang kelenjar adrenalnya tidak berfungsi (penyakit Addison), dimana natrium dikeluarkan dalam jumlah yang sangat banyak. Pembuangan natrium ke dalam air kemih disebabkan oleh kekurangan hormon aldosteron. 14,18
Penderita Syndrome of Inappropriate Secretion of Antidiuretik Hormone (SIADH) memiliki konsentrasi natrium yang rendah karena kelenjar hipofisa di dasar otak mengeluarkan terlalu banyak hormon antidiuretik.
Hormon antidiuretik menyebabkan tubuh menahan air dan melarutkan sejumlah natrium dalam darah.
Penyebab SIADH:
- Meningitis dan ensefalitis - Tumor otak
- Psikosa
- Penyakit paru-paru (termasuk pneumonia dan kegagalan pernafasan akut) - Kanker (terutama kanker paru dan pankreas)
- Obat-obatan:
Chlorpropamide (obat yang menurunkan kadar gula darah)
Carbamazepine (obat anti kejang)
Clofibrate (obat yang menurunkan kadar kolesterol)
Obat-obat anti psikosa
Aspirin, ibuprofen dan analgetik lainnya yang dijual bebas
Vasopressin dan oxytocin (hormon antidiuretik buatan). 18, 20, 21
c. Gejala Klinis
Beratnya gejala sebagian ditentukan oleh kecepatan menurunnya kadar natrium darah. Jika kadar natrium menurun secara perlahan, gejala cenderung tidak parah dan tidak muncul sampai kadar natrium benar-benar rendah.Jika kadar natrium menurun dengan cepat, gejala yang timbul lebih parah dan meskipun penurunannya sedikit, tetapi gejala cenderung timbul. 18, 21
Otak sangat sensitif terhadap perubahan konsentrasi natrium darah. Karena itu gejala awal dari hiponatremia adalah letargi (keadaan kesadaran yang menurun seperti tidur lelap, dapat dibangunkan sebentar, tetapi segera tertidur kembali). Sejalan dengan makin memburuknya hiponatremia, otot-otot menjadi kaku dan bisa terjadi kejang. Pada kasus yang sangat berat, akan diikuti dengan stupor (penurunan kesadaran sebagian) dan koma. 18,21
d. Diagnosa
Diagnosis ditegakkan berdasarkan hasil pemeriksaan darah dan gejala-gejalanya.
Hiponatremia akut : diartikan sebagai kejadian hiponatremia dalam jangka
yang dapat menyebabkan kejang dan penurunan kesadaran. Edema otak yang terjadi, dibatasi oleh kranium disekitarnya, yang mengakibatkan terjadinya hipertensi intrakranial dengan resiko brain injury. 18
Hiponatremia kronik: diartikan sebagai keadaan hiponatremia dalam
jangka waktu yang lebih dari 48 jam. Gejala yang timbul tidak berat karena ada proses adaptasi. Pada keadaan ini, cairan akan keluar dari jaringan otak dalam beberapa jam. Gejala yang timbul hanya berupa lemas dan mengantuk, bahkan dapat tanpa gejala. Keadaan ini dikenal juga dengan hiponatremia asimtomatik. Namun perlu diperhatikan pada proses adaptasi ini dapat menjadi proses yang berlebihan yang berisiko terjadinya demielinisasi osmotik. 18
e. Penatalaksanaan
Langkah pertama yang dilakukan adalah mencari sebab terjadinya hiponatremia dengan cara:
- Anamnesis yang teliti (antara lain riwayat muntah, penggnaan diuresis, penggunaan manitol)
- Pemeriksaan fisik yang teliti (antara lain apakah ada tanda hipovolemi atau tidak)
- Pemeriksaan gula darah, lipid darah
- Pemeriksaan osmolalitas urin atau dapat juga dengan memeriksa Berat jenis urine (interpretasi terhadap adakah ADH yang meningkat atau tidak, gangguan pemekatan)
- Pemeriksaan natrium, kalium dan klorida dalam urine untuk melihat jumlah eksresi eletrolit dalam urine.
- Langkah selanjutnya adalah melakukan pengobatan tepat sasaran. Perlu dibedakan apakah kejadian hiponatremi akut atau kronik
- Tanda atau penyakit lain yang menyertai hiponatremia perlu dikenali (deplesi volume, dehidrasi, gagal jantung, gagal ginjal)
- Hiponatremi akut : koreksi Na dilakukan secara cepat dengan dilakukan pemberian natrium hipertonik intravena. Kadar natrium plasma dinaikkan sebanyak 5 mEq/L dari kadar natrium awal dalam waktu 1 jam. Setelah itu, kadar natrium plasma dinaikkan sebesar 1 mEq/L setiap 1 jam sampai kadar natrium darah mencapai 130 meq/L. Rumus yang dipakai untuk mengetahui jumlah natrium dalam larutan hipertonik yang diberikan adalah:
0,5 x Berat Badan (Kg) x delta Na
Delta Na: selisih antara kadar natrium yang diinginkan dengan kadar natrium awal.
yang diberikan dapat dalam bentuk hipertonik intravena atau natrium oral. 18
2.4.2 Kalium
A. Fisiologi Kalium
Kalium merupakan kation yang memiliki jumlah yang sangat besar dalam tubuh dan terbanyak berada di intrasel. Kalium berfungsi dalam sintesis protein, kontraksi otot, konduksi saraf, pengeluaran hormon, transpot cairan, dan perkembangan janin. Sekitar 98% jumlah kalium dalam tubuh berada di dalam cairan intrasel. Konsentrasi kalium intrasel sekitar 145 mEq/L dan konsentrasi kalium ekstrasel 4-5 mEq/L (sekitar 2%). Jumlah konsentrasi kalium pada orang dewasa berkisar 50-60 per kilogram berat badan (3000-4000 mEq). 22
bersama dengan natrium dan klorida di lengkung henle. Kalium dikeluarkan dari tubuh melalui traktus gastrointestinal kurang dari 5%, kulit dan urine mencapai 90%. dan cairan interstisial dipengaruhi oleh keseimbangan Gibbs-Donnan, sedangkan perbedaan kalium cairan intrasel dengan cairan interstisial adalah akibat adanya transpor aktif (transpor aktif kalium ke dalam sel bertukar dengan natrium). Kadar kalium plasma kurang dari 3,5 meq/L disebut sebagai hipokalemi dan kadar lebih dari 5 meq/L disebut hiperkalemi. Kedua kelainan ini dapat menyebabkan kelainan fatal listrik jantung yaitu disebut aritmia. 21,22
B. Gangguan Keseimbangan Kalium
1. Hiperkalemia
a. Definisi
Disebut hiperkalemia bila kadar kalium dalam plasma lebih dari 5 meq/L. Dalam keadaan normal jarang terjadi hiperkalemia oleh karena adanya mekanisme adaptasi oleh tubuh. 14,18
b. Etiologi
Keluarnya kalium dari intrasel ke ekstrasel.
Berkurangnya eksresi kalium melalui ginjal
Berkurangnya eksresi kalium melalui ginjal terjadi pada keadaan hiperaldosteronisme, gagal ginjal, deplesi volume sirkulsi efektif, pamakaian siklosporin.14,18
c. Gejala Klinis
Hiperkalemia dapat meningkatkan kepekaan membran sel sehingga dengan sedikit perubahan depolarisasi, potensial aksi akan lebih mudah terjadi. Dalam klinik ditemukan gejala akibat gangguan konduksi listrik jantung, kelemahan otot sampai dengan paralisis sehingga pasien merasa sesak napas. Gejala ini timbul pada kadar K >7 meq/L atau kenaikan yang terjadi dalam waktu yang cepat. Dalam keadaan asidosis metabolik dan hipokalsemi, mempermudah timbulnya gejala klinik hipekalemi. 14,18
d. Penatalaksanaan
Prinsip pengobatan hiperkalemia adalah:
Memacu masuknya kembali kalium dari ekstrasel ke intrasel dengan cara:
o Pemberian insulin 10 unit dalam glukosa 40%, 50 ml bolus intravena, lalu diikuti dengan infuse dekstrose 5% untuk mencegah terjadinya hipoglikemi. Insulin akan memacu pompa NaK-ATPase memasukkan kalium kedalam sel, sedangkan glukosa/dekstrose akan memicu pengeluaran insulin endogen.
o Pemberian natrium bikarbonat yang akan meningkatkan pH sistemik. Peningkatan pH akan meangsang ion-H keluar dari dalam sel yang kemudian menyebabkan ion-K masuk kedalam sel. Dalam keadaan tanpa asidosis metabolik, natrium bikarbonat diberikan 50 meq i.v selama 10 menit. Bila ada asidosis metabolik, disesuaikan dengan keadaan asidosis metabolik yang ada.
o Pemberian α2-agonis akna merangsang pompa NaK-ATPase, kalium masuk kedalam sel. Albuterol diberikan 10-20 mg.
Mengeluarkan kelebihan natrium dalam tubuh.
o Pemberian diuretic loop (furosemid) dan tiazid sifatnya hanya sementara.
o Hemodialisa. 17,18,20
2. Hipokalemia
a. Definisi
b. Etiologi
Asupan kalium yang kurang.
pengeluaran kalium yang berlebihan melalui saluran cerna atau ginjal atau keringat.
Kalium masuk kedalam sel
Pengeluaran kalium yang berlebihan dari saluran cerna antara lain muntah, selang naso-gastrik, diare atau pemakaian pencahar. Pada keadaan muntah atau pemakaian selang nasogastrik, pengeluaran kalium bukan melalui saluran cerna atas karna kadar kalium dalam cairan lambung hanya sedikit (5-10 meq/L), akan tetapi kalium akan benayak keluar melalai ginjal. Akibat muntah atau selang nasogastrik, terjadi alkalosis metabolic sehingga banyak bikarbonat yang difiltrasi diglomerulus yang akan mengikat kalium ditubulus distal (duktud kolingentes) yang juga dibantu dengan adanya hiperladosteron akibat munttah. Kesemuanya ini akan meningkatkan ekresi kalium melalui urine dan terjadi hipokalemia. Pada saluran cerna bawah, kalium keluar bersama bikarbonat (asidosis metabolic). Kalium dalam saluran cerna bawah jumlahnya lebih banyak (20-50 meq/L). 12,14,18,21
lumen lalu dikeluarkan dengan urin, pada hipomagnesemia, poliuria (polidipsi primer, diabetes insipidus) dan salt-wasting nephrophaty (sindrom barter atau gitelman, hiperkalsemi). 12,14,18,21
Pengeluaran kalium berlebihan melalui keringat dapat terjadi bila dilakukan latihan berat pada lingkungan yang panas sehingga produksi keringat mencapai 10L. 18
c. Gejala Klinis
Kelemahan otot, perasaan lelah, nyeri otot, restless legs sindrom merupakan gejala otot yang timbul pada kadar kalium kurang dari 3meq/L. penurunan yang lebih berat dapat menimbulkan kelumpuhan.
Aritmia berupa timbulnya fibrilasi atrum, takikardi ventrikular merupakan efek hipokalemia pada jantung. Hal ini terjadi akibat perlambatan repolarisasi ventrikel pada kejadian hipokalemia yang menimbulkan peningkatkan arus re-entry.
Efek hipokalemi pada ginjal dapat berupa timbulnya vakuolisasi pada tubulus proksimal dan distal. Juga terjadi gangguan pemekatan urine sehingga menimbulkan poliuri dan polidipsi. Hipokalemi juga akan meningkatkan produksi HN4 dan produksi bikarbonat di tubulus proksimal yang akan menimbulkan
alkalosis metabolik. 14,18
d. Diagnostik
urine lebih dari 40meq/hari menandakan adanya pembuangan kalium berlebihan melalui ginjal.
Eksresi kalium yang rendah melalui ginjal disertai dengan adanya asidosis metabolic merupakan penanda adanya pembuangan kalium berlebihan melalui saluran cerna seperti diare akibat infeksi atau penggunaan pencahar.
Eksresi kalium berlebihan melalui ginjal dengan disertai asidosis metabolickmerupakan petanda adanya ketoasidosis diabetic atau adanya RTA
(Renal Tubular Acidosis) baik yang distal maupun yang proksimal.
Eksresi kalium urine yang rendah disertai alkalosis metabolik, petanda dari muntah kronik ataupun pemberian diuretic lama.
Eksresi kalium dalam urine tinggi disertai alkalosis metabolic dan tekanan darah yang rendah petanda dari sindrom bartter. 14,18
e. Pemeriksaan Penunjang
. Kadar K dalam serum
Kadar K, Na, Cl dalam urin 24 jam
Kadar Mg dalam serum
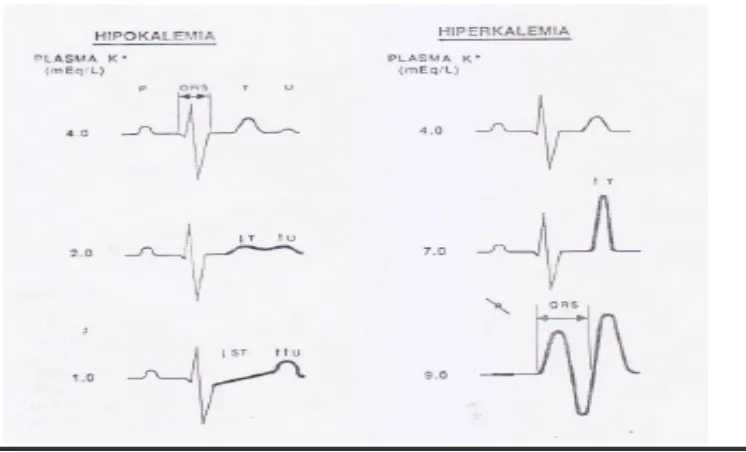
Analisis gas darah
Gambar 3. Gambaran EKG pada gangguan kalium f. Penatalaksanaan
Kalium biasanya dapat dengan mudah digantikan dengan mengkonsumsi makanan yang banyak mengandung kalium atau dengan mengkonsumsi garam kalium (kalium klorida) per-oral. Kalium dapat mengiritasi saluran pencernaan, sehingga diberikan dalam dosis kecil, beberapa kali sehari. 14,18
Diberikan kalium oral atau bila perlu parental sampai sebanyak 3 mEq/kgBB/24 jam. Pada sindrom Bartter atau kehilangan K eksesif melalui urin, kalium dapat diberikan sampaik mEq/I/hari per oral. Pemberian kalium per infus tidak boleh melebihi 40 mEq/I 14,18
Bila ada intoksikasi digitalis, aritmia, atau kadar K serum < 3 mEq/L, koreksi K secara intravena 20 mEq/jam dalam 50-100 cc larutan dekstrosa 5%.
Bila kadar kalium dalam serum > 3 mEq/L, koreksi K cukup per oral.
Monitor kadar kalium tiap 2-4 jam untuk menghindari hiperkalemia terutama pada pemberian secara intravena.
Pemberian K intravena dalam bentuk larutan KCl disarankan melalui vena yang besar dengan kecepatan 10-20 mEq/jam, kecuali disertai aritmia atau kelumpuhan otot pernafasan, diberikan dengan kecepatan 40-100 mEq/jam. KCl dilarutkan sebanyak 20 mEq dalam 100 cc NaCl isotonik.14,18
2.4.3 Kalsium
A. Fisiologi kalsium
membran plasma terhadap ion natrium.2,4 Metabolisme kalsium diatur tiga hormon utama yaitu hormon paratiroid (PTH),kalsitonin dan hormon sterol (1,25 dihidroksikolekalsiferol/ vitamin D). Kadar kalsium normal 4–5,6 mg/dL (1–1,4 mmol/L). 22
Keseimbangan kalsium merupakan hubungan timbal balik antara absorsi usus, eksresi dalam urine dan faktor hormonal. Absorbsi kalsium terjadi diusus halus terutama di duodenum dan jejunum proksimal. 22
B. Gangguan Keseimbangan Kalsium
1. Hiperkalsemia
a. Definisi
Hiperkalsemia (kadar kalsium darah yang tinggi) adalah suatu keadaan dimana konsentrasi kalsium dalam darah lebih dari 10,5 mgr/dL darah. 14,18
b. Etiologi
Terdapat tiga dasar mekanisme patofisiologi yang berkontribusi terhadap kejadian hiperkalsemia yaitu : peningkatan absorpsi kalsium dari traktus gastrointestinal, penurunan ekskresi kalsium ginjal, dan peningkatan resorpsi kalsium tulang.
Hiperparatiroidisme primer
jarang yaitu hiperplasia keempatkelenjar paratiroid (15%) dan yang sangat jarang adalah karsinoma kelenjar paratiroid (<1%). Patofisiologi yang mendasari yaitu sekresi hormone paratiroid berlebihan yang berperan meningkatkan resorpsi tulang oleh osteoklas, meningkatkan absorpsi kalsium intestinal, dan meningkatkan reabsorpsi kalsium tubular ginjal. Sering pula dijumpai penurunan kadar fosfat serum karena PTH menghambat reabsorpsi fosfat pada tubulus proksimal. Umumnya hiperparatiroidisme primer asimptomatik. Peningkatan produksi hormon paratiroid menimbulkan kelainan tulang yang disebut osteitis fibrosa cystica, ditandai oleh resorpsisubperiosteal falang distal, kista tulang, dan tumor coklat di tulang-tulang panjang. Batu ginjal didapatkan pada 15-20% penderita hiperparatiroidisme, dan sebaliknya sekitar 5% penderita dengan batu ginjal mengalami hiperparatiroidisme. Batu ginjal paling sering terbentuk dari kalsium oksalat, dan merupakan faktor utama patogenesis hiperkalsiuria.15,16 Krisis hiperkalsemia merupakan kasus jarang, ditandai dengan kadar kalsium >15mg/dl dengan gejala hiperkalsemia berat. Mekanisme krisis tersebut belum jelas, tetapi dehidrasi, penyakit penyerta, dan mungkin infark dari suatu adenoma paratiroid pada beberapapenderita berperan. 18
Intoksikasi vitamin A
Imobilisasi
Imobilisasi menyebabkan hiperkalsemia pada penderita yang mengalami peningkatan resorpsi tulang; termasuk anak dan remaja, penderita Paget’s disease tulang, HPT ringan dan sekunder, dan keganasan dengan hiperkalsemia ringan. Pasien-pasien tersebut juga berisiko osteopenia. 18
Gagal ginjal
Hiperkalsemia akibat gagal ginjal akut terjadi terutama pada penderita dengan rhabdomiolisis. Awalnya, hiperfosfatemia menyebabkan deposisi kalsium pada jaringan lunak, mengakibatkan hipokalsemia dan HPT sekunder. Selanjutnya ginjal mulai melindungi dengan reentri/ masuknya kembali garam kalsium ke dalam sirkulasi yang dihubungkan dengan kadar PTH tinggi sehingga menyebabkan transien hiperkalsemia. 18
keganasan
Kanker juga menyebar (bermetastasis) ke tulang, menghancurkan sel-sel tulang dan melepaskan kalsium tulang ke dalam darah. Hal ini sering terjadi pada kanker prostat, payudara dan paru-paru. Mieloma multipel (kanker yang melibatkan sumsum tulang) juga dapat menyebabkan penghancuran tulang dan mengakibatkan hiperkalsemia. Kanker yang lain juga meningkatkan konsentrasi kalsium darah, dengan mekanisme yang belum sepenuhnya dapat dimengerti. 18
Sindrom susu-alkali
karbonat berlebihan dalam preparat antasid dan pemakaiannya untuk pencegahan osteoporosis. 18
c. Gejala Klinis
Bila terjadi hiperkalsemia berat dan menahun, kristal kalsium akan terbentuk di dalam ginjal dan menyebabkan kerusakan yang menetap. 17,18
d. Diagnosis
Diagnosis hiperkalsemia paling sering didapatkan secara kebetulan pada pemeriksaan darah penderita asimptomatik. Kadar kalsium serum normal adalah 8- 10 mg/dL (2 - 2,5 mmol/L) dan kadar ion kalsium normal yaitu 4 - 5,6 mg/ dL (1 - 1,4mmol/L). Meskipun pemeriksaan kadar ion kalsium tidak dilakukan rutin, kadarnya dapat diperkirakan berdasarkan kadar kalsium serum; biasanya akurat kecuali apabila terdapat hipoalbuminemia.5,6 Hiperkalsemia ringan adalah jika kadar kalsium serum total 10,5 - 12 mg/dL (2,63 - 3 mmol/L) atau kadar ion kalsium 5,7–8 mg/dL(1,43–2 mmol/L), umumnya asimptomatik. Pada hiperkalsemia sedang, manifestasi multiorgan dapat terjadi. Kadar kalsium >14 mg/dL (3,5 mmol/L) dapat mengancam jiwa. Beberapa faktor dapat mempengaruhi jumlah kalsium terikat protein. Hipoalbuminemia dapat menurunkan dan sebaliknya hiperalbuminemia dapat meningkatkan jumlah kalsium serum terikat albumin (termasuk kadar kalsium serum total) tanpa mempengaruhi kadar kalsium serum terion. Konsentrasi kalsium biasanya berubah 0,8 mg/dL pada setiap perubahan 1,0 g/dL konsentrasi plasma albumin. Koreksi kadar kalsium serum total terhadap perubahan albumin serum : Total kalsium + 0,8 x (4,5 – kadar albumin). 12,14,18
kalsium serum terion. Setiap peningkatan pH 0,1 unit, kadar kalsium serum terion menurun 0,1 mEq/L (= 0,2 mg/dL), dan sebaliknya. 14,18
e. Penatalaksanaan
Penatalaksanaan tergantung kadar kalsium darah dan ada tidaknya gejala. Jika kadar kalsium <12 mg/dL, tanpa gejala, biasanya tidak perlu tindakan terapeutik. Jika kadar kalsium 12-14 mg/dL disertai gejala hiperkalsemia, diperlukan terapi agresif, tetapi jika tidak disertai gejala, cukup diterapi dengan hidrasi adekuat 3000 – 6000 mL cairan NaCl 0,9% pada 24 jam pertama. Perbaikan volume cairan ekstraseluler ke normal akan meningkatkan ekskresi kalsium urin sebesar 100-300mg/hari. Perbaikan gejala klinis, seperti status mental dan mual muntah tampak < 24 jam pertama. Namun rehidrasi merupakan terapi intervensi sementara dan jarang mencapai kadar normal jika digunakan sendiri. Jika terapi sitoreduktif definitive (operasi, radiasi, atau kemoterapi) terhadap penyakit dasar tidak dilakukan, terapi hipokalsemik seharusnya digunakan dalam jangka lama untuk mencapai kontrol. 18
Setelah hidrasi tercapai, dengan kadar kalsium masih tinggi, dapat diberi
Penatalaksanaan dengan:
Meningkatkan eksresi kalsium melalui ginjal
Dilakukan dengan pemberian larutan NaCl isotonis. Pemberian cairan ini akan meningkatkan volume cairan ekstraseluler yang umumnya rendah akibat pengeluaran urine yang berlebihan disebabkan induksi oleh hiperkalsemia, dan muntah-muntah akibat hiperkalsemia. 18
Menghambat reabsorbsi tulang
- Kalsitonin- menghambat reabsorbsi tulang dengan cara menghambat maturasi osteoklas. Diberikan intramuscular atau subkutan setiap 12 jam dengan dosis 4IU/kgBB.
Bifosfonat- menghambat aktivitas metabolic osteoklas dan juga bersifat sitotoksik terhadap osteoklas.
- Gallium nitrat- menghambat reabsorbsi tulang oleh osteoklas dengan menghambat pompa proton ATPase dependen pada membrane osteoklas.18
Mengurangi absorbs kalsium dari usus
- Glukokortikoid (prednisone, 20-40 mg/hari) mengurangi produksi kalsitriol oleh paru dan kelenjar limfe yang diaktivasi produksinya oleh sel mononuclear. Kalsium serum dapat turun dalam 2-5 hari.
Hemodialisis/dialysis peritoneal
disertai insufisiensi ginjal atau pada gagal jantung dimana pemberian cairan dibatasi. 18
2. Hipokalsemia
a. Definisi
Hipokalsemia (kadar kalsium darah yang rendah) adalah suatu keadaan dimana konsentrasi kalsium di dalam darah kurang dari 8,8 mg/dL darah. 14,18
b. Etiologi
Konsentrasi kalsium darah bisa menurun sebagai akibat dari berbagai masalah. Hipokalsemia paling sering terjadi pada penyakit yang menyebabkan hilangnya kalsium melalui air kemih untuk waktu yang lama atau kegagalan untuk memindahkan kalsium dari tulang. 14,17
c. Gejala Klinis
- kebingungan
- kehilangan ingatan (memori) - delirium (penurunan kesadaran) - depresi
- halusinasi
Gejala-gejala tersebut akan menghilang jika kadar kalsium kembali normal. Kadar kalsium yang sangat rendah (kurang dari 7 mgr/dL) dapat menyebabkan nyeri otot dan kesemutan, yang seringkali dirasakan di bibir, lidah, jari-jari tangan dan kaki. Pada kasus yang berat bisa terjadi kejang otot tenggorokan (menyebabkan sulit bernafas) dan tetani (kejang otot keseluruhan). Bisa terjadi perubahan pada sistem konduksi listrik jantung, yang dapat dilihat pada pemeriksaan EKG. Dapat ditemukan tanda Chovtex atau tanda Trousseau, bradukardi dan interval Q-T yang memanjang. 14,17,18
d. Diagnosa
e. Penatalaksanaan
Pengobatan yang diberikan bila timbul gejala adalah pemberian kalsium intravena sebesar 100-200 mg kalsium-elemental atau 1-2 gram kalsium glukonas dalam 10-20 menit. Lalu diikuti dengan infus klasium glukonas dalam larutan dekstrose atau Nacl isotonis dengan dosis 0,5-1,5mg kalsium elemental/KgBB dalam 1 jam. Kalsium infuse kemudian dapt ditukar dengan kalsium oral dan kalsitriol 0,25-0,5 ig/hari. Pada keadaan hipokalsemia kronik disertai hipoparatirod, diberi kalsium karbonat 250 mg kalsium elemental/650 mg tablet.
18
2.4.4. Magnesium
A. Fisiologi Magnesium
Magnesium merupakan kation intraseluler yang penting, berfungsi sebagai kofaktor berbagai jalur enzim. Hanya 1–2% dari total magnesium tubuh yang disimpan di cairan ekstraseluler, 67% terdapat di tulang, dan sisanya 31% ada di intraseluler.14
Kadar magnesium normal dalam serum adalah 1.7–2.1 mEq/L.4
Sedangkan kebutuhan asupan magnesium ialah 0.2–0.5 mEq/kgBB/hari.14,17
B. Gangguan Keseimbangan Magnesium
1. Hipermagnesium
a. Definisi
terjadi selama terapi magnesium sulfat pada hipertensi gestational yang berpengaruh pada ibu dan janin. Penyebab lainnya berupa insufisiensi adrenal, hipotiroidisme, rhabdomiolisis, dan pemberian lithium. 14,18
b. Manifestasi Klinis Hipermagnesemia
Hipermagnesemia simptomatik biasanya meliputi manifestasi neurologis, neuromuskular, dan jantung. Hiporefleksia, sedasi dan kelemahan otot skeletal merupakan tanda hipermagnesemia. Hal ini terjadi akibat kegagalan pelepasan asetilkolin dan penurunan sensitivitas motor end-plate terhadap asetilkolin di otot. Vasodilatasi, bradikardi, dan depresi miokardium dapat berakhir dengan hipotensi pada level > 10 mmol/dL (>24 mg/dL). Tanda EKG tidak konsisten tetapi termasuk pemanjangan interval P–R dan pelebaran kompleks QRS. Hipermagnesemia dapat menyebabkan henti napas. 14,18
c. Pengobatan Hipermagnesemia
Semua sumber intake magnesium (kebanyakan akibat antasida) sebaiknya dihentikan. Kalsium intravena (1 g kalsium glukonat) dapat secara sementara mengantagonis sebagian besar efek dari hipermagnesemia. Loop diuretic yang disertai dengan ½-normal saline dalam dekstrosa 5% dapat meningkatkan ekskresi magnesium. 14,18
2. Hipomagnesemia4 a. Definisi
intake yang tidak adekuat, penurunan absorpsi gastrointestinal, dan peningkatan ekskresi ginjal. β-adrenergik agonis dapat menyebabkan hipomagnesemia transien di mana ion magnesium diambil oleh jaringan adiposa. Obat-obatan yang dapat menyebabkan pengeluaran magnesium oleh ginjal meliputi etanol, teofilin, diuretik, cisplatin, siklosporin, dan amfoterisin-B. 14,18
b. Manifestasi Klinis Hipomagnesemia
Kebanyakan pasien dengan hipomagnesemia tidak menunjukkan gejala, tetapi anoreksia, kelemahan, fasikulasi, parestesia, konfusi, ataksia, dan kejang dapat menonjol. Hipomagnesemia biasanya berhubungan dengan hipokalsemia (kerusakan sekresi hormon paratiroid) dan hipokalemia (akibat pembuangan oleh ginjal). Manifestasi jantung meliputi iritabilitas listrik dan potensiasi intoksikasi digoxin; kedua faktor ini diperburuk oleh hipokalemia. Hipomagnesemia juga berhubungan dengan peningkatan insiden fibrilasi atrium. Pemanjangan interval P–R dan QT dapat nampak seiring dengan hipokalsemia.14,18
c. Pengobatan Hipomagnesemia
2.4.5 Klorida
1. Fisiologi Klorida
Klorida, anion utama dari cairan ekstraseluler, ditemukan lebih banyak pada kompartemen interstitial dan cairan limfoid daripada dalam darah. Klorida juga merupakan bagian dari cairan sekresi lambung dan pankreas, keringat, kantung empedu, dan air liur. Natrium dan klorida merupakan komposisi elektrolit terbesar dalam cairan ekstraseluler dan berperan dalam menentukan tekanan osmotik. Klorida diproduksi dalam lambung, yang dikombinaksikan dengan hidrogen untuk membentuk adam hidroklorida. Kontrol klorida tergantung dari intake klorida, ekskresi, dan absorpsi ion tersebut dari ginjal. Klorida dalam jumlah kecil dibuang dalam feses.17,23
Kadar klorida dalam serum mencerminkan pengenceran atau pemekatan yang terjadi di cairan ekstrseluler serta menunjukkan secara langsung proporsi konsentrasi natrium. Osmolalitas serum paralel dengan kadar klorida. Sekresi aldosteron meningkatkan reabsorpsi natrium, yang juga meningkatkan reabsorpsi klorida. Pleksus koroid, yang mensekresi cerebrospinal fluid di otak, bergantung pada natrium dan klorida untuk menarik air dan membentuk proporsi dari
cerebrospinal fluid.17,23
Ketika kadar salah satu dari elektrolit ini terganggu (natrium, bikarbonat, dan klorida), kedua elektrolit lainnya pun akan terpengaruh. Klorida berperan dalam menjaga keseimbangan asam basa dan bekerja sebagai buffer dalam pertukaran oksigen dan karbondioksida dalam sel darah merah. Klorida diperoleh dari makanan seperti garam dapur. Kadar normal klorida dalam serum ialah 97– 107 mEq/L.6 Sedangkan kebutuhan asupan klorida ialah 1–2 mEq/kgBB/hari.17
2.Gangguan Keseimbangan Klorida
A. Hiperkloremia a. Etiologi
Kadar klorida serum yang tinggi dapat mengakibatkan hiperkloremia asidosis metabolik oleh karena iatrogenik pemberian klorida seperti larutan NaCl 0.9%, larutan NaCL 0.45%, atau larutan Ringer Laktat. Kondisi ini dapat pula disebabkan oleh kehilangan ion bikarbonat dari ginjal dan saluran pencernaan yang diikuti dengan peningkatan ion klorida. Ion klorida dalam bentuk garam asam terakumulasi, dan asidosis terjadi dengan menurunnya ion bikarbonat. Trauma kepala, peningkatan produksi keringat, kelebihan hormon mineralokortikoid, dan penurunan filtrasi ginjal dapat menuju peningkatan kadar klorida serum. 14
b.Manifestasi Klinik Hiperkloremia
output, disaritmia, dan koma. Kadar klorida yang tinggi diikuti dengan kadar natrium yang tinggi serta retensi cairan. 14
c. Pengobatan Hiperkloremia
Koreksi penyakit yang menyebabkan hiperkloremia serta mengembalikan keseimbangan elektrolit, cairan, dan asam-basa sangatlah penting. Larutan hipotonik intravena dapat diberikan untuk mengembalikan keseimbangan. Larutan Ringer Laktat dapat diberikan supaya laktat diubah menjadi bikarbonat di hati, sehingga dapat meningkatkan kadar bikarbonat dan mengoreksi asidosis. Natrium bikarbonat intravena dapat diberikan untuk meningkatkan kadar bikarbonat yang menuju pada ekskresi ginjal terhadap ion klorida akibat kompetisi bikarbonat dan klorida untuk berikatan dengan natrium. Diuretik dapat diberikan untuk mengeliminasi klorida. Natrium, klorida, dan cairan dibatasi.
2.Hipokloremia6 A. Definisi
Hipokloremia dapat terjadi akibat drainase tube gastrointestinal, suction
meningkatkan pH dan berujung pada hiperkloremia asidosis metabolik. b.Manifestasi Klinik Hipokloremia
Tanda dan gejala dari hipokloremia berhubungan dengan ketidakseimbangan asam-basa dan elektrolit. Tanda dan gejala dari hiponatremia, hipokalemia, dan alkalosis metabolik dapat terjadi. Alkalosis metabolik merupakan gangguan akibat kelebihan intake alkali atau kehilangan ion hidrogen. Hipereksibilitas otot, tetani, kelemasan, dan kram otot juga dapat terjadi. Hipokalemia dapat menyebabkan hipokloremia sehingga terjadi disritmia jantung. Selain itu, oleh karena rendahnya kadar klorida paralel dengan rendahnya kadar natrium, kadar air dapat menjadi berlebihan. Hiponatremia dapat menyebabkan kejang dan koma. 12
c.Pengobatan Hipokloremia
Terapi meliputi koreksi penyebab hipokloremia serta ketidakseimbangan asam-basa dan elektrolit. Larutan normal saline (NaCl 0.9%) atau ½ normal saline (NaCl 0.45%) diberikan intravena untuk menggantikan klorida. Jika pasien menerima diuretik (loop, osmotik, atau thiazid), dapat dihentikan atau diberikan diuretik tipe lain. 12
Amonium klorida, sebuah agen yang bersifat asam, dapat diberikan untuk mengatasi alkalosis metabolik; dosisnya tergantung dari berat pasien dan kadar klorida serum. Agen ini dimetabolisasi oleh hati dan berefek sekitar 3 hari. Amonium klorida ini sebaiknya dihindari pada pasien dengan gangguan fungsi hati dan ginjal.12