commit to user
PERBEDAAN KADAR KUERSETIN PADA PROPOLIS EKSTRAK ETANOL DAN PROPOLIS EKSTRAK AIR
SKRIPSI
Untuk Memenuhi Persyaratan Memperoleh Gelar Sarjana Kedokteran
Nurrini Susanti Y. G.0009160
FAKULTAS KEDOKTERAN UNIVERSITAS SEBELAS MARET
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
ii
PENGESAHAN SKRIPSI
Skripsi dengan judul : Perbedaan Kadar Kuersetin pada Propolis Ekstrak
Etanol dan Propolis Ekstrak Air
Nurrini Susanti Y, NIM: G.0009160, Tahun: 2012
Telah diuji dan sudah disahkan di hadapan Dewan Penguji Skripsi
Fakultas Kedokteran Universitas Sebelas Maret Surakarta
commit to user
iii
Muthmainah, dr., M.Kes Prof. Dr. Zainal Arifin Adnan, dr, Sp.PD-KR-FINASIM
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
iv
PERNYATAAN
Dengan ini menyatakan bahwa dalam skripsi ini tidak terdapat karya yang pernah
diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan
sepanjang pengetahuan penulis juga tidak terdapat karya atau pendapat yang
pernah ditulis atau diterbitkan oleh orang lain kecuali yang secara tertulis diacu
dalam naskah dan disebutkan dalam daftar pustaka.
Surakarta,
Nurrini Susanti Y.
commit to user
v
ABSTRAK
Nurrini Susanti Y, G.0009160,2012. Perbedaan Kadar Kuersetin pada Propolis
Ekstrak Etanol dan Propolis Ekstrak Air. Skripsi. Fakultas Kedokteran, Universitas Sebelas Maret, Surakarta.
Latar Belakang: Propolis mengandung berbagai jenis flavonoid, salah satunya adalah kuersetin. Propolis memiliki banyak manfaat di bidang kesehatan. Jenis pelarut yang digunakan dalam ekstraksi propolis mempengaruhi kadar kuersetin. Penelitian ini bertujuan untuk mengetahui perbedaan kadar kuersetin pada propolis ekstrak etanol dan propolis ekstrak air.
Metode Penelitian: Penelitian ini merupakan penelitian eksperimental murni. Subjek penelitian adalah propolis yang berasal dari peternakan lebah di daerah Gejen RT 3 RW 2, Kerjo, Karanganyar. Pengambilan sampel dilakukan dengan cara purposive sampling. Penentuan kadar kuersetin pada propolis dengan menggunakan UV-Vis spektrofotometer metode Prussian-blue. Pada tiap ekstrak propolis masing-masing dibuat lima sampel. Data kadar kuersetin yang diperoleh dianalisis dengan uji statistik yaitu Uji t tidak berpasanganmenggunakan program komputer SPSS 17 for windows.
Hasil Penelitian: Rata-rata kadar kuersetin yang diperoleh dalam penelitian ini adalah 10,0480±0,53798 µg/mL pada Propolis Ekstrak Etanol dan 1,0440±0,06804 µ g/mL pada Propolis Ekstrak Air dengan nilai p < 0,05.
Simpulan Penelitian: Terdapat perbedaan kadar kuersetin pada propolis ekstrak etanol dan propolis ekstrak air
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
vi
ABSTRACT
Nurrini Susanti yulianti, G.0009160,2012. The Difference of Quercetin Level in Ethanol Extract Propolis and Water Extract Propolis. Mini Thesis, Faculty of Medicine, Sebelas Maret University, Surakarta.
Background: Propolis contains flavonoids. One of them is quersetin. Solvent used is propolis extraction influence quercetin level of the extract. This research aims to determine whether there is a difference of Quercetin Level in Ethanol Extract Propolis and Water Extract Propolis.
Methods: This research is an experimental research. Subject of this research is propolis from Gejen RT 3 RW 2, Kerjo, Karanganyar. The samples were carried out by purposive sampling. Concentration of quercetin is determined by using UV-Vis spectrophotometer by Prussian-blue methode. Five samples are made for each extract. The data then analized using unpaired t-test by SPSS 17 for windows.
Results: Averages of quercetin level in this research are 10,0480±0,53798 µg/mL in Ethanol extract propolis and 1,0440±0,06804 µ g/mL in Water Extract propolis with p < 0,05.
Conclusion: There are differences in there is a difference of quercetin content in Ethanol Extract Propolis and Water Extract Propolis.
commit to user
vii
PRAKATA
Alhamdulillaah, segala puji syukur bagi Allah Subhanahu wa ta’ala yang telah memberikan taufik, hidayah, dan kekuatan serta kesabaran sehingga penulis dapat menyelesaikan penelitian dan penyusunan laporan penelitian dengan judul “Perbedaan Kadar Kuersetin pada Propolis di Pasaran Wilayah Surakarta”.
Skripsi ini disusun sebagai salah satu syarat kelulusan tingkat sarjana di Fakultas Kedokteran Universitas Sebelas Maret Surakarta. Kendala dalam penyusunan skripsi ini dapat teratasi atas pertolongan Allah SWT melalui bimbingan dan dukungan banyak pihak. Untuk itu, perkenankan penulis mengucapkan terima kasih kepada :
1. Prof. Dr. Zainal Arifin Adnan, dr, Sp.PD-KR-FINASIM, selaku Dekan Fakultas Kedokteran Universitas Sebelas Maret Surakarta.
2. Muthmainah, dr., M.Kes, selaku Ketua Tim Skripsi beserta Tim Skripsi Fakultas Kedokteran Universitas Sebelas Maret Surakarta.
3. Diding Heri Prasetyo, dr., M.Si, selaku Pembimbing Utama yang telah banyak meluangkan waktu untuk memberikan bimbingan dan nasihat. 4. Sri Hartati, Dra., Apt., S.U, selaku Pembimbing Pendamping yang telah
banyak meluangkan waktu untuk memberikan bimbingan dan nasihat. 5. R.P. Andri Putranto, dr., M.Si, selaku Penguji Utama yang telah
memberikan bimbingan dan nasihat.
6. Sarsono, Drs., M.Si, selaku Penguji Pendamping yang telah memberikan bimbingan dan nasihat.
7. Bapak, Ibu, adik serta seluruh keluarga yang telah memberi dukungan moral, material, serta senantiasa mendoakan untuk terselesaikannya skripsi ini.
8. Semua pihak yang telah membantu terselesainya skripsi ini, yang tidak dapat penulis sebutkan satu persatu.
Meskipun tulisan ini masih belum sempurna, penulis berharap skripsi ini dapat bermanfaat bagi pembaca. Saran, pendapat, koreksi, dan tanggapan dari semua pihak sangat diharapkan.
Surakarta, Mei 2012
perpustakaan.uns.ac.id digilib.uns.ac.id
B. Kerangka Pemikiran ... 15
C. Hipotesis ... 16
commit to user
ix
A. Jenis Penelitian ... 17
B. Lokasi Penelitian... 17
C. Subjek Penelitian ... 17
D. Teknik Sampling...17
E. Rancangan Penelitian ... 18
F. Identifikasi Variabel Penelitian ... 19
G. Definisi Operasional Variabel Penelitian ... 19
H. Alat dan Bahan... 20
I. Cara Kerja ... 20
J. Teknik Analisis Data ... 22
BAB IV HASIL PENELITIAN ... 23
BAB V PEMBAHASAN ... 29
BAB VI SIMPULAN DAN SARAN ... 32
A. Simpulan... 32
B. Saran ... 32
DAFTAR PUSTAKA... 33
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
x
DAFTAR GAMBAR
Gambar 2.1 Struktur Kimia Kuersetin ... 9
Gambar 2.2 Skema Kerangka Pemikiran ... 15
Gambar 3.1 Skema Rancangan Penelitian ... 17
Gambar 4.1 Kurva Kalibrasi Kuersetin dengan Pelarut Etanol dalam Reagen Prussian-Blue pada Panjang Gelombang 700 nm ... 24
Gambar 4.2 Kurva Kalibrasi Kuersetin dengan Pelarut Air dalam Reagen
commit to user
xi
DAFTAR TABEL
Tabel 2.1 Komposisi Kandungan Senyawa Kimia Rata-rata dari Propolis (Krel, 1996)...6
Tabel 4.1 Pengukuran Absorbansi Larutan Kuersetin yang Dilarutkan dalam Etanol 80% pada Panjang Gelombang 700 nm ... 23
Tabel 4.2 Pengukuran Absorbansi Larutan Kuersetin yang Dilarutkan dalam Air pada Panjang Gelombang 700 nm ... 25
Tabel 4.3 Konsentrasi Kuersetin pada Propolis Ekstrak Etanol ...26
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
xii
DAFTAR LAMPIRAN
Lampiran 1.Uji Normalitas Distribusi
Lampiran 2.Uji Homogenitas dan Independent t Test
commit to user
1
BAB I
PENDAHULUAN
A. Latar Belakang Masalah
Propolis merupakan senyawa lengket seperti lem (resin) yang
dikumpulkan lebah madu dari kuncup daun berbagai tumbuhan yang
kemudian dicampur dengan lem lebah dan β-glucosidase yang
disekresikan oleh kelenjar saliva selama pengumpulan propolis. Propolis
digunakan lebah sebagai lem pada sarangnya untuk menanggulangi
berbagai ganguan dari luar (Park dan Ikegaki, 1998).
Propolis umumnya didapatkan dari lebah madu Apis spp., namun
terdapat spesies lebah madu lain yang mengumpulkan lebih sedikit madu
dan lebih banyak propolis misalnya lebah madu Trigona spp (Fatoni et al.,
2008). Komposisi kandungan propolis bervariasi berdasarkan sumbernya,
secara umum, propolis tersusun atas 50% resin, 30% lem lebah, 10%
minyak esensial, 5% serbuk sari dan 5% bahan lain (Coneac et al., 2008).
Propolis diketahui yang yang memiliki berbagai aktivitas biologis.
Berbagai aktivitas ini disebabkan karena di dalam propolis terkandung
flavonoid, aktivitas-aktivitas tersebut di antaranya adalah aktivitas
antibakterial, antiviral, antifungal, antioksidan dan dapat menangkal
radikal bebas (Bahdauria et al., 2006). Flavonoid propolis juga diketahui
commit to user
2
hepatoprotektor, karsinostatik, dan membantu regenerasi jaringan (Farre et
al., 2004).
Kuersetin merupakan salah satu dari dua senyawa flavonoid
terpenting yang terkandung di dalam propolis (Coneac et al., 2009).
Kuersetin diketahui sebagai suatu senyawa yang tidak stabil terutama pada
media basa. Selain itu, kuersetin juga diketahui memiliki bioavailabilitas
yang rendah di dalam air sehinga meyebabkan absorbsi kuersetin secara
oral terbatas (Zheng et al.,2005).
Pietta dalam Susilo (2009) menyatakan bahwa propolis tidak dapat
digunakan sebagai bahan baku dan harus dipurifikasi terlebih lagi melalui
proses ekstraksi dengan zat pelarut. Hal ini disebabkan karena propolis
mentah yang masih mengandung berbagai bahan-bahan kontaminan
seperti kayu, serbuk sari, bahkan lebah yang sudah mati (Sforcin dan
Bankova, 2011) Metode ekstraksi propolis dapat mempengaruhi aktivitas
biologis flavonoid propolis, khususnya kuersetin (Coneac et al., 2008).
Metode ekstraksi yang umumnya digunakan saat ini adalah ekstrak padat,
yaitu ekstraksi dengan menggunakan etanol dengan konsentrasi yang
berbeda-beda, metanol atau air (Nagai et al., 2002). Cunha dalam Sforcin
(2011) menyatakan bahwa pelarut yang berbeda akan mengekstrak
komponen yang berbeda serta mempengaruhi aktivitasnya. Meskipun
propolis ekstrak etanol saat ini lebih umum digunakan, namun propolis
commit to user
manusia sehingga penelitian mengenai Propolis Ekstrak Air semakin
banyak dilakukan (Nagai et al., 2002).
Penelitian ini diharapkan dapat memberikan informasi ilmiah
mengenai perbedaan kadar kuersetin pada Propolis Ekstrak Etanol dan
Propolis Ekstrak Air.
B. Rumusan Masalah
Berdasarkan uraian dalam latar belakang masalah tersebut di atas,
dapat dirumuskan masalah pada penelitian ini adalah: adakah perbedaan
kadar kuersetin pada Propolis Ekstrak Etanol dan Propolis Ekstrak Air?
C. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui perbedaan kadar
kuersetin pada Propolis Ekstrak Etanol dan Propolis Ekstrak Air.
D. Manfaat Penelitian
1. Aspek Teoritis
Memberikan sumbangan pikiran bagi ilmu pengetahuan
kesehatan terutama di bidang biokimia untuk mengetahui ekstrak yang
memiliki kadar kuersetin lebih tinggi diantara Propolis Ekstrak Etanol
dan Propolis Ekstrak Air.
2. Aspek Aplikatif
a. Memberikan informasi kepada klinisi tentang kadar kuersetin yang
lebih tinggi di antara Propolis Ekstrak Etanol dan Propolis Ekstrak
commit to user
4
b. Memberikan informasi kepada masyarakat tentang kadar kuersetin
commit to user
Propolis merupakan senyawa lengket seperti lem (resin)
yang dikumpulkan lebah madu (Apis mallifera) dari kuncup daun
berbagai tumbuhan yang kemudian dicampur dengan lilin lebah dan
β-glucosidase yang disekresikan oleh kelenjar saliva selama
pengumpulan propolis (Park dan Ikegaki, 1998). Propolis umumnya
didapatkan dari lebah madu Apis spp., namun terdapat spesies lebah
madu lain yang mengumpulkan lebih sedikit madu dan lebih banyak
propolis misalnya lebah madu Trigona spp (Fatoni et al., 2008).
b. Kandungan senyawa kimia
Propolis tersusun atas lebih dari 180 senyawa kimia yang
komposisinya berbeda-beda sesuai dengan zona geografis dan
sumber tanamannya (Osman dan Taha, 2008). Selain kedua hal
tersebut, komposisi propolis juga dipengaruhi oleh musim (Saragih
et al., 2006). Komposisi propolis terutama tergantung pada
tumbuh-tumbuhan dari daerah asal propolis, waktu dikumpulkan dan secara
sekunder tergantung pada pelarut yang digunakan untuk ekstraksi
commit to user
6
merupakan produk yang dihasilkan dari tumbuhan telah dibuktikan
bahwa komposisinya tidak diubah oleh lebah (Bankova, 2005).
Propolis mengandung senyawa kompleks vitamin, mineral, enzim,
senyawa fenolik dan flavonoid (Osman dan Taha, 2008). Dalam
tabel di bawah ini, Krell (1996) menjelaskan komposisi kimia
propolis adalah sebagai berikut:
Tabel 2.1. Komposisi Kandungan Senyawa Kimia Rata-Rata dari
Propolis (Krel, 1996)
c. Manfaat Propolis
Propolis berfungsi sebagai lem pada sarang lebah dalam
mengatasi berbagai ganguan dari luar (Park dan Ikegaki, 1998).
Selain itu, propolis juga berfungsi untuk mengkilatkan bagian dalam
sarang dan menjaga suhu lingkungan bagi lebah. Propolisdigunakan
untuk mengisi retakan dan celah pada sarang lebah, mempersempit
Komposisi (%) Kandungan Senyawa dan
Karakteristik
Resin 45-55 Flavonoid, asam fenolik dan ester
Lilin
7,55-35
Lilin lebah, serat tumbuhan
Oil esensial 5-10 Senyawa volatile
commit to user
atau menutup sarang agar tidak terbuka, melindunginya dari
kontaminasi yang berasal dari luar, untuk memperkuat dan
menyambung sel-sel dalam sarang dan melindunginya dari rembesan
air, serta melindungi larva yang tumbuh tidak terkontaminasi oleh
mikroba (Susilo et al., 2009)
Saat ini, manusia memanfaatkan propolis sebagai bahan
kosmetik, teknologi pengolahan pangan dan obat-obatan. Propolis
diketahui yang memiliki aktivitas antibakterial, antiviral, antifungal,
antioksidan dan dapat radikal bebas (Bahdauria et al., 2006).
Propolis juga diketahui memiliki aktivitas antiinflamasi,
menstimulasi imun, hepatoprotektor, karsinostatik, dan membantu
regenerasi jaringan. Efek lain dari propolis yang telah diketahui
antara lain menurunkan tekanan darah, melindungi jaringan hepar
dari tetraklorida, mencegah terjadinya ulkus lambung dan
mempertahankan kadar glukosa darah, bersifat protektif terhadap
jaringan ginjal (El-Khayat, 2009). Propolis menunjukkan aktivitas
antimikroba, baik secara langsung pada berbagai mikroorganisme
maupun secara tidak langsung dengan memacu sistem imun tubuh.
Propolis memacu sistem imun dengan mengaktivasi makrofag dan
meningkatkan aktivitas micobicidal dari makrofag dan
meningkatkan pembentukan antibodi serta menunjukkan efek
sinergis dengan obat-obatan antimikroba (Sforcin, 2007). Penelitian
commit to user
8
propolis memiliki efek antimalaria dengan tingkat efektifias yang
berbeda-beda tergantung dari letak geografis asal propolis. Miyataka
dalam Sforcin (2007) menyebutkan bahwa Propolis Ekstrak Air dan
Propolis Ekstrak Etanol memberikan efek antialergi yaitu dengan
menghambat pengeluaran histamin dari sel mast tikus.
2. Kuersetin
a. Definisi
Kuersetin merupakan suatu zat aktif yang termasuk dalam
golongan flavonol. Flavonol merupakan salah satu dari enam
subgolongan flavonoid. Kuersetin merupakan flavonoid yang secara
luas tersebar pada tumbuhan (Kelly, 2010). Kuersetin juga
merupakan salah satu dari dua senyawa flavonoid terpenting yang
terkandung di dalam propolis (Coneac et al., 2009). Kuersetin
dibedakan menjadi kuersetin aglikon dan kuersetin glikosid.
Kuersetin aglikon merupakan kuersetin yang tidak berikatan dengan
gula, sementara kuersetin glikosid merupakan kuersetin yang
berikatan dengan gugus glikosil (glukosa, rhamnosa, rutinosa).
Kuersetin aglikon ditemukan lebih sedikit daripada kuersetin
commit to user
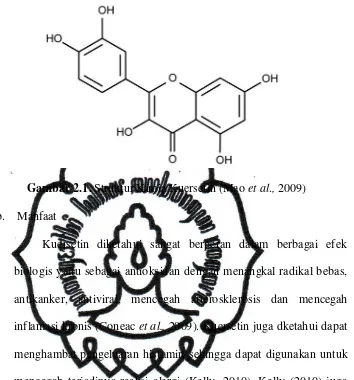
Gambar 2.1. Struktur Kimia Kuersetin (Mao et al., 2009)
b. Manfaat
Kuersetin diketahui sangat berperan dalam berbagai efek
biologis yaitu sebagai antioksidan dengan menangkal radikal bebas,
antikanker, antiviral, mencegah arterosklerosis dan mencegah
inflamasi kronis (Coneac et al., 2009). Kuersetin juga dketahui dapat
menghambat pengeluaran histamin sehingga dapat digunakan untuk
mencegah terjadinya reaksi alergi (Kelly, 2010). Kelly (2010) juga
menyatakan bahwa kuersetin juga memiliki aktivitas menghambat
terjadinya agregasi trombosit dan dan pembentukan trombus
sehingga dapat menurunkan risiko terjadinya penyakit
kardiovaskuler. Gulcin (2010) juga menyatakan bahwa propolis
dapat mencegah terjadinya penyakit jantung koroner. Kuersetin juga
menunjukkan adanya efek antiansietas dan antidepresan pada hewan
walaupun hingga saat ini belum ada penelitian mengenai aktivitas
antiansietas dan antidepresan kuersetin pada manusia. Menurut
commit to user
10
secara signifikan dapat meningkatkan fase non-REM pada tidur dan
mengurangi fase REM yang diduga disebabkan oleh aktivitas
kuersetin yag menginduksi aktivitas reseptor GABA(A) walaupun
sementara ini belum terdapat penelitian mengenai efek kuersetin
terhadap fase tidur pada manusia.
c. Bioavailabilitas
Kuersetin diketahui sebagai suatu senyawa yang tidak stabil
terutama pada media basa (Zheng et al., 2005). Kuersetin aglikon
yang tidak berikatan dengan gugus glikosil seluruhnya tidak dapat
larut dalam air dingin, namun dapat sangat sedikit terlarut dalam air
panas dan sedikit terlarut dalam alkohol dan lemak (lipofilik) (Kelly,
2010). Ikatan kuersetin dengan gugus glikosil pada kuersetin
glikosid diketahui meningkatkan kelarutannya di dalam air. Karena
kuersetin memiliki kelarutan yang rendah di dalam air sehinga
meyebabkan absorbsi kuersetin secara oral terbatas (Zheng et al.,
2005). Terlebih lagi dalam proses pencernaan, enzim-enzim
pencernaan dan bakteri menyebabkan terjadinya hidrolisis kuersetin
sehingga kuersetin glikosil berubah menjadi kuersetin aglikon
sehingga lebih mudah diserap oleh tubuh (Kelly, 2010). Rata-rata
absorbsi oral kuersetin pada hewan maupun manusia rata-rata adalah
commit to user
d. Analisis kadar kuersetin
Analisis flavonoid dapat dilakukan dengan mengunakan
metode UV-Vis spektrofotometer. Metode dengan UV-Vis
spektrofotometer memiliki nilai penyimpangan yang cukup besar
karena faktor yang digunakan untuk menghitung flavonoid total
tidak konstan (Lin-chin et al., 2000). Terdapat beberapa metode
UV-Vis spektrofotometer yang dapat digunakan yaitu metode
Folin-Ciocalteau, metode Prussian-blue dan metode o-Phenanthroline
(Gonzalez et al., 2003). Dalam penelitiannya, Gonzalez (2003)
menemukan bahwa metode Folin-Ciocalteau merupakan metode
yang efektif dan cepat untuk propois dengan konsentrasi komponen
fenolik yang tinggi, Prussian-blue merupakan metode yang cepat
dan sensitif untuk determinasi spektrofotometrik dari fenol total,
sementara prosedur dari metode o-Phenanthroline membutuhkan
waktu yang lebih lama supaya dapat memberikan hasil yang baik.
Dalam penelitiannya, Lin Chin (2000) menggunakan UV-Vis
spektrofotometer dalam mengukur kadar kuersetin pada Propolis
Ekstrak Etanol dan Propolis Ekstrak Air. Berdasarkan penelitian
yang dilakukan oleh Gonzalez (2003) pengukuran dengan metode
Prussian-blue dilakukan dengan cara mengunakan ekstrak air
maupun ekstrak etanol propolis sebanyak 5-400 µm ditambah
dengan raegen Prussian-blue. Larutan yang sudah jadi kemudian
commit to user
12
ml. Setelah tujuh menit, nilai absorbansi diukur menggunakan
UV-Vis spektrofotometer pada panjang gelombang 700 nm, pengukuran
dinyatakan selesai apabila tes strip FeCl3 berubah warna menjadi
biru kehijauan.
3. Ekstrak
a. Ekstrak
Ekstrak merupakan sediaan tumbuh-tumbuhan atau hewan
yang dipekatkan dengan cara melepaskan zat aktif dari
masing-masing bahan, dengan menggunakan pelarut yang sesuai kemudian
sebagian besar atau seluruh pelarut diuapkan dan masa yang tersisa
diatur untuk ditetapkan standarnya. Dengan demikian, ekstrak
merupakan bentuk sediaan yang poten, potensi ekstrak biasanya
dapat mencapai dua sampai enam kali berat bahan mentahnya.
Fungsi ekstrak adalah untuk menyediakan sejumlah kecil dan dalam
kesesuaian bagi bentuk fisik yang mantap serta menunjukkan
aktivitas obat dan sifat dari bahan tersebut (Ansel, 1989).
b. Ekstraksi
Ekstraksi merupakan penarikan zat pokok yang diinginkan
dari suatu bahan mentah dengan menggunakan pelarut. Pelarut
dipilih berdasarkan pada daya larut zat aktif, zat yang tidak
diinginkan, serta tipe preparat farmasi yang dibutuhkan (Ansel,
commit to user
Pelarut serbaguna yang paling luas penggunaannya mungkin
adalah campuran hidroalkohol. Hidroalkohol merupakan gabungan
antara pelarut air dan alkohol yang memungkinkan terbentuknya
kombinasi fleksibel antara air dan alkohol yang paling sesuai untuk
mengektraksi suatu bahan aktif dari obat khusus. Pelarut
hidroalkohol biasanya memberikan perlindungan terpadu terhadap
kontaminasi mikroba dan membantu mencegah pemisahan bahan
yang diekstraksi bila didiamkan (Ansel, 1989).
Metode dasar dari ekstraksi adalah maserasi dan perkolasi.
Metode ekstraksi dipilih berdasarkan sifat bahan metah obat (faktor
utama), daya penyesuaian bahan mentah obat dengan tiap macam
metode ekstraksi, serta kepentingan dalam memperoleh ektrak yang
mendekati sempurna dari obat. Proses perkolasi lebih rumit, mahal,
dan lama dibandingkan dengan proses maserasi. Maserasi
merupakan proses paling tepat, obat yang sudah halus, direndam
dalam pelarut sampai meresap dan melunakkan susunan sel sehingga
zat-zat yang mudah larut akan terlarut. Maserasi dilakukan pada
temperatur 15o-20oC, selama 3 hari sampai bahan-bahan yang dapat
larut kemudian melarut. Pada kenyataannya sering digunakan
kombinasi dari proses maserasi dan perkolasi dalam mengekstraksi
bahan mentah obat. Bahan mentah obat mula-mula dimaserasi untuk
commit to user
14
aktif di dalamnya, kemudian dilakukan proses perkolasi untuk
memisahkan ekstrak dari ampasnya (Ansel, 1989).
c. Propolis Ekstrak Etanol
Ekstraksi dengan pelarut hidroalkohol dengan
mengggunakan jenis etanol yang tidak menyebabkan pembengkakan
membran sehingga dapat memperbaiki stabilitas bahan obat yang
terlarut (Voigt, 1994). Jika bahan pengekstraknya dilarutkan
seluruhnya atau sebagiannya saja, maka dapat diperoleh suatu
ekstrak dengan berbagai konsentrasi sesuai dengan kebutuhan, yang
berdasarkan sifat-sifatnya dibedakan menjadi:
1) Ekstrak encer, yaitu sediaan dengan konsistensi seperti madu
dan dapat dituang. Ekstrak encer sekarang sudah tidak
digunakan lagi.
2) Ekstrak kental, yaitu sediaan dengan konsistensi liat pada
kondisi dingin dan tidak dapat dituang. Kandungan airnya
berjumlah sampai 30%.
3) Ekstrak kering, yaitu sediaan dengan konsistensi kering dan
mudah digosokkan, kandungan airnya tidak lebih dari 5%.
4) Ekstrak cair, yaitu ekstrak yang dibuat sedemikian hingga 1
bagian obat sesuai dengan 2 bagian ekstrak cair. Ekstrak cair
dan ekstrak kering adalah komponen yang paling banyak
commit to user
Ekstrak etanol dibuat dengan cara propolis mentah
dilarutkan dalam etanol dan diaduk setiap 5 menit selama 30 menit
pada suhu 70oC, larutan kemudian dimaserasi/didiamkan selama 24
jam, kemudian disaring menggunakan kertas saring, selanjutnya
larutan yang telah disaring diuapkan dengan menggunakan
waterbath hingga menjadi kental (Saragih, 2006).
d. Ekstrak Air Propolis
Pembuatan ekstrak air propolis dilakukan dengan cara
Gonzalez (2003) dengan modifikasi. Ekstrak air propolis, menurut
Gonzalez, dibuat dengan mengambil 0,1g sampel propolis kering
ditambah dengan 30 ml air. Kemudian dilakukan maserasi selama 12
jam, dilanjutkan dengan memasukkan sampel ke dalam shaker
selama 30 menit pada suhu 30oC dan 50 rpm. Supernatan yang
dihasilkan kemudian difiltrasi 5 jam kemudian. Prosedur yang sama
commit to user
16
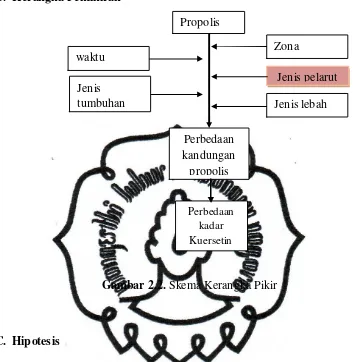
B. Kerangka Pemikiran
Gambar 2.2. Skema Kerangka Pikir
C. Hipotesis
Terdapat perbedaan kadar kuersetin pada Propolis Ekstrak Etanol dan
Propolis Ekstrak Air.
Perbedaan kadar Kuersetin
Propolis
Perbedaan kandungan propolis
Jenis pelarut Zona
geografis
Jenis tumbuhan waktu
commit to user
17
BAB III
METODE PENELITIAN
A. Jenis Penelitian
Penelitian ini merupakan penelitian eksperimental murni.
B. Lokasi Penelitian
Penelitian dilaksanakan di laboratorium biokimia UNS, Surakarta.
C. Subjek Penelitian
Subjek penelitian berupa propolis yang berasal dari peternakan lebah
di daerah Gejen RT 3 RW 2, Kerjo, Karanganyar.
D. Teknik Sampling
commit to user
18
E. Rancangan Penelitian
Rancangan penelitian yang digunakan adalah thepost test only group
design.
Gambar 3.1. Skema Rancangan Penelitian
Keterangan:
A : Propolis Ekstrak Etanol
B : Propolis Ekstrak Air
O1 : Pengukuran kadar kuersetin pada kelompok Propolis Ekstrak
Etanol dengan menggunakan UV-Vis spektrofotometer metode
Prussianiblue.
O2 : Pengukuran kadar kuersetin pada kelompok Propolis Ekstrak
Air dengan menggunakan UV-Vis spektrofotometer metode
commit to user F. Identifikasi Variabel Penelitian
1. variabel bebas : Propolis Ekstrak Etanol
Propolis Ekstrak Air
2. variabel terikat: kadar kuersetin
G. Definisi Operasional Variabel
1. Propolis Ekstrak Etanol
Propolis Ekstrak Etanol adalah ekstrak yang diperoleh dengan
cara mengekstraksi propolis mentah dari peternakan lebah di Daerah
Gejen RT 3 RW 2, Kerjo, Karanganyar dengan menggunakan etanol
sebagai pelarutnya. Skala ukuran variabel ini adalah nominal.
2. Propolis Ekstrak Air
Propolis Ekstrak Air adalah ekstrak yang diperoleh dengan cara
mengekstraksi propolis mentah dari peternakan lebah di Daerah Gejen
RT 3 RW 2,Kerjo, Karanganyar dengan mengunakan air sebagai
pelarutnya. Skala ukuran variabel ini adalah nominal.
3. Kadar Kuersetin
Kadar kuersetin adalah kadar yang ditentukan dengan
menggunakan analisis spektofotometer dimana ekstrak propolis terlebih
dahulu direaksikan dengan reagen Prussian-blue dan diencerkan. Skala
commit to user
20
H. Alat dan Bahan
1. Alat
a) labu takar 10 mL, 100 mL, 250 mL; b) erlenmeyer tutup 100 mL, 250
mL; c) gelas beaker 250 mL; d) pipet tetes; e) pipet mikro 0-10, 10-100,
100-1000 µ L; f) botol timbang; g) satu set spektrofotometer; h) kertas
saring; i) kain lap; j) sabun cuci; k) sikat tabung
2. Bahan
a) kuersetin (1.10-3 s.d 2,98.10-3M); b) asam asetat; c) etanol 80%; d)
aquabidest; e) HCl 0,1 M; f) K3Fe(CN)6 0,0008M/0,1M HCl; g) FeCl3
0,1M/0,1M HCl; h) propolis mentah
I. Cara Kerja
1. Persiapan percobaan
Pembuatan Propolis Ekstrak Etanol dan Propolis Ekstrak Air
dilakukan di Laboratorium Biokimia-UNS Surakarta. Pembuatan ekstrak
propolis dilakukan dengan cara Gonzalez (2003) dengan modifikasi.
Menurut Gonzalez, ekstrak dibuat dengan mengambil 0,1g sampel propolis
kering ditambah dengan 30 ml air. Kemudian dilakukan maserasi selama
12 jam, dilanjutkan dengan memasukkan sampel ke dalam shaker selama
30 menit pada suhu 30oC dan 50 rpm. Supernatan yang dihasilkan
kemudian difiltrasi 5 jam kemudian. Prosedur yang sama kemudian
dilakukan lagi sebanyak 5 kali. Modifikasi yang dilakukan adalah dengan
memperpanjang lama perendaman menjadi 24 jam dan tidak digunakannya
commit to user
2. Pelaksanaan dan Pengukuran Hasil Percobaan
Pengukuran kadar kuersetin Propolis Ekstrak Etanol dan Propolis
Ekstrak Air dilakukan di Laboratorium Biokimia-UNS Surakarta.
Pengkuran kadar kuersetin menggunakan spektrofotometer dengan metode
Prussian-blue dilakukan dengan langkah-langkah sebagai berikut:
1. Standar kuersetin (302,236) ditentukan dengan cara membagi
kuersetin standar menjadi enam kelompok ukuran yaitu 0; 2,5; 5;
7,5; 10; 12,5 µL untuk ekstrak etanol dan 0; 0,31; 0,63; 1,25; 2,5; 5
µL untuk ekstrak air.
2. 400 µL K3Fe (CN)6 0,0008M/0,1M HCl dan 400 µ L FeCl3
0,1M/0,1M HCl ditambahkan pada masing-masing kelompok ukuran
kuersetin standar kemudian diencerkan dengan dengaan
masing-masing pelarut hingga menjadi 10 ml kemudian dikocok.
3. Absorbansi warna diamati pada spektrofotometer dengan panjang
gelombang 700 nm setelah 7 menit.
4. Nilai absorbansi dicatat dan data yang didapat kemudian dibuat
kurva kalibrasi standar dimana sumbu x menunjukkan besarnya
ukuran nilai kuersetin standar dan sumbu y menunjukkan besarnya
nilai absorbansi.
5. Sampel propolis dibagi menjadi dua kelompok yaitu: Propolis
commit to user
22
6. Masing-masing propolis diambil 10 µL kemudian diencerkan
menjadi 10 ml dengan etanol 80% maupun dengan air, kemudian
ditambahkan 400 µ L K3Fe (CN)6 0,0008M/0,1M HCl dan 400 µ L
FeCl3 0,1M/0,1M HCl /10 ml lalu dikocok. Absorbansi diamati pada
spektrofotometer dengan panjang gelombang 700 nm setelah 7
menit. Nilai absorbansi kemudian dicatat dan digunakan untuk
menentukan besar nilai kuersetin yang terdapat dalam sampel
propolis berdasarkan persamaan regresi yang diperoleh dari kurva
standar.
7. Ulangi langkah ke 6 sebanyak lima kali untuk tiap sampel propolis.
8. Nilai rata-rata kadar kuersetin tiap sampel propolis kemudian
dihitung.
9. Kadar kuesetin pada propolis ekstrak etanol dan propolis ekstrak air
kemudian dibandingkan dengan menggunakan uji statistik.
J. Teknik Analisis Data Statistik
Data yang diperoleh dari penelitian dianalisis dengan uji t tidak
berpasangan menggunakan program SPSS 17 for windows untuk
mengetahui adanya perbedaan kadar kuersetin pada Propolis Ekstrak
commit to user
23
BAB IV
HASIL PENELITIAN
Kuersetin standar yang dilarutkan dalam etanol 80% direaksikan
dengan reagen Prussian-blue dan menghasilkan larutan berwarna biru
kehijauan. Warna yang dihasilkan terlalu pekat sehingga perlu dilakukan
pengenceran agar dapat dibaca absorbansinya dengan spektrofotometer
UV-Vis. Berikut ini merupakan hasil pengukuran absorbansi larutan kuersetin
standar yang menggunakan pelarut etanol 80%:
Tabel 4.1. Pengukuran Absorbansi Larutan Kuersetin yang Dilarutkan dalam Etanol 80% pada Panjang Gelombang 700 nm.
Konsentrasi (µ g/mL) Absorbansi
12,5 0,294
Berdasarkan hasil pengukuran di atas, dapat dibuat kurva kalibrasi
antara Absorbansi dengan Konsentrasi. Kurva kalibrasi dibuat untuk
membantu menentukan kadar kuersetin dalam sampel melalui persamaan
regresi dari kurva kalibrasi (Gambar 4.1). Dari gambar tersebut dapat dilihat
bahwa absorbansi berbanding lurus dengan konsentrasi yang mengikuti
commit to user
24
kuersetin standar ke dalam larutan etanol 80% adalah persamaan regresi liner
dengan persamaan regresi Y=0,0238x-0,0084 dan harga koefisien korelasi (r)
adalah 0,993. Nilai (r) yang mendekati 1 tersebut membuktikan bahwa
persamaan regresi tersebut adalah linier. Persamaan tersebut digunakan
sebagai standar pada pengukuran kadar kuersetin pada Propolis Ekstrak
Etanol.
Gambar 4.1. Kurva Kalibrasi Kuersetin dengan Pelarut Etanol dalam Reagen Prussian-blue pada Panjang Gelombang 700 nm
Kuersetin standar yang dilarutkan dalam etanol 80% direaksikan
dengan reagen Prussian-blue dan menghasilkan larutan berwarna biru
kehijauan. Warna yang dihasilkan oleh seluruh sampel terlalu pekat sehingga
perlu dilakukan pengenceran agar dapat nilai absorbansinya dapat dibaca
dengan UV-Vis spektrofotometer. Berikut ini merupakan hasil pengukuran
commit to user
Tabel 4.2. Pengukuran Absorbansi Larutan Kuersetin yang Dilarutkan dalam Air pada Panjang Gelombang 700 nm.
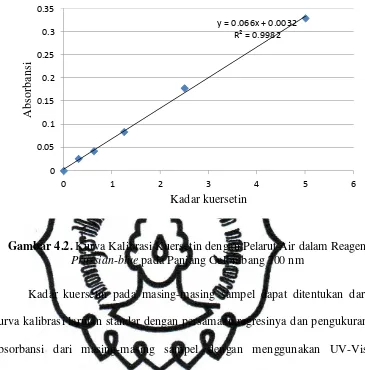
Berdasarkan hasil pengukuran di atas, dapat dibuat kurva kalibrasi
antara absorbansi dengan Konsentrasi. Kurva kalibrasi dibuat untuk
membantu menentukan kadar kursetin dalam sampel melalui persamaan
regresi dari kurva kalibrasi (Gambar 4.2). Dari gambar tersebut dapat
dilihat bahwa absorbansi berbanding lurus dengan konsentrasi yang
mengikuti persamaan linier. Kurva kalibrasi yang diperoleh dengan
melarutkan kuersetin standar ke dalam air adalah persamaan regresi liner
dengan persamaan regresi y = 0,066x + 0,003 dan harga koefisien korelasi
(R2) adalah 0,998. Nilai (R2) yang mendekati 1 tersebut membuktikan
bahwa persamaan regresi tersebut adalah linier. Persamaan tersebut
digunakan untuk melakukan pengukuran kadar kuersetin pada Propolis
Ekstrak Air.
Konsentrasi (µ g/mL) Absorbansi
5 0,329
2,5 0,178
1,25 0,084
0,63 0,042
0,31 0,026
commit to user
26
Gambar 4.2. Kurva Kalibrasi Kuersetin dengan Pelarut Air dalam Reagen
Prussian-blue pada Panjang Gelombang 700 nm
Kadar kuersetin pada masing-masing sampel dapat ditentukan dari
kurva kalibrasi larutan standar dengan persamaan regresinya dan pengukuran
absorbansi dari masing-masing sampel dengan menggunakan UV-Vis
spektrofotometer. Berikut ini merupakan hasil penghitungan kadar kuersetin
pada masing-masing sampel:
Tabel 4.3. Konsentrasi Kuersetin pada Propolis Ekstrak Etanol
Absorbansi Konsentrasi (µ g/mL)
commit to user
Sedangkan konsentrasi kuersetin pada propolis ekstrak air didapatkan hasil
sebagai berikut:
Tabel 4.4. Konsentrasi Kuersetin pada Propolis Ekstrak Air
Absorbansi Konsentrasi (µ g/mL)
0,072 1,03
0,080 1,16
0,068 0,98
0,071 1,02
0,071 1,03
Data-data tersebut dianalisis dengan uji t tidak berpasangan
menggunakan program SPSS 17.0 for windows untuk mengetahui apakah
perbedaan kadar kuersetin pada Propolis Ekstrak Etanol dan Propolis Ekstrak
Air bermakna atau tidak.
Syarat-syarat uji t tidak berpasangan harus dipenuhi terlebih dahulu
sebelum menggunakan uji t tidak berpasangan. Syarat yang pertama adalah
data harus terdistribusi normal. Uji normalitas yang digunakan pada
penelitian ini adalah uji Saphiro-wilk karena jumlah sampel kurang dari 50.
Hasil uji normalitas Saphiro-wilk didapatkan konsentrasi kuersetin pada
Propolis Ekstrak Etanol mempunyai nilai p=0.499 dan pada Propolis Ekstrak
Air p=0,88. Dari hasil tersebut, karena masing-masing nilai p>0.05, maka
dapat disimpulkan bahwa data terdistribusi normal. Syarat kedua adalah
commit to user
28
varian data boleh sama dan boleh tidak sama. Kedua syarat uji t tidak
berpasangan telah terpenuhi sehingga uji t tidak berpasangan dapat dilakukan.
Angka signifikansi yang diperoleh dari analisis dengan uji t tidak
berpasangan adalah <0,05 dengan perbedaan rerata sebesar 9,004. Nilai IK
95% adalah antara 8,339 sampai 9,669. Karena nilai p<5%, maka hasil
penelitian ini menunjukkan adanya perbedaan yang signifikan antara Propolis
commit to user
29
BAB V
PEMBAHASAN
Prosedur ekstraksi perlu dilakukan pada propolis mentah yang
masih mengandung resin tanaman, lem lebah, dan marterial yang tidak
larut untuk mendapatkan komponen bioaktif di dalamnya (Alexandra et
al., 2011). Kualitas ekstrak dipengaruhi oleh berbagai hal di antaranya
bahan yang diekstrak, pelarut yang digunakan dan prosedur ekstraksi.
Kuantitas ekstraksi dipengaruhi oleh tipe ektraksi, waktu ektraksi,
temperatur, pelarut alami, konsentrasi pelarut, serta polaritas. Selama
proses ekstraksi, pelarut akan berdifusi ke dalam material padat dan
melarutkan komponen yang sama polaritasnya (Parshant et al.,2011).
Metode ekstraksi yang umumnya digunakan saat ini adalah ekstrak
padat, yaitu ekstraksi dengan menggunakan etanol dengan konsentrasi
yang berbeda-beda, metanol atau air (Nagai et al., 2002). Dalam penelitian
ini, faktor yang diteliti adalah jenis pelarut yaitu air dan etanol 80%. Air
merupakan pelarut universal yang biasa digunakan untuk mengekstraksi
zat-zat dengan aktivitas antimikroba (Parshant et al., 2011). Sementara
etanol termasuk golongan alkohol yang memiliki sifat melarutkan lebih
banyak polifenol jika dibandingkan dengan akstrak air. Hal ini disebabkan
karena alkohol lebih efektif dalam mendegradasi dinding sel yang
memiliki sifat nonpolar sehingga polifenol dapat lebih banyak terekstraksi.
commit to user
30
menyebabkan polifenol terdegradasi, sementara enzim tersebut tidak aktif
dalam metanol maupun etanol. Ditambah lagi, pelarut air lebih
memungkinkan adanya kontaminasi mikroorganisme dibandingkan
alkohol (Parshant et al., 2011).
Kadar kuersetin rata-rata yang diperoleh dalam penelitian ini
adalah 10,0480±0,53798 µg/mL pada Propolis Ekstrak Etanol dan
1,0440±0,06804 µ g/mL pada Proplis Ekstrak Air. Berdasarkan hasil uji
statistik yang telah dilakukan, diperoleh hasil bahwa Propolis Ekstrak
Etanol dan Propolis Ekstrak Air memiliki perbedaan yang bermakna. Hal
ini dapat dilihat dari nilai p yang kurang dari 5% yaitu 0,013. Hasil
tersebut telah sesuai dengan teori-teori yang ada, seperti yang telah
diyatakan oleh Kelly (2010) bahwa kuersetin tidak dapat larut dalam air
dingin, sangat sedikit larut dalam air panas dan sedikit larut dalam alkohol
dan lemak. Demikian pula penyataan Zheng (2005) yang menyatakan
bahwa absorbsi oral kuersetin yang rendah disebabkan karena kelarutan
kuersetin yang rendah di dalam air. Hasil penelitian ini juga sesuai dengan
penelitian yang dilakukan oleh Park dan Ikegaki (1998) yang meneliti
kadar berbagai flavonoid termasuk kuersetin dalam propolis ekstrak air
dan Propolis Ekstrak Etanol dengan berbagai konsentrasi, hasil dari
penelitian tersebut menunjukkan bahwa ekstrak air merupakan ekstrak
dengan kadar kuersetin terendah, sementara untuk etanol kadar kuersetin
konsentrasi tertinggi terdapat pada konsentrasi 60%. Pada penelitian Park
commit to user
didapatkan pada Propolis Ekstrak Etanol dengan etanol 80% sebagai
pelarutnya. Hasil penelitian ini juga sesuai dengan penelitian yang
dilakukan oleh Bimakr (2010) dalam Parshant et al (2011) yang
menyebutkan bahwa ekstrak etanol yang dapat meghasilkan kadar
flavonoid tertinggi adalah etanol 70% dimana polaritasnya lebih tinggi
dibandingkan dengan etanol murni. Berdasarkan penelitian yang telah
dilakukan, dapat disimpulkan bahwa terdapat perbedaan kadar kuersetin
pada Propolis Ekstrak Etanol dan Propolis Ekstrak Air.
Penelitian ini masih memiliki beberapa kelemahan, di antaranya
adalah penggunaan metode ekstraksi maserasi sederhana yang berakibat
sedikitnya bahan aktif yang terekstrak dari propolis, serta tidak
digunakannya metode isolasi spesifik untuk mengisolasi kuersetin.
Hasil penelitian ini diharapkan dapat menjadi sumbangan ilmu
pengetahuan secara umum bagi masyarakat, serta dapat dimanfaatkan oleh
commit to user
32
BAB VI
SIMPULAN DAN SARAN
A. Simpulan
Terdapat perbedaan kadar kuersetin pada Propolis Ekstrak
Etanol dan Propolis Ekstrak Air.
B. Saran
1. Sebaiknya dilakukan penelitian dengan menggunakan metode
ekstraksi yang lebih baik sehingga zat aktif yang terlarut lebih
banyak.
2. Sebaiknya dilakukan penelitian dengan isolasi kuersetin terlebih
dahulu menggunakan metode isolasi yang spesifik untuk kuersetin