Tugas Akhir 6
BAB II
DASAR TEORI
2.1 SEJARAH HIDROGEN
2.1.1 “Watercar” oleh Issac de Rivas.
Pada tahun 1805 Isaac de Rivas berkebangsaan Swiss sebagai orang pertama
yang menggunakan Hidrogen yang dihasilkan dari elektrilisa sebagai bahan bakar
mesin dengan pembakaran internal, namun rancangannya belum memuaskan dan penemuan ini dikenal dengan “watercar”. Kemudian penelitian ini dikembangkan dan dilanjutkan oleh Luther Wattles dan Rudolf A Erren.
2.1.2 BBA oleh Nicola Tesla dan Stanley Meyer.
Pada tahun 1943 kedua orang tersebut telah mengembangkan penggunaan
bahan bakar air namun karena alasan bisnis hasil temuannya dihilangkan, bahkan
bukan hanya temuannya tetapi juga hasil penelitiannya, kemudian Nicola Tesla
dipenjara dan dihukum mati tahun 1943 dan Stanley Meyer dari Amerika Serikat
Tugas Akhir 7 2.1.3 “Brown Gas”
Yull Brown yang berasal dari Sydney Australia pada tahun 1974 berhasil
mengembangkan BBA untuk menggerakkan mesin, bahan bakar air ini sebenarnya
merupakan campuran gas hidrogen-hidrogen-oksigen yang dihasilkan dari
elektrolisa air. Dalam tabung elektrolisa dipasang kumparan magnetik untuk
memecahkan campuran air destilasi dan soda kue hingga menjadi campuran gas
hidrogen-hidrogen-oksigen (HHO). Hidrogen bersifat eksplosif dan oksigen
mendukung pembakaran, gas ini ditampung dalam tabung elektrolisa yang dialirkan
kedalam ruang pembakaran mesin dan akan bercampur dengan gas hidrokarbon dari
bahan bakar minyak, sehingga terjadi penghematan dalam tingkat yang signifikan.
2.2 Prinsip elektrolisa air
Air adalah substansi kimia yang memiliki rumus H2O. Satu molekul air
tersusun atas dua atom hidrogen yang terikat secara kovalen pada satu atom
oksigen. Dalam bentuk ion, air dapat dideskripsikan sebagai sebuah ion hidrogen
(H+) yang berasosiasi (berikatan) dengan sebuah ion hidroksida (OH-).Prinsip untuk
mengembangkan air sebagai energi adalah dengan mengubahnya menjadi
senyawa-senyawa penyusunnya yaitu hidrogen (H) dan oksigen (O). Elektrolisis air menjadi
prinsip dasar untuk mengubah air menjadi senyawa-senyawa penyusunnya. Gas
H2 hasil elektrolisis tersebut digunakan sebagai energi bahan bakar yang memiliki
Tugas Akhir 8
Elektrolisa air merupakan kunci utama dalam mengubah air menjadi energi.
Dalam proses elektrolisis digunakan sumber energi yang berfungsi untuk memecah
molekul H2O menjadi unsur-unsur asalnya. Pada katoda, dua molekul air bereaksi
dengan menangkap dua elektron, dan akan tereduksi menjadi gas H2 dan OH-. Sedangkan pada anoda, dua molekul air terurai menjadi gas O2 dan melepaskan
4H+ serta mengalirkan elektron ke katoda. Ilustrasi tentang reaksi elektrolisis H2O
dapat dilihat pada gambar dibawah. Pada proses elektrolisis ini, akan timbul
gelembung berupa gas H2 yang dapat dikumpulkan menjadi energi.
Dari prinsip elektrolisis tersebut berkembang teknologi-teknologi pengubah
air menjadi energi, seperti fuel cell dan HOD system, elektrolisa air merupakan
kunci utama dalam mengubah air menjadi energi. Dalam proses elektrolisis
digunakan sumber energi yang berfungsi untuk memecah molekul H2O menjadi
unsur-unsur asalnya.
Pada katoda, dua molekul air bereaksi dengan menangkap dua elektron, dan
akan tereduksi menjadi gas H2 dan OH-. Sedangkan pada anoda, dua molekul air
terurai menjadi gas O2 dan melepaskan 4H+ serta mengalirkan elektron ke katoda.
Ilustrasi tentang reaksi elektrolisis H2O dapat dilihat pada gambar dibawah. Pada
proses elektrolisis ini, akan timbul gelembung berupa gas H2 yang dapat
Tugas Akhir 9
Gambar: proses elektrolisis air
Sumber: modul HHO GENERATOR Ir. Eddy ariffin
Teknologi pemanfaatan air sebagai energi telah banyak dikembangkan, dari
beberapa teknologi yang ada, semuanya menggunakan proses elektrolisis air
sebagai prinsip dasarnya.
Hingga saat ini sudah ditemukan teknologi untuk memanfaatkan air sebagai
energi yaitu fuel cell sistem HOD (Hydrogen Oxygen Demand) yaitu sistem
pembangkit tenaga listrik dari hasil pencampuran H2 dengan O2 lansung pada saat
listrik dibutuhkan, dan elektrolisa HHO (Hydrogen-Oxygen).
Teknologi elektrolisa HHO lebih murah dan lebih efisien. Teknologi optimalisasi
air dengan fuel cell memiliki kelemahan terhadap biaya yang diperlukan dan
Tugas Akhir 10
kelemahan terhadap tingginya biaya yang diperlukan dan masih sulit untuk
menampung gas hidrogen dalam satu tempat. Perbandingan yang lebih lengkap
tentang teknologi optimalisasi air sebagai alternative.
Sudah lebih dari 80 tahun proses elektrolisa ini dipergunakan secara komersial, seperti halnya penyepuhan emas, perak dan lain sebagainya. Prinsip Elektrolisa pada air biasa adalah untuk memecahkan ikatan kimia air (H2O) menjadi
H2 dan O2, diperlukan tegangan listrik searah (DC), yg dialirkan melalui lempengan
plat stainless.
Gambar: Proses elektrolisa air
Pada lempengan plat Kathoda bermuatan (-) akan terjadi / terkumpul gas H2 dan pada bagian plat Anoda bermuatan (+) akan terkumpul gas O2, kedua bentuk gas
tersebut akan keluar bersama-sama sehingga gas tersebut disebut gas HHO. Dalam
proses elektrolisa ini diperlukan elektrolit seperti KOH, NaOH atau Backing soda
Tugas Akhir 11
Apabila gas H2 tersebut dipergunakan untuk pembakaran maka gas O2 yang
masih bercampur tersebut tidak menjadikan halangan pembakaran karena setiap
pembakaran memerlukan O2, bahkan HHO mempunyai kelebihan, tanpa O2 dari
luar dapat dinyalakan atau dibakar.
Hydrogen dengan lambang kimia H merupakan unsur paling sederhana
dilihat dari segi susunan proton dan elektronnya. Satu atom hidrogen hanya
memiliki satu proton dan satu elektron. Gas hidrogen merupakan molekul diatomik,
setiap molekulnya tersusun atas 2 atom hidrogen, yang secara kimia dirumuskan
dengan H2. "Hidrogen merupakan gas paling banyak terdapat di alam semesta dan
keberadaannya di matahari diperkirakan mencapai 75% dari total massa matahari,
2.3 Elektrolisa ada 2 macam:
-Elektrolisa basah (wet cell electrolyse) : yaitu lempengan plat kathoda
danAnoda dicelupkan kedalam air.
-Elektrolisa kering (Dry cell electrolyse = Drycell) : disini lempengan plat
Kathoda dan Anoda berada disebelah luar dan airnya disebelah dalam
2.3.1 Elektrolisa basah (wetcell electrolyse)
Elektrolisa Basah adalah dengan memasukan kedua plat kondensator tersebut kedalam air destilasi atau air - RO (Reverse Osmosis = air murni), apabila
Tugas Akhir 12
Gambar: generator hydrogen sistem cell
terjadi proses pemisahan H2 dan O2, kemudian hasil H2 tersebut perlu dihitung dan
didata dari hasil percobaan,selain itu perlu diteliti variable variabel yang
mempengaruhi produksi H2 tersebut, sehingga dapat diambil kesimpulan penggunaan elektrolisa yang paling efisien & efektif.
2.3.2 Elektrolisa kering (Drycell electrolyse = Drycell)
Elektrolisa Kering (Dry electrolyze) adalah pada proses ini plat kondensotornya tidak direndam kedalam larutan akan tetapi plat nya berada
disebelah luar dan larutannya didalam plat tersebut.
Tugas Akhir 13
Pada proses Dry cell panas yang ditimbulkan oleh plat kondensator dapat dibuang
langsung keluar, sehingga tidak membuat larutan menjadi lebih panas,
dibandingkan dengan elektrolisa biasa atau elektrolisa basah (Wet Electrolyze).
- Rumus Kimia pada proses Elektrolisa:
GAMBAR 2.5: kimia Proses Elektrolisa Sumber: modul Hydroxy Generator
for Motorcycle
Pada elektroda Kathoda terjadi penambahan elektron (e−), sehingga reaksi kimia yang terjadi sbb;
Kathode (reduksi): 2H+(cair) + 2e− → H2(gas)
Sedangkan pada elektroda Anoda, terjadi proses oxidasi dimana pelepasan elektron yang bergerak kearah elektroda kathoda, reaksi kimia pada Anoda sbb;
Tugas Akhir 14
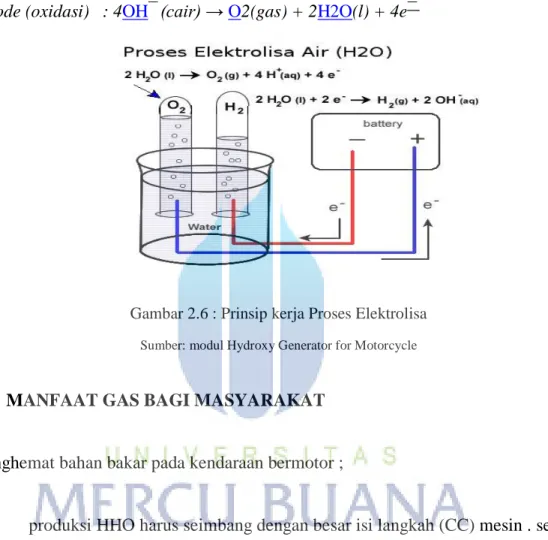
- Reaksi kimia penye-imbangan, reaksi air dengan larutan basa sbb;
Kathode (reduksi): 2H2O(l) + 2e− → H2(gas) + 2OH−(cair) Anode (oxidasi) : 4OH−(cair) → O2(gas) + 2H2O(l) + 4e−
Gambar 2.6 : Prinsip kerja Proses Elektrolisa
Sumber: modul Hydroxy Generator for Motorcycle
2.4 MANFAAT GAS BAGI MASYARAKAT
Penghemat bahan bakar pada kendaraan bermotor ;
produksi HHO harus seimbang dengan besar isi langkah (CC) mesin . sejauh
yang dipraktekan di rumah saya, satu unit EPB cukup untuk menyuplai HHO
keruang bakar mesin ber-CC 2000. Suplai HHO stabil dari putaran rendah hingga
tinggi maupun jarak tempuhnya Respon EPB tidak menbutuhkan waktu lama,
begitu mesin start maka EPB langsung bekerja mensuplai HHO keruang bakar
Tugas Akhir 15
- Instalasi EFB kendaraan roda dua
Gas HHO ini bila dimasukan dalam ruang bakar dan terbakar akan ebih
dapat sebuah pembakaran yang lain baik dan nyaris sempurna sehingga ruang bakar
manjadi lebih bersih dari beberapa dan percobaan yang dilakukan dapat sebuah
sebuah kesimpulan positif bahwa gas hidrogen yang didapat dari hidrogen maker ini
sebagai berikut :
1. Proses pembakaran yang nyaris sempurna diharapkan akan dapat
menghilangkan emisi gas buang berbahaya bagi manusia danalam ,
dengan demikian juga akan dapat mengurangi efek pemanasan global
akibay dari sisa pembakan yang tidak sempurna.
2. Meningkatkan performa dan kekuatan dari pada mesin itu sendiri dan
menurukan suhu mesin, suara dari mesin menjadi lebih halus tidak berisik.
mesin menjadi lebih awet, menghemat bahan bakar (konsumsi yang diuji
70% gas hidrogen dan 30% bensin ) jadi terjadi pengiritan bensin
setidak-tidaknya hinggga 40%.
Sebagai pengguna refrensi orang yang mengaplikasikan hydrogen maker pada
sepeda motornya yang sebelumnya hanya dapat dipacu deangan kecepatan
80km/jam (maksimal) dengan kondisi mesin sangat bergetar setelah memakai
hidrogen maker maupun dipacu dengan kecepatan 100km/jam, mesin masih dalam
Tugas Akhir 16 2.5 Penggunaan gas HHO untuk Industri dan Masyarakat Umum
Api adalah kebutuhan kedua manusia sesudah Air, itu betapa pentingnya api
bagi kelanjutan hidup manusia, yang mana energi dalam bentuk api, dari hari ke
hari makin bertambah mahal, sehingga perlu adanya cara alternatif untuk
mendapatkan energi api yang lebih murah, gas HHO dalam hal ini dapat digunakan,
setelah melalui penelitian yang lebih intensif dan pengamanan yang lebih baik dan
pasti aman, maka api dari gas HHO dapat digunakan seperti lazimnya api dari
bahan bakar lainnya.
Memperhatikan kondisi dan situasi terhadap kebutuhan masyarakat terhadap gas
maka gas hydrogen yang telah diperoleh dari proses elektrolisa, selain dapat
digunakan sebagai penghemat kendaraan berbahan bakar minyak, dapat
menghasilkan nyala api yang dapat digunakan sebagai kompor rumah tangga,
burner di industry atau metode pengelasan dan lain-lain. Hydrogen yang digunakan
untuk keperluan diatas, diperoleh melalui proses elektrolisa. Pada proses elektrolisa
air dengan menggunakan HHO Generator maka terjadilah gas HHO (yaitu gas H2
dan gas O2) yang bersamaan keluar dari HHO Generator tersebut. Gas HHO
merupakan bahan bakar alternatif termasuk energy baru masa depan maka sudah
barang tentu dapat dibakar seperti layaknya bahan bakar gas lainnya.
Dari hasil penelitian memang tidak mudah untuk membuat api dari gas
HHO, hal ini disebabkan sifat gas H2 yang sangat mudah terbakar dan kecepatan
Tugas Akhir 17
banyak peneliti menggatakan gas HHO ini sebagai gas yang liar dan tidak mudah
untuk dikendalikan. Hal yang perlu sekali diperhatikan dan harus disiapkan sebelum
mencoba untuk menyalakan api, yaitu keamanan agar api yang dinyalakan tidak akan
menyerang sumber bahan bakarnya. Oleh sebab itu alat pengamanan tersebut adalah
bagian dari peralatan menyalakan Api yang tak terpisahkan, alat pengaman tersebut dinamakan “ANDUK” (Anti Meleduk) perhatikan gambar 3
Slang Gas-HHO Slang Oksigen
“ANDUK” “BRANDER”
(Anti Meleduk)
Gambar: Peralatan Pengaman anti meleduk (ANDUK) Sumber: modul Hydroxy Generator for Motorcycle
Tugas Akhir 18
Prinsip menyalakan api adalah gas HHO yang berasal dari HHO Generator
disalurkan melalui slang ke kepala brander, untuk mejaga terjadi sesuatu maka pada
slang kedua pada kepala brander disambungkan udara yang berasal dari kompressor
atau erator yang berguna untuk memadamkn api dan mengatur panasnya api sesuai
dengan kebutuhan api tersebut dengan jumlah gas HHO minimal 1(satu) liter/menit.
Sebelum menyalakan api perlu dicek seluruh saluran gas HHO, pengaman pada slang gas HHO yaitu “Anduk”, dryier (filter pengering) dan slang udara tambahan.Type Anduk yang dimaksud adalah dibagian dalam Anduk diisikan bahan
yang tahan api dan tidak bisa dilewati oleh Api.
Pada saat Api akan dinyalakan udara tambahan ditest terlebih dahulu apakah
berfungsi, jika iya maka tombol udara kemudian ditutup dan tombol slang gas HHO
dibuka, barulah api dapat dinyalakan, setelah api menyala maka api dapat dibesar
kecilkan melalui tombol gas HHO, untuk mengatur panas api diatur melalui tombol
udara, yaitu dengan menambah udara api dapat diatur panas apinya. Untuk
mematikan api tombol udara dibuka dan tombol gas HHO di tutup dan HHO
Generator dimatikan.
2.6 Katalis
Katalis merupakan suatu zat yang dapat mempercepat suatu laju reaksi,
namun zat ini sendiri secara kimiawi tidak berubah pada akhir reaksi . Katalis
Tugas Akhir 19
Selain itu, katalis juga bersifat elektrolit yaitu zat yang dapat menghantarkan listrik.
Kemampuan larutan (dalam hal ini air + katalis) menghantarkan listrik disebut juga
daya hantar listrik atau konduktivitas. Konsentrasi elektrolit ini sangat menentukan
besarnya konduktivitas. Dilihat dari kemampuan dalam menghantarkan arus listrik
larutan, maka elektrolit dibagi menjadi dua, yaitu
-Elektrolit kuat
Larutan elektrolit kuat adalah larutan yang dapat menghantarkan arus listrik.
Ion – ion yang bebas bergerak sehingga elektron dapat dengan mudah berpindah
dan mengakibatkan arus listrik yang dihantarkan lebih lancar. Senyawa yang
termasuk elektrolit kuat adalah asam kuat ( dan lain – lain), basa kuat ( dan lain –
lain), dan garam yang mempunyai kelarutan tinggi ( dan lain – lain).
-Elektrolit lemah
Larutan elektrolit lemah yaitu larutan yang dapat menghantarkan listrik tetapi
ion-ionnya tidak sepenuhnya bebas bergerak sehingga elektron tidak dapat dengan
mudah berpindah dan mengakibatkan arus listrik yang dihantarkan lebih kecil.
Senyawa yang termasuk dalam elektrolit lemah adalah asam lemah ( dan lain –
Tugas Akhir 20 2.7 Elektroda
Elektroda adalah konduktor yang digunakan untuk bersentuhan dengan
bagian atau media non-logam. Elektroda dalam sel elektrolisa disebut sebagai anoda
dan katoda. Anoda didefinisikan sebagai elektroda positif dimana elektron diambil
atau diserap dari cell sehingga terjadi oksidasi. Sedangkan katoda didefinisikan
sebagai elektroda negatif dimana elektron dari sumber tegangan memasuki cell dan
reduksi terjadi.
Reduksi adalah proses terpisahnya suatu ikatan senyawa menjadi atom – atom
karena perbedaan potensial elektrode antara suatu larutan dengan kation ketika
adanya aliran listrik. Jika kation berasal dari logam dengan potensial elektrode (E)
lebih kecil daripada air, maka air yang akan tereduksi menjadi gas hidrogen dan
oksigen. Jika kation berasala dari logam dengan E lebih besar daripada air, maka
logam tersebut yang akan tereduksi. Selain itu, elektroda harus memiliki ketahanan
terhadap karat. Maka daripada itu, elektroda yang digunakan adalah konduktor
dengan potensial elektrode lebih kecil daripada air (E ).
2.8 Bahan Baku
Bahan baku elektrolisis haruslah air murni atau air yang tidak mengandung
unsur lain didalamnya seperti mineral, garam, dan sebagainya. Jika air tersebut
mengandung unsur lain, maka hasil elektrolisis tidak hanya gas hidrogen dan
Tugas Akhir 21
terjadi gumpalan berupa agar-agar, yang dapat menyumbat lubang-lubang
pertukaran air). Misal air tersebut mengandung garam NaCl, maka akan timbul
padatan di elektrodanya dan akan terdapat gas klorida juga, sehingga akan
menghambat aliran listrik ke elektroda dan terdapatnya gas yang tidak diharapkan
pada hasil elektrolisis.
Air destilasi yang sudah banyak diperdagangkan adalah;
1. Air untuk penambahan Air Accu (Baterai), tutup botolnya dengan warna biru, jangan yang warna merah.
2. R.O = Reversed Osmosis (Jakarta),
3. TDS Nol = Total Dissolved Solid Nol (Bogor) dan
4. Amidis = Air Minum Distilasi (Bandung).
5. Jika mau murah dan sangat baik dibandingkan air biasa, maka dapat menggunakan air isi ulang.
2.9 Current Leak (Arus Bocor)
Current leak (arus bocor) adalah peningkatan arus pada titik tertentu di
suatu konduktor. Dalam elektrolisis, current leak dapat terjadi pada elektroda yang
memiliki lubang seperti pada metode elektrolisis dry cell. Hal ini dikarenakan
lubang tersebut menyebabkan bagian dalam elektroda terbuka dan bagian dalam
elektroda tidak memiliki lapisan anti karat (stainless) seperti Chromium (Cr) dan
Nickel (Ni) karena pada umumnya pembuatan stainless steel menggunakan metode
Tugas Akhir 22
manganese (Mn). Mn termasuk logam berat, rapuh, dan mudah teroksidasi. Lubang
ini menyebabkan terjadinya reaksi oksidasi antara oksigen yang dihasilkan dengan
Mn.
Reaksi oksidasi adalah reaksi pelepasan elektron oleh molekul, atau ion.
Senyawa yang memiliki kemampuan untuk mengoksidasi senyawa lain disebut
oksidator dan oksidator adalah senyawa yang memiliki unsur – unsur dengan
bilangan oksidasi tinggi seperti atau senyawa yang sangat elektronegatif
(konduktivitas rendah) sehingga mendapatkan elektron dengan mengoksidasi
sebuah senyawa lain, misalnya oksigen, fluorin, dan lain – lain.
Dalam kasus ini, oksidatornya adalah oksigen dan yang dioksidasi adalah
Manganese (Mn) sehingga Mn melepaskan elektronnya. Akibatnya arus listrik yang
mengalir pada larutan meningkat dan seperti yang diketahui bahwa arus meningkat
akan mengakibatkan suhu meningkat, maka suhu air akan meningkat dengan cepat
dan akan menyebabkan air berubah menjadi uap air sehingga gas hidrogen dan
oksigen tidak dapat dihasilkan secara optimal. Selain itu lubang-lubang tersebut
lama kelamaan akan teroksidasi sehingga lubang menjadi lebih besar. Bahaya lain
dari uap air yang terjadi karena panas arus bocor terhadap ruang bakar adalah efek