ix INTISARI
Pedagang Besar Farmasi (PBF) adalah perusahaan berbentuk badan hukum yang memiliki izin untuk pengadaan, penyimpanan, penyaluran obat dan/atau bahan obat dalam jumlah besar sesuai ketentuan peraturan perundang-undangan. Terdapat 11 PBF yang berada di Provinsi Bangka Belitung. Penelitian ini bertujuan untuk memperoleh gambaran bagaimana pelaksanaan CDOB meliputi aspek: manajemen mutu, personalia, peralatan dan bangunan, dokumentasi dan inspeksi diri sudah sesuai dengan SK.Kepala Badan POM nomor: HK.00.05.3.2522 pada Pedagang Besar Farmasi di Provinsi Bangka-Belitung.
Penelitian ini termasuk jenis penelitian non eksperimental dengan rancangan penelitian bersifat deskriptif. Menggunakan instrument kuesioner yang dikonversikan dalam bentuk persentase (%) data kuantitatif. Hasil data kuantitatif tersebut diperkuat dengan data wawancara mendalam terhadap lima aspek CDOB kepada 11 penanggung-jawab PBF yang bersedia menjadi responden.
Hasil penelitian menunjukkan bahwa produk yang disalurkan oleh PBF di Provinsi Bangka-Belitung yakni obat bebas, obat bebas terbatas, obat keras, narkotika, kosmetika, psikotropika, vaksin, susu, minuman, makanan. Pelaksanaan distribusi obat di sebelas PBF yang berada di Provinsi Bangka-Belitung yang ditinjau berdasarkan HK.00.05.3.2522 dalam hal SOP dari aspek manajemen mutu (72,72%), struktur organisasi dari aspek personalia dan dokumentasi diketahui 100% memenuhi. Data kuantitatif ini kemudian diperjelas dengan data wawancara mendalam yang menunjukkan isi SOP secara umum yaitu judul protap, nomor, dokumen, revisi, jumlah halaman, dokumen acuan, uraian proses distribusi; dari aspek personalia ditinjau dari jumlah karyawan sudah memadai; sebelas PBF memiliki dokumentasi, informasi pada dokumen penyaluran meliputi: tanggal penyaluran, nama dan alamat tujuan, bentuk sediaan, nama produk, kekuatan, jumlah, nomor batch dan expire date. Sementara itu, dalam aspek inspeksi diri hanya 9 PBF (81,81%) yang melaksanakan inspeksi diri sedangkan pada aspek bangunan dan peralatan hanya 9 PBF (81,81%) yang memiliki pengontrol temperatur. Adanya PBF yang tidak melakukan inspeksi diri ataupun memiliki pengontrol temperatur dikarenakan belum begitu penting menurut hasil wawancara secara mendalam. Maka dapat disimpulkan belum semua PBF di Bangka Belitung menerapkan CDOB sesuai SK. Badan POM Nomor: HK.00.05.3.2522.
x ABSTRACT
Pharmaceutical Wholesaler (PBF) is a legal entity that has a license for the procurement, storage, distribution of drugs and / or drug ingredients in bulk in accordance with laws and regulations. There are 11 PBF located in the Province of the Pacific Islands. This study aims to gain an idea of how the implementation of CDOB include aspects: quality management, personnel, equipment and buildings, documentation and self-inspections are in accordance with SK.Kepala Badan POM number: HK.00.05.3.2522 at Pharmaceutical Wholesaler in the Province of Bangka-Belitung.
This research includes the type of non-experimental research design was a descriptive study. Using a questionnaire instrument which converted into a percentage (%) of quantitative data. The results of the quantitative data is supported by the data-depth interviews with five aspects CDOB to 11 person in charge of PBF are willing to respondents.
The results showed that the products supplied by the PBF in the province of Bangka-Belitung the drug-free, drug-free is limited, hard drugs, drugs, cosmetics, psychotropic drugs, vaccines, milk, beverages, food. Implementation of drug distribution in eleven PBF located in the Province of Bangka-Belitung were reviewed by HK.00.05.3.2522 in the SOP of the aspects of quality management(72,72%), organizational structure and personnel aspects of documentation known 100% compliant. Quantitative data is then clarified by depth interview data showed that the contents of the general SOP title, number, document revisions, number of pages, document reference, description of the distribution process, from aspects of personnel in terms of the number of employees is sufficient; eleven PBF have documentation, information on the distribution of the document include: date of delivery, the name and address of the destination, the dosage form, product name, strength, quantity, batch number and expire date. Meanwhile, in the aspect of self-inspections PBF only 9 (81.81%) who carry out self-inspections while on aspects of building and equipment only 9 PBF (81.81%) who had a temperature controller. The existence of PBF were not inspected themselves or have a temperature control is not so important because according to the results of in-depth interviews. So we can conclude that not all PBF in the Province of Bangka-Belitung by applying CDOB according to SK. Badan POM Number: HK.00.05.3.2522.
.
i
PELAKSANAAN CARA DISTRIBUSI OBAT YANG BAIK SESUAI SK. KEPALA BADAN POM NOMOR: HK.00.05.3.2522 PADA PEDAGANG BESAR FARMASI DI PROVINSI BANGKA-BELITUNG TAHUN 2012
SKRIPSI
Diajukan untuk memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh :
Yosef Himawan Yudha NIM: 088114089
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
i
PELAKSANAAN CARA DISTRIBUSI OBAT YANG BAIK SESUAI SK. KEPALA BADAN POM NOMOR: HK.00.05.3.2522 PADA PEDAGANG BESAR FARMASI DI PROVINSI BANGKA-BELITUNG TAHUN 2012
SKRIPSI
Diajukan untuk memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh :
Yosef Himawan Yudha NIM: 088114089
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
vi PRAKATA
Puji Syukur kepada Tuhan Yang Maha Esa atas segala penyertaan, rahmat, kekuatan, berkat, dan karunia-Nya, sehingga penulis bisa menyelesaikan skripsi yang berjudul “Pelaksanaan Cara Distribusi Obat yang Baik Sesuai SK.
Kepala Badan POM Nomor: HK.00.05.3.2522 Pada Pedagang Besar Farmasi di Provinsi Bangka-Belitung”.
Penyelesaian penelitian dan penyusunan skripsi ini tidak lepas dari bantuan dan dorongan dari berbagai pihak yang senantiasa mendukung dari segi moral dan materiil. Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada :
1. Ibu Dra.T.B. Titien Sri Hartayu,M.Kes.,Apt.,PhD., selaku dosen pembimbing dan penguji yang selalu memberikan arahan, bimbingan, dorongan, semangat, saran, kritik dan pembelajaran selama selama penyusunan skripsi.
2. Dekan Fakultas Farmasi Universitas Sanata Dharma, beserta seluruh civitas akademika atas ijin dan segala bantuannya dalam penyusunan skripsi.
3. Bapak Ipang Djunarko, M.Sc.,Apt. dan Bapak Drs. Djaman Ginting Manik, Apt. sebagai Dosen Penguji atas pengarahan dan kesediaannya menguji skripsi ini.
vii
di Provinsi Bangka – Belitung yang bersedia membantu penulis dalam pengambilan data.
Penulis berharap, karya ini dapat bermanfaat dan mendorong mahasiswa angkatan berikutnya untuk berkarya lebih baik lagi demi majunya dunia kefarmasian di Indonesia.
ix INTISARI
Pedagang Besar Farmasi (PBF) adalah perusahaan berbentuk badan hukum yang memiliki izin untuk pengadaan, penyimpanan, penyaluran obat dan/atau bahan obat dalam jumlah besar sesuai ketentuan peraturan perundang-undangan. Terdapat 11 PBF yang berada di Provinsi Bangka Belitung. Penelitian ini bertujuan untuk memperoleh gambaran bagaimana pelaksanaan CDOB meliputi aspek: manajemen mutu, personalia, peralatan dan bangunan, dokumentasi dan inspeksi diri sudah sesuai dengan SK.Kepala Badan POM nomor: HK.00.05.3.2522 pada Pedagang Besar Farmasi di Provinsi Bangka-Belitung.
Penelitian ini termasuk jenis penelitian non eksperimental dengan rancangan penelitian bersifat deskriptif. Menggunakan instrument kuesioner yang dikonversikan dalam bentuk persentase (%) data kuantitatif. Hasil data kuantitatif tersebut diperkuat dengan data wawancara mendalam terhadap lima aspek CDOB kepada 11 penanggung-jawab PBF yang bersedia menjadi responden.
Hasil penelitian menunjukkan bahwa produk yang disalurkan oleh PBF di Provinsi Bangka-Belitung yakni obat bebas, obat bebas terbatas, obat keras, narkotika, kosmetika, psikotropika, vaksin, susu, minuman, makanan. Pelaksanaan distribusi obat di sebelas PBF yang berada di Provinsi Bangka-Belitung yang ditinjau berdasarkan HK.00.05.3.2522 dalam hal SOP dari aspek manajemen mutu (72,72%), struktur organisasi dari aspek personalia dan dokumentasi diketahui 100% memenuhi. Data kuantitatif ini kemudian diperjelas dengan data wawancara mendalam yang menunjukkan isi SOP secara umum yaitu judul protap, nomor, dokumen, revisi, jumlah halaman, dokumen acuan, uraian proses distribusi; dari aspek personalia ditinjau dari jumlah karyawan sudah memadai; sebelas PBF memiliki dokumentasi, informasi pada dokumen penyaluran meliputi: tanggal penyaluran, nama dan alamat tujuan, bentuk sediaan, nama produk, kekuatan, jumlah, nomor batch dan expire date. Sementara itu, dalam aspek inspeksi diri hanya 9 PBF (81,81%) yang melaksanakan inspeksi diri sedangkan pada aspek bangunan dan peralatan hanya 9 PBF (81,81%) yang memiliki pengontrol temperatur. Adanya PBF yang tidak melakukan inspeksi diri ataupun memiliki pengontrol temperatur dikarenakan belum begitu penting menurut hasil wawancara secara mendalam. Maka dapat disimpulkan belum semua PBF di Bangka Belitung menerapkan CDOB sesuai SK. Badan POM Nomor: HK.00.05.3.2522.
x ABSTRACT
Pharmaceutical Wholesaler (PBF) is a legal entity that has a license for the procurement, storage, distribution of drugs and / or drug ingredients in bulk in accordance with laws and regulations. There are 11 PBF located in the Province of the Pacific Islands. This study aims to gain an idea of how the implementation of CDOB include aspects: quality management, personnel, equipment and buildings, documentation and self-inspections are in accordance with SK.Kepala Badan POM number: HK.00.05.3.2522 at Pharmaceutical Wholesaler in the Province of Bangka-Belitung.
This research includes the type of non-experimental research design was a descriptive study. Using a questionnaire instrument which converted into a percentage (%) of quantitative data. The results of the quantitative data is supported by the data-depth interviews with five aspects CDOB to 11 person in charge of PBF are willing to respondents.
The results showed that the products supplied by the PBF in the province of Bangka-Belitung the drug-free, drug-free is limited, hard drugs, drugs, cosmetics, psychotropic drugs, vaccines, milk, beverages, food. Implementation of drug distribution in eleven PBF located in the Province of Bangka-Belitung were reviewed by HK.00.05.3.2522 in the SOP of the aspects of quality management(72,72%), organizational structure and personnel aspects of documentation known 100% compliant. Quantitative data is then clarified by depth interview data showed that the contents of the general SOP title, number, document revisions, number of pages, document reference, description of the distribution process, from aspects of personnel in terms of the number of employees is sufficient; eleven PBF have documentation, information on the distribution of the document include: date of delivery, the name and address of the destination, the dosage form, product name, strength, quantity, batch number and expire date. Meanwhile, in the aspect of self-inspections PBF only 9 (81.81%) who carry out self-inspections while on aspects of building and equipment only 9 PBF (81.81%) who had a temperature controller. The existence of PBF were not inspected themselves or have a temperature control is not so important because according to the results of in-depth interviews. So we can conclude that not all PBF in the Province of Bangka-Belitung by applying CDOB according to SK. Badan POM Number: HK.00.05.3.2522.
.
xi DAFTAR ISI
Halaman
HALAMAN JUDUL..………... i
HALAMAN PERSETUJUAN PEMBIMBING... ii
HALAMAN PENGESAHAN... iii
HALAMAN PERSEMBAHAN... iv
LEMBAR PERNYATAAN PUBLIKASI ... v
KATA PENGANTAR... vi
PERNYATAAN KEASLIAN KARYA... viii
INTISARI... ix
ABSTRACT... x
DAFTAR ISI... xi
DAFTAR TABEL... ix
DAFTAR GAMBAR... xv
DAFTAR LAMPIRAN……… xvii
BAB I PENGANTAR... 1
A. Latar Belakang... 1
1. Permasalahan... 3
2. Keaslian penelitian... 4
3. Manfaat penelitian... 5
B. Tujuan Penelitian... 5
xii
A. Praktik Kefarmasian... 7
B. Pedagang Besar Farmasi (PBF)………... 7
1. Definisi Pedagang Besar Farmasi………. 7
2. Penanggung jawab PBF ……… 11
3. Dokumentasi………. 12
C. Cara Distribusi Obat yang Baik (CDOB)... 12
1. Manajemen mutu... 17
2. Personalia... 18
3. Bangunan dan peralatan... 21
4. Dokumentasi... 25
5. Inspeksi diri... 33
D. Keterangan Empiris …... 34
BAB III METODE PENELITIAN... 35
A. Jenis dan Rancangan Penelitian... 35
B. Definisi Operasional... 35
C. Instrumen Evaluasi... 36
D. Subyek Penelitian... 37
E. Tata Cara Penelitian... 37
1. Studi pustaka... 37
2. Pembuatan instrumen penelitian... 37
3. Pengambilan data... 38
xiii
F. Waktu dan Tempat Penelitian... 39
G. Analisis Data... 39
BAB IV HASIL DAN PEMBAHASAN... 40
Pelaksanaan CDOB pada PBF di Propinsi Bangka-Belitung…….. 40
1. Manajemen mutu... 41
2. Personalia ... 46
3. Bangunan dan peralatan... 58
4. Dokumentasi ... 61
5. Inspeksi diri... 64
BAB V KESIMPULAN DAN SARAN A. Kesimpulan... 69
B. Saran... 70
DAFTAR PUSTAKA... 71
LAMPIRAN... 74
xiv
DAFTAR TABEL
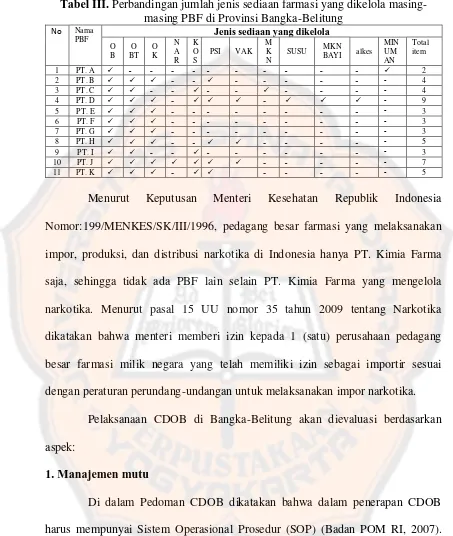
Halaman Tabel I. Syarat kontrol suhu penyimpanan obat………... 23 Tabel II. Syarat kondisi penyimpanan... 24 Tabel III. Perbandingan jumlah jenis sediaan farmasi yang dikelola
masing- masing PBF di Provinsi Bangka-Belitung.... …….... 41 Tabel IV. Perbandingan jumlah PBF terhadap jenis SOP yang ada PBF di Provinsi Bangka Belitung... 45 Tabel V. Perbandingan jenis pelatihan yang diikuti PBF
di Provinsi Bangka –Belitung………... 56 Tabel VI. Perbandingan jumlah sirkulasi udara di PBF
di Provinsi Bangka – Belitung... 59 Tabel VII. Jumlah perbandingan PBF yang memiliki monitoring /
temperatur dan kelembaban di Provinsi Bangka-Belitung…… 61 Tabel VIII. Perbandingan jumlah total jenis Dokumentasi keseluruhan PBF
dengan total per masing-masing dokumentasi yang ada
di Provinsi Bangka-Belitung... 62 Tabel IX. Perbandingan jumlah PBF di Provinsi Bangka-Belitung
xiv
DAFTAR GAMBAR
Halaman
Gambar 1. Cycle distribution ... 16
Gambar 2. Cara melindungi produk dari sinar matahari... 23
Gambar 3. Kriteria rak/pallets yang baik... 25
Gambar 4. Perbandingan jumlah pembuat SOP berdasarkan keahlian di PBF di Provinsi Bangka-Belitung... 46
Gambar 5. Perbandingan jumlah pendidikan terakhir penanggung-jawab PBF di provinsi Bangka-Belitung……… 47
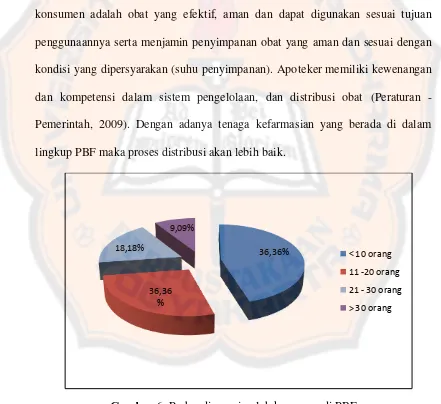
Gambar 6. Perbandingan jumlah Karyawan di PBF Bangka-Belitung……….. 48
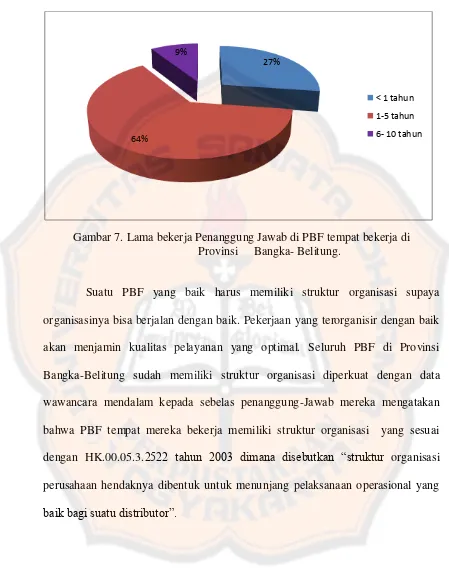
Gambar 7. Lama bekerja penanggung-jawab di PBF tempat bekerja di Provinsi Bangka-Belitung ... 50
Gambar 8. Struktur Organisasi PT. H………... 51
Gambar 9. Struktur Organisasi PT. D………...…... 52
Gambar 10. Strukur Organisasi PT. J…………..………. 53
Gambar 11. Strukur Organisasi PT. I……….………... 54
Gambar 12. Strukur Organisasi Struktur Organisasi PT. B……….. 55
Gambar 13. Perbandingan jumlah frekuensi diadakan pelatihan dalam 1 tahun terakhir di PBF Provinsi Bangka-Belitung... 57
xv
di Propinsi Bangka-Belitung………... 65 Gambar 16. Perbandingan jumlah penyelenggara inspeksi internal pada
PBF di Propinsi Bangka-Belitung... 66 Gambar 17. Perbandingan jumlah frekuensi diadakan inspeksi internal
pada PBF di Propinsi Bangka-Belitung ... 67 Gambar 18. Perbandingan jumlah penyelenggara inspeksi eksternal
pada PBF di Propinsi Bangka-Belitung…... 67 Gambar 19. Perbandingan jumlah Frekuensi diadakan inspeksi
xvi
DAFTAR LAMPIRAN
Halaman Lampiran 1. Data profil penanggung jawab Pedagang Besar Farmasi
(PBF) di Provinsi Bangka Belitung……… 75
Lampiran 2. Pelaksanaan CDOB pada PBF di Provinsi Bangka-Belitung ……….………... 76
Lampiran 3. Manajemen Mutu………... 77
Lampiran 4. Personalia……….. 78
Lampiran 5. Bangunan dan peralatan………... 78
Lampiran 6. Dokumentasi………... 79
Lampiran 7. Inspeksi diri………... 80
Lampiran 8. Wawancara ……… 82
Lampiran 9. Quisioner... 103
Lampiran 13. Struktur organisasi... 112
1 BAB I
PENDAHULUAN
A.Latar Belakang
Di era globalisasi saat ini, banyak pedagang besar farmasi yang telah berkembang di Indonesia. Jumlah PBF yang terdata di Indonesia mencapai 2.821 PBF yang mengedarkan berbagai macam sediaan farmasi sebanyak 79.045 macam yang tersebar di 33 provinsi, demikian pula di Provinsi Bangka-belitung dimana terdapat 11 PBF yang tersebar secara dalam dua wilayah territorial yakni di Kota Pangkalpinang terdapat 9 PBF sedangkan di Kabupaten Belitung ada 2 PBF yang mengedarkan 12 macam sediaan farmasi. Sediaan farmasi harus aman, berkhasiat/bermanfaat, bermutu dan terjangkau oleh para konsumennya. Oleh karena itu diperlukan suatu sistem pengawasan obat secara komprehensif termasuk pada jaringan distribusi obat agar obat yang didistribusikan terjamin mutu, khasiat, keamanan, dan keabsahan obat sampai ke tangan konsumen. (Putera, 2012).
sistem Cara Distribusi Obat yang Baik (CDOB) sehingga keamanan, khasiat, dan kualitas obat yang didistribusikan oleh PBF tetap terjamin sejak dari penyimpanan hingga sampai ke tangan konsumen (Kementerian Hukum dan Hak Asasi Manusia, 2009).
dalam pelaksanaan CDOB untuk melakukan tindakan evaluasi dan tindakan perbaikan yang meliputi seluruh aspek CDOB (BPOM RI, 2007).
Seluruh ketentuan tersebut wajib dilaksanakan oleh PBF yang diatur dalam Peraturan Pemerintah no.51 tahun 2009 dan keputusan kepala badan POM nomor: HK.00.05.3.2522. Tidak menutup kemungkinan adanya PBF yang belum melaksanakan ketentuan-ketentuan tersebut karena berbagai faktor. Obat yang didistribusikan oleh PBF yang tidak melaksanakan ketentuan tersebut berpotensi tidak terjamin keamanan, khasiat dan kualitasnya sehingga dapat merugikan konsumen. Penelitian ini bertujuan untuk memperoleh gambaran pelaksanaan apakah peraturan tersebut telah dilaksanakan oleh PBF di Provinsi Bangka Belitung.
1. Permasalahan
a. Apakah sebelas PBF di Provinsi Bangka-Belitung sudah melaksanakan CDOB sesuai Keputusan Kepala Badan POM nomor: HK.00.05.3.2522 ?
b. Apakah gambaran pelaksanaan distribusi obat di sebelas PBF yang berada di Provinsi Bangka-Belitung sudah sesuai dengan HK.00.05.3.2522 yang meliputi:
1) Aspek manajemen mutu berkaitan dengan pelaksanaan standar operasional prosedur
3) Aspek bangunan dan peralatan berkaitan dengan pelaksanaan pengontrolan kondisi ruangan.
4) Aspek Dokumentasi berkaitan dengan dilaksanakan atau tidak kegiatan dokumentasi
5) Inspeksi diri berkaitan dengan dilaksanakan atau tidak kegiatan inspeksi diri
2. Keaslian penelitian
Sejauh penelusuran pustaka yang dilakukan, penulis menemukan beberapa penelitian yang menyerupai dengan cara distribusi obat yang baik pada pedagang besar farmasi:
Bangka-Belitung. Perbedaan kedua terletak pada daerah yang diteliti, peneliti melakukan penelitian di Provinsi Bangka-Belitung.
3. Manfaat penelitian
Manfaat yang bisa diperoleh dari penelitian ini adalah:
a. Manfaat teoritis. Penelitian ini diharapkan dapat digunakan sebagai data evaluasi cara distribusi obat yang baik meliputi ada tidaknya; SOP, stuktur organisasi, dokumentasi, peralatan pengontrol ruangan, dan inspeksi diri pada PBF yang dibutuhkan peneliti lain yang akan melakukan penelitian serupa.
b. Manfaat praktis. Hasil penelitian ini dapat digunakan oleh PBF di Provinsi Bangka-Belitung sebagai data evaluasi untuk mengetahui kelemahan sistem distribusi obat yang dilakukan sehingga dapat digunakan untuk perbaikan pada masing-masing PBF tersebut.
B. Tujuan Penelitian
1. Tujuan umum
Penelitian ini bertujuan untuk melihat gambaran pelaksanaan cara distribusi obat yang baik pada sebelas pedagang besar farmasi di provinsi bangka-belitung berdasarkan keputusan kepala badan POM nomor: HK.00.05.3.2522. 2. Tujuan khusus
a. Mengidentifikasi gambaran pelaksanaan distribusi obat di sebelas PBF yang berada di provinsi Bangka-Belitung terhadap HK.00.05.3.2522 yang meliputi:
1) Aspek manajemen mutu berkaitan dengan pelaksanaan standar operasional prosedur
2) Aspek personalia berkaitan dengan dilaksanakan atau tidak struktur organisasi.
3) Aspek bangunan dan peralatan berkaitan dengan pelaksanaan pengontrolan kondisi ruangan.
4) Aspek Dokumentasi berkaitan dengan dilaksanakan atau tidak kegiatan dokumentasi
7 BAB II
PENELAAHAN PUSTAKA
A. Praktek Kefarmasian
Berdasarkan Undang-Undang No 36 tahun 2009 bahwa dalam praktek kefarmasian membutuhkan seorang tenaga kefarmasian yang berfungsi untuk mengatur pengendalian mutu sediaan farmasi, pengamanan, pengadaan, dan pendistribusian obat. Tenaga kefarmasian tersebut telah diatur dalam Peraturan Pemerintah No 51 tahun 2009 di mana dalam undang-undang tersebut mengatur tenaga teknis kefarmasian dan apoteker. Tenaga teknis kefarmasian terdiri dari sarjana farmasi, ahli madya farmasi, analis farmasi, dan tenaga menengah farmasi. Apoteker adalah sarjana farmasi yang telah lulus sebagai apoteker dan telah mengucapkan sumpah jabatan. Berdasarkan UU tersebut fasilitas distribusi (PBF) wajib memiliki apoteker sebagai penanggung-jawab PBF (Menteri Kesehatan, 2009).
B. Pedagang Besar Farmasi (PBF)
Distributor merupakan badan atau orang yang berwenang atau yang berhak mendistribusikan perangkat medis sesuai dengan ketentuan per undang-undangan atau hukum yang bersifat memaksa (Tanzania Food And Drugs Authority, 2010). Distributor adalah perusahaan / pihak yang ditunjuk oleh prinsipal untuk memasarkan dan menjual barang-barang prinsipalnya dalam wilayah tertentu untuk jangka waktu tertentu, tetapi bukan sebagai kuasa prinsipal.
prinsipalnya dan kemudian ia menjualnya kepada para pembeli di dalam wilayah yang diperjanjikan oleh prinsipal dengan distributor tersebut. Segala akibat hukum dari perbuatannya menjadi tanggung jawab distributor itu sendiri (Suryawan, 2006).
Pedagang Besar Farmasi (PBF) dalam penyaluran produk farmasi dapat bertindak sebagai Distributor dan Sub Distributor, yang diatur dalam Keputusan Menteri Perindustrian dan Perdagangan Nomor 23/MPR/KEP/I/1998 tentang Lembaga-Lembaga Usaha Perdagangan, BAB I, Ketentuan Umum, Pasal 1: distributor utama adalah perorangan atau badan usaha yang bertindak atas namanya sendiri yang ditunjuk oleh pabrik atau pemasok untuk melakukan pembelian, penyimpanan, penjualan serta pemasaran barang dalam partai besar secara tidak langsung kepada konsumen akhir terhadap barang yang dimiliki/dikuasai oleh pihak yang menunjuknya (Keputusan Menteri Perindustrian dan Perdagangan, 1998).
Menurut Peraturan Pemerintah Republik Indonesia Nomor 51 Tahun 2009 dikatakan bahwa pedagang besar farmasi adalah perusahaan berbentuk badan hukum yang memiliki izin untuk pengadaan, penyimpanan, penyaluran perbekalan farmasi dalam jumlah besar sesuai ketentuan, yang tertuang dalam Bab I Ketentuan umum pasal 12 (Peraturan - Pemerintah No 51, 2009).
Menteri Kesehatan Republik Indonesia Nomor 1148/MENKES/PER/VI/2011 bahwa pedagang besar farmasi, yang selanjutnya disingkat PBF adalah perusahaan berbentuk badan hukum yang memiliki izin untuk pengadaan, penyimpanan, penyaluran obat dan/atau bahan obat dalam jumlah besar sesuai ketentuan peraturan perundang-undangan (Kepmenkes, 2011).
Menurut Keputusan Menteri Kesehatan Republik Indonesia Nomor:199/MENKES/SK/III/1996, pedagang besar farmasi yang melaksanakan impor, produksi, dan distribusi narkotika di Indonesia hanya PT. Kimia Farma saja, sehingga tidak ada PBF lain selain PT. Kimia Farma yang mengelola Narkotika. PT. Kimia Farma merupakan salah satu perusahaan milik negara sehingga memiliki kewenangan berdasarkan undang-undang narkotika tersebut untuk menyalurkan narkotika (Menteri Kesehatan, 2009).
Menurut pasal 15 UU nomor 35 tahun 2009 tentang Narkotika dikatakan bahwa menteri memberi izin kepada 1 (satu) perusahaan pedagang besar farmasi milik negara yang telah memiliki izin sebagai importir sesuai dengan peraturan perundang-undangan untuk melaksanakan impor narkotika, pada UU 22 tahun 1997 bahwa yang dapat memberikan izin khusus penyaluran narkotika adalah menteri kesehatan (Menteri Kesehatan, 2009).
Pada Peraturan Menteri Kesehatan Republik Indonesia Nomor 688/MENKES/PER/VII/1997 tentang peredaran psikotropika, disebutkan pengertian dari pedagang besar farmasi adalah perusahaan yang memiliki izin dari menteri untuk melakukan kegiatan penyaluran sediaan farmasi, termasuk psikotropika dan alat kesehatan (Menteri Kesehatan, 1997).
Dapat disimpulkan bahwa pedagang besar farmasi merupakan perusahaan yang mendapatkan ijin dari menteri untuk mengadakan pengadaan, penyimpanan, penyaluran obat, sediaan farmasi, psikotropika dan narkotika berdasarkan ketentuan perundang-undangan yang berlaku serta pedagang besar farmasi dilarang menjual perbekalan farmasi secara eceran, baik ditempat kerjanya ataupun ditempat lain dan juga pedagang besar farmasi dilarang melayani resep dokter, dilarang melakukan pengadaan, penyimpanan dan penyaluran narkotika dan psikotropika tanpa izin khusus dari menteri.
Berdasarkan PERMENKES No 918 tentang persyaratan Pedagang besar Farmasi pasal (5) Pedagang Besar Farmasi wajib memenuhi persyaratan sebagai berikut:
a. Dilakukan oleh badan hukum berbentuk perseroan terbatas, koperasi, perusahaan nasional maupun perusahaan patungan antara perusahaan penanaman modal asing yang telah memperoleh izin usaha industi farmasi di Indonesia dengan perusahaan nasional.
c. Memiliki asisten apoteker atau apoteker penanggung jawab yang bekerja penuh.( Dalam PP No. 51 tahun 2009 diwajibkan penanggung-jawab PBF adalah seorang apoteker).
d. Anggota direksi tidak pernah terlibat pelanggaran ketentuan perundang-undangan di bidang farmasi.
1. Penanggung Jawab PBF
Menurut Peraturan Pemerintah Republik Indonesia Nomor 51 Tahun 2009 pada Bab II Penyelenggaraan Pekerjaan Kefarmasian Pasal 14 Ayat (1) berbunyi “ Setiap Fasilitas Distribusi atau Penyaluran Sediaan Farmasi berupa
obat harus memiliki seorang Apoteker sebagai penggung jawab, kemudian pada pasal 14 ayat (2) dikatakan “ Apoteker sebagai penanggung jawab sebagaimana
dimaksud pada ayat (1) dapat dibantu oleh apoteker pendamping dan/atau Tenaga teknis kefarmasian. Dalam Peraturan menteri Kesehatan Nomor: 918 /MENKES/PER/X/1993 pada Bab III Persyaratan Pedagang Besar Farmasi Pasal 7 ayat (1) “kewajiban yang dimaksud dalam pasal 6 dipertanggungjawabkan oleh
2. Dokumentasi
Dokumentasi menurut Pedoman CDOB yang dikeluarkan Badan POM adalah seluruh prosedur, instruksi dan catatan tertulis yang berhubungan dengan distribusi obat. Di dalam Keputusan Menteri Kesehatan RI No. 1191/Menkes/SK/IX/2002 dikatakan bahwa Pedagang Besar Farmasi mempunyai kewajiban dalam melaksanakan dokumentasi pengadaan, penyimpanan dan penyaluran secara tertib ditempat usahanya mengikuti pedoman teknis yang ditetapkan oleh Menteri. Di dalam Peraturan Pemerintah Nomor 51 tahun 2009 pasal 17 juga dikatakan bahwa pekerjaan kefarmasian yang berkaitan dengan proses distribusi atau penyaluran Sediaan Farmasi pada Fasilitas Distribusi atau Penyaluran Sediaan Farmasi wajib dicatat oleh Tenaga Kefarmasian sesuai dengan tugas dan fungsinya. Jadi, dapat disimpulkan bahwa di Pedagang Besar farmasi (PBF) harus mempunyai dokumentasi yang berkaitan dengan seluruh proses distribusi yang dilakukan oleh Tenaga Kefarmasian.
C. Cara Distribusi Obat Yang Baik (CDOB)
Distribusi merupakan perpindahan barang dari produsen menuju lembaga kesehatan (Tanzania food and drugs authority, 2007),. Sementara menurut Direktorat Bina Obat Publik dan Perbekalan Kesehatan, (2010), distribusi merupakan suatu rangkaian kegiatan dalam rangka pengeluaran dan pengiriman obat-obatan yang bermutu, terjamin keabsahan serta tepat jenis dan jumlah dari gudang obat secara merata dan teratur untuk memenuhi kebutuhan unit-unit pelayanan kesehatan. Dari pustaka-pustaka di atas, dapat disimpulkan bahwa distribusi adalah perpindahan barang dari produsen (industri farmasi) menuju sarana maupun fasilitas kesehatan.
Sediaan farmasi adalah obat, bahan, bahan obat, obat tradisional dan kosmetika yang terdapat di dalam Undang-Undang Kesehatan No 36 tahun 2009. Obat juga dikelompokkan ke dalam obat keras, obat keras tertentu dan obat narkotika harus diserahkan kepada pasien oleh apoteker. Pengelolaan perbekalan farmasi adalah suatu proses yang merupakan siklus kegiatan, dimulai dari pemilihan, perencanaan, pengadaan, penerimaan, penyimpanan, pendistribusian, pengendalian, penghapusan, administrasi dan pelaporan serta evaluasi yang diperlukan bagi kegiatan pelayanan (Direktorat Jenderal Bina kefarmasian dan alat kesehatan RI, 2006).
Definisi fasilitas distribusi atau penyaluran sediaan farmasi yaitu pedagang besar farmasi dan instalasi sediaan farmasi. Adapun pelaksanaan pekerjaan kefarmasian meliputi: Pekerjaan kefarmasian dalam distribusi atau penyaluran sediaan farmasi. Sebagaimana yang telah tertuang dalam Pasal 14 maka fasilitas distribusi dan penyaluran sediaan farmasi harus mengikuti Cara Distribusi Obat yang Baik yang ditetapkan oleh menteri dan juga tertulis dalam Keputusan Kepala Badan Pengawas Obat Dan Makanan Nomor: HK.00.05.3.2522 Tahun 2003 Tentang Pedoman Cara Distribusi Obat yang Baik (Peraturan-Pemerintah No 51 tentang pekerjaan kefarmasian, 2009).
menerapkan cara distribusi obat yang baik (CDOB) dalam seluruh aspek dan rangkaian kegiatan distribusi obat. Tujuan utama pelaksanaan distribusi obat yang baik adalah terselenggaranya suatu sistem jaminan kualitas oleh distributor, yaitu: 1. Menjamin penyebaran obat secara merata dan teratur agar dapat tersedia
pada saat diperlukan.
2. Terlaksananya pengamanan lalu lintas dan penggunaan obat tepat sampai kepada pihak yang membutuhkan secara sah untuk melindungi masyarakat dari kesalahan penggunaan atas penyalahgunaan.
3. Menjamin keabsahan dan mutu agar obat yang sampai ke tangan konsumen adalah obat yang efektif, aman dan dapat digunakan sesuai tujuan penggunaannya.
4. Menjamin penyimpanan obat aman dan sesuai kondisi yang dipersyaratkan, termasuk selama transportasi (Badan Pengawasan Obat dan Makanan RI, 2007).
Keempat poin di atas dapat dicapai apabila penanggung jawab PBF adalah seorang Apoteker (Peraturan - Pemerintah, 2009).
Menurut Quick. D. J (1997), siklus distribusi meliputi: Port clearing
(pelabuhan kliring) dimana langkah pertama dalam memesan obat-obatan agar tersedia untuk pendistribusian intinya adalah mengidentifikasi barang kiriman, memproses dokumen penting tentang kiriman obat yang tiba di pelabuhan,
dipesan. Inventory control (pengendalian persediaan) ditujukan untuk melihat arus obat-obatan yang keluar dan masuk untuk menghindari pencurian dan korupsi.
Storage (penyimpanan) bertaraf nasional. Lokasi layak, kontruksi, organisasi dan pemeliharaan fasilitas penyimpanan akan membantu kualitas obat, memperkecil pencurian dan memelihara supply langganan tetap untuk fasilitas kesehatan.
[image:36.595.72.520.271.698.2]Requisition of supplies (daftar permintaan pasokan) formulir dan prosedur permintaan adalah bagian kunci sistem inventaris kontrol. Delivery (pengiriman) manajemen transpor seharusnya memilih metode transpor dengan hati-hati dan jadwal pengiriman yang realistik dan sistematik untuk menyediakan tepat waktu dan pelayanan ekonomi. Dispensing to patient (penyerahan ke pasien) proses distribusi mencapai tujuan dimana obat sampai pada rumah sakit, klinik, pusat kesehatan, penulis resep. Consumption reporting ( pelaporan konsumsi) penutupan jaringan dalam siklus distribusi adalah arus informasi dalam konsumsi dan menyeimbangkan stock. Drugs procurement (pengadaan obat) dimana obat-obat yang telah tersedia untuk dikirim ke fasilitas-fasilitas kesehatan (Quick, 1997).
Agar jaringan dalam pendistribusian obat dapat terlaksana dengan baik, maka harus diperhatikan aspek penting yaitu :
1. Manajemen mutu
Dalam suatu organisasi, quality assurance merupakan bagian dari manajemen kualitas. Harus ada prosedur untuk menjamin bahwa obat didistribusikan dan diperoleh dari sumber resmi. Oleh karena itu dalam pelaksanaan penerapan CDOB diperlukan Sistem Operasional Prosedur (SOP) untuk setiap kegiatan operasionalnya (Badan Pengawasan Obat dan Makanan RI, 2007).
Definisi dari Standar Prosedur Operasional (SPO) adalah suatu perangkat instruksi/langkah-langkah yang dibakukan untuk menyelesaikan suatu proses kerja rutin tertentu/standar prosedur operasional memberikan langkah yang benar dan yang terbaik berdasarkan konsensus bersama untuk melaksanakan berbagai kegiatan dan fungsi pelayanan yang dibuat oleh sarana pelayanan kesehatan berdasarkan standar profesi (Peraturan-Pemerintah, 2004). Definisi SOP yang tertuang dalam Peraturan Pemerintah No. 51 adalah prosedur tertulis berupa petunjuk operasional tentang pekerjaan kefarmasian. SOP merupakan sebuah prosedur tertulis untuk memberi perintah menjalankan operasi (Tanzania Food And Drugs Authority, 2010).
suatu proses agar dapat berjalan dengan baik sesuai dengan fungsinya. Tujuan dari SOP adalah untuk menjaga konsistensi dan tingkat kinerja karyawan atau operator dalam suatu organisasi, mengetahui dan memperjelas alur tugas, wewenang dan tanggung jawab karyawan, untuk melindungi organisasi dan karyawan dari kesalahan administrasi (Stup, 2001).
2. Personalia
Sumber daya manusia (SDM) merupakan salah satu faktor yang sangat penting dalam suatu perusahaan disamping faktor lain yaitu modal. Oleh karena itu, sumber daya manusia perlu dikelola dengan baik untuk meningkatkan efektifitas dan efisiensi organisasi, sebagai salah satu fungsi dalam perusahaan yang dikenal dengan manajemen sumber daya manusia (MSDM). Beberapa pengertian dari manajemen sumber daya manusia adalah sebagai berikut manajemen sumber daya manusia merupakan kebijakan dan praktik menentukan aspek manusia atau sumber daya manusia dalam posisi manajemen, termasuk merekrut, menyaring, melatih, memberi penghargaan, dan penilaian (Dessler, 2003). Manajemen sumber daya manusia merupakan aktivitas-aktivitas yang dilaksanakan agar sumber daya manusia di dalam organisasi dapat digunakan secara efektif guna mencapai berbagai tujuan (Simamora, 2004).
rasional kegiatan sejumlah orang untuk mencapai beberapa tujuan umum melalui pembagian kerja dan fungsi melalui hirarki otoritas dan tanggung jawab serta organisasi juga mempunyai karakteristik tertentu yaitu mempunyai struktur, tujuan, saling berhubungan satu bagian dengan bagian lain dan tergantung pada komunikasi anggotanya untuk mengkoordinasi aktifitas dalam program itu. Selanjutnya Kochler tahun 2001 (cit., Samsi, 2004) mengatakan bahwa organisasi adalah sistem hubungan yang terstruktur yang mengkoordinasi usaha suatu kelompok untuk mencapai tujuan tertentu, sedangkan pendapat Wright tahun 2001 (cit., Samsi, 2004) mengatakan bahwa organisasi adalah suatu bentuk sisteim terbuka dari aktivitas yang terkoordinasi oleh dua orang atau lebih untuk mencapai tujuan bersama. Walaupun kedua pendapat mengenai organisasi tersebut kelihatan berbeda perumusannya tetapi ada tiga hal yang sama-sama dikemukakan yaitu: (1) organisasi merupakan sebuah sistim, (2) mengkoordinasikan aktivitas, (3) mencapai tujuan bersama (Samsi, 2004).
Agar pekerjaan berjalan dengan efisien dan efektif, maka pemilihan karyawan harus dengan kualifikasi yang sesuai. Menurut Tanzania food and drugs authority kunci dari personil yang baik adalah bertanggung jawab atas operasi pergudangan serta harus memiliki kemampuan sesuai pengetahuan dan pengalaman, untuk tugas yang diberikan kepada mereka. Setiap personil perusahaan dituntut agar dapat bekerja efektif, efisien, kualitas dan kuantitas pekerjannya baik, sehingga daya saing perusahaan semakin besar. Pengembangan ini dilakukan untuk tujuan nonkarir maupun karir bagi para karyawan baru atau lama melalui pelatihan atau pendidikan (Hasibuan, 2001). Manajemen adalah fungsi yang berhubungan dengan mewujudkan hasil tertentu melalui kegiatan orang-orang. Hal ini berarti bahwa sumber daya manusia berperan penting dan dominan dalam manajemen (Hasibuan, 2001).
Manajer adalah para eksekutif yang dikontrak oleh organisasi untuk mengkoordinasi dengan tujuan untuk mengarahkan karyawan agar dapat bekerja dengan baik sesuai dengan tugas yang telah ditetapkan pada masing-masing karyawan. Tugas seorang manajer adalah mengendalikan operasi sehari-hari yang dilakukan oleh perusahaan (Young, 2009). Rentang manajemen sudah diterima secara umum bahwa jumlah maksimum bawahan yang dapat diawasi dengan baik oleh seorang manajer adalah antara 8 sampai 10 orang (Wahjono, 2009).
yang terkait dengan tugasnya sehingga memiliki pengetahuan, keterampilan dan kemampuan sesuai dengan tugasnya. Selain itu seluruh karyawan harus diberi pelatihan tentang sanitasi dan hygiene. Seluruh karyawan harus memiliki kesehatan fisik dan mental yang baik sehingga mampu melaksanakan tugasnya secara professional dan bertanggung jawab (Badan Pengawasan Obat dan Makanan RI, 2007).
Seluruh karyawan yang langsung ikut serta dalam kegiatan pendistribusian obat, mendapat pelatihan CDOB. Pengetahuan tentang hazardous
obat (seperti toksisitas dan produk infectious/sensitif) harus diberikan selama pelatihan. Harus ada SOP pertolongan pertama dan peralatan yang berhubungan dengan keadaan darurat. Pelatihan hendaklah diberikan oleh tenaga kompeten dan dijalankan secara berkesinambungan dan dengan frekuensi yang memadai untuk menjamin agar karyawan terbiasa dengan persyaratan CDOB yang berkaitan dengan tugasnya (Badan Pengawasan Obat dan Makanan RI, 2007).
3. Bangunan dan peralatan
Syarat gudang penyimpanan khusus narkotika yaitu dinding terbuat dari tembok dan hanya mempunyai satu pintu dengan 2 (dua) buah kunci yang kuat dengan merek yang berlainan, langit-langit dilengkapi dengan jeruji besi, dilengkapi dengan lemari besi yang tidak kurang dari 150 kilogram dan mempunyai kunci yang kuat (Menteri Kesehatan RI, 2009). Bangunan harus memiliki sirkulasi udara yang baik dan selalu dalam keadaan bersih (Menteri Kesehatan RI, 2009). Jika tidak ada instruksi penyimpanan khusus yang diberikan, kondisi penyimpanan diberlakukan secara normal. Kondisi penyimpanan yang normal untuk obat telah didefinisikan sebagai penyimpanan dalam tempat yang kering, yakni tempat yang berventilasi baik pada suhu + 15ºC sampai + 25ºC, atau tergantung pada kondisi iklim, hingga + 30ºC. Suhu 15ºC sampai 25 atau 30ºC diasumsikan adalah zona ber-AC. Oleh karena itu, kelembaban perlu dikontrol. Di wilayah beriklim subtropis, kisaran suhu ini dapat dicapai tanpa AC, tetapi kontrol kelembaban mungkin masih diperlukan (United Nations High Commissioner for Refugees, 2006). Untuk mengurangi efek kelembaban diperlukan:
1. Ventilasi: jendela terbuka atau ventilasi terbuka dari gudang untuk memungkinkan sirkulasi udara. Dipastikan jendela memiliki tirai untuk menahan masuknya serangga dan burung.
2. Sirkulasi: gunakan kipas untuk membuat sirkulasi udara dari luar-dalam lancar
Untuk melindungi produk dari sinar matahari antara lain: 1. Menutup jendela atau menggunakan tirai
2. Jauhkan produk dari paparan sinar matahari, terutama produk dalam bentuk sediaan injeksi
[image:43.595.70.522.217.749.2]3. Jangan menyimpan atau mengemas produk di bawah sinar matahari panas (United Nations High Commissioner for Refugees,2006).
Gambar 2. Cara melindungi produk dari sinar matahari (Snow. 2003) Supaya kondisi obat agar tidak rusak ketika disimpan di dalam gudang penyimpanan, maka untuk itu diperlukan kontrol suhu untuk menjaga mutu obat tersebut agar sesuai dengan standar pabrik.
Tabel I. Syarat kontrol suhu penyimpanan obat (Tanzania food and drugs authority, 2010)
Dalam label Pedoman nilai
Lemari pembeku Suhu termostatik dikontrol antara -20 0 C
dan -100 C
kulkas Suhu termostatik dikontrol antara 20 C dan 80 C
Panas Suhu diantara 300 C dan 400 C Panas sangat tinggi Suhu diatas 400 C
Tidak boleh disimpan diatas 300 C Suhu diantara 20 C dan 300 C Tidak boleh disimpan diatas 250 C Suhu diantara 20 C dan 250 C Tidak boleh disimpan diatas 150 C Suhu diantara 20 C dan 150 C Tidak boleh disimpan diatas 80 C Suhu diantara 20 C dan 80 C Tidak boleh disimpan diatas 80 C Suhu diantara 80 C dan 250 C
Tabel II. Syarat kondisi penyimpanan menurut label (TANZANIA FOOD AND DRUGS AUTHORITY, 2010)
Dalam label Pedoman nilai
Pelindung dari kelembaban Tidak melebihi 60% kelembaban relatif dalam kondisi normal penyimpanan; untuk penyajian kepada pelanggan harus dalam container yang resisten terhadap kelembaban.
Perlindungan dari cahaya Untuk penyajian kepada pelanggan harus dalam container yang resisten terhadap cahaya.
Bangunan mempunyai penerangan yang cukup untuk dapat melaksanakan kegiatan dengan aman dan benar. Penyimpanan yang menuntut ketepatan temperatur dan kelembapan (Badan Nasional Penanggulangan Bencana, 2009). Alat yang digunakan untuk mengukur suhu adalah termometer dan alat yang digunakan untuk mengukur kelembapan di suatu tempat adalah higrometer (Wikipedia, 2012). Berdasarkan UNHCR (2006), meletakkan termometer pada tempat dengan suhu yang paling tinggi di gudang dan memeriksa temperatur saat ketika cuaca paling panas pada hari itu. Bangunan harus selalu dalam keadaan bersih, bebas dari tumpukan sampah dan barang-barang yang tidak diperlukan (United Nations High Commissioner for Refugees, 2006)
1. Minimal 10 cm (4inci) dari lantai
[image:45.595.72.522.167.541.2]2. Minimal 30 cm (1kaki ) dari dinding dan tumpukan lain 3. Tidak lebih dari 2,5 meter (8 kaki) tinggi untuk penyimpan
Gambar 3. Kriteria rak/pallets yang baik (Snow, 2003)
4. Dokumentasi
farmasi pada fasilitas distribusi atau penyaluran sediaan farmasi wajib dicatat oleh tenaga kefarmasian sesuai dengan tugas dan fungsinya. Jadi, dapat disimpulkan bahwa di PBF harus ada dokumentasi yang berkaitan dengan seluruh proses distribusi yang dilakukan oleh tenaga kefarmasian (Peraturan-Pemerintah, 2009).
Semua dokumentasi hendaknya dilaksanakan dengan baik dengan maksud:
a. Untuk menjamin pelaksanaan pengadaan dan distribusi sesuai ketentuan perundang-undangan
b. Untuk dapat menjamin penyediaan data dan informasi yang akurat dan aktual pada pemesanan, penerimaan, keadaan stok, penyaluran, dan sebangainya
c. Untuk dapat menjaga tingkat stok pada kondisi yang dapat menjamin kelancaran pelayanan
d. Untuk dapat menjamin penerimaan produk yang benar meliputi jumlah, identitas, kualitas
e. Untuk dapat melakukan dokumentasi yang benar dan lengkap serta mencatat semua kegiatan yang dilaksanakan dalam pengelolaan pengadaan dan penyaluran obat.
prosedur, metode dan instruksi, catatan, laporan serta jenis dokumentasi lain yang diperlukan dalam perencanaan, pelaksanaan, pengendalian serta evaluasi seluruh rangkaian kegiatan pengadaan dan penyaluran obat. Dokumentasi dapat dilakukan secara manual maupun komputerisasi dan hendaklah jelas, lengkap serta disimpan sekurang-kurangnya lima tahun. sistem dokumen seharusnya memiliki spesifikasi produk, prosedur dan catatan. seharusnya dokumen dibuat untuk proses audit dan lisensi (Health Sciences Authority, 2010).
Dokumentasi di PBF meliputi kegiatan pemesanan, penerimaan,dan penyimpanan:
a. Pemesanan obat
Pesanan dibuat secara tertulis minimal rangkap 2 menggunakan form surat pesanan sesuai formulir D-1. Setiap surat pesanan seharusnya diberi nomor secara berurutan, nomor dicetak dengan baik, jelas dan rapi. Apabila karena sesuatu hal surat pesanan tidak dapat digunakan, maka surat pesanan yang tidak digunakan ini tetap harus diarsipkan dengan diberi tanda pembatalan yang jelas. Surat pesanan supaya ditandatangani oleh penanggung jawab, sambil dicantumkan nama jelas dan nomor surat izin kerja yang bersangkutan. Surat pesanan diarsipkan berdasarkan nomor urut dan tanggal pemesanan (Badan Pengawasan Obat dan Makanan RI, 2007).
stok hidup dan stok pengaman. Stok hidup adalah stok yang digunakan untuk memenuhi pelayanan dalam jangka waktu antara dua pengiriman atau penerimaan.Stok pengaman untuk mencegah kekosongan yang mungkin timbul karena terlambatnya pengiriman atau meningkatnya permintaan (Badan Pengawasan Obat dan Makanan RI, 2007).
b. Penerimaan obat
Digunakan untuk memastikan bahwa obat yang diterima dalam keadaan baik, sah sesuai dengan yang dipesan, sebaiknya dilakukan pemeriksaan pada waktu obat diterima dengan menggunakan “checklist” yang sudah disiapkan untuk
masing-masing jenis produk: kebenaran jumlah kemasan, kebenaran jumlah satuan dalam tiap kemasan, kebenaran jenis produk yang diterima, tidak terlihat tanda-tanda kerusakan, kebenaran identitas produk. Dokumentasi penerimaan, produk yang tidak sesuai kriteria di atas hendaklah diproses untuk pengembalian atau penggantian. Penanggung jawab menentukan penanganan tindak lanjut oleh yang diterima. Faktur atau surat penyerahan barang (SPB) asli atau salinan diberikan kepada penanggung jawab, dan satu salinan dikirim ke bagian administrasi. Bagian administrasi mencatat pada kartu persediaan sesuai dengan formulir D-2, buku pembelian sesuai formulir D-3. Faktur atau surat penyerahan barang sebaiknya diarsipkan berdasarkan nomor urut dan tanggal penerimaan (Badan Pengawasan Obat dan Makanan RI, 2007).
c . Penyimpanan Obat
surat penyerahan barang. Faktur atau surat penyerahan barang diarsipkan berdasarkan nomor urut dan tanggal penerimaan. Semua dokumentasi harus disimpan dan diberikan fasilitas tempat penyimpanan untuk mencegah kerusakan dokumentasi (World Health Organization, 2005).
d. Penyaluran
Kegiatan penyaluran merupakan suatu rangkaian kegiatan yang penting karena obat harus disalurkan kepada pemesan yang sah dan tepat meliputi penerimaan pesanan, pengeluaran dari gudang dan pengiriman kepada pelanggan. Dokumentasi pelaksanaan penyaluran hendaklah dibuat lengkap sehingga setiap penyerahan obat dapat dipertanggung jawabkan setiap saat dilakukan pemeriksaan dan evaluasi.Informasi yang harus ada pada dokumen penyaluran obat paling sedikit adalah meliputi: tanggal penyaluran, nama dan alamat tujuan, informasi identitas produk nama, bentuk sediaan, kekuatan, jumlah dan kualitas produk, nomor batch dan expired date, transportasi yang sesuai dan kondisi penyimpanan (Badan Pengawasan Obat dan Makanan RI, 2007).
1. Penerimaan pesanan.
D-6 dan diterbitkan faktur penjualan yang ditandatangani oleh penanggung jawab sesuai dengan formulir D-7 (Badan Pengawasan Obat dan Makanan RI, 2007). 2. Pengeluaran obat dari gudang
Kepala gudang hendaknya mengeluarkan obat sesuai faktur atau surat penyerahan barang yang ditandatangani penanggung jawab. Pengemasan obat untuk pengiriman kepada pemesan hendaknya disesuaikan dengan persyaratan yang ditetapkan untuk tiap jenis obat. Data obat yang dikeluarkan dicatat pada kartu gudang sesuai formulir D-8. Data tersebut diatas hendaknya mendapat pengesahan dari kepala gudang dengan membubuhkan parafnya (Badan Pengawasan Obat dan Makanan RI, 2007).
3. Pengiriman kepada pelanggan
e. Penarikan kembali obat
Penarikan kembali (recall) dapat dilakukan atas permintaan produsen atau instruksi intansi pemerintah yang berwenang. Tindakan penarikan kembali hendaklah dilakukan segera setelah diterima permintaan/instruksi untuk penarikan kembali. Pelaksanaan penarikan kembali dilakukan kembali dilakukan atas dasar: permintaan produsen atau interuksi instansi pemerintah yang berwenang. Penanggung jawab memeriksa kartu persediaan untuk meneliti stok, penerimaan dan penyaluran obat dari batch. Obat dimaksud yang ada dalam persediaan segera dipisahkan dari stok persediaan yang lain (Badan Pengawasan Obat dan Makanan RI, 2007). Unit yang menerima obat yang dimaksud segera dihubungi dan diberikan permintaan tertulis untuk menghentikan penyerahan dan pengembalian obat. Obat sisa stok beserta hasil penarikan disimpan terpisah dan dicatat dalam buku penerimaan pengembalian barang. Obat tersebut dikembalikan ke produsen obat yang bersangkutan dan dicatat dalam buku pengembalian barang (World Health Organization, 2005).
f. Penanganan produk kembalian
1. Pengembalian obat ke produsen
Hendaknya dibuat prosedur penanganan pengembalian obat kepada produsen menggunakan surat penyerahan barang untuk setiap pengembalian obat kepada produsen. Dicatat dalam buku pengembalian barang, kartu barang atau sistem komputerisasi terhadap jumlah dan identifikasi obat yang dikembalikan lalu melapor ke institusi yang berwenang.
2. Pemusnahan obat
Obat yang sudah tidak memenuhi syarat sesuai standar yang ditetapkan harus dimusnahkan. Prosedur pemusnahan obat hendaknya dibuat mencakup pencegahan pencemaran di lingkungan dan untuk mencegah jatuhnya obat tersebut di kalangan orang yang tidak berwenang. Obat yang akan dimusnahkan supaya disimpan terpisah dan dibuat daftar yang mencakup jumlah dan identitas produk. Hendaknya dibuat laporan terhadap terhadap obat yang akan dimusnahkan kepada instansi pemerintah yang berwenang. Pemusnahan produk farmasi harus dilakukan harus sesuai dengan ketentuan internasional, nasional dan lokal mengenai persyaratan pembuangan produk tersebut, dan dengan memperhatikan perlindungan lingkungan (World Health Organization, 2010). g. Dokumentasi secara komputerisasi
aktivitasnya dapat dilacak secara spesifik (Tanzania Food And Drugs Authority,, 2010).
5. Inspeksi diri
Tujuan Inspeksi diri adalah untuk melakukan penilaian apakah seluruh aspek distribusi dan pengendalian mutu sarana distribusi memenuhi ketentuan CDOB (Badan POM RI, 2007). Program inspeksi diri hendaklah dirancang untuk mendeteksi kelemahan dalam pelaksanaan CDOB dan untuk menetapkan tindakan perbaikan. Harus ada prosedur tertulis tentang inspeksi diri yang menyatakan keterlibatan seseorang dalam inspeksi diri, frekuensi diadakan inspeksi diri dan kriteria inspeksi diri (Health Sciences Authority, 2010).
D. Keterangan Empiris
35 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian mengenai cara distribusi obat yang baik pada pedagang besar farmasi di Provinsi Bangka-Belitung merupakan jenis penelitian non eksperimental dengan rancangan penelitian deskriptif karena tidak ada intervensi yang diberikan kepada responden.
B. Definisi Operasional
3. Definisi operasional
a. Pedagang Besar Farmasi adalah suatu perusahaan yang mempunyai ijin untuk mendistribusikan sediaan farmasi di Provinsi Bangka-Belitung. b. Cara Distribusi Obat yang Baik (CDOB) adalah suatu pedoman yang
digunakan dalam proses distribusi penyaluran obat dan/atau bahan obat di fasilitas distribusi yaitu Pedagang Besar Farmasi (PBF) berdasarkan Keputusan Kepala Badan Pengawas Obat dan Makanan Nomor : HK.00.05.3.2522 Tahun 2003.
C. Instrumen Evaluasi
Instrumen penelitian digunakan dalam penelitian adalah kuesioner (daftar pertanyaan). Total kuesioner terdiri dari 49 pertanyaan yang meliputi :
1. Data demografi responden terdiri dari 4 pertanyaan semi terbuka meliputi : Usia, pendidikan terakhir, lama bekerja, jenis sediaan yang dikelola PBF.
2. Pertanyaan tentang manajemen mutu sebanyak 2 pertanyaan tertutup no: 5, 7 dan 2 pertanyaan semi terbuka no: 6, 8.
3. Pertanyaan tentang personalia sebanyak 2 pertanyaan tertutup no: 9, 15 dan 10 buah pertanyaan semi terbuka no: 11, 12, 13, 14, 16, 17, 18.
4. Pertanyaan tentang bangunan dan peralatan sebanyak 7 pertanyaan tertutup no: 20, 22, 23, 24, 27, 30, 32, dan 8 buah pertanyaan semi terbuka no: 19, 21, 25, 26, 28, 29, 31, 33.
5. Pertanyaan tentang dokumentasi sebanyak 1 buah pertanyaan tertutup no: 40 dan 6 buah pertanyaan semi terbuka no: 35, 36, 37, 38, 39, 41. 6. Pertanyaan tentang inspeksi diri sebanyak 1 buah pertanyaan tertutup
D. Subjek Penelitian
Subjek penelitian adalah semua pedagang besar farmasi yang berada di Provinsi Bangka-Belitung. Kriteria inklusinya adalah penanggung jawab PBF yang bersedia mengisi kuesioner dan kriteria eksklusi adalah penanggung jawab yang tidak bersedia mengisi kuesioner.
E. Tata Cara Penelitian
1. Studi pustaka
Penelitian ini dimulai dengan membaca peraturan perundang-undangan yang berhubungan dengan pengaturan kebijakan Pedagang Besar Farmasi, fungsi dan tanggung jawab apoteker, pendistribusian sediaan farmasi, pedoman CDOB yang diatur oleh Keputusan Kepala Badan Pengawas Obat dan Makanan Nomor : HK.00.05.3.2522 Tahun 2003. Peneliti melakukan studi pustaka untuk memperoleh cara pembuatan kuesioner yang baik, metode penelitian dan perhitungan yang digunakan dalam penelitian ini.
2. Pembuatan instrumen penelitian
a. Uji validitas
b. Uji pemahaman bahasa
Uji pemahaman bahasa dilakukan supaya kuesioner yang dibuat dapat dipahami oleh responden atau tidak. Uji pemahaman bahasa dalam kuesioner dilakukan kepada seorang apoteker penangggung jawab yang bekerja di luar Provinsi Bangka-Belitung yakni apoteker yang bekerja di distributor PBF PT.X di Palembang, yang kemudian mengoreksi bahasa dari kuesioner tersebut apakah mudah dipahami atau tidak.
c. Uji reliabilitas
Uji realibilitas ditujukan sejauh mana suatu alat pengukur dapat dipercaya atau dapat diandalkan. Uji reabilitas dalam penelitian ini tidak dilakukan, karena pertanyaan kuesioner yang dibuat oleh peneliti adalah pertanyaan yang bersifat semi terbuka sehingga tidak bisa dilakukan coding untuk membuat penilaian. 3. Pengambilan data
Proses pengambilan data dilakukan dengan door to door membawa kuisioner ke Pedagang Besar Farmasi di Provinsi Bangka-Belitung. Peneliti menyampaikan kuisioner kepada penanggung jawab (responden) Pedagang Besar Farmasi dan menjelaskan tata cara pengisian Quisioner. Pengisian kuisioner dilakukan sendiri oleh responden saat itu di tempat penelitian. Selama proses pengisian, responden didampingi oleh peneliti sekaligus diwawancarai. 4. Pengolahan data
a. Data kuantitatif
responden. Langkah awal adalah membuat tabel hasil kuesioner yang telah diisi oleh penanggung jawab PBF, kemudian memaparkan jumlah dan persentase pada setiap parameter yang diteliti.
b. Data kualitatif
Data kualitatif diperoleh dari setiap jawaban wawancara sebagai data pendukung kepada sebelas penanggung jawab PBF Bangka Belitung. Seluruh jawaban dari responden disimpulkan oleh peneliti yang mencakup lima aspek CDOB dan aspek status penanggung jawab PBF sebagai data pendukung metode kuesioner. Data tersebut diperoleh dari seluruh materi pertanyaan yang diajukan dari metode wawancara mendalam.
F. Waktu dan Tempat Penelitian
Proses pengambilan data dilakukan oleh peneliti pada pedagang besar farmasi di Provinsi Bangka-Belitung.
G. Analisis Data
40 BAB IV
HASIL DAN PEMBAHASAN
Pelaksanaan CDOB pada PBF di Provinsi Bangka- Belitung
Peran tenaga kefarmasian di PBF ialah mengelola proses distribusi sediaan farmasi. Distribusi sediaan farmasi di PBF Provinsi Bangka-Belitung dilakukan oleh sebelas PBF dimana ada duabelas item sediaan farmasi yang didistribusikan yaitu: obat bebas, obat bebas terbatas, obat keras, narkotika, kosmetika, psikotropika, vaksin, makanan, susu, makanan bayi, minuman dan alkes. PT. A hanya 2 item sediaan farmasi saja yakni: obat bebas dan minuman, PT. B mengelola 4 item sediaan farmasi yakni: obat bebas, obat bebas terbatas, obat keras, psikotropika, PT. C mengelola 4 item sediaan farmasi yakni: obat bebas, obat bebas terbatas, kosmetika dan makanan, PT. D mengelola 9 item
sediaan farmasi yakni: obat bebas, obat bebas terbatas, obat keras, kosmetika, psikotropika, vaksin, susu, makanan bayi dan alkes, sedangkan PBF yang mengelola 3 item sediaan farmasi yang sama yakni: obat bebas, obat bebas terbatas dan obat keras terdiri dari tiga PT yaitu: PT. E, PT. F dan PT. G. Sementara itu PT. H mengelola 5 item sediaan farmasi yakni: obat bebas, obat bebas terbatas, obat keras, psikotropika dan vaksin, PT. I mengelola 3 item sediaan farmasi yakni: obat bebas, obat bebas terbatas dan kosmetika, PT. J mengelola 7 item sediaan farmasi yakni: obat bebas, obat bebas terbatas, obat keras, narkotika, kosmetika psikotropika dan vaksin, PT. K mengelola 5 item
Tabel III. Perbandingan jumlah jenis sediaan farmasi yang dikelola masing-masing PBF di Provinsi Bangka-Belitung
No Nama
PBF Jenis sediaan yang dikelola O B O BT O K N A R K O S
PSI VAK
M K N
SUSU MKN
BAYI alkes
MIN UM AN
Total item
1 PT. A - - - - - - - - - - 2
2 PT. B - - - - - - - - 4
3 PT. C - - - - - - - - 4
4 PT. D - - - 9
5 PT. E - - - - - - - - - 3
6 PT. F - - - - - - - - - 3
7 PT. G - - - - - - - - - 3
8 PT. H - - - - - - - 5
9 PT. I - - - - - - - - - 3
10 PT. J - - - - - 7
11 PT. K - - - - - - 5
Menurut Keputusan Menteri Kesehatan Republik Indonesia Nomor:199/MENKES/SK/III/1996, pedagang besar farmasi yang melaksanakan impor, produksi, dan distribusi narkotika di Indonesia hanya PT. Kimia Farma saja, sehingga tidak ada PBF lain selain PT. Kimia Farma yang mengelola narkotika. Menurut pasal 15 UU nomor 35 tahun 2009 tentang Narkotika dikatakan bahwa menteri memberi izin kepada 1 (satu) perusahaan pedagang besar farmasi milik negara yang telah memiliki izin sebagai importir sesuai dengan peraturan perundang-undangan untuk melaksanakan impor narkotika.
Pelaksanaan CDOB di Bangka-Belitung akan dievaluasi berdasarkan aspek:
1. Manajemen mutu
tempat penyimpanan, SOP pembersihan dan perawatan bangunan, SOP pencatatan produk kembali dimana SOP tersebut yang dapat mempengaruhi kualitas produk atau aktifitas distribusi. Dari sebelas PBF di Provinsi Bangka-Belitung yang memenuhi lima SOP tersebut ada delapan PBF yakni: PT. B, PT. D, PT.E, PT.F, PT.G, PT.H, PT.I, PT.J.
PT. A memiliki enam SOP antara lain: SOP CDOB, SOP penerimaan barang, SOP pengiriman barang, SOP pembersihan dan perawatan bangunan, SOP pencatatan produk kembali, SOP pemusnahan. PT.A tidak memiliki SOP pertolongan pertama dalam keadaan darurat dengan alasan “ tidak tahu, kalau
SOP itu harus diterapkan di PBF kami”. PT.A juga tidak memiliki SOP tempat penyimpanan dengan alasan “kurang begitu tahu, setahu saya di sini kebanyakan
mendistribusikan minuman seperti pocari sweet, bir bintang sehingga SOP tempat penyimpanan mungkin tidak dibutuhkan” sedangkan untuk SOP pengontrolan
penanggung jawab pusat dan cabang untuk melakukan penerapan cara distribusi obat yang baik” dan juga hasil wawancara terhadap PT.C tentang tidak adanya SOP pembersihan dan perawatan bangunan dengan alasan “ Apoteker pusat kami
belum berperan, sehingga tidak adanya komunikasi antar penanggung jawab pusat sama cabang untuk membuat SOP pembersihan dan perawatan bangunan”
sedangkan untuk SOP pengontrolan transportasi vaksin tidak memiliki dikarenakan tidak mendistribusikan vaksin.
PT. E memiliki tujuh SOP yakni: SOP CDOB, SOP penerimaan barang, SOP pengiriman barang, SOP tempat penyimpanan, SOP pembersihan dan perawatan bangunan, SOP pencatatan produk kembali, SOP pemusnahan obat. PT.E tidak memiliki SOP pertolongan pertama dalam keadaaan darurat dengan alasan “belum perlu dibuat karena kebijakan perusahaan SOP utama dalam
pendistribusian obat yang penting” sedangkan tidak adanya SOP pengontrolan transportasi vaksin dikarenakan PT.E tidak mendistribusikan vaksin. PT.F memiliki tujuh SOP yakni: SOP CDOB, SOP penerimaan barang, SOP pengiriman barang, SOP tempat penyimpanan, SOP pembersihan dan perawatan bangunan, SOP pencatatan produk kembali, SOP pemusnahan obat. PT.F tidak memiliki SOP pertolongan pertama dalam keadaaan darurat dengan alasan “belum
menjadi prioritas utama yang menjadi prioritas adalah SOP yang dapat mempengaruhi kualitas produk” sedangkan tidak adanya SOP pengontrolan
transportasi vaksin dikarenakan PT.E tidak mendistribusikan vaksin.
SOP tempat penyimpanan, SOP pembersihan dan perawatan bangunan, SOP pencatatan produk kembali, SOP pemusnahan obat sedangkan tidak adanya SOP pengontrolan transportasi vaksin dikarenakan PT.G tidak mendistribusikan vaksin. PT. I memiliki enam SOP yakni: SOP penerimaan barang, SOP pengiriman barang, SOP tempat penyimpanan, SOP pembersihan dan perawatan bangunan, SOP pencatatan produk kembali, SOP pemusnahan obat. PT.I tidak mempunyai SOP CDOB dengan alasan” belum begitu tahu kalau SOP CDOB dibutuhkan,
sedangkan untuk memulai membuat kurang mengerti”. PT.I juga tidak memiliki
SOP pertolongan pertama dalam keadaaan darurat dengan alasan “belum dibutuhkan, tapi saya kurang begitu tahu tentang SOP dan menjalankan SOP yang telah ada saja” sedangkan tidak adanya SOP pengontrolan transportasi vaksin
dikarenakan PT.I tidak mendistribusikan vaksin. PT.J memiliki delapan SOP yakni: SOP CDOB, SOP penerimaan barang, SOP pengiriman barang, SOP tempat penyimpanan, SOP pembersihan dan perawatan bangunan, SOP pencatatan produk kembali, SOP pemusnahan obat, SOP pengontrolan vaksin. PT. J tidak memiliki SOP pertolongan pertama dalam keadaaan darurat dengan alasan “belum dibuat, PBF tidak sama di industri yang SOPnya lengkap sedangkan untuk
SOP ini tahun ini belum menjadi prioritas yang prioritas hanya khusus untuk obat-obatan saja”. PT. K memiliki enam SOP yakni: SOP CDOB, SOP penerimaan
dikarenakan “ belum diperlukan karena dilapangan belum pernah terdapat
pengembaliaan produk kembali sehingga tidak perlu dibuat SOP nya”. PT.I tidak
[image:65.595.71.517.154.677.2]memiliki SOP pengontrolan transportasi vaksin dikarenakan PT.I tidak mendistribusikan vaksin.
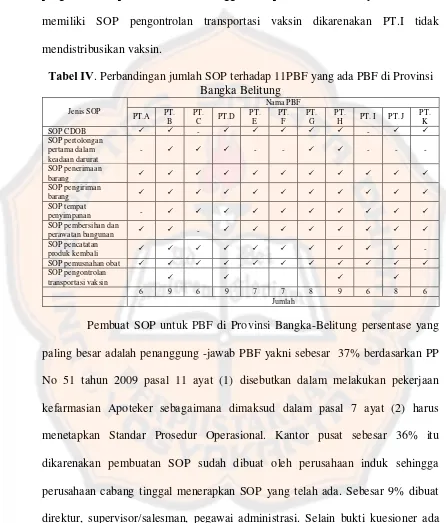
Tabel IV. Perbandingan jumlah SOP terhadap 11PBF yang ada PBF di Provinsi Bangka Belitung
Jenis SOP
Nama PBF
PT.A PT.
B PT.
C PT.D
PT. E PT. F PT. G PT.
H PT. I PT. J
PT. K
SOP CDOB - -
SOP pertolongan pertama dalam keadaan darurat
- - - - - -
SOP penerimaan
barang
SOP pengiriman
barang
SOP tempat
penyimpanan -
SOP pembersihan dan
perawatan bangunan -
SOP pencatatan
produk kembali -
SOP pemusnahan obat
SOP pengontrolan
transportasi vaksin
6 9 6 9 7 7 8 9 6 8 6
Jumlah
sebelas penanggung jawab farmasi sehingga dapat diketahui bahwa sebelas PBF memang memiliki SOP dan melaksanakan SOP tersebut, berdasarkan pendapat umum dari kesebelas penanggung jawab isi SOP memuat antara lain judul protap, nomor, dokumen, revisi, jumlah halaman, dokumen acuan, nama dan tanda tangan pembuat protap, nama dan tanda tangan penanggung jawab yang mengesahkan serta uraian suatu proses distribusi meliputi tujuan, ruang lingkup, definisi dan singkatan, diagram, tanggung-jawab, prosedur, pencatatan. Dalam penelitian ini isi dari SOP masing-masing PBF tidak dapat dijabarkan secara mendetail, karena SOP bersifat rahasia dimana tidak bisa diakses oleh pihak luar.
Gambar 4. Perbandingan jumlah Pembuat SOP berdasarkan keahlian di PBF Provinsi Bangka-Belitung
2. Personalia
Struktur organisasi PBF yang baik hendaklah ditunjang dengan pelaksanaan operasional yang baik, yang dalam hal ini dibutuhkan seorang penanggung jawab yang terlibat dalam seluruh proses penyaluran obat untuk mewujudkan tujuan penyimpanan, penyaluran obat, sebagaimana digariskan ketentuan perundang-undangan. Untuk kriteria struktur organisasi mengacu pada undang-undang yang berlaku di Indonesia yakni Peraturan-Pemerintah No.51
Penanggung Jawab PBF
37% Kantor Pusat
36% Pegawai