PELUANG PEMANFAATAN JAMUR NEMATOFAGUS
UNTUK MENGENDALIKAN NEMATODA PARASIT
PADA TANAMAN DAN TERNAK
Ika Mustika1 dan Riza Zainuddin Ahmad2
1Balai Penelitian Tanaman Rempah dan Obat, Jalan Tentara Pelajar No. 3, Bogor 16111 2Balai Penelitian Veteriner, Jalan R.E. Martadinata No. 30, Bogor 16114
ABSTRAK
Penyakit yang disebabkan oleh nematoda parasit pada tanaman dan ternak (ruminansia kecil) di Indonesia sangat merugikan. Pengendalian dengan menggunakan pestisida kimia pada tanaman dan obat cacing pada ternak dapat menimbulkan dampak negatif berupa resistensi obat dan residu dalam jaringan, bila pestisida atau obat cacing tersebut diberikan secara rutin. Penggunaan agen hayati (jamur nematofagus) merupakan salah satu cara pengendalian yang ramah lingkungan dan berpeluang untuk dikembangkan di Indonesia. Mekanisme jamur tersebut dalam membunuh nematoda adalah dengan membentuk jerat, sebagai endoparasit, merusak larva dan telur nematoda, serta membuat toksin. Penelitian pada tanaman lada, nilam, dan jahe serta ternak kambing dan domba telah mendapatkan beberapa isolat jamur nematofagus seperti Arthrobotrys spp., Dactylaria spp., Dactylella spp.,
Catenaria spp., dan Monacrosporium spp. Uji efektivitas secara in vitro dan in vivo menunjukkan bahwa penggunaan Arthrobotrys spp., Dactylaria spp. atau Dactylella spp. mampu menekan populasi nematoda Meloidogyne incognita
dan Radopholus similis pada tanaman lada. Pada tanaman jahe dan nilam, selain menekan populasi nematoda (Meloidogyne spp. dan Pratylenchus brachyurus), jamur nematofagus juga meningkatkan pertumbuhan dan produktivitas tanaman. Pada ternak ruminansia kecil, penggunaan jamur Arthrobotrys oligospora dapat menekan populasi nematoda Haemonchus contortus. Hasil penelitian ini membuka peluang pemanfaatan jamur nematofagus untuk mengendalikan nematoda parasit pada tanaman dan ternak di mana nematoda menjadi masalah.
Kata kunci: Jamur nematofagus, pengendalian nematoda, lada, jahe, nilam, domba, kambing
ABSTRACT
The opportunity of using nematophagous fungi to control parasitic nematodes on plants and livestock Diseases caused by nematode infection on plant and livestock are very harmful in Indonesia. The use of chemical pesticide (nematicide) in plant or anthelmintic in livestock routinely to control nematodes may cause a negative impact such as plant and livestock resistance and residue in plant and livestock tissues. The use of nematophagous fungi as biological agents is one of the eco-friendly control methods and potential to be developed in Indonesia. The mechanism of the fungi in killing nematodes is by making traps, as endoparasites, destroying larvae or eggs by hyphae, or producing toxins. The results of some experiments revealed that several nematophagous fungi namely
Arthrobotrys spp., Dactylaria spp., Dactylella spp., Catenaria spp., and Monacrosporium spp. were found in plant
(black pepper, ginger, and patchouli) and in small ruminants (goat and sheep). The application of Arthrobotrys spp., Dactylaria spp., and Dactylella spp. on black pepper, ginger, and patchouli were able to reduce nematode population (Meloidogyne incognita, Radopholus similis, and Pratylenchus brachyurus), and increase plant growth and productivity. The use of Arthrobotrys oligospora in small ruminants was able to reduce nematode (Haemonchus
contortus) population. The results gave the opportunity to develop biological control of nematodes attacking
plants and livestock by using nematophagous fungi.
Keywords: Nematophagous fungi, nematode control, Piper nigrum, Zingiber officinale, Pogostemon cablin,
goats, sheep
N
ematoda merupakan salah satu masalah baik pada tanaman maupun ternak. Nematoda yang menyerang tanaman sudah banyak dilaporkan terdapat di Indonesia, di antaranya adalahnematoda buncak akar (Meloidogyne
incognita, M. javanica, M. hapla, dan M. arenaria), nematoda pelubang akar
(Radopholus similis), dan nematoda luka akar (Pratylenchus brachyurus, P.
penetrans). Nematoda yang menginfeksi
ternak antara lain adalah Bunostomum spp., Cooperia spp., Haemonchus spp.,
Mesistorcirrus spp., Oesophagosomum
Tricho-strongyloides spp. (Suhardono et al. 1995;
Beriajaya dan Copeman 1996).
Di Indonesia, cara pengendalian nematoda pada tanaman dan ternak dengan menggunakan agen hayati (jamur nematofagus) sudah banyak dilakukan, bahkan sudah sampai pada tahap aplikasi, karena cara tersebut cukup efektif dan aman baik terhadap manusia maupun ternak. Ditinjau dari segi keamanan lingkungan, pengendalian nematoda dengan menggunakan agen hayati (jamur atau bakteri) merupakan alternatif pilihan yang lebih baik dibandingkan dengan cara konvensional yang menggunakan pes-tisida kimia. Beberapa jamur yang potensial untuk digunakan sebagai agen pengendali hayati, baik terhadap nema-toda parasit tanaman maupun ternak, adalah Arthrobotrys spp., Catenaria spp.,
Dactylella spp., dan Verticillium spp.
(Barron 1977; Nazarudin dan Mustika 1996; Nazarudin 1997; Ahmad 2001).
Tulisan ini bertujuan untuk meng-ungkapkan peluang pemanfaatan jamur nematofagus sebagai agen pengendali hayati nematoda parasit pada tanaman dan ternak, khususnya ruminansia kecil. Diharapkan dengan memanfaatkan jamur nematofagus tersebut, penggunaan in-sekstisida kimia pada tanaman dan obat cacing pada ternak dapat dikurangi sehingga bahaya keracunan bahan kimia dapat dihindarkan.
MASALAH NEMATODA
PARASIT PADA TANAMAN
DAN TERNAK
Nematoda Parasit pada
Tanaman
Nematoda merupakan salah satu jenis Organisme Pengganggu Tumbuhan (OPT) penting yang menyerang berbagai jenis tanaman utama di Indonesia dan negara-negara tropis lainnya. Kehilangan hasil akibat serangan nematoda pada tanaman di seluruh dunia mencapai US$ 80 miliar/tahun (Price 2000). Di In-donesia, nematoda parasit dilaporkan terdapat pada berbagai jenis tanaman, baik tanaman pangan, hortikultura maupun perkebunan (Puskara 2000). Serangan nematoda dapat menurunkan produksi sayuran sebesar 27% pada tomat, 15% pada kentang, dan 20% pada buncis (Hadisoeganda 1991), dan pada
jahe sekitar 65% (Mustika 1995). Pada tanaman lada, serangan nematoda dapat menimbulkan kerusakan sekitar 32% (Sitepu dan Mustika 2000) dan pada tanaman nilam 45% (Mustika dan Nazarudin 1999).
Nematoda parasit tanaman, selain berperan langsung sebagai patogen penyebab penyakit, juga sebagai or-ganisme yang membuat tanaman lebih mudah terserang (predispose) patogen lainnya seperti cendawan, bakteri atau virus. Gejala penyakit akibat serangan nematoda pada tanaman dapat dilihat pada akar, batang, umbi, dan daun. Ke-rusakan akar akibat serangan nematoda dapat menurunkan efisiensi akar dalam menyerap air dan unsur hara. Oleh karena itu, gejala umum serangan nematoda hampir sama dengan gejala kekurangan hara seperti daun menguning, per-tumbuhan terhambat, dan tanaman tidak tahan terhadap cekaman lingkungan.
Beberapa jenis nematoda parasit yang menyerang tanaman di Indonesia disajikan pada Tabel 1. Di antara jenis nematoda tersebut, Meloidogyne spp. (M. graminicola, M. hapla, M. incognita, dan M. javanica), Pratylenchus spp. (P. brachyurus dan P. coffeae), R. similis, dan Globodera rostochiensis merupakan nematoda yang paling merusak. Saat ini pengendalian nematoda parasit masih dilakukan dengan menggunakan pestisida (nematisida) kimia. Pengguna-an bahPengguna-an kimia secara terus-menerus dalam pengendalian nematoda dapat menyebabkan pencemaran lingkungan, resurjensi dan resistensi nematoda, serta terbunuhnya musuh alami yang mempunyai peranan dalam menjaga keseimbangan hayati. Meskipun de-mikian, karena pestisida kimia masih dianggap sebagai cara yang paling efektif dalam mengendalikan nematoda, pemanfaatan jamur nematofagus di lapangan masih sangat terbatas.
Nematoda Parasit pada Ternak
Cacingan (nematodiasis) pada ternak ruminansia merupakan salah satu masa-lah cukup penting di Indonesia, karena penyakit tersebut dapat menurunkan pertumbuhan ternak bahkan pada serangan yang berat dapat mematikan (Beriajaya et al. 1995). Di Indonesia, nematodiasis bersifat endemis, dengan rata-rata prevalensi di Indramayu (Jawa Barat) sebesar 67% (Kusumamihardja danZalizar 1992). Pada tahun 1981−1988, penyakit ini dilaporkan terdapat di daerah Aceh Besar, Lampung, Jawa Timur (Surabaya), Yogyakarta, Bogor, dan Bali dengan prevalensi 45−92% (Suweta 1989). Nematodiasis atau disebut juga haemonchiasis menyebabkan penurun-an bobot badpenurun-an, diare dpenurun-an kekuruspenurun-an (Soulsby 1986). Rachmat et al. (1998) melaporkan bahwa kerugian ekonomi akibat nematoda parasit pada kambing diperkirakan mencapai Rp7 miliar/tahun. Beberapa jenis nematoda parasit dapat menyebabkan cacingan pada domba, kambing, dan sapi (Suhardono et al. 1995; Beriajaya dan Copeman 1996), seperti disajikan pada Tabel 2.
Di antara nematoda parasit pada ternak, Haemonchus contortus merupa-kan salah satu jenis nematoda terpenting pada ruminansia kecil (domba dan kambing). Nematoda ini hidup di dalam abomasum domba dan kambing. Dalam siklus hidupnya, larva stadium 3 me-rupakan larva infektif. Siklus hidup nematoda tersebut terdiri atas prainfektif, infektif, pradewasa, dan dewasa. Dimulai dengan telur yang keluar bersama tinja oleh inang. Pada suhu, kelembapan dan curah hujan yang cocok, telur kemudian menetas menjadi larva stadium 1 dan 2 yang merupakan larva prainfektif. Larva tersebut kemudian berkembang menjadi larva stadium 3 yang infektif, dan dapat bergerak aktif dalam 4−6 hari, kemudian naik ke rerumputan atau batang semak. Bila rumput tersebut dimakan kambing atau domba, maka larva ikut termakan oleh ternak dan menjadi patogenik bila dapat hidup di dalam inang. Di dalam inang, larva stadium 3 yang infektif akan berkembang dan tumbuh menjadi larva stadium 4 (pradewasa), kemudian ber-kembang menjadi dewasa yang siap bertelur pada hari ke-15 sampai ke-20 setelah infeksi (Urquhart et al. 1987).
Pengendalian penyakit cacing pada ternak umumnya dilakukan dengan meng-gunakan obat cacing (antelmintik), di antaranya adalah benzimidazol, levamisol, dan ivermectin (Haryuningtyas dan Beriajaya 2002). Penggunaan obat cacing secara terus-menerus dalam jangka waktu yang lama dapat menimbulkan resistensi, sehingga nematoda jenis baru akan lebih tahan terhadap pengobatan selanjutnya (Hashmi dan Connan 1989), dan adanya residu akibat akumulasi di dalam jaringan tubuh inang (Gronvold et al. 1996). Oleh karena itu, pengendalian nematoda pada
tanaman dan ternak dengan menggunakan jamur nematofagus merupakan suatu pilihan yang tepat dan perlu dilakukan.
JAMUR NEMATOFAGUS
Habitat
Jamur nematofagus adalah salah satu kelompok jamur antagonis terhadap
nematoda baik pada tanaman maupun ternak. Jamur tersebut merupakan peng-huni tanah yang umum terdapat pada berbagai habitat dan jenis tanah, serta dapat ditemukan pada daerah tropis dan subtropis. Jamur nematofagus cukup banyak jenisnya dan menurut Barron (1977) terdapat lebih dari 150 spesies.
Secara umum jamur nematofagus tumbuh pada suhu 20−30o C, kelembapan
90%, pH sedikit asam bergantung pada
spesies, memerlukan oksigen dan sedikit mineral. Sebagai contoh, jamur jenis pembuat perangkap Arthrobotrys
oligo-spora mempunyai suhu pertumbuhan
optimal 25o C dan pH 5−6, kelembapan
90%, dan kadar oksigen murni 100% atau normal 21% untuk dapat memben-tuk perangkap secara optimal (Barron 1977; Gronvold et al. 1987; 1989). Jamur endoparasit umumnya tumbuh lambat, sedangkan jamur pembuat perangkap atau penjerat tumbuh lebih cepat (Waller
et al. 1994; Persmark 1997). Jamur jenis
ini mempunyai kemampuan mengendali-kan pertumbuhan nematoda dengan cara sebagai predator, endoparasit, dan pembuat toksin. Jamur nematofagus merupakan jamur tanah, tumbuh pada iklim sedang, hidup sebagai saprofit, banyak ditemukan pada daun-daunan, sampah, kotoran ternak, tinja, dan kompos pertanian (Gronvold et al. 1985; 1987; Larsen et al. 1991).
Mekanisme Infeksi
Peranan jamur nematofagus dalam mengendalikan nematoda adalah sebagai predator larva dan telur, endoparasit pada larva, dan penghasil toksin. Jamur tersebut membunuh nematoda dengan cara membuat perangkap larva infektif, menjadi endoparasit pada larva, melaku-kan penetrasi pada larva betina dan telur, serta membunuh larva dengan toksin-nya. Mekanisme jamur nematofagus dalam menginfeksi nematoda parasit tanaman dan hewan disajikan pada Tabel 3 dan 4.
Jamur predator seperti A.
oligo-spora membuat perangkap atau penjerat
pada saat larva bergerak mengenai hifa. Jamur tersebut mengeluarkan sekresi
Tabel 1. Nematoda parasit yang terdapat di Indonesia dan tanaman yang diserang serta lokasi ditemukannya.
Jenis nematoda Tanaman Lokasi ditemukan
terserang
Ditylenchus angustus Padi Sumatera, Jawa, Kalimantan Selatan
D. dipsaci Bawang putih Jawa Tengah, Jawa Timur
Globodera rostochiensis Kentang Jawa, Sumatera Utara
Helicotylenchus caudatus Padi Sumatera, Jawa, Kalimantan Selatan
H. dihystera Cengkeh Sumatera Selatan, Sumatera Barat
H. erythrinae Cengkeh Sumatera Selatan, Sumatera Barat
H. multicinctus Lada Sumatera Selatan
Pisang Sumatera Barat
Heterodera glycine Kedelai Jawa, Lampung
Hirschmaniella oryzae Padi Jawa, Sumatera, Kalimantan Selatan
Meloidogyme graminicola Padi Jawa Tengah
M. hapla Pyrethrum Jawa Barat
Kentang Jawa Barat
M. incognita Lada Jawa, Sumatera Selatan, Lampung
Nilam Jawa, Sumatera Barat
Tomat Jawa
Tembakau Indonesia
Tebu Jawa Timur
Cengkeh Sumatera Selatan, Sumatera Barat Kopi Jawa, Bali, Kalimantan Barat
M. javanica Lada Jawa, Sumatera Selatan, Kalimantan Barat
Nilam Jawa
Tembakau Indonesia
Temu lawak Jawa Barat
Jahe Jawa, Bengkulu, Sumatera Utara
Kapulaga Jawa Barat
Kenaf Indonesia
Pratylenchus brachyurus Nilam Jawa Barat, Sumatera Barat, Aceh
P. coffeae Kopi Jawa, Bali, Kalimantan Barat
Lada Babel
Jahe Jawa Barat
P. penetrans Kentang Sumatera, Jawa, Bali
Radopholus similis Lada Babel, Kalimantan Barat
Jahe Jawa Barat, Bengkulu, Sumatera Utara
Nilam Jawa Barat
Teh Jawa Barat
Temu lawak Jawa Barat
Lengkuas Jawa Barat
Kopi Jawa, Bali, Kalimantan Barat
Rotylenchulus reniformis Cengkeh Babel, Sumatera Barat
Tomat Jawa
Kentang Sumatera, Jawa, Bali
Tylenchulus semipenetrans Jeruk Jawa, Bali Sumber: Puskara (2000).
Tabel 2. Nematoda parasit pada ter-nak ruminansia di Indonesia.
Jenis nematoda Ternak yangdiserang
Bunostomum Domba
Cooperia spp. Domba, sapi
Haemonchus spp. Domba, sapi
Mecistocirrus spp. Sapi
Oesophagostomum spp. Domba, sapi
Strongyloides spp. Domba
Trichostronyloides spp. Domba, sapi Sumber: Suhardono et al. (1995); Beriajaya
dan Copeman (1996). .
Pada jamur yang termasuk endo-parasit, benang hifa tidak terbentuk, namun jamur akan membentuk semacam tabung atau konidiospora yang meng-hasilkan spora (Gronvold et al. 1996). Apabila tertelan oleh larva nematoda,, jamur tersebut berkembang biak di dalam tubuh sampai larva mati, contohnya
Harposporium anguillulae. Sementara
itu, Verticillium chlamydosporium membunuh telur nematoda dengan cara benang hifa vegetatif jamur masuk ke dalam alat reproduksi nematoda betina yang telah mati melalui dindingnya dan membunuh telur-telur yang ada di dalamnya. Jamur jenis ini menginfeksi nematoda dengan spora yang punyai perekat. Spora yang tidak mem-punyai perekat akan ditelan atau dicerna oleh nematoda, sedangkan spora yang mempunyai perekat akan melekat masuk ke dalam esofagus. Spora yang mem-punyai perekat juga dapat melekat pada kutikula nematoda, selanjutnya terjadi infeksi pada bagian tersebut. Hampir seluruh siklus hidup jamur endoparasit ini terjadi di dalam tubuh nematoda, misalnya Drechmeria coniospora.
Infeksi pada nematoda betina di-mulai dari interior akar atau secara tidak langsung melalui invasi sel-sel. Contoh-nya, jamur zoospora Catenaria auxiliaris. Sementara itu, infeksi pada telur dila-kukan oleh parasit fakultatif seperti
Verticillium spp. Infeksi terjadi melalui
penetrasi hifa ke dalam kista dan telur (Persmark 1997).
Tabel 3. Jamur nematofagus yang dapat menginfeksi nematoda pada tanaman.
Jenis jamur Mekanisme infeksi
Stylopage hadra Nematoda terperangkap oleh hifa tidak bersepta
Arthrobotrys oligospora Membentuk jaringan bergetah lekat (sticky network)
Dactylaria candida Membentuk cincin dan benjolan adesif, menjerat larva
Dactylaria brochopaga Membentuk cincin yang menjerat larva
Catenaria sp. Zoospora menyerang larva
Ryzocytium humicola Zoospora melekat pada larva
Meristacrum asterospermum Konidia melekat pada kutikula larva
Harposporium angilulae Konidia tertelan larva
Nematoctonus sp. Spora masuk ke dalam tubuh nematoda
Fusarium oxysporum Parasit telur Heterodera schachtii
Verticillium chamidosporium Parasit telur Meloidogyne spp.
Paecilomyces lilacinus Parasit telur Meloidogyne spp.
Nematophthora gynophila Parasit kista Heterodera spp. Sumber: Sayre (1980); Mc Kenry dan Roberts (1985).
perekat yang mengandung zat kemo-atraktan dan enzim pengurai kutikula sehingga larva nematoda melekat, se-lanjutnya terjadi penetrasi pada kutikula (Gronvold et al. 1993). Pada saat itu terbentuk gelembung di dalam tubuh larva, yang selanjutnya jamur akan tumbuh berkembang dalam larva hingga akhirnya larva mati. Pada A. oligospora, jaring perangkap terbentuk dalam keada-an sedikit makkeada-ankeada-an dkeada-an rkeada-angskeada-angkeada-an oleh faktor fisika, kimia atau biologi, seperti larva nematoda (Gronvold et al. 1987).
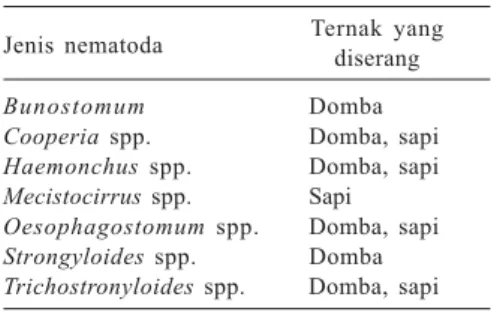
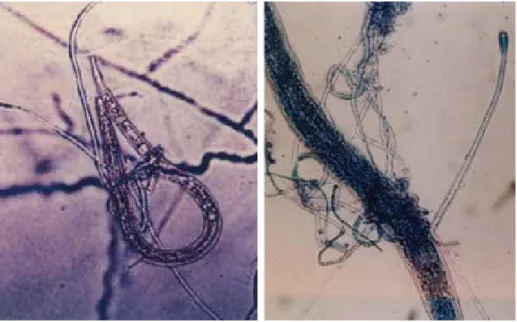
Perangkap yang dibuat dapat berupa perangkap yang sederhana atau kom-pleks, berbentuk cincin (Gambar 1).
Jamur tiram Pleurotus ostreatus dan
Pleurotus pulmonaris membunuh larva Trichostrongyles pada sapi dan larva
cacing tanah dengan cara mengeluarkan nematotoksin (Larsen dan Nansen 1990). Bila jamur tersentuh larva nematoda yang sedang bergerak, maka cacing tersebut akan mati seketika. Toksin tersebut adalah trans-2-decenediocic
acid (Persmark 1997).
Gambar 1. Nematoda parasit tanaman Meloidogyne incognita (kiri) dan nematoda parasit ternak Haemonchus contortus (kanan) yang terperangkap oleh hifa jamur Arthrobotrys sp.
Tabel 4. Jamur nematofagus yang da-pat menginfeksi nematoda pada hewan.
Jenis jamur Mekanisme infeksi
Arthrobotrys spp. Perangkap, toksin
Catenaria spp. Endoparasit
Dactylella spp. Perangkap
Drechmeria spp. Knob
Duddingtonia spp. Perangkap, toksin
Genicularia spp. Knob Harposporium spp. Endoparasit Hohenbuehlia spp. Knob Monacrosporium spp. Perangkap Nematoctonus spp. Knob Pleurotus spp. Toksin Tridentaria spp. Perangkap
Verticillium spp. Merusak telur Sumber: Barron (1977); Waller dan Faedo
PERBANYAKAN JAMUR
NEMATOFAGUS DAN
PEMANFAATANNYA PADA
TANAMAN DAN TERNAK
Penelitian pemanfaatan jamur nema-tofagus di Indonesia dimulai pada tahun 1990an namun berkembang secara per-lahan. Pada tanaman, penelitian dilaku-kan lebih awal (Mustika et al. 1993) dibandingkan pada ternak (Beriajaya dan Ahmad 1999; Ahmad et al. 2001; Beriajaya et al. 2001; Ahmad 2002; Ahmad dan Beriajaya 2002). Pada tanaman, penelitian diarahkan pada penggunaan jamur Arthrobotrys sp., Dactylella sp., dan Dactylaria sp. berdasarkan hasil survei yang dilakukan di Bangka (Babel), Cianjur (Jawa Barat), dan Curup (Beng-kulu) pada tahun 1993 dan 1995, serta potensinya untuk digunakan sebagai agen pengendali nematoda khususnyaMeloidogyne spp. (Nazarudin 1997). Pada
ternak, penelitian diarahkan pada jamur
A. oligospora dan D. flagrans (Waller
dan Larsen 1996), meski pada awalnya terdapat banyak pilihan jenis jamur nematofagus. Namun, sesuai dengan kebutuhan dan kondisi, maka terpilih kedua jamur tersebut.
Sebelum jamur nematofagus di-perbanyak, jamur tersebut harus diisolasi dari tanah, akar atau kotoran ternak. Isolasi jamur di laboratorium dapat meng-gunakan media selektif yang miskin nutrisi agar jamur tumbuh sebagai biakan tunggal (monokultur), selanjutnya larva nematoda ditambahkan sebagai sumber makanannya. Selain itu, untuk mencegah pertumbuhan bakteri diperlukan penam-bahan antibiotik. Semua larva nematoda yang terperangkap akan terbunuh dalam beberapa jam (Nansen et al. 1988). Bila dalam sampel tanah, tinja atau akar terdapat jamur nematofagus, maka jamur ini akan tumbuh dan menginfeksi larva nematoda tersebut dalam media biakan. Selanjutnya biakan jamur diperbanyak dengan menggunakan berbagai media selektif yang diperkaya dengan nutrisi.
Cara Perbanyakan Jamur
Nematofagus
Perbanyakan isolat jamur nematofagus dapat menggunakan berbagai pilihan media, di antaranya potato dextrose agar (PDA), malt agar (MA), yeast malt
agar (YMA), Sabouraud’s glucose agar
(SGA) atau Sabouraud’s dextrose agar (SDA), dan corn malt agar (CMA) (Waller dan Faedo 1993; Waller et al. 1994). Nazarudin (1997) memperbanyak jamur nematofagus (jamur penjerat nematoda) dengan menggunakan beberapa media buatan dan bahan alami seperti PDA,
potato dextrose broth (PDB), EM4,
dedak, dan jagung. Menurut Ahmad (2002), media lokal tepung beras mem-berikan hasil yang lebih baik untuk memperbanyak jamur nematofagus D.
flagrans dan Dactylella spp.
diban-dingkan dengan media jagung, dedak, dan CMA. Selain itu, media lokal harga-nya lebih murah dibanding media impor.
Sebelum diaplikasikan, jamur nema-tofagus diperbanyak dengan meng-gunakan media beras jagung yang dikukus sampai masak, selanjutnya dikemas dalam kantong plastik tahan panas dan disterilkan dalam autoclave pada suhu 1200 C. Setelah dingin, media
diinokulasi dengan potongan biakan agar yang mengandung hifa Arthrobotrys,
Dactylaria, Dactylella atau jamur
nematofagus lainnya. Biakan diinkubasi pada suhu kamar selama 2−3 minggu. Biakan dapat diaplikasikan di lapang bila seluruh media jagung dalam plastik telah tertutup oleh hifa jamur (biakan berwarna putih). Kelemahan cara ini antara lain adalah tidak tahan disimpan lama (tidak stabil), mudah rusak, dan tidak praktis. Untuk mempermudah aplikasi di lapang, dibuat formula antara lain dengan menggunakan kaolin, vermikulit, dan gom arab yang kemudian diproses lebih lanjut menjadi bentuk pelet atau butiran (Harni et al. 2000). Untuk membuat pelet, diperlukan 72 g gom arab, 350 g vermikulit, dan 1.000 g kaolin.
Aplikasi Jamur Nematofagus
pada Tanaman
Beberapa uji pemanfaatan jamur nema-tofagus untuk mengendalikan nematoda pada tanaman telah dilakukan baik di rumah kaca maupun di lapang. Hasil pengujian menunjukkan bahwa aplikasi jamur Arthrobotrys sp., Dactylaria sp., dan Dactylella sp. pada tanaman lada dapat menekan populasi nematoda dan mengurangi penyebaran penyakit kuning yang disebabkan oleh nematoda tersebut. Pada tanaman nilam dan jahe, pengguna-an jamur nematofagus dapat menekpengguna-an populasi nematoda, sehingga produk-tivitas tanaman meningkat.
Pada tanaman lada yang ditanam dalam pot berisi 50 kg tanah, kemudian ditempatkan di lapang dan diinokulasi dengan nematoda Meloidogyne 500 ekor dan R. similis 500 ekor/pot, aplikasi jamur
Arthrobotrys, Dactylaria, dan Dactylella
dalam bentuk biakan jagung sebanyak 150 g/pot/6 bulan dapat meningkatkan pertumbuhan tanaman (tinggi tanaman) dan menekan populasi nematoda (Mus-tika et al. 1997). Penggunaan jamur nematofagus formula butiran dapat menekan populasi M. incognita dan R.
similis pada akar lada berturut-turut
sebesar 59,74−75,79% dan 49,40 – 93,40% (Harni et al. 1999).
Pada tanaman jahe, penggunaan jamur Arthrobotrys, Dactylella, dan
Dactylaria dalam bentuk suspensi
biakan agar sebanyak 125 ml/pot dapat mengurangi populasi nematoda
(Meloi-dogyne spp.) pada akar dan rimpang jahe
berturut-turut sebesar 68,90−70,30% dan 81,84−84,90%. Akibat populasi nematoda rendah, produksi rimpang meningkat berturut-turut sebesar 15,97%, 17,79%, dan 16,98% (Nazarudin dan Mustika 1996). Pada tanaman nilam, penggunaan jamur Arthrobotrys sebanyak 25 g biakan jagung/tanaman/6 bulan dapat menekan populasi nematoda Meloidogyne spp. dan Pratylenchus brachyurus pada akar nilam berturut-turut sebesar 86,84% dan 19,64% serta meningkatkan pro-duksi daun basah 31,32%. Dengan meng-gunakan nematisida kimia (karbofuran), produksi daun basah meningkat 44,93%. Dari penelitian ini terdapat indikasi bahwa jamur Arthrobotrys dapat di-manfaatkan untuk mengurangi peng-gunaan karbofuran (Mustika et al. 2000).
Aplikasi Jamur Nematofagus
pada Kambing dan Domba
Survei terhadap keberadaan jamur nema-tofagus pada kambing dan domba telah dilakukan pada tahun 1995−2000 di Bogor (Jawa Barat), Purworejo, Semarang, dan Kendal (Jawa Tengah), serta Sei Putih (Sumatera Utara). Hasil survei menunjuk-kan bahwa pada tinja (kotoran) ternak dan tanah ditemukan beberapa jenis jamur nematofagus, di antaranya adalah A.oligospora, Verticillium spp., Fusarium
spp., Gliocladium spp., Cephalosporium spp., Paecilomyces spp., Trichoderma spp., Monacrosporium spp., Dactylaria spp., dan Dactylella spp. (Ahmad 1998;
Beriajaya et al. 2001). Beberapa isolat jamur tersebut telah diuji secara in vitro dan in vivo terhadap nematoda yang menyerang kambing dan domba (H.
contortus). Hasil pengujian in vitro
beberapa isolat jamur tersebut di atas terhadap H. contortus menunjukkan bahwa Fusarium poae, Trichoderma spp.,
A. oligospora, dan Duddingtonia flagrans berpotensi untuk digunakan
sebagai pengendali hayati (Ahmad 2001; Dewi 2001; Ahmad dan Beriajaya 2002; Beriajaya dan Ahmad 2002).
Penggunaan jamur A. oligospora di lapang telah dilakukan pada ternak ruminansia kecil untuk mengatasi nematoda parasit H. contortus. Hasil uji pada kambing di Kendal tahun 1999 dan di Bogor pada tahun 2000 tidak mem-perlihatkan hasil yang nyata, namun pada domba di Kendal tahun 1999 dan pada kambing di Sei Putih tahun 2000 memperlihatkan hasil yang sangat nyata. Hasil uji ternyata dipengaruhi oleh berbagai faktor dan yang utama adalah waktu dan dosis pemberian, bila tepat akan terlihat sangat efektif (Beriajaya et
al. 2001).
Secara in vitro, pemberian A.
oligo-spora lebih dari 1.000 konidia/g tinja
kambing yang terinfeksi H. contortus memberi hasil yang baik, artinya jamur dapat digunakan sebagai pengendali hayati. Karena daya tahan hidup jamur di dalam saluran pencernaan cukup rendah, maka dosis yang digunakan harus 2−3 kali lipat.
Pada kambing, pemberian A.
oligo-spora 1 juta konidia/ekor melalui oral
setiap hari selama 2 minggu dapat menurunkan jumlah larva H. contortus dalam tinja sebesar 37,76% dan 19,89% masing-masing pada 14 dan 16 hari setelah pemberian (Beriajaya et al. 2001). Pada domba, pemberian A. oligospora 1 juta spora/ekor dapat mengurangi populasi H.
contortus dalam tinja sebesar 51,80−
63,95% pada 10−12 hari setelah pem-berian (Beriajaya et al. 2001).
Pengelolaan Terpadu Tanaman
dan Ternak
Berdasarkan uraian di atas, dalam upaya meningkatkan pendapatan dan kesejah-teraan petani, pengelolaan tanaman dapat dilakukan secara terpadu dengan ternak. Sistem terpadu tanaman dan ternak ini sangat sesuai untuk diterapkan pada tanaman lada, nilam, jahe atau tanaman lainnya. Melalui introduksi ternak ke dalam sistem pertanaman, kotoran ternak dapat dimanfaatkan secara maksimal untuk meningkatkan kualitas produk tanaman menuju pertanian organik.
Pada lada atau tanaman lainnya dengan jarak tanam yang cukup lebar (2 m x 2 m), ternak kambing atau domba ter-infeksi H. contortus dapat digembalakan secara dilepas, dan diberi makanan yang dicampur dengan jamur nematofagus. Kotoran ternak yang mengandung jamur nematofagus dapat diaplikasikan di sekitar tanaman lada untuk mengendalikan nematoda di dalam tanah. Pada tanaman nilam, jahe atau tanaman lainnya yang berjarak tanam sempit (50 cm x 50 cm),
kambing dan domba tetap dikandang, diberi pakan yang dicampur dengan ja-mur nematofagus, kemudian kotorannya diaplikasikan pada tanaman untuk mengendalikan nematoda pada tanaman tersebut.
KESIMPULAN
Nematoda parasit dapat menyerang tanaman dan ternak sehingga menim-bulkan kerugian. Penggunaan jamur nematofagus dapat mengurangi populasi nematoda baik pada tanaman (lada, jahe, dan nilam) maupun ternak (kambing dan domba). Jamur tersebut merupakan penghuni tanah dan banyak terdapat di berbagai daerah di Indonesia, serta mudah diisolasi dan diperbanyak dengan media buatan dan bahan-bahan alami.
Dalam upaya mengendalikan nema-toda parasit pada tanaman (lada, jahe, dan nilam) dan ternak (kambing dan domba), pemanfaatan jamur nematofagus sebagai pengendali hayati merupakan salah satu alternatif yang sangat poten-sial untuk dikembangkan di Indonesia. Aplikasinya pada tanaman dapat di-lakukan dengan menggunakan biakan jamur tersebut dalam media jagung, beras atau dedak. Aplikasi pada domba dapat dilakukan secara oral dengan men-campur jamur tersebut dengan pakan. Pemanfaatan jamur nematofagus untuk mengendalikan nematoda pada tanaman dan ternak dapat dilakukan melalui sistem pengelolaan terpadu tanaman dan ternak.
DAFTAR PUSTAKA
Ahmad, R.Z. 1998. Penelitian Penanggulangan
Haemonchiasis pada Ternak Domba dengan
Kontrol Biologi. Laporan Penelitian APBN tahun anggaran 1997/1998. Balai Penelitian Veteriner, Bogor.
Ahmad, R.Z. 2001. Isolasi dan Seleksi Kapang Nematofagus untuk Pengendalian
Haemon-chiasis pada Domba. Tesis Program
Pasca-sarjana Institut Pertanian Bogor, Bogor. Ahmad, R.Z., F. Satrija, J. Ridwan, dan M. Larsen.
2001. Isolasi dan identifikasi kandidat kapang nematofagus Arthrobotrys spp., endoparasit, Monacrosporium spp. dari beberapa lokasi di daerah Bogor. Jurnal Mikologi Kedokteran Indonesia 140−144.
Ahmad, R.Z. 2002. Media lokal untuk per-tumbuhan kapang nematofagus sebagai sebuah model. Prosiding Seminar Nasional Teknologi Peternakan dan Veteriner, Ciawi-Bogor, 30 September−1 Oktober 2002. Pu-sat Penelitian dan Pengembangan Peter-nakan, Bogor. hlm. 444−449.
Ahmad, R.Z. dan Beriajaya. 2002. Efek nema-tofagus kapang Fusarium poae isolat lokal terhadap larva 3Haemonchus contortus
secara in vitro. Jurnal Mikologi Kedokteran Indonesia 3(1−2): 9−13.
Barron, G.I. 1977. The nematode destroying fungi. In Tropics in Mycology No.1. Canadian Biological Publication Ltd. Guelph, Ontario, Canada.
Beriajaya, S.E. Estuningsih, Darmono, M.R. Knox, D.R. Stoltz, and A.J. Wilson. 1995. The use of wormolas in controlling gastrointestinal nematode infections in sheep under traditional grazing manage-ment in Indonesia. Jurnal Ilmu Ternak dan Veteriner 1(1): 49−55.
Beriajaya and D.B. Copeman. 1996. Seasonal differences in the effect of nematode parasitism on weight gain of sheep and goats in Cigudeg, West Java. Jurnal Ilmu Ternak dan Veteriner (2): 66−72. Beriajaya dan R.Z. Ahmad. 1999. Kapang
Arthrobotrys oligospora untuk pengendalian
cacing Haemonchus contortus pada domba. Prosiding Seminar Nasional Peternakan dan
Veteriner 1998, Jilid II hlm. 980−985. Pusat Penelitian dan Pengembangan Peternakan, Bogor.
Beriajaya, R.Z. Ahmad, dan E. Kusumaningtyas. 2001. Efikasi kapang nematofagus pada domba dan kambing di daerah Kendal, Jawa Tengah. Prosiding Seminar Peternakan dan Veteriner 2000. Pusat Penelitian dan Pengembangan Peternakan, Bogor. hlm. 498−503.
Beriajaya dan R.Z. Ahmad. 2002. Pengurangan larva cacing Haemonchus contortus oleh konidia kapang Trichoderma sp. secara in
vitro. Prosiding Seminar Nasional Teknologi
Peternakan dan Veteriner, Ciawi-Bogor, 30 September−1 Oktober 2002. Pusat Pe-nelitian dan Pengembangan Peternakan, Bogor. hlm. 398−401.
Dewi, I.P. 2001. Efek dari Gliocladium spp. terhadap Larva 3Haemonchus contortus
secara in vitro. Skripsi Sarjana Biologi, Universitas Nasional, Jakarta.
Gronvold, J., H. Korshollm, J. Wolstrup, P. Nansen, and S.A. Henriksen. 1985. Laboratory experiments to evaluate the ability of Arthrobotrys oligospora to destroy infective larvae Cooperia spesies and to investigate the effect of physical factors on the growth of the fungus. J. Helminthol. (59): 119−125.
Gronvold, J., J. Wolstrup, S.A. Henriksen, and P. Nansen. 1987. Field experiments on the ability of Arthrobotrys oligospora (Hypho-mycetales) to reduce the number of larvae of Cooperia oncophora (Trichostrongy-lidae) in cow pats and surrounding grass. J. Helminthol. 61: 65−71.
Gronvold, J., S.A. Henriksen, P. Nansen, J. Wolstrup, and J. Thylin. 1989. Attemps to control infection with Ostertagia ostertagi (Trichostrongylidae) in grazing calves by adding mycelium of the nematode-trapping fungus Arthrobotrys oligospora (Hyphomy-cetales) to cow pats. J. Helminthol. 63: 115−
126.
Gronvold, J., J. Wolstrup, P. Nansen, S.A. Henriksen, M. Larsen, and J. Bresciani. 1993. Biological control of nematode parasites in cattle with nematode trapping fungi: a survey of Danish studies. Vet. Parasitol. 48: 311−325.
Gronvold, J., S.A. Henriksen, M. Larsen, P. Nansen, and J. Wolstrup. 1996. Biological control aspects of biological control-with special reference to arthropods, protozoans and helminthes of domesticated animals. Vet. Parasitol. 64: 47−64.
Hadisoeganda, A.W. 1991. Pancaran, identifikasi dan prevalensi nematoda bengkok akar di sentra daerah penanaman sayuran dataran tinggi di Indonesia. Buletin Penelitian Hortikultura XX(3): 62−71.
Harni, R., I. Mustika, dan B.N. Susilo. 1999. Kajian teknik informasi jamur pemangsa nematoda untuk pengendalian nematoda penyebab penyakit kuning lada. Laporan
Teknis Penelitian Balai Penelitian Tanaman Rempah dan Obat, Bogor. hlm. 133−140. Harni, R., I. Mustika, dan S.B. Nazarudin. 2000.
Kajian teknik formulasi jamur pemangsa nematoda untuk mengendalikan penyakit kuning lada. Laporan Bagian Proyek Pe-nelitian Tanaman Rempah dan Obat Tahun 1999/2000. Balai Penelitian Tanaman Rem-pah dan Obat, Bogor. hlm. 133−140. Haryuningtyas, D. dan Beriajaya. 2002. Metode
deteksi resistensi terhadap antelmintik pada domba dan kambing. Wartazoa 12(2): 72−
79.
Hashmi, H.A. and R.M. Connan. 1989. Biological control of ruminant Trichostrongylids by
Arthrobotrys oligospora, a predacious
fungus. Parasitol. Today 5(1): 28−30. Kusumamihardja, S. dan L. Zalizar. 1992
Pengaruh musim pada hipobiose
Haemon-chus contortus dan fluktuasi populasi
nematoda saluran pencernaan domba di Indramayu, Jawa Barat. Prosiding Seminar Nasional Hasil Penelitian Perguruan Tinggi. hlm. 171−192.
Larsen, M. and P. Nansen. 1990. Effect of oyster mushroom Pleurotus pulmonarius on preparasitic larvae of bovine Tricho-stronyles. Acta Veterinarian Scandinavia 312: 509−510.
Larsen, M., J. Wolstrup, S.A. Henriksen, C. Dackman, J. Gronvold, and P. Nansen. 1991.
In vitro stress selection of nematophagous
fungi for biocontrol of parasitic nematodes in ruminants. J. Helminthol. 65: 193−200. Mc.Kenry, M.V. and P.A. Roberts. 1985. Phytonematology Study Guide. Cooperation Extension Univ. of California. 56 pp. Mustika, I., A.S. Rachmat, and D. Sudradjat. 1993.
The influence of organic matters on the growth of black pepper, nematode popu-lation and antagonistic microorganism. J. Spice and Medical Crops 11(1): 11−17. Mustika, I. 1995. Serangan nematoda pada
tanaman rempah dan obat. Media Ko-munikasi Penelitian dan Pengembangan Tanaman Industri 15: 28−33.
Mustika, I., B.N. Susilo, dan R. Harni. 1997. kajian teknis aplikasi agensia hayati jamur dan bakteri untuk mengendalikan nematoda pada lada. Laporan Teknis Penelitian. Balai Penelitian Tanaman Rempah dan Obat, Bogor. hlm. 137−143.
Mustika, I. dan S.B. Nazarudin. 1999. Nematoda pada tanaman nilam. Monograf Tanaman Nilam. Balai Penelitian Tanaman Rempah dan Obat, Bogor. hlm. 89−95.
Mustika, I., R.S. Djiwanti, dan R. Harni. 2000. Pengaruh agensia hayati, bahan organik dan pestisida nabati terhadap nematoda tanaman nilam. Laporan Teknis Penelitian Bagian Proyek Penelitian Tanaman Rempah dan Obat Tahun 1999/2000. Buku III. hlm. 85−
91. Balai Penelitian Tanaman Rempah dan Obat, Bogor.
Nansen, P., J. Gronvold, S.A. Henriksen, and J. Wolstrup. 1988. Interactions between the predacious fungus Arthrobotrys oligospora and third-stage larvae of a eries of animal-parasitic nematodes. Vet. Parasitol. 26: 329−
337.
Nazarudin, S.B. dan I. Mustika. 1996. Penggunaan jamur penjerat untuk pengendalian hayati
Meloidogyne spp. pada jahe. Proc. Seminar
on Integrated Control of Main Diseases of Industrial Crops. Bogor, 13−14 March 1996. Research Institute for Spice and Medicinal Crops and Japan International Cooperation Agency. p. 193−197.
Nazarudin, S.B. 1997. Jamur penjerat nematoda dan pemanfaatannya sebagai agensia pe-ngendali hayati nematoda parasit tanaman. Prosiding Kongres Nasional XIV dan Seminar Ilmiah Perhimpunan Fitopatologi Indo-nesia, Palembang 27−29 Oktober 1997. hlm. 202−208.
Persmark, L. 1997. Disertation Ecology of Nematophagous Fungi in Agricultural Soils. Department of Ecology Microbia, Ecology Lund University, Sweden.
Price, T.V. 2000. Plant-parasitic nematodes. Prosiding Pelatihan Nematologi. Jakarta 16−30 Juli 2000. Pusat Karantina Pertanian, Jakarta. hlm. 27−34.
Puskara. 2000. Daftar Organisme Pengganggu Tumbuhan Potensial yang Dilaporkan Telah Terdapat di Dalam Wilayah Republik Indonesia. Puskara, Jakarta. 328 hlm. Rachmat, R., Abd. Rauf, dan M.Z. Kanro. 1998.
Kontribusi getah pepaya dalam pengendalian penyakit cacing pada kambing. Prosiding Seminar Hortikultura. Kerja Sama Fakul-tas Pertanian dan Kehutanan UniversiFakul-tas Hasanuddin dengan Instalasi Penelitian dan Pengkajian Pertanian Jeneponto, Balai Pengkajian Teknologi Pertanian Kendari. hlm. 432−434.
Sayre, R.M. 1980. Promising organisms for biocontrol of nematodes. Plant Dis. 64: 526−
532.
Sitepu, D. and I. Mustika. 2000. Disease of black pepper and their management in Indonesia.
In P.N. Ravindran (Ed.). Black Pepper. Piper nigrum. Medicinal and Aromatic
Plants–Industrial Profiles. Harwood Aca-demic Publishers, Australia, Canada, France, Germany, India, Japan, Luxembourg, Ma-laysia, The Netherland, Russia, Singapore, Switzerland. p. 297−308.
Soulsby, E.J.L. 1986. Helminths, Protozoa and Arthropods of Domesticated Animal. 7th.
Edition. Bailliere Tindall, London. Suweta, I.G.P. 1989. Review on important
helminthic diseases in animal in Indonesia. Buletin Penelitian Kesehatan 17(2): 34−43. Suhardono, S. Partoutomo, dan M.R. Knox. 1995. Pengaruh infeksi cacing nematoda pada sapi perah laktasi di Kabupaten Garut, Jawa Barat. Prosiding Seminar Nasional Teknologi Veteriner. Cisarua Maret 1994.
Balai Penelitian Veteriner, Bogor. hlm. 250−
255.
Urquhart, G.M., J. Armour, J.L. Duncan, A.M. Dunn, and F.W. Jennings. 1987. Veterinary Parasitology. Dept. of Veterinary Parasi-tology, Faculty of Veterinary Medicine, The University of Glasgow, Scotland, Longman Scientific & Technical. Published in USA by Churchill Livingstone Inc., New York.
Waller, P. and M. Faedo. 1993. The potential of nematophagous fungi to control the free-living stages of nematode parasites of sheep: Screening studies. Vet. Parasitol. 49: 285−
297.
Waller, P., M. Larsen, and D.R. Hennessy. 1994. The potential of nematophagous fungi to control the free-living stages of nematode
parasites of sheep: In vitro and in vivo studies. Vet. Parasitol. 51: 289−299.
Waller, P. and M. Larsen. 1996. Workshop summary: Biological control of nematode parasites of livestock. Vet. Parasitol. 64: 135−137.