ISSN 0853-0823
Optimasi Spektrometer Fotoakustik Laser CO
2
dan Aplikasinya
Dalam Pendeteksian Konsentrasi Etilen di Dalam Tanah
Mitrayana1)*, M.A.J. Wasono1) dan Karno1)
1) Lab. Fisika Atom-Inti Jurusan Fisika FMIPA UGM, Yogyakarta, BLS 21 55281 *Email: mitrayana@ugm.ac.id
Abstrak - Telah dilakukan optimasi kinerja spektrometer fotoakustik (SFA) konfigurasi ekstrakavitas bersumberkan laser CO2
pada penentuan batas deteksi terendah (BDT) gas etilen (C2H4). Diperoleh BDT gas etilen sebesar
(
59±7)
ppt. SelanjutnyaSFA digunakan untuk mendeteksi konsentrasi etilen di dalam tanah. Diperoleh konsentrasi etilen di dalam tanah sebesar
(
0,6±0,3)
ppm,(
1,1±0,2)
ppm dan(
2,2±0,5)
ppm, yang secara berurutan untuk daerah selatan, tengah dan utara dari kawasan hutan biologi UGM yang berlokasi di bagian barat gedung biologi dan gedung fisika FMIPA utara UGM. Sementara itu konsentrasi etilen akan semakin membesar ketika kondisi vakum sampel semakin lama.Kata kunci: spektrometer fotoakustik, etilen
I. PENDAHULUAN
Tanah dapat didefinisikan sebagai medium alami untuk pertumbuhan tanaman yang tersusun atas mineral, bahan organik, dan organisme hidup. Bahan-bahan organik tanah terdiri dari sisa-sisa tanaman dan hewan dari semua tahapan dekomposisi karena kerja mikroorganisme tanah [1]. Sparling [2] menyatakan bahwa sejumlah mikroba memegang peranan penting pada tanah yang normal dan sehat, dan merupakan indikator dalam menentukan kualitas tanah.
Etilen diidentifikasi sebagai unsur yang terkandung dalam atmosfer tanah, baik dalam keadaan aerobik maupun anaerobik. Etilen ini dihasilkan oleh aktivitas mikrobia. [3]. Ishii dan Kadoya [4] menduga bahwa etilen dibebaskan oleh aktivitas microbial dan non-microbial, meskipun pembebebasan non-microbial masih diperdebatkan. K. A. Smith dan Restall menduga bahwa sembarang mikroorganisme anaerobik hampir bisa dipastikan menghasilkan etilen di dalam tanah. Produksi etilen terjadi dalam keadaan aerobik maupun anaerobik [3].
Selama ini pengukuran gas etilen (C2H4) yang dihasilkan
oleh sample (cuplikan) biologis dilakukan dengan menggunakan kromatografi gas (GC = Gas Chromatography ) yang dilengkapi dengan detektor ionisasi nyala (FID = Flame Ionization Detector). Cara pengukuran dengan metode GC tersebut mempunyai beberapa kelemahan, masalah kelemahan yang dimiliki oleh pengukuran dengan metode GC tersebut, terpecahkan dengan penggunaan metode baru yaitu metode spektroskopi fotoakustik (FA) laser [5].
Teknik spektoskopi fotoakustik (FA) telah digunakan dalam pendeteksian kelumit, karena menawarkan sensitivitas yang tinggi. Di dalam metode ini, sinar laser energi tinggi digunakan untuk meradiasi bahan yang akan di deteksi. Berkas cahaya akan menghasilkan suatu muai panas (peningkatan suhu) di dalam bahan, yang kemudian membangkitkan suatu gelombang akustik. Ciri-ciri dari gelombang ini tidak hanya ditentukan oleh koefisien serapan optis bahan, juga disebabkan oleh parameter-parameter fisis termal yang berkenaan dengan pemuaian panas, panas jenis dan kecepatan bunyi. gelombang akuistik juga dipengaruhi oleh hamburan optis yang mempengaruhi distribusi cahaya di dalam bahan. Karena itu, sehubungan dengan
spektroskopi serapan optis, teknik FA menawarkan satu derajat sensitivitas yang lebih tinggi [6].
Karena banyaknya kelebihan yang dimiliki oleh spektroskopi fotoakustik laser CO2 ini, banyak para peneliti
mengaplikasikan di berbagai bidang semisal untuk pemantauan lingkungan (di udara ambien, knalpot [pembuangan] mobil dan cerobong emisi gas), pada aplikasi medis dan pada aplikasi biologi (dalam fisiologi pascapanen, fisiologi tanaman, mikrobiologi dan entomologi) [7].
Perbaikan sensitivitas deteksi spektrometer FA telah dilakukan dengan mengoptimasi sel FA resonan yang dikombinasikan dengan sistem gas mengalir untuk kepentingan penelitian di bidang biologi dan pertanian menghasilkan batas deteksi etilen terendah sebesar (0,20 ± 0,02) nl/l pada tekanan 1 atm, lebar pita 1 Hz. Dengan menggunakan spektometer fotoakustik tersebut, etilen yang diemisikan oleh buah-buahan dapat dimonitor secara berketerusan [8]. Spektrometer fotoakustik konvigurasi intrakavitas telah dirancang dan diuji kinerjanya dengan batas detaksi terkecil gas uji adalah (148±16) pptv, (420±40) pptv dan (172±18) pptv, secara berurutan untuk gas etilen, aseton dan amonia. Kemudian spektrometer digunakan untuk mendeteksi konsentrasi ketiga gas biomarker yang diemisikan melalui gas pernapasan yaitu etilen, aseton dan amonia dari berbagai kondisi relawan. Dan telah ditemukan pula korelasi positif antara besar konsentrasi etilen, aseton dan amonia dari emisi pernapasan masing-masing terhadap besar kolestrol total, glukosa puasa dan SGOT dalam darah [8]. Dengan menggunakan kromatografi gas, Arsana dkk. [9] melakukan penelitaian mengamati pengaruh penggenangan dini dan potensi redoks terhadap produksi etilen. Selanjutnya, pada penelitian kali ini akan digunakan metode spektrometer fotoakustik untuk mendeteksi gas etilen di dalam tanah sekaligus menentukan konsentrasinya.
II. METODE EKSPERIMEN
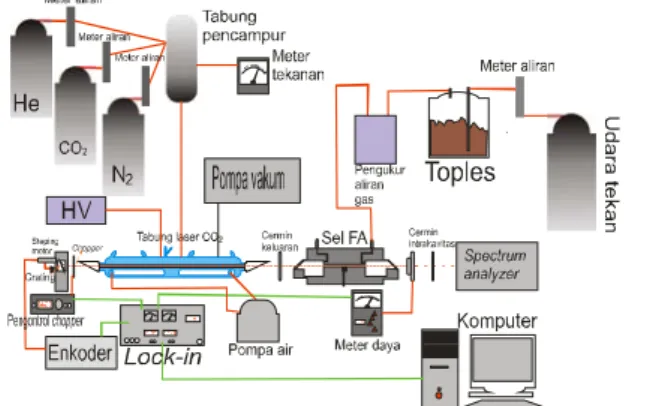
Konfigurasi ekstrakavitas disusun dengan menempatkan sel fotoakustik diluar laser CO2 sebagaimana dalam Gambar
1. konfigurasi ini dipilih karena untuk memudahkan dalam penyetingan rangkainaan, namun jika dibandingkan dengan konfigurasi intrakavitas maka daya laser yang dihasilkan oleh konfigurasi ekstrakavitas lebih kecil. Cuplikan yang
ISSN 0853-0823 akan diselidiki ditempatkan dalam sel fotoakustik dan
dikenai radiasi laser yang dimodulasi oleh chopper. Chopper ditempatkan didekat grating. Hal ini dilakukan untuk mengurangi derau dari chopper sekaligus menghindarkan masuknya sinar laser dari pantulan chopper ke sel fotoakustik.
Gambar 1. Konfiguarasi ekstrakavitas.
Sinyal yang muncul akibat pemanasan cuplikan yang dimodulasi dideteksi dengan mikrofon. Karena sinyal yang muncul sangat kecil maka dikuatkan dengan menggunakan lock-in (lock-in amplifier). Alat ini hanya menguatkan sinyal yang berfrekuensi sama dengan frekuensi referensi yaitu frekuensi choppernya. Karena daya keluaran laser tidaklah sama, maka sinyal dinormalisasi terhadap daya. Hal ini dilakukan dengan mencatat sinyal akustik keluaran lock-in bersamaan dengan daya lasernya yang dioptimasi menggunakan komputerisasi sistem spektroskopi. Konfigurasi eksperimen yang digunakan dalam pendeteksian etilen di dalam tanah ditunjukan dalam Gambar 2
Gambar 2.Konfigurasi eksperimen pendeteksian konsentrasi etilen dalam tanah.
Bahan uji yang digunakan adalah tanah yang diambil dari kawasan hutan biologi yang berlokasi di bagian barat gedung biologi dan MIPA utara UGM. Dari Gambar 2 dapat dilihat bahwa bahan uji yang akan dideteksi diletakan di dalam toples (yang sudah diuji kevakumannya), kemudian di alirkan menuju sel FA dengan cara disentor oleh udara tekan, selanjutnya dialirkan menuju pengukur aliran gas agar laju alirannya stabil, dan diatur pada laju aliran 1 l/j, kemudian dari pengukur aliran gas dilanjutkan dengan mengalirkannya menuju sel FA.
Untuk mendeksi keberadaan etilen di dalam tanah sekaligus menentukan kadar konsentrasinya, bahan uji (sampel tanah) di masukan kedalam toples (volume 1,5 l), tidak terlalu penuh, kurang lebih setengah dari volume toples. Toples yang digunakan sebelumnya diuji dulu tingkat kevakumannya, kemudian toples tersebut ditutup rapat, diusahakan toples tertutup dengan sempurna. Perlakuan untuk sample divariasi menjadi dua yaitu:
1. Untuk mengamati sebaran gas etilen dari beberapa tempat yang berbeda, sampel tanah diambil dari
beberapa tempat yang berbeda (dalam penelitian kali ini daerah/kawasan pengambilan sample dibagi 3 yaitu bagian utara, tengah dan selatan). Untuk masing-masing daerah diambil 3 sampel dari tempat yang berbeda, jadi total sampel ada 9.
2. Untuk mengamati pengaruh lamanya sample dalam keadaan vakum terhadap konsentrasi etilen, sampel diambil dari daerah/kawasan yang memiliki kadar konsentarsi tertinggi, yang didapat dari penelitian sebelumnya. Dan untuk masing-masing sampel di variasi waktunya (lamanya sample dalam keadaan vakum) selama kurang lebih 1 jam untuk masing-masing sampel.
Pendeteksian sinyal fotoakustiknya untuk masing-masing sampel dilakukan pada garis laser yang paling tinggi serapannya yaitu pada garis laser 10P14, frekuensi di mana serapannya tertinggi, dan data disimpan dalam komputer secara otomatis.
III. HASIL DAN PEMBAHASAN
Untuk mendapatkan kinerja spektrometer fotoakustik yang optimal, maka komponen-komponen yang berhubungan langsung dengan aksi laser seperti grating, tabung laser, dan cermin keluaran harus benar-benar lurus. Selanjutnya, optimasi dilakukan dengan cara mengatur komposisi campuran medium aktif, hal ini dilakukan untuk mencari daya tertinggi dengan perbandingan CO2:He:N2
yang tepat. Didapat perbandingan CO2:He:N2 yang berbeda
dalam beberapa waktu penelitian yang berbeda, yang merupakan perbandingan terbaik pada saat itu dimana dayanya tertinggi. Perbandingan CO2:He:N2 yang didapat
adalah 55:20:45, 60:20:50, 60:15:45, dan 50:20:40 didapat daya laser 0,7 W, 0,9 W, 0,6 W, dan 1,6 W sebelum chopper dihidupkan dan 0,3 W, 0,27 W, 0,21 W, dan 0,2 W setelah chopper dihidupkan, secara berurutan.
A. Laser CO2
A.1 Spektrum keluaran
Dari Gambar 3. diperoleh 11 garis laser yang teragih dalam dua cabang (diidentifikasi menggunakan CO2
spectrum analyzer), 7 garis laser pada cabang 10P (10P14, 10P16, 10P18, 10P20, 10P22, 10P24, 10P26) dan 4 garis laser pada cabang 10R (10R26, 10R18, 10R12, 10R8). Hasil ini sudah cukup untuk keperluan dari penelitian ini, yaitu melakukan pengukuran terhadap gas etilen yang memiliki koefisien serapan tertinggi pada garis 10P14.
Gambar 3. Spektrum garis-garis laser CO2 konfigurasi
ISSN 0853-0823 A.2 Kestabilan daya
Kestabilan daya laser yang tampak pada Gambar 4. cukup bagus dan bernilai ≈0,66/menit. Hanya saja tetap daya laser yang didapat masih kurang stabil, oleh karena itu kekurangstabilan daya laser ini diatasi dengan melakukan normalisasi sinyal fotoakustik terhadap daya laser di mana spektrometer beroperasi. 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1,0 Da ya e k stra ka vita s (W a tt ) Waktu (menit)
Gambar 4. Grafik kestabilan daya laser pada garis 10P14.
B. Kurva Resonansi dan Faktor Kualitas
Dari Gambar 5. tampak bahwa frekuensi resonansi untuk gas etilen terjadi pada frekuensi chopper ve =(1620±2) Hz dengan lebar puncak kurvanya (pita resonansinya)
) 4 82
( ±
=
∆v Hz., dan diperoleh nilai
Q
e eksperimen sebesar (20±1). Faktor kualitasQ
menyatakan tingkat kebocoran atau disipsi akustik dan merupakan nisbah antara energi yang disimpan dalam gelombang akustik dengan rugi per siklus yang dialami gelombang tersebut. NilaiQ
yang tidak terlalu tinggi menjamin kestabilan pengukuran terhadap derau dan perubahan frekuensi chopper.1000 1100 1200 1300 1400 1500 1600 1700 1800 1900 2000 -0,1 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1,0 1,1 1572,62 1657,43 Sin y al/ D aya ( m V) Frekuensi Chopper (Hz)
Gambar 5. Kurva resonansi gas etilen pada garis laser 10P14.
C. Spektrum Serapan Gas Kelumit
Dari Gambar 6 diketahui bahwa gas etilen menyerap pada garis 10P12, 10P14, 10P16, 10P18, dan 10P20, dan paling baik menyerap pada garis laser 10P14.
D. Kalibrasi Spektrometer Fotoakustik terhadap Serapan Gas
Kalibrasi dilakukan dengan cara mengalirkan gas etilen 10 ppm, dengan laju aliran 1 l/j, pada garis laser 10P14 dihasilkan sinyal akustik sebesar (44,1±0,5)mV/W (Gambar 7), maka diperoleh hubungan 10ppm ≈ (44,1±0,5) mV/W.
Dari hubungan ini, dan memasukan koefisien absorbs etilen pada garis laser 10P14 sebesarαC2H4 =30,4 atm
-1cm-1, maka
tetapan sel dapat dicari
C FR I
S = α
(tanggap mikrofon R = 7,5 mV/Pa) didapat Feks= 19342,11
Pa cm/W. 0,00 0,50 1,00 1,50 2,00 2,50 3,00 3,50 4,00 10P12 10P14 10P16 10P18 10P20 Si ny al /D ay a (m V /W ) Garis Laser
Gambar 6. Spektrum serapan gas etilen terhadap garis-garis laser CO2. 2400 2600 2800 3000 3200 3400 3600 3800 4000 4200 0,00 0,01 0,02 0,03 0,04 0,05 Sin y al/ D ay a ( V /W ) Waktu (detik)
Gambar 7. Kalibrasi spektrometer fotoakustik terhadap gas etilen 10 ppm pada garis laser 10P14.
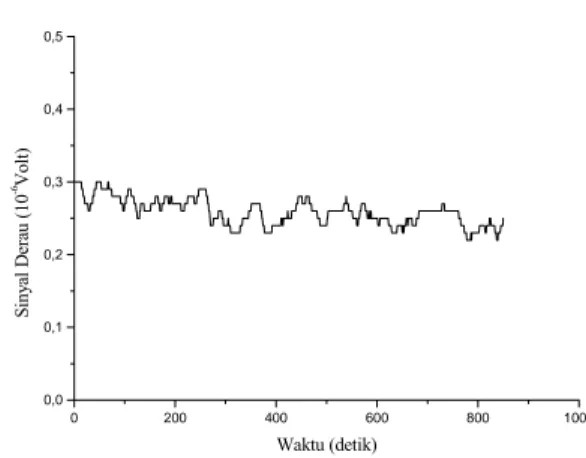
E. Derau dan Batas Deteksi Terendah (BDT)
0 200 400 600 800 1000 0,0 0,1 0,2 0,3 0,4 0,5 Si ny al D erau (10 -6V olt) Waktu (detik)
Gambar 8. Derau sistem spektrometer fotoakustik pada garis laser 10P14.
Dari Gambar 8 diperoleh sinyal derau sebesar (1,8 ± 0,1) µV/Hz1/2. Satuan 1/Hz1/2, kemudian dicari BDT
menggunakan persamaan BDT =
(
C Sn)
N, dengan Ckonsentrasi sampel, Sn sinyal ternormalisasi dan N derau
sistem. Untuk gas etilen 10 ppm didapatkan sinyal ternormalisasi (44,1±0,5) mV/W, maka didapat BDT
ISSN 0853-0823 spektrometer fotoakustik untuk cuplikan gas etilen sebesar
(59 ± 7) ppt. F. Sinyal Latar
Sinyal latar merupakan sinyal fotoakustik yang muncul selain dari hasil serapan sampel seperti akibat pemanasan jendela dan dinding sel dan memiliki nilai fase dan frekuensi yang sama. Dari Gambar 9 diperoleh sinyal latar ternormalisasi untuk garis laser 10P14 sebesar (0,48 ± 0,02) mV/W. 0 200 400 600 800 1000 1200 0 1 2 3 4 5 6 7 8 Si ny al L at ar (1 0 -4V) W aktu (detik)
Gambar 9. Sinyal latar pada garis laser 10P14 dengan daya ekstrakavitas
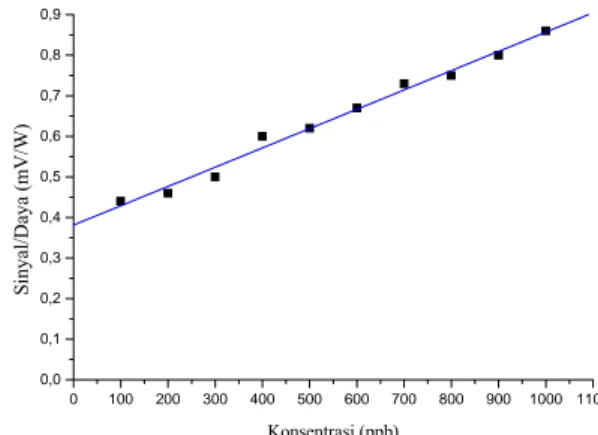
G. Linearitas Gas Kelumit
Linearitas sinyal fotoakustik gas kelumit diperoleh dari hubungan antara sinyal fotoakustik terhadap konsentrasi gas kelumit yang divariasi. Gambar 10 menunjukan kelinearan sistem spektrometer fotoakustik terhadap gas etilen yang ditunjukan dengan nilai r2 =
(
0,99±0,02)
dan P<0,0001. Dari Gambar 10 dapat ditunjukan bahwa semakin besar konsentrasi gas etilen maka sinyal fotoakustik yang dihasilkan oleh serapan gas etilen semakin besar.0 100 200 300 400 500 600 700 800 900 1000 1100 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 Konsentrasi (ppb) Si ny al /D ay a (m V/ W)
Gambar 10. Linearitas sinyal fotoakustik terhadap konsentrasi gas etilen
H. Deteksi dan Penentuan Konsentrasi Etilen di Dalam Tanah
Setelah kinerja spektrometer fotoakustik dalm pendeteksian gas kelumit etilen diketahui, selanjutnya spektrometer digunakan untuk mendeteksi dan menentukan konsentrasi etilen di dalam tanah.
H.1. Konsentrasi etilen di dalam tanah dari tempat yang berbeda (variasi tempat)
Pada penelitian yang pertama akan dideteksi etilen di dalam tanah, di mana sampel tanah diambil di sekitar hutan biologi UGM, yang berada di bagian barat fakultas biologi dan MIPA utara, dan sampel tanah diambil dari bebeapa titik yang berbeda.
0,00 0,50 1,00 1,50 2,00 2,50 3,00
selatan 1 selatan 2 selatan 3 tengah 1 tengah 2 tengah 3 utara 1 utara 2 utara 3
Kon se n tr si e tile n (p p m ) Lokasi pengambilan sampel
Gambar 11. Konsentrasi etilen di dalam tanah dari beberapa tempat yang berbeda.
Dari Gambar 11 dapat diketahui bahwa etilen di dalam tanah dapat dideteksi dan konsentrasinya di setiap tempat berbeda. Berbedanya kadar konsentrasi etilen pada setiap tempat disebabkan karena pada setiap tempat tersebut kandungan bahan-bahan organiknya berbeda-beda. Karena produksi etilen sangat bergantung terhadap bahan-bahan organik juga bergantung pada keberadaan mikroorganisme di dalam tanah. Besarnya konsentrasi etilen di setiap tempat tersebut ditunjukan pada Tabel I.
TABEL I. KONSENTRASI ETILEN DIDALAM TANAH DARI BEBERAPA TEMPAT YANG BERBEDA.
Lokasi pengambilan tanah Konsentrasi (ppm)
selatan 1 0,80 selatan 2 0,32 selatan 3 0,80 tengah 1 0,94 tengah 2 1,28 tengah 3 1,22 utara 1 2,74 utara 2 1,73 utara 3 2,08
Rata-rata konsentrasi etilen dari setiap daerah adalah selatan (0,6±0,3) ppm, tengah
(
1,1±0,2)
ppm dan utara(
2,2±0,5)
ppm.H.2. Pengaruh lamanya keadaan vakum sampel terhadap konsentrasi etilen
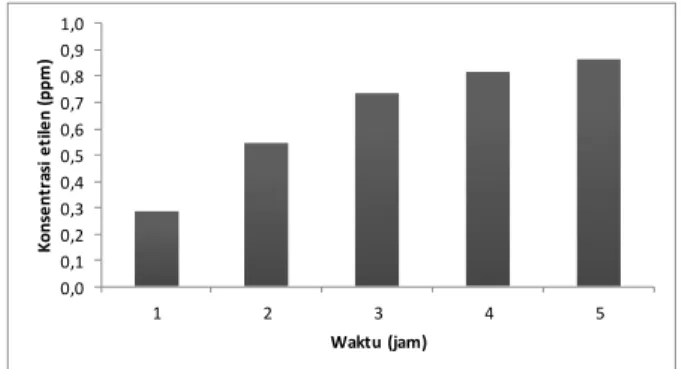
Pada penelitian kedua diamati pengaruh lamanya keadaan vakum sampel terhadap konsentrasi etilen yang dihasilkan, hal ini dilakukan karena etilen dihasilkan dengan baik dalam keadaan anaerob. Dari Gambar 12 diketahui bahwa konsentrasi etilen akan semakin besar ketika keadaan vakum sampel dalam toples semakin lama. Besarnya konsentrasi etilen terhadap lamanya sampel dalam keadaan vakum ditunjukan oleh Tabel II.
ISSN 0853-0823 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1,0 1 2 3 4 5 Kons e n tr as i et ilen (p p m ) Waktu (jam)
Gambar 12. Konsentrasi etilen terhadap lamanya sampel dalam keadaaan vakum
TABEL II. KONSENTRASI ETILEN TERHADAP LAMANYA SAMPEL DALAM KEADAAN VAKUM
Lamanya kevakuman sample
(jam) Konsentrasi etilen (ppm)
1 0,29 2 0,55 3 0,73 4 0,82 5 0,87 IV. KESIMPULAN
Dari hasil penelitian dan analisis data yang diperoleh selama penelitian, dapat disimpulkan
1. Spektrometer fotoakustik laser CO2 yang telah
dioptimasi kinerjanya menghasilkan batas deteksi terendah (BDT) sebesar (59±7) ppt.
2. Rata-rata konsentrasi etilen yang didapat untuk setiap tempat pengambilan sampel di selatan, tengah, dan utara dari hutan biologi UGM, yaitu selatan (0,6±0,3)
ppm, tengah
(
1,1±0,2)
ppm dan utara(
2,2±0,5)
ppm. Konsentrasi etilen sendiri akan membesar ketika kondisi kevakuman sampel semakin lama.PUSTAKA
[1] N.S.S. Rao, Mikroorganisme Tanah dan Pertumbuhan Tanaman,
(diterjemahkan olehSusilo, H.), Penerbit Universitas Indonesia, Jakarta, 1994.
[2] R. Hindersah, dan T Simartama, Potensi Rizobakteri Azotobacter dalam Meningkatkan Kesehatan Tanah, Jurnal Natur Indonesia 5(2), 2004, pp. 127-133
[3] A.M. Smith, Ethylene in Soil Biology, Biological and Chimical
Research Institute, New South Wales Department of Agriculture, Australia, 1976,
[4] T. Ishii dan K. Kadoya, Ethylene Evolution from Organic Materials Applied to Soil and its Relation to The Growth of Graevines, J.
Japan. Soc. Hort. Sci. 53(2), 1984, pp. 157-167.
[5] M.A.J. Wasono, Spektrometer Fotoakustik Ultra-Sensitif Pendeteksian Emisi Gas Produk Hortikultura Pasca Panen, Prosiding
Simposium Spektrometer Fotoakustik dalam Teknologi Pasca Panen
UGM, 25 Mei 2000, 1 dan 9.
[6] Z. Zhaou, Pulsed Photoacoustic Techniques and Glucose
Determination in Human Blood and Tissue, Department of Electrical
Engineering and Infotech Oulu, University of Oulu, Oulu, 2002. [7] F.J.M Herren., G. Cotti, J. Oomens, S.L Hekkert, in Ensyclopedia of
Analytical Chemistry; Photoacuostic Spectroscopy in Gas Monitoring, Meyers, R.R., ed. ,John Wiley & sons Ltd. Chichester,
2000.
[8] Mitrayana, Aplikasi Spektroskofi Laser pada Bidang Lingkungan dan Kedokteran, Lab. Fisika Atom dan Inti Jurusan Fisika FMIPA UGM,
Yogyakarta. 2009.
[9] IGK.D Arsana, dkk., Hubungan Antara Penggenangan Dini dan Potensi Redoks, Produksi Etilen dan Pengaruhnya terhadap Pertumbuhan dan Hasil Padi (Oryza Sativa) Sistem Tabela, Bul.