SIMULASI PENAMBATAN MOLEKULER COUMESTROL PADA
RESEPTOR ESTROGEN ALFA
Oleh:
Chandra Dewa Nata
NIM: 108114190
INTISARI
Kanker payudara merupakan kanker yang paling banyak diderita wanita.
Salah satu yang berperan memicu sel kanker yaitu reseptor estrogen
α
(RE
α
)
yang diekpresikan berlebihan. Untuk mencegah kanker tersebut diperlukan
senyawa yang dapat berperan sebagai antagonis
REα
. Coumestrol merupakan
senyawa fitoestrogen yang terdapat dalam kacang-kacangan, bayam, kedelai, dan
cengkeh. Secara
in vitro
dan
in vivo
diketahui bahwa coumestrol dapat berikatan
dengan
REα
maupun RE
β namun secara
in silico
belum diketahui. Penelitian ini
bertujuan untuk mengetahui dan menguji apakah protokol yang dikembangkan
oleh Radifar dkk. (2013) dapat mengenali coumestrol sebagai ligan bagi
REα
dan
bagaimanakah posenya dalam kantung ikatan
REα
.
Penelitian ini merupakan komputasi eksperimental dengan menggunakan
protokol tervalidasi hasil pengembangan Anita dkk. (2012) dan divalidasi kembali
oleh Radifar dkk. (2013) yang menggunakan perangkat lunak sidik jari interaksi
Python-based Protein-Ligand Interaction Fingerprint
(PyPLIF) yang telah
terbukti dapat meningkatkan kualitas metode penapisan virtual berbasis struktur
(PVBS) dalam proses validasi retrospektif untuk identifikasi ligan bagi
REα
.
Hasil penelitian menunjukkan bahwa protokol yang dikembangkan oleh
Radifar dkk. (2013) tidak dapat mengenali coumestrol sebagai ligan bagi
REα
selain itu protokol tersebut tidak dapat digunakan untuk elusidasi mode ikatan
coumestrol karena tidak mampu mereproduksi mode ikatan ligan kokristal
sehingga digunakan protokol PVBS tanpa sidik jari interaksi untuk elusidasi mode
dan didapatkan setidaknya 3 pose coumestrol.
ABSTRACT
Breast cancer is the most frequent cancer that happened in women.
estrogen receptor alpha (ER
α
) that expressed excessively, has a role in breast
cancer development. To prevent breast cancer, natural compound that has
antagonistic activity on ER
α
is needed. Coumestrol is phytoestrogen compound
which can be found in bean, spinach, soybean, and clove. Both
in vitro
and
in vivo
experimentals show that coumestrol can interact with ER
α
and ER
β
but
in silico
experiment, the activity is not yet known. The purposes of this experiment are to
test whether the protocol developed by Radifar
et al.
(2013) can identify
coumestrol as ligand for ER
α
and to examine the pose of coumestrol in ER
α
binding pocket.
The method of this experiment was computation experimental which
utilized a validated protocol by Anita
et al.
(2012) and revalidated by Radifar
et
al.
(2013) using interaction fingerprint (IFP) software named Python-based
Protein-Ligand Interaction Fingerprint (PyPLIF) that could improve the quality of
structure based virtual screening (SBVS) in retrospective validation to identify
ligands for ERα.
The results showed that the protocol developed by Radifar
et al.
(2013)
could not identify coumestrol as ligand for ER
α
. Moreover the protocol could not
be used for binding mode elucidation because the protocol could not reproduce
co-crystal ligand binding mode, therefore SVBS protocol without IFP was used
for binding mode elucidation and at least 3 pose of coumestrol are found.
i
SIMULASI PENAMBATAN MOLEKULER COUMESTROL PADA
RESEPTOR ESTROGEN ALFA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Chandra Dewa Nata
NIM: 108114190
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
Persetujuan Pembimbing
SIMULASI PENAMBATAI\I MOLEKULER
COT]MESTROL
PADA
RESEPTOR ESTROGEN
ALFA
Skripsi
yang
diajukan
oleh:
Chandra
Dewa
Nata
NIM:108114190
Telah
disetujui
oleh:
Pembimbing Utama
Enade Pe\dqna
Istyastono, Ph.D..
Apt.
Tanggal21
Februari 2014
Pembimbing
Pendamping
11
Pengesahan
Skripsi
Berjudul
SIMULASI PENAMBATAN
MOLEKULTR
COUMESTROL
PADA RESEPTOR ESTROGEN
ALFA
Oleh:
Chandra Dewa
Nata
NIM:
108114190Dipertahankan
di
Hadapan Panitia
Penguji Skripsi
Fakultas Farmasi
iJniversitas
SanataDharma
Pada
tanggal:20
Februari 2014
Mengetahui,
Fakultas Farmasi
Universitas
SanataDharma
Panitia
Penguji Skripsi
1.
Enade PerdanaIstyastono, Ph.D.,
Apt.
Agustina
Setiawati, M.Sc.,
Apt.
.Ieffu
Julianus,
M.Si.
2.
a
lll
ipang Djunarko, M.Sc., Apt.
4.
Nunung
Yuniarti, M.Si.,
Ph.D.,
Apt.
PERNYATAAN
KEASLIAN KARYA
Saya menyatakan dengan
sesungguhnya
bahwa
skripsi yang
berjudul
"Simulasi
Penambatan
Molekuler
Coumestrol pada
Reseptor
Estrogen
Alfa",
tidak
memuat
karya
atau bagian
karya orang
lain,
kecuali yang telah
disebutkan
dalam
kutipan
dandaftar pustaka,
sebagaimanalayaknya karya
ilmiah.
Apabila
di
kemudian
hari
ditemukan
indikasi
plagiarisme dalam
naskahini,
maka
saya bersedia menanggung segala
sanksi
sesuai peraturan
perundang-undangan
yang berlaku.
Yogy
akarta,2I
Febru ert 201 4Penulis
ffiffi
Chandra Dewa hlata
a
LEMBAR PERNYATAAN
PERSETUJUAN
PUBLIKASI
ILMIAH UNTUK KEPENTINGAN
AKADEMIS
Yang
bertanda tangandi
bawah
ini, saya
mahasiswaUniversitas
SanataDharma
:NIama :
Chandra Dewa
}.{ataNomor
Mahasiswa
:
108114190
Demi
pengembangan
ilmu
pengetahuan,
saya memberikan
kepada
Perpustakaan
Universitas
Sanata
Dharma
karya
ilmiah
saya
yang
berjudul:
o'Simulasi Penambatan
Molekuler
Coumestrol
pada Reseptor Estrogen
Alfao
beserta
perangkat yang
diperlukan
(bila ada).
Dengan
demikian
sayamemberikan
kepada
perpustakaan
Universitas
Sanata
Dharma
hak
untuk
menyimpan,
mengalihkan dalam
bentuk media
lain,
mengelolanya
dalam bentuk
pangkalan
data
mendistribusikan
secaraterbatas, dan
mempublikasikannya
di
Internet
ataumedia
lain
untuk
kepentingan akademis
tanpa
perlu
meminta
ijin
dari
sayamaupun memberikan
royalty
kepada
saya selamatetap mencantumkan nama
sayasebagai
penulis.
Demikian
pernyataan
ini
yang
sayabuat
dengan sebenafitya.Dibuat
di
Yogyakarta
Pada
tanggal
:21
Februari
2AI4
Yang menyatakan
vi
HALAMAN PERSEMBAHAN
“A good head and a good heart are always a formidable
combination.” –
Nelson Mandela
“
All things are difficult before they are easy.” –
Thomas
Fuller
“Try not to become a man of success, but rather try
to become a man of value.
” –
Albert Einstein
”I've failed over and over and over again in my life
and that is why I succeed.”
-
Michael Jordan
Karya kecilku ini kupersembahkan untuk:
Tuhan yang Maha Esa yang telah membimbing, melindungi dan
menyertai dalam kehidupanku
Papa dan Mama yang selalu memberikanku dukungan, semangat,
cinta dan kasih sayang
Bapak/Ibu dosen dan staff pengajar Fakultas Farmasi USD
Sahabat-sahabatku tersayang
Serta
vii
PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas rahmat
karunia dan penyertaan yang telah diberikan sehingga penyusunan skripsi yang
berjudul “
SIMULASI PENAMBATAN MOLEKULER COUMESTROL
PADA RESEPTOR ESTROGEN ALFA
” dapat dilaksanakan dengan baik.
Skripsi ini disusun sebagai salah satu syarat untuk meraih gelar Sarjana Farmasi
(S.Farm.) di Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Selama proses penelitian dan penyusunan skripsi ini, penulis mendapatkan
banyak bantuan dan dukungan dari berbagai pihak. Oleh karena itu, penulis
mengucapkan terima kasih kepada:
1.
Ipang Djunarko, M.Sc., Apt., selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma.
2.
C.M. Ratna Rini Nastiti, M.Pharm., Apt., selaku Ketua Program Studi
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
3.
Enade Perdana Istyastono, Ph.D., Apt., selaku dosen pembimbing yang
telah memberikan bimbingan, masukan serta pengarahan dalam penelitian
dan penyusunan skripsi ini.
4.
Agustina Setiawati, M.Sc., Apt., selaku dosen pembimbing yang telah
memberikan bimbingan serta pengarahan dalam penelitian dan
penyusunan skripsi ini.
viii
6.
Mas Ottok selaku laboran Laboratorium Virtual Fakultas Farmasi
Universitas Sanata Dharma yang senantiasa menemani dan memberikan
fasilitas selama proses pelaksanaan penelitian di laboratorium.
7.
Papa, mama, dan kedua kakakku yang telah memberikan doa, semangat,
dan dukungan kepada penulis selama proses penyusunan skripsi.
8.
Astuti Malyawati Soesanto dan Ricardo Kenny Chandra, teman
seperjuangan yang bersama-sama berusaha, bertukar informasi dan saling
memberi dukungan dalam pengerjaan skripsi.
9.
Gisela Winda Permatasari, atas pengertian, semangat, doa, dan
dukungannya selama proses penelitian dan penyusunan skripsi ini.
10.
Sahabatku Hugo, Bram, Reza, Suryo, Christian, Tora atas canda tawa
dalam perkuliahan ini
11.
Teman-teman FST B 2010 atas kebersamaan, canda tawa, dan pengalaman
berharga untuk penulis selama menjalani kuliah di Fakultas Farmasi
Universitas Sanata Dharma.
12.
Semua pihak yang tidak dapat penulis sebutkan satu per satu yang telah
membantu dalam proses penyusunan skripsi ini.
Akhir kata, penulis menyadari bahwa masih banyak kekurangan dalam
penyusunan skripsi ini mengingat keterbatasan kemampuan dan pengetahuan
penulis. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun
dari semua pihak. Semoga skripsi ini dapat memberikan manfaat bagi pembaca.
ix
DAFTAR ISI
HALAMAN JUDUL...
i
HALAMAN PERSETUJUAN PEMBIMBING... ii
HALAMAN PENGESAHAN... iii
PERNYATAAN KEASLIAN KARYA... iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI ILMIAH
UNTUK KEPENTINGAN AKADEMIS...
v
HALAMAN PERSEMBAHAN... vi
PRAKATA... vii
DAFTAR ISI... ix
DAFTAR TABEL... xi
DAFTAR GAMBAR... xii
DAFTAR LAMPIRAN... xiii
DAFTAR SINGKATAN KATA... xiv
INTISARI... xv
ABSTRACT... xvi
BAB I. PENGANTAR ... 1
A.
Latar Belakang... 1
1.
Permasalahan ... 2
2.
Keaslian Penelitian... 2
3.
Manfaat Penelitian ... 3
a.
Manfaat teoretis ...
3
b.
Manfaat praktis ... 3
B.
Tujuan Penelitian ... 3
1.
Tujuan umum ...
3
2.
Tujuan khusus ...
3
BAB II. PENELAAHAN PUSTAKA... 4
x
B.
Kanker Payudara... 5
C.
Reseptor Estrogen... 6
D.
Coumestrol ... 9
E.
Penapisan Virtual Berbasis Struktur... 10
F.
Landasan Teori... 13
G.
Hipotesis ... 15
BAB III. METODE PENELITIAN... 16
A.
Jenis dan Rancangan Penelitian... 16
B.
Variabel dan Definisi Operasional... 16
1.
Variabel Penelitian... 16
a.
Variabel utama... 16
b.
Variabel pengacau... 16
2.
Definisi Operasional... 16
C.
Bahan dan Alat Penelitian... 17
D.
Tata Cara Penelitian... 18
E.
Tata Cara Analisis Hasil ... 20
BAB IV. HASIL DAN PEMBAHASAN... 21
BAB V. KESIMPULAN DAN SARAN... 32
A.
Kesimpulan ... 32
B.
Saran ... 32
DAFTAR PUSTAKA... 33
LAMPIRAN... 36
xi
DAFTAR TABEL
xii
DAFTAR GAMBAR
Gambar 1. Struktur hormon estrogen: (A) Estron, (B) Estradiol, (C) Estriol
6
Gambar 2. Struktur coumestrol... 10
Gambar 3. Diagram pengambilan keputusan... 19
Gambar 4. Histogram sebaran nilai Tc-PLIF coumestrol-
REα
... 24
Gambar 5. Histogram sebaran RMSD penambatan coumestrol-
REα
... 25
Gambar 6. Plot kelompok RMSD coumestrol... 26
Gambar 7. Interaksi 4-hidroksi-tamoksifen pada
REα
... 27
Gambar 8. (A) 3 pose ikatan coumestrol pada
REα
. Pose representatif
kelompok 1, 2, 3 coumestrol pada
REα
(B, C, D)...
29
Gambar 9. Jarak ikatan coumestrol pada
REα
kelompok
1 (A) dan 2 (B)... 31
xiii
DAFTAR LAMPIRAN
Lampiran 1.
Tabel nilai RMSD ChemPLP
non filter
4-hidroksi-tamoksifen.
37
Lampiran 2.
Tabel nilai RMSD ChemPLP f
ilter
4-hidroksi-tamoksifen... 45
Lampiran 3.
Tabel nilai RMSD Tc-PLIF
non filter
4-hidroksi-tamoksifen...
53
Lampiran 4.
Tabel nilai RMSD Tc-PLIF
filter
4-hidroksi-tamoksifen... 60
Lampiran 5.
Script
untuk melakukan penambatan ulang
4-hidroksi-tamoksifen pada
REα
...
68
Lampiran 6.
Script
untuk melakukan penambatan coumestrol pada
REα
... 69
Lampiran 7.
Script
perhitungan nilai RMSD 4-hidroksi-tamoksifen pada
protokol Tc-PLIF
nonfilter
...
70
Lampiran 8.
Script
perhitungan nilai RMSD 4-hidroksi-tamoksifen pada
protokol Tc-PLIF
filter
...
71
Lampiran 9.
Script
perhitungan nilai RMSD 4-hidroksi-tamoksifen pada
protokol ChemPLP
nonfilter
...
72
Lampiran 10.
Script
perhitungan nilai RMSD 4-hidroksi-tamoksifen pada
protokol ChemPLP
filter
...
73
Lampiran 11.
Script
perhitungan nilai RMSD coumestrol pada protokol
ChemPLP
filter..
...
74
xiv
DAFTAR SINGKATAN KATA
AF
Activation function
ChemPLP
Chemical piecewise linear potential
DBD
DNA binding domain
EF1%
Enrichment factor 1%
ER
Estrogen receptor
ERE
Estrogen receptor element
HB-EGF
Heparin binding epitelial growth factor
IFP
Interaction finger print
LBD
Ligand binding domain
PLANTS
Protein ligand ant system
PVBS
Penapisan virtual berbasis struktur
PyPLIF
Python based protein ligand interaction fingerprint
RMSD
Root mean square deviation
SIRS
Sistem informasi rumah sakit
Tc
Tanimoto coefficient
xv
INTISARI
Kanker payudara merupakan kanker yang paling banyak diderita wanita.
Salah satu yang berperan memicu sel kanker yaitu reseptor estrogen
α (REα)
yang diekpresikan berlebihan. Untuk mencegah kanker tersebut diperlukan
senyawa yang dapat berperan sebagai antagonis
REα
. Coumestrol merupakan
senyawa fitoestrogen yang terdapat dalam kacang-kacangan, bayam, kedelai, dan
cengkeh. Secara
in vitro
dan
in vivo
diketahui bahwa coumestrol dapat berikatan
dengan
REα
maupun RE
β namun secara
in silico
belum diketahui. Penelitian ini
bertujuan untuk mengetahui dan menguji apakah protokol yang dikembangkan
oleh Radifar dkk. (2013) dapat mengenali coumestrol sebagai ligan bagi REα dan
bagaimanakah posenya dalam kantung ikatan
REα
.
Penelitian ini merupakan komputasi eksperimental dengan menggunakan
protokol tervalidasi hasil pengembangan Anita dkk. (2012) dan divalidasi kembali
oleh Radifar dkk. (2013) yang menggunakan perangkat lunak sidik jari interaksi
Python-based Protein-Ligand Interaction Fingerprint
(PyPLIF) yang telah
terbukti dapat meningkatkan kualitas metode penapisan virtual berbasis struktur
(PVBS) dalam proses validasi retrospektif untuk identifikasi ligan bagi REα.
Hasil penelitian menunjukkan bahwa protokol yang dikembangkan oleh
Radifar dkk. (2013) tidak dapat mengenali coumestrol sebagai ligan bagi
REα
selain itu protokol tersebut tidak dapat digunakan untuk elusidasi mode ikatan
coumestrol karena tidak mampu mereproduksi mode ikatan ligan kokristal
sehingga digunakan protokol PVBS tanpa sidik jari interaksi untuk elusidasi mode
dan didapatkan setidaknya 3 pose coumestrol.
xvi
ABSTRACT
Breast cancer is the most frequent cancer that happened in women.
estrogen receptor alpha (ERα) that expressed excessively, has a role in breast
cancer development. To prevent breast cancer, natural compound that has
antagonistic activity on ER
α
is needed. Coumestrol is phytoestrogen compound
which can be found in bean, spinach, soybean, and clove. Both
in vitro
and
in vivo
experimentals show that coumestrol can interact with ERα and ERβ but
in silico
experiment, the activity is not yet known. The purposes of this experiment are to
test whether the protocol developed by Radifar
et al.
(2013) can identify
coumestrol as ligand for ERα and to examine the pose of coumestrol in ERα
binding pocket.
The method of this experiment was computation experimental which
utilized a validated protocol by Anita
et al.
(2012) and revalidated by Radifar
et
al.
(2013) using interaction fingerprint (IFP) software named Python-based
Protein-Ligand Interaction Fingerprint (PyPLIF) that could improve the quality of
structure based virtual screening (SBVS) in retrospective validation to identify
ligands for ERα.
The results showed that the protocol developed by Radifar
et al.
(2013)
could not identify coumestrol as ligand for ER
α
. Moreover the protocol could not
be used for binding mode elucidation because the protocol could not reproduce
co-crystal ligand binding mode, therefore SVBS protocol without IFP was used
for binding mode elucidation and at least 3 pose of coumestrol are found.
1
BAB I
PENGANTAR
A.
Latar Belakang
Kanker payudara merupakan sekelompok sel abnormal yang disebabkan
oleh proses pembelahan sel yang berlebihan dan tidak terkoordinasi yang terjadi
pada payudara (Kumar, 2007). Saat ini kanker payudara merupakan kanker
terbanyak kedua yang menyebabkan kematian setelah kanker paru-paru dan
merupakan kanker terbanyak pada wanita. Sebanyak 203.000 kasus ditemukan
pada setiap negara (rasio populasi 1:4) di Asia Tenggara dengan jumlah kematian
93.000 (Globocan, 2008). Di Indonesia, berdasarkan data Sistem Informasi
Rumah Sakit (SIRS) tahun 2007, kanker payudara menempati urutan pertama
pada pasien rawat inap di seluruh RS di Indonesia yaitu sekitar 16,85%. Salah
satu yang berperan memicu sel kanker yaitu reseptor estrogen
α (REα) dimana
pada kanker payudara sekitar 70% ditemukan
REα
yang diekspresikan berlebihan
(Deroo dan Korach, 2006).
Berdasarkan penelitian Hopert, Beyer, Frank, Strunck, Wiinsche, dan
Volimer (1998), coumestrol secara
in vitro
dapat berikatan dengan
REα
. Selain itu
Jacob, Temple, Patisaul, Young, dan Rissman (2000) menunjukan bahwa
coumestrol secara
in vivo
dapat berikatan dengan
REα
. Meskipun secara
in vitro
dan
in vivo
telah diketahui bahwa coumestrol dapat berfungsi sebagai ligan
REα
,
namun perlu diketahui apakah secara
in silico
coumestrol dapat menjadi ligan
REα
, sehingga dapat digunakan untuk pengembangan obat.
Penelitian ini menggunakan protokol tervalidasi hasil pengembangan
Anita, Radifar, Kardono, Hanafi, dan Istyastono (2012) dan divalidasi kembali
oleh Radifar, Yuniarti, dan Istyastono (2013).
Untuk mengetahui dan menguji
kemampuan protokol yang dikembangkan oleh Radifar dkk. (2013) diharapkan
dapat mengenali coumestrol sebagai ligan pada
REα
serta mengetahui pose
coumestrol pada kantung ikatan
REα
.
1.
Permasalahan
Berdasarkan latar belakang tersebut, permasalahan pada penelitian ini
adalah:
1.
Apakah coumestrol merupakan ligan bagi
REα
secara
in silico
menurut
protokol penapisan yang dikembangkan Radifar dkk. (2013)?
2.
Bagaimanakah pose coumestrol di dalam kantung ikatan
REα
?
2.
Keaslian Penelitian
Penelitian mengenai simulasi penambatan molekuler coumestrol pada
REα
belum pernah dilakukan. Adapun beberapa jurnal terkait antara lain
Antagonists
oleh Anita dkk. pada tahun 2012;
In silico Screening and Binding
Mode Analysis of Celexocib as a Ligand for Estrogen Receptor Alpha
oleh
Riswanto, Setiawati, Yuliani, dan Istyastono pada tahun 2013.
3.
Manfaat Penelitian
a.
Manfaat teoretis
Hasil penelitian diharapkan dapat menambah pengetahuan tentang
pengikatan coumestrol pada
REα
, sehingga dapat menjadi acuan dalam
pengembangan antagonis
REα
dan mengetahui apakah protokol penapisan
in silico
yang dikembangkan Radifar dkk. (2013) mampu mengenali
coumestrol sebagai ligan pada
REα
.
b.
Manfaat praktis
Penelitian ini diharapkan menghasilkan protokol yang mampu mengenali
ligan bagi
REα
.
B.
Tujuan Penelitian
1.
Tujuan umum
Untuk mengidentifikasi senyawa yang dapat menjadi ligan bagi
REα
secara
in silico
.
2.
Tujuan khusus
Untuk mengetahui dan menguji apakah protokol penapisan
in silico
yang
4
BAB II
PENELAAHAN PUSTAKA
A.
Kanker
Kanker merupakan kumpulan sel-sel yang tumbuh melampaui batas
normal, yang kemudian dapat menyerang suatu bagian tubuh dan dapat menyebar
ke organ lain (metastasis). Kanker merupakan istilah umum untuk menunjukkan
adanya neoplasma. Neoplasma didefinisikan sebagai massa abnormal jaringan
yang pertumbuhannya berlebihan dan tidak terkoordinasikan dengan pertumbuhan
jaringan normal walaupun rangsangan yang memicu pertumbuhan tersebut telah
berhenti (Kumar, 2007).
Karsinogenesis merupakan proses pembentukan sel kanker yang melalui
banyak tahap, baik pada tingkat fenotip maupun genotip. Dalam kondisi normal,
langkah-langkah proliferasi sel dapat dibagi sebagai berikut: (1) faktor
pertumbuhan terikat pada reseptor pertumbuhan pada permukaan sel; (2) reseptor
faktor pertumbuhan memberi sinyal untuk mengaktifkan protein tranduser; (3)
sinyal ditransmisikan melewati sitosol melalui second messenger menuju inti sel;
(4) faktor transkripsi inti yang memulai pengaktifan transkripsi DNA. Berbeda
dengan sel normal, jumlah proliferasi sel kanker akan meningkat dan sel yang
berapoptosis menurun (Kumar, 2007).
perubahan sel normal dan meningkatkan proliferasi. Pada tahap ini
terjadi kerusakan DNA yang dapat diperbaiki dengan mekanisme enzimatik. Bila
pembelahan sel telah terjadi sebelum DNA diperbaiki maka dapat menyebabkan
perubahan sel yang permanen dan
irreversible
. Pada tahap ini sel normal disebut
juga sel inisiasi (Bertram, 2001).
Promosi adalah tahap setelah inisiasi. Bila senyawa yang dapat
menyebabkan kanker terus terpapar maka akan meningkatkan proliferasi sel,
perubahan ekspresi gen dan peubahan pada kontrol pertumbuhan seluler sehingga
sel inisiasi terus berkembang dan menjadi sel tumor (Trosko, 2001).
Tahap selanjutnya adalah progresi. Pada tahap ini sel dapat berproliferasi
tanpa adanya stimulus. Sel tumor akan semakin berkembang menjadi sel kanker
yang disebabkan oleh perubahan DNA, ekspresi onkogen, dan mutasi tambahan.
Karakteristik sel kanker yaitu
irreversible
, perkembangan yang sangat cepat,
perubahan pada morfologi, biokimia, dan metabolisme sel (Dixon dan Kopras,
2004).
B.
Kanker Payudara
Data WHO (Globocan, 2008) menunjukkan bahwa kanker payudara
adalah kanker yang paling banyak menyebabkan kematian setelah kanker
paru-paru dan merupakan kanker yang paling banyak diderita wanita dengan 203.000
kasus ditemukan pada setiap negara (rasio populasi 1:4) di Asia Tenggara dengan
jumlah kematian 93.000. Di Indonesia kanker payudara menempati urutan
pertama pada pasien rawat inap di seluruh RS di Indonesia (16,85%), disusul
kanker leher rahim (11,78%) (Yayasan Kanker Indonesia, 2012).
C. Reseptor Estrogen
Reseptor estrogen (RE) adalah salah satu anggota reseptor inti yang
diaktivasi oleh hormon estrogen. tiga tipe utama hormon estrogen yang terdapat
pada wanita adalah estron (E1)
yang hanya dapat berikatan pada REα, e
stradiol
(E2) yang dapat berikatan dengan RE
α maupun REβ, dan e
striol (E3) yang hanya
dapat berikatan dengan
REβ
. Estradiol merupakan hormon yang paling dominan
diproduksi selama masa reproduksi. Peran estradiol digantikan oleh estriol pada
saat wanita sedang mengandung. Setelah masuk masa
menopause
hormon
estrogen yang paling berperan adalah estron (Kikandi, 2008). Struktur hormon
estrogen ditunjukkan pada Gambar 1.
Molekul RE memiliki tiga tempat ikatan spesifik, yaitu terhadap ligan
yang disebut
ligand binding domain
(LBD) atau disebut juga
activation function
2
(AF-2) atau terhadap
growth factor
yang biasa disebut AF-1 dan terhadap DNA
yang disebut
DNA binding domain
(DBD). DBD yang nantinya akan berikatan
dengan
estrogen receptor element
(ERE) (Gustaffson, 1999).
Terdapat 2 mekanisme aktivasi RE yaitu aktivasi RE pada kompartemen
inti (
translation transactivation
) dan aktivasi RE yang terdapat pada membran
(
signaling
). Mekanisme aktivasi RE pada kompartemen inti yaitu ligan agonis
berikatan dengan RE akan mengakibatkan terjadinya perubahan konformasi
reseptor yang memungkinkannya berikatan dengan koaktivator. Kemudian
kompleks ligan-reseptor akan berikatan dengan ERE. Setelah berikatan dengan
ERE, kompleks tersebut akan berikatan dengan suatu protein koaktivator dan
mengaktifkan faktor transkripsi. Aktivasi transkripsi gen tadi akan menghasilkan
mRNA yang mengarah pada sintesis protein tertentu dan kemudian
mempengaruhi berbagai fungsi sel bergantung sel target (Gustaffson, 1999).
Mekanisme aktivasi RE pada membran yaitu ligan agonis berikatan pada
RE di membran, kemudian melalui
heparin binding epitelial growth factor
(HB-EGF) mengaktivasi reseptor EGF yang kemudian memberi sinyal melalui jalur
Ras/Raf/MAP kinase memberi sinyal kepada target gen seperti P53 yang akan
menginaktivasi P53 sehingga
tumor supressor gen
tidak bekerja, C-Myc yang
Terdapat 2 jenis RE yaitu
REα
dan RE
β yang disandi oleh gen yang
berbeda.
REα
dapat ditemukan di endometrium, sel kanker payudara, dan
hipotalamus (Yaghmaie, Saeed, Garan, Freitag, Timiras, dan Sternberg, 2005),
sedangkan RE
β dapat ditemukan pada ginjal, otak,
tulang, jantung, prostat,
paru-paru, mukosa intestinal, dan sel endothelial (Babiker, De Windt, van Eickels,
Grohe, Meyer, dan Doevendans, 2002).
REα
dan RE
β dihasilkan oleh gen yang berbeda.
Gen
REα
terletak pada
kromosom 6 lokus q25.I, sedangkan gen RE
β terletak pada pita q22
-24 kromosom
14.
REα
dan RE
β mempunyai kemiripan karakteristik, 95% domain ikatan DNA
dan 55% domain ikatan ligan kedua jenis RE tersebut sama (Shaun, Susan, Sietse,
dan Malcolm, 1997).
REα
dan RE
β dapat membentuk heterodimer u
ntuk merangsang
transkripsi gen-gen yang mengatur proliferasi dan siklus sel. Pada organ yang
mempunyai ekspresi
REα
lebih banyak dari RE
β maka akan banyak terbentuk
homodimer
REα
dan heterodimer
REα/β di
bandingkan dengan homodimer RE
β.
Bentuk heterodimer
REα/β dapat berikatan pada DNA dengan afinitas yang sama
dengan homodimer
REα
dan lebih besar daripada homodimer RE
β.
RE
β dapat
menghambat aktivasi transkripsional yang diperantarai oleh
REα
jika terdapat
dalam bentuk heterodimer (Paruthiyil, Parmar, Kerekatte, Cunha, Firestone,
Leitman, 2004).
pada
REα
dapat menstimulasi proliferasi dari sel payudara sehingga menyebabkan
peningkatan pembelahan sel dan replikasi DNA. Laju replikasi yang sangat cepat
akan menyebabkan sel menjadi rentan terhadap kesalahan penyandian genetik
sehingga memicu mutasi. Hal tersebut mengganggu daur sel, apoptosis, dan
perbaikan DNA yang berujung pada terbentuknya tumor (Deroo dan Korach,
2006).
Radifar dkk. (2013) melakukan penelitian secara
in
silico dengan metode
sidik jari interaksi dengan 4-hidroksi-tamoksifen sebagai ligan bagi
REα
. Dalam
penelitian tersebut Asp351 diketahui berperan menjadi jangkar dalam ikatan suatu
ligan dengan
REα
.
D. Coumestrol
Coumestrol (3,9-dihidroksi-6H-benzofuro[3,2-c] [1]benzopyran-6-one)
merupakan senyawa polifenolik alami golongan pterokarpan yang terdapat dalam
kacang-kacangan, bayam, kedelai, dan cengkeh. Coumestrol paling banyak
terdapat dalam kedelai dan cengkeh dan dapat berfungsi sebagai antioksidan,
antibakteri, antiviral, dan antifungi
(Lee, Lee, Park, Sangurdekar, Chang 2012).
Coumestrol merupakan senyawa fitoestrogen
yang memiliki aktivitas
biologis seperti estrogen sehingga memiliki reseptor yang sama dengan estrogen
yaitu RE. Coumestrol dapat berikatan dengan
REα
maupun RE
β d
engan
kemampuan ikatan dengan RE
β lebih tinggi dibandingkan REα
(Kuiper, Enmark,
Pelto-Huikko, Nilsson, dan Gustaffson, 1996). Berdasarkan penelitian Hopert
dkk. (1998) secara
in vitro
coumestrol dapat menjadi ligan bagi
REα
dengan
Selain itu, secara
in vivo
coumestrol dapat menjadi senyawa anti estrogen pada
otak dan kelenjar pituitari yang bekerja dengan berikatan
REα
(Jacob dkk., 2000).
Struktur coumestrol dapat dilihat pada Gambar 2.
Gambar 2. Struktur coumestrol
E. Penapisan Virtual Berbasis Struktur
Penapisan virtual berbasis struktur (PVBS) adalah teknik komputasi
dalam penemuan obat untuk mengidentifikasi bagaimana suatu senyawa dapat
berikatan pada targetnya seperti enzim atau reseptor dimana struktur dari molekul
target sudah diketahui sehingga dilakukan dengan cara menambatkan ligan
dengan protein target kemudian dilanjutkan dengan
scoring
untuk memperkirakan
afinitas ligan terhadap protein target (Kroemer, 2007).
PVBS bersifat
stochastic
, oleh karena itu diperlukan validasi
.
Ada 2
Protokol suatu PVBS dapat diterima a
pabila memiliki nilai RMSD ≤
2 Å
(Marcou dan Rognan, 2007).
Validasi retrospektif dilakukan dengan menggunakan senyawa yang aktif
terhadap reseptor
target (REα)
dan pengecoh untuk ditambatkan menggunakan
protokol yang sama kemudian dilihat nilai
Enrichment Factor
1% (EF1%). Nilai
EF1% didapat dengan membandingkan
% True Positive
pada 1%
False Positive
.
Nilai EF1% tersebut kemudian dibandingkan dengan EF1% pada pertama kali
dilakukan retrospektif PVBS terhadap
REα
. Apabila nilai EF1% lebih besar dari
EF1% awal maka protokol tersebut dikatakan baik (Huang, Soichet, Irwin, 2006).
Salah satu perangkat lunak penambatan yang dapat digunakan dalam
penapisan virtual berbasis struktur adalah PLANTS 1.2 (Korb, Stutzle, dan Exner,
2007; Korb dkk., 2009). PLANTS 1.2 memberikan luaran ChemPLP (
chemical
piecewise linear potential
) yang merupakan suatu
scoring
function
yang menilai
interaksi yang ada berdasarkan gaya tarik-menarik dan tolak-menolak antara
protein (reseptor) dan ligan. Prinsip dari penilaian ChemPLP adalah memberi nilai
suatu penambatan protein-ligan berdasarkan posisi ligan di dalam reseptor target.
Nilai ChemPLP suatu ligan yang memiliki posisi penambatan yang sama persis
dengan ligan lain akan selalu sama, karena penilaian ini berdasarkan perhitungan
matematis (Korb dkk., 2007).
Kualitas PVBS dapat ditingkatkan dengan menggunakan
Interaction
Fingerprint
(IFP) (Marcou dan Rognan, 2007). Dasar dari IFP yaitu dengan
mengubah bentuk 3 dimensi dari interaksi protein-ligan ke dalam 1 dimensi
interaksi protein-ligan pada
docking tools
terhadap ligan pembanding.
Perbandingan ini menghasilkan nilai yang dapat digunakan untuk meningkatkan
PVBS (Radifar dkk., 2013). Namun kebanyakan
tools
IFP berbayar sehingga
kemampuan untuk megembangkan IFP terbatas. Oleh karena itu Radifar dkk.
(2013) mengembangkan metode penapisan virtual yaitu PyPLIF (
Python-based
Protein-Ligan Interaction Fingerprint
).
PyPLIF merupakan pengembangan IFP dengan mengubah interaksi
molekuler protein-ligan menjadi
bitstrings
sesuai dengan residu dan tipe
interaksinya. Untuk setiap residu terdapat 7 bit yang mewakili 7 tipe interaksi
yaitu (1) apolar, (2) interaksi aromatik (
face to face
), (3) interaksi aromatik (
face
to edge
), (4) ikatan hidrogen (protein sebagai donor), (5) ikatan hidrogen (protein
sebagai akseptor), (6) interaksi elektrostatik (protein bermuatan positif), dan (7)
interaksi elektrostatik (protein bermuatan negatif). Kemudian
bitstrings
tersebut
dibandingkan terhadap standar untuk dilihat kemiripanya dengan menggunakan
Tanimoto coefficient Protein-Ligan Interaction Fingerprint
(Tc-PLIF) (Radifar
dkk., 2013).
Tanimoto coefficient
(Tc) merupakan hasil dari pembagian antara jumlah
F. Landasan Teori
Kanker adalah pertumbuhan sel abnormal dimana pertumbuhan sel
tersebut tidak terkontrol dan tidak dapat berhenti meskipun rangsangan
pertumbuhan sel tersebut telah dihentikan. Kanker payudara yaitu kanker yang
terletak pada payudara yaitu sekitar 50
–
75% terjadi di bagian duktus. Kanker
payudara merupakan kanker terbanyak yang diderita wanita dengan 93.000
kematian pada negara di Asia Tenggara selain itu berdasarkan data Sistem
Informasi Rumah Sakit (SIRS) tahun 2007, kanker payudara menempati urutan
pertama pada pasien rawat inap di seluruh RS di Indonesia yaitu sebesar 16,85%.
RE yaitu reseptor yang memerlukan hormon estrogen dalam proses
pengaktifannya. Aktivasi RE oleh ligan dapat melalui 2 jalur yaitu aktivasi pada
RE dalam kompartemen inti (
transactivation transcription
) dan aktivasi RE pada
membran (
signaling
). Sinyal ini dapat mengaktifkan gen C-Myc yang merupakan
gen untuk proliferasi sel, menginaktivasi gen P53 yang merupakan gen penekan
tumor dan mengaktifkan c-jun yang merupakan anti apoptosis. Terdapat 2 jenis
RE yaitu
REα
dan RE
β. Berdasarkan penelitian sekitar 70% REα
diekspresikan
berlebihan pada penderita kanker payudara dimana ekspresi berlebihan tersebut
dapat mengganggu daur sel, apoptosis, dan perbaikan DNA sehingga dapat
memicu terbentuknya tumor. Berdasarkan penelitian Radifar dkk. (2013) yang
berperan sebagai jangkar ligan bagi
REα
adalah Asp 351.
coumestrol diketahui dapat berikatan dengan
REα
maupun RE
β d
engan
kemampuan ikatan dengan RE
β lebih tinggi dibandingkan REα
.
PVBS adalah teknik komputasi dalam penemuan obat untuk
mengidentifikasi bagaimana suatu senyawa dapat berikatan pada targetnya yaitu
dapat berupa enzim atau reseptor. PVBS bersifat
stochastic
, oleh karena itu
diperlukan validasi yaitu validasi internal dan validasi retrospektif. Pada
penelitian ini hanya digunakan validasi internal. Validasi internal dilakukan
dengan menambatkan kembali ligan standar pada reseptor untuk menguji apakah
protokol PVBS dapat menghasilkan kembali pose ligan ko-kristal. Parameter yang
digunakan adalah RMSD ≤
2 Å.
Penelitian PVBS memerlukan perangkat lunak untuk menambatkan suatu
ligan pada protein. Salah satu perangkat lunak yang dapat digunakan dan tidak
berbayar adalah PLANTS 1.2 yang memberikan luaran ChemPLP, suatu
scoring
function
yang menilai interaksi yang ada berdasarkan gaya tarik-menarik dan
tolak-menolak antara protein (reseptor) dan ligan. Semakin negatif nilai ChemPLP
maka afinitas suatu ligan dalam protein semakin tinggi.
IFP merupakan metode yang dapat digunakan untuk meningkatkan
kualitas PVBS, namun kebanyakan
tools
IFP berbayar sehingga Radifar dkk.
(2013) membuat
tools
IFP yang tidak berbayar yaitu PyPLIF yang merupakan
pengembangan IFP. PyPLIF mengubah interaksi molekuler protein-ligan menjadi
bitstrings
sesuai dengan residu dan tipe interaksinya. Untuk setiap residu terdapat
7 bit yang mewakili 7 tipe interaksi, setelah itu
bitstrings
tersebut dibandingkan
Tc-PLIF memiliki rentang antara 0,000 hingga 1,000 dimana nilai 0,000
memiliki arti tidak ada kemiripan dan nilai 1,000 menunjukkan interaksi sidik jari
ligan standar dan ligan yang ditambatkan identik. Suatu ligan dapat dikatakan
dikenali pada
REα
apabila memiliki nilai Tc-
PLIF ≥ 0,600.
G. Hipotesis
1.
Coumestrol merupakan ligan bagi
REα
secara
in silico
menurut protokol
16
BAB III
METODE PENELITIAN
A.
Jenis dan Rancangan Penelitian
Penelitian yang berjudul “Simulasi Penambatan Molekuler Coumestrol
Pada Reseptor Estrogen Alf
a” termasuk penelitian komputasi
eksperimental yang
terdapat intervensi terhadap variabel yang dilakukan dengan bantuan komputer.
B.
Variabel dan Definisi Operasional
1.
Variabel Penelitian
a.
Variabel utama
1)
Variabel bebas
: Protokol penambatan
coumestrol pada REα
2)
Variabel tergantung : Nilai Tc-PLIF, ChemPLP serta pose coumestrol
di dalam kantung ikatan
REα
b.
Variabel pengacau
1)
Variabel pengacau terkendali
a)
Spesifikasi alat komputasi dan versi perangkat lunak
2)
Variabel pengacau tak terkendali
a)
Sifat algoritma penambatan molekuler yang
stochastic
2.
Definisi Operasional
2.
Pose coumestrol adalah pose coumestrol di dalam kantung ikatan
REα
yang dipilih secara obyektif kuantitatif berdasarkan nilai Tc-PLIF dan
atau ChemPLP.
3.
Filter
adalah penyaringan pose ligan yang memiliki interaksi dengan
residu asam amino Asp351.
C.
Bahan dan Alat Penelitian
1.
Bahan yang digunakan dalam penelitian
a.
Protokol yang telah dikembangkan oleh Anita dkk. (2012) dan telah
divalidasi kembali oleh Radifar dkk. (2013)
b.
Struktur ko-kristal dari
REα
(didapatkan dari PDB kode: 3ERT).
c.
Struktur tiga dimensi coumestrol (didapatkan dari zinc.docking.org,
dengan kode: ZINC00001219)
d.
Docking Software
PLANTS 1.2 (Korb dkk., 2007; Korb dkk., 2009)
untuk simulasi penambatan molekuler, PyPLIF (Radifar dkk., 2013)
untuk menilai kembali pose penambatan,
Open Babel
sebagai pustaka
fingerprinting
open access
, PyMol 1.2rl (Lill dan Danielson, 2011) untuk
memvisualisasikan pose coumestrol, dan R 3.0.1. (R Development Core
Team, 2013) untuk komputasi statistik.
2.
Alat atau instrumen penelitian
dilakukan pada komputer dengan spesifikasi: CPU intel i5-3230 @2.60GHz,
RAM 4GB, dengan sistem operasi ubuntu 12.04 versi kernel 3.8.0-32.
D.
Tata Cara Penelitian
1.
Pengunduhan ko-kristal
REα
Pengunduhan dilakukan dari website PDB (
www.rcsb.org
) dengan
kode PDB: 3ERT.
2.
Pengunduhan struktur coumestrol
Struktur virtual coumestrol didapat dengan mengunduh dari zinc
database dengan kode ZINC00001219 (
http://zinc.docking.org/
).
3.
Penambatan ulang 4-hidroksi-tamoksifen (validasi internal)
4-hidroksi-tamoksifen ditambatkan pada
REα
sebanyak 1.000 kali
dengan 3 kali replikasi. Setelah itu, dilakukan identifikasi sidik jari interaksi
dari hasil penambatan menggunakan aplikasi PyPLIF (Radifar dkk., 2013)
dilanjutkan penyaringan pada ikatan hidrogen dengan Asp351 (Radifar dkk.,
2013) dan pengurutan nilai yang didapatkan. Luaran yang didapat terbagi
menjadi empat bagian: (i) Nilai Tc-PLIF
filter
ikatan hidrogen dengan
Asp351, (ii) Nilai Tc-PLIF
nonfilter
ikatan hidrogen dengan Asp351, (iii)
Nilai ChemPLP
filter
ikatan hidrogen dengan Asp351, dan (iv) Nilai
ChemPLP
nonfilter
ikatan hidrogen dengan Asp351.
4.
Analisis hasil validasi internal
dimulai dari poin i sampai poin iv (tata cara 3). Simulasi penambatan
coumestrol berdasar pada protokol yang dinyatakan valid sesuai Gambar 3.
Gambar 3. Diagram pengambilan keputusan
5.
Simulasi penambatan coumestrol
pose yang memiliki ikatan dengan Asp351 (Radifar dkk., 2013) dan dipilih
pose dengan nilai Tc-PLIF terbesar setiap replikasi. Jika dalam penambatan
terdapat lebih dari satu pose dengan nilai Tc-PLIF terbesar, maka pose dengan
nilai ChemPLP terbesar yang dipilih
6.
Elusidasi pose ikatan coumestrol pada
REα
Pose penambatan dengan nilai terbaik sesuai luaran protokol yang
dinyatakan valid (Gambar 3) dihitung nilai RMSD. RMSD yang didapat
kemudian dikelompokkan menggunakan metode pengelompokkan
k-means
pada aplikasi R komputasi statistik. Nilai median RMSD pada masing-masing
kelompok dipilih sebagai kelompok representatif. Kemudian kelompok
tersebut digambar posenya menggunakan Pymol untuk menggambarkan
bagaimana interaksi coumestrol dengan
REα
.
E.
Tata Cara Analisis Hasil
Data Tc-PLIF dianalisis dengan aplikasi R komputasi statisik
menggunakan
shapiro-wilk
untuk melihat distribusi data tiap kelompok. Jika
didapatkan distribusi data yang normal maka dilanjutkan dengan
var-test
untuk
mengetahui variansi antar kelompok. Apabila distribusi normal selanjutnya
digunakan
t-test
bila tidak terdistribusi normal digunakan
Wilcoxon-test.
Ligan
21
BAB IV
HASIL DAN PEMBAHASAN
Pendekatan kimia medisinal komputasi memiliki peran dalam
meningkatkan efisiensi penemuan obat. Protokol yang digunakan telah banyak
dikembangkan salah satunya adalah protokol yang dikembangkan oleh Anita dkk.
(2012) dan divalidasi kembali oleh Radifar dkk. (2013). Untuk melakukan
pendekatan secara
in silico
dibutuhkan protokol yang tervalidasi. Penelitian ini
menambatkan coumestrol yang secara
in vitro
(Hopert dkk., 1998)
maupun
in vivo
(Jacob dkk., 2000) aktif sebagai ligan bagi
REα
dengan tujuan mengetahui dan
menguji kemampuan protokol yang dikembangkan oleh Radifar dkk. (2013) dapat
mengenali coumestrol sebagai ligan pada
REα
serta mengetahui pose coumestrol
pada kantung ikatan
REα
.
Coumestrol ditambatkan pada
REα
dengan menggunakan aplikasi
PLANTS 1.2 (Korb dkk., 2007; Korb dkk., 2009) luaran yang didapatkan adalah
nilai ChemPLP dimana nilai terendah merupakan nilai yang paling baik.
Kemudian luaran tersebut digunakan untuk mengidentifikasi sidik jari interaksi
REα
-coumestrol menggunakan aplikasi PyPLIF (Radifar dkk., 2013). Untuk
Protokol yang digunakan dalam penelitian ini harus valid, oleh karena itu
sebelum dilakukan penambatan coumestrol pada
REα
perlu dilakukan validasi
internal dengan menambatkan kembali 4-hidroksi-tamoksifen pada
REα
untuk
mengetahui apakah protokol yamg digunakan dapat menghasilkan kembali pose
dari ligan ko-kristal dengan menggunakan parameter nilai RMSD. Protokol dapat
diterima apabila 95% dari data mempu
nyai nilai RMSD ≤
2 Å sesuai dengan
diagram pengambilan keputusan (Gambar 3).
Tabel I. Data RMSD
penambatan ulang 4-hidroksi-tamoksifen
% RMSD
≤
2 Å ChemPLP
% RMSD
≤
2 Å Tc-PLIF
Non Filter
Filter
Non Filter
Filter
Rep.I Rep.II Rep.III Rep.I Rep.II Rep.III Rep.I Rep.II Rep.III Rep.I Rep.II Rep.III
99,9% 99,8% 99,8% 100% 100% 99,9% 89,6% 89,9% 90,5% 91,2% 92,5% 90,6%
Berdasarkan tabel I dapat diketahui bahwa protokol yang menggunakan
parameter Tc-PLIF tidak dapat menghasilkan kembali pose ko-kristal sedangkan
protokol yang menggunakan parameter ChemPLP baik
filter
maupun
non filter
dapat menghasilkan kembali pose ko-kristal yang ditandai dengan lebih dari 95%
data memiliki nilai RMSD ≤
2 Å oleh karena itu protokol dengan parameter
ChemPLP
filter
dapat digunakan untuk menentukan pose penambatan coumestrol
pada
REα
.
Salah satu tujuan dari penelitian ini adalah untuk mengetahui dan
menguji kemampuan protokol yang dikembangkan oleh Radifar dkk. (2013) dapat
mengenali coumestrol sebagai ligan pada
REα
. Dari data validasi internal
diputuskan protokol dengan parameter ChemPLP
filter
yang digunakan, namun
protokol dengan parameter Tc-PLIF
filter
untuk menguji apakah protokol dapat
mengenali coumestrol sebagai ligan pada
REα
.
Protokol dengan parameter Tc-PLIF
filter
digunakan karena protokol
tersebut telah divalidasi oleh Radifar dkk. (2013) bahwa protokol tersebut mampu
mengenali ligan
REα
. Namun protokol tersebut belum dilakukan validasi apakah
dapat menghasilkan kembali pose dari ligan ko-kristal. Oleh karena itu pada
penelitian ini digunakan protokol dengan parameter Tc-PLIF
filter
untuk
mengetahui dan menguji kemampuan protokol yang dikembangkan oleh Radifar
dkk. (2013) dapat mengenali coumestrol sebagai ligan pada
REα
serta protokol
dengan parameter ChemPLP
filter
untuk mengetahui pose coumestrol pada
kantung ikatan
REα
.
4.1. Protokol Tc-PLIF filter
Protokol ini berdasar pada nilai Tc-PLIF terbaik dari coumestrol yang
memiliki ikatan hidrogen dengan ASP351
REα
pada setiap penambatannya.
Penambatan dilakukan sebanyak 1.000 kali (3 kali replikasi). Coumestrol dapat
dikenali sebagai ligan pada
REα
apabila memiliki nilai Tc-
PLIF ≥ 0,600 (Marcou
dan Rognan, 2007). Untuk menguji apakah nilai Tc-
PLIF yang didapatkan ≥
0,600 digunakan aplikasi statistik R 3.0.1. (R Development Core Team, 2013).
Dari penelitian yang dilakukan didapatkan nilai Tc-PLIF dengan nilai
mean
dan
median
berturut-turut 0,356 (SEM=
0,003) dan 0,417 (Lampiran 12)
kemudian dilakukan uji Wilcoxon dengan Hi yaitu Tc-PLIF lebih kecil dari 0,600
didapatkan nilai
p-value
< 2,2e-16 (Lampiran 12) artinya Tc-PLIF < 0,600
Namun berdasarkan penelitian Hopert, dkk. (1998) dan Jacob dkk. (2000) secara
in vitro
maupun
in vivo
coumestrol aktif sebagai ligan pada
REα
. Oleh karena itu
protokol Radifar dkk. (2013) perlu dikembangkan agar dapat mengenali
coumestrol sebagai ligan bagi
REα
. Kelemahan dari metode interaksi sidik jari
yaitu metode tersebut sangat bergantung pada senyawa standar karena prinsip dari
sidik jari interaksi yaitu mengukur kemiripan sidik jari interaksi ligan dengan
sidik jari interaksi senyawa standar. Dalam protokol Radifar dkk. (2013) senyawa
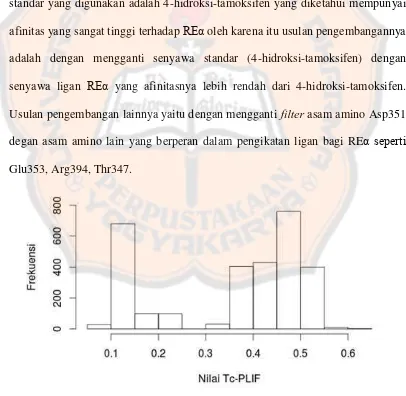
standar yang digunakan adalah 4-hidroksi-tamoksifen yang diketahui mempunyai
afinitas yang sangat tinggi terhadap
REα
oleh karena itu usulan pengembangannya
adalah dengan mengganti senyawa standar (4-hidroksi-tamoksifen) dengan
senyawa ligan
REα
yang afinitasnya lebih rendah dari 4-hidroksi-tamoksifen.
Usulan pengembangan lainnya yaitu dengan mengganti
filter
asam amino Asp351
degan asam amino lain yang berperan dalam pengikatan ligan bagi RE
α seperti
[image:42.595.104.510.310.706.2]Glu353, Arg394, Thr347.
4.2. Protokol ChemPLP filter
Protokol ini berdasar pada nilai ChemPLP terbaik dari coumestrol yang
memiliki ikatan hidrogen dengan ASP351
REα
pada setiap penambatannya.
Protokol ini digunakan untuk mengetahui pose coumestrol pada kantung ikatan
REα
. Penambatan dilakukan sebanyak 1.000 kali dengan 3 kali replikasi,
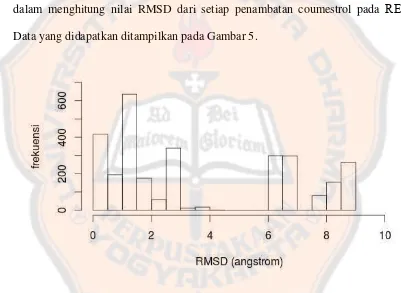
[image:43.595.100.501.277.570.2]kemudian dipilih pose dengan nilai ChemPLP terbaik untuk menjadi pembanding
dalam menghitung nilai RMSD dari setiap penambatan coumestrol pada
REα
.
Data yang didapatkan ditampilkan pada Gambar 5.
Gambar 5. Histogram sebaran RMSD penambatan coumestrol-
REα
Berdasarkan Gambar 5 dapat dilihat bahwa terdapat sebaran nilai RMSD
coumestrol pada
REα
sehingga coumestrol memiliki berbagai pose. Oleh karena
itu selanjutnya perlu dilakukan pengelompokan dengan metode pengelompokkan
k-means
pada aplikasi statistik R 3.0.1. (R Development Core Team, 2013) untuk
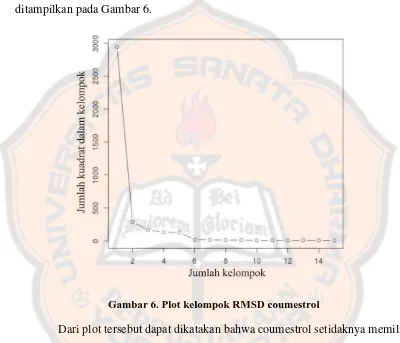
Sebaran nilai RMSD coumestrol kemudian ditampilkan dalam bentuk
plot yang telah dilakukan pengelompokkan dengan menggunakan metode
pengelompokkan
k-means
pada R 3.0.1. (R Development Core Team, 2013) yang
[image:44.595.98.498.194.537.2]ditampilkan pada Gambar 6.
Gambar 6. Plot kelompok RMSD coumestrol
Dari plot tersebut dapat dikatakan bahwa coumestrol setidaknya memiliki
3 pose penambatan, kemudian median dari tiap pose digunakan sebagai pose
representatif penambatan coumestrol pada
REα
untuk divisualisasikan dengan
menggunakan aplikasi PyMOL 1.2rl (Lill dan Danielson, 2011).
Met388, Ile389, Gly390, Leu391, Val392, Arg394, Ser395, Leu402, Leu403,
Phe404, Ala405, Leu408, Leu410, Gly415, Val418, Glu419, Gly420, Met421,
Val422, Glu423, Ile424, Phe425, Leu428, Ile514, His516, Met517, Ser518,
Asn519, Lys520, Gly521, Met522, Glu523, His524, Leu525, Tyr526, Ser527,
Met528, Lys529, Cys530, Leu536, dan Leu539 (Anita dkk., 2012) dan ditemukan
ikatan hidrogen yang diduga berperan penting dalam menentukan interaksi
ligan-REα
yaitu ikatan antara 4-hidroksi-tamoksifen dengan molekul air dan residu
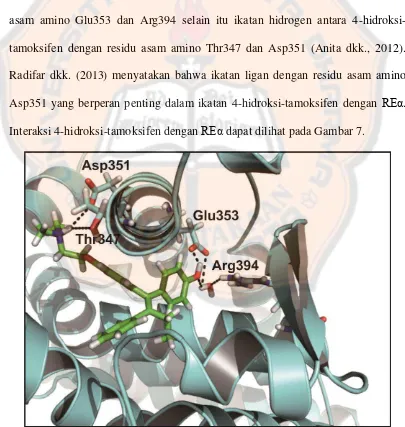
[image:45.595.104.509.293.720.2]asam amino Glu353 dan Arg394 selain itu ikatan hidrogen antara
4-hidroksi-tamoksifen dengan residu asam amino Thr347 dan Asp351 (Anita dkk., 2012).
Radifar dkk. (2013) menyatakan bahwa ikatan ligan dengan residu asam amino
Asp351 yang berperan penting dalam ikatan 4-hidroksi-tamoksifen dengan
REα
.
Interaksi 4-hidroksi-tamoksifen dengan
REα
dapat dilihat pada Gambar 7.
Menurut Marcou dan Rognan (2007), interaksi hidrogen dapat terjadi
antara 2 atom yang berjarak hingga 3,5 Å, interaksi aromatik (
face to face
),
interaksi aromatik (
edge
to face
), interaksi
π
-kation dapat terjadi antara 2 atom
yang berjarak hingga 4 Å, dan ikatan hidrofobik dapat terjadi pada jarak hingga
4,5 Å. Kantung ikatan suatu ligan pada reseptor yaitu asam amino yang berjarak
sekitar 5 Å dari ligan (de Graaf dkk., 2011) sehingga untuk mendeteksi
kemungkinan residu asam amino yang dapat berikatan dengan coumestrol
dilakukan penyaringan dengan menunjukkan residu asam amino yang berjarak
hingga 5 Å dari coumestrol. Kemudian ditentukan asam amino yang berinteraksi
dengan coumestrol berdasarkan jarak maksimum sesuai jenis interaksinya.
Berdasarkan inspeksi visual dan jarak interaksi hidrogen dibawah 3,5 Å,
pada ketiga pose pengikatan coumestrol dalam
REα
(Gambar 8) pada semua
kelompok
didapatkan kemungkinan interaksi hidrogen antara bagian 3-hidroksi
dari coumestrol dengan residu asam amino Asp351 selain itu pada kelompok
1
dan 2 terdapat ikatan hidrogen dari bagian karbonil coumestrol dengan residu
asam amino Thr347. Selain itu terdapat ikatan hidrogen pada bagian 9-hidroksi
coumestrol dengan residu asam amino Met522 serta ikatan hidrogen antara air
dengan residu asam amino Glu353 dan Arg394 pada semua kelompok.
[image:46.595.96.514.223.535.2]Gambar 8. (A) 3 pose ikatan coumestrol pada
REα
. Pose representatif kelompok 1,
2, 3 coumestrol pada
REα
(B, C, D)
Tabel II. Tabel nilai Tc-PLIF tiap kelompok
Kelompok Replikasi
Nama Ligan
Tc-PLIF
1
1078
ZINC00001219_entry_00001_conf_38
0,458
2
786
ZINC00001219_entry_00001_conf_42
0,400
3
878
ZINC00001219_entry_00001_conf_32
0,138
[image:47.595.105.509.110.626.2]kelompok 1 dan 2 lebih mirip dengan sidik jari ligan standar
(4-hidroksi-tamoksifen) dibandingkan dengan kelompok 3. Hal ini dapat dibuktikan pada
Gambar 8 dimana coumestrol dapat berikatan dengan Asp351 dan Thr347 yang
juga merupakan asam amino yang berikatan dengan 4-hidroksi-tamoksifen,
sedangkan pada kelompok 3 coumestrol hanya berikatan dengan Asp351 dan
Met522. Meskipun dapat menilai kemiripan sidik jari interaksi coumestrol dan
4-hidroksi-tamoksifen, protokol sidik jari interaksi yang dikembangkan oleh Radifar
dkk. (2013) tidak dapat mengenali coumestrol yang merupakan ligan bagi
REα
.
Oleh karena itu perlu dilakukan pengembangan protokol agar mampu mengenali
coumestrol sebagai ligan bagi
REα
serta dapat menghasilkan kembali pose ligan
ko-kristal.
Usulan pengembangan yaitu dengan menambahkan gugus karboksilat
pada bagian nomor 9 dari coumestrol. Dengan penambahan gugus karboksilat
tersebut diharapkan akan terjadi interaksi elektrostatik antara senyawa
pengembangan dan residu asam amino Arg394 dan ikatan hidrogen antara gugus
karboksilat senyawa pengembangan dengan air. Struktur senyawa pengembangan
coumestrol ditunjukkan pada Gambar 10.
Gambar 9. Jarak ikatan coumestrol pada
REα
kelompok 1 (A) dan 2 (B)
32
BAB V
KESIMPULAN DAN SARAN
A.
Kesimpulan
1.
Coumestrol bukan merupakan ligan bagi RE
α
menurut
Protokol penapisan
in silico
yang dikembangkan oleh Radifar dkk. (2013) karena protokol
tersebut tidak mampu mengenali coumestrol sebagai ligan pada RE
α
.
2.
Didapatkan setidaknya 3 pose ikatan coumestrol pada
REα
dengan
menggunakan protokol PVBS tanpa interaksi sidik jari untuk elusidasi
mode.
B. Saran
1.
Perlu dilakukan pengembangan terhadap protokol penapisan
in silico
yang
dikembangkan oleh Radifar dkk. (2013) agar dapat mengenali
senyawa-senyawa yang sudah terbukti sebagai ligan pada
REα
DAFTAR PUSTAKA
Anita, Y., Radifar, M., Kardono, L.B.S., Hanafi, M., dan Istyastono, E.P., 2012,
Structure-based design of Eugenol Analogs as Potential Estrogen Receptor
Antagonists,
Bioinformation
, 8 (19), 901-906.
Babiker, F.A, De Windt, L.J., van Eickels, M., Grohe, C., Meyer, R., dan
Doevendans, P.A., 2002, Estrogenic Hormone Action in the Heart:
Regulatory Network and Function,
Cardiovascular Research
, 53 (3), 709
–
19.
Bertram, J.S., 2001, The molecular biology of cancer,
Molecular Aspects of
Medicine
, 21, 167
–
223.
Deroo, B.J., dan Korach, K.S., 2006, Estrogen Receptors and Human
Disease,
Journal of Clinical Investigation
, 116 (3), 561-567.
de Graaf, C., Kooistra, A.J., Vischer, H.F., Katritch, V., Kuijer, M., Shiroishi, M.,
Iwata, S., Shimamura, T., Stevens, R.C., de Esch, I.J., Leurs, R., 2011,
Crystal structure-based virtual screening for fragment-like ligands of the
human histamine H(1) receptor,
Journal of Medicinal Chemistry,
54 (23),
8195-8206.
Dixon, K. dan Kopras, E, 2004, Genetic alterations and DNA repair in human
carcinogenesis,
Seminar in Cancer Biology
, 14, 441
–
448.
Globocan, 2008,
Cancer Fact Sheet,
http://globocan.iarc.fr/factsheets/
cancers/all.asp
, diakses tanggal 13 September 2013.
Gustaffson, J.A., 1999, Estrogen Receptor, a new dimension in estrogen
mechanism of action,
Journal of Endocrinology
, 163, 379-383.
Hopert A.C., Beyer A., Frank K., Strunck E., Wiinsche W., dan Volimer G., 1998,
Characterization of Estrogenicity of Phytoestrogens in an
Endometrial-derived Experimental Model,
Environmental Health Perspectives
, 106 (9),
581-586.
Huang, N., Soichet, B.K., dan Irwin, J.J., 2006, Benchmarking Sets for Molecular
Docking,
Journal of Medicinal Chemistry
, 49 (23), 6789-6801.
Jacob, D.A., Temple, J.L., Patisaul, H.B., Young, L.J., dan Rissman, E.F., 2000,
Coumestrol Antagonizes Neuroendocrine Actions of Estrogen via the
Estrogen
Receptor α,
Society for Experimental Biology and Medicine
, 226
(4), 301-306.
Kikandi, N.S., 2008, Understanding the Mode of Action Estrogenic Compound
and Development of Novel Electroplating Method,
Dissertation
, 3,
Korb, O., Stutzle T., dan Exner, T.E., 2007, An ant colony optimization approach
to flexible protein-ligand docking,
Swarm Intelligence
, 1, 115-134.
Korb, O., Stutzle T., dan Exner, T.E., 2009, Empirical scoring function for
advanced protein-ligand docking with PLANTS.
Journal of Chemical
Information and Modeling,
49 (1)
,
84-96.
Kroemer, R.T., 2007, Structure-based drug design: docking and scoring Curr
Protein Pept,
Current Protein and Peptide Science
, 8 (4): 312
–
328.
Kuiper, G.J.M., Enmark, E., Pelto-Huikko, M., Nilsson S., dan Gustaffson, J.,
1996, Cloning of a novel estrogen receptor expressed in rat prostate and ovary,
Proceedings of the National Academy of Sciences
, 93 (12), 5925-5930.
Kumar, V., 2007,
Buku Ajar Patologi,
Ed. 7, EGC, Jakarta, PP.186-187.
Lee, H., Lee, J., Park, K., Sangurdekar, D., Chang, W., 2012,
Effect of Soybean
Coumestrol on Bradyrhizobium japonicum
Nodulation Ability, Biofilm
Formation, and Transcriptional Profile,
Applied and Environmental
Microbiology
, 78 (8), 2896
–
2903.
Levin, E.R., 2001, Cell localization, physiology, and nongenomic actions of
estrogen receptors,
Journal of Applied Physiology,
91 (4), 1860-1867.
Lill, M.A., dan Danielson, M.L., 2011, Computer-aided drug design platform
using PyMOL,
Journal of Computer-Aided Molecular Design,
25, 13-9.
Linda, B., dan Maria, S., Mechanisms of Estrogen Receptor Signaling :
Convergence of Genomic and Nongenomic Actions on Target Genes,
Molecular Endocrinology
19 (4), 833
–
842.
Marcou, G., dan Rognan, D., 2007, Optimizing fragment and scaffold docking by
use of molecular interaction fingerprints,
Journal of Chemical Information
and Modeling
, 47 (1), 195
–
207.
Paruthiyil, S., Parmar, H., Kerekatte, V., Cunha, G.R., Firestone, G.L., Leitman,
D.C., 2004,
Estrogen Receptor β Inhibits Human Breast Cancer Cell
Proliferation and Tumor Formation by Causing a G2 Cell Cycle Arrest,
Cancer Research,
64, 423
–
428.
Price, 2006,
Patofisiologi Konsep Klinis Proses-Proses Penyakit,
Ed. 6, EGC,
Jakarta, PP. 150 -151
R Development Core Team, 2013,
R:A Language and Environment for Statistical
Computing
, R foundation for Statistical Computing, Vienna.
Riswanto, F.D.A, Setiawati, A., Yuliani, S.H., dan Istyastono, E.P., 2013,
In silico
Screening and Binding Mode Analysis of Celexocib as a Ligand for Estrogen
Receptor Alpha,
Indonesian Journal of Drug Design and Discovery
, 1 (1).
Shaun, M.C., Susan, H., Sietse, M., Malcolm, G.P., 1997, Estrogen Receptors
α
and
β
Form Heterodimers on DNA,
The Journal of Biochemical Chemistry
,
272 (32), 19858-19862.
Trosko, J.E., 2001,
Commentary: is the concept of “tumorpromotion” a useful
paradigm?,
Molecular Carcinogenesis
, 30, 131
–
137.
Yaghmaie, F., Saeed, O., Garan, S.A., Freitag, W., Timiras, P.S., dan Sternberg,
H., 2005, Caloric restriction reduces cell loss and maintains estrogen
receptor-alpha immunoreactivity in the pre-optic hypothalamus of female
B6D2F1 mice
,
Neuro Endocrinology Letters,
26 (3), 197
–
203.
Yayasan Kanker Indonesia, 2012
, YKI Jakarta race
,
http://yayasankanker
1 1,594 1,594 1,836 2 1,593 1,593 1,817 3 1,626 1,626 1,591 4 1,599 1,599 1,596 5 1,829 1,829 1,806 6 1,812 1,812 1,811 7 1,594 1,594 1,596 8 1,717 1,717 1,809 9 1,804 1,804 1,809 10 1,823 1,823 1,808 11 1,808 1,808 1,595 12 1,809 1,809 1,803 13 1,823 1,823 1,599 14 1,604 1,604 1,614 15 1,42 1,42 1,811 16 1,596 1,596 1,818
17 1,6 1,6 1,595
18 1,834 1,834 1,822 19 1,613 1,613 1,607 20 1,819 1,819 1,59 21 1,608 1,608 1,593 22 1,593 1,593 1,806 23 1,312 1,312 1,811 24 1,594 1,594 1,11 25 1,803 1,803 1,618 26 1,613 1,613 1,592 27 1,822 1,822 1,817 28 1,623 1,623 1,61 29 1,816 1,816 1,592 30 1,806 1,806 1,604 31 1,819 1,819 1,601 32 1,804 1,804 1,403 33 1,118 1,118 1,806 34 1,823 1,823 1,599 35 1,599 1,599 1,598 36 1,607 1,607 1,597 37 1,818 1,818 1,59 38 1,822 1,822 1,6 39 1,806 1,806 1,602 40 1,114 1,114 1,808
41 1,601 1,601 1,591 42 1,349 1,349 1,805 43 1,814 1,814 1,599
44 1,6 1,6 1,596
45 1,596 1,596 1,439 46 1,81 1,81 1,81 47 1,597 1,597 1,807 48 1,598 1,598 1,814 49 1,809 1,809 1,147 50 1,599 1,599 1,59 51 1,82 1,82 1,595 52 1,594 1,594 1,122 53 1,816 1,816 1,594 54 1,819 1,819