7
BAB II
TINJAUAN PUSTAKA
2.1. Micro Power Generator
Micro power generator adalah pembangkit listrik tenaga mikro
dengan menggunakan sumber panas pembakaran sebagai sumber energi yang akan dikonversi menjadi energi listrik siap pakai dengan menggunakan
thermoelectric. Pembangkit tenaga micro-TPV adalah jenis alat pengubah
energi langsung, yang diamana menggunakan PV cells untuk mengubah radiasi panas dari pembakaran bahan bakar fosil, menjadi energi listrik. (Aravind, Khandelwal, & Kumar, 2018).
Micro Power Generator terdiri dari ruang bakar kecil. Ruang
pembakaran berdimensi kecil menghasilkan nyala api yang tidak stabil. Hal itu menyebabkan kehilangan panas dari sistem ke lingkungan melalui dinding pembakar atau saluran gas buang. Hal ini menyebabkan nyala api sulit menyebar dan nyala api akan padam.(Kusumaningsih, Yuliati, Raharjo, & Wibowo, 2019)
Microcombustor adalah pembakaran bahan bakar pada skala mikro,
tetapi dalam masalah ukuran dibagi menjadi 2 yaitu microscale dengan besar skala kurang dari 1 mm, mesoscale dengan besar skala lebih dari 1 mm. Syarat microscale combustion yang digunakan untuk pembakaran ukurannya lebih kecil dari 1 x10-3 m. Syarat mesocale combustion yang
digunakan untuk pembakaran ukurannya lebih dari 1 mm tetapi tetap memiliki ciri-ciri karakteristik dari microscale combustion. (Chou et al., 2011)
Tabel 2.1 Definsi micro-scale dan meso-scale combustion menggunakan perbedaaan skala panjang
Definition based on
Combustio
regime Length scale Examples Applications Physical length Mesoscale 1-10 mm Rotary Engine
(CB) MEMS power Microscale 1-1000μm UCMicro-reactor (UIUC) Thruster Flame quenching diameter Mesoscale ~Quenching diameter (equilibrium) Swiss-roll combustor (USC) Power generation Microscale Quenching diameter ~Mean-free path (non equilibrium Fue Cells Nano-particle raector Energi conversion
Devise scale Microscale Smaller than convetional engine size Micro-thruster (PSU) Micro-gas turbine (MIT) Micro-satellites Micro-air planes
Sumber : (Ju & Maruta, 2011)
2.2.Pembakaran dalam Meso Scale Combustor
Proses pembakaran yaitu merupakan rangkaian suatu reaksi kimia yang terjadi antara zat pengoksida berupa oksigen dan bahan bakar, dimana dalam proses pembakaran tersebut menghasilkan energi berupa panas dan perubahan senyawa kimia. Pelepasan energi panas tersebut menimbulkan cahaya dalam bentuk api. Reaksi pembakaran terjadi ketika suatu zat mampu bereaksi cepat dengan oksidator dan mendapat suhu yang cukup untuk memulai awal proses pembakaran atau yang disebut dengan energi aktivasi.
Energi aktivasi yang digunakan pada proses pembakaran umumnya berupa panas, partikel-partikel (molekul) penyusun bahan bakar akan diaktifkan oleh panas, sehingga partikel-partikel (molekul) oksidator akan dibentuk oleh molekul baru dengan melepaskan elektron pada kulit terluarnya dan saling berikatan (Electro, Systems, Generator, & Power, 2016).
Gambar 2.1. Ilustrasi Siklus Pembakaran
Pada penelitian ini, teori tentang pembakaran diperlukan karena
Micro Power Generator menggunakan tenaga pembangkit listrik utama
yaitu api. Dalam menghidupkan api di dalam micro-scale combustor dibutuhkan bahan bakar, oksigen dan energi aktivasi. Pembakaran adalah serangkaian reaksi-reaksi kimia eksotermal antara bahan bakar dan oksidan berupa udara yang disertai dengan produksi energi berupa panas dan konversi senyawa kimia. Bahan bakar gas akan terbakar pada keadaan normal jika terdapat udara yang cukup, pembakaran yang sempurna dan dapat terjadi jika ada oksigen dalam prosesnya.
2.2.1. Reaksi Kimia Pada Proses Pembakaran
Reaksi pembakaran tergolong ke dalam reaksi kimia karena zat yang telah terbakar tidak akan bisa dikembalikan ke bentuk semula. Reaksi pembakaran mengandung pengertian suatu proses oksidasi yang dilakukan secara cepat antara oksigen (𝑂2) dan bahan bakar.Tanpa adanya oksigen dan bahan bakar tentu tidak akan terjadi reaksi pembakaran, tanpa reaksi pembakaran tentu api pun tidak akan dapat dihasilkan.(Samlawi, 2017)
Bahan bakar merupakan substansi yang terbakar sedangkan reaksi pembakaran sering disebut dengan reaksi kombusi. Reaksi pembakaran akan menghasilkan panas dan cahaya serta produk seperti karbon dioksida (𝐶𝑂2), karbon monoksida (CO) ataupun uap air (𝐻2𝑂) tergantung dari jenis reaksi pembakarannya.Pada reaksi pembakaran selalu menghasilkan panas, dan reaksi ini disebut dengan proses oksidasi eksotermis. Persamaan reaksi pembakaran secara sederhana dapat ditulis sebagai berikut:
𝐶𝑥𝐻𝑦 + 𝑎𝑂2+ 𝑒𝑎 → 𝑏 𝐶𝑂2+ 𝑐 𝐻2𝑂 + 𝑞 2-1.
Persamaan diatas ea adalah energi aktivasi dan q adalah energi panas yang dilepaskan akibat reaksi oksidasi. Persamaan 2.1. dalam kenyataannya sulit untuk terjadi, karenakan oksigen yang diambil pada setiap proses pembakaran kebanyakan dari udara bebas yang dimana bukan hanya oksigen saja yang terkandung didalamnya, adapun komposisi udara dapat dilihat pada tabel dibawah ini :
Udara Symbol Volume (%) Nitrogen N2 78.03 Oksigen O2 20.99 Argon A 0.94 Karbon dioksida CO2 0.03 Gas Lain 0.01 Jumlah 100 Sumber : (Citation, 1930)
Dari tabel diatas didapatkan bahwa proporsi oksigen di udara adalah 20,99%, nitrogen 78,03%, dan sisanya berupa argon, CO2 dll,karena jumlah gas lain sangat kecil, jika diasumsikan kandungan nitrogen di udara 79% dan oksigen 21%, maka setiap penggunaan 1 mol oksigen maka penggunaan nitrogen adalah 79
21 = 3,761 𝑚𝑜𝑙 𝑁2.
Keadaan stoikiometri adalah keadaan dimana campuran udara dan bahan bakar memiliki jumlah yang tepat dalam bereaksi secara menyeluruh.Reaksi keadaan stoikiometri dapat terjadi jika seluruh atom C dan H berikatan dengan O2 secara keseluruhan.Adapun reaksi keadaan stoikiometri dapat dituliskan dibawah ini dengan berdasarkan penjelasan pada paragraf sebelumnya.
𝐶𝑥𝐻𝑦 +𝑥+𝑦 4 𝑂2+ 3,76 ( 𝑥+𝑦 4 ) 𝑁2 → 𝑥 𝐶𝑂2 + 𝑦 2𝐻2𝑂 + 3,76 ( 𝑥+𝑦 4 ) 𝑁2 2-2
Kenyataanya pada setiap hasil pembakaran tidak hanya menghasilkan CO2H2O, dan N2 saja, tetapi bisa menghasilkan NOx, CO dan lain-lain.
Pada saat pembakaran, jika kelebihan oksigen maka NO2(Nitrogen dioksida) dapat terbentuk, sebaliknya jika kekurangan oksigen maka NO
akan terbentuk. Adapun pada CO, terbentuk jika pembakaraan kekurangan oksigen, begitu pula sebaliknya.
2.2.2. Rasio Udara Bahan Bakar (AFR)
Rasio udara bahan bakar menyediakan jumlah udara dibagi dengan jumlah bahan bakar yang ada dalam campuran reaktan. Dalam situasi pembakaran tertentu, terdapat dua rasio udara bahan bakar, satu berdasarkan jumlah mol masing-masing zat dan satu berdasarkan massa masing-masing zat dalam reaktan. Meskipun salah satu dapat digunakan untuk setiap situasi pembakaran, kita akan cenderung untuk menemukan nilai molar digunakan untuk bahan bakar cair atau padat. Ini karena kita jauh lebih mungkin mengetahui volumenya, yang berkaitan erat dengan mol bahan bakar gas daripada volume bahan bakar cair atau padat, dan kita lebih cenderung mengetahui massa cairan atau padatan daripada gas. Rasio udara-bahan bakar berbasis massa adalah
𝐴𝐹𝑅 = 𝑚𝑚𝑎𝑖𝑟
𝑓𝑢𝑒𝑙 2-3
Dan rasio bahan bakar udara berbasis mol adalah
𝐴𝐹𝑅 = 𝑛𝑎𝑖𝑟
𝑛𝑓𝑢𝑒𝑙 2-4
Keterangan :
AFR= Rasio udara bahan bakar` mair= Massa udara
mfuel= Massa bahan bakar
nair= Jumlah mol udara
nfuel=Jumlah mol bahan bakar
Saat menghitung nilai ini, ingat bahwa udara terdiri dari O2 dan N2. Meskipun mudah untuk berpikir hanya dengan mengambil koefisien di depan udara sebagai jumlah mol udara, ingat bahwa koefisien dikalikan dengan (1 + 3.76) di dalam istilah yang mewakili udara. Oleh karena itu, untuk metode yang digunakan dalam penulisan persamaan kimia sampai saat ini, jumlah mol udara adalah koefisien di depan udara dikalikan 4,76. (Mesin, Pengajar, & Ups, n.d.)
Kandungan pada udara bebas tidak hanya oksigen saja, namun banyak gas lain yang terkandung didalamnya. Unsur dalam udara terdiri adalah Oksigen 20,94%, Nitrogen 78,08% dan unsur lainnya kurang dari 1% (Petrucci dan Suminar ahmad, 1987:98). Maka jika kandungan unsur lain diabaikan dapat diasumsikan udara hanya terdiri dari 79% Nitrogen (N2) dan 21% Oksigen (O2) saja. Dengan demikian untuk setiap penggunaan 1 mol O2 yang terkandung pada udara untuk reaksi pembakaran akan mencakup pengggunaan (79
21) = 3,76 mol N2.
Dari persamaan (2-2) dapat diperoleh kesetimbangan reaksi oksidasi pada pembakaran sempurna (stoikiometrik) sebagai berikut:
Dimana massa atom relatif (ARr)C = 12, H = 1, O = 16, N =14, maka perbandingan udara terhadap bahan bakar pada pembakaran stoikiometrik heptana (C7H16) dapat dihitung dengan rumus:
𝐴𝐹𝑅𝑠𝑡𝑜𝑖𝑐 = 𝑀𝑢𝑑𝑎𝑟𝑎
𝑀𝑏𝑎ℎ𝑎𝑛𝑏𝑎𝑘𝑎𝑟 2-3
𝐴𝐹𝑅𝑠𝑡𝑜𝑖𝑐 =
(11((16𝑥2)+(6,5𝑥3,76𝑥14𝑥2)))
(12𝑥7)+(16𝑥1) = 15,1
Dari perhitungan AFR diatas diketahui bahwa perbandingan antara heptana dan udara: 1 gr heptana = 15,1gr Udara
2.2.3. Rasio Ekuivalen (ɸ)
Dalam perhitungan pembagian antara AFR stoikiometri dan AFR aktualnya akan menghasilkan angka hasil perhitungan yang disebut dengan rasio ekuivalen, persamaan untuk rasio ekuivalen sebagai berikut :
𝛷 =𝐴𝐹𝑅𝑎
𝐴𝐹𝑅𝑐 2.3
sumber : (Lheywood, n.d.)
Keterangan :
ɸ = Rasio ekuivalen antara AFRs dan AFRa AFRc = Rasio air and fuel dalam kondisi stoikiometrik AFRa = Rasio air and fuel dalam kondisi aktual
Perhitungan rasio ekuivalen berfungsi untuk mengetahui seberapa ideal proses pembakaran yang terjadi serta berguna alat ukur persentase perbandingan udara dan bahan bakar yang terjadi
maupun saat kondisi teoritis stoikiometri. Menurut Lheywood (1988), terdapat tiga jenis rasio ekuivalen :
Untuk kondisi fuel – lean mixtures, dengan ɸ € 1. Kondisi ini terjadi karena jumlah mol bahan bakar yang terkandung dalam campuran reaktan lebih sedikit dibandingkan dengan jumlah mol yang diikat oleh oksigen. Oksigen melimpah, namun proporsi bahan bakar tidak mencukupi untuk pembakaran.
Untuk kondisi stoichiometric mixtures, dengan syarat ɸ = 1. Terjadi karena jumlah mol bahan bakar dan oksigen yang terkandung untuk proses pembakaran dalam keadaan proporsi yang tepat, pembakaran ideal.
Untuk kondisi fuel – rich mixtures, dengan ketentuan ɸ Σ 1. Kondisi ini terjadi karena jumlah mol bahan bakar yang terkandung dalam campuran reaktan melebihi jumlah mol yang diikat oleh oksigen. Pembakaran yang melibatkan banyak bahan bakar akan memungkinkan untuk menimbulkan polusi udara.
2.3. Klasifikasi Pembakaran
Lheywood (1988) berpendapat bahwa, ada dua jenis pembakaran jika ditinjau berdasar tujuan, yaitu internal combustion dan external
combustion.Internal combustion adalah cara untuk menghasilkan energi
mekanik dari energi kimia yang terkandung pada bahan bakar, energi yang diperoleh dapatlangsung dimanfaatkan. Sedangkan external combustion adalah proses pembakaran yang menghasilkan energi yang belum dapat
dimanfaatkan secara langsung, memerlukan perlatan lain agar dapat memanfaatkannya, termasuk pembakaran yang terjadi pada mesoscale –
combustor.
2.3.1. Klasifikasi pembakaran okasidasi
a. Pembakaran Difusi
Bahan bakar pada pembakaran difusi akan bercampur dengan oksigen dalam ruang pencampuran bahan bakar, seperti proses pembakaran pada mesin diesel, bahan bakar diinjeksikan dalam ruang bakar agar tercampur dengan oksigen bertekanan tinggi dan proses pembakaran diruang bakar.
b. Pembakaran Premixed
Pembakaran premixed mengalami proses pembakaran diruang bakar, berbahan bakar dan zat oksida terrcampur secara menyeluruh antara satu sama lain terlebih dialirkan ke dalam ruang bakar (combustor) untuk mengalami proses pembakaran.
2.3.2. Klasifikasi pembakaran berdasarkan sifat reaksi kimia
a. Pembakarann Sempurnam
Proses pembakaranntersebut merupakang jenis pembakaran sempurna, dimana jumlah reaktann secara menyeluruh terbakari dengan udara yang menghasilkani energi panasi, ,karbondioksida dengan uapi airo saja.
b. Pembakarann tidakksempurnaa
Prosesipembakaran berlangsung secaraatidakasempurna disebabkana karena adanya jumlah udara yang tidak mencukupi untuk membakar bahan bakar sehingga menghasilkan zat sisa pembakaran berupa gas buang dan segala yang zat berbahaya bagiikesehatana makhluk hidup.
2.4. Batas Nyala Api
Api yang terbentuk dalam proses pembakaran merupakan hasil dari pelepasan energi panas pada reaksi pembakaran. Api dapat terbentuk apabila terdapat bahan bakar yang bercampur dengan oksidator mendapatkan penambahan energi eksternal untuk mengawali terjadinya reaksi pembakaran. Dalam hal ini terdapat kisaran batas komposisi antara bahan bakar dengan udara agar terbentuk nyala api.
Kisaran batas bawah stabilitas nyala api lebih dikenal juga dengan
lower flammability limit, sedangkan batas atas stabilitas nyala api dikenal
dengan istilah upper flammability limit. Melalui kedua parameter ini kita dapat mengetahui sifat dari suatu reaksi pembakaran, apakah suatu reaksi pembakaran itu memiliki stabilitas nyala api tingggi atau sebalaiknya. Selain itu dengan mengetahui nilai dari stabilitas nyala api dapat dipakai untuk mengatur komposisi campuran udara dan bahan bakar sehingga reaksi pembakaran dapat terjaga kestabilannya.
2.5. Sifat Nyala Api
Dalam reaksi pembakaran, api memiliki satbilitas nyala yang banyak dipengaruhi oleh campuran reaktan. Menurut Mahandari, C.P (2010), dalam reaksi pembakaran dapat terbentuk nyala api dengan sifat nyala yang berbeda-beda(Flame, Premix, & Propana, n.d.). Klasifikasi nyala api berdasarkan sifat nyala adalah sebagai berikut:
a. Flashback
Flashback adalahkeadaan dimana kecepatan pembakaran lebih besar
jika dibandingkan dengan kecepatan campuran reaktan sehingga nyala api merambat kembali menuju ke dalam tabung pembakaran. Istilah lain dari fenomena ini biasa dikenal dengan back fire atau light back.
b. Lift-off
Lift-off merupakan kondisi dimana batas kestabilan yang dicapai
oleh nyala api pada renggang tertentu dari ruang pembakaran,permukaan mulut tabung pembakarantidak tersentuh oleh nyala api. Keadaan nyala api terangkat (lift-off) disebabkan oleh kecepatan nyala api dan sifat campuran aliranreaktan di dekat ujung (mulut) ruang pembakaran. Dengan meningkatnya kecepatan aliran reaktan hingga mencapai kecepatan kritis, nyala ujung akan melompat menuju ke posisi yang jauh dari ujung (mulut) pembakaran dan nyala api menjadi terdorong ke atas.Keadaan nyala terngkat inilah yang dinamakan dengan lift-off, dan api akan padam jika kecepatan reaktan dinaikkan.
c. Blow-off
Blow-off adalah suatu keadaan dimana nyala api matidisebabkanoleh
pembakaran lebih lambat dibandingkan aliran reaktan, oleh sebab itu keadaan ini harus dihindari agar keberlangsungan nyala api dapat terlindung.
2.6. Heptana
Heptana atau C7H16 merupakan senyawa yang termasuk dalam
gugus rantai alkana,dimana memiliki jumlah atom karbon (C) sebanyak tujuh buah dan 16 atom hidrogen (H) dengan struktur H3C(CH2)5CH3.
Ketika digunakan sebagai campuran bahan bakar pada mesin tes anti-ketukan,bahan bakar yang mengandung 100% heptana memiliki angka okta sebesar nol (angka oktan 100 adalah bensin yang mengandung 100% iso-oktana). Angka oktan ini menunjukkan bagaimana kualitas bensin yang digunakan dengan melihat bagaimana perbandingan heptana dan isooktana.Adapun database dari heptana dapat dijelaskan sebagai berikut :
Rumus kimia : C7H16
Massa molar : 100,21 g/mol
Wujud : cairan, tidak berwarna Densitas : 0,648 g/ml, cairan Titik lebur : -90,61o C (182,55 K) Titik didih : 94,42o C (371,58 k) Kelarutan dalam air : bercampur
(Sheet, 2016)
2.7. Penelitian Sebelumnya
Lilis Yuliati (2013) Bereksperimen mempelajari kemungkinan terjadinya pembakaran bahan bakar cair yang stabil pada meso-scale
combustor. Meso-scale combustor yang digunakan berbentuk tube
berdiameter 3,5 mm di dalamnya dipasangkan wire mesh sebagai media pembantu heat recirculation sekaligus sebagai flame holder. Mereka melakukan pengujian dengan bahan bakar liquid campuran antara 70% n-heptana dan 30% etanol, bahan bakar cair tersebut kemudian diatomisasi menjadi droplet menggunakan electrospray (Gambar 2.1).
Hasil dari penelitian menunjukkan menunjukkan bahwa pembakaran bahan bakar cair pada meso-scale combustor dapat terjadi secara stabil dengan debit bahan bakar 1 ml/jam (Gambar 2.2). Dari penelitian didapat kesimpulan bahwa pengaplikasian wire mesh pada combustor memiliki pengaruh yang besar terhadap kestabilan api. Selain itu debit bahan bakar yang digunakan juga harus sangat rendah, karena apabila debit bahan bakar terlalu tinggi dapat mengakibatkan permukaan combustor basah dan akhirnya akan mematikan api.
Gambar 2.2. Proses atomisasi bahan bakar cair menggunakan electrospray Sumber:(Mikami, Maeda, Matsui, Seo, & Yuliati, 2013) Muhammad Rasyid Ridho, et al, (2016) telah melakukan penelitian dengan bertujuan untuk mengetahui pengaruh ruas pemisah stainless steel terhadap flammability limit bahan bakar heksana di dalam meso-scale
combustor. Meso-scale combustor terdiri dari ruang penguap yang terbuat
dari stainless steel dengan menggunakan flame holder lines 8 sebagai resirkulasi panas dan tabung kaca kuarsa dengan diameter dalam 3,5 milimeter. Hasil penelitian menunjukkan bahwa stabilitas nyala api di dalam
meso-scale combustor dapat tercapai dengan menambahkan sisipan tiga
milimeter stainless steel sebagai pemisah antara resirkulator kalor dengan
flame holder(Rasyid & S, 2016).
Gambar 2.3. Detail Dimensi Meso Scale Combustor Sumber : (Rasyid & S, 2016)
M. Mikami, Y. Maeda, K. Matsui et al (2013) telah melakukan penelitian experimental mengenai pembakaran bahan bakar gas dan cair (propana) pada tabung meso scale dengan kawat mesh. Pada penelitian ini tabung pembakaran diberi flame holding berupa kawat mesh, adapun diameter tabung meso scale menggunakan tiga jenis ukuran yang berbeda, yaitu 2,5 mm, 3,5 mm, dan 5,4 mm. Kawat mesh disisipkan pada dua buah potongan tabung meso scalekemudian direkatkan menggunakan lem keramik tahan panas, seperti yang dapat dilihat pada gambar dibawah ini.
Gambar 2.5. Penampakan nyala api pada meso scale combustor. Sumber : (Mikami et al., 2013)
Terdapat 3 jenis nyala api yang terjadi pada penelitian ini yaitu : 1) Nyala stabil pada ujung tabung.
2) Nyala flashback.
3) Nyala stabil pada mesh.
Lilies Yuliati (2018) telah melakukan penelitian tentang stabilitas nyala api dan perilaku api di dalam ruang pembakaran skala mesodengan variasiflame holderberbahan bakar gas butana. Tiga jenisflame
holderyakniwire mesh, pelat datar dengan lubang bundar, dan pelat datar
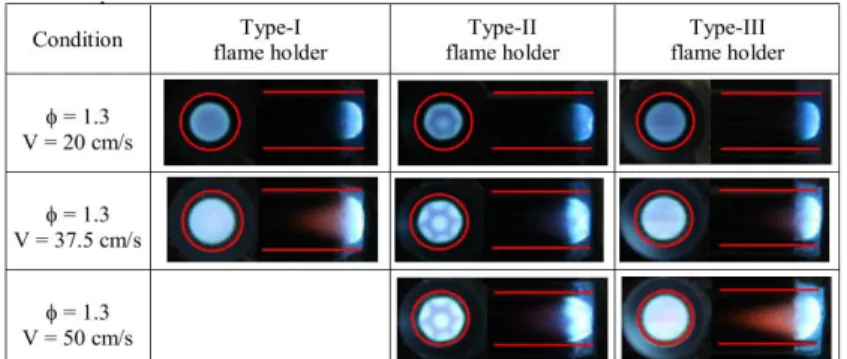
dengan celah sempit, yang mana digunakan untuk meningkatkan stabilitas api di dalam mesoscale combustor.Combustor dengan plat datar - memiliki kestabilan nyala api terbaik, yaitu nyala api stabil yang dihasilkan didalam ruang bakar dengan kecepatan reaktan tertinggi dibandingkan dengan pembakar lain denganFlame holder yang berbeda. Selanjutnya, ruang bakar dengan wire mesh dan disk pipihdengan celah sempit memiliki warna nyala yang relatif seragam pada penampang combustor, dibandingkan dengan visualisasi nyala di dalam mesoscaleruang bakar dengan penahan api dari plat datar dengan lubang bundar.Fenomena ini terkait dengan distribusi reaktan tidak seragam padapenampang pembakaran.(Yuliati, 2018)
Gambar 2.6. Visualisasi nyala api pada meso-scale combustor dengan variasi tipe
flame holder.
Sumber : (Yuliati, 2018)
2.8. Karakteristik Pembakaran pada Meso Scale Combustor
Karakteristik merupakan sifat khas yang sesuai dengan watak tertentu dari suatu objek. Pada penelitian ini yang dimaksudkan karakteristik pembakaran ialah sifat khas dari suatu pembakaran pada
meso scale combustor dengan penambahan mesh sebagai penahan nyala.
Sifat pembakaran yang dibahas pada penelitian ini terkait kestabilan nyala, visualisasi nyala, dan temperatur nyala. dimana kestabilan nyala yang dimaksudkan ialah kisaran batas komposisi antara bahan bakar dengan udara agar terbentuknya nyala api. Visualisasi nyala yang dimaksudkan adalah Bentuk nyala dan warna pada combustor yang dapat berhasil distabilkan dan didokumentasikan menggunakan kamera pada meso scale combustor. Temperatur nyala digunakan untuk mempermudah mengetahui bagaimana nyala api pada combustor. Melalui parameter tersebut kita dapat mengetahi sifat dari suatu pembakaran pada meso scale combustor dengan penambahan mesh.