MEMPELAJARI REAKSI PENCOKLATAN ENZIMATIS
PADA BUAH PISANG DAN APEL
Oleh
ALFONSIUS BIN SIMON
NIM: 100 500 130
PROGRAM STUDI TEKNOLOGI PENGOLAHAN HASIL PERKEBUNAN
JURUSAN TEKNOLOGI PERTANIAN
POLITEKNIK PERTANIAN NEGERI SAMARINDA
SAMARINDA
MEMPELAJARI REAKSI PENCOKLATAN ENZIMATIS
PADA BUAH PISANG DAN APEL
Oleh
ALFONSIUS BIN SIMON
NIM: 100 500 130
Karya ilmiah Sebagai Salah Satu Syarat
Untuk Memperoleh Sebutan Ahli Madya Pada Program Diploma III
Politeknik Pertanian Negeri Samarinda
PROGRAM STUDI TEKNOLOGI PENGOLAHAN HASIL PERKEBUNAN
JURUSAN TEKNOLOGI PERTANIAN
POLITEKNIK PERTANIAN NEGERI SAMARINDA
SAMARINDA
HALAMAN PENGESAHAN
Judul Penelitian : Mempelajari Reaksi Pencoklatan Enzimatis Pada Buah Pisang Dan Apel
Nama : Alfonsius Bin Simon
NIM : 100 500 130
Program Studi : Teknologi Pengolahan Hasil Perkebunan Jurusan : Teknologi Pertanian
Lulus Ujian Pada Tanggal, 21 september 2013
Penguji II,
Edy Wibowo Kurniawan, S. TP., M. Sc NIP. 19741118 200012 1 001 Penguji I, Khusnul Khotimah, S. TP., M. Sc NIP. 19791025 200604 2 002 Pembimbing, Anis Syauqi, S. TP., M. Sc NIP. 19761209 200312 1 002 Mengesahkan, Ketua Jurusan Teknologi Pertanian
Politeknik Pertanian Negeri Samarinda
Heriad Daud Salusu, S. Hut., MP
NIP.19700830 199703 1 001 Menyetujui,Ketua Program Studi
Teknologi Pengolahan Hasil Perkebunan Politeknik Pertanian Negeri Samarinda
Mujibu Rahman, S. TP., M. Si NIP. 19711027 200012 1 002
ABSTRAK
ALFONSIUS BIN SIMON.
Mempelajari Reaksi Pencoklatan Enzimatis
Pencoklatan Terhadap Buah Pisang dan Apel di bawah Bimbingan Bapak
Anis Syauqi.
Latar belakang penelitian ini adalah bahwa buah-buahan memiliki nilai vitamin C dan mineral yang sangat baik dikonsumsi, khususnya pada buah apel dan pisang. Buah ini memiliki manfaat yang sangat baik bagi tubuh misalnya kandungan vitamin C yang terdapat pada buah tersebut yang bisa digunakan sebagai antioksidan. Tujuan penelitian ini adalah untuk mengetahui reaksi pencoklatan enzimatis pada pangan terutamanya pada buah pisang dan apel. Hasil yang diharapkan dari penelitian ini adalah bagaimana cara dapat menghambat pencoklatan enzimatis pada buah sehingga meminimalisasi adanya penurunan mutu pada produk dengan cara mengendalikan reaksi pencoklatan enzimatis yang terjadi pada bahan pangan khususnya pada buah pisang dan apel dengan penambahan inhibitor.
Penelitian ini dilaksanakan di laboratorium Analitik Kimia Politeknik
Pertanian Negeri Samarinda. Penelitian ini mengamati perubahan
intensitas warna pada buah pisang dan apel dengan perendaman dalam
larutan Metabisulfit 1 % dan 5 %, Asam Askorbat, Asam Sitrat, dan Asam
Asetat dengan dua kali ulangan.
Berdasarkan penelitian yang dilakukan pada buah pisang dan apel
dapat disimpulkan bahwa larutan anti pencoklatan yang paling efektif
dalam mencegah reaksi pencoklatan enzimatis adalah larutan metabisulfit
1 %.
RIWAYAT HIDUP
Alfonsius Bin Simon
lahir di Segeliud Estate
tanggal 29 maret 1989. Merupakan anak ke- 5 dari 5
bersaudara dari pasangan Bapak
Simon Jati (Alm)
dan Ibu
Damaris Markus.
Pada tahun 1996 memulai pendidikan di sekolah
Dasar SK. Ulu Dusun sabah Malaysia sampai 1998
dan pindah ke Sekolah Dasar Negeri 251
Balasepang Sulawesi Selatan Tanah Toraja dan lulus pada tahun 2001.
Kemudian melanjutkan Sekolah Menengah Pertama (SMP) Negeri 1
Nunukan Kab. Nunukan dan memperoleh ijazah pada tahun 2004.
Selanjutnya melanjutkan ke Sekolah Menengah Atas ( SMA ) Katolik St.
Santo Gabriel Kab. Nunukan, dan memperoleh ijazah pada tahun 2007.
Pendidikan Perguruan Tinggi dimulai pada Perguruan Tinggi
Politeknik Pertanian Negeri Samarinda, Program Studi Teknologi
Pengolahan Hasil Perkebunan, Jurusan Teknologi Pertanian pada tahun
2010.
Pada bulan Maret - Mei 2013 mengikuti kegiatan Praktik Kerja
Lapang (PKL) di PT. Waru Kaltim Plantation Kecamatan Waru, kabupaten
Penajam Paser Utara, Kalimantan Timur.
Sebagai salah satu syarat untuk memperoleh predikat Ahli Madya
Program Diploma III ( D3 ) Politeknik Pertanian Negeri Samarinda, penulis
menyusun karya ilmiah dengan judul “ Mempelajari Reaksi Pencoklatan
Enzimatis Pada Buah Pisang dan Apel” .
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa atas Rahmat-Nya
sehingga penulis dapat menyelesaikan kegiatan Penelitian Karya Ilmiah
dan penyusunannya.
Penelitian Karya Ilmiah merupakan syarat untuk memperoleh gelar
diploma pada Teknologi Pertanian, Program Studi Pengolahan Hasil
Perkebunan Politeknik Pertanian Negeri Samarinda. Penelitian Karya
Ilmiah disusun berdasarkan hasil pengamatan langsung di Laboratorium
Analitik Kimia Politeknik Pertanian Negeri Samarinda.
Tersusun Karya Ilmiah ini tidak lepas dari bimbingan dan arahan
berbagai pihak, untuk itu dengan segala kerendahan hati dan sikap
hormat penulis mengucapkan terima kasih kepada :
1. Kedua Orang tua serta kakak-kakak tercinta yang telah memberikan dukungan motivasi, dan Doa kepada penulis dalam menyelesaikan studi. 2. Bapak Ir. Wartomo,M.P selaku Direktur Politeknik Pertanian Negeri
Samarinda.
3. Bapak Mujibu Rahman, S.TP., M. Si selaku kepala Program Studi Teknologi Pengolahan Hasil Perkebunan.
4. Bapak Anis Syauqi, S. TP., M. Sc selaku Dosen pembimbing dalam penelitian.
5. Ibu Khusnul Khotimah, S. TP., M. Sc selaku Dosen penguji I
6. Bapak Edy Wibowo Kurniawan, S. TP., M. Sc selaku Dosen penguji II
7. Teman – teman satu angkatan yang telah memberikan motivasi dan dukungan selama melakukan Penelitian.
8. Bapak / Ibu Teknisi yang telah membimbing selama penelitian
Penyusun selaku mahasiswa dari Politeknik Pertanian Negeri Samarinda Mengucapkan banyak terima kasih kepada pihak atas partisipasi dan bimbingannya. Semoga apa yang telah diberikan kepada penyusun mendapatkan pahala dari Tuhan Yang Maha Esa.
Penulis menyadari dalam penyusunan Karya Ilmiah ini masih terdapat kekurangan, untuk itu Penulis mengharapkan saran dan kritik yang bersifat membangun untuk menyempurnakan Karya Ilmiah ini. Demikian Karya Ilmiah ini penulis buat untuk dapat dijadikan acuan pada Penelitian yang akan datang maupun untuk panduan para pembaca laporan ini.
DAFTAR ISI
Halaman
KATA PENGANTAR ... v
DAFTAR ISI ... vii
DAFTAR TABEL... viii
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
I. PENDAHULUAN A. Latar belakang ………... ... 1
B. Tujuan Penelitian………... 2
II. TINJAUAN PUSTAKA A. Tinjauan Umum Pisang……….. ... 3
B. Tinjauan Umum Apel... 4
C. Tinjauan Tentang Browning ... 5
D. Tinjauan Tentang Asam Askorbat ... 7
E. Tinjauan Tentang Asam Sitrat ... 7
F. Tinjauan Tentang Asam Asetat... 8
G. Tinjauan Tentang Metabisulfit ... 9
III. METODE PENELITIAN A. Tempat dan Waktu... 10
B. Alat dan Bahan ... 10
C. Metode Pengumpulan Data ... 11
D. Prosedur Penelitian………... ... 11
IV. HASIL DAN PEMBAHASAN A. Hasil Pengamatan... 14
B. Pembahasan ... 16
V. KESIMPULAN DAN SARAN A. Kesimpulan ... 25
DAFTAR PUSTAK A ... 26 LAMPIRAN... 27
DAFTAR TABEL
Nomor. Halaman
1. Pengamatan Hasil Buah Pisang Pertama ... 14
2. Pengamatan Buah Pisang Kedua... 14
3. Pengamatan Buah Apel Pertama ... 15
DAFTAR GAMBAR
No Halaman
DAFTAR LAMPIRAN
Nomor Halaman
1. Gambar Penimbangan Larutan... 28
2. Gambar Larutan Perendam ... 29
3. Gambar Pengamatan Metabisulfit 1 % Pada Buah Pisang ... 30
1
I.
PENDAHULUAN
A. Latar Belakang
Buah-buahan adalah bahan pangan yang sangat penting sebagai sumber vitamin dan mineral. Pada umumnyabahan pangan ini sangat mudah mengalami pencoklatan pada daging buah jika bahan pangan tersebut terkelupas atau dipotong. Salah satu buah yang mudah mengalami pencoklatan ketika dikupas yaitu buah pisang dan buah apel. Buah pisang dan apel merupakan buah yang paling banyak dikonsumsi oleh masyarakat. Buah ini memiliki manfaat yang sangat baik bagi tubuh misalnya kandungan vitamin C yang terdapat pada buah tersebut yang bisa digunakan sebagai antioksidan. Reaksi ini disebut reaksi pencoklatan karena menyebabkan warnanya berubah menjadi coklat. Pencoklatan (browning) merupakan proses pembentukan pigmen berwarna kuning yang akan segera berubah menjadi coklat gelap (Rahmawati 2008).
Ada beberapa hal yang menyebabkan terjadinya reaksi pencoklatan yaitu salah satunya adalah keberadaan enzim. Reaksi pencoklatan ini dapat diklasifikasikan menjadi dua yaitu reaksi pencoklatan enzimatis dan reaksi pencoklatan non enzimatis. Reaksi pencoklatan enzimatis adalah proses kimia yang terjadi pada sayuran dan buah buahan oleh enzim polifenol oksidase yang menghasilkan pigmen warna coklat (melanin).
Reaksi pencoklatan enzimatis pada bahan pangan memiliki dua macam dampak yaitu dampak yang menguntungkan dan merugikan. Dampak yang menguntungkan misalnya pada teh hitam dan teh hijau dimana reaksi pencoklatan enzimatis bertanggung jawab pada warna dan rasa yang terbentuk. Adapun kerugian yang terjadi akibat reaksi pencoklatan enzimatis
2
yaitu hilangnya nilai gizi pada produk pangan dan merusak rasa dari bahan pangan itu sendiri sehingga perlu dilakukannya langkah-langkah yang dapat meminimalisasi adanya penurunan mutu pada produk dengan cara mengendalikan reaksi pencoklatan enzimatis yang terjadi pada bahan pangan khususnya pada buah pisang dan apel dengan penambahan inhibitor.
B. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui faktor yang dapat mempercepat dan menghambat terjadinya pencoklatan enzimatis dan mengamati pengaruh faktor berdasarkan intensitas warna.
3
II.
TINJAUAN PUSTAKA
A. Tinjauan Umum Pisang (Musa Paradisiaca Linn )
Menurut (Riyadi 2008), pisang adalah tanaman yang bersifat monokarpik, artinya hanya sekali berbuah dan sesudah berbuah akan mati. Tetapi, karena tanaman pisang bersifat merumpun dan berkembang biak dengan tunas, maka keberlangsungan keturunannya bisa berkelanjutan bagai tiada akhir. Jenis pisang mencapai ratusan, tetapi pada dasarnya bisa dibedakan menjadi tiga kelompok yaitu pisang yang tandannya bergantung ke bawah, mendatar, dan tegak ke atas. Pisang yang buahnya enak dimakan adalah salah satu jenis pisang yang tandan buahnya bergantung dan mendatar. Dari jenis pisang yang enak dimakan ini di kenal pisang yang dimakan setelah matang ”buah meja” misalnya pisang Ambon, pisang Raja, pisang Sere, pisang Mas dan lain-lain.
Menurut (Mulyati 2005), pisang adalah tanaman buah berupa herba yang asal mulanya dari kawasan di Asia Tenggara, termasuk Indonesia. Tanaman ini kemudian menyebar ke Daerah Madagaskar di Afrika, Eropa, Amerika Selatan, dan Amerika Tengah. Sebagai bukti penyebaran yang luas, pisang mempunyai nama yang berbeda ditiap tempat. Demikian juga dengan penyebutan pisang dibeberapa tempat di Indonesia. Masyarakat Jawa Barat menamai pisang dengan sebutan Cau, di Jawa Tengah dan Jawa timur dinamakan Gedhang. Jika ditelusuri akan dijumpai penamaan yang beragam disetiap daerah.
Tanaman pisang banyak dimanfatkaan untuk berbagai keperluan hidup manusia. Selain buahnya bagian tanaman lain pula bisa dimanfaatkan, mulai dari bonggol sampai daun (Supriyadi dan Syuanti 2005).
4
Menurut Rukmana (2003) dalam kedudukan pisang dalam sistimatika tumbuhan diklasifikasikan sebagai berikut:
Divisi : Spermatophyta (tumbuhan berbiji)
Subdivisi : Angiospermae (berbiji tertutup )
Klas : Monocotyledoneae (biji keeping satu )
Ordo : Scitaminae
Famili : Musaceae
Genus : Musa
Spesies : Musa Paradisiaca Linn
B. Tinjauan Umum Apel (Malus Sylvestris Mill )
Apel pertama kali ditanam di Asia Tengah, kemudian berkembang luas di wilayah yang lebih dingin. Apel yang dibudidayakan memiliki nama ilmiah
Malus domestica yang Menurut sejarahnya merupakan keturunan dari Malus sieversii dengan sebagian genom dari Malus sylvestris (apel hutan / apel liar) yang ditemui hidup secara liar di pegunungan Asia Tengah, di Kazakhstan, Kirgiztan, Tajikistan, dan Xinjiang, Cina. Tanaman ini masuk ke Indonesia sekitar tahun 1930-an dibawa oleh orang Belanda bernama Kreben kemudian menanamnya di daerah Nongkojajar (Kabupaten Pasuruan). Pada tahun 1953, Bagian Perkebunan Rakyat (sekarang bernama Lembaga Penelitian Hortikultura) mendatangkan beberapa jenis apel dari luar negeri, termasuk Rome Beauty dan Princess Noble. Selanjutnya, sejak tahun 1960 tanaman apel sudah banyak ditanam di Batu, Malang untuk mengganti tanaman jeruk yang mati diserang penyakit. Sejak saat itu tanaman apel terus berkembang hingga sekarang di dataran tinggi Kota Batu,
5
Poncokusumo (Malang) dan Nongkojajar (Pasuruan) dan masa kejayaannya pada sekitar tahun 1970.
Sekarang apel telah tersebar luas di seluruh Indonesia, disukai banyak orang, dan harganya relative terjangkau. Adanya globalisasi perdagangan menyebabkan kita di Indonesia dapat mengkonsumsi apel dariAmerika, Australia, Cina, ataupun Taiwan disamping apel lokal dari Malang. Ketersediaannya melimpah di pasaran dan nyaris tidak tergantung musim. Jadi, setiap saat kita dapat mengkonsumsi apel.
Menurut sistematika, tanaman apel termasuk dalam : Kingdom : Plantae Divisio : Spermatophyta Subdivisio : Angiospermae Klas : Dicotyledonae Ordo : Rosales Famili : Rosaceae Genus : Malus
Spesies : Malus Sylvestris Mill
C. Tinjauan Umum Pencoklatan (Browning)
Peristiwa pencoklatan adalah pristiwa alamiah biasa terjadi pada sistem biologi, suatu proses perubahan adaptif bagian tanaman akibat adanya pengaruh fisik dan biokimia (memar, pengupasan, pemotongan, serangan penyakit, atau kondisi yang tidak normal). Hal ini merupakan gejala alamiah dari proses penuaan, Secara umum pencoklatan dapat dibedakan menjadi 2 macam yaitu :
6
1. Browning enzimatik ialah proses pencoklatan yang terjadi pada buah-buahan yang banyak mengandung substrat senyawa fenolik yang disebabkan oleh pengaruh aktivitas enzim Polypenol Oxidase (PPO), yang dengan bantuan oksigen akan mengubah gugus monophenol menjadi hidroksi phenol, yang selanjutnya diubah lagi menjadi O-kuinon. Gugus O-kuinon inilah yang membentuk warna coklat. Contoh pencoklatan pada buah apel, pencoklatan pada buah peach, pencoklatan pada buah pear, pencoklatan pada buah pisang, dan pencoklatan pada buah salak.
2. Browning non-enzimatik ialah pencoklatan yang sering dijumpai dalam produk bahan olahan. Browning non enzimatik terutama disebabkan reaksi Maillard, yaitu reaksi yang terjadi antara gula pereduksi (melalui sisi keton dan aldehid yang reaktif) dengan asam-amino (melalui gugus amina). Karamelisasi, pencokelatan akibat vitamin C. Reaksi ini banyak terjadi selama penyimpana bahan Reaksi ini dapat menghasilkan warna dan cita rasa yang diinginkan dalam bahan makanan, misalnya pada produk hasil pemanggangan seperti roti, pembuatan dodol, snack, kacang-kacangan, daging panggang, kopi, dan teh. Namun demikian, reaksi ini dapat pula mempunyai pengaruh merugikan, yaitu menurunkan nilai biologis protein terutama untuk asam amino lisin, dapat menghasilkan cita rasa dan tekstur yang tidak disukai (Anonim, 2010). D. Tinjauan Tentang Asam Askorbat
Vitamin C merupakan salah satu jenis vitamin yang larut di dalam air dan memiliki peranan yang penting dalam menangkal berbagai penyakit. Vitamin C juga dikenal dengan nama kimia dari bentuk
7
utamanya yaitu asam askorbat. Vitamin C termasuk golongan vitamin antioksidan yang dapat menangkal berbagai radikal bebas ekstraselular. Beberapa karakteristiknya antara lain sangat mudah teroksidasi oleh panas, cahaya, dan logam. Buah-buahan, seperti jeruk, merupakan sumber utama vitamin C (Anonim, 2011).
Asam askorbat adalah salah satu senyawa kimia yang disebut vitamin C, asam askorbat yang berbentuk bubuk kristal kuning keputihan yang larut dalam air dan memiliki sifat-sifat antioksidan.
E. Tinjauan Tentang Asam Sitrat
Asam sitrat adalah asam trikarboksilat yang tiap molekulnya mengandung tiga gugus karboksilat. Selain itu ada satu gugus hidroksil yang terikat pada atom karbon di tengah. Asam sitrat termasuk asidulan, yaitu senyawa kimia yang bersifat asam dan ditambahkan pada proses pengolahan makanan dengan berbagai tujuan. Asidulan dapat bertindak sebagai penegas rasa dan warna atau menyelubungi after taste yang tidak disukai. Sifat senyawa ini dapat mencegah pertumbuhan mikroba dan bertindak sebagai pengawet. Asam sitrat (yang banyak terdapat dalam lemon) sangat mudah teroksidasi dan dapat digunakan sebagai pengikat oksigen untuk mencegah buah berubah menjadi berwarna coklat. Ini sebabnya mengapa bila potongan apel direndam sebentar dalam jus lemon, warna putih khas apel akan lebih tahan lama. Asam ini ditambahkan pada manisan buah dengan tujuan menurunkan pH manisan yang cenderung sedang sampai di bawah 4,5. dengan turunnya pH maka kemungkinan mikroba berbahaya yang tumbuh semakin kecil. Selain itu pH yang rendah
8
akan mendisosiasi sulfit dan benzoat menjadi molekul-molekul yang aktif dan efektif menghambat mikroorganisme ( Anonim 2011 ).
F. Tinjauan Tentang Asam Asetat
Asam asetat merupakan nama trivial atau namadagang dari senyawa ini, dan merupakan nama yang paling dianjurkan oleh IUPAC. Nama ini berasal dari kata Latin acetum, yang berarti cuka. Nama sistematis dari senyawa ini adalah asam etanoat. Asam asetat glasial merupakan nama trivial yang merujuk pada asam asetat yang tidak bercampur air. Disebut demikian karena asam asetat bebas-air membentuk kristal mirip es pada 16.7 °C, sedikit di bawah suhu ruang. konteks asam-basa, asam asetat juga sering disingkat HAc, meskipun banyak yang menganggap singkatan ini tidak benar. Ac juga tidak boleh disalah artikan dengan lambang unsure Aktinium (Ac).
Asam asetat merupakan salah satu asam karboksilat paling sederhana setelah asam format. Larutan asam asetat dalam air merupakan sebuah asam lemah artinya hanya terdisosiasi sebagian menjadi ion H+ dan CH3COO
.
Asam asetat merupakan pereaksi kimia dan bahan baku industri yang penting. Asam asetat digunakan dalam produksi polimer seperti polietilena tereftalat, selulosa asetat, dan polivinil asetat, maupun berbagai macam serat dan kain. Dalam industri makanan, asam asetat digunakan sebagai pengatur keasaman. Di rumah tangga, asam asetat encer juga sering digunakan sebagai pelunak air (Anonim, 2011).
9
G. Tinjauan Tentang Metabisulfit
Larutan metabisulfit bertujuan untuk mencegah terjadinya browning secara enzimatis maupun non enzimatis, selain itu juga metabisulfit berperan sebagai pengawet. metabisulfit berperan sebagai :
1. Pencegah timbulnya warna coklat
Pada browning non enzimatis, metabisulfit dapat berinteraksi dengan gugus karbonil yang mungkin ada pada bahan. Hasil reaksi tersebut akan mengikat melanoidin sehingga mencegah timbulnya warna coklat. Sedangkan pada browning enzimatis, metabisulfit akan mereduksi ikatan disulfida pada enzim, sehingga enzim tidak dapat mengkatalis oksidasi senyawa fenolik penyebab browning.
2. Pengawet (antimikroba)
Metabisulfit merupakan racun bagi enzim, dengan menghambat kerja enzim esensial. metabisulfit akan mereduksi ikatan disulfida enzim mikroorganisme, sehingga aktivitas enzim tersebut akan terhambat. Dengan terhambatnya aktivitas enzim, maka mikroorganisme tidak dapat melakukan metabolisme dan akhirnya akan mati. metabisulfit akan lebih efektif dalam bentuk yang bebas atau tidak terdisosiasi, sehingga sebelum digunakan metabisulfit dipanaskan terlebih dahulu. Selain itu, metabisulfit yang tidak terdisosiasi akan lebih terbentuk pada pH rendah (2,5 – 4), dan pada pembuatan manisan bengkoang ini, pH rendah atau suasana asam diperoleh dari penambahan asam sitrat(Anonim, 2011).
10
III.
METODE PENELITIAN
A. Tempat dan Waktu Penelitian
1. Tempat
Penelitian ini dilakukan di laboratorium Kimia Analitik Program Studi Teknologi Pengolahan Hasil Perkebunan Politeknik Pertanian Negeri Samarinda.
2. Waktu
Penelitian ini dilaksanakan selama 1 bulan terhitung mulai awal bulan juni hingga akhir bulan Juli 2013 yang meliputi persiapan alat dan bahan hingga penulisan karya ilmiah.
B. Alat dan Bahan
1. Alat
Alat yang digunakan dalam penelitian adalah : a) Pisau b) Piring c) Talenan d) Beaker Glass e) Labu ukur f) Neraca Analitik g) Gelas Ukur h) Spatula i) Stopwatch j) Pinset k) Pipet Tetes l) Pipet Volume
11
2. Bahan
Bahan yang digunakan dalam penelitian adalah : a) Buah pisang b) Buah Apel c) Asam Askorbat d) Asam sitrat e) Asam asetat f) Metabisulfit g) Air
C. Metode Pengumpulan Data
Penelitian ini merupakan penelitian eksperimental. Penelitian eksperimental bertujuan untuk mengetahui suatu gejala atau pengaruh yang timbul akibat adanya perlakuan tertentu.
D. Prosedur Penelitian
1. Persiapan
a. Disiapkan larutan perlakuan ( Aquades, Asam askorbat 1%, Asam Asetat 1%, Asam Sitrat 1%, Metabisulfit 1% dan Metabislufit 5% ) dengan masing-masing volume sebanyak 100 ml.
b. Buah pisang dan apel dipotong sebanyak 6 potongan seragam. c. Masing-masing potongan buah pisang dan apel diberikan perlakuan
dengan cara direndam selama 60 detik ke dalam air, asam askorbat 1% , asam asetat 1%, asam sitrar 1%, metabisulfit 1% dan metabisulfit 5%, kemudian ditiriskan.
d. Buah pisang dan apel yang telah diberikan perlakuan diletakkan pada piring media pengamatan.
12
e. Diamati perubahan warna kecoklatan pada buah apel dimenit ke 0’,10’,20’,40’,60’, dan buah pisang dimenit 0’, 10’, 20’, 40’, 60’, 80’, dan 100’.
2. Perlakuan
Parameter yang diamati dalam penelitian ini yaitu dengan melihat perubahan warna pada buah pisang dan apel agar dapat diketahui faktor- faktor terjadinya reaksi pencoklatan enzimatis serta pengaruh faktor-faktor tersebut terhadap intensitas warna yang tampak pada buah pisang dan apel.
13
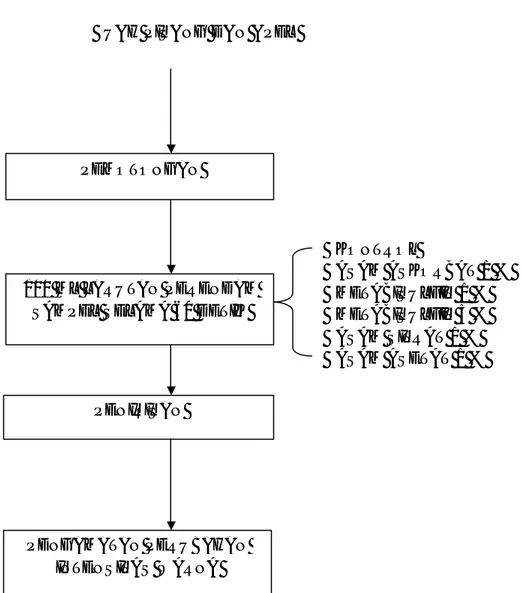
Gambar 1 : Diagram alir proses pencoklatan enzimatis pada buah pisang dan apel
Sumber : ( Zulfahnur Dkk, 2009 ) yang telah dimodifikasi BUAH PISANG DAN APEL
PENGAMATAN PERUBAHAN INTENSITAS WARNA
PEMOTONGAN
100 ML LARUTAN PERENDAM SAMPEL SELAMA 60 DETIK
PENIRISAN ? KONTROL ? ASAM ASKORBAT 1 % ? METABISULFIT 1 % ? METABISULFIT 5 % ? ASAM SITRAT 1 % ? ASAM ASETAT 1 %
14
IV.
HASIL DAN PEMBAHASAN
A. Hasil Pengamatan
1. Tabel 1. Hasil Pengamatan Intensitas Warna Coklat Pada Buah Pisang Ulangan Pertama Menit ke- Kontrol Asam Askorbat 1% Metabisulfit 1% Metabisulfit 5% Asam SItrat 1% Asam Asetat 1% 0’ _ _ _ _ _ _ 10’ + + _ _ + + 20’ ++ + _ _ + + 40’ +++ + _ _ + + 60’ +++ ++ _ _ ++ ++ 80’ +++ ++ _ _ ++ ++ 100’ +++ ++ _ + ++ ++
Sumber : Data Primer 2013
2. Tabel 2. Hasil Pengamatan Intensitas Warna Coklat Pada Buah Pisang Ulangan Kedua
Menit ke- Kontrol
Asam Askorbat 1% Metabisulfit 1% Metabisulfit 5% Asam SItrat 1% Asam Asetat 1% 0’ _ _ _ _ _ _ 10’ - + _ _ + + 20’ + + _ _ + + 40’ + ++ _ _ + ++ 60’ + ++ + _ + ++ 80’ ++ +++ + _ ++ +++ 100’ ++ +++ + + ++ +++
15
3. Tabel 3. Hasil Pengamatan Intensitas Warna Coklat Pada Buah Apel Ulangan Pertama
Menit ke- Kontrol
Asam Askorbat 1% Metabisulfit 1% Metabisulfit 5% Asam SItrat 1% Asam Asetat 1% 0’ _ _ _ _ _ _ 10’ + _ _ _ _ + 20’ ++ + _ _ + ++ 40’ +++ ++ _ _ + ++ 60’ +++ +++ _ + ++ +++
Sumber : Data Primer 2013
4. Tabel 4. Hasil Pengamatan Intensitas Warna Coklat Pada Buah Apel Ulangan Kedua
Menit ke- Kontrol
Asam Askorbat 1% Metabisulfit 1% Metabisulfit 5% Asam SItrat 1% Asam Asetat 1% 0’ _ _ _ _ _ _ 10’ + _ _ _ _ + 20’ ++ + _ _ + ++ 40’ +++ ++ _ + + ++ 60’ +++ +++ _ + ++ +++
Sumber : Data Primer 2013
Keterangan :
- = Tidak bewarna coklat
+ = Hampir sebagian bewarna coklat ++ = Hampir separuh bewarna coklat +++ = Hampir seluruhya bewarna coklat
16
B. Pembahasan
Reaksi pencoklatan dapat dialami oleh buah-buahan dan sayur-sayuran yang tidak berwarna. Reaksi ini disebut reaksi pencoklatan karena menyebabkan warnanya berubah menjadi coklat. Ada beberapa hal yang menyebabkan terjadinya reaksi pencoklatan, salah satunya adalah keberadaan enzim. Reaksi pencoklatan ini dapat diklasifikasikan menjadi dua yaitu reaksi pencoklatan enzimatis dan reaksi pencoklatan non-enzimatis.
Reaksi pencoklatan enzimatis adalah proses kimia yang terjadi pada sayuran dan buah-buahan oleh enzim polifenol oksidase yang menghasilkan pigmen warna coklat (melanin). Proses pencoklatan enzimatis memerlukan enzim polifenol oksidase dan oksigen untuk berhubungan dengan substrat tersebut. Enzim-enzim yang dikenal yaitu fenol oksidase, polifenol oksidase, fenolase/polifenolase, enzim-enzim ini bekerja secara spesifik untuk substrat tertentu ( Winarno, 1995). Reaksi ini dapat terjadi bila jaringan tanaman terpotong, terkupas, dan karena kerusakan secara mekanis.
Buah pisang dan apel ini ketika dikupas ataupun dilakukan pengirisan dapat menyebabkan reaksi pencoklatan pada daging buahnya sendiri, sehingga reaksi pencoklatan tersebut perlu dihambat dengan perlakuan perendaman pada daging buahnya. Pada penelitian ini akan dilakukan beberapa perlakuan yang dapat menghambat terjadinya reaksi pencoklatan enzimatis diantaranya perendaman dengan air (kontrol),
17
asam askorbat 1%, metabisulfit 1%, metabisulfit 5%, asam asetat 1% dan asam sitrat 1%.
1. Pisang a. Kontrol
Pada Tabel. 1, pisang yang direndam dengan air mengalami pencoklatan pada menit ke-10’ hampir sebagian berwarna coklat dan meningkat pada menit ke- 40’ hampir separuhnya berwarna coklat hingga menit ke-100’ hampir seluruhnya berwarna coklat. Sedangkan pada Tabel. 2 pisang yang direndam dengan air mengalami pencoklatan pada menit ke- 20’ hampir berwarna sebagian coklat dan meningkat pada menit ke- 80’ hampir separuhnya berwarna coklat hingga menit ke-100’ hampir seluruhnya berwarna coklat. Hal ini sesuai dengan hasil penelitian menurut Zulfahnur dkk 2009, bahwa dengan perlakuan kontrol air tidak dapat menghambat pencoklatan disebabkan oksigen yang diserap daging buah pisang lebih banyak sehingga mudah terjadinya pencoklatan pada buah kentang dan pir.
b. Asam askorbat 1 %
Pada Tabel. 1 buah pisang yang direndam asam askorbat 1% mengalami pencoklatan pada menit ke- 10’ hampir sebagian berwarna coklat dan meningkat pada menit ke-60’ hampir separuhnya berwarna coklat hingga pada menit ke-100’. Sedangkan pada Tabel. 2 pisang yang direndam asam askorbat 1% mengalami pencoklatan pada menit ke-10’ hampir sebagian
18
berwarna coklat dan meningkat pada menit ke- 40’ hampir separuhnya berwarna coklat hingga pada menit ke-100’ hampir seluruhnya berwarna coklat. Penelitian sebelumnya juga terjadi pencoklatan pada menit ke- 15 bahwa asam askorbat 1 % masih belum efektif menghambat pencoklatan pada buah pisang.
Asam askorbat merupakan senyawa pereduksi yang sangat kuat yang bersifat asam di alam, membentuk garam netral dengan basah, dan memliki kelarutan air yang tinggi Martin, 1994. Penggunaan asam askorbat bertindak sebagai antioksidan karena oksigen akan mengoksidasi askorbat bukan senyawa fenolik sehingga dapat menghambat atau menurunkan terjadinya reaksi pencoklatan. Hal ini sesuai dengan penelitian Zulfahnur dkk 2009, bahwa asam askorbat 1 % baru tampak kecoklatan pada menit 10’. Hal ini menunjukkan bahwa semakin tinggi konsentrasi asam askorbat yang digunakan maka makin efektif penghambatan pencoklatannya.
c. Metabisulfit
1) Metabisulfit 1 %
Pada Tabel. 1 metabisulfit 1 % pada buah pisang sama sekali tidak terjadi pencoklatan sedangkan pada Tabel. 2 buah pisang terjadi pencoklatan pada menit ke- 60’ dimana daging buah pisang hampir sebagian berwarna coklat. 2) Metabisulfit 5 %
Pada Tabel. 1 pada buah pisang terjadi pencoklatan di menit ke- 100’ bahwa hampir sebagian berwarna coklat pada
19
daging buahnya, sedangkan pada Tabel. 2 pada buah pisang terjadinya pencoklatan yang sama di menit ke-100’, daging buah pisang hampir sebagian berwarna coklat.
Penambahan larutan metabisulfit 1 % dan 5 % sebagai senyawa antibrowning bekerja dengan cara membentuk ikatan disufida dengan enzim PPO sehingga menghambat pengikat dengan oksigen. Selain itu sulfit juga dapat beraksi dengan quinon yang dihasilkan dari oksidasi senyawa fenolik sehingga menghambat polimerisasi quinon membentuk pingmen melanin ( coklat ). Dengan adanya metabisulfit buah dan pangan tampak lebih segar, cerah, dan lambat sekali mengalami pencoklatan Margono 1993. Berdasarkan tabel pengamatan terlihat bahwa larutan ini yang paling baik dalam menghambat reaksi pencoklatan pada buah pisang karena hingga menit ke-100’ pada metabisulfit 5 % baru terjadi pencoklatan. Penelitian sebelumnya Zulfahtur dkk 2009 pada buah pisang dengan menggunakan metabisulfit 1 % dan 5 % tidak terjadi pencoklatan dari menit 0’ sampai dengan menit ke- 60’.
d. Asam sitrat 1 %
Pada Tabel. 1 telah terjadi pencoklatan di menit ke-10’ hampir sebagian berwarna coklat dan meningkat pada menit ke-60’ hingga di menit ke-100’ hampir separuhnya berwarna coklat sedangkan pada Tabel. 2 terjadi pencoklatan pada menit ke- 10’ hampir sebagian berwarna coklat dan meningkat di menit ke- 80’ hingga pada menit ke- 100’ hampir separuhnya berwarna coklat.
20
Asam sitrat merupakan senyawa intermediet dari asam organik yang berbentuk kristal atau serbuk putih. Asam sitrat menghambat terjadinya pencoklatan karena dapat mengkompleks ion tembaga yang dalam hal ini berperan sebagai katalis dalam reaksi pencoklatan. Selain itu, asam sitrat juga dapat menghambat pencoklatan dengan cara menurunkan pH sehingga enzim PPO menjadi inaktif (Winarno, 1997).
e. Asam asetat 1 %
Pada Tabel. 1 telah terjadi pencoklatan di menit ke-10’ hampir sebagian berwarna coklat dan meningkat di menit ke-60’ hingga di menit ke-100’ hampir separuhnya berwarna coklat, sedangkan pada Tabel. 2 terjadi pencoklatan di menit ke-10’ hampir sebagian berwarna coklat dan meningkat pada menit ke- 40’ hampir separuhnya berwarna coklat hingga pada menit ke-100’ hampir seluruhnya berwarna coklat.
Asam asetat merupakan asam organik kuat. Asam asetat berperan menurunkan pH jarigan sehingga akan menurunkan kecepatan reaksi pencoklatan enzimatis. Adapun pH optimum fenolase pada kisaran 6-7 dan dibawah 3,0 tidak terjadi aktivitas enzim. Hal ini sesuai dengan Zulfahnur dkk 2009, dapat disimpulkan bahwa kosentrasi asam asetat dapat mempengaruhi keefektifan penghambatan pencoklatan pada kentang.
Pada hasil pembahasan pengamatan intensitas perubahan warna pada buah pisang diatas, dapat dilihat hasil pengamatan pada Tabel 1 dan 2.
21
2. Apel a. Kontrol
Pada Tabel. 1 apel yang direndam dengan air mengalami pencoklatan pada menit ke-10’ hampir sebagian berwarna coklat dan meningkat pada menit ke- 20’ hampir separuhnya berwarna coklat hingga menit ke-60’ hampir seluruhnya berwarna coklat begitupun sebaliknya pada Tabel. 2 yang dilakukan pada buah apel.
Hasil pengamatan intensitas warna kecoklatan pada buah apel pada Tabel. 1 dan 2 bahwa perlakuan kontrol atau perendaman dalam air tidak dapat menghambat terjadinya pencoklatan hal ini disebabkan karena adanya oksigen yang diserap oleh daging buah apel lebih banyak sehingga dimenit 10’ terjadinya perubahan warna. Penelitian sebelumya Zulfahnur dkk 2009, bahwa dengan perlakuan kontrol air tidak dapat menghambat pencoklatan disebabkan oksigen yang diserap daging buah pisang lebih banyak sehingga mudah terjadinya pencoklatan pada buah kentang dan pir.
b. Asam Askorbat 1 %
Pada Tabel. 1 buah apel yang direndam asam askorbat 1% mengalami pencoklatan pada menit ke- 20’ hampir sebagian berwarna coklat dan meningkat pada menit ke- 40’ hampir separuhnya berwarna coklat hingga pada menit ke- 60’ begitupun sebaliknya pada Tabel. 2.
22
Asam askorbat dalam penelitian ini merupakan senyawa pereduksi kuat yang bersifat asam, membentuk garam netral dengan basah dan memiliki kelarutan air yang tinggi Martin, 1994. Dari penelitian sebelumnya zulfhatur dkk 2009, bahwa apel yang direndam dalam asam askorbat 1 % terjadi pencoklatan pada menit ke- 15’
c. Metabisulfit
1) Metabisulfit 1 %
Pada Tabel. 1 pada buah apel sama sekali tidak terjadi pencoklatan sedangkan pada Tabel. 2 pada buah apel tidak terjadi pencoklatan sampai menit ke- 60’ dimana daging buah apel masih kelihatan segar.
2) Metabisulfit 5 %
Pada Tabel. 1 buah apel terjadi pencoklatan pada menit ke- 60’ hampir berwarna coklat sedangkan pada Tabel. 2 buah apel terjadi pencoklatan pada menit ke- 40’ hingga menit ke- 60’ hampir sebagian berwarna coklat.
Metabisulfit dapat mencegah timbulnya reaksi pencoklatan baik yang enzimatis ataupun non enzimatis. Keampuhan metabisulfit dalam hal mencegah reaksi pencoklatan dan sekaligus mengawetkan belum dapat disaingi oleh bahan kimia lain. Itulah sebabnya mengapa metabisulfit luas sekali pemakaiannya. Misalnya untuk sayuran dan buah-buahan kering, beku, asinan, manisan, sari buah, konsentrat, pure, sirup, anggur minuman dan
23
bahkan untuk produk-produk daging serta ikan yang dikeringkan Muchtadi, 1989.
d. Asam Sitrat 1 %
Pada Tabel. 1 telah terjadi pencoklatan di menit ke-20 hampir sebagian berwarna coklat dan meningkat di menit ke-60 hampir separuhnya berwarna coklat sedangkan pada Tabel. 2 terjadi pencoklatan di menit ke- 10’ hampir sebagian berwarna coklat dan meningkat pada menit ke- 60’ hampir separuhnya berwarna coklat.
Asam sitrat menghambat terjadinya pencoklatan karena dapat mengkompleks ion tembaga yang dalam hal ini berperan sebagai katalis dalam reaksi pencoklatan. Selain itu, asam sitrat juga dapat menghambat pencoklatan dengan cara menurunkan pH seperti halnya pada asam asetat sehingga enzim PPO menjadi inaktif Winarno, 1997.
e. Asam Asetat 1 %
Pada Tabel. 1 telah terjadi pencoklatan di menit ke-10’ hampir sebagian berwarna coklat dan meningkat pada menit ke- 20’ hampir separuhnya berwarna coklat hingga pada menit ke-60’ hampir seluruhnya berwarna coklat begitupun sebaliknya pada Tabel. 2.
Asam asetat merupakan asam organik kuat. Asam asetat berperan menurunkan pH jarigan sehingga akan menurunkan kecepatan reaksi pencoklatan enzimatis. Adapun pH optimum
24
fenolase pada kisaran 6-7 dan dibawah 3,0 tidak terjadi aktivitas enzim.
Dalam pembahasan hasil pengamatan pencoklatan pada buah apel diatas dapat dilihat hasil pengamatan intensitas kecoklatan warna pada Tabel 3 dan 4.
25
IV.
KESIMPULAN DAN SARAN
A. Kesimpulan
Faktor yang menyebabkan pencoklatan pada buah pisang dan apel disebabkan ukuran potongan yang terlalu tipis sehingga megakibatkan mudahnya terjadi kontak antara oksigen dengan jaringan bahan, dan terjadinya oksidasi dan bentuk reaksi pencoklatan pada buah pisang dan apel. Larutan yang efektif untuk mencegah atau menghambat pencoklatan pada buah pisang dan apel dengan menggunakan larutan metabisulfit 1 %.
B.
Saran
1. Perlu adanya penelitian selanjutnya pada bahan pagan yang lain yang dapat terjadi reaksi pencoklatan enzimatis pada buah.
2. Disarankan dalam lanjutan penelitian ini agar memperhatikan perendaman buah dalam larutan.
26
DAFTAR PUSTAKA
Anonim, 2011. pengawet (http://id.wikipedia.org/wiki/garam) diakses pada tanggal 29 agustus 2013.
Anonim, 2010. Enzim ( http://harisdianto.files.wordpress.com/2010/01/enzim-com.pdf) diakses pada tanggal 10 september 2013.
Margono, 1993. Buku Panduan Teknologi Pangan, Jakarta
Martin, P. 1994. Food Science and Teknology. Instructional Materials Laboratory, Columbia.
Muchtadi, D.1989. Sulfit Dipermasalahkan dan Nitrit Dikurangi.
(http://web.ipb.ac.id/~tpg/de/pubde_fdsf_sulfit.php) diakses pada tanggal 11 juli 2013.
Mulyati, 2005. Aneka Olahan Pisang, Trubusan Agrisarana Jakarta
Rahmawati, 2008. Pengaruh vitamin C terhadap aktivitas polifenol oksidase buah Apel merah (Pyrus malus) secara in vitro [skripsi]. Surakarta: Universitas Muhammadiyah Surakarta.
Riyadi, 2008. Pasca Panen Pada Pisang, Holtikultura, Jakarta Rukmana, 2003. Usaha Tani Pisang. Penebar Swadaya, Jakarta
Supriyadi, Syuanti , 2005. Budi Daya Pisang Dan Prospek Pasar. Penebaran Swadaya, Jakarta
Winarno, F.G. 1995. Kimia Pangan dan Gizi. Gramedia,Jakarta
Winarno, F. G 1997. Penaganan Buah-buahan Dan Sayur-sayuran Tropis. CV Yasaguna, Jakarta
Zulfahnur dkk, 2009. Mempelajari Enzimatis Pada Buah kreativitas mahasiswa, Bogor
28
Gambar 2. Larutan Perendaman Gambar 1. Penimbangan Larutan
29
Gambar 3. Pengamatan Metabisulfit 1 % Pada Buah Pisang
Menit Ke- 60 Menit Ke- 10 Menit Ke- 20 Menit Ke- 80 Menit Ke- 40 Menit ke- 0 Menit Ke- 100
30
Gambar 4. Pengamatan Metabisulfit 1 % Pada Buah Apel
Menit Ke- 0
Menit Ke- 10
Menit Ke- 40
Menit Ke- 60