BAB II
TINJAUAN PUSTAKA
2.1.Hidrogen
Hidrogen (bahasa Latin: hidrogenium, dari bahasa Yunani: hydro: air, genes:
membentuk) adalah unsur kimia pada tabel periodik yang memiliki simbol H dan
nomor atom 1. Pada suhu dan tekanan standar, hidrogen tidak berwarna, tidak berbau,
bersifat non-logam, bervalensi tunggal, dan merupakan gas diatomik yang sangat
mudah terbakar. Dengan massa atom 1,00794 amu, hidrogen adalah unsur teringan di
dunia (Neni.M 2008).
Dalam keadaan normal di bumi, unsur hidrogen berada dalam keadaan gas
diatomik,yaitu terdiri dari 2 atom dengan lambang H2. Namun, gas hidrogen
sangatlah langka di atmosfer bumi (1 ppm berdasarkan volume) oleh karena beratnya
yang ringan yang menyebabkan gas hidrogen lepas dari gravitasi bumi. Walaupun
demikian, hidrogen masih merupakan unsur paling melimpah di permukaan bumi ini.
Kebanyakan hidrogen bumi berada dalam keadaan bersenyawa dengan unsur lain
seperti hidrokarbon dan air. Gas hidrogen dihasilkan oleh beberapa jenis bakteri dan
ganggang (Neni. M 2008).
2.2.Air
Air adalah senyawa gabungan antara dua atom hidrogen dan satu atom oksigen
Kuncoro,2009pengertian air merupakan suatu senyawa kimia sederhana yang terdiri
atas 2 atomhidrogen (H) dan 1 atom Oksigen (O). Air mempunyai ikatan Hidrogen
yangcenderung bersatu padu untuk menentang kekuatan dari luar yang
akanmemecahkan ikatan- ikatan ini.
2.3.ELEKTROLISIS
Elektrolisis berasal dari kata elektro (listrik) dan lisis (penguraian), yang berarti
penguraian senyawa oleh arus listrik, dan alatnya disebut sel elektrolisis. Dengan kata
lain, sel elektrolisis ini memerlukan energi listrik untuk memompa electron dan
prosesnya kebalikan dari proses sel Galvani. Dalam sel ini harus ada partikel (ion,
molekul, atom) yang dapat menerima elektron dan yang melepaskan elektron (Syukri.
S 2009). Dalam reaksi elektrolisis terdiri dari sumber listrik DC (searah), Elektroda,
Larutan elektrolit.
2.3.1. Sumber Listrik searah (DC)
Sumber listrik searah adalah sumber listrik dengan tipe arus dimana elektron
yang bergerak hanya dari kutub negatif bergerak melalui kabel penghantar ke kutub
positif dalam satu arah saja. Sumber arus listrik searah adalah batterai atau jika
menggunakan listrik perumahan yang merupakan sumber arus AC(bolak-balik) maka
perlu digunakan adaptor untuk mengubah tipe arusnya. Adaptor merupakan
kumpulan alat-alat listrik yang berisi trafo untuk menurunkan tegangan sesuai dengan
kriteria yang diinginkan dan mengubah arah arus menjadi searah. Untuk itu dalam
2.3.2. Elektroda
Elektroda adalah konduktor yang digunakan untuk bersentuhan dengan bagian
atau media non- logam dari sebuah sirkuit (misal semikonduktor, elektrolit atau
vakum). Elektroda ada 2 macam ;
a. Elektroda inert, yaitu elektroda yang tidak mudah bereaksi. Unsur yang
termasuk di dalam elektroda inert adalah yaitu platina (Pt), emas (Aurum/Au),
dan karbon (C)
b. Elektroda tak inert, yaitu elektroda yang mudah bereaksi.Unsur yang termasuk
di dalam elektroda tak inert adalahzat lainnya selain Pt, C, dan Au. Elektroda
yang digunakan dalam percobaan ini adalah carbon karena bersifat inert.
Konduktivitas elektroda listrik dapat dilihat pada deret volta.
Kemampuan menghantarkan listrik dari suatu logam dapat dilihat pada deret volta
dimana semakin ke kanan maka akan semakin mudah menghantarkan listrik.
Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co N i Sn Pb H Sb Bi Cu Hg Ag Pt Au
(Farid M dkk 2012)
2.3.3. Larutan Elektrolit
Elektrolit adalah suatu zat terlarut atau terurai ke dalam bentuk ion-ion dan
selanjutnya larutan menjadi konduktor elektrik. Umumnya, air adalah pelarut (solven)
yang baik untuk senyawa ion dan mempunyai sifat menghantarkan arus listrik.
menyala karena air tersebut merupakan konduktor listrik yang sangat jelek. Apabila
suatu senyawa ion yang larut seperti NaOH ditambahkan pada air, maka solutnya
akan larut sehingga bola lampu mulai menyala dengan terang. Senyawa seperti NaOH
yang membuat larutan menjadi konduktor listrik (Brady, 1999). Elektrolit yang
digunakan dalam penelitian ini adalah larutan causticsoda.
2.3.4. Proses Redoks
Proses oksidasi dan reduksi sebagai reaksi pelepasan dan penangkapan
elektron oleh suatu zat. Oksidasiadalah proses pelepasan elektron dari suatu zat
sedangkan reduksi adalah proses penangkapan electron oleh suatu zat. Bentuk
teroksidasi sering ditandai dengan “ox” dan bentuk tereduksi ditandai dengan “red”.
Kesetimbangan reaksinya ditulis sebagai berikut:
ox + ne = red (proses reduksi)………...(Persamaan 2.1)
red = ox + ne (proses oksidasi)………..……(Persamaan 2.2)
Keterangan : ox = oksidasired = reduksi ne = Jumlah elektron(Rivai 1995)
Sel elektrolisis adalah sel elektrokimia yang bereaksi secara tidak spontan (Eo sel (-)
atau ΔG>0), karena energi listrik disuplai dari sumber luar dan dialirkan melalui
sebuah sel. Elektrolisis diartikan juga sebagai peristiwa penguraian zat elektrolit oleh
arus listrik searah, melainkan juga mengalami perubahan-perubahan kimia.
Perubahan kimia yang terjadi selama elektrolisis dapat dilihat sekitar elektroda.
Elektroda adalah suatu sistem dua fase yang terdiri dari sebuah penghantar elektrolit
positif (+) disebut anoda sedangkan elektroda negatif (-) adalah katoda (Svehla,1985).
Reaksi kimia yang terjadi pada elektroda selama terjadinya konduksi listrik disebut
elektrolisis dan alat yang digunakan untuk reaksi ini disebut sel elektrolisis. Sel
elektrolisis memerlukan energi untuk memompa elektron. (Brady, 1999).
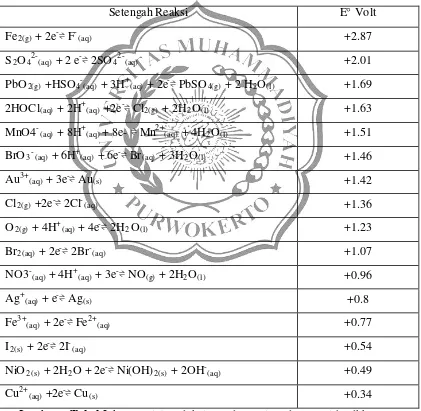
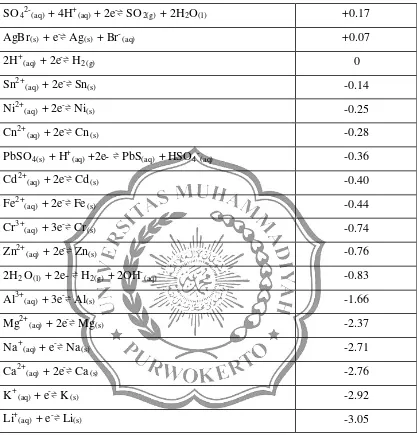
Tabel 2.1Potensial Reduksi Standart (Ni Made Yasmithadkk 2009)
Setengah Reaksi E° Volt
Fe2(g) + 2e-⇌ F-(aq) +2.87
S2O42-(aq) + 2 e-⇌ 2SO42-(aq) +2.01
PbO2(g) +HSO4-(aq) + 3H+(aq) + 2e-⇌ PbSO4(g) + 2 H2O(l) +1.69
2HOCl(aq) + 2H+(aq) +2e-⇌ Cl2(g) + 2H2O(l) +1.63
MnO4-(aq) + 8H+(aq) + 8e- ⇌ Mn2+(aq) + 4H2O(l) +1.51
BrO3-(aq) + 6H+(aq) + 6e-⇌ Br(aq) + 3H2O(l) +1.46
Au3+(aq) + 3e-⇌ Au(s) +1.42
Cl2(g) +2e-⇌ 2Cl-(aq) +1.36
O2(g) + 4H+(aq) + 4e-⇌ 2H2O(l) +1.23
Br2(aq) + 2e-⇌ 2Br-(aq) +1.07
NO3-(aq) + 4H+(aq) + 3e-⇌ NO(g) + 2H2O(l) +0.96
Ag+(aq) + e-⇌ Ag(s) +0.8
Fe3+(aq) + 2e-⇌ Fe2+(aq) +0.77
I2(s) + 2e-⇌ 2I-(aq) +0.54
NiO2(s) + 2H2O + 2e-⇌ Ni(OH)2(s) + 2OH-(aq) +0.49
Cu2+(aq) +2e-⇌ Cu(s) +0.34
SO42-(aq) + 4H+(aq) + 2e-⇌ SO2(g) + 2H2O(l) +0.17
AgBr(s) + e-⇌ Ag(s) + Br-(aq) +0.07
2H+(aq) + 2e-⇌ H2(g) 0
Sn2+(aq) + 2e-⇌ Sn(s) -0.14
Ni2+(aq) + 2e-⇌ Ni(s) -0.25
Cn2+(aq) + 2e-⇌ Cn(s) -0.28
PbSO4(s) + H+(aq) +2e- ⇌ PbS(aq) + HSO4-(aq) -0.36
Cd2+(aq) + 2e-⇌ Cd(s) -0.40
Fe2+(aq) + 2e-⇌ Fe(s) -0.44
Cr3+(aq) + 3e-⇌ Cr(s) -0.74
Zn2+(aq) + 2e-⇌ Zn(s) -0.76
2H2O(l) + 2e- ⇌ H2(g) + 2OH-(aq) -0.83
Al3+(aq) + 3e-⇌ Al(s) -1.66
Mg2+(aq) + 2e-⇌ Mg(s) -2.37
Na+(aq) + e-⇌ Na(s) -2.71
Ca2+(aq) + 2e-⇌ Ca(s) -2.76
K+(aq) + e-⇌ K(s) -2.92
Li+(aq) + e-⇌ Li(s) -3.05
Tabel ini menampilkan data energi dalam listrik yang dibutuhkan agar reaksi
dapat berlangsung tanda – (minus) menunjukan bahwa reaksi berlangsung tidak
spontan ( membutuhkan energi dari luar) sedangkan yang bertanda + (positif)
menunjukan bahwa reaksi berlangsung spontan dan menghasilkan energi
Pada elektroda anoda: 4OH- →Ο2+ 4 e− + 2H2O
Reaksi keseluruhan: 2H2O→ H2+ O2
Elektrolisis ini berkaitan dengan adanya Electromotive Force (emf) atau gaya gerak
listrik (GGL) atau disebut driving force biasanya dinyatakan dalam volt (V). Emf sel
dapat diukur hanya dengan mengetahui voltmeter pada duaelektroda. Emf sel hanya
terjadi pada perbedaan antara dua elektroda potensial (Yoder et.al., 1975). Adapun
ketentuan-ketentuan dalam menghitung e.m.f (electromotive force) dalam sel
elektrokimia antara lain:
a. Reaksi yang terjadi pada elektroda anoda terjadi reaksi oksidasi sedangkan reaksi
reduksi terjadi pada elektroda katoda.
b. E.m.f standar sel dinyatakan sebagai potensial standar elektroda yang dihitung
menggunakan rumus sebagai berikut: Emf = Ekatoda – Eanoda
c. Apabila Emf dihitung dengan menggunakan persamaan (b) didapatkan nilai positif
yang berarti spontan maka reaksi yang terjadi pada sel galvanik sebaliknya nilai
negatif yang berarti tidak spontan maka reaksi yang terjadi pada sel elektrolisis.
(Dogra, 1990)
2.4. Penelitian yang telah dilakukan
PenelitianNi Made Ayu Yasmitha Andewi dkk,2009 dilakukan proses
elektrolisis dengan variasi tegangan dan variasi kadar salinitas. Elektrolit yang
digunakan adalahNaCl (natrium chlorida) dengan variasi tegangan(2,1V;6V;12V) dan
sebagai anoda dan stainless steel sebagai katoda akan dialiri arus bermuatan positif
padaanoda dan bermuatan negatif pada katoda. Penelitian dilakukan selama 180
menit. Hasil penelitianterlihat bahwa salinitas dan tegangan mempengaruhi produksi
gas hidrogen. Semakin besar salinitasyang digunakan maka produksi gas hidrogen
semakin banyak. Begitu juga dengan tegangan, semakinbesar tegangan yang
diberikan semakin banyak produksi gas hidrogen. Produksi optimum sebesar98mL
didapatkan pada salinitas 35% dan tegangan 12 volt.
Penelitian M. Farid R. R., dkk 2012 menyatakan bahwa hasil elektrolisis
dengan menggunakan larutan elektrolit KOH mampu menghasilkan gas Hidrogen
dengan kemurnian 98.56% yang dianalisa dengan menggunakan alat GCMS.