Uji Validasi Pada Estimasi Kandungan Kafein Dan Asam Sitrat Dalam Minuman Energi Secara Spektrofotometri Derivatif
Teks penuh
Gambar
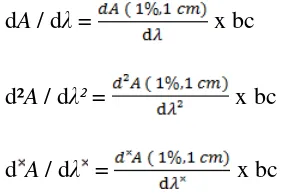
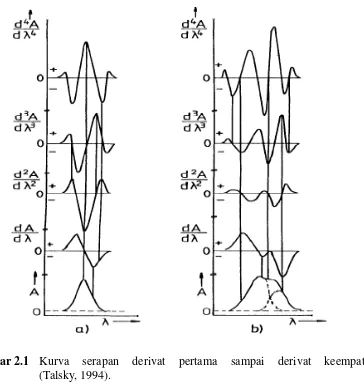
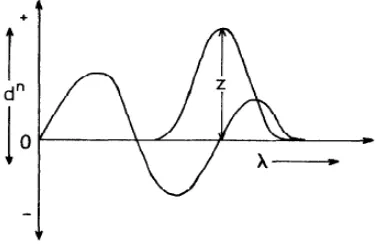
Dokumen terkait
Surat undangan ini disamping dikirimkan melalui e-mail juga akan ditempatkan dalam pengumuman / berita LPSE Provinsi Jawa Tengah, oleh karenanya Pokja 3 tidak dapat menerima
1 Sikap bersyukur Penilaian diri Kegiatan awal sampai akhir 2 Sikap ingin tahu Pengamatan, Penilaian Diri Kegiatan inti dan Penutup 3 Sikap kerja sama Pengamatan Kegiatan inti
PENGADAAN JASA KONSULTASI PADA BINA MARGA PROVINSI JAWA TENGAH ANGGARAN APBD 2013. alasan perubahan jadwal untuk memberikan kesempatan kepada penyedia jasa
Kegiatan Pemeliharaan Saluran Irigasi Pekerjaan Pemeliharaan Saluran Irigasi Desa
SATWIKA SARANA X Paket pekerjaan yang ditawarkan bukan untuk pembangunan gedung PLUT KUMKM Provinsi Jawa Tengah, jangka waktu pelaksanaan pekerjaan lebih dari 120 hari
Lampiran : Surat Panitia Pengadaan Barang/ Jasa Konstruksi Dinas Energi dan Sumber Daya Mineral Provinsi Jawa Tengah TA.. Asli
Demikian Penetapan ini kami buat untuk dapat dipergunakan sebagaimana mestinya.. Semarang, 9
Demikian Penetapan ini kami buat untuk dapat dipergunakan sebagaimana mestinya.. Semarang, 9