TINJAUAN KEPUSTAKAAN
2.1. Penyakit GinjalKronik 2.1.1. Definisi
Penyakit ginjal kronik merupakan masalah kesehatan diseluruh
dunia.Angka kejadiannya terus meningkat mempunyai prognosis yang
buruk,dan memerlukan biaya perawatan yang lebih mahal.Di Amerika
Serikat dijumpai prevalensi yang tinggi dari penyakit ginjal kronis tahap
awal danjuga terjadi peningkatan insidens dan prevalensi gagal ginjal
(National Kidney Foundation,2002)
Penyakit ginjal kronik (PGK) meliputi beberapa proses patofisiologi
yang dikaitkan dengan kelainan fungsi ginjal dan penurunan progresif dari laju
filtrasi glomerulus. Berdasarkan pedoman Kidney Dialysis Outcomes
Quality Initiative (KDOQI), penyakit ginjal kronik dapat dikIasifikasikan
dalam 5 tingkat (1-5). Gagal ginjal kronik (GGK) adalah proses ireversibel
dengan penurunan nefron berlanjut yaitu pada penyakit ginjal kronik tingkat
3-5. Definisi gagal ginjal kronik (GGK) adalah kerusakan ginjal atau laju
filtrasi glomerulus (LFG) dibawah 60 ml/menit/1.73 m2 selama 3 bulan
atau lebih, apapunpenyebabnya.
Prevalensi penyakit ginjal tahap akhir (end stage renal disease,
ESRD) meningkat secara dramatis. Di Amerika Serikat terjadi peningkatan
ini, penyakit ginjal kronik perlu mendapat perhatian besar.
Pada tahun 2002, National Kidney Foundation (NKF) Kidney Disease
Outcome Quality Initiative (K/DOQI) telah menyusun pedoman praktis
penatalaksanaan klinik tentang evaluasi, klasifikasi, dan stratifikasi
penyakit ginjal kronik.
Kriteria Penyakit Ginjal Kronik menurut NKF-K/DOQI :
1. Kerusakan ginjal yang terjadi lebih dari 3 bulan, berupa kelainan
struktural atau fungsional, dengan atau tanpa penurunan laju filtrasi
glomerulus (LFG), denganmanifestasi:
- Kelainanpatologis
- Terdapat tanda kelainan ginjal, termasuk kelainan dalam komposisi darah atau urin, atau kelainan dalam tes pencitraan (imaging tests
Terdapat tanda kelainan ginjal, termasuk kelainan dalam komposisi
darah atau urin, atau kelainan dalam tes pencitraan (imagingtests)
2. Laju filtrasi glomerulus < 60 ml/menit/1,73m2 selama 3 bulan, dengan
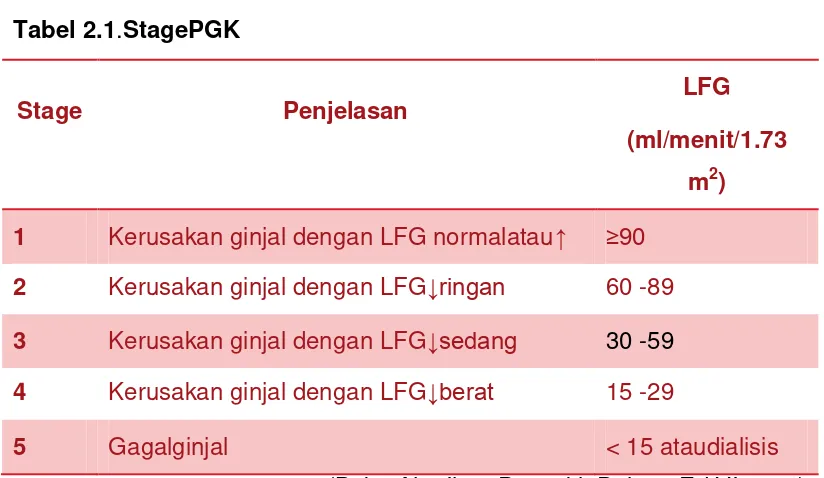
2.1.2. Klasifikasi penyakit ginjal kronik Tabel 2.1.StagePGK
Stage Penjelasan
LFG
(ml/menit/1.73
m2)
2 Kerusakan ginjal dengan LFG↓ringan 60 -89
4 Kerusakan ginjal dengan LFG↓berat 15 -29
(Buku Ajar Ilmu Penyakit Dalam ,Ed.VI,2014)
Dalam hal untuk klasifikasi stage penyakit ginjal kronik maka
penting untuk menaksir laju filtrasi glomerulus (LFG/GFR). Ada 2
persamaan (equation) yang sering dipakai pada orang dewasa, yaitu
Modification of Diet in Renal Disease Study (MDRD) dan Cockcroft-Gault,
yang menggabungkan pengukuran konsentrasi kreatinin plasma, umur,
jenis kelamin, ras dan berat badan (Tabel2.2)
5 Gagalginjal < 15 ataudialisis
1 Kerusakan ginjal dengan LFG normalatau↑ ≥90
Tabel 2.2. Persamaan untuk menaksir LFG
Pada tahun 2012 definisi PGK ditinjau ulang oleh Kidney Disease:
Improving Global Outcomes (KDIGO). Menurut KDIGO, Penyakit Ginjal
Kronik didefinisikan sebagai kelainan struktural atau fungsional ginjal yang
terjadi lebih dari 3 bulan dengan implikasi pada kesehatan. Adapun kriteria
penyakit ginjal kronik menurut KDIGO berdasarkan pemeriksaan albumin
urin, sedimen urin, elektrolit, histologi, pencitraan dan riwayat transplantasi
Tabel 2.3. Kriteria Penyakit Ginjal Kronik
(KDIGO 2012)
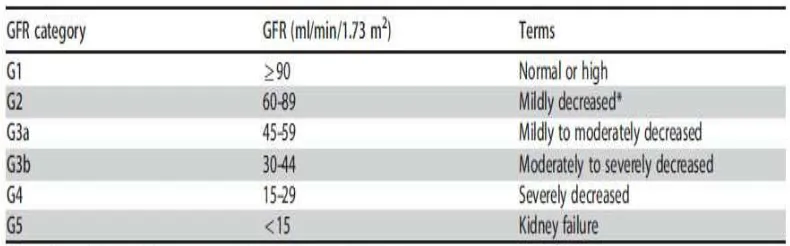
Menurut KDIGO 2012, klasifikasi penyakit ginjal kronik didasarkan
atas penyebab, laju filtrasi glomerulus (Tabel 2.4) dan kategori albuminuria
(Tabel 2.5).
Tabel2.4.Laju Filtrasi Glomerulus pada PGK
2.1.3. Epidemiologi
Di Amerika Serikat, data tahun 1995-1999 menyatakan insidens penyakit
ginjal kronik diperkirakan 100 kasus perjuta penduduk pertahun, dan
angka ini meningkat sekitar 8% setiap tahunnya. Di Malaysia dengan
populasi 18 juta, diperkirakan terdapat 1800 kasus baru gagal ginjal
pertahunnya.Di Negara-negara berkembang lainnya, insidens ini
diperkirakan sekitar 40-60 kasus perjuta penduduk
pertahun(Suwitra.K,Buku Ajar Ilmu Penyakit Dalam,Ed.VI,2014)
Menurut data the National Health and Nutrition Education Survey
(NHANES) prevalensi penyakit ginjal kronis atau disebut juga Chronic
Kidney Disease (CKD) pada orang dewasa usia 20 tahun keatas di
Amerika Serikat diperkirakan 11% dari populasi, dimana 6.3% dari
populasi merupakan kombinasi stage 1 dan 2, 4.3% stage 3, dan 0.2%
merupakan stage 4 dan 5.(Mcciellan et al.,2009)
Di Amerika Serikat, terjadi kenaikan insiden dan prevalensi gagal
ginjal, yang menyebabkan hasil yang buruk dan biaya yang tinggi.
Penyakit ginjal kronis (PGK) mempengaruhi sekitar 11% dari Populasi
orang dewasa Spanyol.(Marrow.,et al D.A 2006 ).Selanjutnya, PGK terkait
dengan serangkaian komplikasi, termasuk anemia (yaswir et al., 2012)
yang telah dikaitkan dengan morbiditas yang lebih tinggi dan mortalitas
dan perkembangan PGK. Penyakit ginjal kronik saat ini merupakan
masalah kesehatan yang penting mengingat insidennya yang meningkat.
Di Indonesia, diperkirakan jumlahnya 100 penderita per satu juta
diperkirakan sebanyak 36 juta orang warga meninggal akibat gagal
ginjal.Penyakit gagal ginjal kronik merupakan penyakit yang diderita oleh 1
dari 10 orang dewasa.Menurut Pernefri 2010 diperkirakan ada 70 ribu
penderita gagal ginjal di Indonesia. Hasil rekam medik RSUP Dr. Soeradji
Tirtonegoro Klaten menunjukkan bahwa perbandingan jumlah pasien
gagal ginjal kronik dengan hemodialisis antara tahun 2010 dan 2011
terdapat peningkatan jumlah pasien yang cukup signifikan, yaitu sebesar
25 % (Rekam Medik,2010/2011).
Berdasarkan hasil penelitian Ginting (2008) terjadi peningkatan
penderita penyakit ginjal kronik di RSUP H.Adam Malik Medan,dimana
selama periode 2004-2007 terdapat 934 penderita penyakit ginjal kronik
yang sangat drastiss mencapai 633 penderita padatahun 2011(Siregar
BY,2012)
2.1.4. Etiologi
Penyebab dari gagal ginjal kronis antara lain :
1. Infeksi saluran kemih ( pielonefritiskronis)
2. Penyakit peradangan(glomerulonefritis)
3. Penyakit vaskuler hipertensi (nefrosklerosis,stenosis arterirenalis)
4. Gangguan jaringan penyambung(SLE,Poliarteritisnodusa,sklerosis)
5. Penyakit kongenital dan herediter(Penyakit ginjalpolikistik)
6. Penyakit metabolik (DM, gout,hiperparatiroidism)
7. Nefropatitoksik
Penyakit ginjal kronik merupakan suatu keadaan yang dapat menjadi
tahapan End Stage Renal Disease (ESRD) dan membutuhkan terapi
dialisa atau transplantasi ginjal. Penyakit ginjal kronik dapat terjadi pada
dewasa maupun anak-anak,dan penyebab penyakit ini adalah berbeda-
beda. (Sudoyo et al., Buku Ajar Ilmu Penyakit Dalam, edisi IV,2006)
2.1.5. Patofisiologi gagal ginjalkronik
Patofisiologi penyakit ginjal kronik pada awalnya tergantung pada
penyakit yang mendasarinya,tapi dalam perkembangan selanjutnya
proses yang terjadi kurang lebih sama.Pengurangan massa ginjal
menyebabkan hipertropi sisa nefron secara struktural dan fungsional
sebagai upaya kompensasi.Hipertropi kompensatori ini akibat hiperfiltrasi
adaptif yang diperantarai oleh penambahan tekanan kapiler dan aliran
glomerulus.
Proses adaptasi ini berlangsung singkat akhirnya diikuti oleh proses
maladaptasi berupa sklerosis nefron yang masih tersisa.Proses ini
akhirnya diikuti dengan penurunan fungsi nefron yang progresif walaupun
penyakit dasarnya sudah tidak aktif lagi.Adanya peningkatan aktifitas
aksis renin-angiotensin-aldosteron intrarenal ikut memberikan kontribusi
terhadap terjadinya hiperfiltrasi, sklerosis dan progresifitas tersebut.
Aktifitas jangka panjang aksis renin - angiotensin - aldosteron, sebagian
diperantarai oleh growth factor β.Beberapa hal yang juga dianggap
berperan terhadap terjadinya progresifitas penyakit ginjal kronis adalah
Pada stadium yang paling dini penyakit ginjal kronik terjadi
kehilangan daya cadang ginjal (renal reserve), pada keadaan mana basal
LFG masih normal atau malah meningkat. Kemudian secara perlahan tapi
pasti akan terjadi penurunan fungsi neuron yang progresif,yang ditandai
dengan peningkatan kadar urea dan kreatinin serum. Sampai pada LFG
sebesar 60 %, pasien masih belum merasakan keluhan. (asimtomatik),
tapi sudah terjadi peningkatan kadar urea dan kreatinin serum.Sampai
pada LFG sebesar 30 %, mulai terjadi keluhan pada pasien seperti
nokturia,badan lemah,mual,nafsu makan kurang dan penurunan berat
badan.Sampai pada LFG dibawah 30 %, pasien memperlihatkan gejala
dan tanda uremia yang nyata seperti anemia,peningkatan tekanan darah,
gangguan metabolisme fosfor dan kalsium,pruritus,mual,muntah dan lain
sebagainya.Pasien juga mudah terkena infeksi seperti infeksi saluran
kemih,infeksi saluran nafas,maupun infeksi saluran cerna.Juga akan
terjadi gangguan keseimbangan air seperti hipo atau hipervolemia,
gangguan keseimbangan elektrolit antara lain natrium dan kalium.Pada
LFG dibawah 15 % akan terjadi gejala dan komplikasi (renal replacement
therapy) antara lain dialisis atau transplantasi ginjal. Pada keadan ini
pasien dikatakan sampai pada stadium gagalginjal.
2.1.5. Hemodialisis
Hemodialisis merupakan suatu proses yang digunakan pada pasien
dalam keadaan sakit akut dan memerlukan terapi dialisis jangka pendek
ginjal stadium akhir atau end stage renal disease (ESRD) yang
memerlukan terapi jangka panjang atau permanen.Tujuan hemodialisa
adalah untuk mengeluarkan zat-zat nitrogen yang toksik dari dalam darah
dan mengeluarkan air yang berlebihan. (R.Roesli et al 2006).
Hemodialisis adalah proses pembersihan darah oleh akumulasi
sampah buangan.Hemodialisis digunakan bagi pasien dengan gagal ginjal
tahap akhir atau pasien berpenyakit akut yang membutuhkan dialisis
waktu singkat.Pada hemodialisis aliran darah yang penuh dengan toksin
dan limbah nitrogen dialihkan dari tubuh pasien ke dializer tempat darah
tersebut dibersihkan dan kemudian dikembalikan lagi ketubuh pasien.
Sebagian besar dializer merupakan lempengan rata atau serat artifisial
ginjal berongga yang berisi ribuan tubulus selofan yang halus dan bekerja
sebagai membran semi permiabel. Aliran darah akan melewati tubulus
tersebut sementara cairan dialisat bersirkulasi disekelilingnya. Pertukaran
limbah dari darah ke dalam cairan dialisat akan terjadi melalui membran
tubulus.
Terdapat tiga prinsip yang mendasari kerja hemodialisis, yaitu difusi,
osmosis, ultrafiltrasi. Toksin dan zat limbah di dalam darah dikeluarkan
melalui proses difusi dengan cara bergerak dari darah yang memiliki
konsentrasi tinggi ke cairan dialisat dengan konsentrasi yang lebih rendah.
Cairan dialisat tersusun dari semua elektrolit yang penting dengan
konsentrasi ekstrasel yang ideal. Kelebihan cairan dikeluarkan dari dalam
tubuh melalui proses osmosis. Pengeluaran air dapat dikendalikan dengan
tekanan yang lebih tinggi (tubuh pasien) ke tekanan yang lebih rendah
(cairan dialisat). Gradien ini dapat ditingkatkan melalui penambahan
tekanan negative yang dikenal sebagai ultrafiltrasi pada mesin dialisis.
Tekanan negative diterapkan Pada alat ini sebagai kekuatan penghisap
pada membran dan memfasilitasi pengeluaran air. (Raharjo et al., Buku
Ajar Ilmu Penyakit Dalam .2011).
2.1.6 Anemia pada penyakitkronik 2.1.6.1. Defenisianemia
Kriteria Kidney Disease Outcome Quality Initiative (KDOQI) dan
national Kidney Foundation (NKF) (2006) mengenai anemia pada penyakit
ginjal kronis, apabila kadar Hb <13,5 pada laki-laki,Hb <12 gr/dl pada
perempuan ( National Kidney Foundation, clinical practice guidelines for
anemia of chronic kidney disease., 2006)
2.1.6.2. Defenisi anemia pada penyakitkronik
Anemia pada penyakit kronik, merupakan anemia dengan
prevalensi terbanyak kedua setelah anemia yang disebabkan defisiensi
besi, terjadi pada pasien dengan aktivasi immun yang akut atau
kronis,kondisi tersebut di istilahkan anemia inflamasi. Kondisi frekuensi
terbanyak yang tergabung dalam anemia pada penyakit kronik.( Weiss G
et al.,2005)
Anemia penyakit kronis dimotori oleh immun, sitokin dan sel-sel dari
sel sistem retikuloendotethel menginduksi perubahan pada
hemostasis besi, proliferasi dari eritroid sel progenitor,produksidari
erithropoietindansiklushidupseldarahmerahdanseluruhnyaterlihat pada
Human Immunodefisiensi virus( HIV). Infeksi hepatitis Cdanmalaria.
Bahkan sel tumor dapat memproduksi proinflamasisitokindan radikal
bebas yang dapat merusak sel progenitoreritroid.Episode perdarahan,
defisiensi vitamin (kobalamin dan asam folat),
hipersplenisme, hemolisis autoimmun, disfungsi renal dan intervensiradio
Ciri khas dari anemia pada penyakit kronis adalah perkembangan
dari ganguan hemostasis besi dengan peningkatan pengambilan dan
retensi dari besi didalam sel sistem retikuloendothelial, dan batasan dari
ketersediaan besi untuk sel progenitor erotroid dan retriksi besi dari
erithropoiesis.
Pada tikus yang diinjeksikan dengan proinflammatori sitokin
interleukin1 dan tumor necrosa factor ( TNFα ) keduanya hypoferremia
dan bekembang anemia.Kombinasi ini pada kondisi berikatan dengan
sitokin yang menginduksi sintesa dari ferritin, protein besar yang
tergabung dalam penyimpanan besi oleh makrofag dan hepatosit.Pada
inflamasi kronik perolehan besi oleh makrofag lebih banyak pengambilan
melalui eritropoiesis dan import transmembran dari besi ferro oleh protein
Interferon ɣ, lipopolisakarida,dan TNF α meningkatkan regulasi
ekspresi dari DMT 1 dengan peningkatan dari pengambilan besi ke dalam
makrofag yang teraktivasi.Stimulus proinflammatori ini juga menginduksi
retensi besi pada makrofag oleh pengaturran menurun ekspresi dari
ferroportin ,ini menghambat pengeluaran besi dari sel-sel.Ferroportin
merupakan eksporter besi transmembran, suatu proses yang diyakini
respon terhadap transfer dari penyerapan besi ferro dari enterosit
duodenum kedalam sirkulasi.
Bahkan, anti inflammatori sitokin seperti IL-10 dapat menginduksi
anemia melalui stimulus transferrin yang dimediasi perolehan dari besi
oleh makrofag dan dengan translasi stimulus dari ekspresihepsidin.
Pengidentifikasian dari hepsidin ,suatu protein regulasi besi fase
akut yang tergabung dalam 25 asam amino,membantu untuk menjelaskan
hubungan dari respon immun ke homeostasis besi dan anemia pada
penyakit kronis.Ekspresi hepsidin diinduksi oleh lipopolisakarida dan IL-6
dan dihambat oleh TNF α. Transgenik atau ekspresi utama yang
berlebihan dari hepsidin pada anemia berat defisiensi besi pada
tikus.Inflamasi pada tikus yang kurang hepsidin tidak mengarah ke
hipoferremia.Suatu penemuan yang mensugesti bahwa hepsidin mungkin
terlibat dalam peralihan perjalanan besi melalui penurunan penyerapan
duodenum dari besi dan penghambatan dan pelepasan besi dari makrofag
yang terjadi pada anemia penyakit kronis.
Induksi dari hypoferremia oleh IL-6 dan hepsidin terjadi dalam
out,yang diterapi dengan turpentine sebagai model dari ekspresi
penemuan yang mensugesti bahwa hepsidin mungkin pusat dari anemia
penyakit kronis. Identifikasi terbaru gen, hemojuvelin bisa berperan dalam
hubungan dengan hepsidin dan menginduksi perubahan-perubahan ini.
( Weiss G.MD et al., 2005).
Respon yang tumpul dari eritropoietin
Eritropoietin mengatur sentral dari proliferasi sel-sel eritroid. Ekspresi
eritropoietin adalah berhubungan terbalik dengan oksigenasi jaringan dan
tingkat hemoglobin.Ikatan affinitas dari eritropoietin meginduksi faktor-
faktor transkripsi dan merusak sel-sel yang memproduksi eritropoietin.
Respon dari erithropoietin kedepannya dikurangi oleh inhibitor dari sitokin
proinflamasi terhadap proliferasi progenitor sel eritroid, regulasi menurun
dari reseptor eritropoietin dan keterbatasan dari ketersediaan besi.
Evaluasi laboratorium
Anemia penyakit kronik adalah normokrom normositik anemia
dengan karakteristik ringan Hb 9,5 g/dl ke sedang Hb 8 g/dl .(Weiss G et
2.1.7. Interleukin 6
IL-6 berfungsi dalam imunitas non spesifik dan spesifik,diproduksi
fagosit mononuklear, sel endothel vaskular, fibroblas dan sel lain sebagai
respon terhadap mikroba dan sitokin lain.IL-6 mempunyai berbagai fungsi.
Dalam imunitas non spesifik, IL-6 merangsang hepatosit untuk
memproduksi APP dan bersama CSF merangsang progenitor di sumsum
tulang untuk memproduksi neutrofil. Dalam imunitas spesifik, IL-6
merangsang pertumbuhan dan differensiasi sel B menjadi sel mast yang
memproduksi antibodi. (Bratawidjaya., 2006)
IL-6 dahulu dikenal sebagai IFN-β2, hepatocyte stimulating factor
dan plasmocytoma growth factor dan merupakan sitokin yang berfungsi
pada immuitas bawaan maupun didapat.Seperti halnya IL-1,IL-6 dibentuk
oleh banyak macam sel dan berpengaruh pada banyak jenis sel sasaran.
Sumber utama IL-6 adalah makrofag. Walaupun limfosit didaerah
diferensiasi sel B, IL-6 merupakan faktor induksi utama pada diferensiasi
fase terminal. IL-6 menginduksi sel B yang terinfeksi EBV untuk
memproduksi Ig,mempercepat sekresi IgA oleh sel B dalam peyer
patch.Dalam kaitannya dengan sel T, IL-6 memegang peran penting pada
respon sel T terhadap aloantigen dan pembentukan sel T sitotoksik,juga
berperan dalam meningkatkan respon thymocyte terhadap IL-1 dan IL-4.
Pertumbuhan dan diferensiasi sel-sel hemopoietik dipengaruhi oleh
interaksi sinergik beberapa jenis sitokin. Dalam hal ini IL-6 berperan
mempercepat masuknya sel kedalam fase G1dari siklus sel.IL-6 juga
memegang peranan penting pada respon fase akut akibat trauma dengan
meningkatkan sintesa protein fase akut akibat trauma dengan
meningkatkan sintesa protein fase akut oleh hepatosit dan memicu
produksi ACTH yang merangsang pembentukan glukokortikoid (Kresna
boedina, 2010)
Interleukin 6 (IL-6) merupakan interleukin yang berperan sebagai
sitokin proinflamasi. IL-6 disekresikan oleh sel T dan makrofag untuk
menstimulasi respons imun seperti infeksi, trauma, dll. IL-6 penting dalam
patofisiologi demam, inflamasi akut, dan kronik. IL-6 dapat disekresikan
oleh makrofag sebagai respons terhadap molekul mikroba spesifik, yang
disebut sebagai pathogen-associated molecular patterns (PAMPs).
PAMPS ini dapat berikatan dengan molekul dari sistem imun bawaan yang
disebut pattern recognition receptors (PRRs) termasuk Toll-like receptors
menginduksi kaskade sinyal intraseluler yang dapat menyebabkan
peningkatan produksi sitokin inflamasi.(Kaplanski,2003)
IL-6 penting dalam respons inflamasi kronik. IL-6 tidak hanya
berperan dalam reaksi fase akut tetapi juga perkembangan respons imun
seluler dan humoral, termasuk diferensiasi sel B tahap akhir, sekresi
imunoglobulin, dan aktivasi sel T. Peralihan dari inflamasi akut ke kronik
yang utama adalah adanya monosit pada area inflamasi. IL-6 ini penting
dalam transisi antara inflamasi akut ke kronik.(Marin V, 2001).
Kompleks IL-6 dan reseptor IL-6 dapat mengaktivasi sel endotel
untuk mensekresikan monocyte chemoattractant protein (MCP)-1 dan
menginduksi ekspresi molekul adesi.Kompleks IL-6/ Reseptor IL-6
memungkinkan transisi dari neutrofil ke monosit dalam patogenesis
inflamasi.Transisi dari akumulasi neutrofil ke monosit bisa akibat
pergeseran tipe kemokin yang diproduksi oleh sel stroma, makrofag atau
neutrofil. Neutrofil yang distimulasi sitokin inflamasi selama beberapa jam
akan secara selektif menghasilkan MCP-1. Aktivasi endotel (atau sel
stroma) oleh molekul proinflamasi menyebabkan sekresi PAF (Platelet
activating factor), IL-8, IL-6. Kombinasi IL-6R dengan IL-6 memungkinkan
ligasi ke gp130 pada membran sel endotel dan meningkatkan sekresi IL-6
dan MCP-1 sel endotel (atau stroma), yang memungkinkan transisi dari
rekrutmen neutrofil ke monosit. Transisi dari akumulasi neutrofil ke
monosit pada lokasi inflamasi tidak hanya terjadi rekrutmen monosit tetapi
membran baru yang dikenali oleh berbagai reseptor makrofag yang
menyebabkan terjadinya fagositosis. Fagositosis dari PMN apoptotik oleh
makrofag menyebakan peningkatan sekresi TGF-β dan sekresi MCP-1,
menyebabkan terjadinya rekrutmen monosit.( Jones SA, 2005)
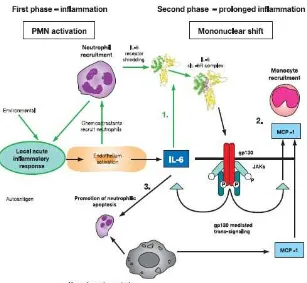
Gambar 2.1. Peranan IL-6 terhadap inflamasi (Gabay C, 2006)
Keterangan. Tahap 1: pada respons inflamasi akut, IL-6 dapat
berikatan dengan dengan reseptornya. Tahap 2 : trans sinyal melalui
gp130 menyebabkan rekrutmen monosit. Tahap 3 : paparan jangka
panjang IL-6 menyebabkan apoptosis neutrofil, fagositosis, dan akumulasi
mononuklear pada lokasi cedera. IL: interleukin; JAK: Janus activated
IL-6 berperan penting dalam pertahanan pejamu sebagai messenger
antara sistem adaptif dan innate dengan menstimulasi produksi IFN-γ di
sel T, dengan meningkatkan sekresi imunoglobulin di sel B yang
teraktivasi dan melalui aktivasi polimorfoneutrofil. (Yamaoka Y,1996).
Jumlah zat besi yang diserap oleh tubuh dipengaruhi oleh jumlah
besi dalam makanan, bioavailabilitas besi dalam makanan dan
penyerapan oleh muosa usus.Di dalam tubuh orang dewasa mengandung
zat besi sekitar 55mg/Kg BB atau sekitar 4 gram. Lebih kurang 67 % zat
besi tersebut dalam bentuk hemoglobin,30 % sebagai cadangan dalam
bentuk ferritin atau hemosiderin dan 3 % dalam bentuk mioglobin.Hanya
Ada 2 cara penyerapan besi dalam usus yang pertama adalah
penyerapan dalam bentu non heme (sekitar 90 % berasal dari makan)
yaitu besi harus diubah dulu menjadi bentuk yang diserap, sedangkan
bentuk yang kedua yaitu bentuk heme (sekitar 10 % berasal dari
makanan) besinya dapat langsung diserap tanpa memperhatikan
cadangan besi dalam tubuh, asam lambung ataupun zat makanan yang
dikomsumsi.
Besi non heme dilumen usus akan berikatan dengan apotransferin
membentukkompleks transferin besi yang kemudian akan masuk ke dalam
sel mukosa, besi akan dilepaskan dan apotransferinnya akan kembali
dalam lumen usus. Selanjutnya sebagian besi bergabung dengan
apoferitin membentuk feritin, sedangkan besi yang tidak diikat oleh
apoferitin akan masuk keperedaran darah dan berikatan dengan
apotransferin serum.
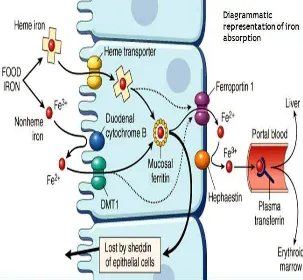
Penyerapan besi oleh tubuh berlangsung melalui mukosa usus
halus, terutama diduodenum sampai pertengahan jejunum,makin kearah
distal usus penyerapan semakin berkurang.Besi dalam makanan
terbanyak ditemukan dalam bentuk senyawa besi non heme berupa
kompleks senyawa besi inorganik (feri/Fe 3+) yang oleh pengaruh asam
lambung ,vitamin C dan asam amino mengalami reduksi menjadi bentuk
fero (Fe2+) bentuk ferro ini kemudian di absorpsi oleh sel mukosa usus dan
didalam sel usus bentuk ferro ini mengalami oksidasi menjadi bentuk ferri
yang selanjutnya berikatan dengan apoferritin menjadi ferritin.Selanjutnya
menjadi bentuk ferro dan didalam plasma in ferro direoksidasi kembali
menjadi bentuk ferri.Yang kemudian berikatan dengan 1 globulin
membentuk transferrin .Absorpsi besi non heme akan meningkat pada
penderita ADB.Transferin berfungsi untuk mengangkut besidan
selanjutnya didistribusikan ke dalam jaringanhati,limpa dan sumsumtulang
serta jaringan lain untuk disimpan sebagai cadangan besitubuh.
Didalam sumsum tulang sebagian besi dilepaskan ke dalam
eritrosit (retikulosit) yang selanjutnya bersenyawa dengan porfirin
membentuk heme dan persenyawaan globulin dengan heme membentuk
hemoglobin. Setelah eritrosit berumur ±120 hari fungsinya kemudian
menurun dan selanjutnya dihancurkan didalam sel retikuloendotelial.
Hemoglobin mengalami proses degradrsi menjadi biliverdin dan besi.
Selanjutnya biliverdin akan direduksi menjadi bilirubin, sedangkan besi
akan masuk ke dalam plasma dan mengikuti siklus seperti diatas atau
akan tetap disimpan sebagai cadangan tergantung aktivitaseritropoiesis.
Bioavailabilitas besi dipengaruhi oleh komposisi zat gizi dalam
makanan. Asam askorbat, daging, ikan dan unggas akan meningkatkan
penyerapan besinon heme. Jenis makanan yang mengandung asam tanat
(terdapat dalam teh dan kopi) kalsium, beras, kuning telur, polifenol,
oksalat, fosfat dan obat-obatan (antasid, tetrasiklin dan kolesitramin) akan
mengurangi penyerapan zat besi.
Besi heme didalam lambung dipisahkan dari proteinnya oleh asam
lambung dan enzim proteosa. Kemudian besi heme mengalami oksidasi
kemudian akan dipecah oleh enzim homeoksigenase menjadi ion feri
bebas dan porfirin. Selanjutnya ion feri bebas ini akan mengalami siklus
seperti diatas.
Didalam tubuh cadangan besi ada 2 bentuk, yang pertama feritin
yang bersifat mudah larut,tersebar disel parenkim dan makrofag,
terbanyak di hati. Bentuk kedua adalah hemosiderin yang tidak mudah
larut, lebih stabil tapi lebih sedikit daripada feritin. Hemosiderin terutama
diditemukan dalam sel kupfer hati dan makrofag dilimpa dan sumsum
tulang. Cadangan besi ini akan berfungsi untuk mempertahankan
homeostasis besi dalam tubuh. Apabila pemasukan besi dari makan tidak
mencukupi, maka terjadi, mobilisasi besidan cadangan besi untuk
mempertahankan kadarHb.
FERRITIN
Kelebihan besi yang tidak dimanfaatkan lagi oleh sel akan diikat oleh
Apoferitin menjadi komplek besi simpanan yang disebut dengan feritin.
Sehingga perneriksaan feritin serum digunakan untuk mengevaluasi
cadangan besi total karena memberikan estimasi yang paling sesuai.
Pada kadar feritin antara 15 -5 ng/ml, tiap 1 ng/ml sebanding dengan kira-
kira I - 10 mg cadangan besi.
Feritin akan meningkat sebagai respon tubuh yang tidak spesifik
tefiadap pengaruh sistemik dari infeksi, inflamasi, penyakit hati, dan
keganasan. Pada penyakit hati feritin serum meningkat karena terjadi
mengalami kerusakan. Peningkatan serum pada keganasan terutama
keganasan hematologi, terjadi karena sintesis langsung dari sel-sel ganas
tersebut, pengaruh reaksi inflamasi, pelepasan dari sel-sel yang rusak
terutama setelah menjalani kemoterapi.
Nilai normal feritin bervariasi sesuai umur dan jenis kelamin. Laki-laki
umumnya lebih tinggi kadarnya dibandingkan perempuan, tetapi setelah
menopause kadarnya meningkat mendekati kadar laki-laki dewasa. Kadar
feritin normal pada laki-laki adalah 28 - 365 ng/ml sedangkan pada
perempuan 10 – 148 (teddy et al.,2011)
Struktur dan fungsi feritin
Ferritin merupakan protein cadangan besi terbesar pada jaringan
manusia.Protein ini memiliki kapasitas sequester diatas 4500 atom besi
diperlukan untuk keperluan metabolik immediate.Hal itu berisi 24 sub unit
dari 2 yipe.Liver (L) dan hati (H) dengan berat molekul masing-masing 19
dan 21 kD.Sub unit H memegang peranan pada rapid detoksifikasi dari
besi karena aktifitas peroksidase,yang mengoksidasi besi ke bentuk Fe(III)
untuk endapan dalam inti. Sedangkan sub unit L memfasilitasi besi
nukleasi,mineralisasi dan penyimpanan besi jangka panjang.Pada invivo
sel spesifik tipe sintesa suatu rasio spesifik dari ferritin H dan ferritin L sub
unit protein selama differensiasi rasio H : L sub unitprotein selalu stabil,
kecuali selama kelebihan besi kronik atau inflamasi (Takeshi et al.,2010)
Regulasi dari ferritin
Beberapa ulasan terbarudikatakan bahwa faktor regulasi dari seluler
ferritin masih sulit dimengerti secara tepat. Sistem yang sensitif tidak
hanya untuk ketersediaan besi tapi juga untuk status oksidasi dari sel.
Faktanya, regulasi besi yangtermasuk transferrin dan reseptor transferrin
(TfR) dan sebagai bagian dari protein pertahanan seluler terhadap stres
dan inflamasi, seperti garis besar dari beberapatulisan.
Takeshi et al., 2010 menemukan baru-baru ini pada pasien
hemodialisis reguler tanpa inflamasi yang jelas, bahwa level serum
hepsidin khususnya digabung dengan level ferritin,independen dari sitokin,
IL-6 dan TNF α.seperti tidak ada evidense korelasi dari ekspresi antara
hepsidin dan ferritin pada model kultur sel, itu mungkin alasan presumsi
bahwa IL-6 dan hepsidin mediasi dengan retensi besi di sel sistem
INFEKSI
2.6. Kerangka Konseptual
ANEMIA RENAL
PERDARAHAN
GANGGUAN FUNGSIHATI DEFISIENSIBESI
FERITIN
IL -6 PENYAKITGINJAL
KRONIK
ERITROPOIETIN
KEGANASAN