BAB 3
METODE PENELITIAN
3.1 Alat dan Bahan 3.1.1 Alat
Adapun alat-alat yang digunakan dalam penelitian ini adalah :
Neraca analitis Mettler Toledo
Hotplate Gallenkamp
Oven Memmert
Ayakan 80 mesh
Tabung Reaksi Pyrex
Erlenmeyer Pyrex
Cawan petri
Botol Aquades
Kertas Saring
Blender
Pisau
Cork borer
Bunsen
Spatula
Alat Autoklaf Fiesher Scientific
Labu Ukur Pyrex
pH Universal p.a. Merck
pH meter
Pipet volume Pyrex
Termometer Fischer
Corong
Kertas Saring Whatman No.42
Penangas Air
Pipet Tetes
Statif dan Klem
Stirer Magnetik
Desikator
Gelas Ukur Pyrex
Tungku Kaki Tiga
Plastik dan Karet
Kapas
Alluminium poil
Cling warp
Serbet
Tissue
Sprayer
3.1.2 Bahan
Adapun bahan-bahan yang digunakan dalam penelitian ini adalah :
Limbah kulit pinang
Isolat Aspergillus Niger
NaOH p.a. Merck
HCl(p) p.a. Merck
Glukosa
Akuades
Media PDA
Agar
Urea
(NH4)2SO4
KH2PO4
CaCl2
MgSO4. 7H2O
Protease Peptone
FeSO4. 7H2O
MnSO4. 7H2O
ZnSO4. 7H2O
CoCl2
Alkohol 70%
3.2Pembuatan Reagen dan Pembuatan Media
3.2.1 Larutan HCl 1%
Sebanyak 2,7 mL HCl 37% diencerkan dengan akuades dalam labu ukur 100 mL
hingga garis tanda lalu dihomogenkan.
3.2.2 Larutan NaOH 2%
Sebanyak 10 g NaOH pellet dilarutkan dengan akuades dalam labu ukur 500 mL
hingga garis tanda lalu dihomogenkan.
3.2.3Reagen DNS
Sebanyak 1 g asam 3,5 –dinitrosalisilat dilarutkan dengan 20 ml 2 N NaOH,
ditambahkan 50 ml H2O kemudian ditambahkan 30 g KNa Tartrat dimasukkan kedalam labu takar 100 ml, ditambahkan akuades hingga garis batas,
dihomogenkan kemudian simpan dan tutup dalam botol gelap.
3.2.4Media PDA
Sebanyak 4,2 g PDA dimasukkan kedalam Erlenmeyer, ditambahkan aquadest 100
ml, diaduk dan dipanaskan sampai mendidih, kemudian disterilkan pada suhu
121oC selama 15 menit.
3.2.5Media Starter Aspergillus Niger
Sebanyak 5 g sampel yang telah didelignifikasi dimasukkan kedalam erlenmeyer,
dan sebanyak 1,5 g agar dimasukkan kedalam Erlenmeyer ditambahkan akuades
100 ml, diaduk dan dipanaskan hingga mendidih, kemudian disterilkan pada suhu
121oC selama 15 menit.
3.2.6Pembuatan Medium Sakarifikasi
3.3 Prosedur Penelitian
3.3.1 Delignifikasi Kulit Pinang
4.Sebanyak 100 g kulit pinang yang telah dikeringkan dan diblender
5.dimasukkan kedalam beaker glass
6.ditambahkan NaOH 2% hingga terendam
7.dipanaskan selama 1 jam pada suhu 600C 8.di oven pada suhu 700C hingga berat konstan 9.diblender kembali hingga halus
10.diayak dengan ayakan 80 mesh.
3.3.2 Peremajaan Isolat Aspergillus Niger
- Disterilkan sekitar tempat kerja dan tangan dengan alkohol 70%
- dituang media PDA ke cawan petri steril didinginkan hingga memadat
- diinokulasikan aspergillus niger dengan metode transfer media
- ditutup cawan petri dengan cling warp dan dibungkus dengan kertas HVS
- diinkubasi selama 5 hari pada inkubator jamur.
3.3.3 Pembuatan Starter Aspergillus Niger
- Disterilkan sekitar tempat kerja dan tangan dengan alkohol 70%
- dituang media starter ke cawan petri steril dibiarkan hingga memadat
- diinokulasikan aspergillus niger dengan metode transfer media
- ditutup cawan petri dengan cling warp dan dibungkus dengan kertas
- diinkubasi selama 7 hari pada inkubator jamur.
3.3.4 Sakarifikasi Kulit Pinang
- Sebanyak 4,5 g sampel yang telah didelignifikasi
- dimasukkan Erlenmeyer
- ditambahkan 150 ml larutan medium sakarifikasi
- diaduk hingga homogen, kemudian diatur pH 5 dengan menambahkan HCl
1%
- disterilkan pada suhu 1210C selama 15 menit
- Disterilkan sekitar tempat kerja dan tangan dengan alkohol 70%
- diinokulasi Aspergillus Niger sebanyak 5 cork borer ke medium sakarifikasi
7 hari, 8 hari, 9 hari, 10 hari dan 11 hari
- di inkubasi diatas shaker.
3.3.5Uji Kualitatif dan Kuantitatif Glukosa
3.3.5.1Uji Kualitatif Glukosa dengan Pereaksi Fehling
- Disaring hasil sakarifikasi menggunakan kertas whattman No.42
- diambil sebanyak 1 ml dan dimasukkan kedalam tabung reaksi
- ditambahkan 1 ml masing- masing fehling A dan B
- dipanaskan dalam air mendidih selama 10 menit
- diamati perubahan warna yang terjadi.
3.3.5.2Uji Kuantitatif Glukosa dengan Reagen DNS
- Disaring hasil sakarifikasi menggunakan kertas whattman No.42
- diambil sebanyak 1 ml dimasukkan kedalam tabung reaksi
- ditambahkan 3 ml reagen DNS, dipanaskan dalam waterbath selama
5 menit
- didinginkan
- diuji dengan alat spektrofotometer UV dengan panjang gelombang
550 nm
3.4 Bagan Penelitian 3.4.1 Bagan Alir Penelitian
Preparasi Sampel (Dicuci, Dicacah, Dijemur, Diblender)
Delignifikasi Menggunakan NaOH 2% ( Dioven pada Suhu 700C)
Pemblenderan Sampel Hasil Delignifikasi ( Diayak Menggunakan Ayakan 80 Mesh )
Peremajaan Isolat Aspergillus Niger
Pembuatan Starter Aspergillus Niger
Penyiapan Medium Sakarifikasi
Sakarifikasi Enzimatis Menggunakan Aspergillus Niger
Produksi Glukosa
3.4.2 Preparasi sampel
Kulit Pinang
3.4.3 Delignifikasi Kulit Pinang
Dicuci bersih
Dicacah kecil-kecil
Dijemur dibawah sinar matahari
Serabut Kulit Pinang Diblender
Dimasukkan kedalam beaker glass
Ditambahkan NaOH 2% hingga terendam
Dipanaskan selama 1 jam pada suhu 60oC
Serbuk Kulit Pinang Terdelignifikasi
Di oven pada suhu 700C hingga berat konstan Diblender kembali hingga halus
100 g Serabut Kulit Pinang
Dicuci hingga pH netral
3.4.4 Peremajaan Isolat Aspergillus Niger
3.4.5 Pembuatan Starter Aspergillus Niger
Media PDA
Didinginkan hingga memadat Diinokulasikan Aspergillus Niger
Ditutup cawan petri dengan cling warp dan dibungkus dengan kertas HVS
Diinkubasi selama 5 hari pada inkubator jamur.
Ditutup cawan petri dengan cling warp dan dibungkus dengan kertas HVS
Diinokulasikan aspergillus niger
Dituang media starter ke cawan petri steril Media Starter
Didinginkan hingga memadat
Diinkubasi selama 7 hari pada inkubator jamur.
Starter Aspergillus Niger
Dituang media PDA kedalam cawan petri steril
3.4.6 Sakarifikasi Limbah Kulit Pinang
3.4.7 Uji Kualitatif dan Kuantitatif Glukosa 3.4.7.1 Uji Kualitatif Glukosa
Dimasukkan kedalam erlenmeyer
Ditambahkan 150 ml medium sakarifikasi Diaduk
4,5 g Kulit Pinang Terdelignifikasi
Dimasukkan kedalam tabung reaksi
Diatur pH 5 dengan menambahkan HCl 1%
Diamati perubahan warna yang terjadi
Ditambahkan 1 ml masing-masing Fehling A dan B
Di lakukan perlakuan yang sama sebanyak 6 erlenmeyer
Hasil Sakarifikasi
Endapan Merah Bata
Dipanaskan dalam air mendidih selama 10 menit Diambil filtrat sebanyak 1 ml
Disaring dengan kertas whatman No.42
Diinokulasi Aspergillus Niger sebanyak 5 cork borer
Di inkubasi diatas shaker dengan variasi 7 hari, 8 hari, 9
hari, 10 hari dan 11 hari.
Disterilkan pada suhu 1210C selama 15 menit. Medium Sakarifikasi
3.4.7.2 Uji Kuantitatif Glukosa
Dimasukkan kedalam tabung reaksi
Didinginkan
Ditambahkan 3 ml reagen DNS
Larutan Kuning Kecoklatan
Di uji dengan alat spektrofotometer UV dengan panjang gelombang 550 nm
Dipanaskan dalam air mendidih selama 5 menit
Diukur absorbansinya
Diambil filtrat sebanyak 1 ml
BAB 4
HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian
Dalam pembuatan glukosa dari subtrat kulit pinang (Areca catechu L.)
menggunakan Aspergillus Niger terlebih dahulu dilakukan proses delignifikasi kulit
pinang sebelum proses sakarifikasi, diperoleh data analisa FT-IR kulit pinang
sebelum dan sesudah delignifikasi dengan NaOH 2% sebagai berikut :
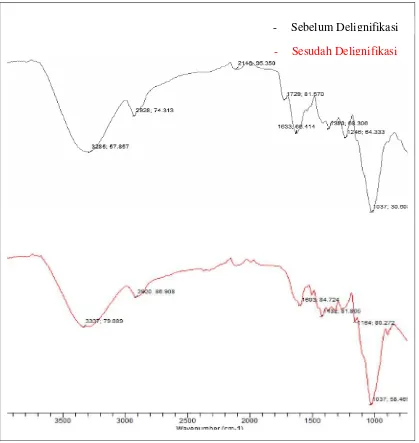
Gambar 4.1 Spektrum FT-IR Kulit Pinang Sebelum dan Sesudah Delignifikasi NaOH 2%
- Sebelum Delignifikasi
Berdasarkan gambar 4.1 menunjukkan puncak khas pada spektrum FT-IR dari kulit
pinang sebelum dan sesudah delignifikasi sebagai berikut (tabel 4.1) :
Tabel 4.1 Data FT-IR Kulit Pinang Sebelum dan Sesudah Delignifikasi NaOH 2%
Gugus Fungsi Bilangan Gelombang Hasil (cm-1) Teori
Regang OH, N-H 3285 (TD) 3750-3000
3337 (SD)
Regang Aldehid 2928 (TD) 3000-2700
CH3, CH2, C-H 2920 (SD)
Regang C=O 1729 dan 1633 (TD) 1900-1650
- (SD)
C-H Bending 1380 (TD) 1475-1300
1432 (SD)
Analisis Struktur Senyawa Organik (Dachriyanus, A. 2002)
Keterangan : TD = Kulit Pinang Tanpa Delignifikasi
SD = Kulit Pinang Sesudah Delignifikasi
Kulit pinang terdelignifikasi kemudian disakarifikasi menggunakan Aspergillus
Niger. Hasil sakarifikasi dianalisis secara kualitatif yang diuji dengan menggunakan
pereaksi Fehling A dan B, sehingga diperoleh hasil sebagai berikut (tabel 4.2) :
Tabel 4.2 Hasil Analisa Kualitatif Kadar Glukosa dari Hasil Sakarifikasi
No. Sampel Penambahan Pereaksi Fehling
1. Larutan Hasil Sakarifikasi Endapan Merah Bata
Kemudian hasil sakarifikasi kulit pinang diuji secara kuantitatif dengan
menggunakan metode DNS menggunakan spektrofotometer UV dengan panjang
gelombang 550 nm, sehingga diperoleh hasil sebagai berikut (tabel 4.3) :
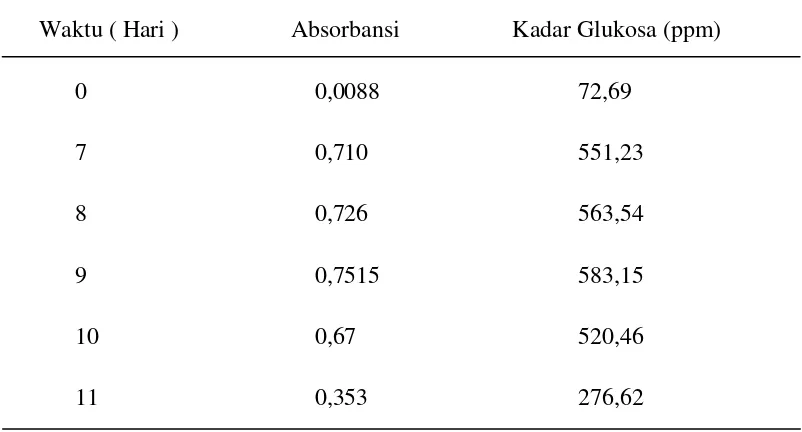
Tabel 4.3 Hasil Analisa Kuantitatif Kadar Glukosa dari Hasil Sakarifikasi Waktu ( Hari ) Absorbansi Kadar Glukosa (ppm)
0 0,0088 72,69
7 0,710 551,23
8 0,726 563,54
9 0,7515 583,15
10 0,67 520,46
4.2 Pembahasan
4.2.1 Analisa FTIR (Fourier Transform Infra Red) Kulit Pinang Sebelum Deignifikasi dan Sesudah Delignifikasi NaOH 2%
Dari gambar 4.1 memberikan puncak dengan intensitas kuat pada panjang
gelombang 3285 cm-1 yang terdapat pada kulit pinang sebelum proses
delignifikasi, 3337 cm-1 pada kulit pinang setelah delignifikasi menunjukkan
gugus – OH dengan stretching vibration. Gugus –OH pada kisaran panjang
gelombang tersebut juga menunjukkan adanya ikatan hidrogen intramolekular dan
merupakan gugus utama pada selulosa, karena selulosa merupakan rantai panjang
dari β glukosa. Terlihat perbedaan puncak serapan gugus O-H pada kulit pinang
sebelum delinifikasi dan kulit pinang setelah delignifikasi, dimana intensitas
serapan setelah delignifikasi lebih tajam yang menunjukkan adanya peningkatan
selulosa. Gugus C=C stretching vibration merupakan karakteristik dari kerangka
lignin yang muncul di sekitar 1500 - 1700 cm-1. Puncak gugus ini pada kulit
pinang sebelum delignifikasi dan hasil setelah delignifikasi terjadi penurunan yang
menunjukkan adanya penghilangan lignin selama proses delignifikasi (Darni, dkk
2016).
Hermiati (2016) menyatakan puncak lignin dapat ditemukan di sampel
tanpa dan dengan perlakuan pada bilangan gelombang 1250 cm-1 untuk unit guaiasil dan 1327 cm-1 untuk unit siringil. Berdasarkan spektrum FTIR tersebut tampak jelas bahwa karakteristik puncak lignin dapat ditemukan di sampel tanpa
delignifikasi pada bilangan gelombang 1246 cm-1 dan pada sampel setelah delignifikasi pada bilangan gelombang 1164 cm-1. Hal ini mengindikasikan bahwa perlakuan alkali meningkatkan laju delignifikasi pada kulit pinang. Gugus
fungsional yang teridentifikasi pada kulit pinang sebelum dan sesudah pra
perlakuan tampak bahwa pra perlakuan delignifikasi menyebabkan kehilangan
beberapa gugus fungsional. Selain itu terjadi perbedaan intensitas pada
masing-masing gugus fungsional yang teridentifikasi. Pra perlakuan NaOH menyebabkan
terjadinya kehilangan gugus fungsi C=O pada hemiselulosa, Hal ini karena dalam
aktifitas penyerangan polimer lignin, pra perlakuan juga menyebabkan terjadinya
hemiselulosa dan derajat polimerisasi yang lebih rendah pada hemiselulosa
menyebabkan polimer ini lebih mudah terdegradasi dibandingkan dengan selulosa
yang didominasi struktur kristalin. Hal ini terlihat pada puncak pada bilangan
gelombang 1729 cm-1 berhubungan dengan gugus C=O stretching vibration yang melambangkan adanya kehadiran hemiselulosa dan terjadinya penurunan puncak
ini pada hasil setelah delignifikasi adalah hasil dari berkurangnya kadar
hemiselulosa.
4.2.2 Analisa Kualitatif Glukosa
Pengujian kualitatif glukosa dilakukan dengan menggunakan pereaksi fehling,
berdasarkan hasil pengujian kualitatif terhadap hasil sakarifikasi dengan
menggunakan larutan Fehling menunjukkan hasil yang positif yaitu memberikan
endapan merah bata. Terbentuknya endapan merah bata menandakan adanya
glukosa .
4.2.3 Analisa Kadar Glukosa
Pengukuran kadar glukosa dilakukan dengan menggunakan metode DNS
menggunakan spektrofotometer UV dengan panjang gelombang 550 nm.
Gambar 4.2 Kurvsa Analisa Kadar Glukosa dengan Variasi Waktu 0
Berdasarkan dari Kurva Kadar Glukosa (ppm) VS Variasi Waktu (Hari)
(Gambar 4.2) dapat dilihat bahwa kadar glukosa mengalami perubahan seiring
bertambahnya waktu sakarifikasi. Pada sakarifikasi 0 hari atau sebelum
ditambahkan A. niger kadar glukosa pada kulit pinang sangat rendah yaitu 72,69
ppm. Hal ini dikarenakan tidak ada enzim selulase yang terbentuk sehingga reaksi
penguraian berlangsung lambat. Kadar glukosa relatif meningkat pada hari ke-7
sampai hari ke-8 dan mencapai waktu maksimal pada hari ke-9, dengan kadar
glukosa yang diperoleh yaitu sebesar 583,15 ppm. Kadar glukosa mulai menurun
pada hari ke-10 dan 11. Menurut Rismawati ( 2016) Hal ini dikarenakan glukosa
yang terbentuk dari hasil penguraian selulosa oleh enzime selulase digunakan
sebagai nutrisi oleh jamur Aspergillus Niger untuk mempertahankan
pertumbuhannya. Sehingga saat dilakukan pengukuran kadar glukosa yang tersedia
lebih sedikit dibanding pada hari-hari sebelumnya.
Pertumbuhan Aspergillus Niger mengalami fase lambat (lag) pada hari
ke-0. Pada fase ini mikroorganisme menyesuaikan diri dengan subtrat dan kondisi
lingkungan di sekitarnya. Pada hari ke-7 sampai hari 9 merupakan fase
pertumbuhan lambat dan fase pertumbuha tetap. Pada fase lambat zat nutrisi di
dalam medium sudah sangat berkurang dan adanya zat hasil-hasil metabolisme
yang mungkin beracun atau dapat menghambat pertumbuhan jasad renik. Pada fase
pertumbuhan tetap ukuran sel pada fase ini lebih kecil karena sel tetap membelah
meskipun zat nutrisi sudah habis. Sedangkan pada hari ke-10 dan 11 merupakan
fase menuju kematian dan fase kematian karena nutrien di dalam medium sudah
habis dan energi cadangan di dalam sel habis. Jumlah sel yang mati semakin lama
akan semakin banyak, kecepatan kematian dipengaruhi kondisi nutrien, lingkungan,
dan jenis jasad renik. Setelah melewati fase ini pertumbuhan mikroba mengalami
kematian yang sangat besar terhadap kadar gluosa yang dihasilkan (Waluyo, L.
2010)
semakin lama proses sakarifikasi, maka kadar glukosa yang dihasilkan
semakin meningkat. Pada sakarifikasi 0 hari atau sebelum ditambahkan A. niger
kadar glukosa pada kulit pinang sangat rendah yaitu 72,69 ppm. Hal ini
dikarenakan tidak ada enzim selulase yang terbentuk sehingga reaksi penguraian
Pada hari ke-7 sampai hari ke-11 mengalami peningkatan dan mencapai titik
maksimum pada hari ke-9 serta mulai mengalami penurunan pada hari ke-10 dan
11. Hal ini selaras dengan penelitian Gunam, dkk. (2010) yang menyatakan bahwa
pH media mengalami penurunan sehingga tidak sesuai dengan kondisi optimum
untuk pertumbuhan A. Niger. Mulyono (2009) menyatakan aktivitas selulase
terlihat meningkat selaras dengan meningkatnya pH awal medium dari 4,4 menuju
5,0 kemudian aktivitas selulase menurun kembali setelah peningkatan pH menjadi
5,5 dan pH awal 5,0 merupakan pH terbaik.
Kadar glukosa yang dihasilkan pada penelitian ini masih relatif rendah.
Menurut Kusumaningati (2008) menyatakan bahwa nilai konversi gula reduksi
yang tidak seberapa besar ini karena menggunakan enzim kasar dari kapang
Aspergillus Niger sp. yang tidak dimurnikan sehingga kemungkinan juga
mengandung enzim-enzim lain seperti hemiselulase dengan hasil akhir xilosa
(pentosa) bukan glukosa (heksosa).
Pada penelitian ini dilakukan 2 kali pengulangan, hasil uji berbeda pada
setiap pengulangan. Hal ini dikarenakan tidak diketahui jumlah kepadatan kapang
pada setiap pengulangan, hal ini sama dengan pada penelitian yang dilakukan
Oktavia, F.I. dkk (2014) menyatakan bahwa karena jumlah kapang yang
disuspensikan dalam media tidak diketahui kepadatan kapangnya, sehingga
BAB 5
KESIMPULAN DAN SARAN 5.1Kesimpulan
1. Kulit pinang dapat dijadikan sebagai subtrat pembuatan glukosa
2. Aspergillus Niger juga dapat dimanfaatkan untuk menghidrolisis kulit
pinang menjadi glukosa dengan proses sakarifikasi.
3. Lama sakarifikasi selama 9 hari merupakan waktu yang optimal untuk
Aspergillus Niger menghidrolisis kulit pinang menjadi glukosa yaitu
sebesar 583,15 ppm.
5.2 Saran
Diharapkan pada peneliti selanjutnya untuk melakukan penelitian lebih
lanjut pada pembuatan glukosa dengan proses sakarifikasi oleh Aspergillus
Niger menggunakan subtrat kulit pinang dengan variasi lain seperti variasi
pH, konsentrasi subtrat dan konsentrasi perlakuan delignifikasi NaOH
sehingga dihasilkan glukosa yang lebih optimal.