1
PENDAHULUAN
Laju pertumbuhan penduduk dan tingkat ekonomi yang semakin meningkat, serta perkembangan teknologi yang semakin pesat dari waktu ke waktu mengakibatkan dunia (termasuk Indonesia) membutuhkan energi yang sangat besar. Bahan bakar fosil seperti minyak bumi dan batu bara merupakan sumber energi utama. Permintaan akan bahan bakar tersebut yang semakin meningkat menyebabkan terjadinya eksplorasi dan eksploitasi sumber energi berbahan bakar fosil secara besar-besaran. Eksploitasi energi yang berlebihan dari sumber daya alam terutama minyak bumi selama ini menyebabkan menipisnya kandungan minyak bumi tersebut, menimbulkan kerusakan lingkungan, perubahan iklim global, dan krisis energi di seluruh dunia (Bockris 2002).
Krisis energi dan kerusakan lingkungan ini memerlukan penanganan serius. Usaha mengurangi dampak negatif terhadap lingkungan dan pengembangan sumber energi alternatif termasuk bioenergi terus diupayakan dan dilakukan. Bioenergi merupakan energi terbarukan yang berasal dari biomassa (Liu & Shen 2004). Bioenergi ini adalah salah satu bentuk energi alternatif yang prospektif untuk dikembangkan. Pengembangan bioenergi ini tidak hanya dapat mengurangi ketergantungan terhadap bahan bakar minyak yang harganya terus melambung, tetapi juga dapat meningkatkan keamanan pasokan energi nasional. Perhatian masyarakat dunia yang semakin meningkat pada penggunaan bahan bakar yang ramah lingkungan menjadikan pengembangan bioenergi sangat strategis dan perlu direalisasikan (Sirait 2007). Oleh karena itu, energi alternatif yang dapat diperbaharui (renewable energy) dan aman lingkungan (green energy) sangat dibutuhkan dan sangat penting untuk diupayakan serta dioptimalkan pengolahan dan penggunaannya.
Hidrogen merupakan salah satu pilihan energi alternatif karena mudah dikonversi dan tidak merusak lingkungan baik dalam proses pembuatan maupun penggunaannya. Hidrogen adalah unsur paling ringan, sangat mudah terbakar, dan paling banyak terdapat di alam semesta. Unsur ini dikandung oleh air dan semua senyawa organik serta makhluk hidup (Mohsin 2007).
Biohidrogen adalah hidrogen yang diproduksi melalui proses biologis atau dari biomassa. Biohidrogen dapat dikembangkan di Indonesia karena bahan bakunya cukup tersedia. Biohidrogen diproduksi dengan memanfaatkan organisme bakteri melalui
proses fermentasi atau fotoproduksi untuk merombak substrat organik (limbah atau nonlimbah) menjadi energi hidrogen (Sirait 2007).
Salah satu mikroorganisme yang mampu memproduksi hidrogen adalah bakteri fotosintetik, seperti Rhodobium marinum dan
Rhodobacter sphaeroides (Kawaguchi 2005).
Bakteri fotosintetik mampu mengubah senyawa organik menjadi gas hidrogen dengan adanya energi cahaya.
Banyak tantangan teknis yang dihadapkan pada masa transisi dari bahan bakar berbasis fosil ke bahan bakar berbasis biohidrogen ini, mulai dari produksi dengan kuantitas memadai, penyimpanan, transmisi, dan distribusinya (Dunn 2002). Oleh karena itu, penelitian ini menjadi salah satu bagian dari transisi menuju penggunaan bahan bakar berbasis biohidrogen.
Penelitian ini bertujuan memproduksi biohidrogen dengan menggunakan glukosa 1% sebagai bahan baku substrat fermentasi oleh bakteri fotosintetik Rhodobium marinum dan isolat Sanur (koleksi Biotechnology
culture collection (BTCC)). Hipotesisnya
adalah fermentasi bakteri fotosintetik
Rhodobium marinum dan isolat Sanur (koleksi
BTCC) dengan substrat glukosa 1% dapat menghasilkan biohidrogen.
TINJAUAN PUSTAKA
BiohidrogenHidrogen dikenal luas sebagai sumber energi yang bersih dan efisien. Gas ini memiliki kandungan energi tertinggi (143 Gjton-1) per unitnya dan merupakan bahan bakar yang tidak terikat secara kimia dengan karbon (Purwanto 2005). Dengan demikian, pembakaran hidrogen tidak akan menimbulkan efek rumah kaca, penipisan lapisan ozon, atau hujan asam. Hal tersebut dikarenakan proses pembakarannya di udara hanya menghasilkan uap air dan energi panas (Nath & Das 2004).
Hidrogen merupakan sumber energi alternatif yang bisa diproduksi dari sumber yang terbarukan, seperti biomassa. Biohidrogen adalah hidrogen yang diproduksi melalui proses biologis atau dari biomassa (Zaborsky et al. 1998). Selain sumber penghasilnya melimpah, biohidrogen juga ramah lingkungan. Hidrogen dapat diproduksi oleh mikroba melalui dua cara, yaitu perubahan secara fotobiologis dan melalui teknik fermentasi (Sirait 2007). Teknik yang
2
pertama hanya dapat dilakukan pada siang hari, yaitu ketika adanya matahari. Hal ini dikarenakan mikroba fotosintetik menggunakan energi dari sinar matahari sebagai sumber energi mereka. Akan tetapi, teknik yang kedua dapat berlangsung pada siang maupun malam hari (dalam keadaan gelap). Hal ini tergantung pada tipe mikroba yang digunakan dalam fermentasi. Sebagian besar bakteri aerob dan anaerob memproduksi biohidrogen dengan pendekatan fotosintesis dan fermentasi (fotofermentasi) (Rahman et
al. 1997).
Beberapa keunggulan dari Biohidrogen antara lain: dapat diperbarui (renewable
energy) dan ramah lingkungan (green energy)
(Zaborsky et al. 1998), hasil samping pembakarannya berupa uap air sehingga tidak menimbulkan efek rumah kaca, hujan asam, dan penipisan lapisan ozon (Nath & Das 2004), proses produksi dapat berlangsung pada tekanan dan suhu normal (Purwanto 2005), biaya produksi lebih rendah dibandingkan dengan cara fisik dan kimia (Nakashimada 2004), dan dapat memanfaatkan limbah dan sampah organik sebagai substrat fermentasi (Liu & Shen 2004). Adapun kendala yang dihadapi untuk energi alternatif ini adalah persetujuan publik, penanaman modal yang besar dan harga hidrogen saat ini yang masih jauh lebih mahal dibandingkan bahan bakar lainnya. Namun demikian, hidrogen dapat diproduksi dengan teknologi yang lebih murah dan mudah, yaitu dengan memanfaatkan organisme bakteri melalui proses fermentasi atau fotoproduksi, untuk merombak substrat organik (limbah dan nonlimbah) menjadi energi hidrogen (Sirait 2007).
Mikroorganisme Penghasil Gas Hidrogen Hidrogen yang diproduksi oleh mikroalga dan bakteri disebut biohidrogen. Bakteri dan mikroalga yang sering digunakan untuk penelitian tersebut adalah bakteri anaerob dan mikroorganisme fotosintetik seperti bakteri fotosintetik dan sianobakteria. Sianobakteria dapat menguraikan air menjadi hidrogen dan oksigen dengan bantuan energi cahaya (Sirait 2007). Keuntungan organisme ini dalam memproduksi hidrogen adalah tidak menggunakan senyawa organik sebagai substrat tetapi menggunakan sinar matahari. Kelemahannya adalah produksi hidrogennya lambat, sistem reaksinya membutuhkan energi yang besar, dan pemisahan gas hidrogen dan oksigen membutuhkan penanganan yang
khusus. Reaksi biofotolisis dari organisme ini adalah sebagai berikut (Zaborsky et al. 1998):
Cahaya
H2O 0.5 O2 + H2 ?G = - 242 kJ
Bakteri anaerob tidak menggunakan air sebagai senyawa penghasil biohidrogen namun menggunakan senyawa organik. Keuntungan dari bakteri ini adalah reaksi pembentukan hidrogen yang cepat dan tidak memerlukan energi matahari. Kelemahan dari bakteri ini dalam memproduksi gas hidrogen adalah hasil dekomposisi/penguraian senyawa organik tersebut meninggalkan asam-asam organik seperti asam asetat, asam butirat, dan lain-lain. Asam organik tersebut menjadi masalah baru jika tujuan dari produksi adalah untuk menanggulangi limbah (Zaborsky et al. 1998).
Bakteri fotosintetik membutuhkan senyawa organik untuk memproduksi hidrogen dan energi cahaya untuk membantu reaksi energi yang terlibat dalam produksi hidrogen. Keuntungan bakteri ini dibandingkan pada sianobakteri yaitu energi yang dibutuhkan untuk produksi hidrogen lebih kecil karena adanya peran senyawa organik. Senyawa organik yang dapat digunakan oleh bakteri ini sebagai substrat untuk produksi hidrogen adalah asam lemak, gula, tepung, selulosa, dan lainnya (Sirait 2007). Bakteri fotosintetik dalam memproduksi hidrogen melibatkan substrat senyawa organik, fotosistem I, feridoksin, dan enzim nitrogenase. Reaksi produksi hidrogen dari substrat glukosa oleh bakteri fotosintetik adalah sebagai berikut (Zaborsky et al. 1998):
Glukosa + 2H2O 6CO2 +12H2 ?G=-33.8 kJ
Ada berbagai macam mikroorganisme yang dapat menghasilkan biohdrogen (Miyake 1998, diacu dalam Zaborsky et al. 1998), baik yang fotosintetik maupun yang nonfotosintetik. Bakteri yang termasuk fotosintetik antara lain Rhodopseudomonas
Rhodobacter, Anabaena, Chlamydomonas, Chromatium, dan Thiocapsa. Sedangkan yang
termasuk nonfotosintetik antar lain Klebsiella,
Clostridium, Enterobacter, Azotobacter, Metanobacteria, dan Eschericia coli. (Miyake
1998, diacu dalam Zaborsky et al. 1998). Salah satu contoh bakteri fotosintetik adalah Rhodopseudomonas marina atau yang lebih dikenal dengan nama Rhodobium
marinum. Bakteri ini termasuk bakteri gram
negatif, berbentuk batang, bergerak, fotoheterotrop anaerob fakultatif, dan
3
memproduksi warna merah (Hirashi et al. 1995). Rhodobium marinum (R. Marinum) diisolasi dari laut pada tahun 1995 (Sirait 2007). Enzim yang terlibat pada fotosintetik produksi hidrogen oleh bakteri ini adalah enzim nitrogenase. Isolat Sanur merupakan konsorsium bakteri fotosintetik yang diisolasi dari air laut pantai Sanur, Bali. Bakteri dominan yang ada dalam isolat ini adalah R.
marinum sehingga isolat tersebut berwarna
merah.
Telah dilaporkan beberapa penelitian mengenai produksi gas hidrogen menggunakan bakteri fotosintetik, di antaranya: Rhodobium Marinum A-150 pada substrat asam laktat (Kawaguchi 2001),
Rhodobacter sphaeroides pada limbah cair
pabrik susu (Turkaslan 1998, diacu dalam Sirait 2007), dan Rhodobacter sphaeroides pada limbah cair tahu (Zhu 1999). Penelitian-penelitian yang telah dilakukan tersebut merupakan acuan dari penelitian ini, sehingga dapat disimpulkan bahwa bakteri fotosintetik merupakan pilihan utama di dalam pemanfaatan limbah hasil perkebunan yang mengandung asam-asam organik.
Proses Produksi Biohidrogen Gas hidrogen yang diproduksi oleh bakteri fotosintetik dihasilkan melalui proses fotofermentasi. Fotosistem pada bakteri fotosintetik hanya melibatkan satu fotosistem (PS1). Fotosistem terjadi dalam membran intraseluler. Fotosistem pada bakteri ini tidak cukup kuat untuk memecah air. Pada kondisi anaerob, bakteri fotosintetik dapat dengan baik menggunakan asam organik sederhana seperti asam asetat sebagai donor elektron (Sirait 2007).
Elektron yang dilepaskan dari senyawa organik akan dipompakan oleh sejumlah besar pembawa elektron (diantara kuinon dan plastosianin). Selama transport elektron, proton dipompakan melewati membran (dalam kompleks protein sitokrom bc1) sehingga terjadi gradien proton. Gradien proton yang terjadi digunakan oleh enzin ATP sintase untuk menghasilkan ATP. Energi ATP yang terbentuk dapat digunakan untuk transport lebih jauh elektron ke elektron akseptor feridoksin (Fd) (Chen et al. 2005).
Jika molekul nitrogen tidak ada, maka enzim nitrogenase dapat mereduksi proton menjadi gas hidrogen (H2) dibantu dengan energi dalam bentuk ATP dan elektron yang diperoleh dari feridoksin (Fd) (Chen et al.. 2005). Secara keseluruhan fotosistem bakteri fotosintetik ini mengubah komponen utama
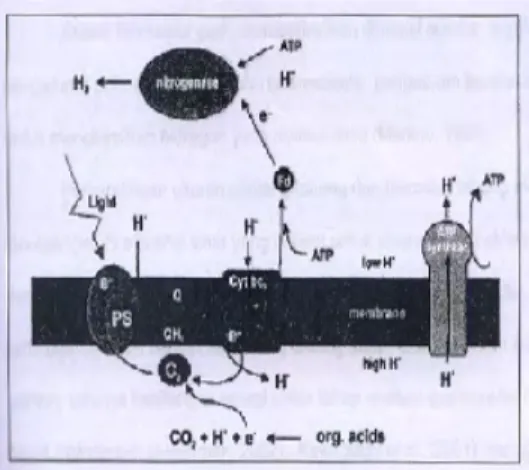
dari asam organik menjadi gas hidrogen (H2) dan karbon dioksia (CO2) (Gambar 1). Fotosistem bakteri ini tidak menghasilkan oksigen (O2) sehingga tidak menghambat kerja enzim nitrogenase, mengingat enzim nitrogenase sensitif terhadap oksigen (Akkerman 2002).
Gambar 1 Fotofermentasi bakteri fotosintetik (Akkerman 2002). Keterangan: PS = fotosistem, C = plastosianin, Q = kuinon, dan Cyt = sitokrom.
Fermentasi
Fermentasi merupakan proses penting dalam kehidupan sehari-hari manusia. Fermentasi berasal dari bahasa latin ferfere yang artinya mendidihkan. Hal ini berdasarkan pengamatan sehari-hari bahwa dalam proses fermentasi minuman beralkohol akan menghasilkan buih yang kemudian satu komponennya diketahui sebagai gas karbondioksida. Fermentasi secara umum dapat dinyatakan sebagai proses katabolisme, suatu pemecahan senyawa organik yang kompleks menjadi bentuk yang lebih sederhana. Aplikasi proses ini dapat dilihat pada produksi minuman beralkohol atau produk yang bersifat asam (seperti asam asetat atau cuka) (Hidayat 2006). Pengetahuan mengenai proses ini berkembang pesat sejak penelitian Louis Pasteur mengenai proses fermentasi yang terjadi dalam pembuatan wine (anggur). Penelitian mengenai proses ini berkembang pesat semenjak tumbuhnya industri minuman beralkohol dan industri antibiotik.
Aplikasi metode ini diawali dengan pembuatan bir sekitar 6.000 tahun sebelum Masehi. Pembuatan roti dengan bantuan khamir atau ragi diperkirakan sudah terjadi sejak 4.000 tahun sebelum Masehi (Pelczar & Chan 1986). Pembuatan produk fermentasi
4
kecap dan tauco di Cina telah dilakukan sejak 722 SM. Fermentasi anggur mulai berkembang kira-kira abad ke-17 dengan menggunakan bakteri Acetobacter
menghasilkan asam asetat (asam cuka) (Hidayat 2006). Kemudian pada tahun 1817 mulai diproduksi enzim dari tumbuhan dan jaringan hewan yang dapat memecah zat pati menjadi maltosa. Begitu juga enzim dari khamir yang dapat memecahkan sukrosa menjadi glukosa dan fruktosa ditemukan pada tahun 1817.
Fermentasi terbagi menjadi dua berdasarkan kebutuhan akan oksigen, yaitu fermentasi aerobik dan anaerobik. Fermentasi aerobik adalah fermentasi yang prosesnya memerlukan oksigen. Keberadaan oksigen membuat mikroorganisme dapat mencerna glukosa menghasilkan air, karbondioksida dan sejumlah besar energi. Fermentasi dalam proses anaerobik tidak memerlukan oksigen. Ada berbagai produk (metabolit) yang bisa dihasilkan dalam proses fermentasi, antara lain berbagai jenis asam (asam laktat, asetat, asam butirat), alkohol, etanol, protein, dan ester (Dunn 1959). Produk suatu hasil fermentasi dapat diubah lebih lanjut melalui proses fermentasi lain untuk menghasilkan produk akhir yang lain, seperti gas hidrogen.
Ada tiga jenis sistem fermentasi yang dioperasikan dalam proses bioteknologi, yaitu sistem diskontinu (batch), kontinu, Dan semikontinu (fed-batch) (Smith 1985). Pada sistem diskontinu, pemberian medium, nutrisi, dan bakteri dilakukan hanya di awal fermentasi (tidak ada penambahan medium, nutrisi, dan bakteri selama fermentasi berlangsung). Sedangkan pada sistem kontinu, pemberian medium dan nutrisi serta pengeluaran sejumlah fraksi dari volume kultur terjadi secara terus-menerus. Sistem semikontinu adalah suatu sistem fermentasi yang medium atau substratnya ditambahkan secara kontinu selama fermentasi berlangsung tanpa mengeluarkan sesuatu dari sistem (Smith 1985).
Kromatografi Gas (GC)
Analisis kromatografi gas adalah suatu metode analisis pemisahan komponen kimia secara fisika. Komponen - komponen yang akan dipisahkan didistribusikan di antara dua fase, yaitu fase diam dan fase gerak. Fase gerak dapat berupa gas atau cairan dan fase diam dapat berupa padatan atau cairan (Black & Read 1997). Fase gerak berfungsi membawa sampel sedangkan fase diam
berfungsi untuk mengadsorpsi atau mempartisi komponen.
Peralatan kromatografi gas terdiri atas injektor, kolom, detektor, pemanas (oven),
amplifier, rekorder, gas pembawa, dan
pengatur aliran dan tekanan (Black &Read 1997). Injektor berfungsi sebagai tempat masuknya sampel yang dirancang sedemikian rupa sehingga sampel dapat langsung masuk ke dalam kolom dengan perantaraan gas pembawa. Kolom berfungsi memisahkan komposisi sampel menjadi komponen-komponennya sehingga dapat terelusi dalam waktu yang berbeda. Detektor berfungsi untuk mendeteksi komponen yang keluar dari kolom. Pemanas berfungsi untuk memanaskan injektor, kolom dan detektor untuk injektor, kolom dan detektor yang dilengkapi dengan
thermostate. Amplifier berfungsi untuk memperbesar sinyal arus listrik yang berasal dari detektor. Rekorder berfungsi sebagai pencatat hasil dalam bentuk kromatogram. Gas pembawa berfungsi sebagai pembawa gas sampel. Gas pembawa yang umum digunakan adalah Helium (He), Nitrogen (N2) dan Argon (Ar) (Black &Read 1997). Pengatur aliran dan tekanan berfungsi sebagai pengatur tekanan yang dapat menentukan kecepatan alir gas pembawa.
Prinsip kerja pada GC, yaitu sampel diinjeksikan ke dalam injektor kemudian diangkut oleh gas pembawa masuk ke dalam kolom yang berisi padatan sebagai fase diam (Black & Read 1997). Fase diam memiliki sifat dapat berinteraksi dengan komponen-komponen dalam sampel sehingga dapat menghambat laju alir masing-masing komponen. Besarnya hambatan untuk masing-masing komponen berbeda-beda sehingga sesampai di ujung kolom tidak bersamaan melainkan satu persatu (Black & Read 1997). Komponen yang keluar dari kolom dilewatkan ke detektor sedangkan sinyal dari detektor dikirim melalui amplifier ke rekorder dan dicatat sebagai kromatogram.
Agar peralatan kromatografi gas bisa bekerja dengan maksimal, maka perlu dilakukan optimasi suhu seperti suhu injektor, kolom, dan detektor (Sudarmadji et al. 1997). Injektor selain berfungsi untuk tempat masuknya sampel, juga berfungsi untuk mengubah sampel yang berfase cair atau padat menjadi gas tanpa terjadi dekomposisi. Pada umumnya suhu injektor kira-kira 50 oC lebih tinggi dari titik didih komponen sampel yang mempunyai titik didih paling tinggi. Bila titik didih komponen belum diketahui, dapat dilakukan secara coba-coba (trial), dengan memulai suhu injektor rendah kemudian
5
dinaikkan. Jika diperoleh puncak-puncak kromatogram lebih baik berarti suhu percobaan pertama terlalu rendah sehingga perlu dicoba kembali dengan cara menaikkan suhu secara bertahap hingga mendapatkan kondisi yang tepat. Namun demikian, suhu injektor tidak boleh terlalu tinggi sebab ada kemungkinan terjadinya dekomposisi (penguraian komponen yang hendak dianalisis) (Sudarmadji et al. 1997).
Kolom merupakan perangkat yang memiliki peranan penting dalam proses analisis dengan metode kromatografi sehingga pemilihan jenis kolom yang tepat dan kondisi yang optimal sangat diperlukan. Pada umumnya suhu kolom dibuat kurang lebih sama dengan titik didih rata-rata dari seluruh komponen dalam sampel (Black & Read 1997). Kontrol suhu pada detektor sangat diperlukan terutama untuk detektor yang sensitivitasnya dipengaruhi oleh adanya fluktuasi suhu. Pada umumnya suhu detektor dijaga 20-50 oC lebih tinggi dari suhu kolom, hal ini agar uap sampel tidak terkondensasi (Black & Read 1997).
BAHAN DAN METODE
Bahan dan AlatBahan-bahan yang digunakan antara lain biakan bakteri fotosintetik Rhodobium marinum NBRC (NITE Biological Resource Center) No. 100434, biakan bakteri fotosintetik isolat Sanur yang merupakan koleksi Biotechnology culture collection (BTCC), Larutan NaOH 0.6 N, larutan HCl 0.3 N, Akuades, air steril (mili-Q), D(+)Glukosa (Merck), ekstrak ragi, K2HPO4, KH2PO4, MgSO4.7H2O, MnCl2.4H2O, FeSO4.7H2O, NaCl, natrium suksinat, amonium asetat, larutan feri sitrat (0.1%), NH4Cl, CaCl2.2H2O, ZnSO4.7H2O, H3BO3, CoCl2.6H2O, CuCl2.2H2O, NiCl2.6H2O, Na2MoO4.2H2O, etanol, larutan stok glukosa 1000 ppm, amonium sulfat, larutan MEM Vit. 100X, EDTA.2Na, Na2S.9H2O, NaHCO3, kertas aluminium foil, plastik tahan panas, karet, asam sulfat pekat, larutan fenol 5%, kertas saring, dan kapas.
Peralatan yang digunakan adalah penangas air, spektrofotometer UV-Vis (Beckman DU 650), sentrifus (Jouan MR 1812), autoklaf (Everlight TA-630), laminar air flow cabinet,
shaker, rak tabung, tabung reaksi, falcon 50
ml, gelas piala, kertas saring, labu Erlenmeyer (100 ml, 250 ml, 300 ml, dan 500 ml), pH meter HM-30G, Sensor hidrogen H2 Scan
model 2240, kromatografi gas (GC) HP 5890,
neraca analitik, botol schott, vorteks, dan autopipet.
Metode Percobaan
Media Tumbuh Bakteri Fotosintetik R. marinum dan Isolat Sanur (Uchino 2006)
Mula-mula dibuat media dasar dengan komposisi: 0.3 g ekstrak ragi, 1 g natrium suksinat, 0.5 g amonium asetat, 5 ml larutan feri sitrat (0.1%), 0.5 g KH2PO4, 0.5 g MgSO4.7H2O, 0.4 g NaCl, 0.4 g NH4Cl, 0.05 g CaCl2.2H2O, 1 ml trace element solution SL-6 (komposisi: 100 mg ZnSO4.7H2O, 30 mg MnCl2.4H2O, 300 mg H3BO3, 200 mg CoCl2.6H2O, 10 mg CuCl2.2H2O, 20 mg NiCl2.6H2O, dan 30 mg Na2MoO4.2H2O, dalam 1L akuades). Kemudian media dasar ini dilarutkan dalam 1 L akuades dan diaduk hingga homogen serta disesuaikan pH-nya hingga 6,8. Setelah itu, media tersebut disterilisasi (autoklaf 121ºC selama 15 menit). Media steril ini setelah dingin kemudian ditambahkan 0.5 ml etanol, 10 ml MEM Vit.
Solution 100X, dan 5 ml larutan Na2S (1.5 g Na2S.9H2O dilarutkan dalam 100 ml akuades dalam botol serum bertutup karet butil. Udara dalam botol tersebut dibebaskan dengan memasukkan gas N2 (1800 kg/cm2 selama 30 menit). Setelah itu disterilisasi dalam autoklaf 121ºC selama 15 menit, kemudian diatur pH-nya hingga pH 7.3 dengan menambahkan H2SO4 2N steril. Larutan dikocok untuk menghindari pengendapan hingga dihasilkan larutan akhir berwarna kuning transparan). Media tumbuh ini siap digunakan.
Kultivasi Bakteri R. marinum dan Bakteri Isolat Sanur (Sirait 2007)
Sebanyak 2 ml suspensi bakteri R.
marinum dan bakteri isolat Sanur
masing-masing ditambahkan ke dalam tabung betutup yang berbeda yang sudah berisi 8 ml media tumbuh. Kemudian dikocok hingga merata. Setelah itu, diinkubasi pada suhu 30 ºC di inkubator goyang selama 3 hari. Optical
density (OD) suspensi bakteri tersebut diukur
setiap hari hingga hari ke-3 (dari jam ke-0 sampai jam ke-76) dengan menggunakan spektrofotometer UV-Vis pada panjang gelombang 660 nm. Kemudian 10 ml suspensi bakteri tersebut disuntikkan ke dalam 100 ml media kultur. Kultur bakteri ini diinkubasi pada suhu 30 ºC di inkubator goyang selama 3 hari. Kultur tersebut siap dipanen untuk digunakan dalam fermentasi produksi hidrogen.