5
BAB II
TINJAUAN PUSTAKA 2.1 Air
Air adalah komponen kimia utama pada organisme hidup. Sifat fisiknya yang unik mencakup kemampuan untuk melarutkan berbagai molekul organik dan anorganik. Tubuh dapat bertahan selama berminggu-minggu tanpa makanan, tapi hanya beberapa hari tanpa air. Air atau cairan tubuh merupakan bagian utama tubuh, yaitu 55-60% dari berat badan orang dewasa atau 70% dari bagian tubuhtanpa lemak. Angka ini lebih besar untuk anak-anak. Pada proses menua manusia kehilangan air. Kandungan air bayi pada waktu lahir adalah 75% berat badan, sedangkan pada usia tua menjadi 50%. Kehilangan ini sebagian besarberupa kehilangan cairan ekstraselular.Kandungan air tubuh relatif berbeda antar manusia, bergatung pada proposi jaringan otot dan jaringan lemak. Tubuh yang mengandung relatif lebih banyak otot mengandung lebih banyak air, sehingga kandungan air atlet dari pada nonatlet, kandungan pada laki-laki lebih banyak daripada perempuan, dan kandungan air pada anak muda lebih banyak daripada orang tua (Murray., et all, 2009; Almatsier,2009)
Air yang ada di bumi ini tidak pernah terdapat dalam keadaan murni bersih, tetapi selalu ada senyawa atau unsur lain yang terlarut didalamnya. Meskipun rumus kimia air murni di lingkungan laboratorium adalah H2O namun kenyataannya di alam, rumus tersebut seolah-olah berubah menjadi H2O + X. Dalam hal ini, X merupakan komponen-komponen yang masuk atau dimasukkan ke dalam badan air sehingga
6
menyebabkan perairan menurun kualitasnya.(Wardhana, 1995; Nugroho, 2006).
Untuk mendapatkan standard air yang bersih tidaklah mudah, karena tergantung pada banyak faktor penentu yang perlu dipertimbangkan dalam dua aspek yang mana pertama berdasarkan kegunaan air yang meliputi air untuk minum, air untuk keperluan rumah tangga, air untuk industri, air untuk mengairi sawah, air untuk kolam perikanan. Sementara yang kedua berdarakan asal sumber air yaitu air dari mata air pegunungan, air danau, air sungai, air sumur, air hujan (Wardhana, 1995)
2.1.1 Air Minum
Air minum adalah air yang melalui proses pengolahan atau tanpa proses pengolahan yang memenuhi syarat kesehatan dan dapat langsung diminum. Sedangkan, air bersih adalah air yang digunakan untuk keperluan sehari-hari yang kualitasnya memenuhi syarat kesehatan dan dapat diminum setelah dimasak (Peraturan MenteriKesehatan Nomor 492Tahun 2010; Peraturan Menteri Kesehatan Nomor 416 tahun 1990)
Menurut Almatsier (2009), air minum mempunyai berbagai fungsi dalam proses vital tubuh diantaranya:
a. Pelarut dan alat angkut.
Air minum diperlukan sebagai pelarut zat-zat gizi monosakarida, asam amino, lemak, vitamin, dan mineral serta bahan-bahan lain yang diperlukan tubuh seperti oksigen dan hormon-hormon. Zat-zat gizi dan hormon ini dibawa ke seluruh sel yang membutuhkan. Selain sebagai pelarut air juga berfungsi mengangkut sisa-sisa metabolisme, termasuk
7
karbon dioksida dan ureum untuk dikeluarkan dari tubuh melalui paru-paru, kulit dan ginjal.
b. Katalisator
Air minum berperan sebagai katalisator dalam bebagai reaksi biologis dalam seltermasuk di dalam saluran cerna. Air diperlukan pula untuk memecah atau menghidrolisis zat gizi kompleks menjadi bentuk-bentuk lebih sederhana.
c. Pelumas
Air minum berperan sebagai pelumas dalam cairan sendi-sendi tubuh serta membersihkan permukaan mata serta melicinkannya, sehigga gerak kelopak mata menjadi lancar.
d. Fasilitator pertumbuhan.
Air minum sebagai bagian jaringan tubuh diperlukan untuk pertumbuhan.Dalam hal ini berperan sebagai zat pembangun.
e. Pengatur suhu tubuh
Karena kemampuan air minum untuk menyalurkan panas, air memegang peranan dalam mendistribusikan panas di dalam tubuh.Sebagian panas yang dihasilkan dari metabolisme energi diperlukan untuk mempertahankan suhu tubuh pada 37°C.Suhu ini paling cocok untuk bekerjanya enzim-enzim di dalam tubuh.Kelebihan panas yang diperoleh dari metabolisme energi perlu segera disalurkan keluar.Sebagian besar pengeluaran kelebihan panas ini dilakukan melaluipenguapan air dari permukaan tubuh (keringat).Tubuh setiap waktu mendinginkan diri melalui penguapan air. Semakin luas permukaan tubuh, semakin besar kehilangn panas melalui kulit.
8 f. Peredam benturan
Air dalam mata, jaringan saraf tulang belakang, dan dalam kantung ketuban melindungi organ-organ tubuh dari benturan.
Air terdapat diseluruh badan. Di tulang terdapat air sebanyak 22% berat tulang, di darah dan ginjal sebanyak 83%. Pentingnya air bagi kesehatan dapat dilihat dari jumlah air yang ada di dalam organ, seperti 80% dari darah terdiri atas air, 25% dari tulang, 75% dari urat syaraf, 80% dari ginjal, 70% dari hati, dan 75% dari otot adalah air. Kehilangan air untuk 15% dari berat badan dapat mengakibatkan kematian. Karenanya orang dewasa perlu minum minimum 1,5 – 2 liter air sehari. Kekurangan air ini menyebabkan banyaknya didapat penyakit batu ginjal dan kandung kemih di daerah tropis seperti Indonesia, karena terjadinya kristalisasi unsur-unsur yang ada di dalam cairan tubuh (Slamet, 2009).
2.1.2 Sumber Air Minum
Sampai saat ini kebanyakan orang memanfaatkan air permukaan tawar dan air tanah sebagai sumber air minum. Sumber-sumber air tawar adalah air permukaan yang merupakan air sungai dan danau. Air permukaan adalah air yang berada di sungai, danau, waduk, rawa dan badan air lainnya yang tidak mengalami infiltrasi ke bawah tanah. Air tanah pada umumnya tergolong bersih dilihat dari segi mikrobiologis, karena sewaktu proses pengaliran mengalami penyaringan alamiah dan dengan demikian kebanyakan mikroba sudah tidak lagi terdapat di dalamnya. Namun demikian, kadar kimia air tanah tergantung sekali dari jenis tanah yang dilaluinya. Pada proses ini mineral-mineral yang
9
dilaluinya dapat larut dan terbawa, sehingga mengubah kualitas air tersebut (Effendi, 2003; Slamet, 2009).
Peraturan Pemerintah NO 20 tahun 1990 mengelompokkan kualitas air menjadi beberapa golongan menurut peruntukannya:
1. Golongan A, yaitu air yang dapat digunakan sebagai air minum secara langsung, tanpa pengolahan terlebih dahulu. 2. Golongan B, yaitu air yang dapat digunakan sebagia air baku
air minum
3. Golongan C, yaitu air yang dapat digunakan untuk keperluan perikanan dan peternakan
4. Golongan D, yaitu air yang dapat digunakan untuk keperluan pertanian, usaha di perkotaan, industi dan pembangkit tenaga listrik (Effendi, 2003).
Walaupun dinyatakan air baku itu langsung dapat diminum. Namun dalam persiapan penyediaan air dan sistem distribusi harus dijelaskan tentang bagaimana air tersebut dinyatakan aman sebagai air minum (Tjokrokusumo, 1995)
Pelayanan air bersih yang dilakukan oleh pemerintah melalui Perusahaan Daerah Air Minum (PDAM), belum dapat menjangkau seluruh wilayah. Sedangkan wilayah yang masyarakatnya sudah dilayani PDAM, belum semua kebutuhan air bersihnya terpenuhi 100%. Sehingga menyebabkan mereka mencari cadangan sumber air bersih lain. Sedangkan wilayah yang sama sekali belum terlayani PDAM, masyarakat harus berusaha sendiri untuk mendapatkan air bersih dan air tanah
10
merupakan pilihan pertama dalam memenuhi kebutuhan air bersih (Kodoatie dan Syarief, 2010)
2.1.3 Kualitas Air Minum
Sumber air baku pada dasarnya harus dapat dipersiapkan sebagai sumber air minum dan karena kenyataannya di alam mengalami berbagai macam dan jenis pencemar baik dari akibat peristiwa alam maupun kegiatan manusia, maka air tersebut dinyatakan tercemar secara potensial oleh kejadian lingkungan (Tjokrokusumo, 1995).
Negara dengan keadaan ekonomi lebih rendah dan teknologi juga rendah, maka biasanya kesehatannyapun rendah. Di Negara sedemikian biasanya standar air minum tidak ketat, karena kemampuan mengelolah air (teknologi) masih belum canggih dan masyarakatbelum mampu membeli air yang harus diolah secara canggih yang tentunya juga mahal. Standar di setiap Negara memang harus layak bagi keadaan social-ekonomi-budaya setempat. Untuk Negara berkembang seperti Indonesia, perlu didapatkan cara-cara pengelolahan ataupun pengelolahan air yang relatif murah (tekologi tepat guna), sehingga kualitas air yang dikonsumsi masyarakat dapat dinyatakan baik atau memenuhi stadar internasional, tapi terjangkau oleh masyarakat (Slamet, 2009).
Maka karena itu air minum yang ideal seharusnya jernih, tidak berasa, tidak berwarna dan tidak berbau. Tidak mengandung zat kimia yang dapat mengubah fungsi tubuh, tidak dapat diterima secara estetis, dan dapat merugikan secara ekonomis. Air itu seharusnya tidak korosif, tidak meninggalkan endapan pada seluruh jaringan distribusinya. Pada hakekatnya, tujuan ini dibuat untuk mencegah terjadinya serta meluasnya
11
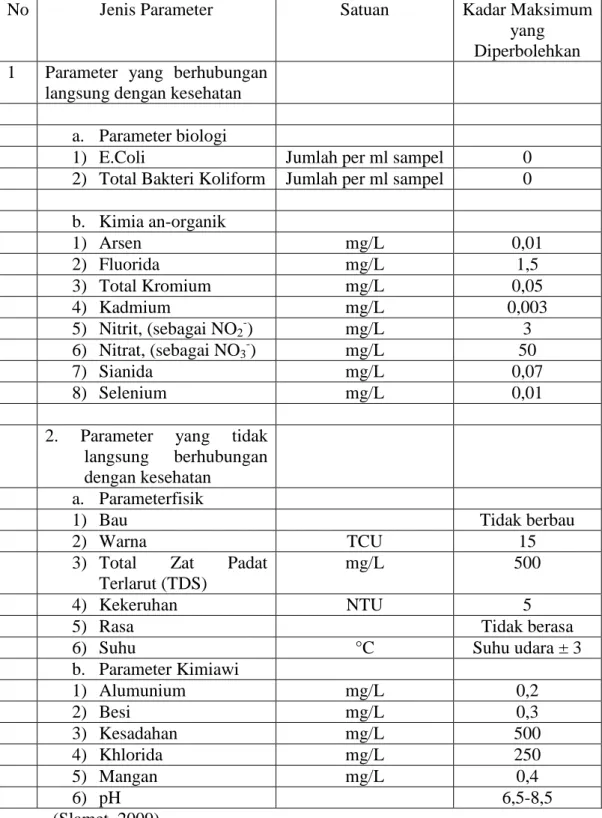
penyakit bawaan air. Karena itu dibuatlah parameter-parameter demi menjaga kualitas air minum. Persyaratan kualitas air minum dapat dilihat dalam tabel 2.1
Tabel 2.1 Persyaratan kualitas air minum Peraturan Menteri Kesehatan
Nomor 492 Tahun 2010
No Jenis Parameter Satuan Kadar Maksimum
yang Diperbolehkan 1 Parameter yang berhubungan
langsung dengan kesehatan a. Parameter biologi
1) E.Coli Jumlah per ml sampel 0
2) Total Bakteri Koliform Jumlah per ml sampel 0 b. Kimia an-organik 1) Arsen mg/L 0,01 2) Fluorida mg/L 1,5 3) Total Kromium mg/L 0,05 4) Kadmium mg/L 0,003 5) Nitrit, (sebagai NO2-) mg/L 3 6) Nitrat, (sebagai NO3-) mg/L 50
7) Sianida mg/L 0,07
8) Selenium mg/L 0,01
2. Parameter yang tidak langsung berhubungan dengan kesehatan
a. Parameterfisik
1) Bau Tidak berbau
2) Warna TCU 15
3) Total Zat Padat Terlarut (TDS)
mg/L 500
4) Kekeruhan NTU 5
5) Rasa Tidak berasa
6) Suhu °C Suhu udara ± 3
b. Parameter Kimiawi 1) Alumunium mg/L 0,2 2) Besi mg/L 0,3 3) Kesadahan mg/L 500 4) Khlorida mg/L 250 5) Mangan mg/L 0,4 6) pH 6,5-8,5 (Slamet, 2009).
12
2.2 Nitrit dan Nitrat Dalam Air Minum
Di perairan alami, nitrit (NO2) biasanya ditemukan dalam jumlah yang sangat sedikit, lebih sedikit daripada nitrat karena bersifat tidak stabil dengan keberadaan oksigen. Nitrit merupakan bentuk sementara antara amonia dan nitrat. Kadar nitrit dalam perairan relatif kecil karena segera dioksidasi menjadi nitrat (Effendi, 2003).
Nitrat merupakan produk peralihan dari senyawa nitrogen. Nitrit terbentuk dari reaksi bakteri dimulai dari ammonia dan nitrogen organik. Tidak ada konsentrasi signifikan yang ditemukan pada permukaan air. Gugus nitrogen ditemukan di dalam air limbah, air tanah dan air pertanian (De Zuane, 1996).
Nitrifikasi adalah proses pembentukan senyawa nitrat dari senyawa amonium. Proses ini merupakan proses dimana ion ammonium dioksidasi menjadi ion nitrit, serta ion nitrit menjadi ion nitrat. Proses ini dapat terjadi di tanah, air laut, maupun air tawar. Nitrifikasi muncul secara almiah di lingkungan dengan keberadaan bakteri khusus nitrifikasi. Tingkat reaksi nitrifikasi sangat tergantung pada sejumlah faktor lingkungan (Jacob dan Cordaro, 2000).
Menurut Jacob dan Cordaro (2000), proses nitrifikasi dipengaruhi oleh dua bakteri berbeda. Nitrosomonas mempengaruhi tahap pertama yaitu pembentukan nitrit:
NH4 + Nitrosomonas + 2O2 NO2 + 2H2O
Hasil nitrit kemudian akan diubah menjadi nitrat oleh bakteri nitrobacter: 2NO2 + Nitrobacter + O2 + 2H2O 2NO3 + 2H2O
13
Hal tersebut terjadi karena beberapa faktor yaitu substrat di dalam air, konsentrasi oksigen, suhu, pH dan adanya zat beracun atau zat yang menghambat proses nitrifikasi.
Semua bakteri nitrifikasi adalah bakteri yang sensitif terhadap temperatur. Perubahan temperatur secara tiba-tiba tidak memengaruhi terhadap kecepatan pertumbuhan dari bakteri itu sendiri sehingga tidak pula berpengaruh terhadap kecepatan reaksi nitrifikasi. Temperatur yang sesuai dalam proses nitrifikasi ini adalah dari 0-20o C sebab pada suhu tersebutlah bakteri nitrifikasi mengalami pertumbuhan yang maksimum sehingga hal tersebut berpengaruh terhadap kecepatan proses nitrifikasi. Selain itu, konsentrasi oksigen pula memengaruhi kecepatan proses nitrifikasi. Hal tersebut berkaitan dengan bakteri nitrifikasi yang membutuhkan oksigen. Kemudian, pH dari lingkungan pula berpengaruh terhadap kecepatan reaksi nitrifikasi. Reaksi nitrifikasi ini terjadi paling cepat pada pH 8-9. Faktor-faktor tersebut berkaitan dengan keberlangsungan hidup bakteri nitrifikasi, sehingga kecepatan dari proses nitrifikasi ini sangat bergantung pada keberadaan bakteri nitrifikasi (Jacob dan Cordaro, 2000).
Nitrat digunakan dalam pupuk, sebagai pengawet makanan dan bahan pengoksidasi pada industri kimia. Nitrit digunakan pada industri makanan sebagai pengawet makanan (garam natrium dan potassium), khususnya pada daging dan keju (De Zuane, 1996).
2.2.1 Penyebaran Nitrit dan Nitrat Dalam Air Minum
Pertambahan penduduk di kota-kota besar umumnya diikuti dengan peningkatan kebutuhan air minum. Kepadatan penduduk dan
14
terbatasnya lahan untuk daerah pemukiman menyebabkan terjadinya pencemaran air tanah terutama oleh zat-zat organik yang berasal dari buangan rumah tangga. Selain itu terdapat pipa instalasi jaringan PDAM yang sudah tua dan menjadi aus sehingga mengakibatkan terjadinya rembesan air buangan ke dalam pipa dan menyebabkan air minum tercemar. Pencemaran air minum oleh bahan organik menyebabkan ammonia meningkat. Ammonia larut di dalam air dan membentuk senyawa ammonium yang cenderung akan mengikat oksigen. Dengan adanya mikroba nitrosomonas senyawa ammonium dan oksigen dapat membentuk senyawa nitrit dengan adaya mikroba nitrobakter akan membentuk senyawa nitrat (Sukar., dkk, 1991).
Nitrat khususnya ditemukan dalam tanah dan tersebar meluas ke dalam lingkungan dimulai dari makanan sampai ke atmosfir dan air. Konsentrasi tinggi kemungkinan berasal dari pupuk yang telah digunakan, pembusukan binatang dan sayuran, kotoran yang terlarut, pembuangan sampah dan limbah industri (WHO, 2011).
2.2.2 Metabolisme Nitrit dan Nitrat
Nitrat diabsorbsi dengan cepat pada saluran pencernaan bagian atas, dan sebagian besar dikeluarkanmelalui urin. Pengeluaran melalui urin mempunyai waktu paruh sekitar lima jam. Asupan nitrit dapat bereaksi dengan zat-zat yang ada dalam saluran pencernaan. Jika diserap ke dalam system sirkulasi, nitrit atau mengoksidasi hemoglobin menjadi methomoglobin (Silalahi, 2005).
Ternyata, sebagian nitrat yang sedang diangkut dalam darah dikeluarkan melalui kelenjar ludah. Nitrat di dalam mulut, mikroba rongga
15
mulut dapat mereduksi nitrat menjadi nitrit dan kemudian tertelan. Sebanyak 25% dari asupan nitrat dikeluarkan melalui kelenjar ludah. Sekitar 20% dari nitrat dalam kelenjar ludahdireduksi menjadi nitrit. Karena itu, sekitar 5% dari asupan nitrat sesungguhnya direduksi menjadi nitrit di dalam ludah dan tertelan kembali. Sintesa nitrit dan nitrat terjadi di dalam tubuh. Jika pH lambung meningkat, bakteriakan berkembang, kemudian dapat mereduksi nitrat menjadi nitrit. Nitrit juga dapat terbentuk melalui reduksi nitrat oleh bakteri pada infeksi kelenjar kemih (Silalahi, 2005).
Keseimbangan nitrat pada orang dewasa dan bayi berbeda. Pada bayi, 100% dari asupan nitrat akan diekskresikan dalam urin, sedangkan pada orang dewasa hanya 30-35%. Sebagian reduksi nitrat menjadi nitrit pada manusia terjadi di saliva seumur hidupnya dan pada saluran gastrointestinal terjadi pada bayi dibawah umur tiga bulan. Itulah mengapa, bayi yang berumur diatas tiga bulan mudah terjadi perubahan sebanyak 100% dari bentuk nitart menjadi nitrit, sementara 10% hanya terjadi pada orang dewasa dan anak-anak (Silalahi, 2005; De Zuane, 1996).
2.2.3 Toksisitas Nitrit dan Nitrat
Peraturan Menteri Kesehatan Nomor 492 Tahun 2010 memberikan persyaratan kualitas air minum yang diperbolehkan mengandung nitrat maksimum 50mg/L dan 3mg/L untuk nitrit. Sedangkan menurut Peraturan Menteri Kesehatan Nomor 416 Tahun 1990 bahwa syarat kualitas air bersih yang digunakan sebagai air minum setelah dimasak adalah 10 mg/L untuk nitrat dan 1 mg/L untuk nitrit.
16
Nitrat dan nitrit dalam jumlah besar dapat menyebabkan gangguan gastro intestinal, diare campur darah, disusul dengan konvulsi, koma dan bila tidak ditolongakan meninggal. Keracunan kronis menyebabkan depresi umum, sakit kepala, dan gangguan mental. Nitrit terutama akan bereaksi dengan hemoglobin membentuk methemoglobin (metHb). Dalam jumlah melebihi normal MetHb akan menimbulkan methemoglobinemia. Pada bayi methemoglobinemia sering dijumpai karena pembentukan pembentukan enzim untuk menguraikan metHb menjadi Hb masih belum sempurna. Sebagai akibat methemoglobinemia, bayi akan kekurangan oxygen, maka mukanya akan tampak membiru (Slamet,2009).
Konsentrasi nitrit yang besar di dalam air berpotensi terbentuknya nitrosamin yang bersifat karsinogenik. Nitrosamin terbentuk melalui reaksi kimia antara agen nitrosasi dan senyawa amin yang mudah dinitrosasi. Pada umumnya, precursor (bahan baku) pembentuk nitrosamine adalah amin sekunder dan tertier. Agen nitrosasi yang paling penting dalam pembentukan nitrosamine adalah N2O3 yang mudah terbentuk dari nitrit dalam suasana asam sebagai berikut:
NO2- + H+ HNO2 HNO2 + H+ H2NO2+
H2NO2+ + NO2- N2O3 + H2O
N2O3 bereaksi dengan pasangan electron bebas yang ada pada amin sekunder membentuk nitrosamin.
17
Reaksi ini terjadi pada suasana dalam air. Kondisi pH yang optimum untuk nitrosasi senyawa amin sekunder berkisar antar 2,5 dan 3,5 (Silalahi, 2005).
2.3 Penentuan Kadar Nitrit dan Nitrat
Prinsip pengukuran kadar nitrit dan nitrat berdasarkan berdasarkan pembentukan senyawa azo yang berwarna merah keunguan yang terjadi bila direaksikan dengan asam sulfanilat dan N-(1-naftil etilen diamin dihidroklorida). Warna yang terbentuk diukur absorbansinya secara spektrofotometri sinar tampak pada panjang gelombang maksimum 543 nm (SNI, 2006).
2.3.1 Spektrofotometri Sinar Tampak
Panjang gelombang sinar tampak lebih pendek daripada panjang gelombang radiasi inframerah. Satuan yang digunakan adalah nanometer (1 nm = 10-7 cm). Spectrum sinar tampak terentang dari sekitar 400 nm ungu sampai 750 nm (merah) (Fessenden dan Fessenden, 1986).
Tabel 2.2 Warna sinar tampak dapat dihubungkan dengan panjang
gelombangnya
Panjang gelombang
Warna yang diserap Warna yang diamati/warna
komplementer
400-435 nm Ungu (lembayung) Hijau kekuningan
450-480 nm Biru Kuning
480-490 nm Biru kehijauan Orange
480-500 nm Hijau kebiruan Merah
500-560 nm Hijau Merah anggur
560-580 nm Hijau kekuningan Ungu (lembayung)
580-595 nm Kuning Biru
595-610 nm Orange Biru kekuningan
610-750 nm Merah Hijau kebiruan
(Gandjar dan Rohman, 2008).
Warna sinar tampak dapat dihubungkan dengan panjang gelombangnya. Sinar pada panjang gelombang tunggal (radiasi
18
monokromatik) diabsorbsi maka sinar yang dihasilkan akan nampk sebagai warna komplemen warna yang diserap tadi. Jadi jika warna biru (450 sampai 480 nm) diabsorbsi maka radiasi yang dihasilkan adalah warna kuning (Gandjar dan Rohman, 2008).
Spektra sinar tampak dapat digunakan untuk informasi kualitatif dan sekaligus dapat digunakan untuk analisis kuantitatif. Data yang diperoleh spektofotometri sinar tampak adalah panjang gelombang maksimal, intensitas, efek pH, dan pelarut, yang kesemuanya itu dapat diperbandingkan dengan data yang sudah dipublikasikan (Gandjar dan Rohman, 2008).
Sementara, dalam aspek kuantitatif suatu berkas radiasi dikenakan pada cuplikan dan intensitas radiasi yang diteruskan diukur besarnya. Radiasi yang diserap oleh cuplikan ditentukan dengan membandingkan intensitas sinar yang diteruskan dengan intensitas sinar yang diserap jika tidak ada spesies penyerap lainnya. Intensitas atau kekuatan radiasi cahaya sebanding dengan sejumlah foton yang melalui satu satuan luas penampang perdetik. Serapan dapat terjadi jika radiasi yang mengenai cuplikan memiliki energi yang sama dengan energi yang dibutuhkan untuk menyebabkan terjadinya perubahan tenaga. Kekuatan radiasi juga mengalami penurunana dengan adanya penghamburan dan pemantulan cahaya, akan tetapi penurunan karena hal ini sangat kecil dibandingkan dengan proses penyerapan (Gandjar dan Rohman, 2008).
Menurut Gandjar dan Rohman (2008), dalam Hukum Lambert Beer menyatakan bahwa intensitas yang diteruskan oleh larutan zat
19
penyerap berbanding lurus dengan tebal dan konsentrasi larutan. Dalam hukum Lambert Beer tersebut ada beberapa pembatasan yaitu;
• Sinar yang digunakan dianggap monokromatis
• Penyerapan terjadi dalam suatu volume yang mempunyai penampang luas yang sama
• Senyawa yang menyerap dalam larutan tersebut tidak tergantung terhadap yang lain dalam larutan tersebut
• Tidak terjadi peristiwa fluoresensi atau fosforiensi • Indeks bias tidak tergantung pada konsentrasi larutan
Suatu zat warna ialah senyawa organik berwarna yang digunakan untuk memberi warna ke suatu objek. Warna merupakan hasil suatu perangkat kompleks respon faali maupun psikologis terhadap panjang gelombang antara 400-750 nm, yang jatuh pada selaput retina mata (Fessendendan Fessenden, 1986).
Ada beberapa hal yang harus diperhatikan dalam analisis dengan spektrofotometri sinar tampak terutama untuk senyawa yang semula tidak berwarna yang akan dianalisis dengan spektrofotometri sinar tampak karena senyawa tersebut harus diubah terlebih dahulu menjadi senyawa yang berwarna. Berikut adalah tahapan-tahapa yang harus diperhatikan: a. Pembentukan yang dapat menyerap sinar tampak
Menurut Gandjar dan Rohman (2008), hal ini perlu dilakukan jika senyawa yang dianalisis tidak menyerap pula pada daerah tersebut. Cara yang digunakan adalah dengan merubah senyawa lain atau direaksikan dengan pereaksi tertentu. Pereaksi yang digunakan harus memenuhi beberapa persyaratan yaitu :
20
• Reaksinya selektif dan sensitif
• Reaksinya cepat, kuantitatif, dan reprodusibel • Hasil reaksi dalam jangka waktu yang lama.
Contohnya dengan cara mengubahnya menjadi senyawa yang berwarna setelah didiazotasi dan dikopling degan naftil etilen diamin (NED). Zat warna azo merupakan kelas zat yang terbesar dan terpenting, jumlahnya mencapai ribuan. Dalam pewarnaan azo, mula-mula senya aromatik teraktifkan terhadap subtitusi elektrofilik, kemudian diolah dengan suatu garam diazonium untuk membentuk zat warna (Svehla, 1985; Gandjar dan Rohman, 2008; Fessenden dan Fessenden, 1986)
b. Waktu operasional (operating time)
Cara ini digunakan untuk pengukuran hasil reaksi atau pembentukan warna.Tujuannya adalah untuk mengetahui waktu pengukuran yang stabil. Waktu operasional ditentukan dengan mengukur hubungan antara waktu pengukuran dengan absorbs larutan (Gandjardan Rohman, 2008).
c. Pemilihan panjang gelombang
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombangg yang mempunyai absorbansi maksimal. Untuk memilih panjang gelombang maksimal dilakukan dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu larutan baku pada konsentrasi tertentu (Gandjardan Rohman, 2008).
d. Pembuatan kurva baku
Dibuat seri larutan baku dari zat yang akan dianalisis dengan berbagai konsentrasi. Masing-masing absorbansi larutan dengan berbagai
21
konsentrasi diukur, kemudian dibuat kurva yang merupakan hubungan antara absorbansi (y) dengan konsentrasi (x) (Gandjardan Rohman, 2008). e. Pembacaan absorbansi sampel atau cuplikan
Absorban yang terbaca pada spektrofotometri hendaknya antara 0,2 sampai 0,8 atau 15% samapai 70% jika dibaca sebagai tramitans. Anjuran ini berdasarkan anggapan bahwa kesalahan dalam pembacaan T adalah 0,005 atau 0,5% (kesalahan fotometrik) (Gandjardan Rohman, 2008).
2.3.2 Reaksi Diazotasi
Reaksi diazotasi merupakan reaksi senyawa aromatik yang teraktifkan terhadap substitusi elektrofilik sehingga terbentuk garam diazonium untuk membentuk warna (Fessenden dan Fessenden, 1986).
Reaksi diazotasi disebut juga dengan uji griess. Reaksi dizotasi antar asam sulfanilat dengan nitrit yang akan membentuk garam diazonium akan diikuti reaksi kopling dengan NED membentuk zat pewarna azo yang merah:
NH2 N=N + HNO2 + 2H2O SO3H SO3H N=N + + HSO3 N=N NH2 SO3 HNH2
22
2.3.3 Kadar Nitrit dan Nitrat Dalam Air Minum
Penelitian tentang kadar nitrit dan nitrat dalam air minum telah dilakukan sebelumnya. Diantaranya pada sampel air sumur di beberapa daerah Sumatera Utara, air minum PDAM di Jakarta, dan air sumur di kecamatan Manggala. Metode yang digunakan pada penentuan kadar nitrit dan nitrit tersebut menggunakan metode spektrofotometri sinar tampak dengan menggunakan pereaksi warna azo. Reaksi warna azo menggunakan asam sulfanilat dan NED. Hasil penelitian dapat dilihat pada Tabel 2.2:
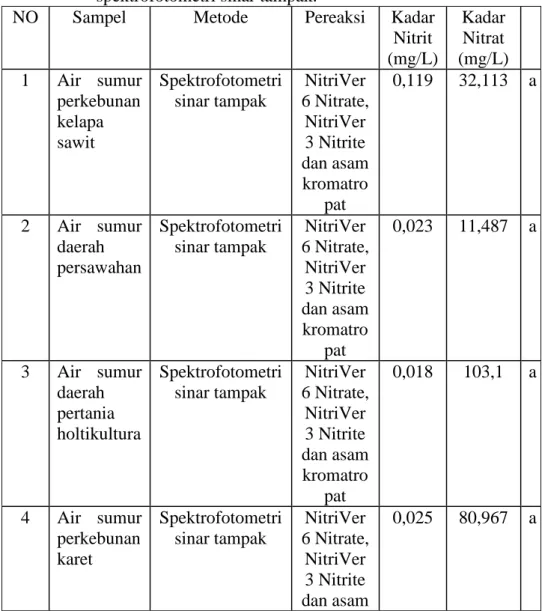
Tabel 2.3 Hasil pemeriksaan kadar nitrit dan nitrat pada air minum secara
spektrofotometri sinar tampak.
NO Sampel Metode Pereaksi Kadar Nitrit (mg/L) Kadar Nitrat (mg/L) 1 Air sumur perkebunan kelapa sawit Spektrofotometri sinar tampak NitriVer 6 Nitrate, NitriVer 3 Nitrite dan asam kromatro pat 0,119 32,113 a 2 Air sumur daerah persawahan Spektrofotometri sinar tampak NitriVer 6 Nitrate, NitriVer 3 Nitrite dan asam kromatro pat 0,023 11,487 a 3 Air sumur daerah pertania holtikultura Spektrofotometri sinar tampak NitriVer 6 Nitrate, NitriVer 3 Nitrite dan asam kromatro pat 0,018 103,1 a 4 Air sumur perkebunan karet Spektrofotometri sinar tampak NitriVer 6 Nitrate, NitriVer 3 Nitrite dan asam 0,025 80,967 a
23 kromatro pat 5 Air sumur dataran rendah pantai Spektrofotometri sinar tampak NitriVer 6 Nitrate, NitriVer 3 Nitrite dan asam kromatro pat 0,042 10,013 a 6 PDAM Penjompon gan Spektrofotometri sinar tampak Asam sulfanilat dan Naftil Etilendia min Dihirdokl orida 1,20 0,39 b 7 PDAM Pulogadun g Spektrofotometri sinar tampak Asam sulfanilat dan Naftil Etilendia min Dihirdokl orida 2,27 1,80 b 8 Air Sumur Sampel I kecamatan Manggala Spektrofotometri sinar tampak Asam sulfanilat dan Naftil Etilendia min Dihirdokl orida 0,0600 7,1097 c 9 Air Sumur Sampel II kecamatan Manggala Spektrofotometri sinar tampak Asam sulfanilat dan Naftil Etilendia min Dihirdokl orida 0,0106 14,300 7 c 10 Air Sumur Sampel III kecamatan Manggala Spektrofotometri sinar tampak Asam sulfanilat dan Naftil Etilendia min Dihirdokl orida 0,1000 2,6852 c
24 11 Air Sumur Sampel IV kecamatan Manggala Spektrofotometri sinar tampak Asam sulfanilat dan Naftil Etilendia min Dihirdokl orida 0,0367 12,105 6 c Keterangan :
a = Sapta Sari Dewi b = Sukar
c = Rusman
Dari tabel diatas dapat dilihat bahwa, pemeriksaan kadar nitrit dan nitrat di dalam air minum yang berasal dari sumur di beberapa daerah Sumatera Utara (Dewi, 2005) kadar nitrat dan nitrit yang terdapat dalam sampel air sumur yang berada di daerah persawahan dan daerah dekat tepi pantai mempunyai kadar yang relatif rendah dan tidak melebihi kadar yang diizinkan, sementara air sumur di daerah perkebunan mengandung nitrat yang relatif tinggi dan sebagian besar berada diatas yang diizinkan yaitu berkisar 103 mg/L. Evaluasi pencemaran nitrit dan nitrat pada air minum PDAM di DKI Jakarta (Sukar., dkk, 1991), kandungan kadar rata-rata nitrat dan nitrit pada air hasil olahan PDAM memenuhi syarat yang telah diizinkan kecuali sampel air dari PDAM Pulogadung yang ditemukan menyimpang dari persyaratan dengan kadar nitrit 2,27 mg/L. Analisis kandungan nitrit dan nitrat pada air sumur di sekitar tempat pembuangan akhir sampah kelurahan tamangapa kecamatan manngala Makasar (Rusman, 2013), terdapat kadar nitrit yang memenuhi persyaratan sementara sebagian kadar nitrat sampel tidak memenuhi syarat yaitu berkisar antara 7,14-14,3 mg/L.